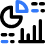Adrian Chin und André van Zundert
DIE GESCHICHTE DER SPINALANÄSTHESIE
Carl Koller, ein Augenarzt aus Wien, beschrieb 1884 erstmals die Anwendung von topischem Kokain zur Analgesie des Auges. William Halsted und Richard Hall, Chirurgen am Roosevelt Hospital in New York City, gingen mit der Idee der Lokalanästhesie einen Schritt weiter, indem sie Kokain in menschliches Gewebe und Nerven injizierten, um eine Anästhesie für die Operation zu erzeugen. James Leonard Corning, ein Neurologe in New York City, beschrieb 1885 die Verwendung von Kokain zur Spinalanästhesie. Weil Corning ein häufiger Beobachter im Roosevelt Hospital war, kam die Idee, Kokain zu verwenden Subarachnoidea Raum könnte durch die Beobachtung von Halsted und Hall bei der Durchführung von Kokaininjektionen entstanden sein. Corning injizierte einem Hund zuerst Kokain intrathekal und innerhalb weniger Minuten hatte der Hund eine deutliche Schwäche in der Hinterhand. Als nächstes injizierte Corning einem Mann Kokain am T11-T12-Zwischenraum in das, was er für den Subarachnoidalraum hielt. Da Corning nach 8 Minuten keine Wirkung bemerkte, wiederholte er die Injektion.
Zehn Minuten nach der zweiten Injektion klagte der Patient über Schläfrigkeit in den Beinen, konnte aber stehen und gehen. Da Corning den Abfluss von Liquor cerebrospinalis (CSF) nicht erwähnte, gab er dem Patienten höchstwahrscheinlich versehentlich eine epidurale statt einer spinalen Injektion.
Das Vorhandensein einer neuraxialen Flüssigkeit wurde erstmals von Galen im Jahr 200 n. Chr. festgestellt, und CSF wurde später im 1500. Jahrhundert von Antonio Valsalva untersucht. Die Duralpunktion wurde 1891 von Essex Wynter beschrieben, kurz darauf 6 Monate später von Heinrich Quincke.
Augustus Karl Gustav Bier, ein deutscher Chirurg, verwendete 1898 Kokain intrathekal bei sechs Patienten für Operationen an den unteren Extremitäten. In wahrhaft wissenschaftlicher Manier beschloss Bier, an sich selbst zu experimentieren und entwickelte eine Kopfschmerz nach Punktion (PDPH) für seinen Einsatz. Sein Assistent, Dr. Otto Hildebrandt, erklärte sich bereit, den Eingriff durchführen zu lassen, nachdem Bier aufgrund der PDPH nicht mehr weitermachen konnte. Nach Injektion von spinalem Kokain in Hildebrandt führte Bier Experimente an der unteren Hälfte von Hildebrandts Körper durch. Bier beschrieb Nadelstiche und Zigarrenverbrennungen an den Beinen, Einschnitte an den Oberschenkeln, Schamhaarausrisse, kräftige Schläge mit einem Eisenhammer auf die Schienbeine und Torsion der Hoden. Hildebrandt berichtete von minimalen bis keinen Schmerzen während der Experimente; danach litt er jedoch unter Übelkeit, Erbrechen, PDPH und Blutergüssen und Schmerzen in seinen Beinen. Bier führte die PDPH auf den Liquorverlust zurück und war der Meinung, dass die Verwendung von Nadeln mit kleinem Durchmesser helfen würde, die Kopfschmerzen zu verhindern.
Dudley Tait und Guido Caglieri führten 1899 in San Francisco die erste Spinalanästhesie in den Vereinigten Staaten durch. Ihre Studien umfassten Leichen, Tiere und lebende Patienten, um den Nutzen der Lumbalpunktion, insbesondere bei der Behandlung von Syphilis, zu bestimmen. Tait und Caglieri injizierten Quecksilbersalze und Jodide in den Liquor, verschlechterten jedoch den Zustand eines Patienten mit tertiärer Syphilis. Rudolph Matas, ein Gefäßchirurg in New Orleans, beschrieb die Anwendung von spinalem Kokain bei Patienten und war möglicherweise der erste, der Morphin im Subarachnoidalraum einsetzte. Matas beschrieb auch die Komplikation des Todes nach Lumbalpunktion. Theodore Tuffier, ein französischer Chirurg in Paris, studierte Spinalanästhesie und berichtete 1900 darüber. Tuffier war der Meinung, dass Kokain nicht injiziert werden sollte, bis CSF erkannt wurde.
Tuffier lehrte zur gleichen Zeit an der Universität von Paris, dass Tait dort Medizinstudent war und höchstwahrscheinlich einer von Taits Mentoren war. Tuffiers Demonstrationen in Paris trugen dazu bei, die Spinalanästhesie in Europa bekannt zu machen.
Arthur Barker, Professor für Chirurgie an der University of London, berichtete 1907 über den Fortschritt der Wirbelsäulentechniken, einschließlich der Verwendung eines hyperbaren spinalen Lokalanästhetikums, der Betonung der Sterilität und der Erleichterung der Mittellinie gegenüber der paramedianen Duralpunktion. Die Förderung der Sterilität und die Untersuchung des Blutdruckabfalls nach der Injektion trugen dazu bei, die Spinalanästhesie sicherer und beliebter zu machen. Gaston Labat war ein starker Befürworter der Spinalanästhesie in den Vereinigten Staaten und führte frühe Studien über die Auswirkungen der Trendelenburg-Position auf den Blutdruck nach Spinalanästhesie durch. George Pitkin versuchte, ein hypobares Lokalanästhetikum zu verwenden, um das Ausmaß der Spinalnervenblockade zu kontrollieren, indem er Procain mit Alkohol mischte. Lincoln Sise, ein Anästhesist an der Lahey Clinic in Boston, verwendete Barkers Technik der hyperbaren Spinalanästhesie sowohl mit Procain als auch mit Tetracain.
Die Spinalanästhesie wurde immer beliebter, als neue Entwicklungen auftraten, einschließlich der Einführung der Anästhesie der Sattelnervenblockade im Jahr 1946 durch Adriani und Roman-Vega. 1947 führte jedoch der viel beachtete Fall von Woolley und Roe (Vereinigtes Königreich) dazu, dass zwei Patienten an einem Tag querschnittsgelähmt wurden. Auf der anderen Seite des Atlantiks veranlassten Berichte über Querschnittslähmung in den Vereinigten Staaten in ähnlicher Weise Anästhesisten, die Anwendung der Spinalanästhesie einzustellen. Die Entwicklung neuartiger intravenöser Anästhetika und neuromuskulärer Blocker fiel mit der rückläufigen Anwendung der Spinalanästhesie zusammen. 1954 beschrieben Dripps und Vandam die Sicherheit der Spinalanästhesie bei mehr als 10,000 Patienten, und die Spinalanästhesie wurde wiederbelebt.
Auf dem Gebiet der Geburtshilfe, Bis Mitte der 500,000er Jahre wurden an amerikanischen Frauen über 1950 Spinals durchgeführt. Obwohl die Spinalanästhesie in den 1950er Jahren die am häufigsten verwendete Technik für die vaginale Entbindung und den Kaiserschnitt war, führten nachfolgende Verbesserungen der Epiduraltechnologie Ende der 1960er Jahre zu einem Rückgang der geburtshilflichen Spinalanästhesie. Das Third National Audit Project (NAP3) schätzte, dass im Jahr 133,525 im Vereinigten Königreich 2006 geburtshilfliche Spinals durchgeführt wurden.
Die frühe Entwicklung der Spinalnadeln verlief parallel zur frühen Entwicklung der Spinalanästhesie. Corning wählte eine goldene Nadel mit einer kurzen abgeschrägten Spitze, einer flexiblen Kanüle und einer Feststellschraube, die die Nadel auf die Tiefe der Duralpenetration fixierte. Corning verwendete auch eine Einführhilfe für die Nadel, die rechtwinklig war. Quincke verwendete eine abgeschrägte Nadel, die scharf und hohl war. Bier entwickelte seine eigene scharfe Nadel, die keine Einführhilfe benötigte. Die Nadel hatte eine größere Bohrung (15 oder 17 Gauge) mit einer langen, schneidenden Abschrägung. Die Hauptprobleme mit Biers Nadel waren Schmerzen beim Einführen und der Verlust des Lokalanästhetikums aufgrund des großen Lochs in der Dura nach der Durapunktion. Die Barker-Nadel hatte keine innere Kanüle, war aus Nickel und hatte eine scharfe, mittellange Abschrägung mit einem passenden Mandrin. Labat entwickelte eine unzerbrechliche Nickelnadel mit einer scharfen, kurzen Abschrägung und einem passenden Mandrin. Labat glaubte, dass die kurze Abschrägung die Beschädigung des Gewebes beim Einführen in den Rücken minimierte.
Herbert Greene erkannte, dass der Liquorverlust ein großes Problem bei der Spinalanästhesie war, und entwickelte eine Nadel mit glatter Spitze und kleinerem Durchmesser, die zu einer geringeren Inzidenz von PDPH führte. Barnett Greene beschrieb die Verwendung einer 26-Gauge-Spinalnadel in Geburtshilfe mit einer verringerten Inzidenz von PDPH. Die Greene-Nadel war bis zur Einführung der Whitacre-Nadel beliebt. Hart und Whitacre29 verwendeten eine Nadel mit Bleistiftspitze, um PDPH von 5–10 % auf 2 % zu senken. Sprotte modifizierte die Whitacre-Nadel und veröffentlichte 1987 seinen Versuch mit über 34,000 Spinalanästhetika. In den 1990er Jahren wurden Modifikationen der Sprotte-Nadel vorgenommen, um die heute verwendete Nadel herzustellen.
Die Spinalanästhesie hat seit 1885 große Fortschritte gemacht. Jeder Aspekt, von verbesserter Ausrüstung und pharmakologischen Wirkstoffen bis hin zu einem besseren Verständnis der Physiologie und Anatomie, hat die Spinalanästhesie immer sicherer gemacht. Durch den Wandel des klinischen Wissens hat sich das, was als Kontraindikation für die Spinalanästhesie gilt, verändert, und die Entwicklung neuartiger Techniken, wie z. B. die Verwendung von Ultraschall, hat die Spinalanästhesie in Situationen ermöglicht, die früher als unmöglich galten. Dennoch ist keine Technik risikofrei, und es müssen alle Anstrengungen unternommen werden, um dies zu verhindern Komplikationen. Zu lernen, wie man eine Spinalanästhesie durchführt, ist eine unschätzbare Fähigkeit, die alle Anästhesisten in ihrem Arsenal haben sollten.
DIE RISIKEN UND VORTEILE DER SPINALANÄSTHESIE
Bevor einem Patienten eine Spinalanästhesie angeboten wird, muss ein Anästhesist nicht nur die Indikationen und Kontraindikationen der Spinalanästhesie kennen, sondern auch die Risiken und Vorteile der Durchführung des Eingriffs abwägen können. Dies erfordert ein gründliches Verständnis der verfügbaren Evidenz, insbesondere des Nutzen-Risiko-Verhältnisses im Vergleich zu anderen Alternativen, und die Fähigkeit, die Evidenz auf ein bestimmtes klinisches Szenario anzuwenden. Somit kann ein informierter Anästhesist dem Patienten helfen, eine informierte Entscheidung zu treffen.
Kontraindikationen und Risiken der Spinalanästhesie
Kontraindikationen für die Spinalanästhesie
Es gibt absolute und relative Kontraindikationen für die Spinalanästhesie (vgl Tabelle 1). Zu den absoluten Kontraindikationen gehören die Ablehnung durch den Patienten; Infektion an der Injektionsstelle; schwere, unkorrigierte Hypovolämie; echte Allergie gegen eines der Medikamente; und erhöhter intrakranieller Druck, außer in Fällen von Pseudotumor cerebri (idiopathischer intrakranieller Hypertonie). Ein hoher intrakranieller Druck erhöht das Risiko einer unkalierten Herniation, wenn Liquor durch die Nadel verloren geht. Eine Spinalanästhesie ist auch kontraindiziert, wenn die Operation voraussichtlich länger dauern wird als die Dauer der Nervenblockade oder zu einem Blutverlust führt, so dass die Entwicklung einer schweren Hypovolämie wahrscheinlich ist.
TABELLE 1. Kontraindikationen für die Spinalanästhesie.
| Absolute Kontraindikationen | Relative Gegenanzeigen |
|---|---|
| • Ablehnung durch den Patienten • Infektion an der Injektionsstelle • Unkorrigierte Hypovolämie • Allergie • Erhöhter Hirndruck | • Koagulopathie • Blutvergiftung • Behobene Zustände des Herzzeitvolumens • Unbestimmte neurologische Erkrankung |
Koagulopathie, die bisher als absolute Kontraindikation galt, kann je nach Grad der Störung in Betracht gezogen werden. Eine weitere relative Kontraindikation der Spinalanästhesie ist eine Sepsis, die sich von der anatomischen Punktionsstelle unterscheidet (z. B. Chorioamnionitis oder Infektion der unteren Extremität). Wenn der Patient Antibiotika erhält und die Vitalfunktionen stabil sind, kann eine Spinalanästhesie in Betracht gezogen werden. Die Spinalanästhesie ist bei Herzerkrankungen mit fixiertem Herzzeitvolumen (CO)-Zustand relativ kontraindiziert. Die einst als absolute Kontraindikation für eine Spinalanästhesie geltende Aortenstenose schließt eine sorgfältig durchgeführte Spinalanästhesie nicht immer aus.
Unbestimmt neurologische Erkrankung ist eine relative Kontraindikation. Multiple Sklerose und andere demyelinisierende Erkrankungen sind eine Herausforderung. In-vitro-Experimente deuten darauf hin, dass demyelinisierte Nerven anfälliger für Toxizität von Lokalanästhetika sind. Keine klinische Studie hat jedoch überzeugend gezeigt, dass eine Spinalanästhesie solche neurologischen Erkrankungen verschlimmert. Mit dem Wissen, dass Schmerzen, Stress, Fieber und Müdigkeit diese Krankheiten verschlimmern, kann eine stressfreie zentrale neuraxiale Nervenblockade (CNB) für die Operation bevorzugt werden.
Auch die Spinalanästhesie beim immungeschwächten Patienten stellt eine Herausforderung für den Anästhesisten dar und ist Gegenstand eines Konsensus-Statements. Obwohl diese Konsenserklärung keine verschreibungspflichtigen Ratschläge für jede Situation gibt, fasst sie die verfügbare Evidenz zusammen. Eine frühere Wirbelsäulenoperation galt früher als Kontraindikation. Die Duralpunktion kann schwierig sein, und die Ausbreitung des Lokalanästhetikums kann durch Narbengewebe eingeschränkt werden. Es gibt jedoch Fallberichte über erfolgreiche Spinalanästhesien in diesem Setting, insbesondere mit Ultraschallunterstützung. Es gibt theoretische Risiken beim Einführen einer Hohlkörpernadel durch Tätowierfarbe. Es gibt jedoch keine Berichte über Komplikationen beim Einführen einer Spinal- oder Epiduralnadel durch eine Tätowierung. Mandrins können die Wahrscheinlichkeit verringern, dass ein Gewebekern in den Subarachnoidalraum übertragen wird, und falls betroffen, kann vor dem Einführen der Nadel ein kleiner Hautschnitt vorgenommen werden. Introducer dienen dazu, eine Kontamination des Liquors mit Epidermisstückchen zu verhindern, die zur Bildung von Dermoid-Rückenmarkstumoren führen könnte.
Risiken der Spinalanästhesie: Komplikationen
Komplikationen der Wirbelsäulenblockade werden oft in größere und kleinere Komplikationen unterteilt. Beruhigenderweise sind die meisten größeren Komplikationen selten. Kleinere Komplikationen sind jedoch häufig und daher nicht von der Hand zu weisen. Geringfügige Komplikationen sind Übelkeit, Erbrechen, leichte Hypotonie, Zittern, Juckreiz, Hörstörungen und Harnverhalt. PDPH und fehlgeschlagener Spinalblock sind signifikante und nicht ungewöhnliche Komplikationen der Spinalanästhesie. Wir betrachten sie daher als moderate Komplikationen (vgl Tabelle 2). Versagen der Spinalanästhesie wurde mit 1 % bis 17 % angegeben und wird in diesem Kapitel weiter diskutiert.
TABELLE 2. Komplikationen der Spinalanästhesie.
| Moll | Moderat | Dur |
|---|---|---|
| • Übelkeit und Erbrechen • Leichte Hypotonie • Zittern • Juckreiz • Vorübergehende leichte Schwerhörigkeit • Harnverhalt | • Ausfall der Wirbelsäule • Postduralpunktionskopfschmerz | • Direktes Nadeltrauma • Infektion (Abszess, Meningitis) • Wirbelkanalhämatom • Ischämie des Rückenmarks • Cauda-equina-Syndrom • Arachnoiditis • Periphere Nervenverletzung • Totale Spinalanästhesie • Herz-Kreislauf-Kollaps • Tod |
Kleinere Komplikationen der Spinalanästhesie
Übelkeit und Erbrechen Übelkeit und Erbrechen nach Spinalanästhesie sind für den Patienten belastend und können den Chirurgen behindern. Die Inzidenz von intraoperativer Übelkeit und Erbrechen (IONV) bei nicht geburtshilflichen Operationen kann bis zu 42 % betragen und kann bei Gebärenden bis zu 80 % betragen.
Die Ursachen sind komplex und multifaktoriell. Ursachen, die nichts mit der Wirbelsäule zu tun haben, können Faktoren des Patienten umfassen (z. B. Angst, verringerter Tonus des unteren Ösophagussphinkters, erhöhter Magendruck, vagale Hyperaktivität, hormonelle Veränderungen); chirurgische Faktoren (Exteriorisation des Uterus, peritoneale Traktion); und andere Faktoren (z. B. systemische Opioide, Uterotonika, Antibiotika, Bewegung). Die Spinalanästhesie selbst kann IONV oder postoperative Übelkeit und Erbrechen (PONV) über eine Vielzahl von Mechanismen verursachen, darunter Hypotonie, intrathekale Zusätze, unzureichende Nervenblockade oder hohe Nervenblockade. Zu den Risikofaktoren für IONV unter Spinalnerven gehören eine maximale Höhe der Nervenblockade von mehr als T6, eine Ausgangsherzfrequenz (HR) von 60 Schlägen/Minute oder mehr, eine Vorgeschichte von Reisekrankheit und eine frühere Hypotonie nach einer Spinalnervenblockade.
Hypotonie muss die erste Überlegung sein, wenn ein Patient über Übelkeit klagt, insbesondere unmittelbar nach Beginn der Spinalanästhesie. Das ist seit langem bekannt. Evans bemerkte in seinem Lehrbuch über Spinalanästhesie von 1929, dass „dem plötzlichen Abfall des Blutdrucks Übelkeit folgt“. Mechanismen und Management von Hypotonie werden an anderer Stelle ausführlicher behandelt (siehe Abschnitt über kardiovaskuläre Wirkungen der Spinalanästhesie).
Es hat sich gezeigt, dass eine Vielzahl intrathekaler Zusatzstoffe IONV oder PONV erhöhen. Intrathekales Morphin, Diamorphin, Clonidin und Neostigmin verstärken Übelkeit und Erbrechen. Intrathekales Fentanyl reduziert jedoch IONV, möglicherweise durch Verbesserung der Qualität der Nervenblockade, Verringerung der zusätzlichen Opioide oder Verringerung der Hypotonie.
Während eine niedrige Spinalnervenblockade Übelkeit durch chirurgische Stimulation verursachen kann, kann eine hohe sympathische Spinalnervenblockade (mit relativer parasympathischer Überaktivität) ebenfalls zu Übelkeit führen. Es wurde gezeigt, dass Glycopyrrolat die Übelkeit während des Kaiserschnitts besser reduziert als Placebo, obwohl die Übelkeitsrate immer noch hoch war (42 %). Die prophylaktische Gabe von Glycopyrrolat kann jedoch die Hypotonie nach einer Spinalanästhesie verstärken.
Eine kürzlich durchgeführte Metaanalyse deutete darauf hin, dass Metoclopramid (10 mg) zur Prävention von IONV und PONV im Rahmen einer Kaiserschnittgeburt unter neuraxialer Nervenblockade wirksam und sicher ist.
Eine weitere Meta-Analyse zeigte, dass die Serotonin-5-HT3-Rezeptor-Antagonisten das Auftreten von Übelkeit und Erbrechen und die Notwendigkeit eines postoperativen Notfall-Antiemetikums reduzierten, wenn intrathekales Morphin für den Kaiserschnitt verwendet wurde.
Obwohl einige Studien einen Nutzen der P6-Stimulation (Perikard 6 nei guan point) auf der Grundlage der chinesischen Akupunktur zeigten, fand eine systematische Überprüfung von 2008 widersprüchliche Ergebnisse bei der Prävention von IONV und PONV.
Unterdruck Mechanismen und Behandlung von Hypotonie werden an anderer Stelle behandelt (siehe Abschnitt über kardiovaskuläre Wirkungen der Spinalanästhesie).
Zittern Crowley et al. überprüften Zittern und neuraxiale Anästhesie. Spinal- und Epiduralanästhesie und sogar Vollnarkose können Zittern hervorrufen. Die Inzidenz von Schüttelfrost als Folge einer neuraxialen Nervenblockade ist angesichts der Heterogenität der Studien schwer einzuschätzen, liegt aber bei etwa 55 %. In den ersten 30 Minuten nach einer Nervenblockade senkt die Spinalanästhesie die Körperkerntemperatur schneller als die Epiduralanästhesie. Nach 30 Minuten führen beide Techniken dazu, dass die Temperatur mit der gleichen Geschwindigkeit abfällt. Trotzdem ist das Zittern nach einer Spinalanästhesie nicht stärker als nach einer Periduralanästhesie. Tatsächlich scheint die Intensität des Zitterns bei Epiduralanästhesien höher zu sein. Postulierte Mechanismen hierfür sind eine Unfähigkeit zu zittern aufgrund einer ausgeprägteren motorischen Blockade bei Spinalanästhesie und eine verringerte Schüttelschwelle mit mehr blockierten Dermatomen (und damit thermoregulatorischen Afferenzen) während einer Spinalanästhesie. Es wurden mehrere Strategien vorgeschlagen, um das neuraxiale Zittern zu reduzieren (vgl Tabelle 3).
TABELLE 3. Vorgeschlagene Strategien zur Vorbeugung und Behandlung von Zittern bei neuraxialer Anästhesie.
| abwehr | Behandlung |
|---|---|
| • 15 Minuten lang mit Umluftwärmer vorwärmen • Vermeiden Sie kalte epidurale oder intravenöse Flüssigkeiten • Intrathekales Fentanyl 20 μg • Intrathekales Meperidin 0.2 mg/kg oder 10 mg • Ondansetron 8 mg intravenös • Epidurales Fentanyl • Epidurales Meperidin | • Intravenöses Meperidin 50 mg • Intravenöses Tramadol 0.25 mg/kg oder 0.5 mg/kg oder 1 mg/kg • Intravenöses Clonidin 30, 60, 90 oder 150 μg |
Jucken Juckreiz ist eine bekannte Nebenwirkung von Opiaten und tritt bei Verabreichung über die Wirbelsäule (46 %) häufiger auf als bei epiduraler (8.5 %) und systemischer Verabreichung. Die Schwere des Juckreizes ist proportional zur intrathekalen Morphindosis, aber nicht zur epiduralen Morphindosis. Juckreiz im Zusammenhang mit neuraxialen Opioiden ist häufig um die Nase und das Gesicht verteilt. Obwohl die Symptome möglicherweise nicht über Opioidrezeptoren vermittelt werden, kann Pruritis mit dem Opioidrezeptorantagonisten Naloxon behandelt werden.
Es gibt Berichte über die Anwendung von Ondansetron bei Opioid-induziertem Pruritus, was auf eine Rolle von Serotoninrezeptoren bei Morphin-induziertem Pruritus hindeutet. Eine Metaanalyse von geburtshilflichen Patientinnen aus dem Jahr 2009, die intrathekales Morphin erhalten hatten, zeigte, dass 5-HT3-Rezeptorantagonisten das Auftreten von Juckreiz nicht verringerten, aber die Schwere des Juckreizes und die Notwendigkeit einer Behandlung von Juckreiz verringerten. Die 5-HT3-Rezeptor-Antagonisten waren nützlich bei der Behandlung von bestehender Pruritis (Anzahl zur Behandlung erforderlich [NNT] = 3).
Hören Beeinträchtigung Hörverlust, insbesondere im Niederfrequenzbereich, wurde nach Spinalanästhesie berichtet. Die angegebenen Inzidenzen schwanken stark (3 %–92 %). Otoakustische Emissionen, eine objektive Messung des Gehörs, die die Funktion der äußeren Haarzellen widerspiegelt, zeigten, dass Hörverlust häufiger auftritt als vermutet, aber vorübergehend ist, wobei die vollständige Erholung innerhalb von 15 Tagen eintritt. Andere Autoren sind ebenfalls zu dem Schluss gekommen, dass Hörverlust häufig spontan verschwindet. Ein Vergleich der Schwerhörigkeit nach Vollnarkose und Spinalanästhesie ergab, dass Hörminderung unabhängig von der Technik auftritt. Hörverlust kann damit verbunden sein oder auch nicht PDPH und kann sich mit einem epiduralen Blutpflaster verbessern. Ein Hörverlust nach einer Spinalnervenblockade kann mit der Nadelstärke zusammenhängen und in der geburtshilflichen Bevölkerung weniger häufig auftreten. Finegold zeigte, dass bei Frauen mit elektiven Kaiserschnitten kein Hörverlust auftrat, wenn 24-Gauge-Sprotte-Nadeln oder 25-Gauge-Quincke-Nadeln verwendet wurden. Es wurde vorgeschlagen, dass die Zustimmung zur Spinalanästhesie aus gerichtsmedizinischen Gründen eine Diskussion über einen möglichen Hörverlust beinhalten sollte.
Postoperativer Harnverhalt Die Miktion ist das Produkt eines komplexen Wechselspiels der Physiologie. Der postoperative Harnverhalt (POUR) ist daher oft multifaktoriell bedingt. Patientenrisikofaktoren für POUR sind männliches Geschlecht und frühere urologische Dysfunktion. Zu den chirurgischen Risikofaktoren gehören Beckenoperationen oder längere Operationen. Zu den anästhetischen Faktoren gehören Anticholinergika, Opioide und die Verabreichung von Flüssigkeiten (> 1000 ml). POUR kann sowohl bei neuraxialer als auch bei Vollnarkose auftreten.
Das Auftreten von POUR nach einer neuraxialen Nervenblockade ist auf eine neurale Unterbrechung des Miktionsreflexes sowie eine Überdehnung der Blase zurückzuführen. Neuroaxiale Opioide wirken am Rückenmark und am pontinen Miktionszentrum. Die durch die Spinalanästhesie induzierte parasympathische Blockade muss beendet sein, bevor es zur Entleerung kommt. Dies entspricht normalerweise der Rückkehr der Segmente S2–S4. Die Art und Dosis des Lokalanästhetikums sowie die Verwendung von neuraxialen Opioiden beeinflussen die Rückkehr der spontanen Miktion. Die Zeit bis zur Miktion ist mit 2-Chloroprocain am schnellsten und mit Bupivacain am langsamsten.
Eine kürzlich durchgeführte systematische Übersichtsarbeit ergab sechs Studien, die die Wirkung der neuraxialen Anästhesie mit anderen Techniken verglichen. Vier Studien verglichen lokale Infiltration mit intrathekaler Anästhesie; drei von ihnen fanden eine geringere Inzidenz von Harnverhalt mit lokaler Infiltration. Die anderen beiden Studien fanden keinen Unterschied in der Zeit bis zur Miktion, wenn die intrathekale Anästhesie mit einer Vollnarkose im ersten Fall und einer Vollnarkose und einer peripheren Nervenblockade im zweiten Fall verglichen wurde.
Postduralpunktionskopfschmerz Postduralpunktionskopfschmerz, der oft als geringfügige (oder zumindest nicht als schwerwiegende) Komplikation eingestuft wird, kann schwerwiegend und schwächend sein und wurde als neurologische Komplikation der Spinalanästhesie angesehen. Es ist eine häufige Ursache für medizinrechtliche Ansprüche. Die Inzidenz von PDPH wird von der Patientendemographie beeinflusst und ist weniger verbreitet in ältere Patienten. In einer Hochrisikogruppe, wie z. B. geburtshilflichen Patienten, liegt das Risiko nach einer Lumbalpunktion mit einer 27-Gauge-Nadel von Whitacre bei etwa 1.7 %. Nadelgröße und -typ beeinflussen die PDPH-Rate. Andere Risikofaktoren sind ein geringerer Body-Mass-Index (BMI), weibliches Geschlecht, wiederkehrende Kopfschmerzen in der Vorgeschichte und frühere PDPH.
Postduralpunktionskopfschmerz sollte weder als häufige „kleinere“ noch als seltene „schwere“ Komplikation betrachtet werden, sondern als nicht seltene „mittelschwere“ Komplikation.
Auf den Leser wird verwiesen Postduralpunktionskopfschmerz für weitere detaillierte Informationen.
Hauptkomplikationen der Spinalanästhesie Zu den Hauptkomplikationen der Spinalanästhesie gehören direktes Nadeltrauma, Infektion (Meningitis oder Abszessbildung), Wirbelkanalhämatom, Rückenmarkischämie, Cauda-Equina-Syndrom (CES), Arachnoiditis und periphere Nervenverletzung. Das Endergebnis dieser Komplikationen kann eine dauerhafte neurologische Behinderung sein. Andere schwerwiegende Komplikationen sind totale Spinalanästhesie (TSA), kardiovaskulärer Kollaps und Tod.
Direktes Nadeltrauma Neurologische Verletzung kann nach Nadeleinführung in das Rückenmark oder Nerven auftreten. Obwohl die Auslösung von Parästhesien während einer Spinalanästhesie als Risikofaktor für anhaltende neurologische Verletzungen in Betracht gezogen wurde, ist nicht bekannt, ob ein Eingriff nach einer Parästhesie die Entwicklung einer Parästhesie verhindern kann neurologische Komplikationen. Eine retrospektive Analyse ergab, dass bei 298 von 4767 (6.3 %) Patienten Parästhesien während der Einführung der Spinalnadel auftraten. Von den 298 Patienten hatten vier Patienten postoperativ anhaltende Parästhesien. Bei zwei weiteren Patienten mit postoperativer Parästhesie traten keine Parästhesien während des Einführens der Nadel auf. Alle sechs Patienten hatten nach 24 Monaten ein Abklingen der Symptome. Wenn eine Parästhesie auftritt, kann die Spinalnadel an Nervengewebe angrenzen oder es durchdringen; Im letzteren Fall kann die Injektion eines Lokalanästhetikums in den Spinalnerv zu dauerhaften neurologischen Schäden führen. Analoge Kontroversen bestehen bei peripherer Nervenblockade; Die Implikationen von Parästhesietechniken und extraneuraler und intraneuraler Injektion sind Gegenstand vieler Debatten.
Meningitis Meningitis, entweder bakteriell oder aseptisch, kann nach Durchführung einer Spinalanästhesie auftreten. Infektionsquellen sind kontaminierte Spinalschienen und Medikamente, die Mundflora des Anästhesisten und des Patienten Infektion. Die meisten Fälle von Meningitis nach Spinalanästhesie in der ersten Hälfte des 20. Jahrhunderts waren aseptisch und konnten auf chemische Verunreinigungen und Reinigungsmittel zurückgeführt werden.
Marinac zeigte, dass zu den Ursachen von medikamenten- und chemikalieninduzierter Meningitis nichtsteroidale entzündungshemmende Medikamente, bestimmte Antibiotika, Röntgenmittel und Muromonab-CD3 gehören. Es scheint auch einen Zusammenhang zwischen dem Auftreten der Reaktionen vom Überempfindlichkeitstyp und der zugrunde liegenden Kollagen-, Gefäß- oder rheumatologischen Erkrankung zu geben. Carp und Bailey führten bei bakteriämischen Ratten eine Lumbalpunktion durch, und nur diejenigen mit einer zirkulierenden Escherichia coli-Zahl von mehr als 50 KBE/ml zum Zeitpunkt der Lumbalpunktion entwickelten eine Meningitis. Obwohl eine Meningitis nach Lumbalpunktion auch bei bakteriämischen Kindern beschrieben wurde, unterscheidet sich die Inzidenz einer Meningitis nach diagnostischer Lumbalpunktion bei bakteriämischen Patienten nicht signifikant von der spontanen Inzidenz einer Meningitis. Die Mundflora kann den Liquor kontaminieren, wenn eine Spinalanästhesie durchgeführt wird, was die Bedeutung des Tragens einer Maske begründet. Streptococcus salivarius, Streptococcus viridans, Staphylococcus aureus, Pseudomonas aeruginosa, Acinetobacter und Mycobacterium tuberculosis wurden alle bei bakterieller Meningitis nach Spinalanästhesie oder Lumbalpunktion isoliert.
Hämatom des Wirbelkanals Wirbelkanal Bluterguss Bildung ist eine seltene, aber verheerende Komplikation nach Spinalanästhesie. Obwohl die meisten spinalen Hämatome aufgrund des prominenten epiduralen Venenplexus im Epiduralraum auftreten, haben einige Berichte Subarachnoidalblutungen als Ursache für neurologische Defizite erwähnt. Die Quelle der Blutung kann entweder aus einer verletzten Arterie oder einer verletzten Vene stammen. Spinalhämatom und Rückenmarkischämie haben eine schlechtere Prognose als infektiöse Komplikationen. Wenn sich neue oder fortschreitende neurologische Symptome entwickeln, sollte sofort eine neurochirurgische Beratung eingeholt und so schnell wie möglich eine Magnetresonanztomographie (MRT) der Wirbelsäule durchgeführt werden.
Ischämie des Rückenmarks Das oberflächliche Arteriensystem des Rückenmarks besteht aus drei Längsarterien (der vorderen Spinalarterie und zwei hinteren Spinalarterien) und einem Pialplexus.
Das hintere Rückenmark ist durch zahlreiche Anastomosen relativ vor Ischämie geschützt. Der zentrale Bereich des vorderen Rückenmarks ist abhängig von der A. spinalis anterior und daher anfälliger für Ischämie. Zu den vorgeschlagenen Mechanismen für Rückenmarkischämie als Folge einer Spinalblockade gehören eine anhaltende Hypotonie, die Zugabe von Vasokonstriktoren zu Lokalanästhetika und die Kompression der arteriellen Versorgung durch ein Wirbelkanalhämatom.
Cauda Equina-Syndrom Cauda equina-Syndrom (CES) wurde bei der Verwendung von kontinuierlichen spinalen Mikrokathetern berichtet. Die Verwendung von hyperbarem 5%igem Lidocain zur Spinalanästhesie ist mit einer erhöhten Inzidenz von CES verbunden, obwohl andere Lokalanästhetika eine Rolle gespielt haben.
Weitere Risikofaktoren für CES sind die Steinschnittlage, die wiederholte Gabe von Lokalanästhesielösung durch kontinuierliche Spinalkatheter und möglicherweise mehrere Einzelinjektionen von Spinalanästhetika.
Zu den Vorschlägen zur Prävention von CES nach Spinalanästhesie gehört die Aspiration von Liquor vor und nach der Injektion des Lokalanästhetikums. Einige schlagen vor, dass, wenn Liquor nicht aspiriert werden kann, nachdem die halbe Dosis injiziert wurde, keine volle Dosis verabreicht werden sollte.
Die Begrenzung der Menge an Lokalanästhetikum, die in den Subarachnoidalraum gegeben wird, kann helfen, CES zu verhindern.
Arachnoiditis Arachnoiditis kann nach spinaler Injektion einer Lokalanästhesielösung auftreten, ist aber auch dafür bekannt, dass sie nach intrathekaler Steroidinjektion auftritt. Zu den Ursachen der Arachnoiditis gehören Infektionen; Myelogramme von Farbstoffen auf Ölbasis; Blut im intrathekalen Raum; neuroreizende, neurotoxische oder neurolytische Substanzen; chirurgische Eingriffe an der Wirbelsäule; intrathekale Kortikosteroide; und Traumata. Arachnoiditis wurde nach traumatischer Durapunktion und nach unbeabsichtigter intrathekaler Injektion von Lokalanästhetika, Reinigungsmitteln, Antiseptika oder anderen Substanzen berichtet.
Periphere Nervenverletzung Eine Spinalanästhesie kann indirekt zu einer Verletzung peripherer Nerven führen. Die durch die Spinalanästhesie induzierte sensorische Nervenblockade hebt vorübergehend die normalen Schutzreflexe auf. Daher muss auf eine angemessene Positionierung, die Vermeidung enger Gipsverbände und die Beobachtung der distalen Zirkulation geachtet werden. Daher ist eine gute Pflege der durch die Spinalanästhesie gefühllos gewordenen Gliedmaßen unerlässlich.
Totale Spinalanästhesie Totale Spinalanästhesie (TSA) führt zu Atemdepression, kardiovaskulärer Beeinträchtigung und Bewusstlosigkeit. Dem können Taubheit, Parästhesien oder Schwäche der oberen Extremität vorausgehen oder nicht; Kurzatmigkeit; Brechreiz; oder Angst. Der Mechanismus von TSA ist unklar.
Die Bedeutung der Bereitstellung von kardiorespiratorischer Unterstützung und Anxiolyse wird durch die Behandlung absichtlicher TSA veranschaulicht. Die totale Spinalanästhesie wird therapeutisch bei hartnäckigen Erkrankungen eingesetzt Schmerz. Nach der Injektion von 20 ml 1.5 % Lidocain auf L3–L4-Ebene wurden die Patienten mit dem Kopf nach unten geneigt. Thiopental wurde verabreicht, um unangenehmen Empfindungen vorzubeugen. Nach Bewusstlosigkeit, Lähmung (ohne Muskelrelaxans) und Pupillenerweiterung wurde eine Larynxmaske (LMA) eingeführt und eine Überdruckbeatmung angewendet. Ephedrin und Atropin wurden bei Bedarf zur Herz-Kreislauf-Unterstützung eingesetzt. Für etwa eine Stunde war eine mechanische Beatmung erforderlich, danach wurde die LMA entfernt.
Herz-Kreislauf-Kollaps Nach einer Spinalanästhesie kann ein kardiovaskulärer Kollaps auftreten, obwohl dies ein seltenes Ereignis ist. Auroy und Mitarbeiter berichteten von 9 Herzstillständen bei 35,439 durchgeführten Spinalanästhesien. Siehe Abschnitt über kardiovaskuläre Wirkungen der Spinalanästhesie.
Abschätzung der Risiken der Hauptkomplikationen der Spinalanästhesie
Während geringfügige Risiken oft als Nebenwirkungen angesehen werden, sind größere Komplikationen für Kliniker und Patienten von größerer Bedeutung. Die Risikowahrnehmung kann durch aufsehenerregende Fallberichte wie die von Woolley und Roe beeinflusst werden. Frühe Bemühungen zur Risikobewertung wurden durch das Fehlen guter Daten zum Zähler (Anzahl der Komplikationen) und Nenner (Anzahl der Spinalnervenblockaden) behindert. Vandam und Dripps untersuchten die Aufzeichnungen von über 20 Spinalanästhetika, um „unbegründete klinische Eindrücke“ von Anästhesisten aus der Mitte des 10,000. Jahrhunderts zu korrigieren. Sie kamen zu dem Schluss, dass Einwände gegen die Spinalanästhesie unverdient seien. Retrospektive Daten aus Finnland für den Zeitraum 1987–1993 schätzten das Risiko schwerer Komplikationen nach Spinalanästhesie auf 1 zu 22,000. Es wurde angenommen, dass ein No-Fault-Kompensationsschema die Datengenauigkeit erhöht. Schwedische Daten (Moen) aus dem Zeitraum 1990–1999 ergaben ein ähnliches Risiko von 1 zu 20,000–30,000. Obwohl die skandinavischen Beweise damals gute Beweise waren, wurden sie wegen des retrospektiven Designs kritisiert, bei dem die Gefahr einer Unterberichterstattung besteht. Darüber hinaus geben Zählerdaten, die aus Verwaltungsdatenbanken stammen, möglicherweise weder die Ursache noch das Endergebnis an.
Auroy versuchte, Schwächen einer früheren Studie zu beheben, indem er eine Telefon-Hotline einrichtete, die eine gleichzeitige Bewertung der Kausalität ermöglichte. Diese prospektive Studie von 1998 bis 1999 untersuchte Komplikationen bei jeder Art von Regionalanästhesie. Die Ergebnisse von Auroy stützten sich auf freiwillige Beiträge französischer Anästhesisten (<6 % Teilnahmerate) und wurden möglicherweise durch unterschiedliche Komplikationsraten bei denjenigen verzerrt, die bereit waren, teilzunehmen. Eine Überprüfung aus dem Jahr 2007 ergab eine viel höhere Inzidenz neurologischer Komplikationen nach Spinalanästhesie in Auroys Arbeit (3.7–11.8 pro 10,000) im Vergleich zu Moens Arbeit (0.4 pro 10,000). Auroy hat im Gegensatz zu Moen periphere Neuropathie und Radikulopathie in die Zählerdaten aufgenommen.
Das Design einer prospektiven Studie zur genauen Quantifizierung des Risikos einer Spinalanästhesie war aufgrund der geringen Inzidenz schwerer Komplikationen schwierig. Der NAP3 des Royal College of Anesthetists ist die bisher beste Evidenz zu schwerwiegenden Komplikationen nach CNB. NAP3 ist aus mehreren Gründen bemerkenswert: Es ist die bisher größte prospektive Prüfung der CNB; es erreichte eine Rücklaufquote von 100 %; und es sammelte Zähler- und Nennerdaten aus einer Vielzahl von Quellen. Es untersuchte auch Kausalität und Ergebnis.
Zählerdaten in NAP3 bezogen sich auf schwerwiegende Komplikationen über einen Zeitraum von 12 Monaten (2006–2007). Berichte kamen von lokalen Krankenhausreportern und Klinikern. Gerichtsverfahren, medizinische Verteidigungsorganisationen, Zeitschriften und sogar Google-Suchen von Medienberichten wurden überprüft, um übersehene Komplikationen zu identifizieren. Als Komplikationen wurden Infektionen, Blutergüsse, Nervenverletzungen, Herz-Kreislauf-Kollaps und Irrwege klassifiziert. Insbesondere wurde PDPH nicht als Hauptkomplikation eingeschlossen. Komplikationen wurden von einem Gremium untersucht und die Wahrscheinlichkeit von CNB als Ursache festgestellt. Nennerdaten wurden aus einer zweiwöchigen Volkszählung bezogen und durch Kontaktaufnahme mit einer Reihe von Organisationen und Datenbanken validiert.
Die Erkenntnisse über bleibende Schäden wurden optimistisch oder pessimistisch dargestellt (vgl Tabelle 4). Optimistische Zahlen schlossen Komplikationen aus, bei denen eine Genesung wahrscheinlich oder die Kausalität schwach war.
TABELLE 4. Nützliche Zahlen zum Zitieren von Risiken für Patienten.
| Zentraler neuraxialer Block | Risiko (pessimistisch) | Risiko (optimistisch) |
|---|---|---|
| Dauerhafter Schaden durch schwere Komplikationen | 1 in 25,000 | 1 in 50,000 |
| Tod und Querschnittslähmung | 1 in 50,000 | 1 in 150,000 |
Der dauerhafte Schaden nach jeder Art von CNB lag pessimistisch bei 1:23,500 und optimistisch bei 1:50,500. Das Risiko für Tod oder Querschnittslähmung nach jeder Art von CNB lag pessimistisch bei 1:54,500 und optimistisch bei 1:141,500. Die Inzidenz von Komplikationen bei spinalen und kaudalen war mindestens halb so hoch wie bei Epiduralanästhesie und kombiniert spinal-epidural (CSE) Nervenblockaden. Von ungefähr 700,000 CNBs waren 46 % Wirbelsäulen. Obwohl die Autoren vor einer Subgruppenanalyse warnten, wurde festgestellt, dass die geburtshilfliche Einstellung eine geringe Inzidenz von Komplikationen aufwies, während die perioperative Einstellung für Erwachsene die höchsten Komplikationen aufwies. Eine vollständige oder nahezu vollständige neurologische Erholung trat in 61 % der Fälle auf.
Wichtig ist, dass NAP3 keine geringfügigen Komplikationen oder schwerwiegenden Komplikationen ohne dauerhaften Schaden untersuchte. Beispielsweise können Patienten einen kardiovaskulären Kollaps erlitten haben, der eine Intensivbehandlung erforderte, oder eine Meningitis hatten, aber da sie sich vollständig erholten, wurden sie sogar von der pessimistischen Berechnung ausgeschlossen. Dies sind Komplikationen, die ein Patient als schwerwiegend einstufen würde. Die Autoren räumten ein, dass ihre Zahlen eine minimal mögliche Inzidenz von Komplikationen darstellen; Andere haben jedoch spekuliert, dass sie das Risiko möglicherweise überschätzt haben. Da es keine Kontrollgruppe gab, kann NAP3 nicht beantworten, ob CNB sicherer ist als andere Techniken wie Vollnarkose.
Die NAP3-Studie hat uns versichert, dass bleibende Schäden als Folge einer Spinalanästhesie selten sind. Aufgrund des großen Anwendungsbereichs und der hervorragenden Methodik von NAP3 ist eine baldige Wiederholung einer ähnlichen Prüfung unwahrscheinlich. Es sollten Anstrengungen unternommen werden, um „geringfügige“ und „mittelschwere“ Komplikationen zu lindern, die unsere Patienten eher belasten. Insbesondere PDPH verdient besondere Aufmerksamkeit.
Dennoch treten größere Komplikationen auf, und es müssen alle Anstrengungen unternommen werden, um sie zu verhindern. Das Bewusstsein um das geringe Risiko schwerwiegender Komplikationen sollte nicht zu Selbstzufriedenheit führen.
Tatsächlich kann eine bestimmte Komplikation so selten werden, dass es unwahrscheinlich ist, dass ein einzelner Anästhesist ihr während seines ganzen Berufslebens begegnet. Angesichts der katastrophalen Natur solcher Komplikationen ist jedoch ständige Wachsamkeit von größter Bedeutung.
Indikationen und Vorteile der Spinalanästhesie
Indikationen
Die Spinalanästhesie bietet hervorragende Operationsbedingungen für Operationen unterhalb des Nabels. Daher wurde es auf den Gebieten der urologischen, gynäkologischen, geburtshilflichen und allgemeinen Unterbauch- und Perinealchirurgie verwendet. Ebenso wurde es in der vaskulären und orthopädischen Chirurgie der unteren Extremitäten verwendet. In jüngerer Zeit wird die Spinalanästhesie bei Operationen oberhalb des Nabels eingesetzt (siehe Abschnitt über laparoskopische Chirurgie).
Vorteile der Spinalanästhesie
Obwohl die Spinalanästhesie mit schätzungsweise 324,950 Spinalanästhesien pro Jahr allein im Vereinigten Königreich eine häufig verwendete Technik ist, sind die Vorteile für Mortalität und Morbidität schwer zu beweisen oder zu widerlegen. Es wurde die Hypothese aufgestellt, dass die Regionalanästhesie aufgrund der vorteilhaften Modulation der Stressreaktion sicherer wäre als die Vollnarkose. Die klinischen Studien waren jedoch widersprüchlich, und die Debatten über die Überlegenheit einer Technik gegenüber der anderen gehen weiter. Bewertungen der Vorteile der Spinalblockade werden durch die Heterogenität der Studien und Argumente darüber, ob die Analyse die Behandlungsabsicht beinhalten sollte, beunruhigt. Darüber hinaus beziehen sich viele Beweise für die Vorteile der neuraxialen Blockade auf die Epiduralanästhesie, und einige Übersichtsarbeiten unterscheiden nicht zwischen Spinal- und Epiduralanästhesie. Zum Beispiel hat sich gezeigt, dass CNB den Blutverlust und thromboembolische Ereignisse reduziert. Die Autoren dieser Studien waren jedoch klug, Wirbelsäulen- und Wirbelsäulenerkrankungen nicht zu analysieren Epidural Anästhesie einzeln, da die Stichprobengröße der Subgruppe unzureichend gewesen wäre. Weitere Studien sind erforderlich, um die relativen Vorteile jeder Technik aufzuklären.
Ein offensichtlicher Vorteil der Spinalanästhesie ist die Vermeidung der vielen Risiken einer Vollnarkose. Allerdings muss bedacht werden, dass immer die Möglichkeit einer Umstellung auf eine Vollnarkose besteht und eine notfallmäßige Vollnarkose riskanter sein kann als eine geplante Vollnarkose.
Spinalanästhesie ist in bestimmten klinischen Umgebungen vorteilhaft. Es ist heute üblich, dass Frauen mit Kaiserschnitt eine neuraxiale Nervenblockade haben. Die Spinalanästhesie vermeidet die mit der Vollnarkose verbundenen Probleme schwanger Patienten, insbesondere Risiken eines schwierigen Atemwegs, Bewusstseins und Aspiration. Beziehen auf Geburtshilfe Regionalanästhesie.
Es wurde festgestellt, dass der mütterliche Blutverlust bei Spinalanästhesie geringer ist als bei Vollnarkose. Sinkende Müttersterblichkeitsraten wurden auf die zunehmende Praxis der Regionalanästhesie zurückgeführt. Darüber hinaus ermöglicht die Regionalanästhesie, dass eine Mutter bei der Geburt wach ist und auf Wunsch ein Partner anwesend ist. Ein Cochrane-Review ergab jedoch keine Hinweise auf die Überlegenheit der Regionalanästhesie gegenüber der Allgemeinanästhesie in Bezug auf schwerwiegende mütterliche oder neonatale Ergebnisse. Ebenso zeigte eine Metaanalyse aus dem Jahr 2005, dass der pH-Wert der Nabelschnur, ein Indikator für das Wohlbefinden des Fötus, im Vergleich zur Wirbelsäule niedriger ist mit Peridural- und Allgemeinanästhesie, obwohl dies möglicherweise auf die Verwendung von Ephedrin in den analysierten Studien zurückzuführen ist.
Dennoch bleibt die Spinalanästhesie aufgrund ihrer Sicherheit, Zuverlässigkeit und Patientenerwartung die Technik der Wahl für viele geburtshilfliche Anästhesisten.
Eine Überprüfung der „Best Practice“ für Hüftfrakturen aus dem Jahr 2005 ergab, dass die Spinalanästhesie konsistente Vorteile hat, und empfahl die Verwendung einer Regionalanästhesie „wann immer möglich“. Zu den genannten Vorteilen gehörten eine geringere Sterblichkeit, tiefe Venenthrombose (DVT), Transfusionsanforderungen und pulmonale Komplikationen. Diese Empfehlungen, die auf zwei Reviews basieren, verdeutlichen jedoch die Mängel der verfügbaren Evidenz. Die erste Überprüfung hatte eine heterogene Population und eine begrenzte Aussagekraft für die Subgruppenanalyse; Eine Übertragbarkeit der Befunde auf die Spinalanästhesie bei Hüftfrakturoperationen ist daher fraglich. Die zweite Überprüfung ergab nur einen grenzwertigen Unterschied in der Sterblichkeit nach 1 Monat und keinen Unterschied nach 3 Monaten. Darüber hinaus wiesen alle eingeschlossenen Studien methodische Mängel auf.
Die Stressreaktion auf Herzoperationen wird durch intrathekales Bupivacain in Kombination mit Allgemeinanästhesie reduziert122 und teilweise durch intrathekales Morphin abgeschwächt. Es hat sich gezeigt, dass niedrig dosiertes intrathekales Morphin (259 ± 53 μg) die frühe Extubation nach einer Herzoperation erleichtert. Eine Metaanalyse von intrathekalem Morphin in der Herzchirurgie zeigte eine mäßige Abnahme des Morphinverbrauchs und der Schmerzscores, obwohl eine frühere Extubation nur bei einer Untergruppe von Patienten beobachtet wurde, die weniger als 500 μg intrathekales Morphin erhielten.
Da die moderne Anästhesie und perioperative Versorgung sicherer werden, wird es immer schwieriger, einen Vorteil einer Technik gegenüber einer anderen nachzuweisen. Die ideale Technik kann tatsächlich eine Permutation von Vollnarkose, neuraxialer Nervenblockade, peripherer Nervenblockade oder lokaler Infiltrationsanalgesie sein.
Spinalanästhesie: Die endgültige Nutzen-Risiko-Analyse
Sobald der Anästhesist mit den Beweisen zu den Risiken und Vorteilen der Spinalanästhesie ausgestattet ist, muss er entscheiden, ob die Beweise für den einzelnen Patienten und die klinische Situation gelten. Obwohl Komplikationen verheerend sein können, versicherte uns NAP3, dass größere Komplikationen bei der Spinalanästhesie selten sind. Überzeugende Vorteile sind schwerer nachzuweisen, dennoch gibt es Vorteile in bestimmten klinischen Situationen. Außerdem muss das Nutzen-Risiko-Verhältnis mit dem Nutzen-Risiko-Verhältnis verfügbarer Alternativen verglichen werden. Der historische Anstieg der Sicherheit der Spinalanästhesie ging mit einem Anstieg der Sicherheit alternativer Techniken einher, darunter Epiduralanästhesie, periphere Nervenblockade, lokale Infiltrationsanästhesie und natürlich Vollnarkose. Dieser Wettbewerb zwischen alternativen Techniken wird wahrscheinlich weitergehen. Darüber hinaus können verschiedene Modalitäten in Verbindung verwendet werden, was die endgültige Entscheidung erschwert. Der moderne Anästhesist muss diese Matrix von Nutzen-Risiko-Verhältnissen berücksichtigen, was den Rahmen dieses Kapitels sprengen würde.
FUNKTIONELLE ANATOMIE DES WIRBELSÄULEN-Blocks
Bei der Überprüfung der Funktionelle Anatomie einer Spinalblockade muss eine genaue Kenntnis der Wirbelsäule, des Rückenmarks und der Spinalnerven vorhanden sein. Dieses Kapitel gibt einen kurzen Überblick über die Anatomie, Oberflächenanatomie und Sonoanatomie des Rückenmarks.
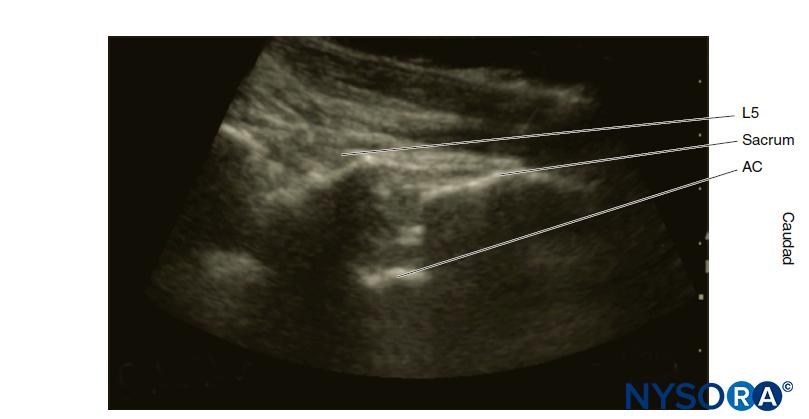
Die Wirbelsäule besteht aus 33 Wirbeln: 7 Hals-, 12 Brust-, 5 Lenden-, 5 Sakral- und 4 Steißbeinsegmente. Die Wirbelsäule enthält normalerweise drei Kurven. Die zervikalen und lumbalen Krümmungen sind anterior konvex, und die thorakale Krümmung ist posterior konvex. Die Krümmung der Wirbelsäule beeinflusst zusammen mit der Schwerkraft, der Barizität des Lokalanästhetikums und der Patientenposition die Ausbreitung des Lokalanästhetikums im Subarachnoidalraum. Figure 1 zeigt die Wirbelsäule, Wirbel und Bandscheiben und Foramina.
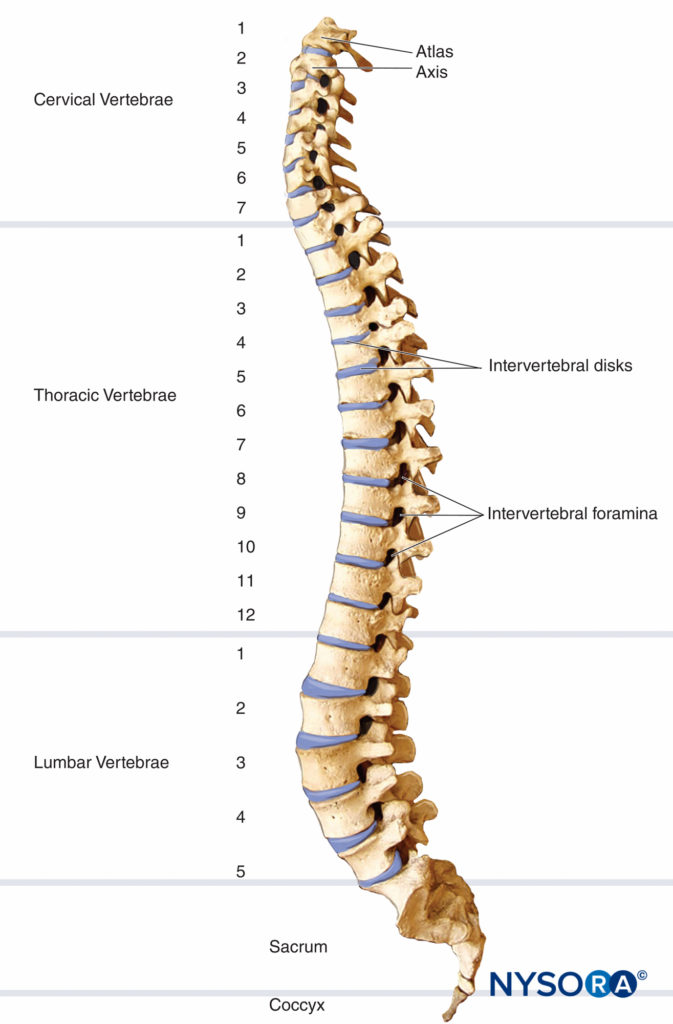
ABBILDUNG 1. Wirbelsäule, Wirbel und Bandscheiben und Foramina.
Fünf Bänder halten die Wirbelsäule zusammen (Figure 2). Die Ligamenta supraspinale verbinden die Spitzen der Dornfortsätze vom siebten Halswirbel (C7) mit dem Kreuzbein. Das Ligamentum supraspinale ist im Bereich oberhalb von C7 als Ligamentum nuchae bekannt. Die interspinalen Bänder verbinden die Dornfortsätze miteinander. Das Ligamentum flavum oder gelbes Band verbindet die Laminae oben und unten miteinander. Schließlich binden die hinteren und vorderen Längsbänder die Wirbelkörper zusammen.
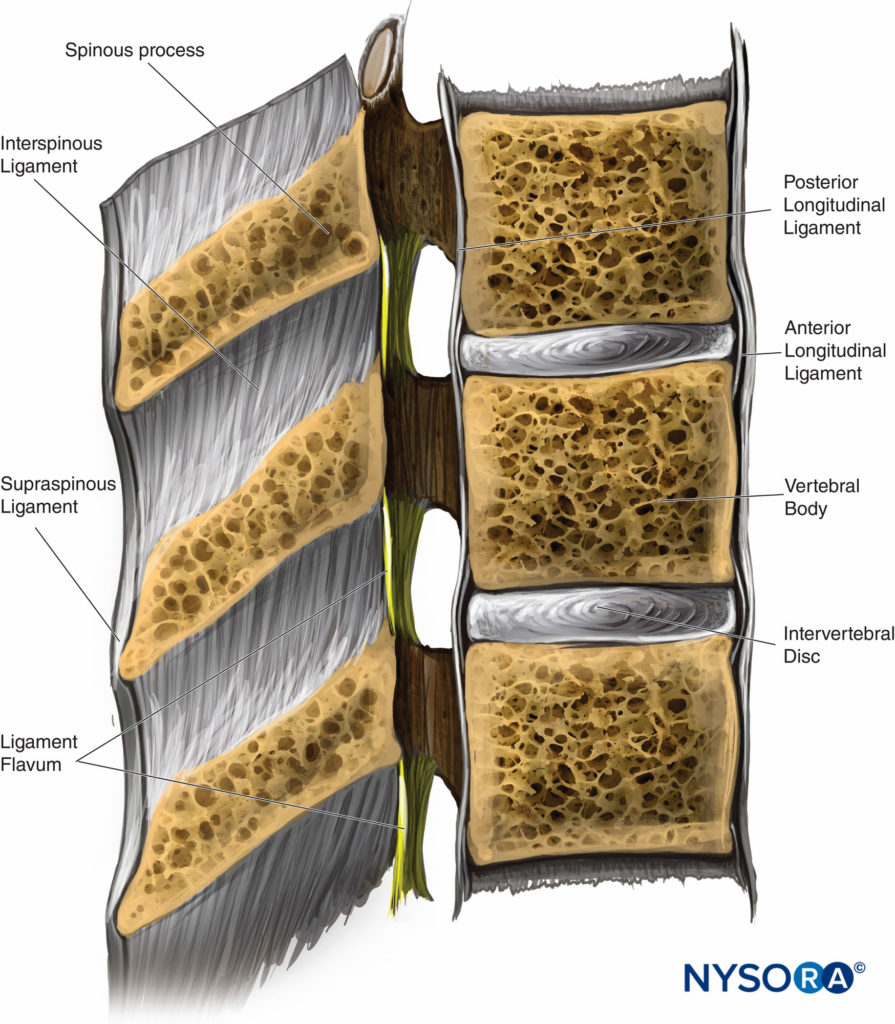
ABBILDUNG 2. Querschnitt des Spinalkanals und der angrenzenden Bänder. (Wiedergabe mit freundlicher Genehmigung von Leffert LR, Schwamm LH: Neuraxiale Anästhesie bei Gebärenden mit intrakranieller Pathologie: eine umfassende Überprüfung und Neubewertung des Risikos. Anesthesiology. 2013 Sep;119(3):703-718.)
Die Drei Membranen die das Rückenmark schützen, sind die Dura mater, die Arachnoidea und die Pia mater. Die Dura Mater oder zähe Mutter ist die äußerste Schicht. Der Duralsack erstreckt sich bis zum zweiten Sakralwirbel (S2). Die Arachnoidea ist die mittlere Schicht, und der Subduralraum liegt zwischen der Dural- und der Arachnoidea. Die Arachnoidea mater oder Spinnennetzmutter endet ebenfalls bei S2, wie der Duralsack. Die Pia mater oder weiche Mutter haftet an der Oberfläche des Rückenmarks und endet im Filum Terminale, das hilft, das Rückenmark am Kreuzbein zu halten. Der Raum zwischen der Arachnoidea und der Pia mater ist als Subarachnoidalraum bekannt, und die Spinalnerven verlaufen in diesem Raum, ebenso wie der Liquor. Figure 3 zeigt das Rückenmark, dorsale Wurzelganglien und ventrale Wurzeln, Spinalnerven, sympathischen Stamm, rami communicantes und Pia, Arachnoidea und Dura maters.
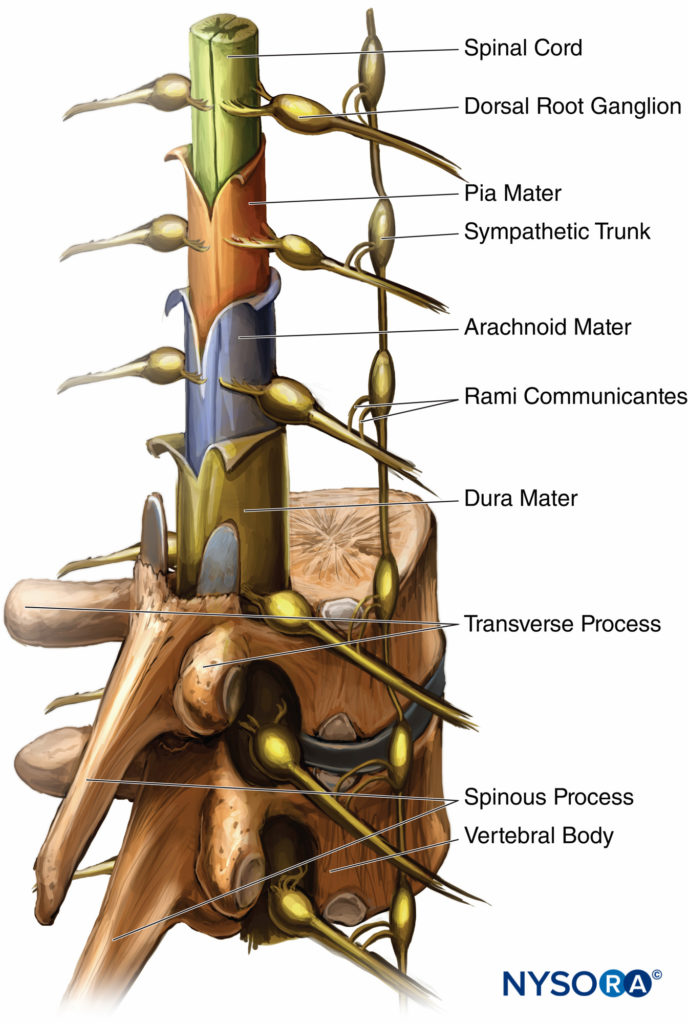
ABBILDUNG 3. Rückenmark mit meningealen Schichten, Spinalganglien und dem sympathischen Nervenstamm.
Bei der Durchführung einer Spinalanästhesie über den Mittellinienzugang sind die anatomischen Schichten, die (von posterior nach anterior) durchlaufen werden, Haut, subkutanes Fett, Ligamentum supraspinale, Ligamentum interspinale, Ligamentum flavum, Dura mater, Subduralraum, Arachnoidea mater und schließlich die Subarachnoidalraum. Wenn die paramediane Technik angewendet wird, sollte die Spinalnadel die Haut, das subkutane Fettgewebe, den paraspinösen Muskel, das Ligamentum flavum, die Dura mater, den Subduralraum und die Arachnoidea durchqueren und dann in den Subarachnoidalraum vordringen.
NYSORA-Tipps
Bei der Durchführung einer Spinalanästhesie über den Mittellinienansatz werden die anatomischen Schichten (von posterior nach anterior) durchquert
• Haut
• Subkutanes Fett
• Ligamentum supraspinale
• Ligamentum interspinale
• Ligamentum flavum
• Dura Mater
• Subduralraum
• Arachnoidea mater
• Subarachnoidalraum
Bei der Durchführung einer Spinalanästhesie über den paramedianen Zugang sollte die Spinalnadel traversieren
• Haut
• Subkutanes Fett
• Paraspinaler Muskel
• Ligamentum flavum
• Dura Mater
• Subduralraum
• Arachnoidea mater
• Subarachnoidalraum
Die Anatomie des Subduralraums erfordert besondere Aufmerksamkeit. Der Subduralraum ist eine meningeale Ebene, die zwischen der Dura und der Arachnoidea liegt und sich von der Schädelhöhle bis zum zweiten Kreuzbeinwirbel erstreckt. Eine ultrastrukturelle Untersuchung hat gezeigt, dass dies ein erworbener Raum ist, der erst nach dem Aufreißen von Neurothelzellen innerhalb des Raums real wird. Der Subduralraum erstreckt sich seitlich um die dorsale Nervenwurzel und das Ganglion. Die potenzielle Kapazität des Subduralraums neben den ventralen Nervenwurzeln ist geringer. Dies kann die Schonung der vorderen motorischen und sympathischen Fasern während der subduralen Nervenblockade (SDB) erklären (Figure 4).

ABBILDUNG 4. Epiduralkatheter im Subduralraum. Verbesserte Ansicht eines Epiduralkatheters in einem subduralen Raum, erhalten von einer Leiche unter dem Rasterelektronenmikroskop. Vergrößerung ×20. (Wiedergabe mit freundlicher Genehmigung von Reina MA, Collier CB, Prats-Galino A, et al.: Unintentional subdural placement of epiduralcatheters during tryed epidural ansthetics: an anatomic study of spinal subdural Compartment. Reg Anesth Pain Med. 2011 Nov-Dez;36( 6):537-541.)
Die Länge des Rückenmarks variiert je nach Alter. Im ersten Trimester erstreckt sich das Rückenmark bis zum Ende der Wirbelsäule, aber mit zunehmendem Alter des Fötus verlängert sich die Wirbelsäule stärker als das Rückenmark. Bei der Geburt endet das Rückenmark etwa bei L3. Beim Erwachsenen liegt das als Conus edullaris bekannte Ende des Rückenmarks ungefähr bei L1. Allerdings haben MRT- und Leichenstudien einen Conus medullaris unterhalb von L1 bei 19–58 % und unterhalb von L2 bei 0–5 % gemeldet. Der Conus medullaris kann irgendwo zwischen T12 und L3 liegen.
Figure 5 Zeigt einen Querschnitt der Lendenwirbel und des Rückenmarks. Dargestellt sind die typische Lage von Conus medullaris, Cauda equina, Duralsackende und Filum terminale. Bei einem Erwachsenen wurde über ein sakrales Rückenmark berichtet, obwohl dies äußerst selten vorkommt. Bei einer neuroaxialen Anästhesie muss immer auf die Länge des Rückenmarks geachtet werden, da eine Injektion in das Rückenmark große Schäden verursachen und zu Lähmungen führen kann.
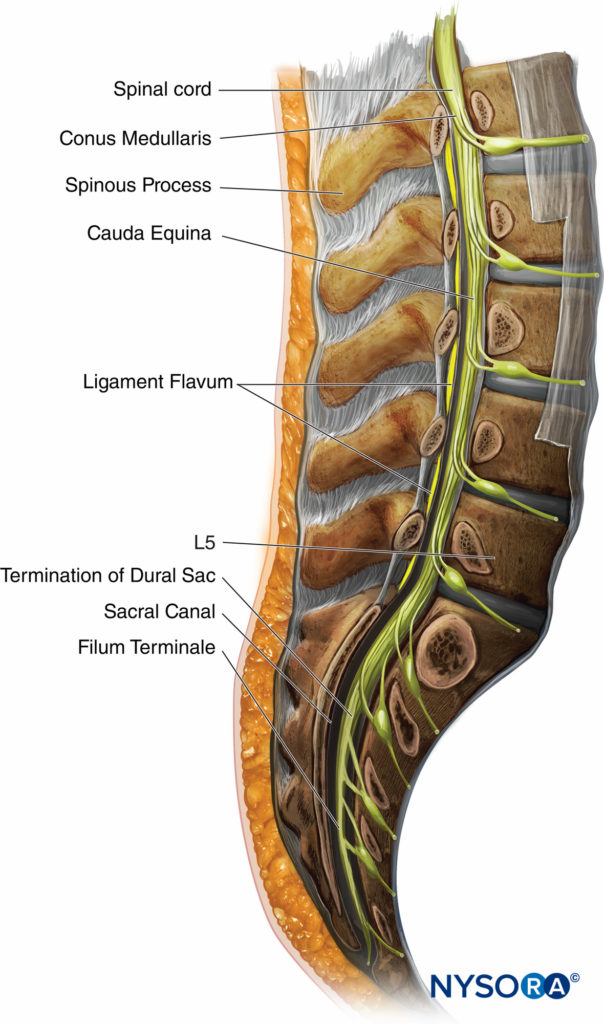
ABBILDUNG 5. Querschnitt der Lendenwirbel.
Es gibt acht zervikale Spinalnerven und sieben Halswirbel. Die zervikalen Spinalnerven 1 bis 7 sind nach dem darunter liegenden Wirbelkörper nummeriert. Der achte Halsnerv tritt unterhalb des siebten Halswirbelkörpers aus. Darunter sind die Spinalnerven entsprechend dem darüber liegenden Wirbelkörper nummeriert. Die Spinalnervenwurzeln und das Rückenmark dienen als Zielorte für die Spinalanästhesie.
Oberflächenanatomie
Bei der Vorbereitung auf eine Spinalanästhesie-Blockade ist es wichtig, Orientierungspunkte am Patienten genau zu identifizieren.
Die Mittellinie wird durch Abtasten der Dornfortsätze identifiziert. Die Beckenkämme befinden sich in der Regel auf gleicher vertikaler Höhe wie der vierte lumbale Dornfortsatz oder der Zwischenraum zwischen dem vierten und fünften Lendenwirbel. Zwischen den Beckenkämmen kann eine interkristalline Linie gezogen werden, um diesen Zwischenraum zu lokalisieren. Es muss darauf geachtet werden, den weichen Bereich zwischen den Dornfortsätzen zu ertasten, um den Zwischenraum zu lokalisieren. Abhängig von der für die Operation erforderlichen Anästhesiestärke und der Fähigkeit, den Zwischenraum zu fühlen, kann der L3-L4-Zwischenraum oder der L4-L5-Zwischenraum zum Einführen der Spinalnadel verwendet werden. Da das Rückenmark üblicherweise auf der L1-zu-L2-Ebene endet, ist es üblich, auf oder über dieser Ebene keine Spinalanästhesie zu versuchen. In jüngerer Zeit wurde die segmentale Thorax-Spinal-Anästhesie beschrieben.
Es wäre unvollständig, die Oberfläche zu diskutieren Anatomie ohne die für die Spinalanästhesie wichtigen Dermatome zu erwähnen. Ein Dermatom ist ein Hautbereich, der von sensorischen Fasern eines einzelnen Spinalnerven innerviert wird. Das zehnte thorakale (T10) Dermatom entspricht dem Nabel, das sechste thorakale (T6) Dermatom dem Xiphoid und das vierte thorakale (T4) Dermatom den Brustwarzen. Figure 6 illustriert die Dermatome des menschlichen Körpers. Um eine chirurgische Anästhesie für einen bestimmten Eingriff zu erreichen, muss das Ausmaß der Spinalanästhesie ein bestimmtes dermatomales Niveau erreichen. Dermatomale Ebenen der Spinalanästhesie für gängige chirurgische Eingriffe sind in aufgeführt Tabelle 5.
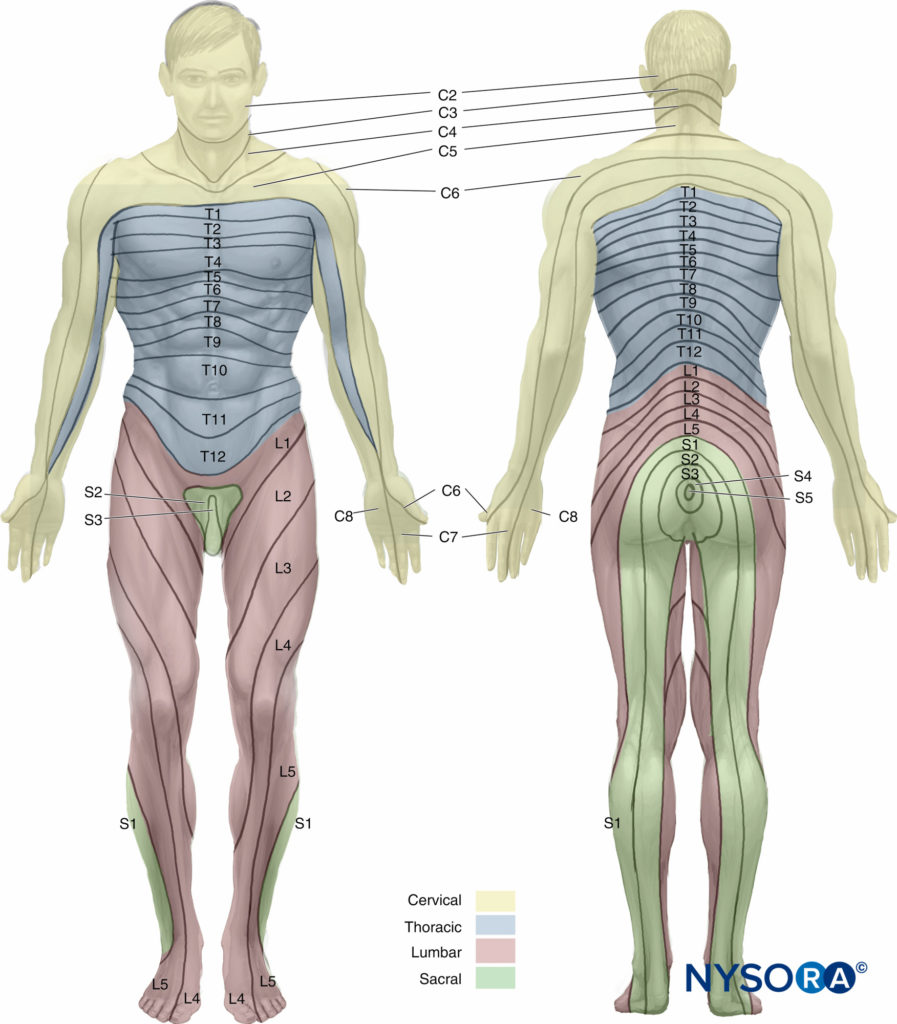
ABBILDUNG 6. Dermatome des menschlichen Körpers.
TABELLE 5. Dermatomale Ebenen der Spinalanästhesie für gängige chirurgische Eingriffe.
| Verfahren | Dermatomebene |
|---|---|
| Oberbauchchirurgie | T4 |
| Darm-, gynäkologische und urologische Chirurgie | T6 |
| Transurethrale Resektion des Prostata | T10 |
| Vaginale Geburt eines Fötus und Hüftoperation | T10 |
| Oberschenkeloperation und Unterschenkel Amputationen | L1 |
| Fuß- und Sprunggelenksoperation | L2 |
| Damm- und Analchirurgie | S2 bis S5 (Sattelblock) |
NYSORA-Tipps
• T10-Dermatom entspricht dem Nabel.
• T6-Dermatom entspricht dem Xiphoid.
• T4 Dermatom entspricht den Brustwarzen.
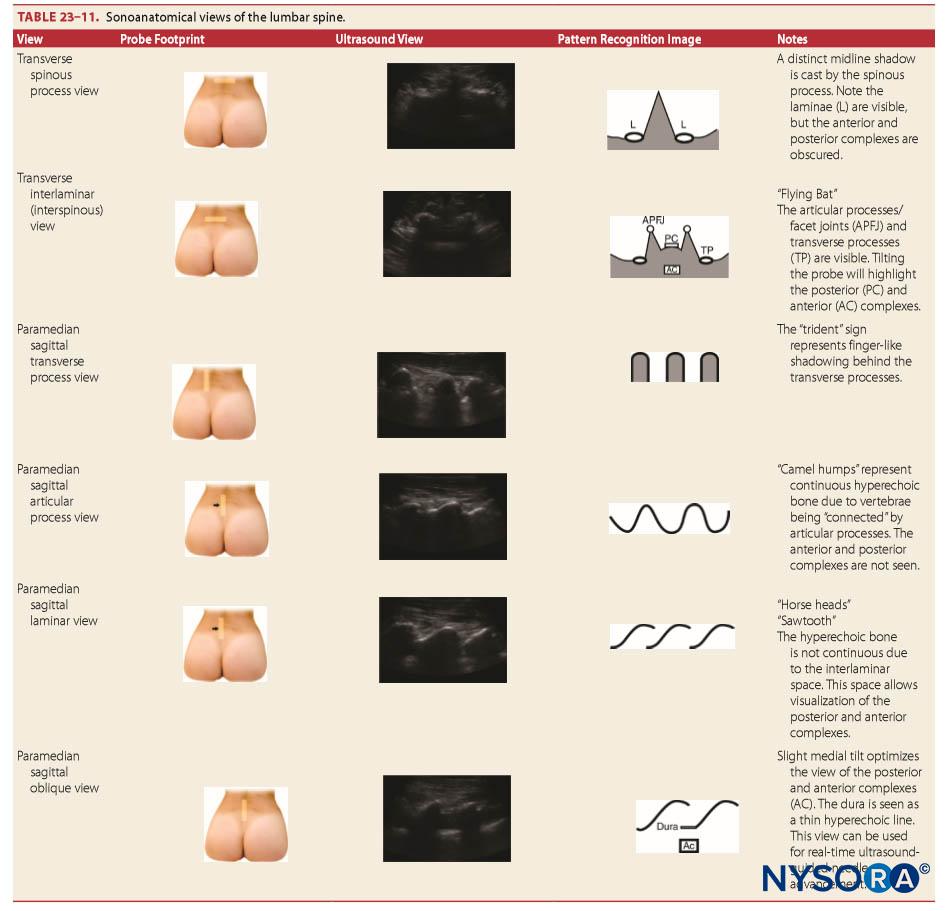
Sonoanatomie
„Oberflächen“-Anatomie bezieht sich auf Strukturen, die nahe genug an der Haut sind, dass sie tastbar sind. Aufgrund des Körperhabitus ist dies jedoch möglicherweise nicht möglich. Neuroaxialer Ultraschall ermöglicht die sonoanatomische Visualisierung dieser Strukturen und tieferer Strukturen. Da der Ultraschallstrahl jedoch die knöchernen Wirbel nicht durchdringen kann, sind spezielle Ultraschallfenster erforderlich, um die Neuraxis sichtbar zu machen. Die Technik des neuraxialen Ultraschalls wird an anderer Stelle diskutiert (siehe Abschnitt über neuere Entwicklungen in der Spinalanästhesie).
PHARMAKOLOGIE
Die Wahl des Lokalanästhetikums basiert auf der Wirksamkeit des Mittels, dem Beginn und der Dauer der Anästhesie und den Nebenwirkungen des Arzneimittels. In der Spinalanästhesie werden zwei unterschiedliche Gruppen von Lokalanästhetika verwendet, Ester und Amide, die durch die Bindung gekennzeichnet sind, die den aromatischen Teil und die Zwischenkette verbindet.
Ester enthalten eine Esterbindung zwischen dem aromatischen Teil und der Zwischenkette, und Beispiele umfassen Procain, Chlorprocain und Tetracain. Amide enthalten eine Amidbindung zwischen dem aromatischen Teil und der Zwischenkette, und Beispiele schließen Bupivacain, Ropivacain, Etidocain, Lidocain, Mepivacain und Prilocain ein. Obwohl der Metabolismus für die Bestimmung der Aktivität von Lokalanästhetika wichtig ist, beeinflussen auch Lipidlöslichkeit, Proteinbindung und pKa die Aktivität.
NYSORA-Tipps
• Die Wirksamkeit von Lokalanästhetika hängt von der Lipidlöslichkeit ab.
• Die Wirkungsdauer eines Lokalanästhetikums wird durch die Proteinbindung beeinflusst.
• Der Wirkungseintritt hängt von der Menge des in der Grundform verfügbaren Lokalanästhetikums ab.
Die Lipidlöslichkeit bezieht sich auf die Potenz von Lokalanästhetika. Eine geringe Lipidlöslichkeit weist darauf hin, dass höhere Konzentrationen des Lokalanästhetikums verabreicht werden müssen, um eine Nervenblockade zu erreichen. Umgekehrt erzeugt eine hohe Lipidlöslichkeit eine Anästhesie bei niedrigen Konzentrationen. Die Proteinbindung beeinflusst die Wirkungsdauer eines Lokalanästhetikums. Eine höhere Proteinbindung führt zu einer längeren Wirkungsdauer. Der pKa eines Lokalanästhetikums ist der pH-Wert, bei dem ionisierte und nichtionisierte Formen gleichermaßen in Lösung vorhanden sind, was wichtig ist, da die nichtionisierte Form es dem Lokalanästhetikum ermöglicht, durch die lipophile Nervenscheide zu diffundieren und die Natriumkanäle in der Nervenmembran zu erreichen. Der Wirkungseintritt bezieht sich auf die Menge des in der Grundform verfügbaren Lokalanästhetikums. Die meisten Lokalanästhetika folgen der Regel, dass die Wirkung umso schneller einsetzt, je niedriger der pKa-Wert ist und umgekehrt. Bitte beziehen Sie sich auf Klinische Pharmakologie der Lokalanästhetika.
Pharmakokinetik von Lokalanästhetika im Subarachnoidalraum
Die Pharmakokinetik von Lokalanästhetika umfasst die Aufnahme und Ausscheidung des Arzneimittels. Bei der Aufnahme von Lokalanästhetika aus dem Subarachnoidalraum in neuronales Gewebe spielen vier Faktoren eine Rolle: (1) Konzentration des Lokalanästhetikums im Liquor, (2) Oberfläche des dem Liquor ausgesetzten Nervengewebes, (3) Lipidgehalt des Nervengewebes, und (4) Blutfluss zum Nervengewebe.
Die Aufnahme des Lokalanästhetikums ist an der Stelle der höchsten Konzentration im Liquor am größten und nimmt oberhalb und unterhalb dieser Stelle ab. Wie zuvor diskutiert, werden die Aufnahme und Ausbreitung von Lokalanästhetika nach einer Spinalinjektion durch mehrere Faktoren bestimmt, einschließlich Dosis, Volumen und Barizität des Lokalanästhetikums und der Positionierung des Patienten. Sowohl die Nervenwurzeln als auch das Rückenmark nehmen nach Injektion in den Subarachnoidalraum Lokalanästhetika auf. Je mehr Oberfläche der Nervenwurzel freigelegt ist, desto größer ist die Aufnahme des Lokalanästhetikums. Das Rückenmark hat zwei Mechanismen zur Aufnahme von Lokalanästhetika. Der erste Mechanismus ist die Diffusion vom Liquor zur Pia mater und in das Rückenmark, was ein langsamer Prozess ist. Nur der oberflächlichste Teil des Rückenmarks ist von der Diffusion von Lokalanästhetika betroffen. Die zweite Methode der Aufnahme von Lokalanästhetika ist die Ausdehnung in die Räume von Virchow-Robin, die die Bereiche der Pia Mater sind, die die Blutgefäße umgeben, die das zentrale Nervensystem durchdringen. Die Virchow-Robin-Räume verbinden sich mit den perineuronalen Spalten, die die Nervenzellkörper im Rückenmark umgeben, und dringen in die tieferen Bereiche des Rückenmarks vor. Figure 7 ist eine Darstellung der periarteriellen Virchow-Robin-Räume um das Rückenmark herum.
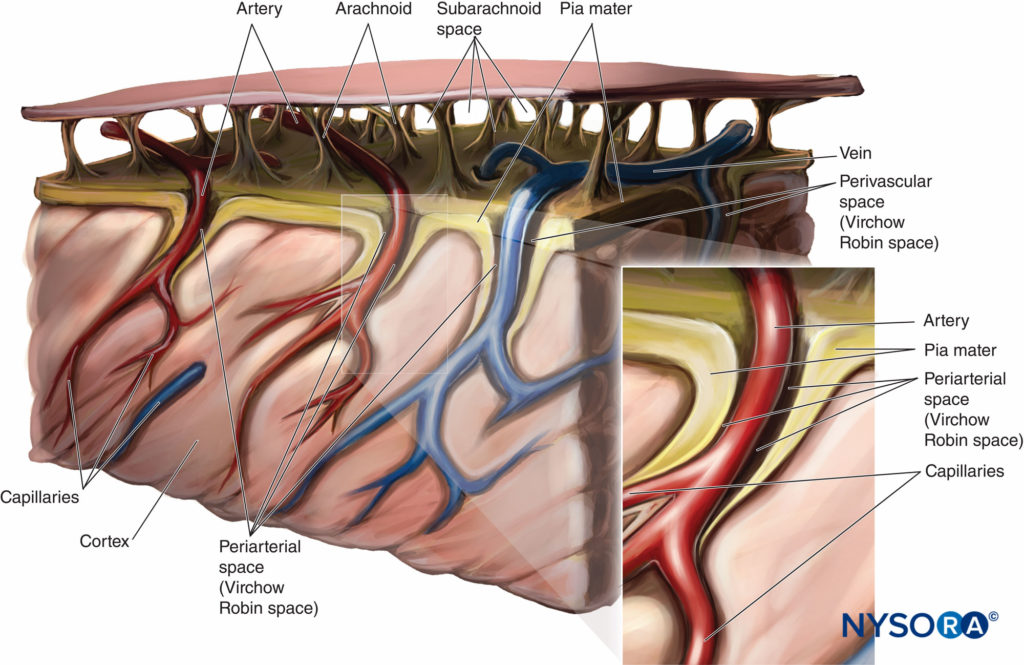
ABBILDUNG 7. Virchow-Robin-Raum.
NYSORA-Tipps
Die drei wichtigsten modifizierbaren Faktoren bei der Bestimmung der Verteilung von Lokalanästhetika sind:
• Barizität der Lokalanästhesielösung
• Position des Patienten während und direkt nach der Injektion
• Dosis des injizierten Anästhetikums
Der Lipidgehalt bestimmt die Aufnahme von Lokalanästhetika. Stark myelinisiertes Gewebe im Subarachnoidalraum enthält nach der Injektion höhere Konzentrationen von Lokalanästhetika. Je höher der Myelinisierungsgrad ist, desto höher ist die Konzentration des Lokalanästhetikums, da das Myelin einen hohen Lipidgehalt hat. Wenn ein Bereich der Nervenwurzel kein Myelin enthält, besteht in diesem Bereich ein erhöhtes Risiko einer Nervenschädigung.
Der Blutfluss bestimmt die Entfernungsrate von Lokalanästhetika aus dem Rückenmarksgewebe. Je schneller das Blut im Rückenmark fließt, desto schneller wird das Anästhetikum weggespült. Dies kann teilweise erklären, warum die Konzentration von Lokalanästhetika im hinteren Rückenmark größer ist als im vorderen Rückenmark, obwohl das vordere Rückenmark leichter von den Virchow-Robin-Räumen zugänglich ist. Nach der Verabreichung eines Spinalanästhetikums kann der Blutfluss zum Rückenmark erhöht oder verringert werden, abhängig von dem jeweiligen verabreichten Lokalanästhetikum; Beispielsweise erhöht Tetracain den Nabelschnurfluss, aber Lidocain und Bupivacain verringern ihn, was die Eliminierung des Lokalanästhetikums beeinflusst.
Die Elimination des Lokalanästhetikums aus dem Subarachnoidalraum erfolgt durch vaskuläre Absorption im Epiduralraum und im Subarachnoidalraum. Lokalanästhetika wandern in beide Richtungen über die Dura. Im Epiduralraum kann es ebenso wie im Subarachnoidalraum zu Gefäßresorptionen kommen. Die Gefäßversorgung des Rückenmarks besteht aus Gefäßen, die sich auf dem Rückenmark und in der Pia mater befinden. Da die vaskuläre Durchblutung des Rückenmarks unterschiedlich ist, variiert die Eliminationsrate von Lokalanästhetika.
Vertrieb
Die Verteilung und Konzentrationsabnahme von Lokalanästhetika richtet sich nach dem Bereich der höchsten Konzentration, der unabhängig von der Injektionsstelle sein kann. Viele Faktoren beeinflussen die Verteilung von Lokalanästhetika im Subarachnoidalraum. Tabelle 6 listet einige dieser Faktoren auf.
TABELLE 6. Determinanten der Ausbreitung von Lokalanästhetika im Subarachnoidalraum.
| Eigenschaften der Lokalanästhesielösung • Barizität • Dosis • Lautstärke • Spezifisches Gewicht |
| Patientencharakteristika • Position während und nach der Injektion • Größe (extrem klein oder groß) • Anatomie der Wirbelsäule • Verringertes Liquorvolumen (erhöhter intraabdomineller Druck aufgrund von Gewichtszunahme, Schwangerschaft usw.) |
| Technik • Injektionsstelle • Richtung der Nadelabschrägung |
Die Barizität spielt eine wichtige Rolle bei der Bestimmung der Ausbreitung des Lokalanästhetikums im Spinalraum und ist gleich der Dichte des Lokalanästhetikums dividiert durch die Dichte des Liquors bei 37°C. Lokalanästhetika können im Vergleich zum Liquor hyperbar, hypobar oder isobar sein, und Barizität ist die Hauptdeterminante dafür, wie das Lokalanästhetikum verteilt wird, wenn es in den Liquor injiziert wird. Tabelle 7 vergleicht die Dichte, das spezifische Gewicht und die Barizität verschiedener Substanzen und Lokalanästhetika.
TABELLE 7. Dichte, spezifisches Gewicht und Barizität verschiedener Substanzen und Lokalanästhetika.
| Signaldichte | Spezifisches Gewicht | Barizität | ||
|---|---|---|---|---|
| Wasser | 0.9933 | 1.0000 | 0.9930 | |
| Zerebrospinalflüssigkeit | 1.0003 | 1.0069 | 1.0000 | |
| Hypobar | ||||
| • Tetracain | 0.33 % in Wasser | 0.9980 | 1.0046 | 0.9977 |
| • Lidocain | 0.5 % in Wasser | N / A | 1.0038 | 0.9985 |
| Isobar | ||||
| • Tetracain | 0.5 % in 50 % CSF | 0.9998 | 1.0064 | 0.9995 |
| • Lidocain | 2 % in Wasser | 1.0003 | 1.0066 | 1.0003 |
| • Bupivacain | 0.5 % in Wasser | 0.9993 | 1.0059 | 0.9990 |
| Überdruck | ||||
| • Tetracain | 0.5 % in 5 % Dextrose | 1.0136 | 1.0203 | 1.0133 |
| • Lidocain | 5 % in 7.5 % Dextrose | 1.0265 | 1.0333 | 1.0265 |
| • Bupivacain | 0.5 % in 8 % Dextrose | 1.0210 | 1.0278 | 1.0207 |
| • Bupivacain | 0.75 % in 8 % Dextrose | 1.0247 | 1.0300 | 1.0227 |
Hypobare Lösungen sind weniger dicht als CSF und neigen dazu, gegen die Schwerkraft aufzusteigen. Isobare Lösungen sind so dicht wie CSF und neigen dazu, auf dem Niveau zu bleiben, auf dem sie injiziert wurden. Überdrucklösungen sind dichter als CSF und neigen dazu, nach der Injektion der Schwerkraft zu folgen.
Hypobare Lösungen haben eine Barizität von weniger als 1.0 relativ zu Liquor und werden normalerweise durch Zugabe von destilliertem sterilem Wasser zum Lokalanästhetikum hergestellt. Tetracain, Dibucain und Bupivacain wurden alle als hypobare Lösungen in der Spinalanästhesie verwendet. Die Positionierung des Patienten ist nach der Injektion eines hypobaren Spinalanästhetikums wichtig, da die ersten Minuten die Ausbreitung der Anästhesie bestimmen. Befindet sich der Patient nach der Injektion in Trendelenburg-Lage, breitet sich das Anästhetikum in kaudaler Richtung aus, und wenn sich der Patient in umgekehrter Trendelenburg-Lage befindet, breitet sich das Anästhetikum nach der Injektion kranial aus.
Die Barizität isobarer Lösungen ist gleich 1.0. Tetracain und Bupivacain wurden beide erfolgreich für die isobare Spinalanästhesie verwendet. Anders als bei hypo- oder hyperbaren Lokalanästhetika spielt die Schwerkraft bei der Ausbreitung isobarer Lösungen keine Rolle. Daher hat die Patientenpositionierung keinen Einfluss auf die Ausbreitung isobarer Lösungen. Die Injektion kann in jeder Position vorgenommen werden, und dann kann der Patient in die für die Operation erforderliche Position gebracht werden.
Überdrucklösungen haben eine Barizität von mehr als 1.0. Eine Lokalanästhesielösung kann durch Zugabe von Dextrose oder Glucose hyperbar gemacht werden. Bupivacain, Lidocain und Tetracain wurden alle als hyperbare Lösungen in der Spinalanästhesie verwendet. Die Patientenpositionierung beeinflusst die Ausbreitung des Anästhetikums. Bei einem Patienten in Trendelenburg-Position würde das Anästhetikum in kraniale Richtung wandern und umgekehrt.
Dosis und Volumen spielen beide eine Rolle bei der Verteilung von Lokalanästhetika nach einer Spinalinjektion. Weitere Informationen finden Sie im Abschnitt Volumen, Konzentration und Dosis des Lokalanästhetikums.
Auswirkungen des Volumens der lumbalen Zisterne auf die Höhe der Nervenblockade
Liquor wird im Gehirn mit 0.35 ml/min produziert und füllt den Subarachnoidalraum. Diese klare, farblose Flüssigkeit hat ein ungefähres Erwachsenenvolumen von 150 ml, wovon sich die Hälfte im Schädel und die andere Hälfte im Spinalkanal befindet. Das CSF-Volumen variiert jedoch beträchtlich, und ein verringertes CSF-Volumen kann aus Fettleibigkeit, Schwangerschaft oder anderen Ursachen für erhöhten abdominalen Druck resultieren. Dies ist zum Teil auf die Kompression des Foramen intervertebrale zurückzuführen, wodurch der Liquor verdrängt wird.
Klinische Perle
Aufgrund der großen Variabilität des Liquorvolumens ist die Fähigkeit, das Ausmaß der Spinalblockade nach der Lokalanästhesie-Injektion vorherzusagen, sehr schlecht, selbst wenn der BMI berechnet und verwendet wird.
Mehrere Faktoren beeinflussen die Verteilung der Lokalanästhesie nach Spinalblockade, einer davon ist das Liquorvolumen. Carpenter zeigte, dass das lumbosakrale CSF-Volumen mit der maximalen Höhe der sensorischen Nervenblockade und der Dauer der chirurgischen Anästhesie korrelierte. Die Dichte des Liquors steht im Zusammenhang mit dem höchsten Grad der sensorischen Nervenblockade, und das lumbosakrale Liquorvolumen korreliert mit dem höchsten Grad der sensorischen Nervenblockade sowie dem Beginn und der Dauer der motorischen Nervenblockade. Aufgrund der großen Variabilität des Liquorvolumens ist die Vorhersage des Ausmaßes der Spinalblockade nach Lokalanästhesie-Injektion jedoch schlecht, selbst wenn der BMI berechnet und verwendet wird.
Lokale Anästhetika
Kokain war das erste verwendete Spinalanästhetikum, und bald darauf folgten Procain und Tetracain. Lidocain, 2-Chlorprocain, Bupivacain, Mepivacain und Ropivacain wurden ebenfalls intrathekal verwendet. Darüber hinaus besteht ein wachsendes Interesse an Medikamenten, die Anästhesie und Analgesie bewirken und gleichzeitig Nebenwirkungen begrenzen. Eine Vielzahl von Medikamenten, darunter Vasokonstriktoren, Opioide, α2-adrenerge Agonisten und Acetylcholinesterase-Hemmer, wurden zu Wirbelsäulenmedikamenten hinzugefügt, um die Analgesie zu verbessern und gleichzeitig die durch Lokalanästhetika verursachte motorische Blockade zu reduzieren.
Lidocain wurde erstmals 1945 als Spinalanästhetikum verwendet und ist seitdem eines der am häufigsten verwendeten Spinalanästhetika. Der Beginn der Anästhesie erfolgt in 3 bis 5 Minuten mit einer Anästhesiedauer von 1 bis 1.5 Stunden. Lidocain-Spinalanästhesie wurde für Fälle in Operationssälen von kurzer bis mittlerer Länge verwendet. Der Hauptnachteil von Lidocain ist die Assoziation mit transienten neurologischen Symptomen (TNSs), die sich als Rückenschmerzen und Dysästhesien der unteren Extremitäten mit Bestrahlung des Gesäßes, der Oberschenkel und der unteren Gliedmaßen nach der Erholung von der Spinalanästhesie zeigen. TNS treten bei etwa 14 % der Patienten auf, die eine Spinalanästhesie mit Lidocain erhalten. Die Steinschnittposition ist mit einer höheren Inzidenz von TNSs verbunden. Wegen des TNS-Risikos wurde Lidocain meist durch andere Lokalanästhetika ersetzt.
Die intrathekale Anwendung von 2-Chlorprocain wurde 1952 beschrieben. In den 1980er Jahren wurden Bedenken hinsichtlich der Neurotoxizität bei der Anwendung von 2-Chlorprocain geäußert. Studien haben gezeigt, dass Natriumbisulfit, ein Antioxidans, das in Kombination mit 2-Chlorprocain verwendet wird, dafür verantwortlich ist. Chronische neurologische Defizite wurden bei Kaninchen berichtet, wenn Natriumbisulfit in den lumbalen Subarachnoidalraum injiziert wurde, aber wenn konservierungsmittelfreies 2-Chlorprocain injiziert wurde, wurden keine dauerhaften neurologischen Folgen festgestellt. Ergebnisse aus klinischen Studien haben gezeigt, dass konservierungsmittelfreies 2-Chlorprocain sicher, kurz wirksam und für ambulante Operationen geeignet ist. Die Zugabe von Epinephrin wird jedoch aufgrund einer Assoziation mit grippeähnlichen Symptomen und Rückenschmerzen nicht empfohlen. Intrathekales 2-Chlorprocain ist derzeit nicht von der Food and Drug Administration (FDA) zugelassen, obwohl auf der Packungskennzeichnung angegeben ist, dass es für die Epiduralanästhesie verwendet werden kann. Die Wirkungszeit ist schnell und die Dauer beträgt etwa 100 bis 120 Minuten. Die Dosis reicht von 20 bis 60 mg, wobei 40 mg die übliche Dosis ist.
Procain ist ein kurz wirkendes Ester-Lokalanästhetikum. Procain hat eine Wirkungsdauer von 3 bis 5 Minuten und eine Wirkungsdauer von 50 bis 60 Minuten. Für Operationen am Damm und an den unteren Extremitäten wurde eine Dosis von 50 bis 100 mg vorgeschlagen. Es gibt jedoch eine 14%ige Inzidenz von Nervenblockadeversagen im Zusammenhang mit 10% Procain. Bedenken hinsichtlich der Neurotoxizität von Procain haben seine Verwendung eingeschränkt. Aus all diesen Gründen wird Procain derzeit kaum zur Spinalanästhesie eingesetzt.
Bupivacain ist eines der am häufigsten verwendeten Lokalanästhetika für die Spinalanästhesie und bietet eine angemessene Anästhesie und Analgesie für Operationen mit mittlerer bis langer Dauer. Bupivacain hat eine geringe Inzidenz von TNSs. Der Beginn der Anästhesie erfolgt in 5 bis 8 Minuten, mit einer Anästhesiedauer von 90 bis 150 Minuten. Für die ambulante Spinalanästhesie werden kleine Dosen von Bupivacain empfohlen, um eine verlängerte Entlassungszeit aufgrund der Dauer der Nervenblockade zu vermeiden. Bupivacain wird oft als 0.75 % in 8.25 % Dextrose verpackt. Andere Formen von spinalem Bupivacain umfassen 0.5 % mit oder ohne Dextrose und 0.75 % ohne Dextrose.
NYSORA-Tipps
• Die Anwendung von intrathekalem Lidocain wird durch TNS eingeschränkt.
• Bupivacain hat eine sehr geringe Inzidenz von TNSs.
• Die Anästhesie setzt mit Bupivacain in 5 bis 8 Minuten ein und die Anästhesie dauert 210 bis 240 Minuten; daher ist es für mittlere bis lange OP-Fälle geeignet.
Tetracain hat einen Beginn der Anästhesie innerhalb von 3 bis 5 Minuten und eine Dauer von 70 bis 180 Minuten und wird wie Bupivacain für Fälle mit mittlerer bis längerer Dauer verwendet. Die 1%ige Lösung kann zu gleichen Teilen mit 10%iger Glukose gemischt werden, um ein hyperbares Spinalanästhetikum zu bilden, das für perineale und abdominale Operationen verwendet wird. Unter Tetracain treten TNSs mit einer geringeren Rate auf als unter Lidocain-Spinalanästhesie. Die Zugabe von Phenylephrin kann bei der Entwicklung von TNSs eine Rolle spielen.
Mepivacain ähnelt Lidocain und wird seit den 1960er Jahren zur Spinalanästhesie verwendet. Die Inzidenz von TNSs, die nach Mepivacain-Spinalanästhesie berichtet wird, variiert stark, mit Raten von 0 % bis 30 %.
Ropivacain wurde in den 1990er Jahren eingeführt. Für Anwendungen in der Spinalanästhesie hat sich Ropivacain als weniger wirksam als Bupivacain erwiesen. Dosisfindungsstudien haben die ED95 von spinalem Ropivacain bei Operationen an den unteren Extremitäten (11.4 mg), schwangeren Patienten (26.8 mg) und Neugeborenen (1.08 mg/kg) gezeigt. Die intrathekale Anwendung von Ropivacain ist nicht weit verbreitet, und umfangreiche Sicherheitsdaten werden erwartet. Eine frühe Studie identifizierte Rückenschmerzen bei 5 von 18 Freiwilligen, denen intrathekales hyperbares Ropivacain injiziert wurde. Bei spinalem Ropivacain wurden TNSs berichtet, obwohl die Inzidenz nicht so häufig ist wie bei Lidocain. Andere kleine Studien haben keine größeren Nebenwirkungen gezeigt.
Tabelle 8 zeigt einige der für die Spinalanästhesie verwendeten Lokalanästhetika sowie die Dosierungsdauer und -konzentration für verschiedene Grade der Spinalblockade.
TABELLE 8. Dosis, Dauer und Wirkungseintritt von Lokalanästhetika in der Spinalanästhesie.
| Dosis (mg) Bis T10 | Dosis (mg) zu T4 | Dauer (Minuten) Ebene | Mit Adrenalin | Beginn (Minuten) | |
|---|---|---|---|---|---|
| Häufig verwendete Bupivacain 0.75 % | 8-12 | 14-20 | 90-110 | 100-150 | 5-8 |
| Weniger häufig verwendet | |||||
| • Lidocain 5 % • Tetracain 0.5 % • Mepivacain 2 % • Ropivacain 0.75 % • Levobupivacain 0.5 % • Chloroprocain 3 % | 50-75 6-10 N / A 15-17 10-15 30 | 75-100 12-16 60-80 18-20 N / A 45 | 60-70 70-90 140-160 140-200 135-170 80-120 | 75-100 120-180 N / A N / A N / A N / A | 3-5 3-5 2-4 3-5 4-8 2-4 |
Zusätze zur Lokalanästhesie
Lokalanästhetika wurden Vasokonstriktoren zugesetzt, und sowohl Epinephrin als auch Phenylephrin wurden untersucht. Die Anästhesie wird intensiviert und verlängert mit kleineren Dosen von Lokalanästhetika, wenn Epinephrin oder Phenylephrin hinzugefügt wird. Es wird eine Gewebevasokonstriktion erzeugt, wodurch die systemische Reabsorption des Lokalanästhetikums begrenzt und die Wirkungsdauer verlängert wird, indem das Lokalanästhetikum in Kontakt mit den Nervenfasern gehalten wird. Allerdings können nach der Anwendung von Vasokonstriktoren in der Spinalanästhesie ischämische Komplikationen auftreten. In einigen Studien wurde Epinephrin aufgrund einer Ischämie der A. spinalis anterior als Ursache des CES ins Feld geführt. Unabhängig davon zeigen viele Studien keinen Zusammenhang zwischen der Verwendung von Vasokonstriktoren zur Spinalanästhesie und der Inzidenz von CES. Phenylephrin erhöht nachweislich das TNS-Risiko und kann die Höhe der Nervenblockade verringern.
Es wird angenommen, dass Epinephrin wirkt, indem es die Aufnahme von Lokalanästhetika verringert und somit die Wirbelsäulenblockade einiger Lokalanästhetika verlängert. Vasokonstriktoren können jedoch Ischämie verursachen, und es gibt eine theoretische Besorgnis über eine Ischämie des Rückenmarks, wenn Epinephrin zu Spinalanästhetika hinzugefügt wird. Tiermodelle haben keine Abnahme der Rückenmarksdurchblutung oder Zunahme der Rückenmarksischämie gezeigt, wenn Epinephrin zur Spinalblockade gegeben wurde, obwohl einige neurologische Komplikationen im Zusammenhang mit der Zugabe von Epinephrin bestehen.
NYSORA-Tipps
• Die Zugabe von 0.1 ml Adrenalin 1:1000 zu 10 ml Lokalanästhetikum ergibt eine Adrenalinkonzentration von 1:100,000.
• Die Zugabe von 0.1 ml Adrenalin 1:1000 zu 20 ml Lokalanästhetikum ergibt eine Konzentration von 1:200,000 usw. (0.1 ml in 30 ml = 1:300,000).
Die Verdünnung von Epinephrin mit einem Lokalanästhetikum ist eine potenzielle Quelle für Arzneimittelfehler, wobei Fehler möglicherweise um den Faktor 10 oder 100 falsch sind. Wenn Sie Epinephrin verwenden, das als 1 mg in 1 ml verpackt ist, was eine 1: 1000-Lösung ist, kann eine einfache Regel sein gefolgt. Die Zugabe von 0.1 ml Adrenalin zu 10 ml Lokalanästhetikum ergibt eine Adrenalinkonzentration von 1:100,000. Die Zugabe von 0.1 ml Epinephrin zu 20 ml Lokalanästhetikum ergibt eine Konzentration von 1:200,000 usw. (0.1 ml in 30 ml = 1:300,000).
Epinephrin verlängert die Dauer der Spinalanästhesie. In der Vergangenheit wurde angenommen, dass Epinephrin keine Wirkung auf hyperbares spinales Bupivacain hat, wobei eine Zwei-Segment-Regression zum Testen einer neuralen Blockade verwendet wurde. Eine andere Studie zeigte jedoch, dass Epinephrin die Dauer von hyperbarem spinalem Bupivacain verlängert, wenn Nadelstiche, transkutane elektrische Nervenstimulation (TENS), die einer chirurgischen Stimulation entspricht, und die Toleranz eines pneumatischen Oberschenkel-Tourniquets verwendet wurden, um eine neurale Blockade zu bestimmen. Es gibt Kontroversen bezüglich der Verlängerung der spinalen Bupivacain-Neuralblockade, wenn Epinephrin hinzugefügt wird. Die gleiche Kontroverse besteht über die Verlängerung von spinalem Lidocain mit Epinephrin.
Alle vier Arten von Opioidrezeptoren befinden sich im Hinterhorn des Rückenmarks und dienen als Ziel für die intrathekale Opioidinjektion. Rezeptoren befinden sich auf Rückenmarksneuronen und Enden von Afferenzen, die ihren Ursprung im Spinalganglion haben.
Fentanyl, Sufentanil, Meperidin und Morphin wurden alle intrathekal verwendet. Mögliche Nebenwirkungen sind Juckreiz, Übelkeit und Erbrechen sowie Atemdepression.
Die α2-adrenergen Agonisten können zu spinalen Injektionen von Lokalanästhetika hinzugefügt werden, um die Schmerzlinderung zu verbessern und die sensorische und motorische Nervenblockade zu verlängern. Eine verbesserte postoperative Analgesie wurde bei Kaiserschnittgeburten, Fixierung von Femurfrakturen und Kniearthroskopien nachgewiesen, wenn Clonidin der Lokalanästhesielösung zugesetzt wurde. Clonidin verlängert die sensorische und motorische Blockade eines Lokalanästhetikums nach einer Injektion in die Wirbelsäule.
Es wird angenommen, dass die sensorische Blockade sowohl durch präsynaptische als auch durch postsynaptische Mechanismen vermittelt wird. Clonidin induziert eine Hyperpolarisation am Vorderhorn des Rückenmarks und erleichtert die Wirkung des Lokalanästhetikums, wodurch die Motorblockade verlängert wird, wenn es als Zusatz verwendet wird. Bei alleiniger Anwendung in intrathekalen Injektionen verursacht Clonidin jedoch keine motorische Nervenblockade oder -schwäche. Nebenwirkungen können bei der Anwendung von spinalem Clonidin auftreten und umfassen Hypotonie, Bradykardie und Sedierung. Neuraxiales Clonidin wurde zur Behandlung von hartnäckigen Schmerzen eingesetzt.
Acetylcholinesterase-Hemmer verhindern den Abbau von Acetylcholin und bewirken bei intrathekaler Injektion eine Analgesie. Die antinozizeptiven Wirkungen beruhen auf erhöhtem Acetylcholin und der Bildung von Stickstoffmonoxid. In einem Rattenmodell wurde gezeigt, dass die diabetische Neuropathie nach intrathekaler Neostigmin-Injektion gelindert werden kann.222 Zu den Nebenwirkungen von intrathekalem Neostigmin gehören Übelkeit und Erbrechen, Bradykardie, die Atropin erfordert, Angst, Unruhe, Unruhe und Schwäche der unteren Extremitäten. Obwohl spinales Neostigmin eine erweiterte Schmerzkontrolle bietet, erlauben die auftretenden Nebenwirkungen keinen breiten Einsatz.
PHARMAKODYNAMIK DER SPINALANÄSTHESIE
Die Pharmakodynamik der spinalen Injektion von Lokalanästhetika ist breit gefächert. Als nächstes werden die kardiovaskulären, respiratorischen, gastrointestinalen, hepatischen und renalen Folgen der Spinalanästhesie diskutiert.
Kardiovaskuläre Wirkungen der Spinalanästhesie
Es ist allgemein anerkannt, dass Spinalanästhesie zu Hypotonie führt. Tatsächlich gibt ein gewisser Grad an Hypotonie dem Anästhesisten oft die Gewissheit, dass die Nervenblockade tatsächlich spinal ist. Hypotonie kann jedoch Übelkeit und Erbrechen, Ischämie kritischer Organe, Herz-Kreislauf-Kollaps verursachen und im Fall der schwangeren Mutter den Fötus gefährden. In der Vergangenheit gab es Verschiebungen in den Definitionen, vorgeschlagenen Mechanismen und dem Management von Hypotonie.
Die Definition von Hypotonie ist mühsam. Eine Studie fand 15 verschiedene Definitionen von Hypotonie in 63 Publikationen. Einige Definitionen verwendeten ein einzelnes Kriterium (Abnahme um 80 % gegenüber dem Ausgangswert), während andere Kombinationen verwendeten (ein Abfall um 80 % gegenüber dem Ausgangswert oder ein systolischer Blutdruck von weniger als 100 mmHg). Die Inzidenz von Hypotonie in einer einzelnen Kohorte von Patienten variierte je nach verwendeter Definition zwischen 7.4 % und 74.1 %.
Es wurden viele Mechanismen für eine durch Spinalanästhesie induzierte Hypotonie vorgeschlagen, darunter direkte Kreislaufwirkungen von Lokalanästhetika, relative Nebenniereninsuffizienz, Skelettmuskellähmung, aufsteigende medulläre vasomotorische Nervenblockade und gleichzeitige respiratorische Insuffizienz. Die primäre Beleidigung ist jedoch die präganglionäre sympathische Nervenblockade, die durch Spinalanästhesie hervorgerufen wird. Da die Höhe der Nervenblockade das Ausmaß der Sympathikusblockade bestimmt, folgt daraus, dass dies wiederum das Ausmaß der Änderung der kardiovaskulären Parameter bestimmt. Dieser Zusammenhang kann jedoch nicht vorhergesagt werden. Die sympathische Nervenblockade kann variabel zwischen zwei und sechs Dermatomen über der sensorischen Ebene liegen und unterhalb dieser Ebene unvollständig sein. Die plötzliche Blockade des Sympathikus bei Spinalanästhesie gibt wenig Zeit für eine kardiovaskuläre Kompensation, was zu einer ähnlichen Blockade des Sympathikus bei Epiduralanästhesie, aber weniger Hypotonie, führen kann.
NYSORA-Tipps
• Spinalanästhesie-Nerven blockieren die sympathische Kette, die der Hauptmechanismus für kardiovaskuläre Veränderungen ist.
• Die Höhe der Nervenblockade bestimmt den Grad der Sympathikusblockade, die den Grad der Veränderung der kardiovaskulären Parameter bestimmt.
Die sympathische Nervenblockade verursacht Hypotonie über ihre Auswirkungen auf Vorlast, Nachlast, Kontraktilität und HR – mit anderen Worten, die Determinanten des Herzzeitvolumens (CO) – und durch Verringerung des systemischen Gefäßwiderstands (SVR). Die Vorlast wird durch eine sympathische Nervenblockade-vermittelte Venodilatation verringert, was zu einer Ansammlung von Blut in den Peripherien und einem verringerten venösen Rückfluss führt. Während einer sympathischen Nervenblockade ist das Venensystem maximal vasodilatiert und daher auf die Schwerkraft angewiesen, um Blut zum Herzen zurückzuführen. Somit beeinflusst die Positionierung des Patienten und die aortokavale Kompression im Falle eines graviden Uterus deutlich den venösen Rückfluss während der Spinalanästhesie.
Der arterielle vasomotorische Tonus kann auch durch Sympathikusblockade, Verringerung des SVR und Nachlast verringert werden. Die arterielle Vasodilatation ist im Gegensatz zur Venenerweiterung nach einer Spinalblockade nicht maximal, und die glatte Gefäßmuskulatur behält nach sympathischer Denervation weiterhin einen gewissen autonomen Tonus. Dieser verbleibende Gefäßtonus kann bei Hypoxie und Azidose verloren gehen, was nach hoher Spinalanästhesie ohne kardiorespiratorische Unterstützung zum kardiovaskulären Kollaps führen kann. Obwohl es unterhalb der Spinalblockade eine Vasodilatation gibt, gibt es darüber eine kompensatorische Vasokonstriktion, vermittelt durch Karotis- und Aortenbogen-Barorezeptoren. Dies ist aus zwei Gründen wichtig. Erstens kann eine Blockierung bei höheren Dermatomspiegeln zu einer geringeren Kompensation führen. Zweitens kann die Verwendung von gefäßerweiternden Arzneimitteln wie Glyceryltrinitrat (GTN), Natriumnitroprussid oder flüchtigen Anästhetika diesen Kompensationsmechanismus aufheben und die Hypotonie verschlimmern oder sogar zu einem Herzstillstand führen.
Es kann einen anfänglichen CO-Anstieg geben, der mit einer verringerten Nachlast einhergeht. Alternativ kann CO aufgrund einer verringerten Vorlast abfallen. Einige Studien haben gezeigt, dass CO zu Beginn der Spinalanästhesie unverändert oder leicht reduziert ist. Andere, bei älteren Patienten, zeigten eine zweiphasige Änderung des HZV mit einem anfänglichen Anstieg in den ersten 7 Minuten, gefolgt von einem Abfall (Figure 8). Dies kann einem Abfall der Nachlast zugeschrieben werden, der einem Abfall der Vorlast vorausgeht.
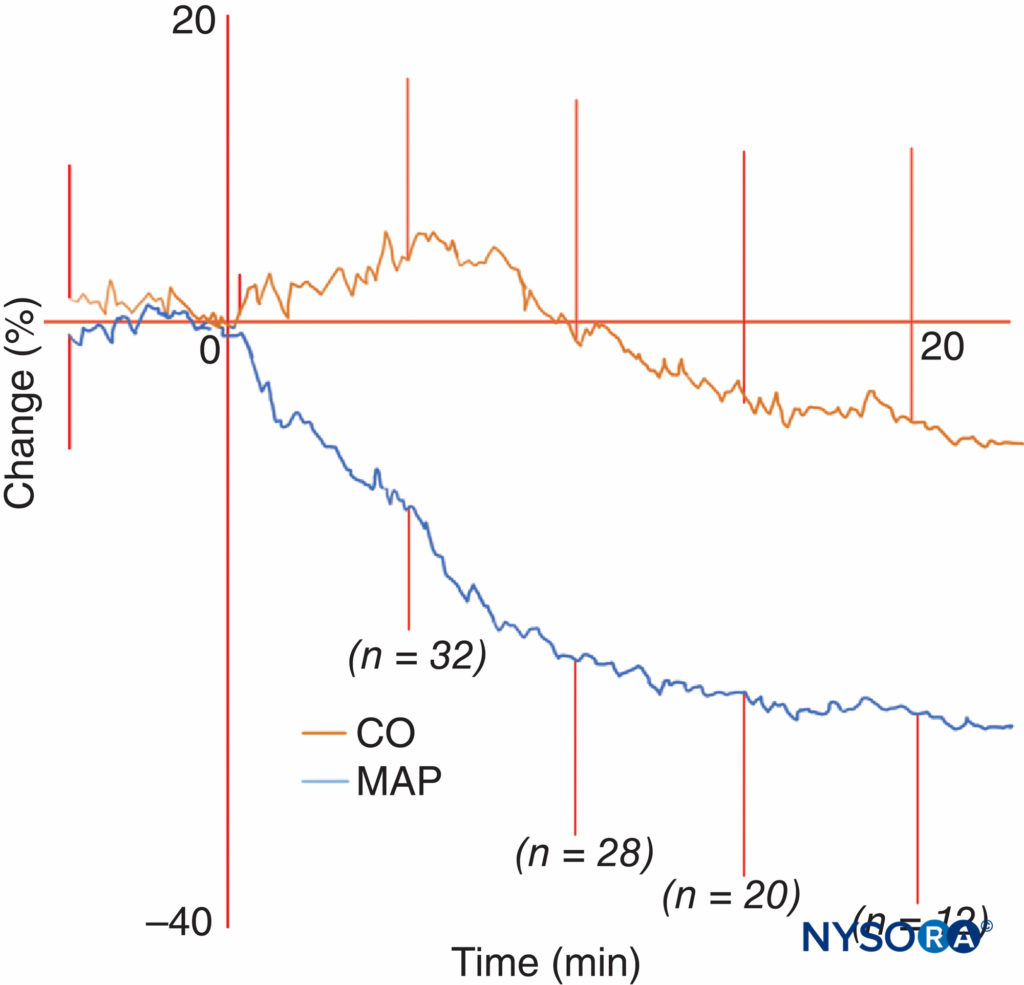
ABBILDUNG 8. Abbildung aus der Arbeit von Meyhoff et al., die einen Abfall des mittleren arteriellen Drucks (MAP) und des biphasischen Herzzeitvolumens (CO) nach Spinalanästhesie zeigt. Durchschnittliche CO- und MAP-Änderungen plus oder minus Standardabweichung zu Beginn der Spinalanästhesie bei älteren Patienten. Subarachnoidale Injektion wird zum Zeitpunkt = 0 Minuten gegeben. Nach Beendigung der Datenerfassung werden die letzte CO- und MAP-Aufzeichnung weiterhin im Durchschnitt über den Rest des Diagramms dargestellt. Jede Linie ist daher hypothetisch, da sie selbst nach Datenbeendigung aus Durchschnittswerten von 32 Patienten besteht; dies dient nur zu Illustrationszwecken. (Wiedergabe mit freundlicher Genehmigung von Meyhoff CS, Hesselbjerg L, Koscielniak-Nielsen Z, et al: Biphasic heart output changes during onset of spinal ansthetics in älteren Patienten. Eur J Anaesthesiol. 2007 Sep;24(9):770-775.)
Die Kontraktilität kann durch eine Blockade der oberen thorakalen sympathischen Nerven beeinträchtigt werden. Interessanterweise fand eine Studie, die das häufige Phänomen der ST-Streckensenkung bei gesunden Frauen untersuchte, die sich einem Kaiserschnitt unterziehen (25-60%), heraus, dass die ST-Senkung mit einem hyperkinetischen kontraktilen Zustand assoziiert ist.
Die Wirkung der Spinalanästhesie auf die Herzfrequenz ist komplex. Die HF kann ansteigen (sekundär zu Hypotonie über den Barorezeptorreflex) oder abnehmen (entweder durch sympathische Nervenblockade von Herzbeschleunigungsfasern, die von T1–T4-Wirbelsäulensegmenten ausgehen, oder über den umgekehrten Bainbridge-Reflex). Der umgekehrte Bainbridge-Reflex ist eine Abnahme der Herzfrequenz aufgrund eines verringerten venösen Rückflusses, der von Dehnungsrezeptoren im rechten Vorhof erkannt wird, und ist schwächer als der Barorezeptorreflex. Der Bezold-Jarisch-Reflex (BJR) ist ein weiterer Reflex, der die Herzfrequenz verringert. Die BJR wurde als Ursache für Bradykardie, Hypotonie und kardiovaskulären Kollaps nach zentraler neuraxialer Anästhesie, insbesondere Spinalanästhesie, in Betracht gezogen.
Der BJR ist ein kardioinhibitorischer Reflex und normalerweise kein dominanter Reflex. Die Assoziation zur Spinalanästhesie ist wahrscheinlich schwach. Der BJR wurde für Bradykardie nach Spinalanästhesie verantwortlich gemacht, insbesondere nach Blutungen. Kräftige Kontraktionen eines unterfüllten Herzens können die BJR auslösen. Dies ist eher bei der Verwendung von Ephedrin als bei Phenylephrin der Fall.
Junge, gesunde (American Society of Anesthesiologists Klasse 1) Patienten haben ein höheres Bradykardierisiko. Die Anwendung von Betablockern erhöht auch das Risiko einer Bradykardie. Die Inzidenz von Bradykardie in der nichtschwangeren Bevölkerung beträgt etwa 13 %. Obwohl Bradykardie normalerweise gut vertragen wird, können Asystolie und Herznervenblockade zweiten und dritten Grades auftreten, daher ist es ratsam, bei der Überwachung eines Patienten nach einer Spinalanästhesie wachsam zu sein und umgehend zu behandeln.
Risikofaktoren im Zusammenhang mit Hypotonie sind Hypovolämie, präoperativer Bluthochdruck, hohe sensorische Nervenblockade, Alter über 40 Jahre, Fettleibigkeit, kombinierte Vollnarkose und Spinalanästhesie, chronischer Alkoholkonsum, erhöhter BMI und Dringlichkeit eines nicht geburtshilflichen Eingriffs. Eine Hypotonie ist bei Frauen in den Wehen weniger wahrscheinlich als bei Frauen, die sich einem elektiven Kaiserschnitt unterziehen. Beziehen auf Regionalanästhesie und Herz-Kreislauf-Erkrankungen.
Behandlung von Hypotonie nach Spinalanästhesie
Glaubenssätze ändern Wechselnde Überzeugungen in Bezug auf die theoretische Grundlage der spinal-induzierten Hypotonie wurden durch Änderungen im Management widergespiegelt. Wenn zum Beispiel angenommen wird, dass eine verringerte Vorlast von primärer Bedeutung ist, dann sind Lagerung und Flüssigkeitstherapie die Behandlungen der Wahl, und wenn Vasodilatation der Grund ist, sollte ein Vasokonstriktor die erste Wahl sein. Dies hat zu heftigen Diskussionen geführt. In den 1970er Jahren wurde vorgeschlagen, keine Vasopressoren zu verabreichen, bis „alle anderen Methoden zur Bekämpfung von Hypotonie“ angewendet wurden, was die Bedeutung der Vorlast unterstreicht. Beweise dafür wurden aus fehlerhaften Studien an trächtigen Mutterschafen extrapoliert, die sich einer Vollnarkose unterzogen, die darauf hindeuteten, dass Vasopressoren den uteroplazentaren Kreislauf nachteilig beeinflussten. Der Titel Vasopressor der Wahl hat in ähnlicher Weise viele Kontroversen ausgelöst. Ephedrin wurde traditionell nominiert, da es die Durchblutung der Gebärmutter aufrechterhielt (in den oben erwähnten Tierstudien). Die Arbeit von Ngan Kee und anderen hat nahegelegt, dass Phenylephrin der Vasopressor der Wahl sein könnte, zumindest in der elektiven Geburtshilfe.
Behandlung Die Behandlung einer Hypotonie nach einer Spinalanästhesie sollte neben Elektrokardiogramm (EKG), Sauerstoffsättigung und fötaler Überwachung im Falle einer schwangeren Patientin eine häufige (anfangs jede Minute) Überwachung des Blutdrucks umfassen. Bei erheblichen kardialen Begleiterkrankungen sollte eine invasive Blutdruckmessung in Erwägung gezogen werden. Eine Flüssigkeitstherapie sollte bei einem dehydrierten Patienten angewendet werden, um das Volumen vor Beginn der Spinalanästhesie wiederherzustellen.
Nichtpharmakologische Methoden zur Behandlung von Hypotonie umfassen Lagerung, Beinkompression und Uterusverlagerung. Die Trendelenburg-Lagerung kann den venösen Rückfluss zum Herzen erhöhen.
Diese Position sollte 20° nicht überschreiten, da eine extreme Trendelenburg zu einer Abnahme der zerebralen Perfusion und des Blutflusses aufgrund eines Anstiegs des Jugularvenendrucks führen kann. Wenn die Höhe der Spinalanästhesie nicht fixiert ist, kann die Trendelenburg-Position die Höhe der Spinalanästhesie verändern und bei Patienten, die hyperbare Lokalanästhesielösungen erhalten, eine hohe Spinalanästhesie verursachen.
Dies kann minimiert werden, indem der Oberkörper mit einem Kissen unter den Schultern angehoben wird, während der Unterkörper über Herzhöhe gehalten wird. Ein Cochrane-Review bei schwangeren Frauen ergab, dass die Kompression der unteren Extremitäten einen gewissen Nutzen hat, obwohl verschiedene Methoden unterschiedliche Wirksamkeiten aufwiesen. Eine aortokavale Kompression durch einen graviden Uterus sollte vermieden werden. Eine vollständige seitliche Positionierung führt zu einer geringeren Hypotonie als eine linke seitliche Neigung, obwohl dies möglicherweise nicht praktikabel ist. Ein Keil unter der rechten Hüfte oder ein Kipptisch können verwendet werden, um eine Linksseitenneigung zu erreichen. Der optimale Neigungsgrad ist jedoch unbekannt, und es kann bei verschiedenen Patienten beträchtliche Unterschiede geben.
Über ein angemessenes Flüssigkeitsmanagement während der Spinalanästhesie gibt es widersprüchliche Meinungen. Frühe Studien deuteten darauf hin, dass eine kristalloide „Vorbelastung“ vor der Wirbelsäulenblockade wirksam war. Neuere Arbeiten zeigten einen minimalen Effekt der Vorspannung. Kolloid-Vorbeladung scheint effektiv zu sein, obwohl dies gegen das Risiko allergischer Reaktionen und erhöhte Kosten abgewogen werden muss. "Coloading" (schnelle Verabreichung von Flüssigkeit unmittelbar nach der Spinalanästhesie) mit Kristalloid ist besser als Preloading, um Hypotonie zu verhindern.
Hypotonie kann begrenzt werden, indem die Dosis des spinalen Lokalanästhetikums verringert wird. Eine Überprüfung ergab, dass 5–7 mg Bupivacain für einen Kaiserschnitt ausreichend sind. Eine vollständige motorische Nervenblockade war jedoch selten, die Dauer war begrenzt, und ein Epiduralkatheter für frühe Aufstockungsdosen war unerlässlich. Eine Metaanalyse aus dem Jahr 2011 ergab, dass niedrigere Dosen von Bupivacain mit einer geringeren anästhetischen Wirksamkeit, aber weniger Hypotonie und Übelkeit verbunden sind.
Es bestehen widersprüchliche Meinungen bezüglich des Vasopressors der Wahl bei spinal-induzierter Hypotonie. Ephedrin und Phenylephrin waren die beiden Hauptkonkurrenten; Es wurden jedoch andere verwendet. Ephedrin ist ein direkter und indirekter α- und β-Rezeptoragonist. Es wurde als sicherer als Phenylephrin erachtet, da es in frühen Tierversuchen die Vasokonstriktion des uteroplazentaren Kreislaufs begrenzte. Ephedrin hat jedoch einen langsamen Wirkungseintritt, ist anfällig für Tachyphylaxie und hat eine begrenzte Wirksamkeit bei der Behandlung von Hypotonie. Besorgniserregender ist das erhöhte Risiko einer fetalen Azidose. Ob dies zu schlechteren klinischen Ergebnissen führt, ist ungewiss.
Phenylephrin ist ein direkter α1-Rezeptoragonist. Es wurde in den 1960er Jahren erfolgreich für die Spinalanästhesie in New York eingesetzt, geriet jedoch aufgrund von Bedenken hinsichtlich einer schlechten Gewebedurchblutung in Ungnade. Insbesondere wurde in (etwas fehlerhaften) schwangeren Tiermodellen eine uteroplazentare Vasokonstriktion festgestellt. Jüngste Arbeiten haben gezeigt, dass eine fetale Azidose nicht auftritt, wenn übliche Dosen verwendet werden. Darüber hinaus scheint Phenylephrin Ephedrin bei der Verringerung von Hypotonie und Übelkeit überlegen zu sein. Phenylephrin wurde als Bolus oder Infusion verwendet und zur prophylaktischen sowie reaktiven Behandlung von Hypotonie eingesetzt (Tabelle 9).
Optimale Dosierungsschemata müssen noch etabliert werden. Ngan Kee verhinderte effektiv Hypotonie bei elektiven geburtshilflichen Patientinnen durch die Verwendung einer Kombination aus kristalloider Coload mit einer prophylaktischen Infusion von Phenylephrin.
Phenylephrin ist der derzeitige Vasopressor der Wahl für spinale Hypotonie, zumindest in der elektiven geburtshilflichen Einstellung. Es gibt jedoch Nachteile. Erstens führt Phenylephrin zu einer Verringerung von CO, obwohl die Bedeutung davon ungewiss ist. Zweitens hat sich gezeigt, dass intravenöses Phenylephrin die Höhe der Spinalnervenblockade bei schwangeren und nicht schwangeren Patientinnen verringert. Drittens verwies Cooper auf zwei Fallberichte über hypertensive Krisen mit Phenylephrin und Atropin, die zu einer erheblichen Morbidität führten. Es wird vermutet, dass durch Vasopressoren induzierter Bluthochdruck durch eine reflektorische Abnahme der Herzfrequenz begrenzt wird. Atropin kann in dieser Situation daher zu einer hypertensiven Krise führen. Schließlich ist die übliche Darreichungsform von Phenylephrin hochkonzentriert (10 mg/ml) und muss in einem 100-ml-Beutel Kochsalzlösung (100 μg/ml) verdünnt werden. Anästhesisten, die besser mit Ephedrin vertraut sind, können dies als lästig empfinden oder, noch schlimmer, einen Konzentrationsfehler begehen. Da außerdem in der Regel viel weniger als ein 100-ml-Beutel Phenylephrin benötigt wird, besteht die Gefahr einer Kreuzkontamination, wenn Beutel wiederverwendet werden. Nach einer Spinalanästhesie kann ein kardiovaskulärer Kollaps auftreten, obwohl dies ein seltenes Ereignis ist. Auroy und Mitarbeiter berichteten von 9 Herzstillständen bei 35,439 durchgeführten Spinalanästhesien. Eine Bradykardie geht normalerweise einem Herzstillstand voraus, und eine frühzeitige, aggressive Behandlung der Bradykardie ist gerechtfertigt. Die Behandlung von Bradykardie umfasst intravenöses Atropin, Ephedrin und Epinephrin. Bei Herzstillstand nach Spinalanästhesie sollte Epinephrin frühzeitig eingesetzt und das Advanced Cardiac Life Support (ACLS)-Protokoll eingeleitet werden. Weitere Arbeiten zur spinal-induzierten Hypotonie sind erforderlich.
Obwohl die Behandlung normalerweise auf den systolischen Blutdruck abzielt, kann der mittlere Blutdruck ein besseres Ziel sein.
Es können auch verschiedene Rezeptoren angegriffen werden. Zum Beispiel wurde gezeigt, dass prophylaktisches intravenöses Ondansetron Hypotonie reduziert, möglicherweise durch Modulation des BJR. Unterschiedliche Patientensubpopulationen können unterschiedliche Therapien erfordern. Die meisten Beweise beziehen sich auf die elektive, gesunde geburtshilfliche Einstellung, und inwieweit dies auf andere Gruppen extrapoliert werden kann, bleibt abzuwarten. Schließlich gibt es trotz veröffentlichter Beweise für die Vorteile von Phenylephrin gegenüber Ephedrin bei einem elektiven Kaiserschnitt Widerwillen, die Praxis zu ändern. Psychologische und institutionelle Hindernisse für Veränderungen müssen angegangen werden.
Atmungseffekte der Spinalanästhesie
Bei Patienten mit normaler Lungenphysiologie hat die Spinalanästhesie wenig Einfluss auf die Lungenfunktion. Lungenvolumen, Ruheminutenvolumen, Totraum, arterielle Blutgasspannungen und Shuntfraktion zeigen minimale Veränderungen nach Spinalanästhesie. Die hauptsächliche respiratorische Wirkung der Spinalanästhesie tritt während einer hohen Spinalblockade auf, wenn die aktive Ausatmung aufgrund einer Lähmung der Bauch- und Interkostalmuskulatur beeinträchtigt ist. Während eines hohen Spinalblocks sind das exspiratorische Reservevolumen, der exspiratorische Spitzenfluss und die maximale Minutenventilation reduziert. Patienten mit obstruktiver Lungenerkrankung, die für eine ausreichende Beatmung auf den Einsatz der Hilfsmuskulatur angewiesen sind, sollten nach einer Spinalblockade sorgfältig überwacht werden. Patienten mit normaler Lungenfunktion und hoher Spinalnervenblockade können über Dyspnoe klagen, aber wenn sie in der Lage sind, deutlich und mit normaler Stimme zu sprechen, ist die Beatmung normalerweise ausreichend. Die Dyspnoe ist normalerweise auf die Unfähigkeit zurückzuführen, die Bewegung der Brustwand während der Atmung zu spüren, und eine einfache Sicherung ist normalerweise wirksam, um das Leiden des Patienten zu lindern.
NYSORA-Tipps
• Die arteriellen Blutgaswerte ändern sich während einer hohen Spinalanästhesie bei Patienten, die spontan Raumluft atmen, nicht.
• Da eine hohe Wirbelsäule normalerweise den zervikalen Bereich nicht beeinträchtigt, wird der N. phrenicus und die normale Funktion des Zwerchfells geschont, und die Inspiration wird nur minimal beeinträchtigt.
Die arteriellen Blutgaswerte ändern sich während einer hohen Spinalanästhesie bei Patienten, die spontan Raumluft atmen, nicht. Die Hauptwirkung einer hohen Spinalanästhesie liegt auf der Exspiration, da die Exspirationsmuskulatur beeinträchtigt wird. Da eine hohe Wirbelsäule normalerweise den zervikalen Bereich nicht beeinträchtigt, wird der Zwerchfellnerv und die normale Zwerchfellfunktion geschont, und die Inspiration wird minimal beeinträchtigt. Obwohl Steinbrook und Kollegen feststellten, dass die Spinalanästhesie nicht mit signifikanten Veränderungen der Vitalkapazität, des maximalen Inspirationsdrucks oder des endexspiratorischen PCO2 im Ruhezustand verbunden war, wurde bei der Spinalanästhesie mit Bupivacain eine erhöhte Reaktionsfähigkeit der Atmung auf CO2 beobachtet. Beziehen auf Regionalanästhesie und systemische Erkrankungen.
Gastrointestinale Wirkungen der Spinalanästhesie
Die sympathische Innervation zu den Bauchorganen entsteht von T6 bis L2. Aufgrund der sympathischen Blockade und der ungehinderten parasympathischen Aktivität nach der Spinalblockade nehmen die Sekrete zu, die Schließmuskeln entspannen sich und der Darm verengt sich.
Eine erhöhte vagale Aktivität nach Sympathikusblockade verursacht eine erhöhte Peristaltik des Gastrointestinaltrakts, was zu Übelkeit führen kann. Übelkeit kann auch aus einer durch Hypotonie induzierten Darmischämie resultieren, die Serotonin und andere emetogene Substanzen produziert. Die Inzidenz von IONV bei nicht-geburtshilflichen Eingriffen kann bis zu 42 % und bei Gebärenden bis zu 80 % betragen.
Hepatische und renale Auswirkungen der Spinalanästhesie
Der hepatische Blutfluss korreliert mit dem arteriellen Blutfluss. Es gibt keine Autoregulation des hepatischen Blutflusses; Wenn also der arterielle Blutfluss nach der Spinalanästhesie abnimmt, nimmt auch der hepatische Blutfluss ab. Wenn der mittlere arterielle Druck (MAP) nach Platzierung eines Spinalanästhetikums aufrechterhalten wird, wird auch der hepatische Blutfluss aufrechterhalten. Patienten mit Lebererkrankungen müssen sorgfältig überwacht werden, und ihr Blutdruck muss während der Anästhesie kontrolliert werden, um die Leberdurchblutung aufrechtzuerhalten. Keine Studie hat die Überlegenheit der Regional- oder Allgemeinanästhesie bei Patienten mit Lebererkrankungen eindeutig gezeigt. Bei Patienten mit Lebererkrankungen kann entweder eine Regionalanästhesie oder eine Vollnarkose verabreicht werden, solange der MAP nahe am Ausgangswert gehalten wird.
NYSORA-Tipps
• Wenn der mittlere Blutdruck nach Platzierung eines Spinalanästhetikums aufrechterhalten wird, nimmt weder der hepatische noch der renale Blutfluss ab.
• Die Spinalanästhesie verändert die Autoregulation des renalen Blutflusses nicht.
Die renale Durchblutung wird autoreguliert. Die Nieren bleiben perfundiert, wenn der MAP über 50 mm Hg bleibt. Vorübergehende Abnahmen des renalen Blutflusses können auftreten, wenn der MAP unter 50 mm Hg liegt, aber selbst nach langen Abnahmen des MAP kehrt die Nierenfunktion wieder auf den Normalwert zurück, wenn der Blutdruck wieder normal ist.
Auch hier ist nach der Platzierung einer Spinalanästhesie die Aufmerksamkeit auf den Blutdruck wichtig, und der MAP sollte so nah wie möglich am Ausgangswert liegen. Die Spinalanästhesie hat keinen Einfluss auf die Autoregulation des renalen Blutflusses. Bei Schafen wurde gezeigt, dass sich die Nierendurchblutung nach einer Spinalanästhesie kaum veränderte.
FAKTOREN, DIE DAS LEVEL DES WIRBELSÄULEN-Blocks beeinflussen
Viele Faktoren wurden als mögliche Determinanten für das Ausmaß der Spinalblockade vorgeschlagen. Die vier Hauptkategorien von Faktoren sind (1) Eigenschaften der Lokalanästhesielösung, (2) Patienteneigenschaften, (3) Spinalblockadetechnik und (4) Diffusion. Zu den Merkmalen der Lokalanästhesielösung gehören Barizität, Dosis, Konzentration und injiziertes Volumen. Zu den Patienteneigenschaften gehören Alter, Gewicht, Größe, Geschlecht, intraabdominaler Druck, Anatomie der Wirbelsäule, Eigenschaften der Spinalflüssigkeit und Position des Patienten. Zu den Techniken der Spinalblockade gehören die Injektionsstelle, die Injektionsgeschwindigkeit, die Richtung der Nadelschräge, die Injektionskraft und die Zugabe von Vasokonstriktoren. Obwohl postuliert wurde, dass alle diese Faktoren die spinale Ausbreitung des Anästhetikums beeinflussen, hat sich nicht gezeigt, dass viele die Verteilung der Blockade verändern, wenn alle anderen Faktoren, die die Blockade beeinflussen, konstant gehalten werden.
Injektionsstelle
Die Injektionsstelle von Lokalanästhetika für die Spinalanästhesie kann das Ausmaß der Blockade bestimmen. In einigen Studien erzeugt isobares spinales 0.5 %iges Bupivacain eine sensorische Blockade, die um zwei Dermatome pro Zwischenraum reduziert wird, wenn die Injektion an den Zwischenräumen L2–L3, L3–L4 und L4–L5 verglichen wird. Es besteht jedoch kein Unterschied in der Höhe der Nervenblockade, wenn hyperbares Bupivacain oder Dibucain als Spinalanästhetikum in verschiedenen Zwischenräumen injiziert wird.
Alter
Einige Studien berichteten über Veränderungen der Höhe der Nervenblockade nach Spinalanästhesie bei älteren Patienten im Vergleich zu jüngeren Patienten, aber andere Studien berichteten über keinen Unterschied in der Höhe der Nervenblockade. Diese Studien wurden sowohl mit isobarem als auch mit hyperbarem 0.5 % Bupivacain durchgeführt.
NYSORA-Tipps
Die Barizität spielt eine wichtige Rolle bei der Bestimmung der Höhe der Nervenblockade nach Spinalanästhesie bei älteren Bevölkerungsgruppen.
Isobares Bupivacain scheint die Höhe der Nervenblockade zu erhöhen, und hyperbares Bupivacain scheint die Höhe der Nervenblockade mit zunehmendem Alter nicht zu verändern. Besteht ein Zusammenhang zwischen zunehmendem Alter und Höhe der Spinalanästhesie, so ist dieser alleine nicht stark genug, um im klinischen Umfeld ein zuverlässiger Prädiktor zu sein. Genau wie bei der Injektionsstelle scheint die Barizität bei der Bestimmung der Höhe der Nervenblockade nach Spinalanästhesie bei älteren Bevölkerungsgruppen eine wichtige Rolle zu spielen, und das Alter ist kein unabhängiger Faktor.
Position
Die Positionierung des Patienten ist für die Bestimmung des Blockadegrades nach hyperbarer und hypobarer Spinalanästhesie wichtig, nicht jedoch für isobare Lösungen. Sitz-, Trendelenburg- und Klappmesserlagerungen können die Ausbreitung des Lokalanästhetikums aufgrund der Schwerkraftwirkung stark verändern.
NYSORA-Tipps
Die Positionierung des Patienten ist für die Bestimmung des Blockadegrades nach hyperbarer und hypobarer Spinalanästhesie wichtig, nicht jedoch für isobare Lösungen.
Die Kombination aus Barizität der Lokalanästhesielösung und Patientenpositionierung bestimmt die Höhe der Spinalnervenblockade. Die Sitzposition in Kombination mit einer hyperbaren Lösung kann Analgesie im Perineum hervorrufen. Die Trendelenburg-Positionierung beeinflusst auch die Ausbreitung von hyperbaren und hypobaren Lokalanästhetika aufgrund der Wirkung der Schwerkraft. Die Bauchlage wird für rektale, perineale und lumbale Eingriffe mit einem hypobaren Lokalanästhetikum verwendet. Dies verhindert eine rostrale Ausbreitung der Spinalblockade nach der Injektion.
Die Beugung der Hüften und Knie des auf dem Rücken liegenden Patienten flacht die Lordose der Lendenwirbelsäule ab und verringert die sakrale Ansammlung von Lokalanästhetikum.
In Kombination mit der Trendelenburg-Positionierung kann dies die Ausbreitung des Kopfes unterstützen. Diese Position kann unbeabsichtigt erreicht werden, wenn ein Blasenkatheter nach dem Einführen in die Wirbelsäule platziert wird.
Geschwindigkeit der Injektion
Es wurde berichtet, dass die Injektionsgeschwindigkeit die Höhe der Spinalnervenblockade beeinflusst, aber die in der Literatur verfügbaren Daten sind widersprüchlich. In Studien mit isobarem Bupivacain gab es keinen Unterschied in der Höhe der Spinalnervenblockade bei unterschiedlichen Injektionsgeschwindigkeiten. Auch wenn sich die Höhe der Spinalnervenblockade nicht mit der Injektionsgeschwindigkeit ändert, sollte bei der Verabreichung eines Spinalanästhetikums eine gleichmäßige, langsame Injektion erfolgen. Wenn eine kräftige Injektion verabreicht wird und die Spritze nicht fest mit der Spinalnadel verbunden ist, kann sich die Nadel von der Spritze lösen, was zu einem Verlust des Lokalanästhetikums führt.
NYSORA-Tipps
Auch wenn sich die Höhe der Spinalnervenblockade nicht mit der Injektionsgeschwindigkeit ändert, verwenden Sie bei der Verabreichung eines Spinalanästhetikums eine sanfte, langsame Injektion.
Volumen, Konzentration und Dosis des Lokalanästhetikums
Es ist schwierig, das Volumen, die Konzentration oder die Dosis des Lokalanästhetikums konstant zu halten, ohne eine der anderen Variablen zu ändern; Daher ist es schwierig, qualitativ hochwertige Studien zu erstellen, die diese Variablen einzeln untersuchen. Axelsson und Mitarbeiter zeigten, dass das Volumen des Lokalanästhetikums die Höhe und Dauer der Spinalnervenblockade beeinflussen kann, wenn äquivalente Dosen verwendet werden.
Peng und Mitarbeiter zeigten, dass die Konzentration des Lokalanästhetikums bei der Bestimmung einer wirksamen Anästhesie in direktem Zusammenhang mit der Dosis steht. Die Dosis des Lokalanästhetikums spielt jedoch die größte Rolle bei der Bestimmung der Dauer der Spinalnervenblockade, da weder das Volumen noch die Konzentration von isobarem Bupivacain oder Tetracain die Dauer der Spinalnervenblockade verändern, wenn die Dosis konstant gehalten wird. Studien haben wiederholt gezeigt, dass die Spinalnervenblockade länger dauert, wenn höhere Dosen von Lokalanästhetika verabreicht werden. Achten Sie bei der Durchführung einer Spinalanästhesie nicht nur auf die Dosis des Lokalanästhetikums, sondern auch auf das Volumen und die Konzentration, damit der Patient nicht über- oder unterdosiert wird.
NYSORA-Tipps
Achten Sie bei der Durchführung einer Spinalanästhesie nicht nur auf die Dosis des Lokalanästhetikums, sondern auch auf das Volumen und die Konzentration, damit der Patient nicht über- oder unterdosiert wird.
Die Verwendung von hyperbaren Lösungen minimiert die Bedeutung von Dosis und Volumen, außer wenn Dosen von hyperbarem Bupivacain von gleich oder weniger als 10 mg verwendet werden. In diesen Fällen gibt es eine geringere kraniale Ausbreitung und eine kürzere Wirkungsdauer. Eine Dosis von hyperbarem Bupivacain zwischen 10 und 20 mg führt zu einer ähnlichen Höhe der Nervenblockade. Bei der Verwendung von hyperbaren Lösungen ist es wichtig zu beachten, dass die Positionierung des Patienten und die Barizität die Faktoren mit dem größten Einfluss auf die Höhe der Nervenblockade sind, außer wenn niedrige Dosen von hyperbarem Bupivacain verwendet werden.
GERÄTE FÜR DIE SPINALANÄSTHESIE
Aufrechterhaltung der Asepsis
Kein einzelner Eingriff garantiert Asepsis. Daher empfiehlt sich ein mehrgleisiger Ansatz.
In der Vergangenheit verfügten die meisten Einrichtungen über wiederverwendbare Siebe für die Spinalanästhesie. Diese Schalen mussten von Anästhesisten oder Anästhesiepersonal vorbereitet werden, um sicherzustellen, dass keine bakterielle und chemische Kontamination auftritt. Gegenwärtig sind im Handel hergestellte Einweg-Wirbelsäulenschalen erhältlich und werden von den meisten Einrichtungen verwendet. Diese Schalen sind tragbar, steril und einfach zu verwenden. Abbildung 9 zeigt den Inhalt einer standardmäßigen, kommerziell hergestellten Spinalanästhesieschale.
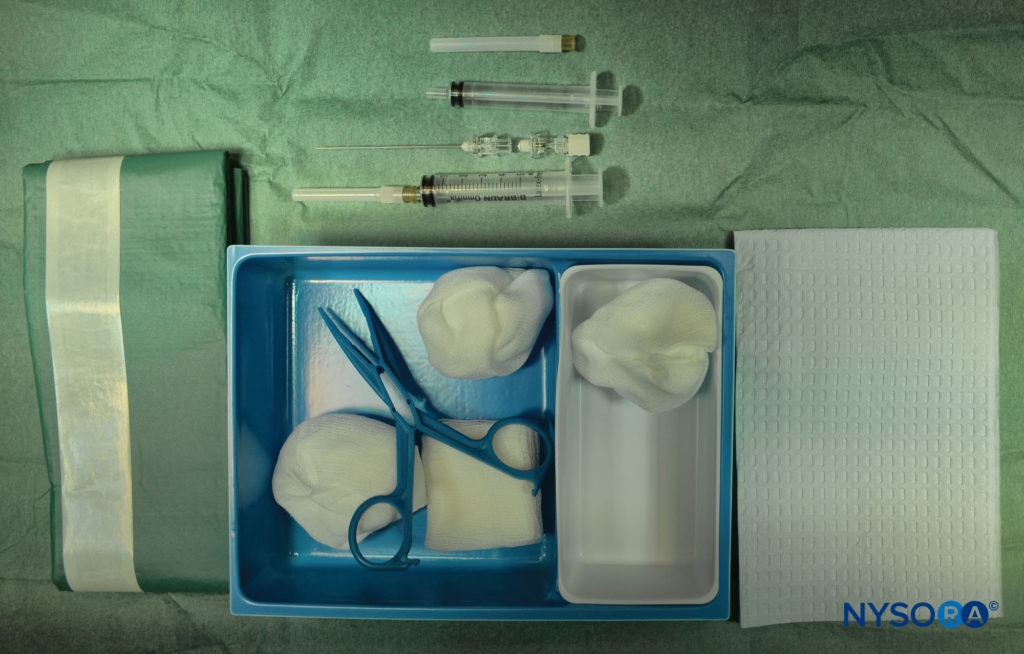
ABBILDUNG 9. Inhalt einer handelsüblichen Spinalanästhesie-Schublade.
Die ideale Hautvorbereitungslösung sollte bakterizid sein und einen schnellen Wirkungseintritt und eine lange Dauer haben. Chlorhexidin ist Povidon-Jod in all diesen Punkten überlegen. Außerdem sollte das ideale Mittel nicht neurotoxisch sein. Leider sind bakterizide Mittel neurotoxisch. Es ist daher ratsam, die niedrigste wirksame Konzentration zu verwenden und das Präparat trocknen zu lassen. Obwohl umstritten, wird derzeit von einigen Gruppen 0.5 % Chlorhexidin in 70 % Alkohol empfohlen. Die Kontamination von Geräten mit Hautpräparaten kann theoretisch zum Eintrag neurotoxischer Substanzen in Nervengewebe führen. Besorgniserregender ist die versehentliche neuraxiale Injektion einer antiseptischen Lösung, möglicherweise von einer antiseptischen Lösung und einem Lokalanästhetikum, die in benachbarte Töpfe gegeben werden. Daher sollten nach der Hautvorbereitung nicht verwendete Antiseptika vor Beginn des Eingriffs entsorgt werden (und intrathekale Arzneimittel sollten direkt aus sterilen Ampullen entnommen werden). Getönte antiseptische Lösungen können die Wahrscheinlichkeit eines Arzneimittelfehlers verringern und eine einfache Identifizierung übersehener Haut während der Anwendung ermöglichen.
Der Nachweis eines Nutzens individueller Infektionsschutzmaßnahmen ist aufgrund der Seltenheit infektiöser Komplikationen schwierig. Frühere Beweise waren widersprüchlich. Beispielsweise wurde vermutet, dass Hautschuppen durch das „Wackeln“ der Maske abgestoßen werden können, was die bakterielle Kontamination erhöht. 1995 wurde jedoch die routinemäßige Verwendung von Gesichtsmasken gefordert, nachdem mittels Polymerase-Kettenreaktion (PCR)-Fingerabdruck eindeutig nachgewiesen wurde, dass ein Fall von Streptococcus salivarius-Meningitis im Rachen des Arztes entstand, der eine Lumbalpunktion durchgeführt hatte.
Wir sind der festen Überzeugung, dass das Tragen einer Gesichtsmaske bei der Durchführung einer Spinalanästhesie obligatorisch sein sollte. Ein Praxisratgeber der American Society of Regional Anästhesie und Schmerzmedizin (ASRA) aus dem Jahr 2006 empfahl das Tragen einer Maske zusätzlich zum Entfernen von Schmuck, gründliches Händewaschen und sterile OP-Handschuhe für alle Regionalanästhesietechniken.
Zu den Hauptbestandteilen einer aseptischen Technik gehörten auch ein OP-Hut und eine sterile Abdeckung. Andere internationale Berufsverbände haben ähnliche Richtlinien.
Bei der Spinalanästhesie sind prophylaktische Antibiotika unnötig. Wenn, wie es der Fall ist, eine Antibiotikaprophylaxe zur Vorbeugung einer postoperativen Wundinfektion erforderlich ist, kann es ratsam sein, vor dem Einführen einer Spinalnadel Antibiotika zu verabreichen.
Auf den Leser wird verwiesen Infektionskontrolle in der Regionalanästhesie um mehr zu erfahren.
Wiederbelebung und Überwachung
Bei jeder Durchführung einer Spinalanästhesie muss eine Reanimationsausrüstung verfügbar sein. Dazu gehören Geräte und Medikamente, die zur Sicherung der Atemwege, zur Beatmung und zur Unterstützung der Herzfunktion erforderlich sind. Alle Patienten, die eine Spinalanästhesie erhalten, sollten einen intravenösen Zugang haben.
Der Patient muss es sein überwacht während der Platzierung der Spinalanästhesie mit Pulsoximeter, Blutdruckmanschette und EKG. Bei schwangeren Patientinnen sollte eine fetale Überwachung durchgeführt werden. Der nichtinvasive Blutdruck sollte anfänglich in 1-Minuten-Intervallen gemessen werden, da eine Hypotonie plötzlich auftreten kann.
Zittern und Körpergewohnheiten können die nichtinvasive Blutdruckmessung erschweren. Wenn der Patient an einer signifikanten kardiovaskulären Erkrankung leidet, sollte eine invasive Blutdrucküberwachung in Erwägung gezogen werden.
Nadeln
Für die Spinalanästhesie wurden Nadeln mit unterschiedlichen Durchmessern und Formen entwickelt. Die derzeit verwendeten haben einen eng anliegenden, abnehmbaren Mandrin, der verhindert, dass Haut und Fettgewebe die Nadel verstopfen und möglicherweise in den Subarachnoidalraum eindringen. Figure 10 zeigt die verschiedenen Arten von Nadeln, die zusammen mit der Art der Spitze am Ende der Nadel verwendet werden.
Die Pencil-Point-Nadeln (Sprotte und Whitacre) haben einen abgerundeten, nicht schneidenden Anschliff mit fester Spitze. Die Öffnung befindet sich seitlich an der Kanüle 2–4 mm proximal zur Kanülenspitze. Zu den Nadeln mit Schneidschliff gehören die Quincke- und die Pitkin-Nadel. Die Quincke-Nadel hat eine scharfe Spitze mit einer mittellangen Schneidnadel, und die Pitkin-Nadel hat eine scharfe Spitze und eine kurze Abschrägung mit Schneidkanten. Schließlich hat die Spinalnadel nach Greene eine abgerundete Spitze und eine abgerundete, nicht schneidende Abschrägung. Wenn ein kontinuierlicher Spinalkatheter platziert werden soll, kann eine Tuohy-Nadel verwendet werden, um den Subarachnoidalraum vor der Platzierung des Katheters zu finden.
Nadeln mit Bleistiftspitze bieten ein besseres taktiles Gefühl der angetroffenen Bänderschichten, erfordern jedoch mehr Kraft zum Einführen als Nadeln mit abgeschrägter Spitze. Die Abschrägung der Nadel sollte in Längsrichtung gerichtet sein, um das Auftreten von PDPH zu verringern.

ABBILDUNG 10. Verschiedene Arten von Nadeln.
Nadeln mit kleiner Stärke und Nadeln mit abgerundeten, nicht schneidenden Abschrägungen verringern ebenfalls das Auftreten von PDPH, werden jedoch leichter abgelenkt als Nadeln mit größerer Stärke. Auf den Leser wird verwiesen Ultrastrukturelle Anatomie der Wirbelsäulenhäute und verwandter Strukturen und Postduralpunktionskopfschmerz.
NYSORA-Tipps
• Nadeln mit Bleistiftspitze bieten ein besseres taktiles Gefühl der angetroffenen Bänderschichten, erfordern jedoch mehr Kraft zum Einführen als Nadeln mit abgeschrägter Spitze.
• Die Verwendung von Einführungsinstrumenten trägt dazu bei, den Durchgang epidermischer Verunreinigungen in den Liquor zu verhindern.
Einführungshilfen wurden entwickelt, um die Platzierung von Spinalnadeln im Subarachnoidalraum zu unterstützen, da es schwierig ist, Nadeln mit kleinem Durchmesser durch das Gewebe zu führen. Introducer dienen auch dazu, eine Kontamination des Liquors mit kleinen Stücken der Epidermis zu verhindern, die zur Bildung von Dermoid-Rückenmarkstumoren führen könnte. Die Einführhilfe wird in der beabsichtigten Richtung der Spinalnadel in das Ligamentum interspinale platziert, und die Spinalnadel wird dann durch die Einführhilfe platziert.
POSITION DES PATIENTEN
Die richtige Positionierung des Patienten für die Spinalanästhesie ist für eine schnelle und erfolgreiche Nervenblockade unerlässlich. Es hat sich als unabhängiger Prädiktor für einen erfolgreichen ersten Versuch einer neuraxialen Nervenblockade erwiesen.316 Bei der Positionierung des Patienten spielen viele Faktoren eine Rolle. Vor Beginn des Verfahrens sollten sich sowohl der Patient als auch der Anästhesist wohl fühlen. Dazu gehören die Einstellung der Höhe des OP-Tisches, die Bereitstellung angemessener Decken oder Abdeckungen für den Patienten, die Gewährleistung einer angenehmen Raumtemperatur und die Bereitstellung einer Sedierung für den Patienten, falls erforderlich. Personal, das in der Positionierung von Patienten geschult ist, ist von unschätzbarem Wert, und kommerzielle Positionierungsgeräte können nützlich sein.
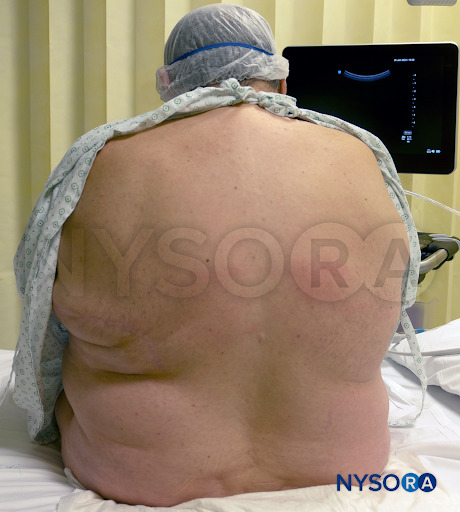
Aus dem Kompendium der Regionalanästhesie: Lagerung für die Spinalanästhesie eines Patienten mit großem Body-Mass-Index.
Bei der Sedierung ist es wichtig, eine Übersedierung zu vermeiden. Der Patient sollte vor, während und nach der Verabreichung der Spinalanästhesie kooperieren können. Es gibt drei Hauptpositionen für die Verabreichung einer Spinalanästhesie: die Seitenlage, die sitzende und die Bauchlage.
Seitenlage
Eine häufig verwendete Position zum Platzieren einer Spinalanästhesie ist die Seitenlage. Die ideale Positionierung besteht darin, den Rücken des Patienten parallel zur Bettkante zu haben, die dem Anästhesisten am nächsten ist, wobei die Knie des Patienten zum Bauch und der Nacken gebeugt sind. Figure 11 zeigt einen Patienten in Seitenlage.
Es ist vorteilhaft, einen Assistenten zu haben, der hilft, den Patienten zu halten und ihn dazu ermutigt, in dieser Position zu bleiben. Je nach Operationssitus und Operationsposition kann eine hypo-, iso- oder hyperbare Lösung eines Lokalanästhetikums injiziert werden.
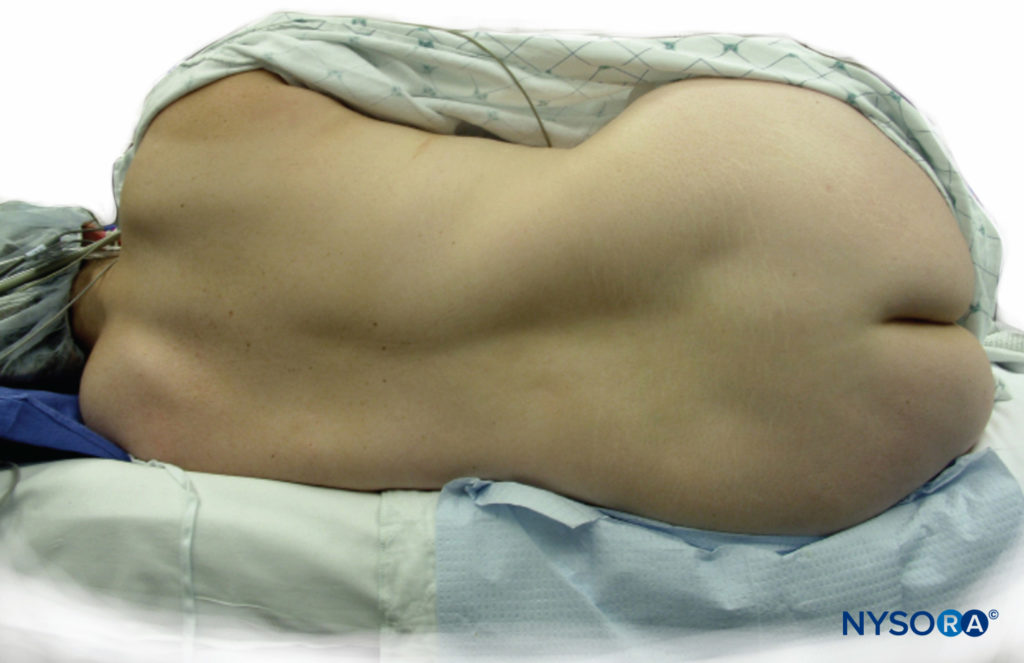
ABBILDUNG 11. Patient in Seitenlage.
NYSORA-Tipps
• Eine häufig verwendete Position zum Platzieren einer Spinalanästhesie ist die Seitenlage.
• Die ideale Positionierung besteht darin, dass der Rücken des Patienten parallel zur Bettkante liegt, die dem Anästhesisten am nächsten ist, die Knie zum Bauch gebeugt und der Nacken gebeugt sind.
Sitzposition und „Sattelnervenblockade“
Genau genommen eignet sich die sitzende Position am besten für tiefe Lumbal- oder Sakralanästhesien und in Fällen, in denen der Patient übergewichtig ist und es schwierig ist, die Mittellinie zu finden. In der Praxis bevorzugen jedoch viele Anästhesisten bei allen Patienten, die so gelagert werden können, die sitzende Position. Die Sitzposition vermeidet die mögliche Rotation der Wirbelsäule, die bei der Seitenlage auftreten kann. Die Verwendung eines Hockers als Fußstütze und eines Kissens, das der Patient festhalten kann, kann in dieser Position hilfreich sein. Der Patient sollte den Nacken beugen und den unteren Rücken herausdrücken, um die lumbalen Zwischenwirbelräume zu öffnen. Figure 12 zeigt einen Patienten in sitzender Position, und der L4-L5-Zwischenraum ist markiert.
Bei der Durchführung einer „Sattelnervenblockade“ sollte der Patient mindestens 5 Minuten lang sitzen bleiben, nachdem ein hyperbares Spinalanästhetikum platziert wurde, damit sich das Spinalanästhetikum in dieser Region festsetzen kann. Wenn eine stärkere Blockierung erforderlich ist, sollte der Patient unmittelbar nach der Platzierung an der Wirbelsäule in Rückenlage gebracht und der Tisch entsprechend angepasst werden.
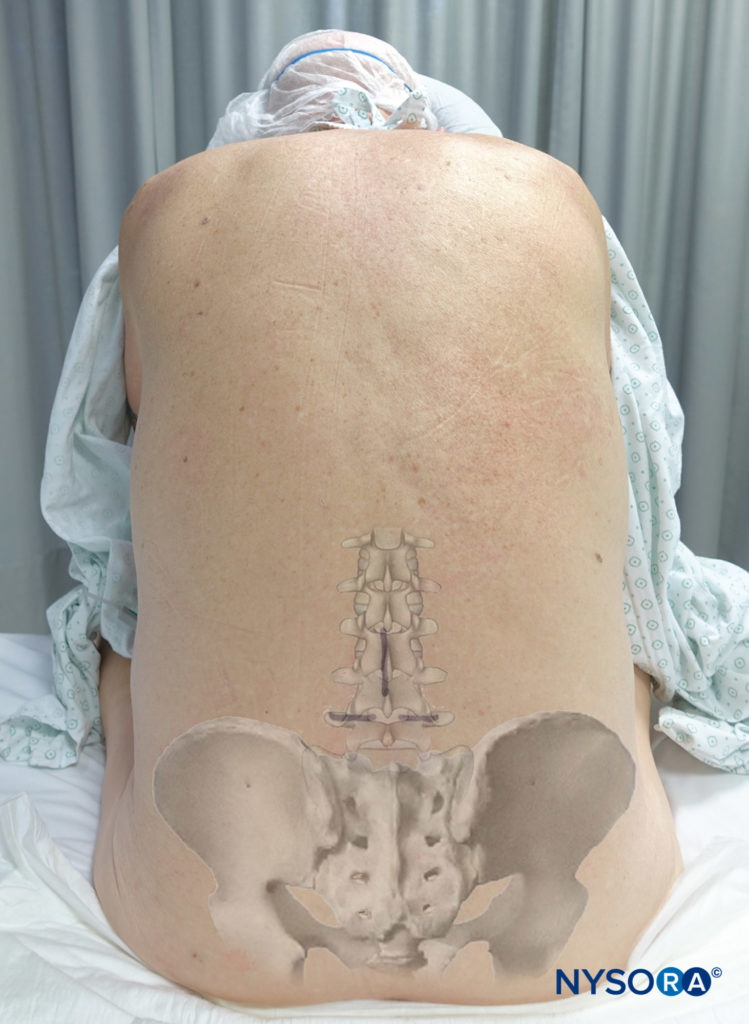
Abbildung 12.Patient in sitzender Position mit markiertem L4-L5-Zwischenraum
NYSORA-Tipps
• Die sitzende Position wird für eine tiefe Lenden- oder Kreuzbeinanästhesie und in Fällen verwendet, in denen der Patient übergewichtig ist und es schwierig ist, die Mittellinie in der Seitenlage zu finden.
• Bei der Durchführung einer Sattelnervenblockade sollte der Patient mindestens 5 Minuten lang sitzen bleiben, nachdem ein hyperbares Spinalanästhetikum platziert wurde, damit sich die Wirbelsäule in dieser Region einpendeln kann.
Bauchlage
Die Bauchlage kann zur Einleitung einer Spinalanästhesie verwendet werden, wenn der Patient für die Operation in dieser Position sein muss, beispielsweise für rektale, perineale oder lumbale Eingriffe. Für diese Verfahren wird eine hypobare oder isobare Lösung eines Lokalanästhetikums in Bauchlage bevorzugt. Dies vermeidet eine rostrale Ausbreitung des Lokalanästhetikums und verringert das Risiko einer hohen Spinalanästhesie.
NYSORA-Tipps
Die Bauchlage wird für die Spinalanästhesie verwendet, wenn der Patient für die Operation in dieser Position sein muss, beispielsweise für rektale, perineale oder lumbale Eingriffe.
Eine andere, weniger elegante Lösung besteht darin, dem Patienten in sitzender Position eine hyperbare Lösung eines Lokalanästhetikums zu injizieren und zu warten, bis die Spinalanästhesie „einsetzt“, was typischerweise 15–20 Minuten nach der Injektion der Fall ist. Der Patient wird dann unter aufmerksamer Überwachung in Bauchlage positioniert, einschließlich häufiger verbaler Kommunikation mit dem Patienten.
Technik der Lumbalpunktion
Bei der Durchführung einer Spinalanästhesie sollten geeignete Monitore aufgestellt werden und Atemwegs- und Wiederbelebungsgeräte sollten leicht verfügbar sein. Alle Geräte für die Spinalblockade sollten einsatzbereit sein, und alle notwendigen Medikamente sollten bereitgestellt werden, bevor der Patient für die Spinalanästhesie positioniert wird. Eine angemessene Vorbereitung der Wirbelsäule reduziert die Zeit, die für die Durchführung der Nervenblockade benötigt wird, und trägt dazu bei, dass sich der Patient wohlfühlt.
Die richtige Positionierung ist der Schlüssel zu einer schnellen und erfolgreichen Spinalanästhesie. Sobald der Patient richtig positioniert ist, sollte die Mittellinie palpiert werden. Die Beckenkämme werden palpiert und eine Linie zwischen ihnen gezogen, um den Körper von L4 oder den L4-L5-Zwischenraum zu finden. Andere Zwischenräume können identifiziert werden, je nachdem, wo die Nadel eingeführt werden soll.
Die Haut sollte mit einer Hautvorbereitungslösung wie 0.5 % Chlorhexidin gereinigt und der Bereich steril abgedeckt werden. Die Hautvorbereitungslösung sollte trocknen gelassen werden, und unbenutzte Hautvorbereitungslösung muss aus dem Arbeitsbereich des Anästhesisten entfernt werden. An der geplanten Einstichstelle wird eine kleine Quaddel Lokalanästhetikum in die Haut injiziert.
Dann wird mehr Lokalanästhetikum entlang dem beabsichtigten Weg der Einführung der Spinalnadel bis zur geschätzten Tiefe des Lig. supraspinale verabreicht. Dies dient einem doppelten Zweck: zusätzlicher Anästhesie für die Einführung der Spinalnadel und Identifizierung des richtigen Pfads für die Platzierung der Spinalnadel. Bei dünnen Patienten muss in diesem Stadium darauf geachtet werden, dass eine Duralpunktion und eine unbeabsichtigte Spinalanästhesie vermieden werden.
NYSORA-Tipps
• Bei der Durchführung einer Spinalanästhesie sollten geeignete Monitore aufgestellt werden und Atemwegs- und Reanimationsgeräte sollten leicht verfügbar sein.
• Alle Geräte für die Spinalblockade sollten einsatzbereit sein und alle notwendigen Medikamente sollten vorbereitet sein, bevor der Patient für die Spinalanästhesie positioniert wird.
Midline-Ansatz
Wenn der Mittellinienzugang verwendet wird, palpieren Sie den gewünschten Zwischenraum und injizieren Sie ein Lokalanästhetikum in die Haut und das subkutane Gewebe. Die Einführnadel wird mit einem leichten kranialen Winkel von 10° bis 15° platziert. Als nächstes wird die Spinalnadel durch die Einführhilfe geführt. Die Nadel geht durch das subkutane Gewebe, das Ligamentum supraspinale, das Ligamentum interspinale, das Ligamentum flavum, den Epiduralraum, die Dura mater und die Subarachnoidalhöhle, um den Subarachnoidalraum zu erreichen.
Aus dem Kompendium der Regionalanästhesie: Injektion der Spinalanästhesie über den Mittellinienzugang.
Der Widerstand ändert sich, wenn die Spinalnadel auf dem Weg zum Subarachnoidalraum jede Ebene durchläuft. Subkutanes Gewebe bietet der Spinalnadel weniger Widerstand als Bänder. Wenn die Spinalnadel durch die Dura mater geht, wird oft ein „Plopp“ geschätzt. Sobald dieses Knacken zu spüren ist, sollte das Mandrin von der Nadel entfernt werden, um den CSF-Fluss zu überprüfen. Bei Spinalnadeln mit höherem Gauge (26–29 Gauge) dauert dies normalerweise 5–10 Sekunden, aber bei manchen Patienten kann es eine Minute oder länger dauern. Wenn kein Durchfluss vorhanden ist, schlagen einige vor, die Nadel um 90° zu drehen, da die Nadelöffnung verstopft sein könnte. Trümmer können die Öffnung der Spinalnadel verstopfen. Falls erforderlich, ziehen Sie die Nadel zurück und reinigen Sie die Öffnung, bevor Sie die Spinalanästhesie erneut versuchen. Eine häufige Ursache für das Ausbleiben des CSF-Flusses ist, dass die Spinalnadel von der Mittellinie abweicht. Die Mittellinie sollte neu beurteilt und die Nadel neu positioniert werden.
Wenn die Spinalnadel den Knochen berührt, sollte die Tiefe der Nadel notiert und die Nadel weiter kranial platziert werden. Wenn Knochen erneut kontaktiert wird, sollte die Nadeltiefe mit der des letzten Knochenkontakts verglichen werden, um festzustellen, welche Struktur kontaktiert wird. Wenn beispielsweise der Knochenkontakt tiefer ist als beim ersten Einstich, sollte die Nadel weiter nach kranial umgelenkt werden, um den unteren Dornfortsatz zu vermeiden. Wenn der Knochenkontakt ungefähr in der gleichen Tiefe wie die ursprüngliche Insertion ist, kann es sein, dass die Lamina berührt wird, und die Mittellinie sollte neu beurteilt werden. Wenn der Knochenkontakt flacher ist als bei der ursprünglichen Einführung, sollte die Nadel nach kaudal umgelenkt werden, um den oberen Dornfortsatz zu vermeiden.
NYSORA-Tipps
• Wenn die Spinalnadel durch die Dura mater sticht, wird oft ein „Plopp“ geschätzt.
• Sobald dieses Knallen zu spüren ist, sollte das Mandrin aus der Einführhilfe entfernt werden, um den CSF-Fluss zu überprüfen.
• Bei Spinalnadeln mit höherem Gauge (26–29 Gauge) dauert dies normalerweise 5–10 Sekunden, aber bei manchen Patienten kann es länger dauern.
• Wenn kein Fluss vorhanden ist, könnte die Nadel durch eine Nervenwurzel verstopft sein und es kann hilfreich sein, sie um 90° zu drehen.
Wenn die Spinalnadel erneut eingeführt werden muss, ist es wichtig, die Nadel vor der Neuausrichtung auf Hautniveau zurückzuziehen. Nehmen Sie beim Wiedereinführen der Spinalnadel nur kleine Richtungsänderungen vor, da kleine Änderungen an der Oberfläche zu großen Richtungsänderungen führen, wenn die Nadel in größere Tiefen gelangt. Das Biegen und Krümmen der Spinalnadel beim Einführen durch die Haut oder den Einführer kann die Nadel auch vom Kurs ablenken, wenn versucht wird, den Subarachnoidalraum zu kontaktieren.
Beim Passieren einer Spinalnadel können Parästhesien ausgelöst werden. Der Stilett sollte von der Spinalnadel entfernt werden, und wenn Liquor gesehen wird und die Parästhesie nicht mehr vorhanden ist, ist es sicher, das Lokalanästhetikum zu injizieren. Möglicherweise wurde eine Cauda equina-Nervenwurzel angetroffen. Wenn kein Liquorfluss vorhanden ist, ist es möglich, dass die Spinalnadel eine Spinalnervenwurzel berührt hat, die den Epiduralraum durchquert. Die Nadel sollte entfernt und auf die der Parästhesie gegenüberliegende Seite umgelenkt werden.
Nachdem der freie Liquorfluss hergestellt ist, injizieren Sie das Lokalanästhetikum langsam mit einer Geschwindigkeit von weniger als 0.5 ml/s. Eine zusätzliche Aspiration von Liquor in der Mitte und am Ende der Injektion kann versucht werden, um die fortgesetzte subarachnoidale Verabreichung zu bestätigen, ist aber möglicherweise nicht immer möglich, wenn kleine Nadeln verwendet werden. Sobald die Injektion des Lokalanästhetikums abgeschlossen ist, werden die Einführhilfe und die Spinalnadel als eine Einheit vom Rücken des Patienten entfernt. Der Patient sollte dann entsprechend dem chirurgischen Eingriff und der Stärke des verabreichten Lokalanästhetikums gelagert werden. Der Tisch kann je nach Bedarf entweder in die Trendelenburg- oder in die Anti-Trendelenburg-Position gekippt werden, um die Höhe der Nervenblockade nach dem Testen der sensorischen Ebene anzupassen. Der Anästhesist sollte die Vitalfunktionen sorgfältig überwachen und unterstützen.
Aus dem Kompendium der Regionalanästhesie: Spinalanästhesie-Injektion, die die Ausbreitung des Lokalanästhetikums im intrathekalen Raum zeigt.
Paramedianer (lateraler) Zugang
Wenn der Patient ein verkalktes Ligamentum interspinale oder Schwierigkeiten beim Beugen der Wirbelsäule hat, kann ein paramedianer Zugang zur Durchführung einer Spinalanästhesie verwendet werden. Der Patient kann sich für diesen Zugang in jeder Position befinden: sitzend, seitlich oder sogar in Bauchlage. Nach Palpation der oberen und unteren lumbalen Dornfortsätze des gewünschten Zwischenraums wird Lokalanästhetikum 1 cm lateral des oberen Anteils des unteren Dornfortsatzes infiltriert. Die Nadel sollte leicht nach medial gerichtet sein. Ein medialer Winkel von 10° und 15° der Nadel erreicht die Mittellinie in einer Tiefe von etwa 5.7 cm (tan 80°) bzw. 3.7 cm (tan 75°). Dies zeigt, dass kleine Änderungen der Angulation deutliche Auswirkungen auf die Platzierung der Nadelspitze haben können. Obwohl auch eine leichte kraniale Winkelung erforderlich ist, ist ein häufiger Fehler ein zu steiler anfänglicher Ansatz. Wenn die Lamina berührt wird, sollte die Nadel nach kranial abgewinkelt und von der Lamina in den Subarachnoidalraum „abgeführt“ werden.
Andere Verfahren wurden beschrieben. Alle Techniken beinhalten eine ähnliche vertikale Achse für die Punktionsstelle (1–1.5 cm von der Mittellinie). Sie unterscheiden sich in der horizontalen Achse (z. B. 1 cm lateral des Dornfortsatzes, 1 cm lateral des Zwischenraums, 1 cm lateral und 1 cm unterhalb des Zwischenraums, 1 cm lateral und 1 cm unterhalb des unteren Aspekts des oberen Dornfortsatzes Prozess) und der Grad der erforderlichen Kopfwinkelung.
Abbildung Figure 13 zeigt die Orientierungspunkte, die für einen paramedianen Zugang zur Spinalanästhesie verwendet werden. Figure 14 zeigt die erfolgreiche Durchführung einer paramedianen Spinalanästhesie.

ABBILDUNG 13. Orientierungspunkte, die in einem paramedianischen Ansatz zur Spinalanästhesie verwendet werden.
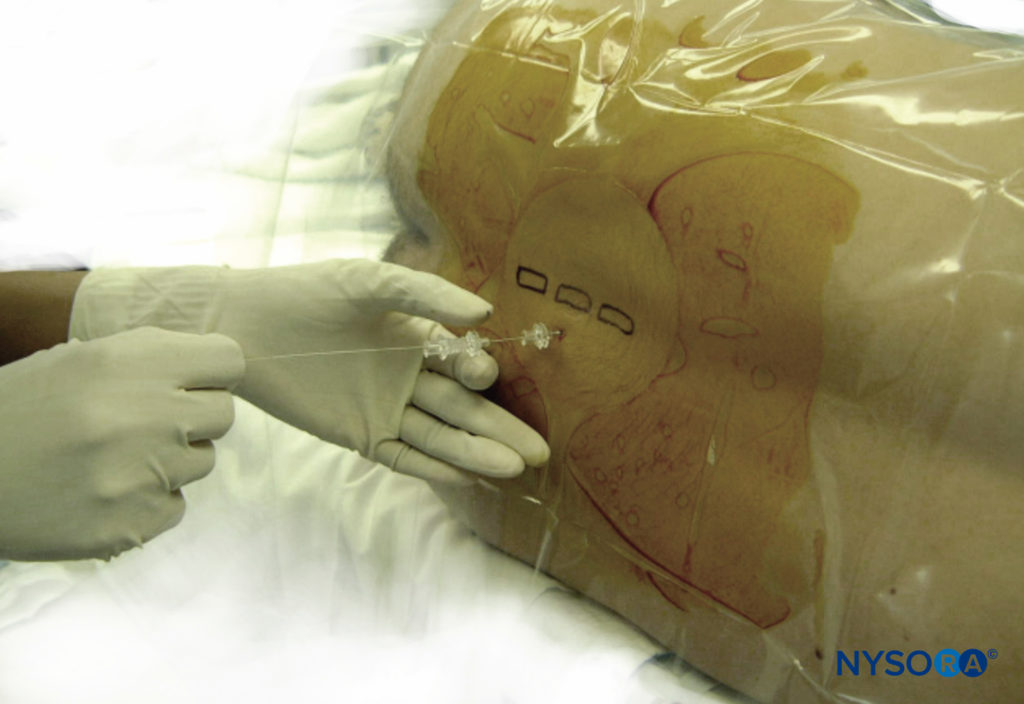
FIGUR 14. Paramedianer Zugang: Nadelplatzierung.
NYSORA-Tipps
Für den paramedianen Ansatz:
• Nach Abtasten der oberen und unteren lumbalen Dornfortsätze des gewünschten Zwischenraums wird Lokalanästhetikum 1 cm lateral des oberen Anteils des unteren Dornfortsatzes infiltriert.
• Die Nadel sollte leicht nach medial und kranial abgewinkelt sein.
• Wenn die Lamina berührt wird, sollte die Nadel nach kranial abgewinkelt und von der Lamina in den Subarachnoidalraum „abgeführt“ werden.
• Das Ligamentum flavum ist normalerweise der erste identifizierte Widerstand.
Taylor-Ansatz
Der Taylor- oder lumbosakrale Zugang zur Spinalanästhesie ist ein paramedianer Zugang, der auf den L5-S1-Zwischenraum gerichtet ist. Da dies der größte Zwischenraum ist, kann der Taylor-Ansatz verwendet werden, wenn andere Ansätze nicht erfolgreich sind oder nicht durchgeführt werden können. Wie beim paramedianen Zugang kann sich der Patient bei diesem Zugang in jeder Position befinden: sitzend, seitlich oder in Bauchlage.
Die Nadel sollte an einem Punkt 1 cm medial und unterhalb der Spina iliaca posterior superior eingeführt werden, dann kranial um 45°–55° und medial abgewinkelt werden. Dieser Winkel sollte medial genug sein, um die Mittellinie im L5-S1-Zwischenraum zu erreichen. Nach dem Einführen der Nadel
Der erste spürbare Widerstand ist das Ligamentum flavum, und dann wird die Dura mater punktiert, um einen freien Liquorfluss beim Eintritt in den Subarachnoidalraum zu ermöglichen. Figure 15 zeigt den Taylor-Ansatz zur Spinalanästhesie. Eine ultraschallgeführte Echtzeit-Spinalanästhesie in Bauchlage über den Taylor-Ansatz wurde beschrieben und kann den Patientenkomfort und die Compliance während des Verfahrens verbessern.
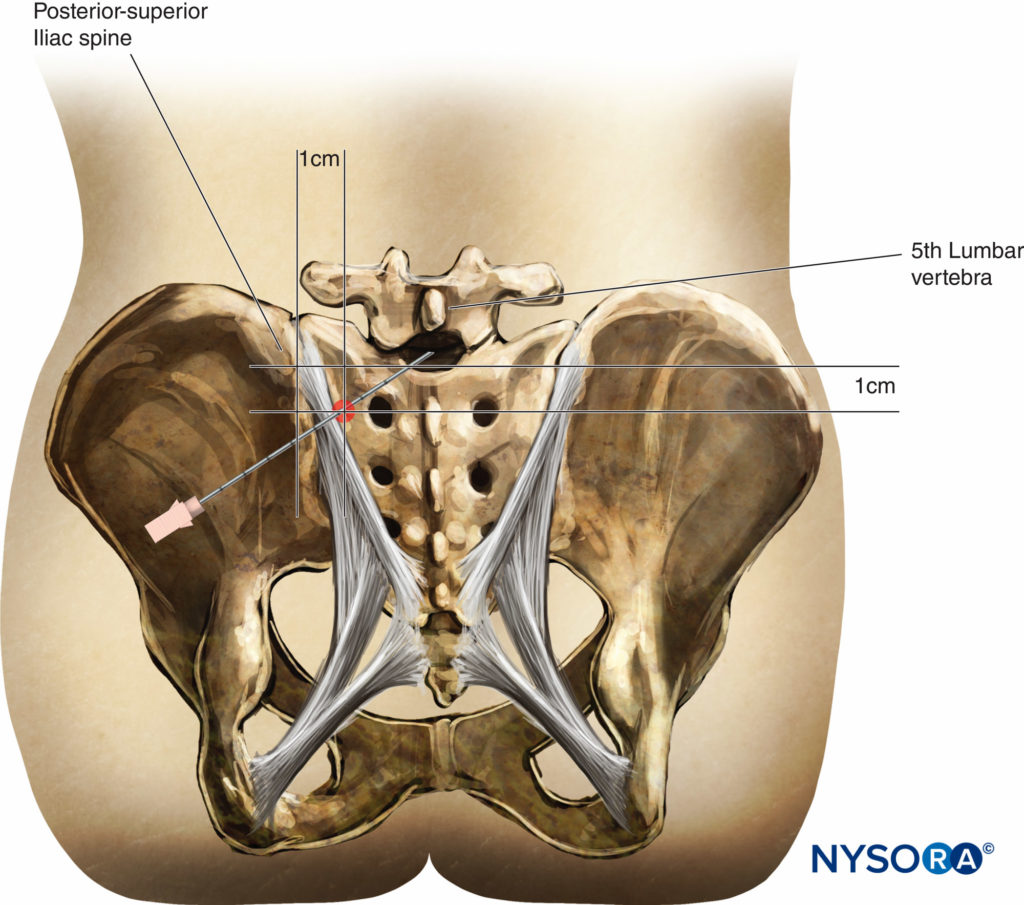
ABBILDUNG 15. Taylor-Ansatz zur Spinalanästhesie.
NYSORA-Tipps
Für den Taylor-Ansatz:
• Die Nadel sollte an einem Punkt 1 cm medial und unterhalb der Spina iliaca posterior superior eingeführt werden, dann kranial um 45°–55° und medial abgewinkelt werden.
• Dieser Winkel sollte medial genug sein, um die Mittellinie im L5-S1-Zwischenraum zu erreichen.
• Nach dem Einführen der Nadel ist der erste spürbare Widerstand das Ligamentum flavum.
KONTINUIERLICHE KATHETERTECHNIKEN
Zur kontinuierlichen Spinalanästhesie kann ein Verweilkatheter gelegt werden. Lokalanästhetika können wiederholt über den Katheter verabreicht und die Stärke und Dauer der Anästhesie je nach Bedarf für den chirurgischen Eingriff angepasst werden. Die Platzierung eines kontinuierlichen Spinalkatheters erfolgt auf ähnliche Weise wie bei einer normalen Spinalanästhesie, außer dass eine Nadel mit größerer Stärke, wie z. B. eine Tuohy, verwendet wird, um den Durchgang des Katheters zu ermöglichen. Nach Einbringen der Tuohy-Nadel wird der Subarachnoidalraum gefunden und der Spinalkatheter 2–3 cm in den Subarachnoidalraum eingeführt. Wenn es schwierig ist, den Katheter zu passieren, versuchen Sie, die Tuohy-Nadel um 180° zu drehen. Ziehen Sie den Katheter niemals zurück in den Nadelschaft, da die Gefahr besteht, dass der Katheter abgeschert wird und ein Stück davon im Subarachnoidalraum verbleibt. Wenn der Katheter zurückgezogen werden muss, ziehen Sie den Katheter und die Nadel zusammen zurück und versuchen Sie, die Wirbelsäule an einem anderen Zwischenraum fortzusetzen. Die Kommunikation ist entscheidend, um zu vermeiden, dass ein Spinalkatheter mit dem häufigeren Epiduralkatheter verwechselt wird. Dazu gehören Kennzeichnung, Dokumentation, Übergabe und Überwachung.
NYSORA-Tipps
• Nach Einführen der Tuohy-Nadel wird der Subarachnoidalraum erreicht und der Spinalkatheter 2–3 cm in den Subarachnoidalraum eingeführt.
• Wenn beim Einführen des Katheters Schwierigkeiten auftreten, versuchen Sie, die Tuohy-Nadel um 180° zu drehen.
• Die Kommunikation ist entscheidend, um zu vermeiden, dass ein Spinalkatheter mit dem häufigeren Epiduralkatheter verwechselt wird.
Da die zum Einführen des Spinalkatheters verwendete Nadel eine Nadel mit großem Durchmesser ist, besteht ein viel höheres Risiko für PDPH, insbesondere bei jungen weiblichen Patienten. Das Cauda-equina-Syndrom kann bei kleinen Spinalkathetern auftreten, daher hat die FDA von der Verwendung von Kathetern mit einem Durchmesser von weniger als 24 Gauge für die kontinuierliche Spinalanästhesie abgeraten.
Im Jahr 2008 berichtete eine randomisierte klinische Studie (FDA Investigational Device Exemption) über die Sicherheit kontinuierlicher spinaler „Mikrokatheter“ bei geburtshilflichen Patienten. Bei 28 Patienten wurde ein 329-Gauge-Katheter gelegt; Es wurden keine dauerhaften neurologischen Folgen berichtet. Die Studie verglich eine kontinuierliche Spinalanalgesie mit einer Epiduralanalgesie und fand niedrigere anfängliche Schmerzwerte, eine höhere Patientenzufriedenheit und weniger motorische Nervenblockaden in der Wirbelsäulengruppe, ohne Unterschied in den neonatalen oder geburtshilflichen Ergebnissen. Die Wirbelsäulengruppe hatte jedoch höhere Juckreizwerte und einen Trend zu mehr PDPH (9 % im Vergleich zu 4 % in der Epiduralgruppe). Intrathekalkatheter waren schwieriger zu entfernen als Epiduralkatheter. Bei einem Patienten war ein intrathekaler Katheter beim Entfernen gebrochen, wenn auch von einer ungeschulten Person, wodurch ein Fragment im Rücken des Patienten zurückblieb.
KLINISCHE SITUATIONEN IN DER PRAXIS DER SPINALANÄSTHESIE
Das Schwierige u Fehlgeschlagene Wirbelsäule
Die Spinalanästhesie gilt seit langem als zuverlässige Nervenblockade mit Ausfallraten von weniger als 1 %. In einer prospektiven Kohortenstudie mit geburtshilflichen Patientinnen betrug die Konversion zur Vollnarkose nur 0.5 %. Es wurden jedoch Ausfallraten von bis zu 17 % gemeldet. Eine fehlgeschlagene Spinalanästhesie kann sich als vollständiges Fehlen einer Nervenblockade, partielle Nervenblockade oder unzureichende Dauer der Nervenblockade äußern.
Obwohl Fachwissen die Wahrscheinlichkeit einer fehlgeschlagenen Wirbelsäule verringern kann, werden selbst erfahrene Kliniker mit fehlgeschlagenen Spinalnervenblockaden konfrontiert. Nachdem er durch das Auftreten von CSF beruhigt wurde, kann eine anschließende fehlgeschlagene oder lückenhafte Nervenblockade einen Anästhesisten frustriert und verwirrt zurücklassen. Bei der Behandlung einer fehlgeschlagenen Spinalblockade ist ein methodischer Ansatz erforderlich.
In einem hervorragenden Übersichtsartikel klassifizierten Fettes et al. das Versagen der Spinalanästhesie in fünf Gruppen: Versagen der Lumbalpunktion, Versagen der Lösungsinjektion, Ausbreitung der Lösung im Liquor, Arzneimittelwirkung auf die Nervenwurzeln und das Rückenmark sowie Patientenmanagement. Ihre Bewertung wird als nächstes zusammengefasst.
Fehlgeschlagene Lumbalpunktion
Bei Problemen mit der Platzierung einer Spinalanästhesie sollte der Anästhesist die Lage des Patienten neu beurteilen. Es sollte ein Mitglied des OP-Personals eingesetzt werden, das für die Unterstützung bei der Patientenpositionierung geschult ist. Alternativ kann die Positionierung des Patienten mit handelsüblichen Positionierungsvorrichtungen verbessert werden. Diese Geräte können helfen, die Wirbelsäulenflexion aufrechtzuerhalten und eine stabile Stütze für den Patienten zu schaffen, was nützlich sein kann, wenn kein geschultes OP-Personal zur Verfügung steht, um bei der Positionierung zu helfen.
Wenn der vorgeschlagene Zwischenraum nicht gefunden werden kann, kann der Zwischenraum über oder unter der ursprünglichen Stelle der spinalen Injektion versucht werden. Wenn die Sitzposition nicht verwendet werden kann oder nicht erfolgreich ist, kann die Seitenlage verwendet werden. Es kann entweder die Mittellinien- oder die laterale Paramedian-Technik versucht werden. Der größte interlaminare Raum befindet sich bei L5, und dieser kann über Taylors Ansatz gesucht werden, der zuvor in diesem Kapitel beschrieben wurde.
Drei unabhängige Prädiktoren für den Erfolg bei der Durchführung einer neuraxialen Nervenblockade wurden identifiziert: adäquate Positionierung, die Erfahrung des Anästhesisten und die Fähigkeit, anatomische Landmarken zu palpieren. Eine falsche Positionierung kann eher auf die Unfähigkeit des Patienten zurückzuführen sein, die Wirbelsäule zu beugen, als auf das Versäumnis des Anästhesisten, die Beugung zu fördern. Ein vorhersehbar schwieriger Rücken sollte nicht verwendet werden, um unerfahrene Auszubildende zu unterrichten. Bei nicht wahrnehmbaren anatomischen Orientierungspunkten kann die Spinalsonographie zur Unterstützung der Lumbalpunktion eingesetzt werden (siehe Abschnitt Neuroaxialer Ultraschall).
Ausfall der Lösungsinjektion
Aufgrund der geringen Injektatvolumina, die bei der Spinalanästhesie verwendet werden, können scheinbar unbedeutende Verringerungen des Lösungsvolumens zu einer nicht ausreichenden Nervenblockade führen. Eine Verringerung der injizierten Lösung kann das Ergebnis eines Injektatverlusts sein, wenn die Spinalspritze an der Nadelnabe befestigt ist, oder ein Verlust in Gewebe neben dem Subarachnoidalraum aufgrund einer Wanderung der Nadelöffnung oder der Öffnung, die mehrere potenzielle Räume überspannt (z. B. Subarachnoidalraum). und subduraler oder epiduraler Raum). Auch absichtliche Dosisreduktionen, in der Regel um Nebenwirkungen zu verringern, können zu einer verminderten Wirksamkeit führen.
Fehler der Lösungsausbreitung innerhalb des Liquors
Das Versagen der Verteilung der Lösung im Liquor kann auf spinale Deformitäten wie Kyphose oder Skoliose, frühere Operationen, transversale oder longitudinale Spinalsepten, Spinalstenose oder extradurale Zysten zurückzuführen sein. Tarlov-Zysten sind eine Art von extraduraler Zyste, die zufällig bei MRT-Scans gesehen werden und eine Inzidenz von bis zu 9% haben.
Obwohl sie normalerweise asymptomatisch sind, enthalten sie Liquor und können für eine positive Aspiration von Liquor, jedoch für ein Versagen einer vollständigen Nervenblockade verantwortlich sein. Das lumbale Liquorvolumen ist eine wichtige Determinante der Ausbreitung.
Versagen der Arzneimittelwirkung
Das Versagen der Arzneimittelwirkung kann durch die Verabreichung des falschen Arzneimittels verursacht werden. Das richtige Medikament kann aufgrund physikalisch-chemischer Instabilität (weniger wahrscheinlich bei modernen Wirkstoffen) inaktiv sein oder aufgrund chemischer Inkompatibilitäten beeinträchtigt sein, wenn zwei oder mehr Wirkstoffe verwendet werden. Das Phänomen der Lokalanästhesieresistenz wird in der Literatur hinterfragt.
Versagen des Patientenmanagements
Descartes‘ klassisches Schmerzbild aus dem 17. Jahrhundert, das eine Verbindung zwischen dem brennenden Fuß eines Jungen und seinem Gehirn über die Mitte seines Rückens zeigt – „so wie wenn Sie an einem Ende einer Schnur ziehen, Sie eine am anderen Ende hängende Glocke zum Klingen bringen“ – könnte zu der Annahme verleiten, dass eine Spinalanästhesie alle Schmerzen heilen kann. Die Schmerzwahrnehmung ist jedoch weitaus komplexer, und trotz perfekter Wirbelsäulenblockade kann ein Patient Beschwerden oder Schmerzen verspüren. Die Patienten sollten präoperativ über erwartete „normale“ Empfindungen wie Ziehen, Drücken und Strecken aufgeklärt werden. Ein präoperativer Spinalblocktest zur Beruhigung sowohl des Patienten als auch des Anästhesisten kann den Patienten paradoxerweise belasten, wenn er zu früh durchgeführt wird. Intraoperativ kann ein Patient eine zusätzliche Anxiolyse und Analgesie oder Vollnarkose benötigen.
Die Behandlung einer fehlgeschlagenen Spinalnervenblockade hängt davon ab, ob sie präoperativ oder intraoperativ auftritt, und von der Art des Versagens. Zu den Optionen zur Optimierung der Spinalanästhesie gehören die Änderung der Position des Patienten, um die Ausbreitung zu verbessern, und die Wiederholung der Spinalanästhesie. Bei der Wiederholung einer Spinalnervenblockade müssen zwei wichtige Prinzipien beachtet werden. Erstens darf der zweite Versuch nicht mit dem ersten identisch sein. Dies dient nicht nur dazu, ein erneutes Versagen zu vermeiden, sondern möglicherweise auch zu verhindern, dass sich eine zweite Dosis Lokalanästhetikum auf engstem Raum ansammelt, was zu neurologischen Schäden führen kann. Zweitens kann eine wiederholte Gabe zu einer übermäßigen Ausbreitung des Lokalanästhetikums führen. Alternativen wie Epiduralanästhesie, periphere Nervenblockade, lokale Infiltration, systemische Analgesie und Vollnarkose sollten je nach Fall in Betracht gezogen werden und würden den Rahmen dieses Kapitels sprengen.
Unbeabsichtigte subdurale Nervenblockade
Eine fehlgeschlagene Subarachnoidalnervenblockade kann das Ergebnis einer versehentlichen subduralen Injektion sein und verdient besondere Aufmerksamkeit. Der Subduralraum ist ein potentieller Raum, der erst nach dem Zerreißen von Neurothelzellen innerhalb des Raums durch iatrogene Nadeleinführung und Flüssigkeitsinjektion real wird (vgl Figure 4). Charakteristische Merkmale einer SDB sind ein hohes sensorisches Niveau mit motorischer und sympathischer Schonung. Dies kann das Ergebnis der begrenzten ventralen Kapazität des Raums sein, was zu einer Schonung der vorderen motorischen und sympathischen Fasern führt. Eine SDB kann sich jedoch auch auf verschiedene Arten zeigen: fehlgeschlagene Nervenblockade, einseitige Nervenblockade, Horner-Syndrom, Trigeminuslähmung, respiratorische Insuffizienz oder Bewusstlosigkeit aufgrund einer Beteiligung des Hirnstamms. Die Nervenblockade setzt langsamer ein als die Subarachnoidal-Nervenblockade, aber schneller als die Epidural-Nervenblockade und verschwindet normalerweise nach 2 Stunden.
Die Inzidenz einer subduralen Injektion nach Kontrastmittelmyelographie liegt zwischen 1 % und 13 %. Die Inzidenz von SDB nach versuchter Spinalanästhesie ist nicht bekannt. Da die Dura während einer versuchten Spinalanästhesie absichtlich verletzt wird, kann die Inzidenz von SDB höher sein als bei einer Epiduralnervenblockade (verschiedene Angaben zwischen 0.024 % und 0.82 %). Die Größe des erworbenen Subduralraums ist wahrscheinlich proportional zum injizierten Flüssigkeitsvolumen. Daher sind die typischen Volumina, die bei der Spinalanästhesie verwendet werden, möglicherweise nicht so signifikant wie die Volumina, die bei der Epiduralanästhesie verwendet werden
Ambulante Spinalanästhesie
Die Zahl der Operationen nimmt von Jahr zu Jahr zu und es werden mehr ambulant durchgeführt. Als Anästhesisten suchen wir immer nach neuen Wegen, um eine effiziente Anästhesieversorgung bereitzustellen, die sicher ist, Schmerzen kontrolliert, eine rechtzeitige Entlassung des Patienten nach Hause gemäß dem Protokoll der Pflegeeinheit nach der Anästhesie ermöglicht und einfach durchzuführen und reproduzierbar ist. Es wurde bereits vorgeschlagen, die Spinalanästhesie in das ambulante Operationsmodell aufzunehmen.
Einseitige Spinalnervenblockade
Die Verwendung einer einseitigen Spinalnervenblockade bei älteren Patienten und ambulanten Operationen hat ein Wiederaufleben erlebt. Die einseitige Spinalanästhesie wurde 1950 von Ruben und Kamsler beschrieben. Ihr Bericht betraf 116 Patienten zur chirurgischen Reposition einer Hüftfraktur, die unter einseitiger Spinalblockade durchgeführt wurde. Es wurden keine Todesfälle gemeldet und es wurde kein erhöhtes Betriebsrisiko festgestellt. In letzter Zeit ist die Aufmerksamkeit wieder auf die Anwendung der einseitigen Spinalanästhesie bei älteren Patienten326 und für ambulante Operationen gelenkt worden.
Die Anwendung einer einseitigen Spinalanästhesie führt zu verringerten Veränderungen des systolischen, mittleren und diastolischen Drucks oder der Sauerstoffsättigung bei älteren Traumapatienten (z. B. Hüftfraktur). Das Halten der Operationsseite nach oben und die Verwendung einer hypobaren Spinallösung in niedriger Dosis für diese Fälle führt zu einer hervorragenden Anästhesie und bemerkenswerten Blutstillung, wenn der Patient für 5–10 Minuten in Seitenlage gehalten wird, bevor er in Rückenlage gebracht wird. Bei der Verwendung von hyperbaren Lösungen sollte die operative Seite abhängig sein.
Ambulante Operationen mit hyperbarem 0.5%igem Bupivacain benötigen etwa 16 Minuten für die Entwicklung der chirurgischen Anästhesie ab dem Zeitpunkt der Injektion bei unilateraler Spinalanästhesie und 13 Minuten bei traditioneller bilateraler Spinalanästhesie. Weniger hämodynamische Veränderungen finden sich in der Gruppe mit einseitiger Spinalanästhesie, mit schnellerer Rückbildung der Nervenblockade und gleicher Zeit bis zur Entlassung nach Hause.
Im Vergleich zu anderen ambulanten Operationen ist bei der Kniearthroskopie eine geringere motorische Nervenblockade erforderlich. Dosen von hyperbarem Bupivacain von nur 4–5 mg sind wirksam, wenn sie mit einer einseitigen Lagerung kombiniert werden. Höhere Dosen verzögern die Genesung. Die Zugabe von intrathekalen Opioiden verbessert die Analgesie, verstärkt jedoch die opioidbedingten Nebenwirkungen. Ropivacain verbessert die Erholungszeit nicht.
Bei der Durchführung einer einseitigen Spinalanästhesie wird die Verwendung einer 25-Gauge- oder 27-Gauge-Kanüle mit Bleistiftspitze empfohlen, deren Öffnung zur Operationsseite zeigt. Niedrig dosiertes Bupivacain sollte verwendet werden, mit hyperbarem Bupivacain (operative Seite nach unten) bei ambulanten Operationen und hypobarem Bupivacain (operative Seite nach oben) bei älteren Traumapatienten. Es sollte eine langsame Injektionsrate verwendet werden, um einen laminaren Fluss zu erzeugen, der die Erzeugung eines einseitigen Blocks unterstützt. Es gibt kaum Hinweise darauf, dass es hilfreich ist, einen Patienten länger als 15 Minuten in Seitenlage zu halten.
Der geburtshilfliche Patient
1901 beschrieb Kreis das erste Spinalanästhetikum zur vaginalen Entbindung. Im folgenden Jahr führte Hopkins die erste erfolgreiche Spinalanästhesie für einen Kaiserschnitt bei einer Frau mit Placenta praevia durch. Seit dieser Zeit hat sich die Spinalanästhesie für Wehen und Entbindung stark weiterentwickelt. Obwohl aufgrund des erhöhten Aspirationsrisikos und der schwierigen Intubation viele Argumente gegen eine Vollnarkose bei der Schwangeren vorgebracht werden, muss der Anästhesist bereit sein, angesichts einer erfolglosen oder totalen Spinalanästhesie eine Vollnarkose einzuleiten.
Die geburtshilfliche Regionalanästhesie ist ein Thema für sich und wird als solches behandelt Geburtshilfe Regionalanästhesie. Beispiele dafür, wie sich die Spinalanästhesie in der geburtshilflichen Population unterscheidet, sind in aufgeführt Tabelle 10.
TABELLE 10. Spinalanästhesie bei der geburtshilflichen Patientin.
| Zustimmung | • Es kann schwierig sein, bei einer Patientin in den Wehen eine wirklich informierte Einwilligung zu erhalten. |
| Risiken | • Geringeres Risiko schwerwiegender dauerhafter Komplikationen im Vergleich zur neuraxialen Blockade bei nicht-geburtshilflichen Eingriffen.26 • Höheres Risiko für postduralpunktionsbedingte Kopfschmerzen. • Eine Metaanalyse aus dem Jahr 2005 zeigte, dass der pH-Wert der Nabelschnur, ein Indikator für das Wohlbefinden des Fötus, bei Spinalanästhesie im Vergleich zu Epiduralanästhesie und Allgemeinanästhesie niedriger war, obwohl dies möglicherweise auf die Verwendung von Ephedrin in den analysierten Studien zurückzuführen ist.118 |
| Benefits | • Vermeidung der mütterlichen Risiken einer Vollnarkose, insbesondere der drei As: Aspiration, Awareness und schwieriger Atemweg. • Vermeidung einer fetalen Exposition gegenüber Vollnarkosemitteln. • Frühe mütterliche Bindung zum Neugeborenen. • Partner oder Begleitperson können anwesend sein. |
| Indikationen | • Eine Spinalanästhesie kann zur Analgesie der Wehen, Zangengeburt, Kaiserschnitt, manuelle Entfernung der Plazenta, Dammreparatur oder nicht-geburtshilfliche Chirurgie bei geburtshilflichen Patientinnen eingesetzt werden. |
| Anatomie | • Eine übertriebene Lendenlordose während der Schwangerschaft kann die Höhe der Interkristalllinie erhöhen, so dass 6 % der termingerechten Frauen eine Interkristalllinie bei oder über L3.352 haben • Die zur Durchführung einer Spinalanästhesie erforderliche ausgeprägte Lendenbeugung kann aufgrund des graviden Uterus schwierig sein. |
| Physiologie | • Aortokavale Kompression durch einen trächtigen Uterus kann eine durch die Wirbelsäule induzierte Hypotonie verschlimmern, was sowohl für die Mutter als auch für den Fötus Risiken birgt. |
| Pharmakologie | • Schwangere Frauen benötigen weniger Lokalanästhetika, um das gleiche Anästhesieniveau zu erreichen wie nicht schwangere Frauen. Diese Beobachtung ist wahrscheinlich sowohl auf hormonelle als auch auf mechanische Faktoren zurückzuführen. |
| Technik | • Bereiten Sie sich auf die Umstellung auf Vollnarkose vor. Vor der Platzierung eines Spinalanästhetikums sollte die schwangere Patientin 30 ml 0.3 M Natriumcitrat oral erhalten, um die Magensäure zu verringern. Ausrüstung und Medikamente, die für die Durchführung einer Vollnarkose erforderlich sind, sollten leicht verfügbar sein. • Nach Verabreichung der Spinalanästhesie sollte sich die Patientin in Rückenlage mit Uterusverlagerung nach links befinden. Die fetale Herzfrequenz sollte mittels Doppler oder fetalem Kopfhaut-Elektrokardiogramm (EKG) überwacht werden. • Für einen Kaiserschnitt ist normalerweise eine Blockade auf T4-Ebene erforderlich, da auf das Peritoneum gezogen wird und der Uterus nach außen zeigt. • Einige Patienten klagen über Dyspnoe aufgrund einer abdominalen und interkostalen motorischen Blockade, aber wenn der Patient deutlich sprechen kann, ist normalerweise nur eine Beruhigung und Überwachung erforderlich. Ein Sensibilitätsverlust in der oberen Extremität oder die Unfähigkeit, den Unterarm zu strecken (C7/C8), sollten den Arzt vor einer drohenden Zwerchfelllähmung (C3/C4/C5) warnen. • Wenn die Mutter das Neugeborene stillen möchte, sollte eine Beurteilung der Kraft der oberen Extremitäten vorgenommen werden. Eine angemessene Personalausstattung sollte es jemand anderem als dem Anästhesisten ermöglichen, für das Wohlergehen des Neugeborenen verantwortlich zu sein. • Hypotonie und Übelkeit sind häufig, insbesondere in der Wahltherapie (siehe Abschnitt zur Behandlung von Hypotonie nach Spinalanästhesie). Prophylaktisches Phenylephrin und „Coloading“ mit Flüssigkeit beugen Hypotonie und Übelkeit wirksam vor. Tabelle 23–9 enthält einen empfohlenen Behandlungsplan für die Behandlung von Hypotonie während eines elektiven Kaiserschnitts. |
Der antikoagulierte Patient
Mit zunehmendem Alter der Bevölkerung stellen sich immer mehr Patienten mit prä-, intra- oder postoperativen Anforderungen an eine gerinnungshemmende, gerinnungshemmende oder thrombolytische Therapie zur Operation vor. Es werden weiterhin neuartige Wirkstoffe entwickelt, was Anlass zur Sorge bei Patienten gibt, die sich einer Spinalanästhesie unterziehen. Diese Bedenken führten zur Entwicklung der evidenzbasierten ASRA-Leitlinien zur Regionalanästhesie bei Patienten, die eine antithrombotische oder thrombolytische Therapie erhalten, jetzt bis zu ihrer dritten Ausgabe
Auf den Leser wird verwiesen Neuraxiale Anästhesie und periphere Nervenblockaden bei Patienten unter Antikoagulanzien für eine eingehende Diskussion über die Anwendung der neuraxialen Anästhesie bei antikoagulierten Patienten.
Andere klinische Situationen
Spinalanästhesie bei pädiatrischen Patienten und Patienten mit vorbestehender Neurologie sind abgedeckt Pädiatrische Epidural- und Spinalanästhesie & Analgesie und Regionalanästhesie bei Patienten mit vorbestehender neurologischer Erkrankung, Bzw.
JÜNGSTE ENTWICKLUNGEN IN DER SPINALANÄSTHESIE
Neuroaxialer Ultraschall
Die herkömmliche Palpation der Oberflächenanatomie hat sich als unzuverlässig erwiesen. Der neuraxiale Ultraschall zielt darauf ab, die Ungenauigkeiten der Oberflächenanatomie mit der Sonoanatomie zu überwinden. Die erste Beschreibung der ultraschallgestützten Lumbalpunktion erfolgte im Jahr 1971. In jüngerer Zeit wurde neuraxialer Ultraschall als Scan vor dem Eingriff und zur Nadelplatzierung in Echtzeit verwendet. Ein Großteil der Beweise zum neuraxialen Ultraschall bezieht sich auf präprozedurale Scans vor der Epiduralanästhesie, insbesondere im Rahmen der geburtshilflichen Anästhesie, und wurde von einer begrenzten Anzahl spezialisierter Zentren erstellt. Diese Beweise zeigen, dass das Scannen Nadelversuche verringert, die Tiefe des Epiduralraums genau vorhersagt und die Erfolgsrate von jungen Auszubildenden verbessern kann.
Weniger gut untersucht ist die Spinalsonographie im Rahmen einer Single-Shot-Spinalanästhesie. Die Sonographie ermöglicht eine erhöhte Genauigkeit bei der Identifizierung von Lendenzwischenräumen. Dies ist wichtig, da die Palpation der Lendenwirbelsäule wahrscheinlich einen höheren Zwischenraum als erwartet erzeugt und der Conus medullaris zeitweise niedriger als das konventionell gelehrte L1-Niveau ist. Diese beiden Tatsachen stellen nicht nur ein theoretisches Risiko dar, sondern haben auch zu anhaltenden neurologischen Schäden geführt. Eine Beobachtungsstudie bei orthopädischen Patienten zeigte eine genaue Ultraschallvorhersage der Tiefe der Dura vor der Einführung in die Wirbelsäule. Die präprozedurale Sonographie wurde verwendet, um eine Spinalanästhesie in klinisch schwierigen Situationen wie Fettleibigkeit, Kyphoskoliose und früheren Wirbelsäulenoperationen, einschließlich Harrington-Stäbchen, zu erreichen. Eine ultraschallgeführte Spinalanästhesie in Echtzeit wurde bei technisch schwierigen Patienten und in Bauchlage über den Taylor-Ansatz beschrieben. Eine randomisierte Studie, die präoperatives Scannen mit Standard-Palpation für die Spinalanästhesie bei Patienten mit schwierigen anatomischen Orientierungspunkten auf der Oberfläche vergleicht, zeigte einen zweifachen Unterschied im Erfolg des ersten Versuchs (62 % Ultraschall vs. 32 % Kontrolle).
Das Ultraschallscannen der Neuraxis lernt man am besten in maßgeschneiderten Workshops und Simulationen. Das Ultraschallvorschieben einer Spinalnadel in Echtzeit in den Subarachnoidalraum ist eine fachmännische Fähigkeit, und der Arzt sollte über beträchtliche Sonden- und Nadelkenntnisse verfügen. Das Scannen und Markieren des Rückens eines Patienten vor dem Eingriff erfordert weniger Hand-Auge-Koordination, kann aber auch schwierig zu erlernen sein. Die Kompetenz bei der Identifizierung bestimmter Dornfortsätze wurde nach dem Scannen von 22–36 Patienten erreicht. Hier skizzieren wir sechs sonoanatomische Ansichten der Lendenwirbelsäule und eine vereinfachte Methode zur Durchführung eines neuraxialen Scans vor dem Eingriff und skizzieren häufige Fallstricke für Anfänger.
Sonoanatomie
Verschiedene Forscher haben eine unterschiedliche Anzahl von notwendigen sonografischen Ansichten beschrieben, die oft mit phantasievollen Spitznamen verbunden sind. Karmakar bezieht sich auf „Pferdeköpfe“, „Kamelbuckel“ und „Dreizack“-Zeichen (paramediane Längsansichten), während Carvalho sich auf eine „Säge“ (Längsansicht) und eine „fliegende Fledermaus“ (Queransicht) bezieht. Der Anfänger sollte sich nicht durch die unterschiedliche Nomenklatur verwirren lassen, da es sich lediglich um Werkzeuge zur Mustererkennung handelt.
Aufgrund der knöchernen Strukturen, die sie umhüllen, sind spezielle Ultraschallfenster erforderlich, um die Neuraxis sichtbar zu machen. Sechs Grundansichten sind in dargestellt Tabelle 11.
Die vorderen und hinteren Komplexe sind nützliche Begriffe zur Identifizierung von Strukturen. Der vordere Komplex repräsentiert die vordere Dura, das hintere Längsband und den hinteren Wirbelkörper. Der hintere Komplex repräsentiert das Ligamentum flavum, den Epiduralraum und die hintere Dura.
Während das „Ziel“ der Spinalanästhesie der hintere Komplex ist, bedeutet die Darstellung des vorderen Komplexes ein klares sonographisches Fenster durch den Interlaminarraum.
Neuraxialer Ultraschall-Scan vor dem Eingriff
- Nach konventioneller Lagerung des Patienten Wenden Sie eine gebogene Array-Sonde mit niedriger Frequenz (2 bis 5 MHz) an zur Mitte des unteren Rückens des Patienten in Querrichtung.
- Optimieren Sie das Bild für Tiefen-, Frequenz- und Zeitverstärkungskompensation.
- Markieren Sie die Mittellinie. Dies erfolgt durch einfaches Ausrichten der transversal ausgerichteten Sonde, so dass eine Symmetrie des Ultraschallbildes besteht (die linke Seite des Bildschirms ist ein Spiegel der rechten Seite). Dies entspricht entweder der transversalen Dornfortsatz- oder der transversalen interlaminaren Ansicht. Durch Schieben der quer angelegten Sonde in kranialer Richtung wird ein Markierstift in Abständen verwendet, um die Haut neben der Mitte der langen Kante der Sonde zu markieren. Praktischerweise hilft es, niedrig zu beginnen und oberhalb der Sonde auf ultraschallfreier Haut zu markieren Gel. Diese Technik geht davon aus, dass die Anatomie des Patienten tatsächlich symmetrisch ist (keine Skoliose, Rotation oder Metallarbeiten).
- Identifizieren Sie den lumbosakralen Übergang. Die Sonde ist so ausgerichtet, dass sie eine paramediane sagittale laminare Ansicht erhält. Nach der Identifizierung der Lamina wird die Sonde nach kaudal geschoben, bis eine kontinuierliche echoreiche Linie (Kreuzbein) zu sehen ist. Zwischen dem Kreuzbein und der fünften Lendenleiste sollte ein vorderer Komplex zu sehen sein (siehe Abbildung 16 ).
- Markieren Sie die Schicht von L1–L5. Die Sonde kann dann unter Beibehaltung einer paramedianen Ausrichtung als Markierungsstift nach kranial bewegt werden, wiederum in der Mitte der langen Kante der Sonde, und wird verwendet, um die Lamina oder interlaminaren Räume zu markieren.
- Erhalten Sie eine transversale interlaminare Ansicht auf der gewünschten Höhe. Die Sonde wird auf der gewünschten Höhe (z. B. L3–L4) transversal gedreht. Leichtes Neigen und Gleiten von kranial-kaudal ist notwendig, um das Erscheinungsbild des posterioren und anterioren Komplexes zu optimieren.
- Identifizieren Sie die Dura (hinterer Komplex) und markieren Sie die Tiefe mit Bremssätteln.
- Beachten Sie die Neigung der Sonde (normalerweise leicht kopfwärts). Dies zeigt den erforderlichen Winkel der Nadel an, sobald sie am optimalen Einstichpunkt eingeführt ist.
- Markieren Sie den optimalen Einstichpunkt der Nadel. Ein Stift wird verwendet, um die vier Mittelpunkte der langen und kurzen Kanten der Sonde zu markieren. Die Sonde wird abgelegt und eine horizontale und vertikale Linie konstruiert. Wo sie sich schneiden, ist der optimale Nadeleinführpunkt. Die vertikale Linie sollte mit der zuvor markierten Mittellinie übereinstimmen.
- Überprüfen Sie den optimalen Einführpunkt, indem Sie die Sonde erneut ansetzen und Gewährleistung einer guten Sicht auf den vorderen Komplex.


ABBILDUNG 16. Ultraschallbild des lumbosakralen Übergangs. Eine kontinuierliche echoreiche Linie (Sacrum) ist zu sehen. Zwischen dem Kreuzbein und der fünften Lendenleiste sollte ein anteriorer Komplex (AC) zu sehen sein.
Zusätzliche Ansichten der Wirbelsäule können erhalten werden, indem die Sonde in einer paramedianen sagittalen Ausrichtung platziert und seitlich durch die paramedianen Laminar-, Gelenkfortsatz- und Querfortsatzansichten geschoben wird. Die Paramedian-Schrägansicht wird erhalten, indem die Sonde nach medial geneigt wird, um die posterioren und anterioren Komplexe durch den Interlaminarraum hervorzuheben. Diese Ansicht kann für eine ultraschallgeführte Spinalanästhesie in Echtzeit verwendet werden.
Fallstricke
Der größte Fallstrick besteht darin, nach der anfänglichen Schulung auf den schwierigen Patienten zu warten, bevor man einen neuroaxialen Ultraschall versucht. Das Ultraschallscannen erfordert eine Mustererkennung, und Fähigkeiten müssen durch das Scannen von „einfachen“ Rücken erreicht werden. Als Grund für das Versagen wurde eine ungenaue Hautmarkierung postuliert. Achten Sie darauf, dass die gebogene Array-Sonde bei Verwendung eines Markierungsstifts senkrecht zur Haut steht. Die Verwechslung des vorderen Komplexes mit dem hinteren Komplex birgt die Gefahr einer groben Überschätzung der Tiefe der (hinteren) Dura. Beim Messen der Duraltiefe kann die Sonde die Haut eindrücken und dadurch die Tiefe unterschätzen. Eine falsche Identifizierung des lumbosakralen Übergangs oder das Nichterkennen von Anomalien des Übergangs, die bei 12 % der Bevölkerung vorhanden sind, führt zu einer falschen Kennzeichnung der interlaminaren Räume. Zuletzt sollte Ultraschallgel von der Haut entfernt werden, bevor eine neuraxiale Nervenblockade durchgeführt wird.
Laparoskopische Chirurgie mit lumbaler Spinalanästhesie
Lumbale Spinalanästhesie wurde in den Einstellungen der laparoskopischen extraperitonealen und intraperitonealen Leistenhernienreparatur, der ambulanten gynäkologischen Laparoskopie, der laparoskopischen Cholezystektomie und der laparoskopischen ventralen Hernienreparatur verwendet. Die laparoskopische Chirurgie bei einem wachen Patienten erfordert einige besondere Überlegungen. Erstens sind die Auswahl und Aufklärung der Patienten von größter Bedeutung. Bei der Interpretation der Konversionsraten für Vollnarkosen in klinischen Studien ist Vorsicht geboten, da Patienten, die der Studie zustimmen, ein waches Verfahren möglicherweise eher tolerieren. Eine Anxiolyse sollte angeboten werden, und die Patienten sollten über erwartete Empfindungen beraten werden. Pneumoperitoneum kann als Gewicht auf dem Bauch wahrgenommen werden. Die Möglichkeit einer Umstellung auf eine Vollnarkose, die häufig auf Schulterspitzenschmerzen zurückzuführen ist, sollte diskutiert werden.
Operationstechnik und Trokarstellen müssen möglicherweise modifiziert werden. Pneumoperitoneum mit Distickstoffmonoxid-Insufflation wurde verwendet, um peritoneale Reizungen und Schmerzen zu vermeiden, von denen angenommen wird, dass sie mit einer herkömmlichen Kohlendioxid-Insufflation verbunden sind.
Später wurde jedoch eine Kohlendioxid-Insufflation verwendet. Es wurde vorgeschlagen, eine mit Zwerchfellreizungen verbundene seitliche Neigung des Kopfes nach oben nach links zu vermeiden. Einige Studien haben die Insufflation auf weniger als 11 mmHg begrenzt und eine Magensonde verwendet, um den Magen zu dekomprimieren und das Aspirationsrisiko zu verringern. Andere änderten die Operationstechnik nicht, mit Ausnahme der Low-Flow-Insufflation (nasogastrale Sonden wurden vermieden und die Kohlendioxid-Insufflation bei 15 mmHg beibehalten).
Die Zugabe von intrathekalem Fentanyl oder Clonidin kann die Schmerzen an der Schulterspitze verringern.
Die beiden Hauptnachteile der Spinalanästhesie für die laparoskopische Cholezystektomie schienen Schulterspitzenschmerzen zu sein, die zu einer Unzufriedenheit des Patienten oder zur Umstellung auf eine Vollnarkose und einer hohen PDPH-Rate (bis zu 10 %) führten. Aufgrund der geringen Anzahl und der heterogenen Techniken in früheren Studien war es schwierig, die ideale Technik zu etablieren.
Tzovaras und Kollegen veröffentlichten 2008 eine Zwischenanalyse einer randomisierten Studie. Einhundert Patienten wurden randomisiert entweder einer Vollnarkose oder einer Spinalanästhesie für die laparoskopische Cholezystektomie zugeteilt. Beide Studienarme hatten eine Magensonde und eine Kohlendioxid-Insufflation bis zu einem Maximum von 10 mmHg. Der Wirbelsäulengruppe wurden 3 ml 0.5%iges hyperbares Bupivacain, 250 μg Morphin und 20 μg Fentanyl auf L2-L3-Ebene über eine 25-Gauge-Bleistiftspitzennadel in die rechte Seitenlage injiziert. Anschließend wird der Patient für 3 Minuten in Trendelenburg-Lagerung gelagert. Trotz intraoperativer Beschwerden oder Schmerzen an der Schulterspitze bei 43 % der Patienten der Wirbelsäulengruppe benötigte nur die Hälfte dieser Patienten Fentanyl und kein Patient musste auf eine Vollnarkose umgestellt werden.
96 % bzw. 94 % der Patienten in der Spinal- und Allgemeinanästhesiegruppe waren mit ihrem Verfahren sehr oder ziemlich zufrieden. Darüber hinaus waren die postoperativen Schmerzen in der Wirbelsäulengruppe geringer als in der Vollnarkosegruppe. Die Studie wurde abgebrochen, da der primäre Endpunkt (Schmerz) bei den ersten 100 Patienten erreicht wurde. Kein Patient in der Wirbelsäulengruppe hatte eine klassische PDPH (G. Tzovaras, persönliche Mitteilung, 2012).
Thorakale Spinalanästhesie
Die thorakale Spinalanästhesie wurde in den frühen 1900er Jahren von Professor Thomas Jonnesco beschrieben, obwohl er von seinen Zeitgenossen, einschließlich Professor Bier, kritisiert wurde. Er nannte seine Technik „allgemeine spinale Analgesie“ und beschrieb zwei Punktionsstellen, die Zwischenräume T1–T2 und T12–L1, je nach erforderlicher Operation. In seinem Artikel stellte er erstaunliche Behauptungen auf, er sei in der Lage, Kopf- und Halsoperationen, einschließlich einer totalen Laryngotomie, unter hochthorakaler Analgesie durchzuführen, und sagte 1909 fälschlicherweise voraus, dass seine Technik „in kurzer Zeit allgemein akzeptiert“ werden würde.
Im Jahr 2006 wurde über eine thorakale Spinalanästhesie bei einem Patienten berichtet, der eine laparoskopische Cholezystektomie benötigte. Die segmentale thorakale Spinalanästhesie zur laparoskopischen Cholezystektomie hat sich bei einer kleinen Anzahl gesunder Patienten als wirksam erwiesen, obwohl die Autoren warnen, dass die noch in den Kinderschuhen steckende Technik nicht in der Routinepraxis eingesetzt werden sollte.
Die Spinalanästhesie wird traditionell im Lendenwirbelbereich unterhalb der Höhe des Conus medullaris durchgeführt, um eine Verletzung des Rückenmarks zu vermeiden. Allerdings haben MRT-Bilder, wenn auch in Rückenlage, gezeigt, dass das mittlere bis untere thorakale Segment des Rückenmarks anterior liegt, sodass zwischen der Dura und dem Rückenmark ein mit Liquor gefüllter Raum vorhanden ist (vgl Figure 17).
ABBILDUNG 17. Mittellinien-MRT der Wirbelsäule. In den thorakalen Segmenten ist das Rückenmark anterior positioniert, wobei ein erheblicher Raum (*) zwischen der hinteren Dura und dem Rückenmark verbleibt. Auf der Lendenwirbelsäule verschwindet der Raum fast vollständig. (Wiedergabe mit freundlicher Genehmigung von van Zundert AA, Stultiens G, Jakimowicz JJ, et al: Segmental spinal ansthetic for cholecystecomy in a patient with heavy lung disease. Br J Anaesth. 2006 Apr;96(4):464-466.)
ZUSAMMENFASSUNG
Die Spinalanästhesie ist eine zuverlässige, sichere und wirksame Form der Anästhesie. Seit den Anfängen Ende des 19. Jahrhunderts hat sich viel verändert. Die Beherrschung der Spinalanästhesie erfordert Übung, Fleiß und Kenntnisse in Physiologie, Pharmakologie und Anatomie.
Bei der Durchführung einer Spinalanästhesie muss die Patientensicherheit immer im Vordergrund stehen. Die Spinalanästhesie ist eine unverzichtbare Technik in der Praxis der modernen Anästhesie. Ein ergänzendes Video zur Spinalanästhesie finden Sie unter Lehrvideos für NYSORA-Studenten: Spinalanästhesie.
Dieser Text ist ein Inhaltsbeispiel aus der Kompendium der Regionalanästhesie auf dem NYSORA LMS.
NYSORAs Kompendium der Regionalanästhesie ist einfach der umfassendste und praktischste Lehrplan für Regionalanästhesie von A bis Z mit NYSORAs Premium-Inhalten. Im Gegensatz zu Lehrbüchern und E-Books wird das Kompendium kontinuierlich aktualisiert und enthält die neuesten Videos, Animationen und visuellen Inhalte von NYSORA.
Das Kompendium ist einer von mehreren Goldstandard-Bildungskursen im Lernsystem von NYSORA (das NYSORA LMS) und die Registrierung bei NYSORALMS.com ist gratis. Der VOLLSTÄNDIGE Zugriff auf das Kompendium basiert jedoch auf einem Jahresabonnement, da eine Armee von Illustratoren, Videoeditoren und ein Schulungsteam erforderlich sind, um es weiterhin zum BESTEN Werkzeug für die Schulung in allen Bereichen der Regionalanästhesie zu machen. Während Sie sich das Kompendium als E-Book über Steroide vorstellen können, wird Ihnen eine schnelle Probefahrt in Echtzeit ein Gefühl dafür geben, wie unglaublich das Kompendium wirklich ist. Ihr Abonnement wird die Art und Weise verändern, wie Sie über Regionalanästhesie lesen:
- Visuell lernen: Alles Regionale, einschließlich Wirbelsäulen-, Epidural- und Nervenblockadeverfahren und Behandlungsprotokolle
- Sehen Sie sich Schritt-für-Schritt-Techniken für über 60 Nervenblockaden an
- Greifen Sie auf die sagenumwobenen Illustrationen, Animationen und Videos von NYSORA zu (z. B. Reverse Ultrasound Anatomy)
- Greifen Sie über die Desktop-Plattform und die mobile App auf RA-Informationen auf jedem Gerät zu
- Erhalten Sie Echtzeit-Updates
- Review-Infografiken zur Prüfungsvorbereitung (z. B. EDRA)
- Verwenden Sie den Community-Feed mit echten Falldiskussionen, Bildern und Videos, die von Abonnenten und weltweit führenden Experten gleichermaßen gepostet und diskutiert werden.
Auch wenn Sie das Kompendium nicht abonnieren möchten, registrieren Sie sich doch beim NYSORA LMS, erfahren Sie als Erster, was es Neues in der Regionalanästhesie gibt, und beteiligen Sie sich an Fallbesprechungen.
Hier ist, wovon sich die Aktivität ernährt NYSORA LMS sieht aus wie:
Wir sind davon überzeugt, dass, sobald Sie das erleben Kompendium auf die NYSORA LMS, und Sie werden nie wieder zu Ihren alten Büchern zurückkehren, und Ihr Abonnement wird dazu beitragen, NYSORA.com für den Rest der Welt kostenlos zu halten.
Zusätzliche Lektüre
- Koller C: Vorlaufende Mittheilung über locale Anasthesirung am Auge. Klin Mbl Augenheilk 1884;22:60–63.
- Halsted WS: Praktische Kommentare zum Gebrauch und Missbrauch von Kokain; vorgeschlagen durch seinen ausnahmslos erfolgreichen Einsatz in mehr als tausend kleineren chirurgischen Eingriffen. NY Med J 1885;42:294.
- Corning JL: Spinalanästhesie und lokale Medikation der Nabelschnur. NY Med J 1885;42:483–485.
- Gorelick PB, Zych D: James Leonard Corning und die frühe Geschichte der Spinalpunktion. Neurologie 1987;37(4):672–674.
- Arendt K, Demaerschalk BM, Wingerchuk DM, Camann W: Atraumatische Lumbalpunktionsnadeln: Verfehlen wir nach all den Jahren immer noch den Punkt? Neurologe 2009;15(1):17–20.
- Wynter E: Vier Fälle von tuberkulöser Meningitis, bei denen eine Parazentese der Theca vertebralis zur Entlastung des Flüssigkeitsdrucks durchgeführt wurde. Lancet 1891: 981–982.
- Ball C, Westhorpe R: Lokalanästhesie – frühe Spinalanästhesie. Anaesth Intensive Care 2003;31(5):493.
- Bier A: Experimente zur Kokainisierung des Rückenmarks. Dtsch Z Chir 1899;51:361–369.
- Marx GF: Die erste Spinalanästhesie. Wer verdient die Lorbeeren? Reg Anesth 1994;19(6):429–430.
- Wulf HF: Das 1998-jährige Jubiläum der Spinalanästhesie. Anesthesiology 89;2(500):506–1996. Larson MD: Tait und Caglieri. Das erste Spinalanästhetikum in Amerika. Anesthesiology 85;4(913):919–XNUMX.
- Matas R: Lokal- und Regionalanästhesie mit Kokain und anderen Schmerzmitteln, einschließlich der Subarachnoidalmethode, wie sie in der allgemeinen chirurgischen Praxis angewendet wird. Phil Med J 1900;6:820–843.
- Vandam LD: Über die Ursprünge der intrathekalen Anästhesie. Reg Anesth Pain Med 1998;23(4):335–339; Diskussion 84–87.
- Tuffier T: Anesthesie medullaire chirurgicale par injection sous-arachnoidienne lombaire de cocaine; Technik und Ergebnisse. Semin Med 1900;20:167.
- Barker AE: Ein Bericht über klinische Erfahrungen mit Spinalanalgesie in 100 Fällen und einige Überlegungen zum Verfahren. BMJ 1907;1:665–674.
- Labat G: Durchblutungsstörungen im Zusammenhang mit einer Subarachnoidalnervenblockade. Long Island Med J 1927;21:573.
- Pitkin G: Kontrollierbare Spinalanästhesie. Am J Surg 1928;5:537.
- Größe LF: Spinalanästhesie für Ober- und Unterbauchoperationen. N Engl J Med 1928;199:61.Sise LF: Pontocainglucose für die Spinalanästhesie. Surg Clin North Am 1935;15:1501.
- Brown DL, Fink BR: Die Geschichte der Neuralblockade und der Schmerzbehandlung. In Cousins MJ, Bridenbaugh PO (Hrsg.): Neural block, 3rd ed. Lippincott-Raven, 1998, S. 3–27.
- Adriani J, Roman-Vega D: Sattelnervenblockadeanästhesie. Am J Surg 1946;71:12.
- Maltby JR, Hutter CD, Clayton KC: Der Fall Woolley und Roe. Br. J. Anaesth 2000;84(1):121–126.
- Kennedy F, Effron AS, Perry G: Die schwere Rückenmarkslähmung durch Spinalanästhesie. Surg Gynecol Obstet 1950;91(4):385–398.
- Dripps RD, Vandam LD: Langzeit-Follow-up von Patienten, die 10,098 Spinalanästhetika erhalten haben: Versäumnis, größere neurologische Folgen zu entdecken. JAMA 1954;156(16):1486–1491.
- Morgan P: Spinalanästhesie in der Geburtshilfe. Can J Anaesth 1995;42(12): 1145–1163.
- Cook TM, Counsell D, Wildsmith JA: Schwerwiegende Komplikationen der zentralen neuraxialen Nervenblockade: Bericht über das Third National Audit Project des Royal College of Anaesthetists. Br. J. Anaesth 2009;102(2):179–190.
- Greene HM: Lumbalpunktion und die Prävention von Kopfschmerzen nach Punktion. JAMA 1926;86:391–392.
- Greene BA: Eine 26-Gauge-Lumbalpunktionsnadel: Ihr Wert bei der Prophylaxe von Kopfschmerzen nach Spinalanalgesie bei vaginaler Entbindung. Anästhesiologie 1950;11:464–469.
- Hart JR, Whitacre RJ: Bleistiftspitzennadel zur Vorbeugung von postspinalen Kopfschmerzen. JAMA 1951;147(7):657–658.
- Sprotte G, Schedel R, Pajunk H: [Eine „atraumatische“ Universalnadel für die Single-Shot-Regionalanästhesie: klinische Ergebnisse und eine 6-Jahres-Studie in über 30,000 Regionalanästhesien]. Reg Anaesth 1987;10(3):104–108.
- Calthorpe N: Die Geschichte der Spinalnadeln: Auf den Punkt gebracht. Anästhesie 2004;59(12):1231–1241.
- McDonald SB: Ist eine neuraxiale Blockade bei Patienten mit Aortenstenose kontraindiziert? Reg Anesth Pain Med 2004;29(5):496–502.
- O'Keefe JH Jr, Shub C, Rettke SR: Risiko nichtkardialer chirurgischer Eingriffe bei Patienten mit Aortenstenose. Mayo Clin Proc 1989;64(4): 400–405.
- Collard CD, Eappen S, Lynch EP, Concepcion M: Kontinuierliche Spinalanästhesie mit invasiver hämodynamischer Überwachung zur chirurgischen Reparatur der Hüfte bei zwei Patienten mit schwerer Aortenstenose. Anesth Analg 1995; 81(1):195–198.
- Bamford C, Sibley W, Laguna J: Anästhesie bei Multipler Sklerose. Can J Neurol Sci 1978;5(1):41–44.
- Kytta J, Rosenberg PH: Anästhesie für Patienten mit Multipler Sklerose. Ann Chir Gynaecol 1984;73(5):299–303.
- Bouchard P, Caillet JB, Monnet F, Banssillon V: [Spinalanästhesie und Multiple Sklerose]. Ann Fr. Anesth Reanim 1984;3(3):194–198.
- Levesque P, Marsepoil T, Ho P, Venutolo F, Lesouef JM: [Multiple Sklerose offenbart durch Spinalanästhesie]. Ann Fr. Anesth Reanim 1988; 7(1):68–70.
- Vadalouca A, Moka E, Sykiotis C: Kombinierte Spinal-Epidural-Technik zur totalen Hysterektomie bei einer Patientin mit fortgeschrittener, progressiver Multipler Sklerose. Reg Anesth Pain Med 2002;27(5):540–541.
- Horlocker TT, Wedel DJ: Regionalanästhesie beim immunkompromittierten Patienten. Reg Anesth Pain Med 2006;31(4):334–345.
- Chin KJ, Macfarlane AJ, Chan V, Brull R: Die Verwendung von Ultraschall zur Erleichterung der Spinalanästhesie bei einem Patienten mit vorheriger lumbaler Laminektomie und Fusion: Ein Fallbericht. J Clin Ultrasound 2009;37(8):482–485.
- Prasad GA, Tumber PS, Lupu CM: Ultraschallgeführte Spinalanästhesie. Can J Anaesth 2008;55(10):716–717.
- Costello JF, Balki M: Kaiserschnittgeburt unter ultraschallgeführter Spinalanästhesie [korrigiert] bei einer Gebärenden mit Poliomyelitis und Harrington-Instrumentierung. Can J Anaesth 2008;55(9):606–611.
- Douglas MJ, Swenerton JE: Epiduralanästhesie bei drei Gebärenden mit lumbalen Tätowierungen: Eine Überprüfung möglicher Auswirkungen. Kann J Anaesth 2002; 49(10):1057–1060.
- Mavropoulos A, Camann W: Verwendung eines Lendentattoos zur Unterstützung der Spinalanästhesie bei Kaiserschnittgeburten. Int J Obstet Anesth 2009;18(1):98–99.
- Balki M, Carvalho JC: Intraoperative Übelkeit und Erbrechen beim Kaiserschnitt unter Regionalanästhesie. Int J Obstet Anesth 2005; 14(3):230–241.
- Mishriky BM, Habib AS: Metoclopramid zur Prophylaxe von Übelkeit und Erbrechen während und nach Kaiserschnitt: Eine systematische Überprüfung und Metaanalyse. Br. J. Anaesth 2012;108(3):374–383.
- Carpenter RL, Caplan RA, Brown DL, Stephenson C, Wu R: Inzidenz und Risikofaktoren für Nebenwirkungen der Spinalanästhesie. Anesthesiology 1992;76(6):906–916.
- Evans CH: Prinzipien und Technik der Spinalanästhesie. Höber, 1929.
- Ure D, James KS, McNeill M, Booth JV: Glycopyrrolat reduziert Übelkeit während der Spinalanästhesie für den Kaiserschnitt, ohne das Ergebnis des Neugeborenen zu beeinträchtigen. Br. J. Anaesth 1999;82(2):277–279.
- George RB, Allen TK, Habib AS: Serotonin-Rezeptor-Antagonisten zur Vorbeugung und Behandlung von Juckreiz, Übelkeit und Erbrechen bei Frauen, die sich einem Kaiserschnitt mit intrathekalem Morphin unterziehen: Eine systematische Überprüfung und Metaanalyse. Anesth Analg 2009;109(1):174–182.
- Allen TK, Habib AS: P6-Stimulation zur Vorbeugung von Übelkeit und Erbrechen im Zusammenhang mit einem Kaiserschnitt unter neuraxialer Anästhesie: Eine systematische Überprüfung randomisierter kontrollierter Studien. Anesth Analg 2008;107(4):1308–1312.
- Crowley LJ, Buggy DJ: Zittern und neuraxiale Anästhesie. Reg Anesth Pain Med 2008;33(3):241–252.
- Saito T, Sessler DI, Fujita K, Ooi Y, Jeffrey R: Thermoregulatorische Wirkungen der Spinal- und Epiduralanästhesie während der Kaiserschnittgeburt. Reg Anesth Pain Med 1998;23(4):418–423.
- Ballantyne JC, Loach AB, Carr DB: Juckreiz nach epiduralen und spinalen Opiaten. Pain 1988;33(2):149–160. Bauchat JR: Focused Review: Neuraxiales Morphin und orale Herpes-Reaktivierung in der geburtshilflichen Bevölkerung. Anesth Analg 2010;111(5): 1238–1241.
- Crighton IM, Hobbs GJ, Reid MF: Ondansetron zur Behandlung von Juckreiz nach spinalen Opioiden. Anästhesie 1996;51(2):199–200.
- Schaffartzik W, Hirsch J, Frickmann F, Kuhly P, Ernst A: Hörverlust nach Spinal- und Allgemeinanästhesie: Eine vergleichende Studie. Anesth Analg 2000;91(6):1466–1472.
- Karatas E, Goksu S, Durucu C, Isik Y, Kanlikama M: Bewertung des Hörverlusts nach Spinalanästhesie mit otoakustischen Emissionen. Eur Arch Otorhinolaryngol 2006;263(8):705–710.
- Lee CM, Peachman FA: Einseitiger Hörverlust nach Spinalanästhesie, behandelt mit epiduralem Blutpflaster. Anesth Analg 1986;65(3):312.
- Fog J, Wang LP, Sundberg A, Mucchiano C: Hörverlust nach Spinalanästhesie hängt mit der Nadelgröße zusammen. Anesth Analg 1990;70(5):517–522.
- Finegold H., Mandell G., Vallejo M., Ramanathan S.: Verursacht eine Spinalanästhesie einen Hörverlust in der geburtshilflichen Bevölkerung? Anesth Analg
2002;95(1):198–203; Inhaltsverzeichnis. - Michel O, Brusis T: Hörverlust als Folge einer Lumbalpunktion. Ann Otol Rhinol Laryngol 1992;101(5):390–394.
- Mulroy MF, Alley EA: Management von Blasenvolumina bei der Verwendung von neuraxialer Anästhesie. Int Anesthesiol Clin 2012;50(1):101–110.
- Choi S, Mahon P, Awad IT: Neuraxiale Anästhesie und Blasenfunktionsstörung in der perioperativen Phase: Eine systematische Überprüfung. Can J Anaesth 2012;59(7):681–703.
- Lambert DH: Komplikationen der Spinalanästhesie. Int Anesthesiol Clin 1989;27(1):51–55.
- Harrington BE: Postduralpunktionskopfschmerz und die Entwicklung des epiduralen Blutpflasters. Reg Anesth Pain Med 2004;29(2):136–163; Diskussion 35.
- Vandam LD, Dripps RD: Langzeit-Follow-up von Patienten, die 10,098 Spinalanästhetika erhielten; Syndrom des verminderten intrakraniellen Drucks (Kopfschmerzen und Augen- und Hörprobleme). JAMA 1956;161(7): 586–591.
- Choi PT, Galinski SE, Takeuchi L, Lucas S, Tamayo C, Jadad AR: PDPH ist eine häufige Komplikation der neuraxialen Blockade bei Gebärenden: Eine Metaanalyse geburtshilflicher Studien. Can J Anaesth 2003;50(5): 460–469.
- Horlocker TT: Komplikationen der Spinal- und Epiduralanästhesie. Anesthesiol Clin North Am 2000;18(2):461–485.
- Horlocker TT, McGregor DG, Matsushige DK, Schroeder DR, Besse JA: Eine retrospektive Überprüfung von 4767 aufeinanderfolgenden Spinalanästhetika: zentral
Komplikationen des Nervensystems. Gruppe für perioperative Ergebnisse. Anesth Analg 1997;84(3):578–584. - Reiss W, Shariat AN, Kurapati S, Hadzic A: Intraneurale Injektionen. Reg Anesth Pain Med 2011;36(1):97–98.
- Burke D, Wildsmith JA: Meningitis nach Spinalanästhesie. Br. J. Anaesth 1997;78(6):635–636.
- Goldman WW Jr, Sanford JP: Eine „Epidemie“ chemischer Meningitis. Am J Med 1960;29:94–101.
- Hurst EW: Adhäsive Arachnoiditis und Gefäßverschluss durch Detergenzien und andere chemische Reizstoffe: Eine experimentelle Studie. J Pathol
Bacteriol 1955;70(1):167–178.Marinac JS: Drug- and chemical-induced aseptic meningitis: A review of theliteratur. Ann Pharmacother 1992;26(6):813–822. - Carp H, Bailey S: Der Zusammenhang zwischen Meningitis und Duralpunktion bei bakteriämischen Ratten. Anesthesiology 1992;76(5):739–742.
- Teele DW, Dashefsky B, Rakusan T, Klein JO: Meningitis nach Lumbalpunktion bei Kindern mit Bakteriämie. N. Engl. J. Med. 1981;305(18):1079–1081.
- Eng RH, Seligman SJ: Lumbalpunktion-induzierte Meningitis. JAMA 1981;245(14):1456–1459.
- G. Conangla, L. Rodriguez, C. Alonso-Tarres, A. Avila, AG de la Campa: [Streptococcus-salivarius-Meningitis nach Spinalanästhesie]. Neurologie
2004;19(6):331–333. - Pandian JD, Sarada C, Radhakrishnan VV, Kishore A: Iatrogene Meningitis nach Lumbalpunktion – ein vermeidbares Gesundheitsrisiko. J Hosp Infect 2004;56(2):119–124.
- Kocamanoglu IS, Sener EB, Tur A, Ustun E, Sahinoglu H: Streptokokken-Meningitis nach Spinalanästhesie: Fallbericht. Kann J Anaesth 2003; 50(3):314–315.
- Yaniv LG, Potasman I: Iatrogene Meningitis: Eine zunehmende Rolle für resistente Viridans-Streptokokken? Fallbericht und Rückblick auf die letzten 20 Jahre. Scand J Infect Dis 2000;32(6):693–696.
- Santillan A, Nacarino V, Greenberg E, Riina HA, Gobin YP, Patsalides A: Gefäßanatomie des Rückenmarks. J Neurointerv Surg 2012;4(1):
67-74. - Ilias WK, Klimscha W, Skrbensky G, Weinstabl R, Widhalm A: Kontinuierliche Mikrospinalanästhesie: Mechanismen aus einer anderen Perspektive
Cauda-Equina-Syndrom hervorrufen. Anästhesie 1998;53(7):618–623. - Rigler ML, Drasner K, Krejcie TC, et al: Cauda equina-Syndrom nach kontinuierlicher Spinalanästhesie. Anesth Analg 1991;72(3):275–281.
- Benson JS: Sicherheitswarnung der US Food and Drug Administration: Cauda equina-Syndrom im Zusammenhang mit der Verwendung von kleinkalibrigen Kathetern bei kontinuierlicher Spinalanästhesie. AANA J 1992;60(3):223.
- Mollmann M, Holst D, Lubbesmeyer H, Lawin P: Kontinuierliche Spinalanästhesie: Mechanische und technische Probleme der Katheterplatzierung. Reg Anesth 1993;18(6 Suppl):469–472.
- Loo CC, Irestedt L: Cauda-Equina-Syndrom nach Spinalanästhesie mit hyperbarem 5% Lignocain: Eine Überprüfung von sechs Fällen von Cauda-Equina-Syndrom, die der schwedischen Arzneimittelversicherung 1993–1997 gemeldet wurden. Acta Anaesthesiol Scand 1999;43(4):371–379.
- Panadero A, Monedero P, Fernandez-Liesa JI, Percaz J, Olavide I, Iribarren MJ: Wiederholte transiente neurologische Symptome nach Spinalanästhesie mit hyperbarem 5% Lidocain. Br. J. Anaesth 1998;81(3): 471–472.
- Pavon A, Anadon Senac P: [Neurotoxizität von intrathekalem Lidocain]. Rev. Esp Anestesiol Reanim 2001;48(7):326–336.
- Moen V, Dahlgren N, Irestedt L: Schwere neurologische Komplikationen nach zentralen neuroaxialen Blockaden in Schweden 1990–1999. Anesthesiology 2004;101(4):950–959.
- Akioka K, Torigoe K, Maruta H, et al: Ein Fall von Cauda-Equina-Syndrom nach Spinalanästhesie mit hyperbarem Dibucain. J Anesth 2001;
15 (2): 106-107. - Lopez-Soriano F, Lajarin B, Verdu JM, Rivas F, Lopez-Robles J: [Cauda equina hemisyndrome after intradurale Anästhesie mit Bupivacain für
Hüftoperation]. Rev. Esp Anestesiol Reanim 2002;49(9):494–496. - Vianna PT, Resende LA, Ganem EM, Gabarra RC, Yamashita S, Barreira AA: Cauda equina-Syndrom nach spinalem Tetracain: Elektromyographische Auswertung – 20 Jahre Nachbeobachtung. Anesthesiology 2001;95(5): 1290–1291.
- Woods WW, Franklin RG: Progressive adhäsive Arachnoiditis nach Spinalanästhesie. Calif Med 1951;75(3):196–198.
- Joseph SI, Denson JS: Spinalanästhesie, Arachnoiditis und Querschnittslähmung. JAMA 1958;168(10):1330–1333.
- Parnass SM, Schmidt KJ: Nebenwirkungen von Spinal- und Epiduralanästhesie. Drug Saf 1990;5(3):179–194.
- Roche J: Steroidinduzierte Arachnoiditis. Med. J. Aust 1984;140(5):281–284.
- Aldrete JA: Neurologische Defizite und Arachnoiditis nach neuroaxialer Anästhesie. Acta Anaesthesiol Scand 2003;47(1):3–12.
- Yokoyama M, Itano Y, Kusume Y, Oe K, Mizobuchi S, Morita K: Die totale Spinalanästhesie bietet eine vorübergehende Linderung hartnäckiger Schmerzen. Can J Anaesth 2002;49(8):810–813.
- Auroy Y, Benhamou D, Bargues L, et al.: Schwerwiegende Komplikationen der Regionalanästhesie in Frankreich: Der SOS-Hotline-Service für Regionalanästhesie.
Anesthesiology 2002;97(5):1274–1280. - Vandam LD, Dripps RD: Langzeit-Follow-up von Patienten, die 10,098 Spinalanästhetika erhielten. IV. Neurologische Erkrankung Vorfall zu traumatischen
Lumbalpunktion während der Spinalanästhesie. JAMA 1960;172:1483–1487. - Aromaa U, Lahdensuu M, Cozanitis DA: Schwere Komplikationen im Zusammenhang mit Epidural- und Spinalanästhesien in Finnland 1987–1993. Eine Studie
basierend auf Patientenversicherungsansprüchen [siehe Kommentar]. Acta Anaesthesiol Scand 1997;41(4):445–452. - Auroy Y, Narchi P, Messiah A, Litt L, Rouvier B, Samii K: Schwerwiegende Komplikationen im Zusammenhang mit der Regionalanästhesie: Ergebnisse einer prospektiven Umfrage in Frankreich. Anesthesiology 1997;87(3):479–486.
- Brull R, McCartney CJ, Chan VW, El-Beheiry H: Neurologische Komplikationen nach Regionalanästhesie: Zeitgenössische Risikoschätzungen.
Anesth Analg 2007;104(4):965–974. - Buggy DJ: Zentrale neuraxiale Nervenblockade: Risiko klarer definieren. Br. J. Anaesth 2009;102(2):151–153.
- van Zundert AA, Stultiens G, Jakimowicz JJ, et al: Laparoskopische Cholezystektomie unter segmentaler Thoraxspinalanästhesie: Eine Durchführbarkeit
lernen. Br. J. Anaesth 2007;98(5):682–686. - van Zundert AA, Stultiens G, Jakimowicz JJ, van den Borne BE, van der Ham WG, Wildsmith JA: Segmentale Spinalanästhesie zur Cholezystektomie bei einem Patienten mit schwerer Lungenerkrankung. Br J Anaesth 2006; 96(4):464–466.
- Hamad MA, El-Khattary OA: Laparoskopische Cholezystektomie unter Spinalanästhesie mit Lachgas-Pneumoperitoneum: Eine Machbarkeitsstudie. Surg Endosc 2003;17(9):1426–1428.
- Tzovaras G, Fafoulakis F, Pratsas K, Georgopoulou S, Stamatiou G, Hatzitheofilou C: Laparoskopische Cholezystektomie unter Spinalanästhesie: Eine Pilotstudie. Surg Endosc 2006;20(4):580–582.
- G. Tzovaras, F. Fafoulakis, K. Pratsas, S. Georgopoulou, G. Stamatiou, C. Hatzitheofilou: Wirbelsäulen- versus Allgemeinanästhesie für die laparoskopische Cholezystektomie: Zwischenanalyse einer kontrollierten randomisierten Studie. Arch Surg 2008;143(5):497–501.
- Yuksek YN, Akat AZ, Gozalan U, et al: Laparoskopische Cholezystektomie unter Spinalanästhesie. Am J Surg 2008;195(4):533–536.
- Cook TM: Bericht und Ergebnisse des 3. National Audit Project des Royal College of Anaesthetists. 2009: 17–26.
- Guay J: Die Wirkung von neuraxialen Nervenblockaden auf den chirurgischen Blutverlust und die Anforderungen an Bluttransfusionen: Eine Metaanalyse. J Clin Anesth 2006;18(2):
124-128. - Mauermann WJ, Schilling AM, Zuo Z: Ein Vergleich zwischen neuraxialer Nervenblockade und Vollnarkose bei elektivem Hüftgelenkersatz: Eine Metaanalyse. Anesth Analg 2006;103(4):1018–1025.
- Afolabi BB, Lesi FE, Merah NA: Regionalanästhesie versus Vollnarkose für den Kaiserschnitt. Cochrane Database Syst Rev 2006(4):CD004350.
- Reynolds F, Seed PT: Anästhesie für Kaiserschnitt und Säure-Basen-Status bei Neugeborenen: Eine Meta-Analyse. Anästhesie 2005;60(7):636–653.
- Beaupre LA, Jones CA, Saunders LD, Johnston DW, Buckingham J, Majumdar SR: Best Practices für ältere Patienten mit Hüftfrakturen. Ein systematischer Überblick über die Evidenz. J Gen Intern Med 2005;20(11): 1019–1025.
- Rodgers A, Walker N, Schug S, et al: Reduktion der postoperativen Mortalität und Morbidität mit Epidural- oder Spinalanästhesie: Ergebnisse einer Übersicht randomisierter Studien. BMJ 2000;321(7275):1493.
- Parker MJ, Handoll HH, Griffiths R: Anästhesie für Hüftbruchoperationen bei Erwachsenen. Cochrane Database Syst Rev. 2004(4):CD000521.
- Lee TW, Grocott HP, Schwinn D, Jacobsohn E: Hohe Spinalanästhesie für die Herzchirurgie: Auswirkungen auf die Funktion des beta-adrenergen Rezeptors, die Stressreaktion und die Hämodynamik. Anesthesiology 2003;98(2):499–510.
- Hall R, Adderley N, MacLaren C, et al.: Verändert intrathekales Morphin die Stressreaktion nach einer koronaren Bypassoperation? Can J Anaesth 2000;47(5):463–466.
- Parlow JL, Steele RG, O'Reilly D: Niedrig dosiertes intrathekales Morphin erleichtert die frühe Extubation nach einer Herzoperation: Ergebnisse eines retrospektiven Audits zur kontinuierlichen Qualitätsverbesserung. Can J Anaesth 2005;52(1):94–99.
- Liu SS, Nerve Block BM, Wu CL: Auswirkungen der perioperativen zentralen neuraxialen Analgesie auf das Ergebnis nach einer Koronararterien-Bypass-Operation: Eine Meta-Analyse. Anesthesiology 2004;101(1):153–161.
- Agarwal D, Mohta M, Tyagi A, Sethi AK: Subduralnervenblockade und der Anästhesist. Anaesth Intensive Care 2010;38(1):20–26.
- Reina MA, De Leon Casasola O, Lopez A, De Andres JA, Mora M, Fernandez A: Der Ursprung des spinalen Subduralraums: Ultrastrukturbefunde. Anesth Analg 2002;94(4):991–995; Inhaltsverzeichnis.
- Broadbent CR, Maxwell WB, Ferrie R, Wilson DJ, Gawne-Cain M, Russell R: Fähigkeit von Anästhesisten, einen markierten lumbalen Zwischenraum zu identifizieren. Anästhesie 2000;55(11):1122–1126.
- Saifuddin A, Burnett SJ, White J: Die Variation der Position des Conus medullaris in einer erwachsenen Bevölkerung. Eine Magnetresonanztomographie-Studie. Wirbelsäule (Phila Pa 1976) 1998;23(13):1452–1456.
- Reiman A, Anson B: Wirbelendes Ende des Rückenmarks mit Bericht über einen Fall von Sakralmark. Anat Rec 1944;88:127.
- Bromage PR: Neurologische Komplikationen der Subarachnoidal- und Epiduralanästhesie. Acta Anaesthesiol Scand 1997;41(4):439–444.
- Reynolds F: Schädigung des Conus medullaris nach Spinalanästhesie. Anästhesie 2001;56(3):238–247.
- Covino BG: Pharmakologie der Lokalanästhetika. Br. J. Anaesth 1986;58(7):701–716.
- Greene NM: Aufnahme und Ausscheidung von Lokalanästhetika während der Spinalanästhesie. Anesth Analg 1983;62(11):1013–1024.
- Stienstra R, Greene NM: Faktoren, die die subarachnoidale Ausbreitung von Lokalanästhesielösungen beeinflussen. Reg Anesth 1991;16(1):1–6.
- Cohen DE: Verteilung von Lokalanästhetika in der Neuraxis des Hundes. Anesthesiology 1968;29(5):1002–1005.
- Schell RM, Brauer FS, Cole DJ, Applegate RL 2nd: Anhaltende sakrale Nervenwurzelausfälle nach kontinuierlicher Spinalanästhesie. Can J Anaesth 1991;38(7):908–911.
- Hogan Q: Größe der menschlichen unteren thorakalen und lumbosakralen Nervenwurzeln. Anesthesiology 1996;85(1):37–42.
- Kaneko S, Matsumoto M, Tsuruta S, Hirata T, Gondo T, Sakabe T: Die Nervenwurzel-Eintrittszone ist sehr anfällig für intrathekales Tetracain bei Kaninchen. Anesth Analg 2005;101(1):107–114; Inhaltsverzeichnis.
- Takenami T, Yagishita S, Asato F, Hoka S: Die Neurotoxizität von intrathekal verabreichtem Tetracain beginnt an den hinteren Wurzeln nahe dem Eintritt in das Rückenmark. Reg Anesth Pain Med 2000;25(4):372–379.
- Kristensen JD, Karlsten R, Gordh T: Rückenmarksblutfluss nach intrathekaler Injektion von Ropivacain und Bupivacain mit oder ohne Epinephrin bei Ratten. Acta Anaesthesiol Scand 1998;42(6):685–690.
- Dohi S, Matsumiya N, Takeshima R, Naito H: Die Auswirkungen von subarachnoidalem Lidocain und Phenylephrin auf das Rückenmark und den zerebralen Blutfluss bei Hunden. Anesthesiology 1984;61(3):238–244.
- Kozody R, Palahniuk RJ, Cumming MO: Rückenmarksblutfluss nach subarachnoidalem Tetracain. Can Anaesth Soc J 1985;32(1):23–29.
- Greene NM: Verteilung von Lokalanästhesielösungen im Subarachnoidalraum. Anesth Analg 1985;64(7):715–730.
- Horlocker TT, Wedel DJ: Dichte, spezifisches Gewicht und Barizität von Spinalanästhesielösungen bei Körpertemperatur. Anesth Analg 1993;76(5): 1015–1018.
- Hallworth SP, Fernando R, Columb MO, Stocks GM: Die Wirkung von Körperhaltung und Barizität auf die Ausbreitung von intrathekalem Bupivacain bei elektiven Kaiserschnitten. Anesth Analg 2005;100(4):1159–1165.
- McLeod GA: Dichte von Spinalanästhesielösungen von Bupivacain, Levobupivacain und Ropivacain mit und ohne Dextrose. Br. J. Anaesth 2004;92(4):547–551.
- Brown DT, Wildsmith JA, Covino BG, Scott DB: Wirkung von Barizität auf die Spinalanästhesie mit Amethocain. Br. J. Anaesth 1980;52(6):589–596.
- Siker ES, Wolfson B, Stewart WD, Pavilack P, Pappas MT: Mepivacain für die Spinalanästhesie: Auswirkungen von Konzentrationsänderungen und Barizität. Anesth Analg 1966;45(2):191–196.
- Chambers WA, Edstrom HH, Scott DB: Wirkung der Barizität auf die Spinalanästhesie mit Bupivacain. Br. J. Anaesth 1981;53(3):279–282.
- Denson DD, Bridenbaugh PO, Turner PA, Phero JC: Vergleich von neuraler Blockade und Pharmakokinetik nach subarachnoidalem Lidocain beim Rhesusaffen. II: Auswirkungen von Volumen, Osmolalität und Barizität. Anesth Analg 1983;62(11):995–1001.
- Hare GM, Ngan JC: Dichtebestimmung von lokalanästhetischen Opioidmischungen für die Spinalanästhesie. Can J Anaesth 1998;45(4):341–346.
- Bodily MN, Carpenter RL, Owens BD: Lidocain 0.5 % Spinalanästhesie: eine hypobare Lösung für kurzfristige perirektale Operationen. Can J Anaesth 1992;39(8):770–773.
- Lui AC, Polis TZ, Cicutti NJ: Dichten von Liquor und Spinalanästhesielösungen bei chirurgischen Patienten bei Körpertemperatur. Can J Anaesth 1998;45(4):297–303.
- Hogan QH, Prost R, Kulier A, Taylor ML, Liu S, Mark L: Magnetresonanztomographie des Liquorvolumens und der Einfluss von Körperhabitus und Bauchdruck. Anesthesiology 1996;84(6): 1341–1349.
- Carpenter RL, Hogan QH, Liu SS, Crane B, Moore J: Das Volumen der lumbosakralen Zerebrospinalflüssigkeit ist die primäre Determinante für das Ausmaß und die Dauer der sensorischen Nervenblockade während der Spinalanästhesie. Anesthesiology 1998;89(1): 24–29.
- Higuchi H, Hirata J, Adachi Y, Kazama T: Einfluss der Dichte, Geschwindigkeit und des Volumens der lumbosakralen Liquor cerebrospinalis auf Ausmaß und Dauer einer einfachen Bupivacain-Spinalanästhesie. Anesthesiology 2004;100(1): 106–114.
- Schneider M, Ettlin T, Kaufmann M, et al: Transiente neurologische Toxizität nach hyperbarer Subarachnoidalanästhesie mit 5% Lidocain. Anesth Analg 1993;76(5):1154–1157.
- Zaric D, Christiansen C, Pace NL, Punjasawadwong Y: Vorübergehende neurologische Symptome nach Spinalanästhesie mit Lidocain im Vergleich zu anderen Lokalanästhetika: Eine systematische Überprüfung randomisierter, kontrollierter Studien. Anesth Analg 2005;100(6):1811–1816.
- Wang BC, Hillman DE, Spielholz NI, Turndorf H: Chronische neurologische Defizite und Nesacain-CE – eine Wirkung des Anästhetikums 2-Chloroprocain oder des Antioxidans Natriumbisulfit? Anesth Analg 1984;63(4):445–447.
- Smith KN, Kopacz DJ, McDonald SB: Spinales 2-Chloroprocain: eine Dosisfindungsstudie und die Wirkung von zugesetztem Epinephrin. Anesth Analg 2004;98(1):81–88; Inhaltsverzeichnis.
- Hejtmanek MR, Pollock JE: Chloroprocain für die Spinalanästhesie: Eine retrospektive Analyse. Acta Anaesthesiol Scand 2011;55(3):267–272.
- Pollock JE: Intrathekales Chloroprocain – nach US-amerikanischen FDA-Parametern noch nicht „sicher“. Int Anesthesiol Clin 2012;50(1):93–100.
- HH Le Truong, M. Girard, P. Drolet, Y. Grenier, C. Boucher, L. Bergeron: Spinalanästhesie: Ein Vergleich von Procain und Lidocain. Can J Anaesth 2001;48(5):470–473.
- Johnson ME: Neurotoxizität von spinalem Procain – eine Warnung. Reg Anesth Pain Med 2001;26(3):288.
- Hampl KF, Schneider MC, Ummenhofer W, Drewe J: Transiente neurologische Symptome nach Spinalanästhesie. Anesth Analg 1995; 81(6):1148–1153.
- Hampl KF, Heinzmann-Wiedmer S, Luginbuehl I, et al: Transiente neurologische Symptome nach Spinalanästhesie: eine geringere Inzidenz mit Prilocain und Bupivacain als mit Lidocain. Anästhesiologie 1998; 88(3):629–633.
- Keld DB, Hein L, Dalgaard M, Krogh L, Rodt SA: Die Inzidenz transienter neurologischer Symptome (TNS) nach Spinalanästhesie bei Patienten, die sich einer Operation in Rückenlage unterziehen. Hyperbares Lidocain 5 % versus hyperbares Bupivacain 0.5 %. Acta Anaesthesiol Scand 2000; 44(3):285–290.
- Freedman JM, Li DK, Drasner K, Jaskela MC, Larsen B, Wi S: Transiente neurologische Symptome nach Spinalanästhesie: Eine epidemiologische Studie an 1863 Patienten. Anesthesiology 1998;89(3):633–641.
- Sumi M, Sakura S, Kosaka Y: Intrathekales hyperbares 0.5 % Tetracain als mögliche Ursache vorübergehender neurologischer Toxizität. Anesth Analg 1996; 82(5):1076–1077.
- Sakura S, Sumi M, Sakaguchi Y, Saito Y, Kosaka Y, Drasner K: Die Zugabe von Phenylephrin trägt zur Entwicklung von Transienten bei
Neurologische Symptome nach Spinalanästhesie mit 0.5 % Tetracain. Anesthesiology 1997;87(4):771–778. - Liguori GA, Zayas VM, Chisholm MF: Vorübergehende neurologische Symptome nach Spinalanästhesie mit Mepivacain und Lidocain. Anästhesiologie
1998;88(3):619–623. - Salazar F, Bogdanovich A, Adalia R, Chabas E, Gomar C: Vorübergehende neurologische Symptome nach Spinalanästhesie mit isobaren 2%
Mepivacain und isobares 2%iges Lidocain. Acta Anaesthesiol Scand 2001; 45(2):240–245. - Eberhart LH, Morin AM, Kranke P, Geldner G, Wulf H: Transiente neurologische Symptome nach Spinalanästhesie. Eine quantitative Systematik
Überblick (Meta-Analyse) randomisierter kontrollierter Studien]. Anaesthesist 2002;51(7):539–546. - Ganapathy S, Sandhu HB, Stockall CA, Hurley D: Transientes neurologisches Symptom (TNS) nach intrathekalem Ropivacain. Anesthesiology 2000;93(6):1537–1539.
- Lee YY, Ngan Kee WD, Chang HK, So CL, Gin T: Spinales Ropivacain für die Operation der unteren Extremitäten: Eine Dosis-Wirkungs-Studie. Anesth Analg 2007;105(2):520–523.
- Khaw KS, Ngan Kee WD, Wong EL, Liu JY, Chung R: Spinales Ropivacain für den Kaiserschnitt: eine Dosisfindungsstudie. Anesthesiology 2001;95(6):1346–1350.
- Frawley G, Skinner A, Thomas J, Smith S: Ropivacain-Spinalanästhesie bei Neugeborenen: Eine Studie zur Ermittlung des Dosisbereichs. Kinderarzt Anaesth
2007;17(2):126–132. - McDonald SB, Liu SS, Kopacz DJ, Stephenson CA: Hyperbares spinales Ropivacain: Ein Vergleich mit Bupivacain bei Freiwilligen. Anästhesiologie
1999;90(4):971–977. - Wahedi W, Nolte H, Klein P: [Ropivacain für die Spinalanästhesie. Eine Dosisfindungsstudie]. Anaesthesist 1996;45(8):737–744.
- van Kleef JW, Veering BT, Burm AG: Spinalanästhesie mit Ropivacain: Eine Doppelblindstudie zur Wirksamkeit und Sicherheit von 0.5 % und 0.75 %
Lösungen bei Patienten, die sich einer kleineren Operation an den unteren Extremitäten unterziehen. Anesth Analg 1994;78(6):1125–1130. - Hughes D, Hill D, Fee JP: Intrathekales Ropivacain oder Bupivacain mit Fentanyl für die Wehen. Br. J. Anaesth 2001;87(5):733–737.
- Breebaart MB, Vercauteren MP, Hoffmann VL, Adriaensen HA: Harnblasenscanning nach Arthroskopie am Tag unter Spinalanästhesie: Vergleich zwischen Lidocain, Ropivacain und Levobupivacain. Br. J. Anaesth 2003;90(3):309–313.
- Braun DL: Spinal-, Epidural- und Kaudalanästhesie. In Miller RD (Hrsg.). Anästhesie, 4. Aufl. Churchill Livingston, 1994, S. 1505–1533.
- Pawlowski J., Sukhani R., Pappas AL, et al.: Das Anästhetikum- und Erholungsprofil von zwei Dosen (60 und 80 mg) von reinem Mepivacain für die ambulante Behandlung
Spinalanästhesie. Anesth Analg 2000;91(3):580–584. - Kallio H, Snall EV, Kero MP, Rosenberg PH: Ein Vergleich von intrathekalen einfachen Lösungen mit 20 oder 15 mg Ropivacain im Vergleich zu 10 mg Bupivacain. Anesth Analg 2004;99(3):713–717; Inhaltsverzeichnis.
- McNamee DA, Parks L, McClelland AM, et al: Intrathekales Ropivacain für totale Hüftarthroplastik: Doppelblinde Vergleichsstudie mit isobaren
7.5 mg ml(-1) und 10 mg ml(-1) Lösungen. Br. J. Anaesth 2001;87(5):743–747. - Burke D, Kennedy S, Bannister J: Spinalanästhesie mit 0.5 % S(-)-Bupivacain für elektive Operationen an den unteren Extremitäten. Reg Anesth Pain Med 1999;24(6):519–523.
- Glaser C, Marhofer P, Zimpfer G, et al: Levobupivacain versus racemisches Bupivacain für die Spinalanästhesie. Anesth Analg 2002;94(1):194–198;
Inhaltsverzeichnis. - Alley EA, Kopacz DJ, McDonald SB, Liu SS: Hyperbares spinales Levobupivacain: Ein Vergleich mit racemischem Bupivacain bei Freiwilligen. Anesth Analg 2002;94(1):188–193; Inhaltsverzeichnis.
- Bridenbaugh PO, Greene NM, Brull SJ: Spinale (Subarachoid-) Neuralblockade. In Cousins MJ, Bridenbaugh PO (Hrsg.). Neuronale Blockade, 3. Aufl. Lippincott-Raven, 1998.
- Tetzlaff JE, Dilger J, Yap E, Smith MP, Schoenwald PK: Cauda equina-Syndrom nach Spinalanästhesie bei einem Patienten mit schwerer Gefäßerkrankung. Can J Anaesth 1998;45(7):667–669.
- Lee DS, Bui T, Ferrarese J, Richardson PK: Cauda equina-Syndrom nach zufälliger totaler Spinalanästhesie mit 2% Lidocain. J Clin Anesth 1998;10(1):66–69.
- Maehara Y, Kusunoki S, Kawamoto M, et al: Eine prospektive multizentrische Studie zur Bestimmung der Inzidenz vorübergehender neurologischer Symptome nach Spinalanästhesie mit Phenylephrin, das zu 0.5 % Tetracain hinzugefügt wurde. Hiroshima J Med Sci 2001;50(2):47–51.
- Kozody R, Palahniuk RJ, Wade JG, Cumming MO, Pucci WR: Die Wirkung von subarachnoidalem Epinephrin und Phenylephrin auf den Blutfluss im Rückenmark. Can Anaesth Soc J 1984;31(5):503–508.
- Porter SS, Albin MS, Watson WA, Bunegin L, Pantoja G: Reaktionen des Rückenmarks und des zerebralen Blutflusses auf die subarachnoidale Injektion von Lokalanästhetika mit und ohne Epinephrin. Acta Anaesthesiol Scand 1985;29(3):330–338.
- Concepcion M, Maddi R, Francis D, Rocco AG, Murray E, Covino BG: Vasokonstriktoren in der Spinalanästhesie mit Tetracain – Ein Vergleich von
Epinephrin und Phenylephrin. Anesth Analg 1984;63(2):134–138. - Armstrong IR, Littlewood DG, Chambers WA: Spinalanästhesie mit Tetracain – Wirkung zugesetzter Vasokonstriktoren. Anesth Analg 1983;62(9):
793-795. - Rice LJ, DeMars PD, Whalen TV, Crooms JC, Parkinson SK: Dauer der Spinalanästhesie bei Säuglingen unter einem Jahr. Vergleich von drei hyperbaren Techniken. Reg Anesth 1994;19(5):325–329.
- Chambers WA, Littlewood DG, Scott DB: Spinalanästhesie mit hyperbarem Bupivacain: Wirkung von zugesetzten Vasokonstriktoren. Anesth Analg
1982;61(1):49–52. - Moore JM, Liu SS, Pollock JE, Neal JM, Knab JH: Die Wirkung von Epinephrin auf die Spinalanästhesie mit hyperbarem Bupivacain in kleiner Dosis: klinisch
Implikationen für die ambulante Chirurgie. Anesth Analg 1998;86(5):973–977. - Racle JP, Poy JY, Benkhadra A, Jourdren L, Fockenier F: [Verlängerung der Spinalanästhesie mit hyperbarem Bupivacain durch Adrenalin und
Clonidin bei älteren Menschen]. Ann Fr. Anesth Reanim 1988;7(2):139–144. - Vercauteren MP, Jacobs S, Jacquemyn Y, Adriaensen HA: Intrathekale Wehenanalgesie mit Bupivacain und Sufentanil: Die Wirkung der Zugabe von 2.25 Mikrogramm Epinephrin. Reg Anesth Pain Med 2001;26(5):473–477.
- Goodman SR, Kim-Lo SH, Ciliberto CF, Ridley DM, Smiley RM: Epinephrin ist keine sinnvolle Ergänzung zu intrathekalem Fentanyl oder Fentanylbupivacain zur Analgesie der Wehen. Reg Anesth Pain Med 2002;27(4):374–379.
- Gautier PE, Debry F, Fanard L, Van Steenberge A, Hody JL: Ambulante kombinierte Spinal-Epidural-Analgesie für die Wehen. Einfluss von Epinephrin auf die Bupivacain-Sufentanil-Kombination. Reg Anesth 1997;22(2):143–149.
- Chambers WA, Littlewood DG, Logan MR, Scott DB: Wirkung von zugesetztem Epinephrin auf die Spinalanästhesie mit Lidocain. Anesth Analg 1981;60(6):417–420.
- Chiu AA, Liu S, Carpenter RL, Kasman GS, Pollock JE, Neal JM: Die Wirkung von Epinephrin auf die Lidocain-Spinalanästhesie: Eine Cross-Over-Studie.
Anesth Analg 1995;80(4):735–739. - Racle JP, Benkhadra A, Poy JY: Subarachnoidalanästhesie durch hyperbares Lignocain bei älteren Patienten. Wirkungsverlängerung mit
Adrenalin. Br. J. Anaesth 1988;60(7):831–835. - Spivey DL: Epinephrin verlängert die Spinalanästhesie mit Lidocain bei termingerechten Gebärenden nicht. Anesth Analg 1985;64(5):468–470.
- Moore DC, Chadwick HS, Ready LB: Epinephrin verlängert Lidocain Wirbelsäule: Schmerzen an der Operationsstelle die genaueste Methode zur Bestimmung
Dauer der Lokalanästhesie. Anesthesiology 1987;67(3):416–418. - Glynn CJ, Mather LE, Cousins MJ, Wilson PR, Graham JR: Spinale Narkotika und Atemdepression. Lancet 1979;2(8138):356–357.
- Cunningham AJ, McKenna JA, Skene DS: Spinalanästhesie mit Einzelinjektion mit Amethocain und Morphin für die transurethrale Prostatektomie. Br. J. Anaesth 1983;55(5):423–427.
- Nordberg G, Hedner T, Mellstrand T, Dahlstrom B: Pharmakokinetische Aspekte der intrathekalen Morphin-Analgesie. Anesthesiology 1984;60(5): 448–454.
- Abouleish E, Rawal N, Rashad MN: Die Zugabe von 0.2 mg Subarachnoidalmorphin zu hyperbarem Bupivacain für die Kaiserschnittentbindung: Eine prospektive Studie mit 856 Fällen. Reg Anesth 1991;16(3):137–140.
- Borgeat A, Singer T: Übelkeit und Erbrechen nach Spinalanästhesie mit Morphin. Acta Anaesthesiol Scand 1998;42(10):1231.
- Bonnet F, Buisson VB, Francois Y, Catoire P, Saada M: Auswirkungen von oralem und subarachnoidalem Clonidin auf die Spinalanästhesie mit Bupivacain. Reg.-Nr
Anesth 1990;15(4):211–214. - Dobrydnjov I, Axelsson K, Thorn SE, et al: Clonidin in Kombination mit Bupivacain in geringer Dosis während der Spinalanästhesie bei Leistenbruch: Eine randomisierte Doppelblindstudie. Anesth Analg 2003;96(5):1496–1503; Inhaltsverzeichnis.
- Strebel S, Gurzeler JA, Schneider MC, Aeschbach A, Kindler CH: Smalldose intrathecal Clonidin and isobaric Bupivacaine for orthopedic
Chirurgie: eine Dosis-Wirkungs-Studie. Anesth Analg 2004;99(4):1231–1238;Inhaltsverzeichnis. - Filos KS, Goudas LC, Patroni O, Polyzou V: Hämodynamisches und analgetisches Profil nach intrathekalem Clonidin beim Menschen. Eine Dosis-Wirkungs-Beziehung
lernen. Anesthesiology 1994;81(3):591–601; Diskussion 27A–28A. - Hassenbusch SJ, Gunes S, Wachsman S, Willis KD: Intrathekales Clonidin bei der Behandlung hartnäckiger Schmerzen: Eine Phase-I/II-Studie. Pain Med 2002;3(2):85–91.
- Ackerman LL, Follett KA, Rosenquist RW: Langzeitergebnisse während der Behandlung chronischer Schmerzen mit intrathekalem Clonidin oder Clonidin/Opioid-Kombinationen. J Pain Symptom Manage 2003;26(1):668–677.
- Chen SR, Khan GM, Pan HL: Die antiallodynische Wirkung von intrathekalem Neostigmin wird durch spinales Stickoxid in einem Rattenmodell für diabetischen neuropathischen Schmerz vermittelt. Anesthesiology 2001;95(4):1007–1012.
- Ho KM, Ismail H, Lee KC, Branch R: Verwendung von intrathekalem Neostigmin als Zusatz zu anderen Wirbelsäulenmedikamenten bei perioperativer und peripartaler Analgesie: Eine Metaanalyse. Anaesth Intensive Care 2005;33(1):41–53.
- Yegin A, Yilmaz M, Karsli B, Erman M: Analgetische Wirkungen von intrathekalem Neostigmin in der perianalen Chirurgie. Eur J Anaesthesiol 2003;20(5): 404–408.
- Tan PH, Kuo JH, Liu K, Hung CC, Tsai TC, Deng TY: Wirksamkeit von intrathekalem Neostigmin zur Linderung von postinguinalen Hämorrhaphieschmerzen. Acta Anaesthesiol Scand 2000;44(9):1056–1060.
- Klohr S, Roth R, Hofmann T, Rossaint R, Heesen M: Definitionen der Hypotonie nach Spinalanästhesie bei Kaiserschnitt: Literaturrecherche und Anwendung bei Gebärenden. Acta Anaesthesiol Scand 2010; 54(8):909–921.
- Mark JB, Steele SM: Kardiovaskuläre Wirkungen der Spinalanästhesie. Int Anesthesiol Clin 1989;27(1):31–39.
- Cooper DW: Vasopressor-Management bei Kaiserschnittgeburt. Curr Opin Anaesthesiol 2012;25(3):300–308.
- Khaw KS, Ngan Kee WD, Lee SW: Hypotonie während der Spinalanästhesie für den Kaiserschnitt: Auswirkungen, Erkennung, Prävention und Behandlung. Fetal Matern Med Rev 2006;17(2):157–183.
- Shimosato S, Etsten BE: Die Rolle des venösen Systems in der Herz-Kreislauf-Dynamik während der Spinal- und Epiduralanästhesie beim Menschen. Anesthesiology 1969;30(6):619–628.
- Cooper J: Herzstillstand während der Spinalanästhesie. Anesth Analg 2001; 93(1):245.
- Salinas FV, Sueda LA, Liu SS: Physiologie der Spinalanästhesie und praktische Vorschläge für eine erfolgreiche Spinalanästhesie. Best Pract Res Clin Anaesthesiol 2003;17(3):289–303.
- Meyhoff CS, Hesselbjerg L, Koscielniak-Nielsen Z, Rasmussen LS: Biphasische Veränderungen des Herzzeitvolumens während des Beginns der Spinalanästhesie bei älteren Patienten. Eur J Anaesthesiol 2007;24(9):770–775.
- Roy L, Ramanathan S: ST-Streckensenkung und myokardiale Kontraktilität während eines Kaiserschnitts unter Spinalanästhesie. Can J Anaesth 1999;46(1):52–55.
- Ou CH, Tsou MY, Ting CK, Chiou CS, Chan KH, Tsai SK: Auftreten des Bezold-Jarisch-Reflexes beim Kaiserschnitt unter Spinalanästhesie – Ein Fallbericht. Acta Anaesthesiol Taiwan 2004;42(3):175–178.
- Mackey DC, Carpenter RL, Thompson GE, Brown DL, Bodily MN: Bradykardie und Asystolie während der Spinalanästhesie: Ein Bericht über drei Fälle ohne Morbidität. Anesthesiology 1989;70(5):866–868.
- Campagna JA, Carter C: Klinische Relevanz des Bezold-Jarisch-Reflexes. Anesthesiology 2003;98(5):1250–1260.
- Lesser JB, Sanborn KV, Valskys R, Kuroda M: Schwere Bradykardie während Spinal- und Epiduralanästhesie, aufgezeichnet von einem Anästhesie-Informationsmanagementsystem. Anesthesiology 2003;99(4):859–866.
- Kinsella SM, Tuckey JP: Perioperative Bradykardie und Asystolie: Beziehung zur vasovagalen Synkope und zum Bezold-Jarisch-Reflex. Br. J. Anaesth 2001;86(6):859–868.
- Bernards CM, Hymas NJ: Fortschreiten einer Herznervenblockade ersten Grades zu einer hochgradigen Nervenblockade zweiten Grades während der Spinalanästhesie. Can J Anaesth 1992;39(2):173–175.
- Tarkkila P, Isola J: Ein Regressionsmodell zur Identifizierung von Patienten mit hohem Risiko für Hypotonie, Bradykardie und Übelkeit während der Spinalanästhesie. Acta Anaesthesiol Scand 1992;36(6):554–558.
- Klasen J, Junger A, Hartmann B, et al: Unterschiedliche Inzidenzen einer relevanten Hypotonie bei kombinierter Spinal-Epiduralanästhesie und Spinalanästhesie. Anesth Analg 2003;96(5):1491–1495; Inhaltsverzeichnis.
- Hartmann B, Junger A, Klasen J, et al: Die Inzidenz und Risikofaktoren für Hypotonie nach Spinalanästhesie-Induktion: eine Analyse mit automatisierter Datenerhebung. Anesth Analg 2002;94(6):1521–1529; Inhaltsverzeichnis.
- Ngan Kee WD, Khaw KS, Lau TK, Ng FF, Chui K, Ng KL: Randomisierter doppelblinder Vergleich von Phenylephrin versus Ephedrin zur Aufrechterhaltung des Blutdrucks während der Spinalanästhesie für nicht-elektiven Kaiserschnitt. Anästhesie 2008;63(12):1319–1326.
- James FM 3rd, Greiss FC Jr, Kemp RA: Eine Bewertung der Vasopressortherapie bei mütterlicher Hypotonie während der Spinalanästhesie. Anesthesiology 1970;33(1):25–34.
- Wildsmith JA: Management von Hypotonie während der Spinalanästhesie. Reg Anesth Pain Med 2000;25(3):322.
- Sinclair CJ, Scott DB, Edstrom HH: Wirkung der Trendelenberg-Position auf die Spinalanästhesie mit hyperbarem Bupivacain. Br. J. Anaesth 1982;54(5):497–500.
- Cyna AM, Andrew M, Emmett RS, Middleton P, Simmons SW: Techniken zur Verhinderung von Hypotonie während der Spinalanästhesie für den Kaiserschnitt. Cochrane Database Syst Rev. 2006(4):CD002251.
- Husaini SW, Russell IF: Volumenvorlast: Mangelnde Wirkung bei der Prävention von spinal-induzierter Hypotonie bei Kaiserschnitt. Int J Obstet Anesth 1998;7(2):76–81.
- Jackson R, Reid JA, Thorburn J: Die Volumenvorbelastung ist nicht unbedingt erforderlich, um eine spinal induzierte Hypotonie beim Kaiserschnitt zu verhindern. Br. J. Anaesth 1995;75(3):262–265.
- Dahlgren, G., Granath, F., Pregner, K., Rosblad, PG, Wessel, H., Irestedt, L.: Kolloid vs. kristalloide Vorbelastung zur Verhinderung einer mütterlichen Hypotonie während der Spinalanästhesie für einen elektiven Kaiserschnitt. Acta Anaesthesiol Scand 2005;49(8):1200–1206.
- Dyer RA, Farina Z, Joubert IA, et al: Kristalloid-Vorbelastung versus schnelle Kristalloid-Verabreichung nach Einleitung einer Spinalanästhesie (Kobelastung) für einen elektiven Kaiserschnitt. Anaesth Intensive Care 2004;32(3): 351–357.
- Roofthooft E, Van de Velde M: Niedrigdosierte Spinalanästhesie für den Kaiserschnitt zur Vorbeugung einer spinalinduzierten Hypotonie. Curr Opin Anaesthesiol 2008;21(3):259–262.
- Arzola C, Wieczorek PM: Wirksamkeit von niedrig dosiertem Bupivacain in der Spinalanästhesie bei Kaiserschnitt: Systematische Überprüfung und Metaanalyse. Br. J. Anaesth 2011;107(3):308–318.
- Ngan Kee WD, Lee A: Multivariate Analyse von Faktoren, die mit dem pH-Wert der Nabelarterien und dem Standard-Basenüberschuss nach einem Kaiserschnitt unter Spinalanästhesie zusammenhängen. Anästhesie 2003;58(2):125–130.
- Labartino L, Mojdehi E, Mauro AL: Management von Hypotonie nach Spinalanästhesie für Kaiserschnitt. Anesth Analg 1966;45(2):179–182.
- Ngan Kee WD, Khaw KS, Ng FF: Vergleich von Phenylephrin-Infusionsschemata zur Aufrechterhaltung des mütterlichen Blutdrucks während der Spinalanästhesie für den Kaiserschnitt. Br. J. Anaesth 2004;92(4): 469–474.
- Ngan Kee WD, Khaw KS, Ng FF: Prävention von Hypotonie während der Spinalanästhesie bei Kaiserschnitt: Eine effektive Technik mit einer Kombination aus Phenylephrin-Infusion und Kristalloid-Kohydratation. Anesthesiology 2005;103(4):744–750.
- Habib AS: Eine Überprüfung der Auswirkungen der Phenylephrin-Verabreichung auf die mütterliche Hämodynamik und die mütterlichen und neonatalen Ergebnisse bei Frauen, die sich einem Kaiserschnitt unter Spinalanästhesie unterziehen. Anesth Analg 2012;114(2):377–390.
- Park YH, Ryu T, Hong SW, Kwak KH, Kim SO: Die Wirkung des intravenösen Phenylephrins auf das Niveau der Spinalanästhesie. Korean J Anesthesiol 2011;61(5):372–376.
- Caplan RA, Ward RJ, Posner K, Cheney FW: Unerwarteter Herzstillstand während der Spinalanästhesie: Eine geschlossene Schadensanalyse prädisponierender Faktoren. Anesthesiology 1988;68(1):5–11.
- Lovstad RZ, Granhus G, Hetland S: Bradykardie und asystolischer Herzstillstand während der Spinalanästhesie: Ein Bericht über fünf Fälle. Acta Anaesthesiol Scand 2000;44(1):48–52.
- Pan PH, Moore CH, Ross VH: Schwere mütterliche Bradykardie und Asystolie nach kombinierter spinal-epiduraler Wehenanalgesie bei einer krankhaft fettleibigen Gebärenden. J Clin Anesth 2004;16(6):461–464.
- Pollard JB: Herzstillstand während der Spinalanästhesie: gemeinsame Mechanismen und Strategien zur Prävention. Anesth Analg 2001;92(1):252–256.
- Cooper DW: Wirkung von Vasopressoren auf den systolischen, mittleren und diastolischen Arteriendruck während der Spinalanästhesie in der Schwangerschaft. Int J Obstet Anesth 2008;17(1):90–92.
- Sahoo T, SenDasgupta C, Goswami A, Hazra A: Reduktion der spinal-induzierten Hypotonie mit Ondansetron bei Gebärenden, die sich einem Kaiserschnitt unterziehen: Eine doppelblinde, randomisierte, Placebo-kontrollierte Studie. Int J Obstet Anesth 2012;21(1):24–28.
- Smiley RM: Beweislast. Anesthesiology 2009;111(3):470–472.
- Greene NM, Brull SJ: Physiologie der Spinalanästhesie, 4. Aufl. Williams & Wilkins, 1981.
- Steinbrook RA, Concepcion M, Topulos GP: Beatmungsreaktionen auf Hyperkapnie während einer Spinalanästhesie mit Bupivacain. Anesth Analg 1988;67(3):247–252.
- Nakayama M, Kanaya N, Fujita S, Namiki A: Auswirkungen von Ephedrin auf die Indocyaningrün-Clearance während der Spinalanästhesie: Bewertung nach der Fingerstückmethode. Anesth Analg 1993;77(5):947–949.
- Zinn SE, Fairley HB, Glenn JD: Leberfunktion bei Patienten mit leichter alkoholischer Hepatitis, nach Enfluran, Lachgas-Narkotikum und Rückenmark
Anästhesie. Anesth Analg 1985;64(5):487–490. - Igarashi M, Kawana S, Iwasaki H, Namiki A: [Anästhesiemanagement für einen Patienten mit Citrullinämie und Leberzirrhose]. Masui 1995;
44 (1): 96-99. - Fukuda T, Okutani R, Kono K, Yoshimura Y, Ochiai N: [Anästhesiemanagement für einen Kaiserschnitt eines Patienten mit vorübergehendem Diabetes
insipidus und akute schwere Leberfunktionsstörung]. Masui 1993;42(10):1511–1516. - McNeill MJ, Bennet A: Einsatz von Regionalanästhesie bei einem Patienten mit akuter Porphyrie. Br. J. Anaesth 1990;64(3):371–373.
- Consolo D, Ouardirhi Y, Wessels C, Girard C: [Geburtshilfeanästhesie und Porphyrien]. Ann Fr. Anesth Reanim 2005;24(4):428–431.
- Runciman WB, Mather LE, Ilsley AH, Carapetis RJ, Upton RN: Ein Schafpräparat zur Untersuchung der Wechselwirkungen zwischen Blutfluss und Arzneimittel
Anordnung. III: Auswirkungen von Allgemein- und Spinalanästhesie auf regionalen Blutfluss und Sauerstoffspannungen. Br. J. Anaesth 1984;56(11):1247–1258. - Runciman WB, Mather LE, Ilsley AH, Carapetis RJ, Upton RN: Ein Schafpräparat zur Untersuchung der Wechselwirkungen zwischen Blutfluss und Arzneimittel
Anordnung. IV: Die Wirkungen von Allgemein- und Spinalanästhesie auf den Blutfluss und die Cefoxitin-Disposition. Br. J. Anaesth 1985;57(12):1239–1247. - Runciman WB, Mather LE, Ilsley AH, Carapetis RJ, Upton RN: Ein Schafpräparat zur Untersuchung der Wechselwirkungen zwischen Blutfluss und Arzneimittel
Anordnung. VI: Auswirkungen einer Allgemein- oder Subarachnoidalanästhesie auf den Blutfluss und die Chlormethiazol-Disposition. Br. J. Anaesth 1986;58(11):1308–1316. - Mather LE, Runciman WB, Ilsley AH, Carapetis RJ, Upton RN: Ein Schafpräparat zur Untersuchung der Wechselwirkungen zwischen Blutfluss und Medikamentendisposition. V: Die Wirkungen der Allgemein- und Subarachnoidalanästhesie auf den Blutfluss und die Pethidin-Disposition. Br. J. Anaesth 1986;58(8): 888–896.
- Taivainen T, Tuominen M, Rosenberg PH: Einfluss von Adipositas auf die Ausbreitung von Spinalanalgesie nach Injektion von reinem 0.5% Bupivacain bei der
Zwischenraum L3–4 oder L4–5. Br. J. Anaesth 1990;64(5):542–546. - Tuominen M, Taivainen T, Rosenberg PH: Ausbreitung der Spinalanästhesie mit reinem 0.5% Bupivacain: Einfluss des verwendeten Wirbelzwischenraums
zur Injektion. Br. J. Anaesth 1989;62(4):358–361. - Tuominen M, Kuulasmaa K, Taivainen T, Rosenberg PH: Individuelle Vorhersagbarkeit der wiederholten Spinalanästhesie mit isobarem Bupivacain. Acta Anaesthesiol Scand 1989;33(1):13–14.
- Sundnes KO, Vaagenes P, Skretting P, Lind B, Edstrom HH: Spinale Analgesie mit hyperbarem Bupivacain: Auswirkungen des Lösungsvolumens. Br
J Anaesth 1982;54(1):69–74. - Konishi R, Mitsuhata H, Saitoh J, Hirabayashi Y, Shimizu R: [Die Verbreitung von subarachnoidalem hyperbarem Dibucain im Begriff der Geburt]. Masui 1997;46(2):184–187.
- Veering BT, Ter Riet PM, Burm AG, Stienstra R, Van Kleef JW: Spinalanästhesie mit 0.5% hyperbarem Bupivacain bei älteren Patienten: Wirkung
der Injektionsstelle auf die Ausbreitung der Analgesie. Br. J. Anaesth 1996;77(3):343–346. - Cameron AE, Arnold RW, Ghorisa MW, Jamieson V: Spinalanalgesie mit Bupivacain 0.5 % pur. Variation im Ausmaß der Nervenblockade mit
Patientenalter. Anästhesie 1981;36(3):318–322. - Pitkanen M, Haapaniemi L, Tuominen M, Rosenberg PH: Einfluss des Alters auf die Spinalanästhesie mit isobarem 0.5% Bupivacain. Br. J. Anaesth 1984;56(3):279–284.
- Veering BT, Burm AG, Vletter AA, van den Hoeven RA, Spierdijk J: Die Auswirkung des Alters auf die systemische Absorption und systemische Disposition von Bupivacain nach subarachnoidaler Verabreichung. Anesthesiology 1991;74(2):250–257.
- Racle JP, Benkhadra A, Poy JY, Gleizal B: Spinale Analgesie mit hyperbarem Bupivacain: Einfluss des Alters. Br. J. Anaesth 1988;60(5): 508–514.
- Schiffer E, Van Gessel E, Gamulin Z: Einfluss des Geschlechts auf die Liquordichte bei Erwachsenen. Br. J. Anaesth 1999;83(6):943–944.
- Pargger H, Hampl KF, Aeschbach A, Paganoni R, Schneider MC: Kombinierte Wirkung von Patientenvariablen auf sensorischer Ebene nach spinal 0.5 %
reines Bupivacain. Acta Anaesthesiol Scand 1998;42(4):430–434. - Povey HM, Jacobsen J, Westergaard-Nielsen J: Subarachnoidale Analgesie mit hyperbarem 0.5% Bupivacain: Wirkung einer 60-minütigen Sitzperiode. Acta Anaesthesiol Scand 1989;33(4):295–297
- Alston RP, Littlewood DG, Meek R, Edstrom HH: Spinalanästhesie mit hyperbarem Bupivacain: Effekte von Konzentration und Volumen, wenn
im Sitzen verabreicht. Br. J. Anaesth 1988;61(2):144–148. - Alston RP: Spinalanästhesie mit 0.5 % Bupivacain 3 ml: Vergleich von einfachen und hyperbaren Lösungen, die sitzenden Patienten verabreicht werden. Br. J. Anaesth 1988;61(4):385–389.
- Mitchell RW, Bowler GM, Scott DB, Edstrom HH: Auswirkungen von Körperhaltung und Barizität auf die Spinalanästhesie mit 0.5 % Bupivacain 5 ml. Eine Doppelblindstudie. Br. J. Anaesth 1988;61(2):139–143.
- Povey HM, Olsen PA, Pihl H: Spinale Analgesie mit hyperbarem 0.5% Bupivacain: Auswirkungen verschiedener Patientenpositionen. Acta Anaesthesiol Scand 1987;31(7):616–619.
- Maroof M, Khan RM, Siddique M, Tariq M: Hypobare Spinalanästhesie mit Bupivacain (0.1 %) ergibt eine selektive sensorische Nervenblockade für anorektale Operationen. Can J Anaesth 1995;42(8):691–694.
- Fettes PD, Jansson JR, Wildsmith JA: Fehlgeschlagene Spinalanästhesie: Mechanismen, Management und Prävention. Br. J. Anaesth 2009;102(6):739–748.
- Tuominen M, Pitkanen M, Rosenberg PH: Wirkung der Injektionsgeschwindigkeit von 0.5% reinem Bupivacain auf die Ausbreitung der Spinalanästhesie. Br. J. Anaesth 1992;69(2):148–149.
- Van Gessel EF, Praplan J, Fuchs T, Forster A, Gamulin Z: Einfluss der Injektionsgeschwindigkeit auf die subarachnoidale Verteilung von isobarem Bupivacain
0.5 %. Anesth Analg 1993;77(3):483–487. - Stienstra R, Van Poorten F: Die Injektionsgeschwindigkeit hat keinen Einfluss auf die subarachnoidale Verteilung von reinem Bupivacain 0.5 %. Reg Anesth 1990;
15 (4): 208-210. - Bucx MJ, Kroon JW, Stienstra R: Wirkung der Injektionsgeschwindigkeit auf das maximale sensorische Niveau für Spinalanästhesie mit reinem Bupivacain
0.5 % bei Raumtemperatur. Reg Anesth 1993;18(2):103–105. - Axelsson KH, Edstrom HH, Sundberg AE, Widman GB: Spinalanästhesie mit hyperbarem 0.5% Bupivacain: Effekte des Volumens. Akt
Anaesthesiol Scand 1982;26(5):439–445. - Peng PW, Chan VW, Perlas A: Minimale wirksame Anästhesiekonzentration von hyperbarem Lidocain für die Spinalanästhesie. Can J Anaesth 1998;45(2):122–129.
- Alfonsi P, Brusset A, Levy R, Gauneau P, Chauvin M: [Spinalanästhesie mit Bupivacain ohne Glukose bei älteren Menschen: Wirkung von Konzentration und Volumen auf das hämodynamische Profil]. Ann Fr. Anesth Reanim 1991;10(6):543–547.
- Pflug EA, Aasheim GM, Beck HA: Spinalanästhesie: Bupivacain versus Tetracain. Anesth Analg 1976;55(4):489–492.
- Sheskey MC, Rocco AG, Bizzarri-Schmid M, Francis DM, Edstrom H, Covino BG: Eine Dosis-Wirkungs-Studie von Bupivacain für die Spinalanästhesie. Anesth Analg 1983;62(10):931–935.
- Kopacz DJ: Spinales 2-Chloroprocain: Minimale wirksame Dosis. Reg Anesth Pain Med 2005;30(1):36–42.
- Van Zundert AA, Grouls RJ, Korsten HH, Lambert DH: Spinalanästhesie. Volumen oder Konzentration – worauf kommt es an? Reg Anesth 1996;21(2):112–118.
- Cook TM, Fischer B, Bogod D, et al: Antiseptic solutions for central neuraxial block: Welche Konzentration von Chlorhexidin in Alkohol sollten wir verwenden? Br J Anaesth 2009;103:456–457.Schweizer RT: Maskenwackeln als mögliche Wundursache
contamination. Lancet 1976;2(7995):1129–1130. - Veringa E, van Belkum A, Schellekens H: Iatrogene Meningitis durch Streptococcus salivarius nach Lumbalpunktion. J Hosp Infect 1995;29(4):316–318.
- Hebl JR: Die Bedeutung und Auswirkungen aseptischer Techniken während der Regionalanästhesie. Reg Anesth Pain Med 2006;31(4):311–323.
- Verband der Anästhesisten von Großbritannien und Irland. Infektionskontrolle in der Anästhesie. Anästhesie 2008;63(9):1027–1036.
- Ross BK, Chadwick HS, Mancuso JJ, Benedetti C: Sprotte-Nadel für die geburtshilfliche Anästhesie: Verringerte Inzidenz von Post-Dural-Punktionen
Kopfschmerzen. Reg Anesth 1992;17(1):29–33. - de Filho GR, Gomes HP, da Fonseca MH, Hoffman JC, Pederneiras SG, Garcia JH: Prädiktoren für eine erfolgreiche neuraxiale Nervenblockade: Eine prospektive Studie. Eur J Anaesthesiol 2002;19(6):447–451.
- Lee PJ, Tang R, Sawka A, Krebs C, Vaghadia H: Kurzbericht: Echtzeit-Ultraschall-geführte Spinalanästhesie nach Taylors Ansatz. Anesth
Analg 2011;112(5):1236–1238. - Palmer CM: Kontinuierliche Spinalanästhesie und Analgesie in der Geburtshilfe. Anesth Analg 2010;111(6):1476–1479.
- Arkoosh VA, Palmer CM, Yun EM, et al: Ein randomisierter, doppelmaskierter, multizentrischer Vergleich der Sicherheit einer kontinuierlichen intrathekalen Wehenschmerzbehandlung mit einem 28-Gauge-Katheter im Vergleich zu einer kontinuierlichen epiduralen Wehenschmerzbehandlung. Anesthesiology 2008;108(2):286–298.
- Sng BL, Lim Y, Sia AT: Eine beobachtende prospektive Kohortenstudie zu Inzidenz und Merkmalen fehlgeschlagener Spinalanästhesie bei Kaiserschnitt
Sektion. Int J Obstet Anesth 2009;18(3):237–241. - Levy JH, Islas JA, Ghia JN, Turnbull C: Eine retrospektive Studie über die Inzidenz und Ursachen von fehlgeschlagenen Spinalanästhesien in einer Universitätsklinik.
Anesth Analg 1985;64(7):705–710. - Hoppe J, Popham P: Vollständiges Versagen der Spinalanästhesie in der Geburtshilfe. Int J Obstet Anesth 2007;16(3):250–255.
- Reina MA, Collier CB, Prats-Galino A, Puigdellivol-Sanchez A, Maches F, De Andres JA: Unbeabsichtigte subdurale Platzierung von Epiduralkathetern während einer versuchten Epiduralanästhesie: Eine anatomische Studie des subduralen Spinalkompartiments. Reg Anesth Pain Med 2011;36(6):537–541.
- Capdevila X, Dadure C: Perioperatives Management für einen Tag Krankenhausaufenthalt: Regionalanästhesie ist besser als Vollnarkose. Acta Anaesthesiol Belg 2004;55(Suppl):33–36.
- Ruben JE, Kamsler PM: Unilaterale Spinalanästhesie zur chirurgischen Reposition von Hüftfrakturen. Am J Surg 1950;79(2):312–317.
- Khatouf M, Loughnane F, Boini S, et al: [Unilaterale Spinalanästhesie bei älteren Patienten mit Hüfttrauma: Eine Pilotstudie]. Ann Fr. Anesth Reanim 2005;24(3):249–254.
- Cappelleri G, Aldegheri G, Danelli G, et al: Spinalanästhesie mit hyperbarem Levobupivacain und Ropivacain für die ambulante Kniearthroskopie: Eine prospektive, randomisierte, doppelblinde Studie. Anesth Analg 2005;101(1):77–82; Inhaltsverzeichnis.
- Fanelli G, Borghi B, Casati A, Bertini L, Montebugnoli M, Torri G: Unilaterale Bupivacain-Spinalanästhesie für die ambulante Kniearthroskopie. Italienische Studiengruppe für einseitige Spinalanästhesie. Can J Anaesth 2000;47(8):746–751.
- Nair GS, Abrishami A, Lermitte J, Chung F: Systematische Überprüfung der Spinalanästhesie mit Bupivacain für die ambulante Kniearthroskopie. Br. J. Anaesth 2009;102(3):307–315.
- Casati A, Fanelli G: Unilaterale Spinalanästhesie. Der letzte Stand der Technik. Minerva Anestesiol 2001;67(12):855–862.
- Schneider MC, Holzgreve W: [Vor 100 Jahren: Oskar Kreis, ein Pionier der spinalen geburtshilflichen Analgesie an der Universitätsfrauenklinik Basel]. Anaesthesist 2001;50(7):525–528.
- Horlocker TT, Wedel DJ, Rowlingson JC, et al.: Regionalanästhesie bei Patienten, die eine antithrombotische oder thrombolytische Therapie erhalten: Evidenzbasierte Leitlinien der American Society of Regional Anästhesie und Schmerzmedizin (dritte Ausgabe). Reg Anesth Pain Med 2010;35(1):64–101.
- Bogin IN, Stulin ID: [Anwendung der Methode der 2-dimensionalen Echospondylographie zur Bestimmung von Landmarken bei Lumbalpunktionen]. Zh Nevropatol Psikhiatr Im SS Korsakova 1971;71(12):1810–1811.Perlas A: Beweise für die Verwendung von Ultraschall bei neuraxialen Nervenblockaden. Reg Anesth Pain Med 2010;35(2 Suppl):S43–S46.
- Chin KJ, Karmakar MK, Peng P: Ultraschall der erwachsenen Brust- und Lendenwirbelsäule bei zentraler neuraxialer Blockade. Anesthesiology 2011;114(6):1459–1485.
- Chin KJ, Perlas A: Ultraschall der Lendenwirbelsäule für neuraxiale und lumbale Plexus-Nervenblockaden. Curr Opin Anaesthesiol 2011;24(5):567–572.
- Chin KJ, Perlas A, Singh M, et al: Ein ultraschallgestützter Ansatz erleichtert die Spinalanästhesie für die Totalgelenksendoprothetik. Can J Anaesth 2009;56(9):643–650.
- O'Donnell D, Prasad A, Perlas A: Ultraschallunterstützte Spinalanästhesie bei adipösen Patienten. Can J Anaesth 2009;56(12):982–983.
- Chin KJ, Chan VW, Ramlogan R, Perlas A: Echtzeit-Ultraschall-geführte Spinalanästhesie bei Patienten mit einer herausfordernden Wirbelsäulenanatomie: Zwei Fallberichte. Acta Anaesthesiol Scand 2010;54(2):252–255.
- Chin KJ, Perlas A, Chan V, Brown-Shreves D, Koshkin A, Vaishnav V: Die Ultraschallbildgebung erleichtert die Spinalanästhesie bei Erwachsenen mit schwierigen anatomischen Oberflächenmerkmalen. Anesthesiology 2011;115(1):94–101.
- Margarido CB, Arzola C, Balki M, Carvalho JC: Anästhesisten-Lernkurven für die Ultraschallbeurteilung der Lendenwirbelsäule. Can J Anaesth 2010;57(2):120–126.
- Halpern SH, Banerjee A, Stocche R, Glanc P: Die Verwendung von Ultraschall zur Identifizierung von lumbalen Dornfortsätzen: Eine Pilotstudie. Can J Anaesth 2010;57(9):817–822.
- Carvalho JC: Ultraschallunterstützte Epiduralanästhesie und Spinalanästhesie in der Geburtshilfe. Anesthesiol Clin 2008;26(1):145–158, vii–viii.
- Bron JL, van Royen BJ, Wuisman PI: Die klinische Bedeutung lumbosakraler Übergangsanomalien. Acta Orthop Belg 2007;73(6):687–695.
- Spivak H, Nudelman I, Fuco V, et al: Laparoskopische extraperitoneale Leistenhernienreparatur mit Spinalanästhesie und Lachgas-Insufflation. Surg Endosc 1999;13(10):1026–1029.
- Schmidt J, Carbajo MA, Lampert R, Zirngibl H: Laparoskopische intraperitoneale Onlay-Polytetrafluorethylen-Mesh-Reparatur (IPOM) für Leistenbruch während der Spinalanästhesie bei Patienten mit schweren Erkrankungen. Surg Laparosc Endosc Percutan Tech 2001;11(1):34–37.
- Vaghadia H, Viskari D, Mitchell GW, Berrill A: Selektive Spinalanästhesie für die ambulante Laparoskopie. I: Eigenschaften von drei hypobaren Lösungen. Can J Anaesth 2001;48(3):256–260.
- Tzovaras G, Zacharoulis D, Georgopoulou S, Pratsas K, Stamatiou G, Hatzitheofilou C: Laparoskopische ventrale Hernienreparatur unter Spinalanästhesie: Eine Machbarkeitsstudie. Am J Surg 2008;196(2):191–194.
- Chilvers CR, Vaghadia H, Mitchell GW, Merrick PM: Klein dosierte hypobare Lidocain-Fentanyl-Spinalanästhesie für kurzzeitige ambulante Laparoskopie. II. Optimale Fentanyl-Dosis. Anesth Analg 1997; 84(1):65–70.
- Ghodki PS, Sardesai SP, Thombre SK: Bewertung der Wirkung von intrathekalem Clonidin zur Verringerung von Schulterspitzenschmerzen bei der Laparoskopie unter Spinalanästhesie. Indian J Anaesth 2010;54(3):231–234.
- Jonnesco T. Bemerkungen zur allgemeinen Wirbelsäulen-Analgesie. Br Med J 1909;2(2550):1396–1401.
- Lee AJ, Ranasinghe JS, Chehade JM, Arheart K, Saltzman BS, Penning DH, et al: Ultraschallbeurteilung der Wirbelebene der Interkristalllinie in der Schwangerschaft. Anesth Analg 2011;113(3):559–564.