Miguel A. Reina, Carlo D. Franco, Alberto Prats-Galino, Fabiola Machés, Andrés López und Jose A de Andrés
EINFÜHRUNG
Jüngste Forschungen zur Ultrastruktur des menschlichen spinalen Duralsacks und seines Inhalts haben unser Verständnis der Mikrostruktur der Dura mater, der Arachnoidalschicht, der trabekulären Arachnoidea, der Pia mater und der Nervenwurzelmanschetten verbessert. Dieses Kapitel gibt einen Überblick über neue und traditionelle Konzepte in Bezug auf diese Strukturen und diskutiert ihre möglichen klinischen Implikationen. Die Verteilung des epiduralen Fetts und seine mögliche Rolle bei der Disposition und Kinetik von neuraxialen Injektionen werden ebenfalls diskutiert.
Duralbeutel
Der Duralsack umgibt das Rückenmark innerhalb der Wirbelsäule. Er trennt den Epiduralraum vom Subarachnoidalraum und endet am zweiten Kreuzbeinwirbel. In einer idealisierten Form ist der Duralsack zylindrisch mit einer Dicke, die von etwa 1 mm im Halsbereich abweicht und nach unten hin allmählich dünner wird (Figuren 1 und 2). In der Lendengegend erreicht die Dicke des Duralsacks 0.3 mm, obwohl Messungen von anteroposterior oder lateral selbst auf derselben Wirbelhöhe etwas variieren können. Die Dura mater ist die äußerste Schicht des Duralsacks und macht 90 % seiner Gesamtdicke aus. Obwohl diese Faserstruktur durchlässig ist, bietet sie dem Rückenmark und seinen neuralen Elementen einen gewissen mechanischen Schutz. Die inneren 10 % des Duralsacks werden von der Arachnoidalschicht gebildet, einer Zellschicht, die wenig zusätzlichen mechanischen Widerstand hinzufügt.
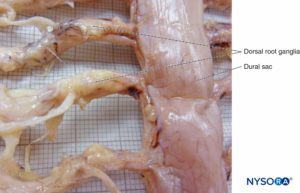
ABBILDUNG 1. Menschlicher Duralsack. (Wiedergegeben mit Genehmigung von Reina MA, López García A, de Andrés JA, et al: Thickness variation of the dural sac. Rev Esp Anestesiol Reanim. 1999 Oct;46(8):344-349.)
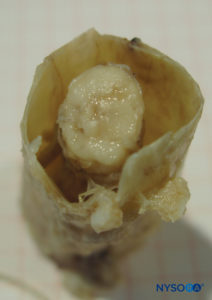
ABBILDUNG 2. Menschlicher Duralsack und Ende des Rückenmarks. (Wiedergegeben mit Genehmigung von Reina MA, Pulido P, López A. El saco dural humano: Rev Arg Anestesiol. 2007; 65:167-184.)
DURA MATER
Dura mater besteht aus etwa 80 konzentrischen Laminas (Figure 3). Jede Duralschicht hat eine Dicke von etwa 5 μm und besteht aus dünneren Schichten, die hauptsächlich Kollagenfasern enthalten (Figuren 4 und 5). Die Kollagenfasern sind in verschiedene Richtungen orientiert, aber immer innerhalb der konzentrischen Ebene der Durallamina; daher kreuzen sie sich nicht zwischen den Plättchen. Jede Kollagenfaser hat eine glatte Oberfläche und misst etwa 0.1 μm (Figure 6). Die elastischen Fasern sind mit 2 μm Durchmesser weniger und haben eine rauere Oberfläche als die Kollagenfasern (Figure 7).
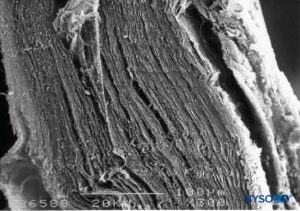
ABBILDUNG 3. Dicke des Duralsacks. Rasterelektronenmikroskopie. Vergrößerung ×300. (Wiedergabe mit freundlicher Genehmigung von Reina MA, Dittmann M, López A, et al: New perspectives in the microscopic structure of human dura mater in the dorso lumbar region. Reg Anesth. 1997 Mar-Apr;22(2):161-166. )
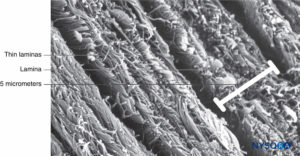
ABBILDUNG 4. Partielle Dicke des Duralsacks. Details der Durallamina. Rasterelektronenmikroskopie. Vergrößerung ×4,000. (Wiedergabe mit freundlicher Genehmigung von Reina MA, López A, Dittmann M, et al: Structure of human Dura Mater Thickness by Scanning Electron Microscopy. Rev Esp Anestesiol Reanim. 1996 Apr;43(4):135-137.)
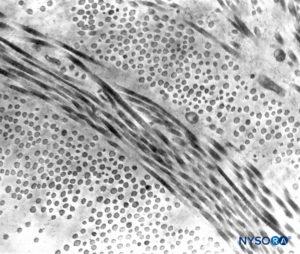
ABBILDUNG 5. Partielle Dicke des Duralsacks. Details der Durallamina. Transmissionselektronenmikroskopie. Vergrößerung ×20,000. (Wiedergabe mit freundlicher Genehmigung von Raj P: Textbook of Regional Anästhesie. Philadelphia: Churchill Livingstone; 2002.)
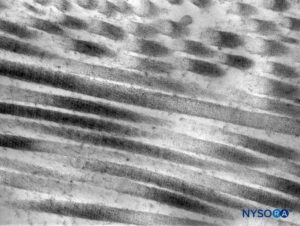
ABBILDUNG 6. Kollagenfasern in der Dicke des Duralsacks. Transmissionselektronenmikroskopie. Vergrößerung ×50,000. (Wiedergabe mit freundlicher Genehmigung von Raj P: Textbook of Regional Anästhesie. Philadelphia: Churchill Livingstone; 2002.)
Im Gegensatz zu der klassischen Beschreibung, dass Fasern innerhalb der Durallamina längs und parallel zur Längsachse der Wirbelsäule angeordnet sind, sind die Fasern tatsächlich multidirektional und willkürlich innerhalb jeder der konzentrischen Durallamina verteilt (Figuren 8 zu 10). Mastozyten und Makrophagen sind auch in der Dura mater vorhanden (Figuren 11 und 12).
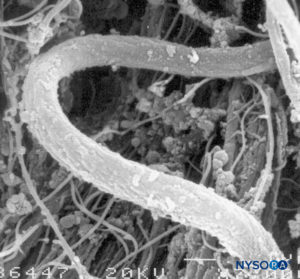
ABBILDUNG 7. Elastische Fasern des Duralsacks. Rasterelektronenmikroskopie. Vergrößerung ×7000. (Wiedergabe mit freundlicher Genehmigung von Reina MA, López A, Dittmann M, et al: External and internal surface of human dura mater by Scanning Electron Microscopy. Rev Esp Anestesiol Reanim. 1996 Apr;43(4):130-4.)

ABBILDUNG 8. Detail der epiduralen Oberfläche des Duralsacks. Rasterelektronenmikroskopie. Vergrößerung ×6500. (Wiedergabe mit freundlicher Genehmigung von Dittmann M, Reina MA, López A: Neue Ergebnisse bei der Darstellung der Dura mater spinalis mittles rasterelektronenmikroskopie. Anaesthesist. 1998 May;47(5):409-413.)
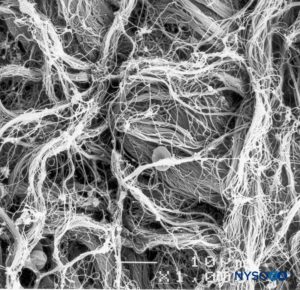
ABBILDUNG 9. Detail der epiduralen Oberfläche des Duralsacks. Rasterelektronenmikroskopie. Vergrößerung ×1000. (Wiedergabe mit freundlicher Genehmigung von Reina MA, López A, Dittmann M, et al: External and internal surface of human dura mater by Scanning Electron Microscopy. Rev Esp Anestesiol Reanim. 1996 Apr;43(4):130-4.)
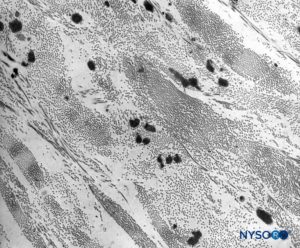
ABBILDUNG 10. Kollagen und elastische Fasern in der Dicke des Duralsacks. Transmissionselektronenmikroskopie. Vergrößerung ×7,000. (Wiedergabe mit freundlicher Genehmigung von Raj P: Textbook of Regional Anästhesie. Philadelphia: Churchill Livingstone; 2002.)
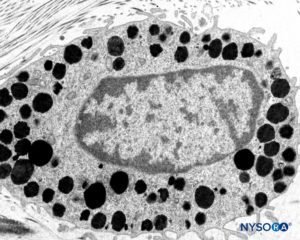
ABBILDUNG 11. Mastozyt in der Dicke der Dura mater. Transmissionselektronenmikroskopie. Vergrößerung ×15,000. (Wiedergegeben mit Genehmigung von Reina MA, Pulido P, López A. El saco dural humano: Rev Arg Anestesiol. 2007;65:167-184.)
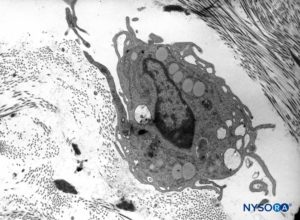
ABBILDUNG 12. Makrophage in der Dicke der Dura mater. Transmissionselektronenmikroskopie. Vergrößerung ×7000. (Wiedergabe mit freundlicher Genehmigung von Raj P: Textbook of Regional Anästhesie. Philadelphia: Churchill Livingstone; 2002.)
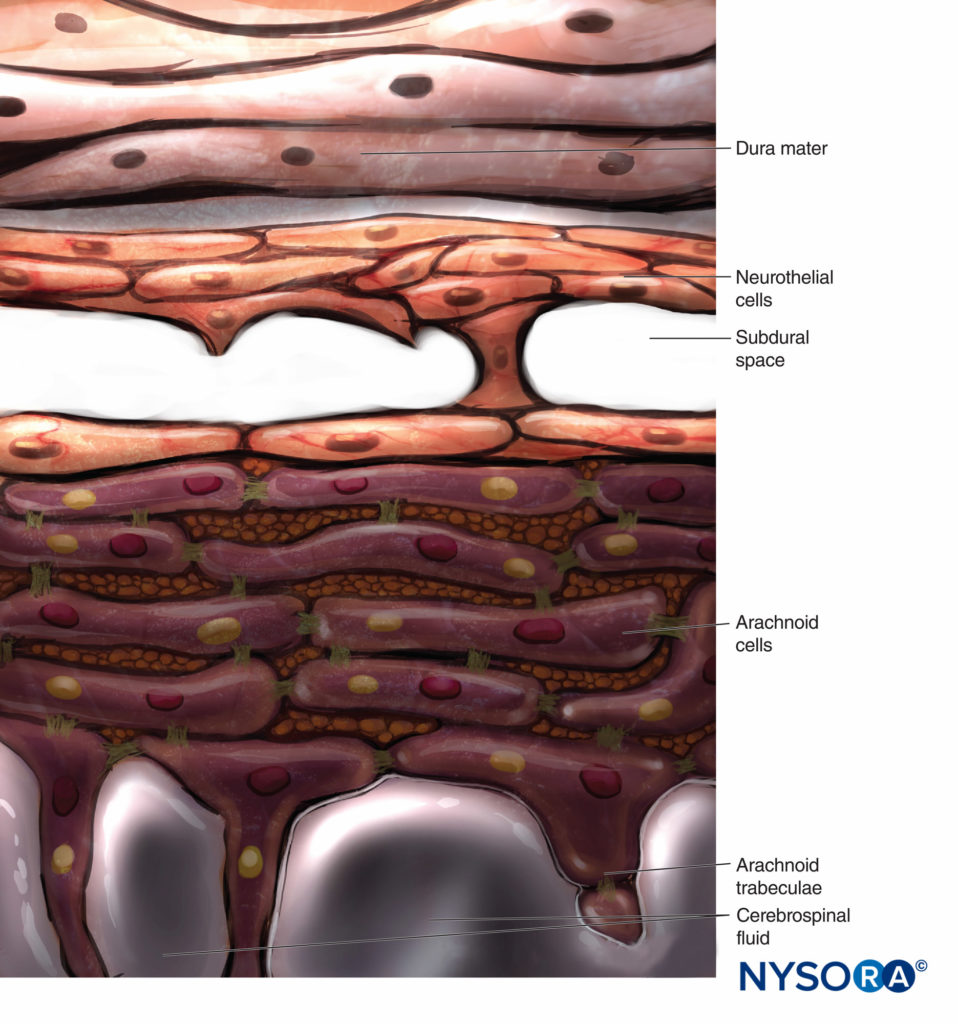
ARACHNOIDE SCHICHT
Herkömmlicherweise wird die Arachnoidalschicht als eine feine Membran beschrieben, die in engem Kontakt mit der inneren Oberfläche der Dura mater steht, jedoch nicht daran haftet. Jüngste Forschungen haben jedoch festgestellt, dass zwischen der Dura mater und der Arachnoidalschicht kein Zwischenraum besteht (siehe Subduralraum). Die Arachnoidea ist semipermeabel und dient als Barriere, um den Durchgang von Substanzen durch den Duralsack zu begrenzen (Figuren 13 und 14). Seine Dicke beträgt etwa 50-60 μm (Figuren 15 und 16). In ihrem Inneren verbinden sich Arachnoidea-Zellen stark durch spezifische Membrankontakte mit einer Dicke von etwa 10–15 μm. Kollagenfasern in der Mitte der Arachnoidea verleihen der Lamina Festigkeit und verbessern ihre mechanische Widerstandsfähigkeit. Flache, längliche Neurothelzellen nehmen den äußeren Teil der Schicht ein. Durch Abreißen der Arachnoidalschicht wird der Subduralraum freigelegt. Neurothelzellen finden sich entweder an der inneren Oberfläche der Dura oder an der äußeren Oberfläche der Arachnoidea (Figure 17).
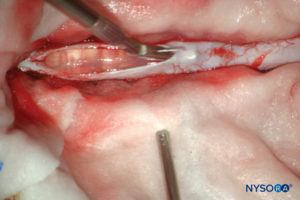
ABBILDUNG 13. Dissektion des menschlichen Duralsacks. (Wiedergegeben mit Genehmigung von Reina MA, Pulido P, López A. El saco dural humano. Rev Arg Anestesiol. 2007; 65:167-184.)
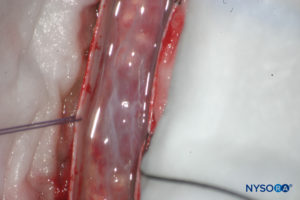
ABBILDUNG 14. Dissektion des menschlichen Duralsacks. Dura mater ist offen; Arachnoidalschicht ist geschlossen. (Wiedergegeben mit Genehmigung von Reina MA, Pulido P, López A. El saco dural humano. Rev Arg Anestesiol. 2007; 65:167-184.)
NEURAXIALER Block UND DURALÄSIONEN
Das Durchstechen des Duralsacks während einer Subarachnoidalblockade verursacht eine mechanische Zerstörung sowohl der Dura mater als auch der Arachnoidalschicht. Die Querschnittsfläche der Punktionsstelle, die durch eine 25-Gauge-Nadel erzeugt wird, ist ähnlich, unabhängig davon, ob die Nadel eine Bleistiftspitze oder ein schneidendes Ende hat. Die Morphologie der Läsion variiert jedoch je nach Design der Nadelspitze. Nadeln mit Bleistiftspitze erzeugen eine größere und gröber erscheinende Verletzung der Duralfasern, während schneidende Nadeln eine U-förmige Läsion oder einen Lappen erzeugen, der dem offenen Deckel einer Konservendose ähnelt (Figuren 8 zu 31).
Bei der Verwendung von schneidenden (lang abgeschrägten) Nadeln hat die Ausrichtung der Abschrägung (z. B. parallel oder senkrecht zur Hauptachse des Rückenmarks) keinen signifikanten Einfluss auf die Größe oder Morphologie der Läsionen in der Dura und Arachnoidea (siehe Figure 24). Die Läsion, die die Nadel im Duralsack erzeugt, hat zwei Komponenten, Dural und Arachnoidea. Es wird angenommen, dass die arachnoidale Komponente bei der Begrenzung des Austretens von Cerebrospinalflüssigkeit aus dem Subarachnoidalraum in den Epiduralraum von entscheidender Bedeutung ist. Daher scheinen die Größe und Morphologie von Arachnoidalläsionen für die laminare Abdichtung und zerebrospinale Leckage wichtiger zu sein als die Größe und Morphologie von Duraverletzungen.
Es wurde angenommen, dass das Auftreten von Kopfschmerzen nach Punktion (PDPH) durch die Art der verwendeten Nadel (Bleistiftspitze oder Schneiden) und die Abschrägung beeinflusst wird. Der traditionelle Glaube, dass schneidende Nadeln zu größeren Duralläsionen (Risse) führen, wurde in den 1940er Jahren etabliert und könnte die Folge der Unvollkommenheiten im Nadeldesign dieser Zeit gewesen sein. Moderne Nadeln erzeugen jedoch saubere, U-förmige Läsionen oder Lappen, die dem offenen Deckel einer Konservendose ähneln (vgl Figure 24).
Nach dem Herausziehen der Nadel neigt der U-förmige Lappen aufgrund des Liquordrucks und der elastischen Eigenschaften der Dura mater dazu, in seine ursprüngliche Position zurückzukehren. Die Duralöffnung ist nach etwa 15 Minuten fast vollständig verschlossen. Andererseits umfassen Läsionen, die durch Bleistiftspitzennadeln erzeugt werden, eine komplexere Läsion mit Faserriss, Schnitt und Trennung. Das Ausmaß der durch eine Nadel verursachten Duralläsion hängt von mehreren Faktoren ab, einschließlich des Außendurchmessers der Nadel, der Dura- und Arachnoidal-Dichtungsmechanismen, des Designs der Nadelspitze und der Qualität der Nadelherstellung. Nadeln mit dem gleichen Spitzendesign, aber unterschiedlichen Herstellungsverfahren haben möglicherweise nicht die gleiche Oberflächenqualität und können Mikrofrakturen oder Fehler enthalten, was zu mehr oder weniger ausgedehntem Reißen der Durafaser und Restläsionen führt.
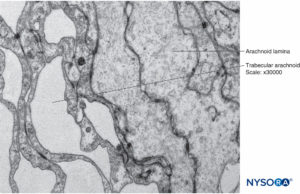
ABBILDUNG 15. Arachnoidalzellen in der Dicke der Arachnoidalschicht. Transmissionselektronenmikroskopie. Vergrößerung ×40,000.
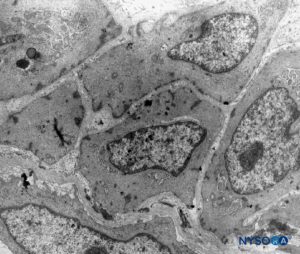
ABBILDUNG 16. Arachnoidalzellen in der Dicke der Arachnoidalschicht. Transmissionselektronenmikroskopie. Vergrößerung ×4400. (Wiedergabe mit freundlicher Genehmigung von Raj P: Textbook of Regional Anästhesie. Philadelphia: Churchill Livingstone; 2002.)
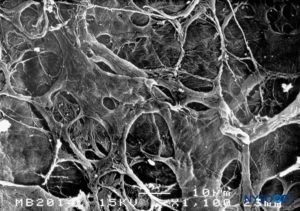
ABBILDUNG 17. Innere Oberfläche der Dura mater. Rasterelektronenmikroskopie. Vergrößerung ×1100. (Wiedergabe mit freundlicher Genehmigung von Reina MA, Dittmann M, López A, et al: New perspectives in the microscopic structure of human dura mater in the dorso lumbar region. Reg Anesth. 1997 Mar-Apr;22(2):161-166. )
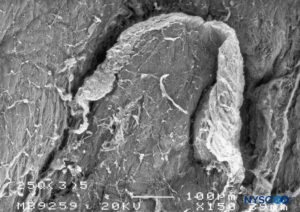
ABBILDUNG 18. Dura-Arachnoidal-Läsion, die mit einer 25-G-Quincke-Nadel erzeugt wurde. Epidurale Oberfläche. Rasterelektronenmikroskopie. Vergrößerung ×150. (Reproduziert mit Genehmigung von Reina MA, Castedo J, López A, et al.: Cefalea pospuncion dural: Ultraestructura de las pests Durables y Abuja's Spindles Usages en las Punciones Lumbers. Rev Arg Anesthesiol. 2008 Jan-Mar 66(1):6- 26)
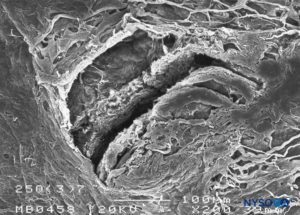
ABBILDUNG 19. Dura-Arachnoidal-Läsion, die mit einer 25-G-Quincke-Nadel erzeugt wurde. Arachnoidale Oberfläche. Rasterelektronenmikroskopie. Vergrößerung ×200. (Wiedergegeben mit Genehmigung von Reina MA, Castedo J, López A. Cefalea pospunción dural: Ultraestructura de las lesiones durales y agujas espinales usadas en las punciones lumbares. Rev Arg Anestesiol. 2008 Jan-Mar 66(1):6-26.)
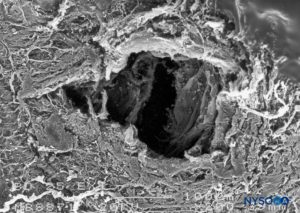
ABBILDUNG 20. Dura-Arachnoidal-Läsion, erzeugt mit einer 25-G-Whitacre-Nadel. Epidurale Oberfläche. Rasterelektronenmikroskopie. Vergrößerung ×200. (Wiedergabe mit freundlicher Genehmigung von Reina MA, López-García A, de Andrés-Ibáñez JA, et al.: Electron microscopy of the damage made in the human dura mater by Quincke beveled and Whitacre needles. Rev Esp Anestesiol Reanim. 1997 Feb;44( 2):56-61.)
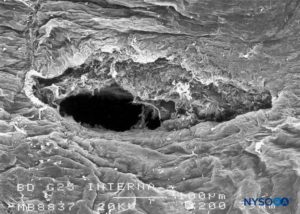
ABBILDUNG 21. Dura-Arachnoidal-Läsion, erzeugt mit einer 25-G-Whitacre-Nadel. Arachnoidale Oberfläche. Rasterelektronenmikroskopie. Vergrößerung ×200. (Wiedergabe mit freundlicher Genehmigung von Reina MA, López-García A, de Andrés-Ibáñez JA, et al.: Electron microscopy of the damage made in the human dura mater by Quincke beveled and Whitacre needles. Rev Esp Anestesiol Reanim. 1997 Feb;44( 2):56-61.)
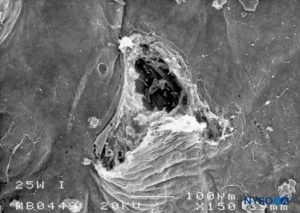
ABBILDUNG 22. Dura-Arachnoidal-Läsion, erzeugt mit einer 25-G-Whitacre-Nadel. Arachnoidale Oberfläche. Rasterelektronenmikroskopie. Vergrößerung ×200. (Wiedergegeben mit Genehmigung von Reina MA, De Leon Casasola OA, et al: An in vitro study of durale Läsionen, die durch Rasterelektronenmikroskopie erzeugt wurden. Reg Anesth Pain Med. 2000 Jul-Aug;25(4):393-402.)

ABBILDUNG 23. Dura-Arachnoidal-Läsion, die mit einer 22-G-Quincke-Nadel erzeugt wurde. Epidurale Oberfläche. Rasterelektronenmikroskopie. Vergrößerung ×80. (Reproduziert mit Genehmigung von Reina MA, Castedo J, López A. Cefalea pospunción dural: Ultraestructura de las lesiones durales y agujas espinales usadas en las punciones lumbares. Rev Arg Anestesiol. 2008 Jan-Mar 66(1):6-26.)
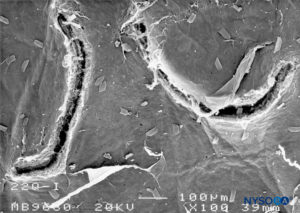
ABBILDUNG 24. Dura-Arachnoidal-Läsion, die mit einer 22-G-Quincke-Nadel erzeugt wurde. Arachnoidale Oberfläche. Rasterelektronenmikroskopie. Vergrößerung ×100. (Wiedergabe mit freundlicher Genehmigung von Raj P: Textbook of Regional Anästhesie. Philadelphia: Churchill Livingstone; 2002.)
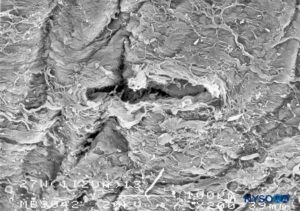
ABBILDUNG 25. Dura-Arachnoidal-Läsion, erzeugt mit einer 27-G Whitacre-Nadel. Epidurale Oberfläche. Rasterelektronenmikroskopie. Vergrößerung ×200. (Reproduziert mit Genehmigung von Reina MA, Castedo J, López A. Cefalea pospunción dural: Ultraestructura de las lesiones durales y agujas espinales usadas en las punciones lumbares. Rev Arg Anestesiol. 2008 Jan-Mar 66(1):6-26.)
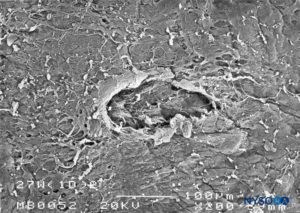
ABBILDUNG 26. Dura-Arachnoidal-Läsion, erzeugt mit einer 27-G Whitacre-Nadel. Epidurale Oberfläche. Rasterelektronenmikroskopie. Vergrößerung ×200. (Reproduziert mit Genehmigung von Reina MA, Castedo J, López A. Cefalea pospunción dural: Ultraestructura de las lesiones durales y agujas espinales usadas en las punciones lumbares. Rev Arg Anestesiol. 2008 Jan-Mar 66(1):6-26.)
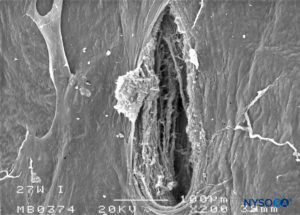
ABBILDUNG 27. Dura-Arachnoidal-Läsion, erzeugt mit einer 27-G Whitacre-Nadel. Arachnoidale Oberfläche. Rasterelektronenmikroskopie. Vergrößerung ×200. (Wiedergegeben mit Genehmigung von Reina MA, Castedo J, López A. Cefalea pospunción dural: Ultraestructura de las lesiones durales y agujas espinales usadas en las punciones lumbares. Rev Arg Anestesiol. 2008 Jan-Mar 66(1):6-26.)
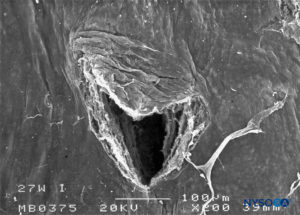
ABBILDUNG 28. Dura-Arachnoidal-Läsion, erzeugt mit einer 27-G Whitacre-Nadel. Arachnoidale Oberfläche. Rasterelektronenmikroskopie. Vergrößerung ×200. (Wiedergegeben mit Genehmigung von Reina MA, Castedo J, López A. Cefalea pospunción dural: Ultraestructura de las lesiones durales y agujas espinales usadas en las punciones lumbares. Rev Arg Anestesiol. 2008 Jan-Mar 66(1):6-26.)
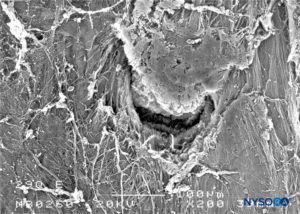
ABBILDUNG 29. Dura-Arachnoidal-Läsion, die mit einer 29-G-Quincke-Nadel erzeugt wurde. Epidurale Oberfläche. Rasterelektronenmikroskopie. Vergrößerung ×200. (Reproduziert mit Genehmigung von Reina MA, Castedo J, López A. Cefalea pospunción dural: Ultraestructura de las lesiones durales y agujas espinales usadas en las punciones lumbares. Rev Arg Anestesiol. 2008 Jan-Mar 66(1):6-26.)
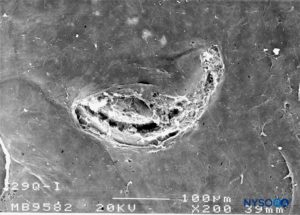
ABBILDUNG 30. Dura-Arachnoidal-Läsion, die mit einer 29-G-Quincke-Nadel erzeugt wurde. Arachnoidale Oberfläche. Rasterelektronenmikroskopie. Vergrößerung ×200. (Reproduziert mit Genehmigung von Reina MA, Castedo J, López A. Cefalea pospunción dural: Ultraestructura de las lesiones durales y agujas espinales usadas en las punciones lumbares. Rev Arg Anestesiol. 2008 Jan-Mar 66(1):6-26.
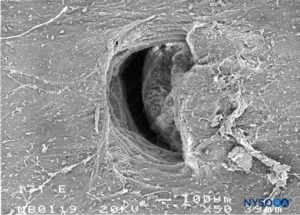
ABBILDUNG 31. Dura-Arachnoidal-Läsion, erzeugt mit einer 17-G-Tuohy-Nadel. Arachnoidale Oberfläche. Rasterelektronenmikroskopie. Vergrößerung ×50. (Reproduziert mit Genehmigung von Reina MA, Castedo J, López A. Cefalea pospunción dural: Ultraestructura de las lesiones durales y agujas espinales usadas en las punciones lumbares. Rev Arg Anestesiol. 2008 Jan-Mar 66(1):6-26.)
Eine Verformung der Spinalnadel, die durch Kontakte mit Wirbelknochen oder anderen widerstandsfähigen Strukturen während des neuraxialen Eingriffs verursacht wird, kann ebenfalls die Größe der Duraläsion vergrößern. Auch eine iatrogene Einbringung von Hautfragmenten in den Subarachnoidalraum kann auftreten.
KOPFSCHMERZEN NACH DER POSTDURALEN Punktion und Art der Nadeln
Die Ätiologie der PDPH ist multifaktoriell. Während sich das spezifische Kapitel über PDPH auf Pathophysiologie, Prävention und Behandlung konzentriert, konzentriert sich dieser Abschnitt auf anatomische und gerätebezogene Faktoren, die das Auftreten und den Schweregrad von PDPH beeinflussen können. Anfänglich wurde angenommen, dass Nadeln mit Bleistiftspitze zu weniger traumatischen Perforationen des Duralsacks führten. Als die Morphologie von Duralläsionen besser bekannt wurde, wurden andere Erklärungen vorgeschlagen. Mikroskopische Untersuchungen von Läsionen, die durch Spinalnadeln verursacht wurden, zeigten, dass die Nadeln mit Bleistiftspitze eine „platzende“ Läsion mit ausgedehnten Faserschäden erzeugen. Allerdings kann das verstärkte Faserreißen, das durch Bleistiftspitzennadeln erzeugt wird, eine stärkere Entzündungsreaktion an den Rändern der Läsion fördern, was paradoxerweise zu einem früheren Verschluss und einer geringeren Inzidenz von PDPH führt. Schneidende Nadeln hingegen erzeugen einen „saubereren“ Riss der Dura mit weniger Entzündungsreaktion, was zu einer verzögerten Versiegelung der Punktion führt, was das Auftreten von Wirbelsäulenkopfschmerzen erhöhen könnte.
Eine nach dem Aufprall auf Knochen abgestumpfte Nadelspitze kann die Fasern stärker schädigen. Die Verformung der Spitze hängt vom Kollisionswinkel und der aufgebrachten Kraft ab. Schneidende Nadeln sind im Gegensatz zu Nadeln mit Bleistiftspitze besonders anfällig für eine Verformung der Nadelspitze nach dem Aufprall auf Knochen. Da PDPH-Studien jedoch im Allgemeinen viele Anästhesisten und verschiedene Techniken umfassen, ist die endgültige Auswirkung der Nadelverformung auf PDPH schwierig zu untersuchen und bleibt zu diesem Zeitpunkt nur hypothetisch.
Wie erwähnt, hat die durch die Spinalnadel erzeugte Dura-Läsion zwei Komponenten, eine Dura-Mater-Läsion und eine Arachnoidalschicht-Läsion. Während die äußere oder durale Komponente des Sacks mechanischen Widerstand bietet, ist sie nicht elastisch genug, um ein Austreten von Zerebrospinalflüssigkeit zu verhindern. Im Gegensatz dazu kann sich die innere oder arachnoidale Läsion zurückziehen, um den Defekt zu schließen, der durch das Einführen der Nadel in den Subarachnoidalraum erzeugt wurde, und das Austreten von Liquor cerebrospinalis verhindern. Da die Arachnoidalkomponente in der Pathophysiologie von PDPH wahrscheinlich wichtiger ist als die Dura selbst, sollten diese Läsionen als „Dura-Arachnoidal“-Läsionen bezeichnet werden.
TRABEKULÄRE ARACHNOIDE
Die Arachnoidea besteht aus zwei Schichten, der trabekulären Arachnoidea und der Arachnoidea. Die trabekuläre Arachnoidea verschmilzt mit der Zellebene der Pia mater und sendet Projektionen an alle Strukturen aus, die den Subarachnoidalraum durchqueren, einschließlich Blutgefäße und Nervenwurzeln. Die Vorsprünge, die die Nervenwurzeln bedecken, werden Arachnoidalscheiden genannt (Figuren 32 zu 40).
Bei Bewegung stabilisieren und verhindern diese Hüllen übermäßige Bewegungen der Nervenwurzeln innerhalb des Duralsacks. Die Hüllen verleihen jedoch wenig mechanischen Schutz gegen Traumata. Die Merkmale der Arachnoidalscheiden in der Cauda equina sind variabel; einige sind locker, während andere durch überlagerte Ebenen der gleichen Komponenten mit einem kompakteren Aussehen gebildet werden. Die Dicke einer Arachnoidea reicht von 10 bis 60 μm. In manchen Fällen sind eine oder mehrere Nervenwurzeln von einer einzigen Arachnoidalscheide umhüllt, in anderen hat die Nervenwurzel überhaupt keine Scheide.
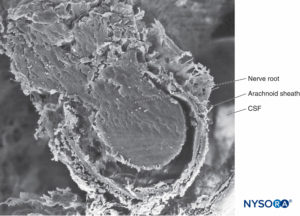
ABBILDUNG 32. Trabekuläre Arachnoidalschicht. Die Vorsprünge der trabekulären Arachnoidea, die Nervenwurzeln bedecken, werden als Arachnoidalscheiden bezeichnet. CSF = Liquor cerebrospinalis. Rasterelektronenmikroskopie. Vergrößerung ×100. (Wiedergabe mit freundlicher Genehmigung von Reina MA, López A, De Andrés JA: Hypothese betreffend die anatomische Grundlage des Cauda-Equina-Syndroms und der vorübergehenden Nervenwurzelirritation nach Spinalanästhesie. Rev Esp Anestesiol Reanim. 1999 Mar;46(3):99-105. )
ARACHNOID-HÜLLEN VON NERVENWURZELN UND IHRE POTENZIELLE ROLLE BEI NERVENLÄSIONEN
Einige Fälle des Cauda-Equina-Syndroms und des transienten neurologischen Syndroms könnten durch das Vorhandensein von Arachnoidalscheiden um die Nervenwurzeln innerhalb des Duralsacks und die Tatsache, dass Nadeln oder (Mikro-)Katheter in sie eingeführt werden können, erklärt werden. Eine versehentlich in die Arachnoidalscheide eines Spinalnerven injizierte Anästhesielösung wird möglicherweise nicht durch die umgebende Zerebrospinalflüssigkeit verdünnt, wodurch die Nervenwurzel einer höheren Anästhesiekonzentration als erwartet ausgesetzt wird. Folglich könnte die Konzentration des Lokalanästhetikums im Vergleich zur Konzentration des Anästhetikums im restlichen Duralsack um Größenordnungen höher sein (z. B. 20- bis 25-mal).
Eine solch hohe Konzentration des Lokalanästhetikums innerhalb der Arachnoidalscheide könnte schädliche Wirkungen auf die Nervenwurzeln haben, im Gegensatz zu einer typischen Injektion derselben Anästhetikumlösung innerhalb des Duralsacks, aber außerhalb der Arachnoidalscheide. Da es Zeit braucht, um innerhalb und außerhalb der Hülle ein Gleichgewicht herzustellen, könnte sich eine Nervenläsion ohne direktes Nadeltrauma entwickeln. Injektionen eines Lokalanästhetikums durch einen Mikrokatheter in diese Arachnoidalhüllen könnten verheerender sein als eine einzelne Injektion. Dies liegt daran, dass die Injektion eines einzelnen großen Volumens schließlich durch Leckagen außerhalb der Schleuse verdünnt würde, während wiederholte Dosen kleiner Volumina aufgrund der kontinuierlichen oder wiederholten Exposition gegenüber einer hohen Konzentration von Lokalanästhetika eher zu Neurotoxizität führen können. Das transiente Wurzelirritationssyndrom und das Cauda-Equina-Syndrom können unterschiedliche Grade der Nervenschädigung in Abhängigkeit von der Konzentration des Lokalanästhetikums und der Expositionsdauer widerspiegeln. Die Injektion eines Lokalanästhetikums in Arachnoidalscheiden in Bereichen in der Nähe des Rückenmarks oder des Conus medullaris kann mehrere Nervenwurzeln betreffen, während eine Injektion in distalere Bereiche einzelne Nervenwurzeln betreffen kann.

ABBILDUNG 33. Trabekuläre Arachnoidalschicht. Detail der Arachnoidea. CSF = Liquor cerebrospinalis. Rasterelektronenmikroskopie. Vergrößerung x500. (Wiedergabe mit freundlicher Genehmigung von Raj P: Textbook of Regional Anästhesie. Philadelphia: Churchill Livingstone; 2002.)
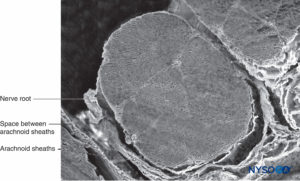
ABBILDUNG 34. Nervenwurzel und Arachnoidea. Rasterelektronenmikroskopie. Vergrößerung ×60. (Wiedergabe mit freundlicher Genehmigung von Torres LM: Lehrbuch der Anästhesie und Schmerzbehandlung. Aran Ed; 2001.)
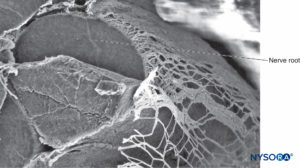
ABBILDUNG 35. Nervenwurzel und Arachnoidea. Rasterelektronenmikroskopie. Vergrößerung ×80. (Wiedergegeben mit Genehmigung von Reina MA, Villanueva MC, López A: Aracnoides trabecular, piamadre espinal humana y anestesia subaracnoidea, Rev Arg Anestesiol 2008;66: 111–133.)
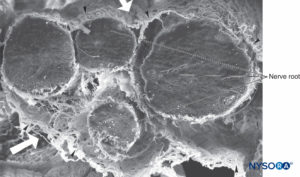
ABBILDUNG 36. Vier-Nerven-Wurzel und ihre Arachnoidea. Rasterelektronenmikroskopie. Vergrößerung ×100. (Wiedergabe mit freundlicher Genehmigung von Reina MA, López A, De Andrés JA: Hypothese betreffend die anatomische Grundlage des Cauda-Equina-Syndroms und der vorübergehenden Nervenwurzelirritation nach Spinalanästhesie. Rev Esp Anestesiol Reanim. 1999 Mar;46(3):99-105. )

ABBILDUNG 37. Menschliches Rückenmark und trabekuläre Arachnoidalschicht. CSF = Liquor cerebrospinalis. Rasterelektronenmikroskopie. Vergrößerung ×40. (Wiedergabe mit freundlicher Genehmigung von Reina MA, Machés F, López A, et al: The ultrastructure of the spinal arachnoid in humans and its impact on spinal ansthetics, cauda equina syndrome, and transitorisches neurologisches Syndrom. Tech Reg Anesth Pain Management. Juli 2008; 12(3):153-160.)
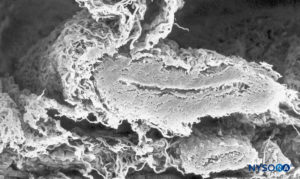
ABBILDUNG 38. Subarachnoidalgefäß und trabekuläre Arachnoidalschicht. Rasterelektronenmikroskopie. Vergrößerung ×120. (Wiedergabe mit freundlicher Genehmigung von Raj P: Textbook of Regional Anästhesie. Philadelphia: Churchill Livingstone; 2002.)
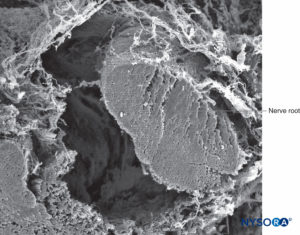
ABBILDUNG 39. Nervenwurzel und Arachnoidea. Rasterelektronenmikroskopie. Vergrößerung ×100. (Wiedergabe mit freundlicher Genehmigung von Torres LM: Lehrbuch der Anästhesie und Schmerzbehandlung. Aran Ed; 2001.)
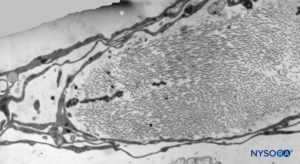
ABBILDUNG 40. Detail der trabekulären Arachnoidalschicht. Transmissionselektronenmikroskopie. Vergrößerung ×5000. (Wiedergegeben mit Genehmigung von Reina MA, Villanueva MC, López A: Aracnoides trabecular, piamadre espinal humana y anestesia subaracnoidea. Rev Arg Anestesiol. 2008;66:111–133.)
PIA MATER
Die Struktur der Pia mater umfasst eine Zellschicht und ein subpiales Kompartiment (Figuren 41 und 42). Die Zellschicht besteht aus flachen, überlappenden Pialzellen mit einem glatten und hellen Aussehen (Figure 43). Seine Dicke beträgt 3 bis 5 Pialzellen (10–15 μm) auf Markhöhe (Figuren 44 zu 46) und 2 bis 3 Zellen (3–4 μm) auf Nervenwurzelebene. Um die Pialzellen herum befindet sich amorphe Grundsubstanz, und die Zellen messen im Durchschnitt 0.5–1 μm.
Das subpiale Kompartiment weist große Mengen an Kollagenfasern, amorpher Grundsubstanz, Fibroblasten und eine kleine Anzahl Makrophagen und Blutgefäße auf. Das subpiale Kompartiment ist zwischen der pialen Zellschicht und einer Basalmembran in Kontakt mit Neurogliazellen eingeschlossen.
Das subpiale Kompartiment der unteren Brustwirbel hat eine Dicke von 130–200 μm; hier sind die Messabweichungen signifikanter als in der Pialzellschicht (vgl Figuren 41 und 42). Auf Höhe des Markkegels ist die Dicke der Pia mater auf 80–100 μm reduziert; seine Dicke nimmt im Ursprung der Cauda equina weiter auf nur noch 50–60 μm ab. Auf Nervenwurzelebene beträgt die Dicke des subpialen Kompartiments 10–12 μm.
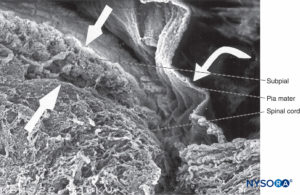
ABBILDUNG 41. Menschliche Pia mater und Rückenmark. Rasterelektronenmikroskopie. Vergrößerung ×70. (Wiedergabe mit freundlicher Genehmigung von Reina MA, De Leon Casasola O, et al: Ultrastructural Findings in Human Spinal Pia Mater in Relation zur Subarachnoidalanästhesie. Anesth Analg. 2004 May;98(5):1479-1485.)
Auf Höhe des Markkegels befinden sich auf der gesamten Oberfläche der Zellschicht der Pia mater Perforationen oder kreisförmige, eiförmige oder elliptische Fensterungen (Figuren 47 zu 49). Während die Größe dieser Fenster variiert, sind die meisten 12–15 μm lang und 4–8 μm breit. Auf der Ebene der Nervenwurzeln zeigt die Pia mater ähnliche Fensterungen, aber eine geringere Größe (1–4 μm) (Figure 50). Zahlreiche Makrophagen umgeben die Pialzellen. Die Makrophagen unterscheiden sich von Pialzellen dadurch, dass ihnen lange Zytoplasmafortsätze fehlen, die membrangebundene Einschlüsse und eine unterschiedliche Anzahl von Vakuolen enthalten, insbesondere in den peripheren Bereichen ihres Zytoplasmas. Die Makrophagen und andere Entzündungszellen, die in der Pia mater zu sehen sind, könnten von subpialen und subarachnoidalen Blutgefäßen oder von unreifen Piazellen als Ergebnis eines unbekannten Stimulus stammen. Die in der Pia mater gefundenen Fenestrationen scheinen mit der Migration einiger unreifer Piazellen als Teil einer Entzündungsreaktion verbunden zu sein.
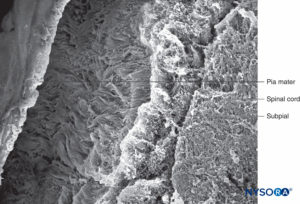
ABBILDUNG 42. Menschliche Pia mater und subpiales Kompartiment. Rasterelektronenmikroskopie. Vergrößerung ×100. (Wiedergabe mit freundlicher Genehmigung von Raj P: Textbook of Regional Anästhesie. Philadelphia: Churchill Livingstone; 2002.)

ABBILDUNG 43. Detail der Pia Mater. Rasterelektronenmikroskopie. Vergrößerung ×500. (Wiedergegeben mit Genehmigung von Reina MA, Wikinski J, De Andrés JA: Una rara complicación de la anestesia epidural y subaracnoidea. Tumores epidermoideos espinales iatrogénicos. Rev Arg Anestesiol. 2008;66:319-336.)
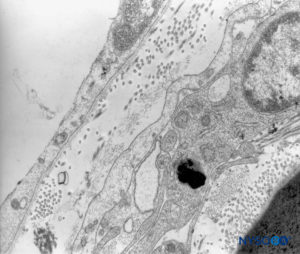
ABBILDUNG 44. Menschliche Pia Mater. Detail der Pialzellen. Transmissionselektronenmikroskopie. Vergrößerung ×12,000. (Wiedergegeben mit Genehmigung von Reina MA, Wikinski J, De Andrés JA: Una rara complicación de la anestesia epidural y subaracnoidea. Tumores epidermoideos espinales iatrogénicos. Rev Arg Anestesiol. 2008;66:319-336.)
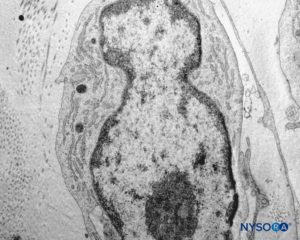
ABBILDUNG 45. Detail der Pialzellen. Transmissionselektronenmikroskopie. Vergrößerung ×12,000. (Wiedergegeben mit Genehmigung von Reina MA, Wikinski J, De Andrés JA: Una rara complicación de la anestesia epidural y subaracnoidea. Tumores epidermoideos espinales iatrogénicos. Rev Arg Anestesiol. 2008;66:319-336.)
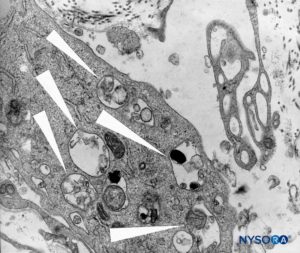
ABBILDUNG 46. Detail makrophagischer Zellen in spinaler Pia mater. Transmissionselektronenmikroskopie. Vergrößerung ×12,000. (Wiedergegeben mit Genehmigung von Reina MA, Wikinski J, De Andrés JA: Una rara complicación de la anestesia epidural y subaracnoidea. Tumores epidermoideos espinales iatrogénicos. Rev Arg Anestesiol. 2008;66:319-336.)
DURAL SAC BÄNDER
Der Epiduralraum enthält Fasergebilde, die den Duralsack kreuzen und im Wirbelkanal verankern. Diese Bindegewebsformationen werden als vordere, seitliche und hintere meningo-vertebrale Bänder bezeichnet (Figuren 51 und 52). Kompakter ist das vordere meningo-vertebrale Band, das den Duralsack mit dem hinteren Längsband der Wirbelsäule verbindet. Bei einigen Patienten können fibröse Lappen, die den Duralsack am hinteren Längsband fixieren, den vorderen Epiduralraum unvollständig teilen. Die vorderen Bänder erstrecken sich von C7 bis L5 mit kraniokaudaler Ausrichtung und erhalten eine transversale Ausrichtung auf Brusthöhe T8–9. Die Länge dieser Bänder variiert von etwa 0.5 bis 29 mm. Im Sakralkanal verdicken sich die Bänder zu einem perforierten medialen Septum, dem „anterioren Sakralband von Trolard“. Das laterale meningo-vertebrale Band und das posteriore („Giorda-lengo“) meningo-vertebrale Band sind dünner und beeinträchtigen nicht die Zirkulation von Flüssigkeiten, die in den Epiduralraum injiziert werden. Die „Plica mediana dorsalis“ ist eine längliche und diskontinuierliche Faserstruktur, die im mittleren Sagittalbereich entlang des hinteren Epiduralraums, insbesondere im Lendenbereich, zu finden ist.
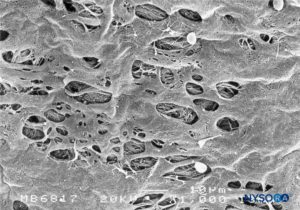
ABBILDUNG 47. Fenestrationen in der menschlichen Pia mater des Conus medullaris. Rasterelektronenmikroskopie. Vergrößerung ×1000. (Wiedergabe mit freundlicher Genehmigung von Reina MA, López García A, de Andrés JA: Anatomical description of a natural perforation present in the human lumbar pia mater. Rev Esp Anestesiol Reanim. 1998;45:4-7.)
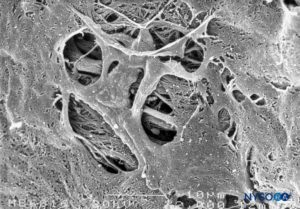
ABBILDUNG 48. Fenestrationen in der menschlichen Pia mater des Conus medullaris. Rasterelektronenmikroskopie. Vergrößerung ×2000. (Wiedergabe mit freundlicher Genehmigung von Reina MA, López García A, de Andrés JA: Anatomical description of a natural perforation present in the human lumbar pia mater. Rev Esp Anestesiol Reanim. 1998;45:4-7.)
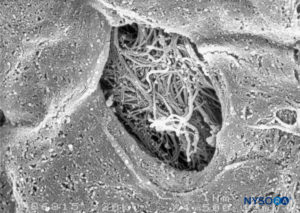
ABBILDUNG 49. Detail der Fensterung in der menschlichen Pia Mater. Rasterelektronenmikroskopie. Vergrößerung ×1500. (Wiedergabe mit freundlicher Genehmigung von Reina MA, López García A, de Andrés JA: Anatomical description of a natural perforation present in the human lumbar pia mater. Rev Esp Anestesiol Reanim. 1998;45:4-7.)
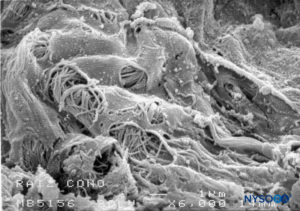
ABBILDUNG 50. Fenestrationen in der menschlichen Pia mater der Nervenwurzel. Rasterelektronenmikroskopie. Vergrößerung ×6000. (Wiedergegeben mit Genehmigung von Reina MA, Villanueva MC, López A: Aracnoides trabecular, piamadre espinal humana y anestesia subaracnoidea. Rev Arg Anestesiol. 2008;66:111–133.)
EPIDURALES FETT
Das Epiduralfett erstreckt sich lateral in Richtung der Stelle, an der sich die Gelenkfacetten und das Ligamentum flavum treffen. Zwischen den Wirbelbögen und den Foramina intervertebrale gelegen, umschließt Fett die Nervenwurzeln innerhalb der Duralhüllen, ohne jedoch an ihnen zu haften. Dies ermöglicht eine Verschiebung der Dura innerhalb des Wirbelkanals während Flexion/Extension. Epiduralfett haftet in der Mittellinie posterior durch einen Gefäßstiel an einem Punkt, an dem sich der rechte und der linke Teil des Ligamentum flavum treffen. Die Menge des posterioren Epiduralfetts nimmt kaudal von L1–2 nach L4–5 zu und kann 16–25 mm erreichen. Seine Breite nimmt auch in kraniokaudaler Richtung von 6 mm im L1–2-Zwischenraum auf 13 mm im L4–5-Zwischenraum zu. Der Stiel des hinteren Epiduralfetts entspricht topographisch der Plica mediana dorsalis.
Epidurale Fettablagerungen stehen in Kontakt mit der hinteren Oberfläche des Duralsacks und der Wirbelschicht, haften aber nur am Gefäßstiel. Im hinteren Bereich ist das Epiduralfett homogen und nicht durch fibröse Septen getrennt; lateral erscheint epidurales Fett geteilt. Manchmal erstreckt sich eine Septumebene zwischen dem Nervenwurzelausgang an der Vertebralleiste und dem hinteren Längsband. Von vorne betrachtet mündet die Dura mater in Höhe der Bandscheiben in den Wirbelkanal. In dieser vorderen Epiduralregion befinden sich die vorderen venösen Gefäße.
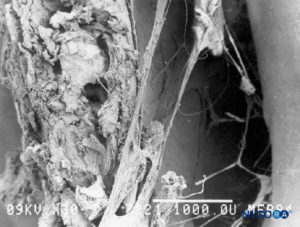
ABBILDUNG 51. Epiduralraum. Fasergebilde, die den Epiduralraum durchqueren. Rasterelektronenmikroskopie. Vergrößerung ×30. (Wiedergegeben mit Genehmigung von Reina MA, Pulido P, López A. El saco dural humano. Rev Arg Anestesiol. 2007;65:167-184.)
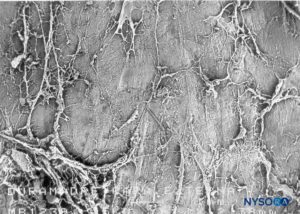
ABBILDUNG 51. Epiduralraum. Fasergebilde, die den Epiduralraum durchqueren. Rasterelektronenmikroskopie. Vergrößerung ×30. (Wiedergegeben mit Genehmigung von Reina MA, Pulido P, López A. El saco dural humano. Rev Arg Anestesiol. 2007;65:167-184.)
MERKMALE DES EPIDURALEN FETTS IN DEN HALS-, THORAKAL-, LENDEN- UND SAKRALREGIONEN
Die Verteilung des Epiduralfetts ist entlang des Spinalkanals variabel, neigt jedoch dazu, auf verschiedenen Wirbelebenen konsistenter zu sein. Zum Beispiel ist auf zervikaler Ebene Fettgewebe nicht vorhanden oder fast nicht vorhanden und bildet manchmal eine kleine hintere Ablagerung, die in axialen Schnitten der Magnetresonanztomographie (C7 bis T1) mit erhöhter Signalintensität in T1-gewichteten Sequenzen zu sehen ist. Epiduralfett wird im Allgemeinen nicht in den vorderen und seitlichen Regionen gefunden. Auf Brusthöhe bildet Epiduralfett ein breites hinteres Band mit „Einkerbungen“. Dieses Band ist um den Zwischenwirbelraum und um die Bandscheibe herum dicker und wird auf Höhe der Wirbelkörper und nahe der Basis der Spinalfortsätze jedes Wirbels dünner. In der mittleren oberen Thoraxregion (T1–7) folgt das epidurale Fett einem kontinuierlichen Muster mit deutlicheren Vertiefungen, während in der unteren Thoraxregion (T8–12) das epidurale Fett diskontinuierlich wird.
Auf lumbaler Ebene bleibt das Epiduralfett im vorderen und hinteren Epiduralraum getrennt. Das hintere Epiduralfett ist um die Bandscheiben von L3–4 und L4–5 stärker ausgeprägt. Bei manchen Patienten ist das hintere Epiduralfett kegelförmig, wobei die Spitze hinten liegt. Die Dicke des Epiduralfetts in der unteren Lendenzone nimmt etwa 32 % des Querschnittsdurchmessers des Wirbelkanals ein. Unterhalb von L4–5 endet der Duralsack und der Sakralkanal beginnt. Hier sind Nervenwurzeln von Duralhüllen umhüllt, und epidurales Fett ist der Hauptbestandteil innerhalb der Hüllen.
Die Morphologie und Verteilung des Epiduralfetts kann unter pathologischen Bedingungen verändert sein. Die epidurale Lipomatose beispielsweise ist durch eine Zunahme des epiduralen Fettvolumens gekennzeichnet. Übermäßige Fettablagerungen um den Duralsack herum können eine Kompression des Rückenmarks oder der Nervenwurzeln verursachen, was zu neurologischen Symptomen führt. Bei der Kyphoskoliose ist das Epiduralfett asymmetrisch verteilt und das Fettgewebe überwiegt im konkaven Teil der Krümmung, während das Rückenmark gegen den Wirbelbogen verschoben ist. Bei Patienten mit Spinalkanalstenose fehlt epidurales Fett charakteristischerweise oder ist um die stenotische Zone herum deutlich reduziert.
EPIDURALES FETT UND PHARMAKOKINETIK VON EPDIURALEN INJEKTEN
Die Verteilung des Epiduralfetts im lumbalen Wirbelkanal ist ungleichmäßig, wobei es in der dorsalen Region häufiger vorkommt als in den ventralen und lateralen Regionen. Die Gesamtmenge, Verteilung und Morphologie von Fett im Epiduralraum und in den Nervenwurzelmanschetten beeinflussen die Diffusion von Substanzen durch diese Kompartimente.
Veränderungen in der Menge an epiduralem Fett während pathologischer Prozesse können die Resorption von Arzneimitteln während einer epiduralen Blockade verändern. Aber auch ohne pathologische Prozesse könnten lokale Schwankungen der Fettmenge im lumbalen Spinalkanal die Arzneimittelkinetik verändern. Es ist möglich, dass Schwankungen im Abstand zwischen Fett und benachbarten Nervengeweben die Disposition der injizierten Arzneimittel und die Kinetik der lipophilen Arzneimittel beeinflussen. Gegenwärtig ist jedoch der Einfluss der Ultrastruktur von Epidural- und Nervenwurzelmanschetten auf die Arzneimittelkinetik während der epiduralen Injektion unklar.
SUBDURALER RAUM
Im Gegensatz zur klassischen Beschreibung eines „subduralen Raums“ zwischen der Dura mater und der Arachnoidea dorsalis haben Studien das Vorhandensein eines festen, aber zarten Gewebes gezeigt, das aus spezialisierten Neurothelzellen besteht (Figure 53). Neurothelzellen werden auch als Durarandzellen bezeichnet. Diese länglichen, spindelförmigen Zellen mit verzweigten Verlängerungen sind zerbrechlich und kaum miteinander verbunden (Figuren 54 und 55). Interzelluläre Verbindungen zwischen Neurothelzellen sind am anfälligsten für Risse, und neben zerrissenen Neurothelzellen können Zellfragmente zu sehen sein (Figuren 56 und 57). Wenn entlang des subduralen Kompartiments ein Riss auftritt, verschmelzen kleine Risse zu größeren. Schwache Kohäsionskräfte zwischen Neurothelzellen und das Fehlen von Kollagenfasern erleichtern die Aufweitung einer Fissur, wodurch der Eindruck eines subduralen Raums entsteht. Der klassische Subduralraum scheint also ein iatrogenes Artefakt zu sein.
Die Untersuchung der Struktur des subduralen Kompartiments kann Aufschluss über den Ursprung von subduralen Hämatomen des Schädels und der Wirbelsäule geben, die mit einer Hypotonie des Liquor cerebrospinalis verbunden sind.
Eine subduralanästhetische Blockade, die durch eine versehentliche teilweise oder vollständige Injektion eines Lokalanästhetikums zwischen Dura und Arachnoidea verursacht wird, führt zu einer höchst unvorhersehbaren Spinal- oder Epiduralanästhesie und zu Komplikationen aufgrund einer unerwarteten hochgradigen Blockade. Die Dissektion der schwachen interzellulären Verbindungen zwischen den Neurothelzellen kann dazu führen, dass sich injizierte Flüssigkeiten im subduralen Raum ansammeln. Das Ausmaß des subduralen Blocks ist unvorhersehbar, da es von der Menge des injizierten Lokalanästhetikums und der Art der Dissektion (kranial oder zirkulär) abhängt. Wenn die Dissektion hauptsächlich kopfwärts erfolgt, können nur wenige Milliliter Anästhesielösung kardiorespiratorische Symptome blockieren.
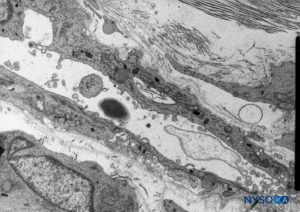
ABBILDUNG 53. Neurothelzellen im subduralen Kompartiment. Transmissionselektronenmikroskopie. Vergrößerung ×5000. (Wiedergegeben mit Genehmigung von Reina MA, De León Casasola OA, et al: The origin of the spinal subdural space. Ultrastructurefinding. Anesth Analg. 2002 Apr;94(4):991-995.)

ABBILDUNG 54. Neurothelzellen im subduralen Kompartiment. Rasterelektronenmikroskopie. Vergrößerung ×3000. (Wiedergegeben mit Genehmigung von Reina MA, De León Casasola OA, et al: The origin of the spinal subdural space. Ultrastructurefinding. Anesth Analg. 2002 Apr;94(4):991-995.)
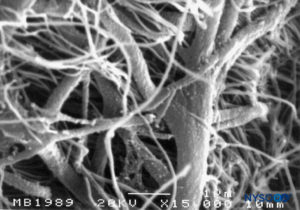
ABBILDUNG 54. Neurothelzellen im subduralen Kompartiment. Rasterelektronenmikroskopie. Vergrößerung ×3000. (Wiedergegeben mit Genehmigung von Reina MA, De León Casasola OA, et al: The origin of the spinal subdural space. Ultrastructurefinding. Anesth Analg. 2002 Apr;94(4):991-995.)
NERVENWURZEL MANSCHETTEN
Bilaterale Vorsprünge des Duralsacks (Materie) auf die Nervenwurzeln bilden die Nervenwurzelmanschetten oder Duralmanschetten (Figure 58). Laterale Verlängerungen der Dura mater und der Arachnoidea umgeben die Nervenwurzeln, wenn sie den Wirbelkanal verlassen. Der Duralsack kann um die Nervenwurzel herum eine gewisse Menge Liquor cerebrospinalis enthalten. Nervenwurzelmanschetten (Ärmel) haben interne zelluläre und externe fibrilläre Komponenten (Figure 59). Leptomeningeale Zellen, ähnlich den Arachnoidal- oder Pialzellen, bilden die zelluläre Komponente der Wurzelmanschetten. Diese Zellen sind länglich, breiter um den Kern herum, geschichtet und längs zur Nervenwurzelachse orientiert (Figure 60).
Bei der Präganglion Ebeneist die zelluläre Komponente einer Wurzelmanschette 5.8–13 μm dick. Diese Zellen haben zytoplasmatische Verlängerungen, die in benachbarte Zellen eindringen und wenig extrazellulären Raum lassen. Verbindungen zwischen Zellmembranen sind vom Typ Desmosome und haben Tight Junctions (Figure 61). Zellen enthalten Mitochondrien in ihrem Zytoplasma und im rauhen endoplasmatischen Retikulum. Jede Zelle ist an beiden Enden etwa 0.15–0.8 μm dick und am Kern 2.2–4.9 μm dick. Die Zellkomponente ist in zwei konzentrischen Schichten angeordnet, die durch Kollagenfasern voneinander getrennt sind.
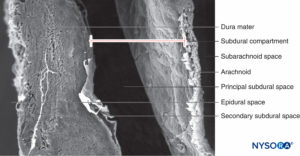
ABBILDUNG 56. Subduralraum des Menschen in den Lendenmeningen. Rasterelektronenmikroskopie. Vergrößerung ×180. (Wiedergabe mit freundlicher Genehmigung von Reina MA, López A, De Andrés JA, Villanueva MC, Cortés L: Is the subdural space exist? Rev Esp Anestesiol Reanim. 1998 Nov;45(9):367-376.)
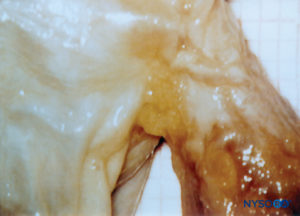
ABBILDUNG 58. Menschliche Nervenwurzelmanschette. (Wiedergabe mit freundlicher Genehmigung von Reina MA, Villanueva MC, López A, et al: Fat inside the dural shell of lumbar nerve roots in humans. Rev Esp Anestesiol Reanim. 2007 May;54(5):297-301.)
Auf der Postganglion-Ebene hat die zelluläre Komponente 9–14 einzellige konzentrische Schichten und misst 18–50 μm. Ihre Vereinigungen sind vom Desmosom-Typ. Die Morphologie der zellulären Komponente auf der Ganglionebene zeigt Übergangsveränderungen, während viele der auf der Postganglionebene gezeigten Eigenschaften beibehalten werden. Die Zellkomponente besteht aus 25–30 konzentrischen einzelligen Plättchen und hat eine Dicke von 55–60 μm. Ultrastrukturelle Aspekte der zellulären Komponente auf Prä-, Post- und Ganglionebene sind ähnlich. Die Zellen haben ein raues endoplasmatisches Retikulum, das weit verbreitet ist, und einige enthalten auch große Vakuolen (0.1 μm), die fast die Hälfte des zytoplasmatischen Raums einnehmen. Eine membranähnliche Struktur in ihrem Zytoplasma kann an der Produktion von Vesikeln (0.05–0.07 μm) beteiligt sein, die für die Pinozytose benötigt werden. Kollagenfasern zusammen mit myelinisierten und unmyelinisierten Axonen sind auf der Innenseite der Zellebene zu sehen und sind Teil der endoneuralen Fibrillenstruktur. Spezialisierte Membranvereinigungen zwischen Zellen auf Prä-, Post- und Ganglionebene sorgen für eine Barrierewirkung, die den Durchgang von Substanzen aus dem Epiduralraum zu den Nervenaxonen begrenzt.
Die fibrilläre Komponente befindet sich im äußeren Teil der Wurzelmanschette und hat eine Dicke von 100–150 μm (Figure 62). Es besteht hauptsächlich aus Kollagenfasern, die in konzentrischen Schichten mit wenigen elastischen Fasern angeordnet sind. Eine große Anzahl von Adipozyten trennt Durallamina in Gruppen von drei bis fünf konzentrischen Schichten (Figure 63). Rasterelektronenmikroskopie zeigt Adipozyten (Figure 63) erstreckt sich vom Duralsack bis zu den Spinalganglien. Adipozyten können gefunden werden, die aus dem Inneren der Wand herausragen, die von der fibrillären Komponente gebildet wird, aus der äußeren epiduralen Oberfläche der Wurzelmanschette (Figuren 64 und 65).Der fibrilläre Anteil im Duralsack enthält etwa 80 Duralschichten mit in verschiedene Richtungen orientierten Kollagenfasern und wenigen elastischen Fasern. Seine Dicke variiert zwischen 270 und 350 μm auf Lumbalebene. Adipozyten werden nicht innerhalb der Dicke des Duralsacks gefunden.
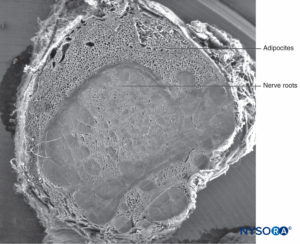
ABBILDUNG 59. Menschliche Nervenwurzelmanschette. Rasterelektronenmikroskopie. Vergrößerung ×12. (Wiedergegeben mit Genehmigung von Reina MA, Villanueva MC, Machés F, et al: Ultrastructure of human spinal nerve root cuff in lumbar spine. Anesth Analg. 2008 Jan;106(1): 339-344.)
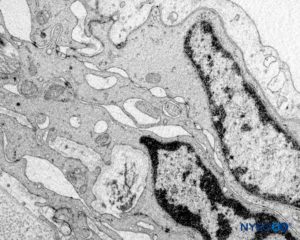
ABBILDUNG 60. Menschliche Nervenwurzelmanschette. Detail der Übergangszellbarriere. Transmissionselektronenmikroskopie. Vergrößerung ×20,000. (Wiedergegeben mit Genehmigung von Reina MA, Villanueva MC, Machés F, et al: Ultrastructure of human spinal nerve root cuff in lumbar spine. Anesth Analg. 2008 Jan;106(1):339-344.)
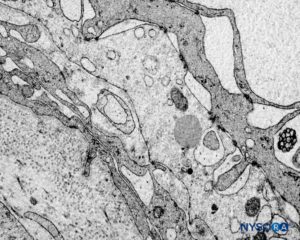
ABBILDUNG 61. Menschliche Nervenwurzelmanschette. Detail der Übergangszellbarriere. Transmissionselektronenmikroskopie. Vergrößerung ×3000. (Wiedergegeben mit Genehmigung von Reina MA, Machés F, Pulido P, López A, De Andrés JA. Ultrastructure of Human Spinal Meninges. In: Aldrete A. Arachnoiditis, Mexico: Alfil Ed; 2010. S. 29-46.)
Schwankungen der Duraldicke entlang des Duralsacks und Unterschiede in Bezug auf die externe fibrilläre Komponente ändern nicht die Barrierewirkung, die ausschließlich in der Verantwortung der zellulären Komponente liegt.
Die Rasterelektronenmikroskopie hat gezeigt, dass Adipozyten 50–70 μm messen und denen ähneln, die in peripheren Nervenproben des Ischiasnervs gefunden werden. Die Tatsache, dass Adipozyten kleiner erscheinen und keine Kugelform haben, ist höchstwahrscheinlich auf einen Fettverlust aus ihren Vakuolen während der Probenvorbereitung zurückzuführen. Fett in Wurzelmanschetten bedeckt Gruppen von Wurzelaxonen, obwohl Adipozyten nicht gesehen werden, wie sie einzelne Axone umschließen. Dieses Fett nimmt entweder teilweise oder vollständig die Dicke der fibrillären Komponente der Wurzelmanschetten ein.
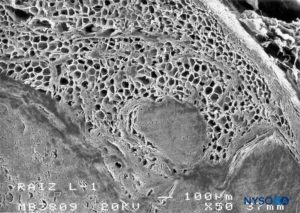
ABBILDUNG 62. Menschliche Nervenwurzelmanschette. Detail des Fettgewebes in der Dicke der Nervenwurzelmanschette. Rasterelektronenmikroskopie. Vergrößerung ×50. (Wiedergabe mit freundlicher Genehmigung von Reina MA, Villanueva MC, López A, et al: Fat inside the dural shell of lumbar nerve roots in humans. Rev Esp Anestesiol Reanim. 2007 May;54(5):297-301.)
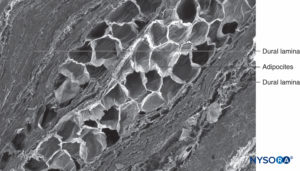
ABBILDUNG 63. Menschliche Nervenwurzelmanschette. Detail der Durallamina in der Dicke der Nervenwurzelmanschette. Rasterelektronenmikroskopie. Vergrößerung ×150. (Wiedergegeben mit Genehmigung von Reina MA, Villanueva MC, Machés F, et al: Ultrastructure of human spinal nerve root cuff in lumbar spine. Anesth Analg. 2008 Jan;106(1):339-344.)

ABBILDUNG 64. Menschliche Nervenwurzelmanschette. Adipozyten in der Nervenwurzelmanschette. Rasterelektronenmikroskopie. Vergrößerung ×400. (Wiedergegeben mit Genehmigung von Reina MA, Villanueva MC, Machés F, et al: Ultrastructure of human spinal nerve root cuff in lumbar spine. Anesth Analg. 2008 Jan;106(1):339-344.)
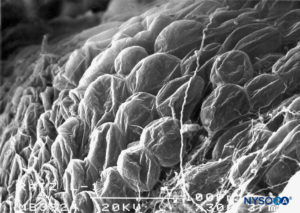
ABBILDUNG 65. Adipozyten auf der epiduralen Oberfläche der Nervenwurzelmanschette. Rasterelektronenmikroskopie. Vergrößerung ×300. (Wiedergabe mit freundlicher Genehmigung von Reina MA, Villanueva MC, López A, et al: Fat inside the dural shell of lumbar nerve roots in humans. Rev Esp Anestesiol Reanim. 2007 May;54(5):297-301.)
FETTGEWEBE IN WURZELMANSCHETTEN UND DROGENKINETIK
Fettgewebe findet sich im Epiduralraum und in den Nervenwurzelmanschetten. Fett in Nervenmanschetten steht in direktem Kontakt mit Nervenwurzelaxonen und kann eine Rolle bei der Kinetik von lipophilen Substanzen spielen, die in der Nähe der Nervenwurzeln injiziert werden. Der kleine Raum innerhalb der Wurzelmanschetten und die große Menge an Medikamenten, die im Falle einer Injektion in die Manschette verfügbar sind, können die neuralen Elemente einer hohen Konzentration von Lokalanästhetikum sowie einer retrograden Ausbreitung in Richtung des Subarachnoidalraums aussetzen.
ZUSAMMENFASSUNG
Dieses Kapitel skizzierte die anatomischen Merkmale der neuraxialen Meningen und verwandter Strukturen und erörterte ihre möglichen klinischen Auswirkungen.
REFERENZEN
- Reina MA, López A, De Andrés JA: Variation der menschlichen Dura mater Dicke [auf Spanisch]. Rev. Esp Anestesiol Reanim 1999;46:344–349.
- Reina MA, Pulido P, López A: El saco dural humano. Rev. Arg Anestesiol 2007; 65:167–184.
- Reina MA, López A, Dittmann M, De Andrés JA: Struktur der menschlichen Dura Mater-Dicke durch Rasterelektronenmikroskopie [auf Spanisch]. Rev. Esp Anestesiol Reanim 1996;43:135–137.
- Reina MA, Dittmann M, López A, van Zundert A: Neue Perspektiven in der mikroskopischen Struktur der menschlichen Dura mater in der dorso-lumbalen Region. Reg Anesth 1997;22:161–166.
- Dittmann M, Reina MA, López A: Neue Ergebnisse bei der Darstellung der Dura mater spinalis mittles rasterelektronenmikroskopie. Anaesthesist 1998;47:409–413.
- Reina MA, López A, Dittmann M, De Andrés JA: Äußere und innere Oberfläche der menschlichen Dura Mater durch Rasterelektronenmikroskopie [auf Spanisch]. Rev. Esp Anestesiol Reanim 1996;43:130–134.
- Reina MA, Villanueva MC, López A: Aracnoides trabecular, piamadre espinal humana y anestesia subaracnoidea. Rev. Arg Anestesiol 2008;66: 111–133.
- Reina MA, De León Casasola OA, López A, De Andrés JA, Mora M, Fernández A: Der Ursprung des spinalen Subduralraums. Ultrastrukturbefund. Anesth Analg 2002;94:991–995.
- Reina MA, López A, De Andrés JA, Villanueva MC, Cortés L: ¿Existiert subduraler Raum? [in Spanisch]. Rev. Esp Anestesiol Reanim 1998;45:367–376.
- Reina MA, De León Casasola OA, López A, De Andrés JA, Martín S, Mora M: Eine In-vitro-Studie zu Duralläsionen, die durch 25-Gauge-Quincke- und Whitacre-Nadeln erzeugt wurden, bewertet durch Rasterelektronenmikroskopie. Reg Anesth Pain Med 2000;25:393–402.
- Reina MA, López A, Badorrey V, De Andrés JA, Martín S: Dura-Arachnoidal-Läsionen, die durch 22G Quincke-Spinalnadeln während einer Lumbalpunktion erzeugt werden. J Neurol Neurosurg Psychiatry 2004;75:893–897.
- Reina MA, López-García A, de Andrés-Ibáñez JA, et al: Elektronenmikroskopie der Läsionen, die in der menschlichen Dura Mater durch abgeschrägte Quincke- und Whitacre-Nadeln erzeugt werden [auf Spanisch]. Rev. Esp Anestesiol Reanim 1997;44:56–61.
- Jokinen MJ, Pitkänen MT, Lehtonen E: Deformierte Spinalnadelspitzen und damit verbundene Duralperforationen, die durch Rasterelektronenmikroskopie untersucht wurden. Acta Anaesthesiol Scand 1996;40:687–690.
- Puolakka R, Andersson LC, Rosenberg PH: Mikroskopische Analyse von drei verschiedenen Spinalnadelspitzen nach experimenteller Subarachnoidalpunktion. Reg Anesth Pain Med 2000;25:163–169.
- Benham M: Spinalnadelschaden während der klinischen Routinepraxis. Anästhesie 1996;51:843–845.
- Reina MA, López A, Manzarbeitia F, Amador V, Goxencia I, Olmedilla MC: Von Spinalnadeln getragene Hautfragmente in Leichen [auf Spanisch]. Rev. Esp Anestesiol Reanim 1995;42:383–385.
- Reina MA, López-García A, Dittmann M, de Andrés JA, Blázquez MG: Iatrogene spinale Epidermoidtumoren. Eine Spätkomplikation der Spinalpunktion [auf Spanisch]. Rev. Esp Anestesiol Reanim 1996;43:142–146.
- Reina MA, Wikinski J, De Andrés JA: Una rara complicación de la anestesia epidural y subaracnoidea. Tumores epidermoideos espinales iatrogenicos. Rev. Arg Anestesiol 2008; 66:319–336.
- Reina MA, Castedo J, López A: Cefalea pospunción dural: Ultraestructura de las lesiones durales y agujas espinales usadas en las punciones lumbares. Rev. Arg Anestesiol 2008;66:6–26.
- Reina MA, López A, De Andrés JA: Hypothese über die anatomischen Grundlagen des Cauda-Equin-Syndroms und des transitorischen radikulären Irritationssyndroms nach Spinalanästhesie [auf Spanisch]. Rev. Esp Anestesiol Reanim 1999;46:99–105.
- Reina MA, Machés F, López A, De Andrés JA: Die Ultrastruktur der spinalen Arachnoidea beim Menschen und ihre Auswirkungen auf die Spinalanästhesie, das Cauda-Equina-Syndrom und das transiente neurologische Síndrom. Tech Reg Anesth Pain Management 2008;12:153–160.
- Reina MA, De Leon Casasola O, Villanueva MC, López A, Maches F, De Andrés JA: Ultrastrukturelle Befunde bei der menschlichen spinalen Pia mater in Bezug auf die Subarachnoidalanästhesie. Anesth Analg 2004;98:1479–1485.
- Reina MA, López García A, de Andrés JA: Anatomische Beschreibung einer natürlichen Perforation in der menschlichen lumbalen Pia mater [auf Spanisch]. Rev. Esp Anestesiol Reanim 1998;45:4–7.
- Luyendijk W: Die Plica mediana dorsalis der Dura mater und ihre Beziehung zur lumbalen Peridurographie. Neuroradiology 1976;11:147–149.
- Blomberg R: Das dorsomediane Bindegewebsband im lumbalen Epiduralraum des Menschen: Eine anatomische Studie mittels Epiduroskopie bei Autopsiefällen. Anesth Analg 1986;65:747–752.
- Reina MA, Pulido P, Castedo J, Villanueva MC, López A, De Sola R: Eigenschaften und Verteilung des Epiduralfetts [auf Spanisch]. Rev. Esp Anestesiol Reanim 2006;53: 315–324.
- Reina MA, Pulido P, Castedo J, Villanueva MC, López A, De Andrés JA: Das Epiduralfett bei verschiedenen Erkrankungen. Beiträge der Magnetresonanztomographie und mögliche Implikationen in der Epidural- und Spinalanästhesie [auf Spanisch]. Rev. Esp Anestesiol Reanim 2007;54:173–178.
- Reina MA, López A, Benito-Leon J, Pulido P, María F: Intrakraneales und spinales Hämatom, eine seltene Komplikation der Epidural- und Spinalanästhesie [auf Spanisch]. Rev. Esp Anestesiol Reanim 2004;51:28–39.
- Reina MA, López A, Maches F, De Andrés JA: Ursprung des subduralen Hämatoms der Wirbelsäule [auf Spanisch]. Rev. Esp Anestesiol Reanim 2004;51:240–246.
- Reina MA, Villanueva MC, Machés F, Carrera A, López A, De Andrés JA: Ultrastruktur der menschlichen Spinalnervenwurzelmanschette in der Lendenwirbelsäule. Anesth Analg 2008;106:339–344.
- Reina MA, De Andrés J, Machés F, López A: Neue Erkenntnisse über menschliche Spinalwurzelmanschetten. In van Zundert A: Höhepunkte in Schmerz, Therapie und Regionalanästhesie, 16. Aufl. Permanyer, 2007, S. 163–173.
- Reina MA, Villanueva MC, López A, De Andrés JA: Fett in der Duralscheide der Lendennervenwurzeln beim Menschen [auf Spanisch]. Rev. Esp Anestesiol Reanim 2007;54:169–172.
- Reina MA, López A, De Andrés JA: Fettgewebe in peripheren Nerven. Untersuchung des menschlichen Ischiasnervs [auf Spanisch]. Rev. Esp Anestesiol Reanim 2002;49:397–402.
- Reina MA, Machés F, Pulido P, López A, De Andrés JA: Ultrastructure of human spinal meninges. In Aldrete A: Arachnoiditis. Alfil Ed, 2010, S. 29–246.
- Reina MA. Atlas der funktionellen Anatomie für Regionalanästhesie und Schmerzmedizin. Menschliche Struktur, Ultrastruktur und 3D-Rekonstruktionsbilder. Springer, 2015, S. 705–748.
- Reina MA, De Andrés JA, López A: Subarachnoidal- und Epiduralanästhesie. In Raj P: Lehrbuch der Regionalanästhesie. Churchill Livingston, 2002, S. 307–324.
- Reina MA, De Andrés JA, López García A: Anatomie bei Wirbelsäulenblockade [auf Spanisch]. In Torres LM (Hrsg.). Lehrbuch der Anästhesie und Schmerztherapie. Aran Ed, 2001, S. 1135–1155.
- Selander D, Sjöstrand J: Längsausbreitung intraneural injizierter Lokalanästhetika. Eine experimentelle Studie der anfänglichen neuralen Verteilung nach intraneuralen Injektionen. Acta Anaesthesiol Scand 1978;22:622–634.
NYSORA-Tipps
- Die Form des Duralsacks ist zylindrisch, und seine Dicke ist variabel.
- Die Dura mater ist durchlässig und nimmt 90 % der Dicke des Duralsacks ein.
- Die Arachnoidea ist semipermeabel und regelt den Stofftransport.
- Dura-Arachnoidal-Läsionen können sich je nach Art der Spinalnadel unterscheiden.
- Bleistiftspitzennadeln erzeugen eine destruktivere Läsion, während Schneidnadeln eine U-förmige Läsion erzeugen, obwohl die Größe beider ähnlich ist.
- Die trabekuläre Arachnoidea bedeckt die Nervenwurzeln und bildet Arachnoidalscheiden.
- Pia mater hat Fensterungen auf Höhe des Markkegels.
- Die epidurale Fettverteilung ist entlang des Spinalkanals variabel, aber auf verschiedenen Wirbelebenen konsistent.
- Das epidurale Fettvolumen ist bei epiduraler Lipomatose erhöht, bei Kyphoskoliose asymmetrisch verteilt und bei Stenose nicht vorhanden.
- Der „Subduralraum“ wird tatsächlich von feinem Gewebe eingenommen, das aus spezialisierten Neurothelzellen besteht. Das Aufreißen des subduralen Kompartiments führt zu dem, was wir als subduralen Raum kennen.
- In Wurzelmanschetten gibt es eine zelluläre Komponente, die die Diffusion von Substanzen steuert. Wurzelmanschetten enthalten in ihrer Dicke auch eine große Anzahl von Adipozyten.