J. Sudharma Ranasinghe, Elyad Davidson und David J. Birnbach
EINFÜHRUNG
In den letzten Jahren wurden regionale Anästhesietechniken für Operationen, Geburtshilfe, und postoperative Schmerztherapie werden immer häufiger eingesetzt. Die kombinierte spinal-epidurale (CSE) Technik, eine vergleichsweise neue Wahl der Anästhesie, umfasst eine anfängliche Subarachnoidalinjektion, gefolgt von der Platzierung eines Epiduralkatheters und der anschließenden Verabreichung von Epiduralmedikamenten. Dies ermöglicht eine schnelle Linderung von Schmerzen oder die Einleitung einer Regionalanästhesie durch das schnelle Einsetzen der Spinalmedikamente und die anschließende Verabreichung von Medikamenten für eine verlängerte Anästhesie. Darüber hinaus kann über längere Zeiträume eine postoperative Analgesie über den Epiduralkatheter verabreicht werden. Klinische Studien haben gezeigt, dass die CSE-Technik ebenso schnell wie die Single-Shot-Subarachnoidalblockade und mit Vorteilen gegenüber der konventionellen Epiduralblockade hervorragende OP-Bedingungen bietet. Der Vorteil liegt darin, dass die CSE-Anästhesie Vorteile von beiden bietet Spinale und Epiduralanästhesie.
Obwohl die CSE-Technik in den letzten zwei Jahrzehnten immer beliebter geworden ist, handelt es sich um eine komplexere Technik, die ein umfassendes Verständnis der Epidural- und Epiduralanästhesie erfordert Wirbelsäulenphysiologie und Pharmakologie. Dieses Kapitel behandelt die technischen Aspekte, Vorteile, möglichen Komplikationen und Einschränkungen der CSE-Technik für Operationen, postoperative Schmerzbehandlung und Wehen Analgesie.
KLINISCHE ANWENDUNGEN VON CSE
Die Ergebnisse einer von Blanshard und Cook durchgeführten Umfrage zeigten große Unterschiede bei der Verwendung und Praxis der CSE-Anästhesie unter erfahrenen Anästhesisten. Dies spiegelt die Besorgnis über die Häufigkeit von CSE-bedingten Komplikationen, Kontroversen über die Technik und das Potenzial für höhere Ausfallraten bei der CSE-Technik wider im Vergleich zu einzelnen Wirbelsäulen- bzw anderes Anästhetikum Techniken.
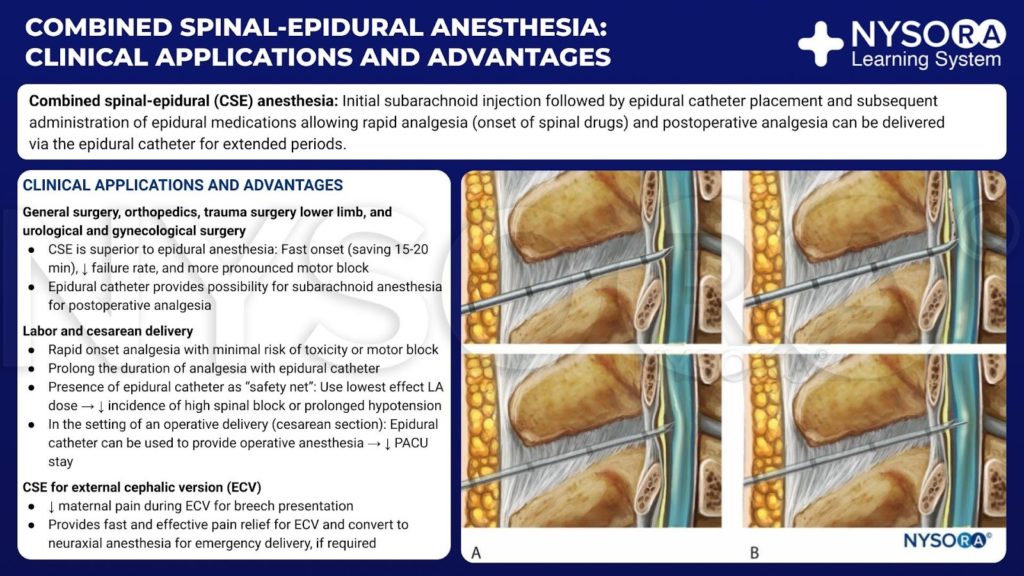
Aus dem Kompendium der Regionalanästhesie: Infografik Klinische Anwendungen und Vorteile der kombinierten Spinal-Epiduralanästhesie.
Allgemeine Chirurgie
Die CSE-Technik wurde in der medizinischen Literatur zur Verwendung in der allgemeinen Chirurgie, Orthopädie, Unfallchirurgie einer unteren Extremität und urologischen und gynäkologischen Chirurgie beschrieben. Klinische Studien haben gezeigt, dass die CSE-Technik so schnell wie bei einem Single-Shot-Subarachnoidalblock hervorragende chirurgische Bedingungen bietet, die besser sind als bei einem Epiduralblock allein. Mit der CSE-Technik wird die chirurgische Anästhesie schnell etabliert und spart 15–20 Minuten im Vergleich zur Epiduralanästhesie. Darüber hinaus bietet die Epiduralkatheterisierung die Möglichkeit, die Subarachnoidalanästhesie zu ergänzen, die allein unzureichend sein kann. Dies wurde kürzlich von Mane et al. veranschaulicht, die eine Fallserie einer laparoskopischen Appendektomie präsentierten, die erfolgreich unter CSE-Anästhesie durchgeführt wurde. Die CSE-Anästhesie in ihrer Serie wurde unter Verwendung separater Nadeln an zwei verschiedenen Zwischenräumen durchgeführt. Spinalanästhesie wurde am L2-L3-Zwischenraum mit 2 ml 0.5 % (10 mg) hyperbarem Bupivacain, gemischt mit 25 μg Fentanyl, durchgeführt. Der Epiduralkatheter wurde zur Ergänzung der Spinalanästhesie und zur postoperativen Schmerzlinderung am T10–T11-Zwischenraum eingeführt. In einem geburtshilflichen Artikel wurde auch beobachtet, dass verschiedene Nadeln bei der Durchführung der CSE-Technik in unterschiedlichen Kombinationen verwendet werden können und für verschiedene Patienten und Situationen unterschiedliche Vor- und Nachteile haben können. Dies wird weiter in dem Kapitel diskutiert.
Wehen Analgesie
Die CSE-Technik wird in der geburtshilflichen Praxis häufig verwendet, um eine optimale Analgesie für Gebärende bereitzustellen. Es bietet eine wirksame, schnell einsetzende Analgesie mit minimalem Risiko einer Toxizität oder Motorblockade. Darüber hinaus bietet diese Technik die Möglichkeit, die Dauer der Analgesie, wie sie oft während der Wehen erforderlich ist, durch die Verwendung eines Epiduralkatheters zu verlängern. Sollte außerdem eine operative Entbindung erforderlich werden, kann derselbe Epiduralkatheter verwendet werden, um eine operative Anästhesie bereitzustellen. Der Beginn der Spinalanalgesie ist fast sofort und die Dauer beträgt zwischen 2 und 3 Stunden, je nachdem, welches Mittel oder welche Mittel gewählt werden. Es wurde jedoch festgestellt, dass die Dauer der Spinalanalgesie verringert ist, wenn sie einer Frau in fortgeschrittenen Wehen verabreicht wird, im Vergleich zu einer Frau in frühen Wehen. Gebärende Patientinnen können mit der CSE-Anästhesie zufriedener sein als mit der Standard-Epiduralanästhesie, vielleicht aufgrund eines größeren Gefühls der Selbstkontrolle. Die ursprünglichen Beschreibungen der Analgesie der Wirbelsäulenarbeit verwendeten Sufentanil oder Fentanyl, aber die Zugabe von isobarem Bupivacain zum Opioid erzeugt eine größere Dichte der sensorischen Blockade, während die motorische Blockade immer noch minimiert wird. Ursprünglich wurden 25 μg Fentanyl oder 10 μg Sufentanil befürwortet, spätere Studien legten jedoch die Verwendung geringerer Dosen von Opioiden in Kombination mit einem Lokalanästhetikum nahe.
Beispielsweise verwenden viele Kliniker jetzt routinemäßig 10–15 μg intrathekales Fentanyl. Mehrere Studien legen nahe, dass Ropivacain und Levobupivacain das intrathekale Bupivacain ersetzen können, insbesondere wenn es zu einem Opioid hinzugefügt wird, um eine Wehenschmerzlinderung zu erzielen. Die CSE-Technik hat auch vielen Frauen, die eine neuraxiale Analgesie erhalten, das Gehen ermöglicht, obwohl das Gehen auch mit anderen Techniken möglich sein kann. Wilson et al. zeigten, dass signifikant mehr Frauen mit CSE-Anästhesie über einen längeren Zeitraum eine überlegene Beinkraft aufrechterhielten als mit einer niedrig dosierten Standard-Epiduralanästhesie. Zusätzlich zu dem Vorteil des schnellen Einsetzens der Schmerzlinderung kann die CSE-Technik das Auftreten mehrerer potenzieller Probleme reduzieren, die mit der konventionellen Epiduraltechnik verbunden sind, einschließlich unvollständiger (fleckiger) Blockade, motorischer Blockade und schlechter sakraler Ausbreitung. Ein weiterer potenzieller Vorteil der CSE-Technik besteht darin, dass sie mit einer signifikanten Verkürzung der Dauer der ersten Wehenphase bei Erstgebärenden verbunden sein kann. Laut einer neueren Studie von Pascual-Ramirez et al. verkürzte die CSE-Technik im Vergleich zur konventionellen Epiduralanalgesie jedoch nicht die Gesamtdauer der Wehen, reduzierte jedoch den Bedarf an Lokalanästhesie und die motorische Schwäche. Die Reduzierung der motorischen Blockade ist für Gebärende vorteilhaft, auch für diejenigen, die nicht gehen werden.
Kombinierte Spinal-Epidural-Technik für Kaiserschnittgeburten
Die CSE-Technik, die erstmals 1984 als Option für die Kaiserschnittentbindung beschrieben wurde, hat in letzter Zeit dramatisch an Popularität gewonnen. Der Vorteil dieser Technik besteht darin, dass sie einen schnellen Beginn einer dichten chirurgischen Anästhesie ermöglicht und gleichzeitig die Möglichkeit bietet, die Blockade mit einem Epiduralkatheter zu verlängern. Da die Blockade jederzeit ergänzt werden kann, ermöglicht die CSE-Technik außerdem die anfängliche Anwendung geringerer Dosen von spinalen Lokalanästhetika, was wiederum das Auftreten einer starken Spinalblockade oder einer anhaltenden Hypotonie verringern kann. Es kann auch die Dauer des Aufenthalts auf der Postanästhesiestation (PACU) verkürzen. Zu den möglichen Problemen der CSE-Technik für die Kaiserschnittentbindung gehören die Unfähigkeit, den Katheter zu testen, die Möglichkeit eines fehlgeschlagenen Epiduralkatheters nach der Spinalinjektion und das Risiko einer verstärkten Ausbreitung eines zuvor injizierten Spinalmedikaments nach Verwendung des Epiduralkatheters.
Kombinierte Spinal-Epidural-Technik für die externe Cephalic-Version der Breech-Präsentation
Neuraxiale Analgesie wurde verwendet, um die mütterlichen Schmerzen während der externen kranialen Version (ECV) für die Beckenendlage zu reduzieren. Ein potenzieller Vorteil der CSE-Technik ist die Fähigkeit, eine schnelle und effektive Schmerzlinderung für ECV bereitzustellen und bei Bedarf für eine Notfallentbindung auf eine neuraxiale Anästhesie umzustellen. Kawase et al. berichteten über einen erfolgreichen Fall von ECV unter CSE-Technik, gefolgt von einer vaginalen Entbindung. Sullivan und Kollegen untersuchten die Wirkung der CSE-Technik auf den Erfolg von ECV im Vergleich zu systemischer Opioid-Analgesie und fanden keinen Unterschied; Die Schmerzwerte waren jedoch niedriger und die Zufriedenheit mit der CSE-Analgesie höher. Erfahren Sie mehr darüber Geburtshilfe Regionalanästhesie.
VORTEILE DER KOMBINIERTEN SPINAL-EPIDURAL-TECHNIK
Beginn der Blockade
Beim Vergleich der CSE-Blockade entweder mit der Epidural- oder der Subarachnoidalblockade bei Hüft- oder Knieendoprothetik stellte sich heraus, dass die CSE-Anästhesie der Epiduralanästhesie überlegen war. Mit der CSE-Technik wurde die chirurgische Anästhesie schnell etabliert und sparte 15–20 Minuten im Vergleich zu Epiduralanästhesie. Darüber hinaus bot der Epiduralkatheter die Möglichkeit, eine unzureichende Subarachnoidalanästhesie zu ergänzen. Patienten, die die CSE-Technik erhielten, hatten eine stärkere motorische Blockade als diejenigen, die nur eine Epiduralanästhesie erhielten.
Fehlerrate
Es wurde berichtet, dass die CSE-Technik die Ausfallrate und das Auftreten mehrerer anderer unerwünschter Ereignisse im Zusammenhang mit neuraxialer Analgesie verringert. In einer retrospektiven Analyse von fast 20,000 Entbindungen (75 % neuraxiale Wehenschmerzrate) betrug die Gesamtausfallrate bei dieser Technik 12 %. Die Patientinnen hatten von der anfänglichen Platzierung an eine ausreichende Analgesie, aber 6.8 % der Patientinnen hatten anschließend eine unzureichende Analgesie während der Wehen und benötigten einen Ersatz des Epiduralkatheters. Letztendlich erhielten 98.8 % aller Patienten in Pans Bericht eine angemessene Analgesie, obwohl bei 1.5 % der Patienten ein oder mehrere Epiduralkatheter ersetzt wurden. Im Vergleich zur reinen Epiduralanalgesie während der Wehen wurde jedoch wiederholt gezeigt, dass die Vorfälle von Gesamtversagen, versehentlichen intravaskulären Epiduralkathetern, versehentlichen Durapunktionen, unzureichender Epiduralanalgesie und Katheterwechseln bei Patienten, die eine CSE-Analgesie erhielten, signifikant geringer waren. Darüber hinaus berichteten Eappen et al., dass die CSE im Vergleich zur konventionellen Epiduraltechnik eine höhere Erfolgsrate hatte. Dieser Unterschied kann auf die Fähigkeit zurückzuführen sein, eine fragwürdige epidurale Lokalisation durch erfolgreiche Spinalplatzierung und Beobachtung der Zerebrospinalflüssigkeit (CSF) zu bestätigen.
Anforderung an ein Lokalanästhetikum
Während der Operation CSE ermöglicht eine niedrig dosierte Spinalanästhesie für Kaiserschnittgeburten. Bei der Verwendung einer Single-Shot-Spinalanästhesie (SSS) für ambulante Operationen neigen viele Anästhesisten dazu, mehr Medikamente zu verabreichen als nötig, da es nur eine Chance gibt, eine wirksame Spinalblockade sicherzustellen. Das Vorhandensein eines Epiduralkatheters als „Sicherheitsnetz“ ermöglicht es dem Anästhesisten, die niedrigste wirksame Dosis des Lokalanästhetikums zu verwenden. Urmey et al. verwendeten die CSE-Technik, um die geeignete Dosis von intrathekalem isobarem Lidocain 2 % für die Arthroskopie am Tag zu untersuchen. Die CSE-Technik bot allen 90 Patienten in seiner Studie eine hervorragende Anästhesie. Patienten, die die kleinste Dosis (40 mg) erhielten, hatten eine signifikant kürzere Anästhesiedauer, was eine schnellere Entlassung ermöglichte als bei Patienten, die 60 oder 80 mg intrathekales Lidocain erhielten.
Norris et al. schlugen die Verwendung einer CSE-Technik mit intrathekalem Sufentanil allein für die ambulante Stoßwellenlithotripsie vor, wobei die Verwendung eines Epiduralkatheters für Patienten reserviert wurde, die keine ausreichende Analgesie erreichten.
Während der Wehen Analgesie Patel et al. untersuchten den Einfluss von Rückenmarksmedikamenten, die als Teil einer CSE-Technik verabreicht wurden, auf den nachfolgenden epiduralen Bupivacain-Bedarf. In einer prospektiven, randomisierten, doppelblinden Studie wurde die MLAC (minimale lokale analgetische Konzentration) von epiduralem Bupivacain zur Analgesie der Wehen nach initialer intrathekaler (CSE) oder epiduraler Medikation (Standard-Epiduralanästhesie) bewertet. Sie berichteten, dass die MLAC von epiduralem Bupivacain durch die Anwendung einer intrathekalen Medikation nicht reduziert, sondern tatsächlich um den Faktor 1.45 erhöht wurde. (MLAC in der Standard-Epiduralgruppe betrug 0.032 % Gew./Vol. und in der CSE-Gruppe 0.047 % Gew./Vol.)
Dies deutet darauf hin, dass die CSE-Analgesie über die Anfangsdosis hinaus keinen quantitativen Analgesievorteil gegenüber der Standard-Epiduralanalgesie bieten könnte.
Epidurale Volumenerweiterung: Eine Modifikation des CSE
Während der CSE-Anästhesie hat sich gezeigt, dass die Ergänzung des Epiduralraums mit epiduraler Kochsalzlösung („epidurale Volumenerweiterung“, EVE) das Anästhesieniveau und die Qualität der Spinalanästhesie beeinflussen kann. Der vorgeschlagene Mechanismus für diese Augmentation ist ein komprimierender Effekt auf den Subarachnoidalraum, der die kraniale Ausbreitung des Lokalanästhetikums fördert. Takiguschi et al. zeigten in einer Studie mit Myelographie an menschlichen Probanden, dass das Kontrastmittel im Subarachnoidalraum nach lumbaler epiduraler Kochsalzinjektion nach kranial verlagert und der Durchmesser des Subarachnoidalraums aufgrund des Volumeneffekts verengt wurde. Dies ist ein zeitabhängiges Phänomen mit maximalem Nutzen, wenn es früh durchgeführt wird. In ähnlicher Weise zeigten Blumgart et al., dass EVE mit 10 ml normaler Kochsalzlösung nach der Verabreichung von 8–9 mg subarachnoidalem hyperbarem Bupivacain bei Frauen, die sich einem Kaiserschnitt unterziehen mussten, zu einer Erhöhung der sensorischen Blockhöhe um vier Segmente führte.
Eine neuere Studie von Loubert et al. zeigte jedoch keinen Unterschied in der Höhe der sensorischen Blockade nach EVE mit 5 ml normaler Kochsalzlösung. Es ist möglich, dass das 5-ml-Volumen bei dieser Patientenpopulation nicht ausreichte, obwohl das Volumen normaler Kochsalzlösung, das sich zuvor als wirksam für EVE erwiesen hat, etwa 5–10 ml beträgt. Die Ergebnisse können auch auf einen Positionseffekt zurückzuführen sein; In beiden Studien wurde die CSE-Technik im Sitzen durchgeführt. Blumgart injizierte jedoch 10 ml Kochsalzlösung epidural durch den Katheter innerhalb von 5 Minuten nach der hyperbaren Spinalmedikation, nachdem der Patient mit einer 15°-Linksseitenneigung auf den Rücken gedreht worden war. In Louberts Studie wurden 5 ml normale Kochsalzlösung durch die Tuohy-Nadel unmittelbar nach der spinalen Überdruckmedikation injiziert, während die Patienten noch in sitzender Position waren. Schließlich wurde der Epiduralkatheter eingefädelt und den Patienten wurde in die Rückenlage um 15° nach links seitlich gekippt.
Spielt die Barizität des Lokalanästhetikums eine Rolle? Eine Studie von Tyagi et al. zeigte (bei nicht geburtshilflichen Patientinnen), dass EVE mit reinem Bupivacain wirksamer war als mit hyperbarem Bupivacain, wobei eine geringere Dosis erforderlich war, während eine stärkere sensorische Blockade mit einem früheren Beginn hervorgerufen wurde. Sie führten diesen Unterschied auf die eingeschränkte Ausbreitung hyperbarer Lokalanästhetika im Subarachnoidalraum im Vergleich zur reinen Lösung zurück.
Eine weitere Studie von Tyagi et al. fand heraus, dass die intrathekale Blockade in Dauer und Ausmaß mit hyperbarem Bupivacain ähnlich war, unabhängig davon, ob es als SSS- oder CSE-Verabreichung mit oder ohne EVE bei Gebärenden mit elektivem Kaiserschnitt verabreicht wurde. Viele Faktoren scheinen EVE zu beeinflussen. Dazu gehören das Timing, die Menge der Kochsalzlösung, Merkmale des Lokalanästhetikums (hyperbar vs. hypobar), die Position während oder nach der Spinalanästhesie und geburtshilfliche versus nicht geburtshilfliche Patienten. Obwohl vorgeschlagen wurde, dass EVE eine reduzierte Subarachnoidaldosis des Lokalanästhetikums für Operationen ermöglichen und folglich das Auftreten von hämodynamischen Effekten im Zusammenhang mit einer Spinalblockade verringern könnte, gibt es einen Mangel an Einheitlichkeit zwischen Protokollen und Studienergebnissen. Daher bleibt der Einfluss der epiduralen Kochsalzinjektion auf die Qualität der Spinalanästhesie unklar.
Sequentielle CSE
In einer Studie von Fan et al. wurden vier verschiedene intrathekale Dosen von hyperbarem Bupivacain (2.5, 5, 7.5 und 10 mg) bei Patienten verglichen, die sich einem Kaiserschnitt unter sequentieller CSE-Blockade unterzogen, einer Technik, bei der eine relativ kleine Subarachnoidalblockade verabreicht wird kann bei Bedarf durch epidurale Lokalanästhetika ergänzt werden. Die Autoren zeigten, dass 5 mg intrathekales Bupivacain in Kombination mit einer angemessenen Dosis epiduralem Lidocain eine angemessene chirurgische Analgesie bei gleichzeitiger Aufrechterhaltung einer optimalen hämodynamischen Stabilität lieferte. Höhere Dosen von intrathekalem Bupivacain waren mit typischen Nebenwirkungen eines hohen Subarachnoidalblocks wie Übelkeit, Erbrechen und Dyspnoe verbunden. Macfarlane et al. zeigten, dass die CSE-Anästhesie im Vergleich zur SSS-Anästhesie bei Kaiserschnittgeburten keine hämodynamischen Vorteile zu bieten scheint, wenn die gleiche Dosis des Lokalanästhetikums verabreicht wird. Die hämodynamische Stabilität wurde direkt durch Messen des nichtinvasiven Blutdrucks und indirekt durch den Ephedrinbedarf, den systemischen Gefäßwiderstandsindex und den Herzindex unter Verwendung der Thoraximpedanzkardiographie untersucht.
Kombinierte Spinal-Epiduralanästhesie für Risikopatienten
Die sequentielle CSE-Technik kann besonders vorteilhaft bei Hochrisikopatienten sein, z Herzerkrankung, wenn ein langsameres Einsetzen der sympathischen Blockade wünschenswert ist. Die meisten Spinalanästhetika werden als Einzelinjektionsverfahren verabreicht, und ein rasches Einsetzen der Sympathikusblockade kann zu einer plötzlichen, schweren Hypotonie führen. Traditionell werden Hochrisikopatienten mit langsam einsetzender kontrollierter Epiduralanästhesie behandelt, die eine viel höhere Gesamtdosis an Lokalanästhetika erfordert als dies bei der sequentiellen CSE der Fall ist. Bei sorgfältiger Positionierung des Patienten vor Einleitung der Subarachnoidalblockade und durch Titration mit kleinen inkrementellen Epiduraldosen bis zum genau gewünschten Anästhesieniveau kann die sequenzielle CSE-Technik die Sicherheit der neuraxialen Blockade erhöhen. Agarwal et al. berichteten über ein erfolgreiches Management der Hysterektomie bei einer Patientin mit Ventrikelseptumdefekt und Lungenatresie (VSD-PA) unter Verwendung von CSE mit der EVE-Technik. Entlang ähnlicher Hochrisikolinien stellten Month et al. zwei Gebärende mit idiopathischer intrakranieller Hypertonie vor, die sowohl Wehenschmerz als auch symptomatische Linderung unter Verwendung der CSE-Technik mit kleinvolumigem Liquorentzug erreichten.
Zusammenfassend lässt sich sagen, dass die CSE viele der Nachteile der Subarachnoidal- oder Epiduralanästhesie allein reduzieren oder beseitigen kann, während ihre jeweiligen Vorteile erhalten bleiben. Der CSE-Block bietet die Geschwindigkeit des Einsetzens, die Wirksamkeit und die minimale Toxizität eines Subarachnoidalblocks, kombiniert mit dem Potenzial, einen unzureichenden Block zu verbessern oder die Dauer der Anästhesie mit epiduralen Ergänzungen zu verlängern; mit der Epiduralanästhesie kann man die Analgesie weit in die postoperative Phase hinein verlängern. Obwohl die sequenzielle CSE-Technik etwas länger dauert als die Standard-CSE-Technik, hat sich gezeigt, dass die Verwendung minimaler Dosen von Lokalanästhetika die Häufigkeit und Schwere von Hypotonie im Vergleich zu Epidural- oder Spinaltechniken verringert. Trotz zahlreicher Studien, die CSE befürworten, kam ein Cochrane-Review von 2007 zu 19 randomisierten Studien mit 2658 gebärenden Frauen zu dem Schluss, dass CSE im Vergleich zur herkömmlichen Epiduralanalgesie wenig Nutzen bringt und es keinen Unterschied in der Gesamtzufriedenheit der Frauen zwischen den beiden Techniken gab. Die Autoren räumten jedoch ein, dass CSE zu einem etwas schnelleren Einsetzen einer wirksamen Schmerzlinderung und einem geringeren Bedarf an Notfall-Analgetika führte und mit einer geringeren Harnretention verbunden war. Später kritisierte Van de Velde diesen Cochrane-Review und erklärte, dass eine Reihe von gut durchgeführten Studien von der Analyse ausgeschlossen wurden. Er schrieb: „Bei konventioneller Epiduralanalgesie besteht eine größere Variabilität zwischen den Patienten in Bezug auf den Beginn der Analgesie. Bei CSE ist die Beginnzeit bei allen Patienten kurz, unabhängig von den anderen Faktoren.“
FUNKTIONELLE ANATOMIE IM ZUSAMMENHANG MIT CSE
Bei der Durchführung einer Epiduralblockade sind der Abstand zwischen Haut und Epiduralraum (SED) und der hintere Epiduralraumabstand (PED) Maßnahmen, die dazu beitragen können, das versehentliche Eindringen in die Dura und die Verletzung neuraler Strukturen zu reduzieren. Die Kenntnis dieser Abstände ist auch für die Erfolgsrate von Epiduralblockaden wichtig. Besonders wichtig bei der CSE-Nadel-durch-Nadel (NTN)-Technik ist die PED, ein Maß für die Tiefe des Epiduralraums. Eine Unterschätzung dieses Abstands (kurzer Vorsprung der Spinalnadel durch die Epiduralnadel) führt zu einer höheren Inzidenz von Spinalblockversagen.
Jeder Ansatz außerhalb der Mittellinie würde auch das Risiko erhöhen, den Subarachnoidalraum nicht zu erreichen, da der Duralsack eine dreieckige Form hat, wobei die Spitze nach dorsal zeigt. Eine Überschätzung der PED führt zu einem Übervorstehen der Spinalnadel, was das Risiko einer Nervenschädigung erhöhen kann. Diese Abstände wurden mit verschiedenen Methoden gemessen, einschließlich Magnetresonanztomographie (MRT), Computertomographie (CT), Ultraschall und Messung des CSE-Spitzenabstands oder des Ausmaßes des Vorsprungs der Spinalnadel über die Tuohy-Nadel hinaus. Der Abstand zur SED beträgt am häufigsten 4 cm (50 %) und beträgt laut detaillierter Aufzeichnungen von 4 Fällen bei 6 % der Bevölkerung 80–3200 cm. Die Breite der PED variiert mit der Wirbelhöhe, wobei sie in der Mitte der Lendenwirbelsäule am breitesten ist (5–6 mm) und zur Halswirbelsäule hin abnimmt. In der Mitte des Brustkorbs beträgt er in der Mittellinie 3–5 mm und verjüngt sich seitlich. Im unteren Halsbereich beträgt er in der Mittellinie nur 1.5–2 mm. Diese Abstände korrelieren auch mit dem Verhältnis von Gewicht zu Körpergröße und dem Body-Mass-Index (BMI). Basierend auf diesen Maßnahmen variiert das gegenwärtige Design des Vorsprungs der Spinalnadel zwischen 10 und 15 mm über die Epiduralnadel hinaus. Erfahren Sie mehr darüber Funktionelle neuroaxiale Anatomie.
Epiduralraum und Ligament Flavum
Die Dicke des Ligamentum flavum, der Abstand zur Dura und der Haut-zu-Dura-Abstand variieren mit der Fläche des Wirbelkanals (vgl Tabelle 1).
Die beiden Ligamenta flava sind in der Mittellinie variabel verbunden (fusioniert), und diese Fusion oder fehlende Fusion des Ligamenta flavum tritt bei einzelnen Patienten auf verschiedenen Wirbelebenen auf. Lirk et al. untersuchten die Häufigkeit von Lücken in der Mittellinie des lumbalen Ligamentum flavum bei einbalsamierten Leichen. Wirbelsäulenproben wurden von 45 menschlichen Leichen erhalten. Die Lücken im lumbalen Ligamentum flavum sind am häufigsten zwischen L1 und L2 (22.2 %), aber selten unterhalb dieser Ebene (L2–L3 = 11.4 %, L3–L4 = 11.1 %, L4–L5 = 9.3 %, L5–S1 = 0). Daher kann man sich bei einem Mittellinienzugang nicht darauf verlassen, dass das Ligamentum flavum bei allen Patienten das Eindringen in den Epiduralraum behindert.
TABELLE 1. Eigenschaften des Ligamentum flavum auf verschiedenen Wirbelebenen.
| Site | Haut zu Ligament (cm) | Banddicke (mm) |
|---|---|---|
| Zervikal | - | 1.5-3.0 |
| Brust- | - | 3.0-5.0 |
| Lenden- | 3.0-8.0 | 5.0-6.0 |
| Fließen | Variable | 2.0-6.0 |
Für eine umfassendere Übersicht siehe Neuroaxiale Anatomie
TECHNISCH
In einer Reihe von Reviews wurden die technischen Faktoren im Zusammenhang mit der Leistung und dem Erfolg von CSE diskutiert. Obwohl CSE als relativ neue Technik gilt, beschrieb Soresi 1937 tatsächlich die absichtliche Injektion von Anästhetika außerhalb und innerhalb des Subarachnoidalraums. Etwas anders als die derzeitige Praxis verwendete Soresi absichtlich eine einzelne Nadel. Er injizierte zuerst etwas Lokalanästhetikum in den Epiduralraum und schob dann die Nadel vor und injizierte den Rest des Medikaments, um einen Subarachnoidalblock zu verursachen. Obwohl diese Technik sowohl Spinal- als auch Epiduralanästhesie umfasste, wurde kein Katheter verwendet. 1979 berichtete Curelaru über den ersten CSE mit Einführung eines Epiduralkatheters durch eine Tuohy-Nadel. Auf die Einführung des Katheters folgte eine Testdosis und dann eine traditionelle Duralpunktion, die an einem anderen Zwischenraum unter Verwendung einer 26-Gauge-Spinalnadel durchgeführt wurde. Im selben Jahr schlug Brownridge die Verwendung von CSE für die Geburtshilfe vor. Er beschrieb 1981 die erfolgreiche Verwendung von CSE für einen elektiven Kaiserschnitt. 1982 wurde die NTN-CSE-Technik erstmals unabhängig von Coates und Mumtaz beschrieben, und ihre aktive Verwendung in der Geburtshilfepraxis wurde erstmals 1984 von Carrie veröffentlicht. Die Popularität der Technik begann Ende der 1990er Jahre. In der neueren Literatur wurden mehrere Ansätze zur Initiierung von CSE beschrieben.

Aus dem Kompendium der Regionalanästhesie: Techniken der kombinierten Spinal-Epiduralanästhesie Infografik.
Nadel-durch-Nadel-Technik
Im Gegensatz zu Soresis anfänglicher Beschreibung von CSE, bei der eine einzelne Nadel in den Epiduralraum eingeführt und dann in den Subarachnoidalraum vorgeschoben wurde, umfasst die derzeit bevorzugte NTN-Technik die Verwendung von separaten Epidural- und Spinalnadeln. Typischerweise wird der Epiduralraum mit einer herkömmlichen Epiduralnadel und -technik lokalisiert, und dann wird eine lange Spinalnadel durch die Epiduralnadel geführt, bis CSF in der Nabe der Spinalnadel erscheint. Das Medikament wird über die Spinalnadel in den Subarachnoidalraum verabreicht, die Spinalnadel entfernt und schließlich ein Epiduralkatheter in den Epiduralraum eingeführt. Obwohl mehrere verschiedene CSE-Techniken in der klinischen Praxis verwendet werden (einschließlich der Zwei-Nadel-Zwei-Zwischenraum-Technik), ist NTN die am weitesten verbreitete CSE-Technik in den Vereinigten Staaten.
Separate Nadeltechnik
Die CSE-Technik kann unter Verwendung von zwei separaten Nadeln mit der separaten Nadeltechnik (SNT) durchgeführt werden, mit spinaler Blockade und Epiduralkatheterplatzierung entweder in einem einzigen oder in zwei verschiedenen Zwischenräumen. Wenn der Epiduralkatheter zuerst platziert wird, kann die richtige Platzierung vor der Verabreichung von Wirbelsäulenmedikamenten getestet werden, wodurch möglicherweise das Risiko einer versehentlichen intravaskulären oder intrathekalen Kathetermigration verringert wird. Das erste Platzieren des Epiduralkatheters kann auch das Risiko einer neuralen Schädigung reduzieren, die auftreten kann, wenn der Katheter nach einer Subarachnoidalblockade eingeführt wird, da Parästhesien und andere Warnzeichen für eine unsachgemäße Nadelplatzierung nach der Verabreichung von Wirbelsäulenmedikamenten fehlen können.
Allerdings besteht auch die Gefahr, mit der Spinalnadel den Epiduralkatheter zu treffen. Einige Autoren halten dies für ein rein hypothetisches Risiko und haben gezeigt, dass es nicht möglich ist, einen Epiduralkatheter mit üblichen Spinalnadeln zu perforieren.
Cook et al. berichteten über eine Reihe von 201 aufeinanderfolgenden CSEs, die mit einem neuartigen SNT durchgeführt wurden. Die Studie wurde entwickelt, um potenzielle und tatsächliche Probleme im Zusammenhang mit der CSE-Technik zu vermeiden.
Cook et al. platzierten die Spinalnadel im Subarachnoidalraum und ersetzten dann das Spinalnadelstilett, um das Liquorleck zu stoppen. Als nächstes wurde der Epiduralkatheter durch einen anderen Zwischenraum platziert und dann zur Spinalnadel zurückgeführt, um das Subarachnoidalmedikament zu injizieren, wodurch das Einführen eines Epiduralkatheters bei einem anästhesierten Patienten vermieden wurde. Diese Methode der CSE-Anästhesie ist zwar viel arbeitsintensiver, kann aber mit hohem Erfolg und geringen Komplikationsraten verbunden sein. Unabhängig davon, welche Komponente zuerst durchgeführt wird, besteht der Hauptnachteil der Technik mit zwei Nadeln und zwei Zwischenräumen darin, dass die Durchführung länger dauert und zwei separate Injektionen erforderlich sind.
Vergleich der Techniken
Die SNT-Technik hat gegenüber der NTN-Technik einige theoretische Vorteile. Es ermöglicht die Platzierung des Epiduralkatheters vor Beginn der Spinalblockade. Der SNT kann daher theoretisch das Risiko für neurologische Verletzungen reduzieren, da Parästhesien und andere Symptome nicht maskiert werden. Da der Epiduralkatheter früh platziert wird, werden Probleme vermieden, die aufgrund einer verzögerten Katheterplatzierung (technische Probleme) nach der Injektion einer hyperbaren Spinallösung auftreten können (z. B. einseitige, sakrale oder untere lumbale regionale neuraxiale Blockade). Mehrere Studien haben NTN- und SNT-Techniken verglichen. Einige berichten von besseren Erfolgen und niedrigeren Ausfallraten mit dem SNT. Diese Studien berichteten jedoch auch über eine größere Patientenakzeptanz und weniger Beschwerden mit der NTN-Technik.
Backe et al. verglichen in einer prospektiven randomisierten Studie die Ergebnisse und Techniken von NTN- und SNT-CSE (Doppelraum) bei 200 Patientinnen mit elektivem Kaiserschnitt. Erfolgreiche Blocks zu T5 mit der Double-Space- und der NTN-Technik waren jeweils 80 gegenüber 54, Odds Ratio 0.29. SNT hatte eine größere Erfolgsrate als die NTN-Technik; das T5-Dermatom wurde mit weniger Korrekturmaßnahmen (Epiduralaugmentation oder wiederholte Blockaden) erreicht. Bei 29 Patienten in der NTN-Gruppe trat ein Versäumnis auf, den Intrathekalraum zu betreten, nachdem der Epiduralraum lokalisiert worden war. Die Zeit bis zur OP-Bereitschaft war jedoch mit SNT leicht erhöht (15 Minuten mit SNT vs. 12.9 Minuten mit NTN). Sadashivaiah et al analysierten retrospektiv Daten von 3519 elektiven Kaiserschnittgeburten, die mit der SNT-Technik durchgeführt wurden. Sie berichteten von einer niedrigeren Konversionsrate zur Vollnarkose aufgrund einer fehlgeschlagenen neuraxialen Blockade (0.23 %) als zuvor berichtet (0.8 %–1.3 %). Eines der Probleme bei der NTN-Technik besteht darin, dass viele Patienten über Parästhesien/Dysästhesien klagen oder auf eine Duralpunktion während des Einführens einer Nadel mit Bleistiftspitze reagieren (Bewegung, Grimassen, Lautäußerungen). Van den Berg et al. verglichen die Auswirkungen von Kochsalzlösung gegenüber Luft auf den Widerstandsverlust (LOR) auf das Auftreten dieser Beschwerden und berichteten, dass die Verwendung von Kochsalzlösung mit weniger Patientenreaktionen (18 % vs. 44 %) zum Zeitpunkt der Thecal verbunden ist Penetration. Obwohl der Mechanismus dieser reduzierten Reaktion mit Kochsalzlösung für LOR nicht klar ist, postulierten die Autoren, dass möglicherweise die Platzierung von Kochsalzlösung im Epiduralraum die durale Empfindlichkeit modulierte.
Techniken zur Verbesserung des Erfolgs und der Sicherheit der kombinierten Spinal-Epiduralanästhesie
Der Erfolg eines CSE-Blocks hängt stark von der genauen Kanülierung des Epiduralraums ab. Die Identifizierung des Epiduralraums wird traditionell durch eine blinde LOR-Technik erreicht. Bei dieser Handhabung der Nadeln, bei der die Rückmeldung an den Bediener lediglich taktil ist, kann eine Abweichung der Achse der Nadelbahn auftreten. Aufgrund der dreieckigen Form des Duralsacks führt eine Abweichung der Spinalnadel von der Mittellinie dazu, dass der Duralsack verfehlt wird, was zu einem Versagen der Wirbelsäulenkomponente oder einer erfolglosen Duralpunktion führt. Grau et al. führten eine Echtzeit-Ultraschalluntersuchung der Lendenwirbelsäule durch, um eine genaue Ablesung der Position der Nadelspitze zu ermöglichen und die Durchführung der CSE-Anästhesie zu erleichtern. Ihr Ziel war es, eine weniger invasive Methode zu etablieren, um den Vorschub der Nadel in Echtzeit zu überwachen. Dreißig Gebärende, die für einen Kaiserschnitt vorgesehen waren, wurden randomisiert in drei gleiche Gruppen eingeteilt. Zehn Kontrollpatienten erhielten eine auf herkömmliche Weise durchgeführte CSE-Anästhesie. Zehn erhielten Ultraschalluntersuchungen durch eine Offline-Technik. Die restlichen 10 erhielten während der Punktion eine Online-Bildgebung der Lendenregion. Die Tuohy-Nadel wurde in allen drei Gruppen unter Verwendung des Mittellinienzugangs eingeführt. In der Kontrollgruppe wurde CSE unter Verwendung einer Single-Space-NTN-Technik mit der Standardmethode von LOR zu Kochsalzlösung durchgeführt. In der Offline-Gruppe wurden unmittelbar vor der Punktion Ultraschallbilder aufgenommen, um die Nadelbahn zu verbessern. In der Online-Gruppe wurden Ultraschallbilder aufgenommen, um die Nadelbahn in Echtzeit zu überwachen und zu identifizieren.
Die Autoren berichteten, dass in beiden Ultraschallgruppen eine signifikante Reduktion der Anzahl notwendiger Punktionsversuche festgestellt wurde (p < 036); die Anzahl der für die Punktion notwendigen Zwischenräume wurde reduziert (p < 036); und die Anzahl der Spinalnadelmanipulationen wurde signifikant reduziert (p < 036). Dauerzelten wurde bei 9 von 10 der Online-Gruppe beobachtet (Zeltlänge 2.4 mm). Eine asymmetrische Blockade wurde bei 10 % der Patienten in der Kontrollgruppe beobachtet, aber bei keiner der Personen in den Ultraschallgruppen. Die Autoren schlussfolgerten, dass der Einsatz von Ultraschallbildgebung offensichtlich hilfreich war, um die ideale Nadelbahn zu finden und die Punktionsbedingungen durch Demonstration der relevanten Anatomie zu verbessern. Bei der CSE-NTN-Technik gibt es keinen praktischen Test, um die korrekte Platzierung des Epiduralkatheters zu bestätigen. Tsui und Kollegen schlugen die Verwendung von Nervenstimulatoren vor, um die korrekte Platzierung des Epiduralkatheters zu bestätigen. Sie untersuchten 39 geburtshilfliche Patientinnen in den Wehen, die Epiduralkatheter (nicht CSE) zur Analgesie erhielten. Zur Bestätigung der korrekten Platzierung des Epiduralkatheters (1-Gauge Arrow Flextip plus) wurde eine schwache elektrische Stimulation (10 bis 19 mA) verwendet. Eine positive motorische Reaktion (Rumpf oder Extremität) zeigte an, dass sich der Katheter im Epiduralraum befand. Sie berichteten, dass die Sensitivität und Spezifität dieses Tests 100 % bzw. 100 % betrugen, mit 38 richtig positiven Tests und einem richtig negativen Test. Mit diesem neuen Test wurde ein Fall von intravaskulärer Epiduralkatheterwanderung festgestellt und anschließend durch einen positiven Epinephrin-Test bestätigt. Wenn die motorische Reaktion nur bei größeren Strömen (>1 mA) auftritt oder überhaupt nicht reagiert (vor Erhalt einer Lokalanästhesie), befindet sich der Katheter höchstwahrscheinlich außerhalb des Epiduralraums. Wenn eine positive Reaktion bei einer ungewöhnlich niedrigen Milliamperezahl (<10 mA) auftritt, ist eine intrathekale Platzierung wahrscheinlich.
Der elektrische Stimulationstest ist möglicherweise nicht anwendbar, wenn die CSE-Technik für Operationen verwendet wird, bei denen vor der Platzierung des Epiduralkatheters intrathekal anästhetische Dosen von Lokalanästhetika verabreicht werden. Bei Verwendung der CSE-Technik zur Analgesie der Wehen kann dieser Test als einfache und praktische Methode zur Bestimmung der Platzierung des Epiduralkatheters verwendet werden. Die in den Vereinigten Staaten verwendete Standard-Testdosis (3 ml 1.5 %iges Lidocain mit 1:200,000 Epinephrin) kann helfen, die intravaskuläre und intrathekale Platzierung zu identifizieren, verifiziert jedoch nicht die angemessene epidurale Platzierung oder Funktion.
ARZNEIMITTEL FÜR KOMBINIERTE SPINAL-EPIDURALE
Sufentanil und Fentanyl, mit oder ohne Lokalanästhetika, werden am häufigsten intrathekal verabreicht, um der gebärenden Frau, die CSE erhält, Analgesie zu verleihen. Die übliche Dosierung von Sufentanil beträgt 2.5–10 μg; Die meisten Praktiker verwenden jedoch jetzt 2.5 oder 5 μg. Die ED50 und ED95 für Wehen betrugen 2.6 bzw. 8.9 μg. Die verwendeten Dosen von Fentanyl betragen typischerweise 10–25 μg. Die mediane effektive Dosis (ED50) und die effektive Dosis bei 95 % der Bevölkerung (ED95) bei Wehen betragen 5.5 bzw. 17.4 μg. Obwohl die ursprünglichen Studien viel höhere Dosen intrathekaler Opioide (10 μg Sufentanil und 25–50 μg Fentanyl) verwendeten, haben spätere Studien die Verwendung geringerer Dosen mit reduzierten Nebenwirkungen und ähnlicher analgetischer Wirkung vorgeschlagen.
Morphin, ein stark ionisiertes, wasserlösliches Opioid, bewirkt eine Analgesie von langer Dauer, aber langsamem Einsetzen (ungefähr 60 Minuten zwischen neuraxialer Injektion und Einsetzen). Darüber hinaus kann es mit einer unannehmbar hohen Häufigkeit von Nebenwirkungen wie Übelkeit, Erbrechen, Pruritus sowie der Möglichkeit einer verzögerten Atemdepression verbunden sein. Diese Nebenwirkungen, gekoppelt mit dem langsamen Einsetzen der Schmerzlinderung, schränken die Nützlichkeit von intrathekalem Morphin für die Analgesie der Wehen ein. Intrathekales Meperidin (10 mg) kann bei fortgeschrittenen Wehen eine zuverlässige Analgesie bewirken, wurde jedoch mit einer hohen Inzidenz von Übelkeit, Erbrechen, Hypotonie und der Notwendigkeit einer Behandlung des niedrigen Blutdrucks in Verbindung gebracht. Darüber hinaus ist es das einzige Opioid, das bei klinisch angemessenen Dosen intrinsische lokalanästhetische Eigenschaften besitzt, indem es die Nervenleitung am proximalen Ende der Dorsalwurzel über einen anderen Mechanismus als die Natriumkanalblockade blockiert. Diese Nervenleitungsblockade ist mit Naloxon nicht reversibel.
Bei vielen Patientinnen reicht eine einzige intrathekale Injektion eines fettlöslichen Opioids nicht aus, um während der gesamten Wehendauer Analgesie zu bewirken. Wenn die zweite Wehenphase bevorsteht, sollte zur Erzielung einer tieferen Schmerzlinderung die subarachnoidale Gabe von Lokalanästhetikum plus Opioid in Betracht gezogen werden. Die Kombination von 2.5–5 μg Sufentanil plus 2.5 mg Bupivacain bietet eine schnelle Analgesie ohne motorische Blockade, lindert die Schmerzen der zweiten Wehenphase und hält länger an als Sufentanil allein. Obwohl die ursprünglichen Berichte die Verwendung von 10 μg Sufentanil empfahlen, zeigten Sia und Kollegen, dass eine angemessene Linderung der Geburtsschmerzen durch die Verabreichung der halben Dosis von intrathekalem Sufentanil plus Bupivacain sicher erreicht werden kann.
Frühere Studien haben versucht, die ED50 von intrathekalem Bupivacain, definiert als minimale Lokalanästhesiedosis (MLAD) oder ED50, zu bestimmen und diese dann zur Beurteilung der Wirkung verschiedener Fentanyldosen zu verwenden. Es wurde festgestellt, dass die MLAD von intrathekalem Bupivacain 1.99 mg beträgt, und die Zugabe von 5 μg intrathekalem Fentanyl bot eine ähnlich signifikante Schonwirkung wie 15 oder 25 μg Fentanyl, was zu weniger Juckreiz, aber mit einer verkürzten Wirkungsdauer führte. ED95 wurde aus diesen Studien geschätzt.
Whitty et al. führten eine Up-Down-Dosisfindungsstudie durch, um die ED95 für intrathekales Bupivacain (klinisch relevanter als die aus ED50 berechnete) in Kombination mit einer festen Menge Fentanyl zu bestimmen. Sie empfahlen 1.75 mg Bupivacain mit 15 μg Fentanyl, um die Schmerzen von Gebärenden in der aktiven Phase der Wehen zuverlässig und schnell zu lindern. Im Jackson Memorial Hospital (Miami, FL) verwenden wir derzeit 1.25 mg Bupivacain plus 15 μg Fentanyl als unser Rückenmarksmedikament. Levin et al. verglichen eine Standarddosis von intrathekalem Bupivacain mit Sufentanil für CSE-Analgesie unter Verwendung von zwei Dosen Ropivacain (2 und 4 mg) mit Sufentanil. Sie kamen zu dem Schluss, dass beide Lokalanästhetika eine ähnliche Dauer der Wehenschmerzbehandlung bei gleichen Nebenwirkungen lieferten. Erfahren Sie mehr darüber Lokalanästhetika.
KOMPLIKATIONEN UND BEDENKEN DER CSE-TECHNIK
Versagen der Wirbelsäulenkomponente
Die gebräuchlichste Methode zum Durchführen eines CSE ist die Single-Interspace-NTN-Technik. In der Vergangenheit wurde in 10–15 % der Fälle berichtet, dass mit dieser Technik keine Wirbelsäulenblockade erreicht werden konnte,111,112 obwohl dieses Risiko in erfahrenen Händen nur 2–5 % betragen kann.
Mögliche Ursachen für das Scheitern von CSE sind:
1. Spinalnadel zu kurz. Die Nadel reicht nicht weit genug über die Epiduralspitze hinaus oder spannt die Dura auf. Holloway und Telford beobachteten die Distanz von der Identifizierung des Epiduralraums bis zur Penetration der Dura bei 31 Patienten während der Verwendung einer Tuohy-Nadel, um eine absichtliche Duralpunktion zum Einführen von Lumbaldrainagen durchzuführen. Obwohl viele Referenzlehrbücher geringere Abstände von der Lokalisation der Epiduralräume bis zur Durapunktion angeben, fanden diese Autoren einen unerwartet großen Abstand von bis zu 2.25 cm und postulierten, dass das Zelten der Dura durch die stumpfe atraumatische Spinalnadel die Ursache für diesen Befund sein könnte.
2. Nichteintritt in die Dura. Dies kann bei Nadeln mit sehr kleinem Kaliber auftreten, denen die Steifigkeit zum Durchstechen der Dura fehlt. Wie von Holloway und Telford postuliert, begrenzt das Fehlen eines negativen Epiduralraumdrucks den transduralen Druckgradienten und minimiert die Reaktionskräfte über die Dura. Daher erfordert das Eindringen in die Dura (eine relativ zähe Membran) eine beträchtliche Reaktionskraft.
3. Abweichung von der Mittellinie. Dies kann dazu führen, dass die Spinalnadel die Dura passiert, obwohl der Epiduralraum identifiziert wurde.
4. Verwendung einer langen, schmalen Spinalnadel. Eine lange, schmale Spinalnadel kann die Dura durchdringen und dann aufgrund der Verzögerung des Liquorrückflusses zu weit (bis zum vorderen Epiduralraum) vorgeschoben werden.
5. Verwendung einer langen Spinalnadel mit Bleistiftspitze. Ein weiteres potentielles Problem kann bei den derzeit verwendeten Spinalnadeln mit langer Bleistiftspitze auftreten. Die Spinalnadel kann schlecht verankert sein, da sie sich in der Epiduralnadel befindet und nicht fest im Gewebe gehalten wird. Da sich die Spinalnadel wahrscheinlich während der Injektion bewegt, kann das Medikament daher nur teilweise in den Subarachnoidalraum verabreicht werden. Die Fähigkeit, die Spinalnadel gleichmäßig zu halten, erfordert Übung, ist aber leicht zu erlernen.
6. Verzögerung beim Platzieren des Epiduralkatheters. Nach Verabreichung eines Subarachnoidalmedikaments kann es beim Legen des Epiduralkatheters zu Verzögerungen kommen. Dies ist normalerweise kurz und ohne Folgen, aber nach Ansicht einiger Autoren
es kann die endgültigen Eigenschaften des Blocks verändern. Diese Komplikation ist von größerer klinischer Bedeutung, wenn CSE für einen Kaiserschnitt durchgeführt wird. Sollte es jedoch zu einer Verzögerung kommen und die Blockade nicht die optimale Höhe erreichen, kann der Epiduralkatheter zur Ergänzung der Blockade eingesetzt werden.
Die meisten aktuellen Nadeldesigns ermöglichen eine Verlängerung der Spinalnadel um 12–15 mm über die Spitze der Tuohy-Nadel hinaus. Übermäßig lange Nadeln werfen jedoch Probleme bei der Handhabung und Platzierungstiefe auf. Eine Abweichung von der Mittellinie verlängert den Epidural-Dural-Abstand und kann auch dazu führen, dass die Spinalnadel den Spinalraum seitlich verfehlt (Zahlen und 1 2). Außerdem kann konservierungsmittelfreie physiologische Kochsalzlösung, die zur Identifizierung des Epiduralraums verwendet wird, als Liquor fehlinterpretiert werden.
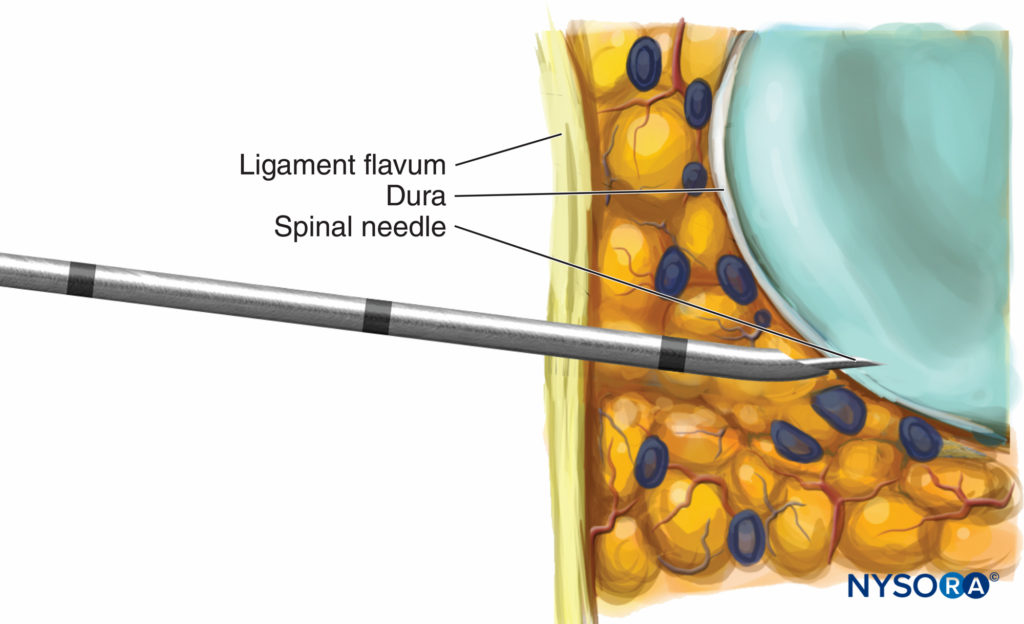
ABBILDUNG 1. Seitliche Abweichung der Epiduralnadel.
Komplikationen im Zusammenhang mit der spinalen Migration des Epiduralkatheters
oder intrathekale Verabreichung von epiduralen Arzneimitteln
Subarachnoidale Platzierung von Beabsichtigt
Epiduralkatheter
Eines der Bedenken bei der CSE-Technik besteht darin, dass der Epiduralkatheter während der CSE-Technik unbeabsichtigt durch das Duralpunktionsloch in den Subarachnoidalraum gelangen kann. Dies scheint bei der NTN-CSE-Technik wahrscheinlicher als bei der SNT oder bei Epiduralnadeln mit hinteren Löchern (Figure 3). Obwohl dies ein seltenes theoretisches Problem zu sein scheint, haben mehrere Veröffentlichungen über sein Auftreten berichtet. Angle et al. untersuchten Faktoren, die zu einer unbeabsichtigten Passage eines Subarachnoidalkatheters nach einer epiduralen Platzierung beitragen, mit einem In-vitro-Modell unter Verwendung von menschlichem Duralgewebe. In dieser Studie wurde die Dura mit 25-Gauge-Whitacre punktiert® Spinalnadeln. Die Wahrscheinlichkeit, dass der Katheter in den Subarachnoidalraum eindringt, wurde zwischen der intakten Dura verglichen mit der Dura mit offensichtlichen Epiduralnadelpunktionen und einzelnen 25-Gauge-Whitacre-Spinalnadelpunktionen nach einer CSE-Technik.

ABBILDUNG 3. Epiduralnadel mit Rückenloch.
Sie kamen zu dem Schluss, dass die Katheterpassage bei intakter Dura oder nach einer unkomplizierten CSE-Technik unwahrscheinlich ist. Daher deutet eine unbeabsichtigte Subarachnoidalpassage des Epiduralkatheters auf eine Duraschädigung durch die Epiduralnadel hin.
Holtz et al untersuchten in einem anatomischen Präparat den möglichen Durchgang des Epiduralkatheters in den Subarachnoidalraum. In 10 Versuchsreihen wurde das Epiduralkompartiment mit einer 18-Gauge-Tuohy-Nadel betreten. Die Spinalpunktion (27- oder 29-Gauge-Quincke-Nadel) wurde mit der NTN-Technik durchgeführt. Anschließend wurde die Innenseite des intrathekalen Kompartiments endoskopisch auf Penetration des Epiduralkatheters untersucht. In ähnlicher Weise wurde das Endoskop epidural eingeführt, um die Bewegungen des Epiduralkatheters im Epiduralfach zu visualisieren. In diesem Modell der simulierten physiologischen intrathekalen Bedingungen konnten sie unter Verwendung der Ein-Raum-NTN-Technik den intrathekalen Durchgang des Epiduralkatheters nicht erkennen.
Holmstrom und Kollegen berichteten in einer perkutanen Epiduroskopie-Studie mit frischen Leichen auch, dass es unmöglich war, einen Epiduralkatheter nach einer einzigen Perforation der Dura mit einer kleinen Spinalnadel in den Subarachnoidalraum zu zwingen. Sie fanden jedoch heraus, dass das Risiko einer intrathekalen Kathetermigration nach mehreren Duralpunktionen mit der Spinalnadel auf etwa 5 % anstieg. Die Duralpenetration des Epiduralkatheters nach einer Duralpunktion mit einer Tuohy-Nadel wurde in derselben Studie eindeutig nachgewiesen.
Ob die Inzidenz einer unbeabsichtigten Passage des Epiduralkatheters in den Subarachnoidalraum bei CSE im Vergleich zur alleinigen Standard-Epiduraltechnik erhöht ist, ist umstritten. Daher sollten alle Epiduralmedikamente unabhängig von der verwendeten Technik in aufsteigenden Dosen verabreicht werden.
Subarachnoidale Ausbreitung von Epidural
Verabreichte Medikamente
Leighton und Kollegen berichteten, dass nach einem CSE eine Dosis eines epiduralen Lokalanästhetikums zu einem höheren Dermatomspiegel als erwartet führt, vermutlich aufgrund des subarachnoidalen Flusses des Arzneimittels. Wenn es jedoch zur Analgesie der Wehen verwendet wird, sollte das Flussmittel klinisch nicht signifikant sein, es sei denn, die Dura wird mit der Epiduralnadel durchbrochen oder es werden große Bolusvolumina verabreicht. Suzuki et al. fanden bei nichtschwangeren Patientinnen heraus, dass eine Duralpunktion mit einer 26-Gauge-Whitacre-Spinalnadel vor der epiduralen Injektion die kaudale Ausbreitung der durch epidurale Lokalanästhetika induzierten Analgesie erhöhte, ohne dass sich die kraniale Ausbreitung änderte.
Holtz et al. untersuchten endoskopisch den möglichen Durchgang von Periduralanästhetika durch das Duralpunktionsloch in das Liquorkompartiment in einem anatomischen Präparat. Auch 1 Stunde nach epiduraler Gabe von 20 ml Methylenblau-gefärbtem Lokalanästhetikum (Bupivacain 0.5 %, isobar) war unter kontinuierlicher endoskopischer Überwachung kein Übertritt von Lokalanästhetikum in das intrathekale Kompartiment nachweisbar.
In einer Studie von Kamiya et al. wurde die Lidocainkonzentration im Liquor nach epiduraler Verabreichung an verschiedenen Zwischenräumen mit oder ohne vorangegangener Spinalanästhesie gemessen. Sie kamen zu dem Schluss, dass es keinen Unterschied in den Lidocainkonzentrationen im Liquor mit oder ohne Hirnhautloch gab. Die Autoren erklärten den möglichen Grund für den fehlenden Unterschied in der Lidocain-Konzentration wie folgt: Lidocain dringt leicht durch meningeales Gewebe ein, und diese Übertragungseffizienz wurde höchstwahrscheinlich nicht durch das Vorhandensein eines kleinen meningealen Lochs beeinflusst. Das Gleichgewicht der Lidocain-Konzentration im Liquor nahe der Verabreichungsstelle würde aufgrund dieser schnellen Penetration innerhalb weniger Minuten erreicht werden.
Anders ausgedrückt, die Menge an Lokalanästhetikum, die durch das kleine Loch in der Dura hindurchgeht, ist trivial im Vergleich zu der Menge, die durch die Hirnhäute hindurchtritt. Diese Studie bestätigte, dass CSE sicher ist und dass die Durallöcher keinen klinisch signifikanten Einfluss auf die Dauer oder das Ausmaß der Wirbelsäulenblockaden bei Patienten haben, die sich einem Kaiserschnitt unterziehen. Die Daten aus mehreren klinischen Studien der CSE-Technik haben nicht auf eine Zunahme der Ausbreitung der sensorischen Blockade aufgrund von subarachnoidalem Auslaufen von epidural verabreichten Medikamenten hingewiesen.
Die Größe des Flusses ist jedoch eine Funktion des Durchmessers der Spinalnadel, und das Risiko kann durch die Verwendung einer größeren Spinalnadel oder bei Vorhandensein eines mit einer Tuohy-Nadel hergestellten Lochs erhöht werden. Die Möglichkeit dieser Gefahr wird durch Berichte über einen starken oder totalen Spinalblock während einer Epiduralanästhesie gestützt, die nach einer unbeabsichtigten Duraperforation mit der Epiduralnadel verabreicht wurde. Die Verabreichung einer Testdosis für die spinale Platzierung eines Epiduralkatheters kann problematisch sein und die Aspiration kann fehlschlagen, aber es wurde festgestellt, dass Testdosen mehr intrathekale Katheter erkennen als Aspiration allein während der Analgesie der Wehen.
Trotz Studien, die berichtet haben, dass eine intrathekale Migration sehr selten ist und dass das Flussmittel keine klinisch relevanten Komplikationen hervorrufen sollte, wird der Leser darauf hingewiesen, dass Epiduralmedikamente oder -katheter nach CSE in den Spinalraum wandern können. Daher sollten alle epiduralen Dosen inkrementell erfolgen, und Patienten, die kontinuierliche epidurale Infusionen zur Analgesie erhalten, sollten etwa stündlich untersucht werden, um eine übermäßige motorische oder sensorische Blockade auszuschließen, die auf eine unbeabsichtigte intrathekale Verabreichung von Arzneimitteln hindeuten könnte.
Unterdruck
Ergibt ein durch CSE (unter Verwendung von LOR to air) induzierter Subarachnoidalblock ein höheres Maß an sensorischer Anästhesie als SSS, wenn eine identische Menge an intrathekalem Anästhetikum injiziert wurde? Goy et al. führten eine prospektive randomisierte Studie zum Vergleich von CSE (unter Verwendung von LOR zu Luft) mit SSS bei 60 Patientinnen durch, die sich kleineren gynäkologischen Eingriffen unterzogen, und kamen zu dem Schluss, dass eine durch CSE induzierte Subarachnoidalblockade eine stärkere sensomotorische Anästhesie (p < 01) und eine verlängerte Erholung (p < 05) als SSS. Sie fanden auch eine häufigere Inzidenz von Hypotonie und Vasopressor-Einnahme in der CSE-Gruppe (p < 05), trotz der Verwendung identischer Dosen von intrathekalen Medikamenten. Eine andere Studie berichtete ähnliche Ergebnisse, wenn nur 4 ml Luft als Teil der LOR-Technik verwendet wurden. Das Ziel dieser Studie war die Bestimmung der ED50 von intrathekalem hyperbarem Bupivacain für CSE und SSS unter Verwendung der sequentiellen Up-Down-Zuordnungstechnik. In einem doppelblinden, randomisierten, prospektiven Studiendesign wurden 50 Teilnehmer in zwei Gruppen eingeteilt. Sie kamen zu dem Schluss, dass unter ähnlichen klinischen Bedingungen die ED20 von intrathekalem hyperbarem Bupivacain bei CSE um XNUMX % niedriger war als bei SSS. Obwohl der Mechanismus, der für diesen Befund verantwortlich ist, nicht bestimmt wurde, ist eine mögliche Erklärung, dass die LOR-zu-Luft-Technik bei CSE Lufteinschlüsse in den Epiduralraum einführen könnte. Die MRT hat gezeigt, dass sich verbleibende Lufteinschlüsse bis zu drei lumbalen Wirbelsegmenten erstrecken und den lumbalen Thekalsack dorsal und lateral komprimieren. Dies könnte möglicherweise zu einer Verringerung des lumbosakralen Liquorvolumens führen und das Ausmaß der sensorischen Anästhesie erhöhen.
Die epidurale Verabreichung von Medikamenten scheint den thekalen Inhalt zu beeinflussen und damit die Ausbreitung eines früher induzierten Subarachnoidalblocks zu beeinflussen. Die Größe dieses Effekts hängt vom Zeitintervall zwischen den Injektionen und dem Volumen des epiduralen Injektats ab. Ursprünglich wurde als Mechanismus für diesen Effekt das Subarachnoidalleck von epidural verabreichten Medikamenten vorgeschlagen. Hypotonie kann nach intrathekaler Verabreichung von Fentanyl oder Sufentanil auftreten, auch wenn keine Sympathikusblockade auftritt. Die hämodynamischen Wirkungen von intrathekalem Fentanyl sind jedoch in der Regel gutartig und können tatsächlich auf eine Abnahme der Katecholamine als Folge der Schmerzlinderung zurückzuführen sein. Eine Vasodilatation aufgrund einer Sympathektomie verursacht jedoch eine Abnahme der Vorlast, des enddiastolischen Index und des Schlaganfallindex und eine Erhöhung der Herzfrequenz. Da in einer Studie von Mandell und Kollegen der enddiastolische Index und der Schlaganfallindex relativ stabil blieben und die Herzfrequenz abnahm, schlossen diese Autoren, dass die beobachtete Hypotonie nicht auf eine Vasodilatation zurückzuführen sei. Die Hypotonie-Episoden nach Verabreichung von neuraxialen Opioiden während der Wehen sind vorübergehend, leicht zu behandeln und nicht unbedingt mit nachteiligen Veränderungen der fötalen Herzfrequenz verbunden.
Neurologische Verletzung
Neurologische Komplikationen, die in direktem Zusammenhang mit der Spinalanästhesie stehen, können durch Trauma, Nabelschnurischämie, Infektion und Neurotoxizität verursacht werden.
Nadeltrauma
Ein nadel- oder katheterinduziertes Trauma führt selten zu einer dauerhaften neurologischen Schädigung. Allerdings kamen Horlocker et al. in einer retrospektiven Überprüfung von 4767 aufeinanderfolgenden Spinalanästhetika bei Komplikationen des Zentralnervensystems zu dem Schluss, dass das Vorhandensein von Parästhesien während der Nadelplatzierung das Risiko einer anhaltenden Parästhesie signifikant erhöhte (p < 001). In dieser Übersicht wurde in 298 (6.3 %) Fällen während der Nadelplatzierung Parästhesie ausgelöst. Sechs Patienten berichteten über Schmerzen (anhaltende Parästhesien) nach Abklingen der Spinalanästhesie; Vier dieser Personen hatten Schmerzen, die innerhalb von 1 Woche verschwanden, und die Schmerzen der verbleibenden zwei verschwanden in 18–24 Monaten. Nach einer neueren Studie von Bigeleisen zur peripheren Nervenblockade führten Nervenpunktionen und intraneurale Injektionen nicht zwangsläufig zu neurologischen Verletzungen. Es gibt einige Gründe für ein mögliches erhöhtes Risiko für neurologische Folgeschäden nach der CSE-Technik. Bei der Single-Space-NTN-Technik der CSE kann das Einführen der Epiduralnadel und des Katheters nach der Verabreichung von spinalen Lokalanästhetika die Erkennung von Parästhesien verhindern, die den Anästhesisten vor einer Fehlplatzierung der Nadel warnen könnten. Eine höhere Inzidenz von Parästhesien während CSE ist ein anerkannter Faktor. Tatsächlich wurde berichtet, dass bei bis zu 11 % der Patienten, die sich einer CSE unterziehen, Parästhesien auftreten.
Browne et al. berichteten über eine 14 %ige Inzidenz von Parästhesien mit der Espocan-Nadel (18-Gauge-Tuohy-Epiduralnadel mit einem zusätzlichen Lumen in der Nadelschräge) und eine 42 %-ige Inzidenz mit einer herkömmlichen Tuohy-Epiduralnadel. In einer randomisierten prospektiven Studie berichteten McAndrew et al. in ähnlicher Weise, dass 37 % (17 von 46) der Frauen in der NTN-CSE-Gruppe und nur 9 % (4 von 43) in der SSS-Gruppe Parästhesien beim Einführen einer Spinalnadel hatten (p < 0.05). . Die verwendete Ausrüstung war ein 16-Gauge/26-Gauge-CSE-Kit und eine 26-Gauge-Bleistiftspitzen-Spinalnadel mit Einführhilfe (beide Sims Portex, Australien). Sie postulierten, dass die höhere Inzidenz von Parästhesien mit einer tieferen Penetration des Subarachnoidalraums mit der CSE-Technik zusammenhängen könnte. Interessanterweise hatte in dieser Studie keiner der Patienten anhaltende neurologische Symptome bei der Untersuchung am postoperativen Tag 1. Holloway et al. führten eine Pilotumfrage zu den Erfahrungen von Anästhesisten mit neurologischen Folgen nach Spinal- und CSE-Anästhesie in den Geburtskliniken im Vereinigten Königreich durch. Aufgrund des retrospektiven Charakters der Umfrage fehlten vielen gemeldeten neurologischen Problemen Details. Es gab jedoch keine offensichtlichen Unterschiede in der Inzidenz von Problemen im Zusammenhang mit CSE im Vergleich zu den SSS-Techniken.
Turner und Shaw schlugen die Möglichkeit vor, dass das schmerzhafte Einsetzen und die nachfolgende Wurzelschädigung durch die Verwendung von atraumatischen Spinalnadeln mit Bleistiftspitze verstärkt werden könnten. In dieser Umfrage wurden Probleme sowohl mit Whitacre- als auch mit Sprotte-Nadeln gemeldet, jedoch keine mit Quincke-Nadeln. Allerdings waren die Zahlen unter Verwendung von Quincke-Nadeln zu klein, um eine statistische Analyse zu ermöglichen. Gefährlicher als Wurzelschäden ist eine Schädigung des Rückenmarks selbst, und in dieser Umfrage gab es zwei Fälle von Konusschäden, einen mit CSE und einen mit SSS. Diese Komplikation ist kein Fehler atraumatischer Nadeln, sondern eher der Technik geschuldet. Es ist wichtig, sich daran zu erinnern, dass bei 19 % der Patienten das Rückenmark unterhalb von L1 endet. Noch besorgniserregender ist, dass in mehr als 50 % der Fälle der gewählte Raum falsch identifiziert wird. Daher sollte für CSE oder SSS ein Leerzeichen L3/L4 oder darunter gewählt werden.
Risiko einer Metalltoxizität bei CSE
Es wurde behauptet, dass während der NTN-CSE-Technik winzige Metallpartikel, die durch die Spinalnadel von der Innenkante der Tuohy-Nadel abgerieben wurden, in das Epidural- oder Spinalkompartiment eingeführt werden könnten. Um dieses Problem zu untersuchen, simulierten Holst und Kollegen die NTN-Technik in einem In-vitro-Modell. Sie verwendeten Atomabsorptionsspektrographie (AAS), um abgeriebene Metallpartikel zu identifizieren. Die Nadeln wurden dann unter einem Elektronenmikroskop untersucht. Sie berichteten, dass weder nach zweifacher noch nach fünffacher Punktion im Vergleich zu den Kontrollmessungen erhöhte Legierungsbestandteile in der Spüllösung festgestellt wurden. Nach fünf Einstichen und praxisüblicher Handhabung der Nadel konnten elektronenmikroskopisch keine Gebrauchsspuren am Innenschliff der Tuohy-Nadel festgestellt werden.
Gewebeentkernung
Das Entkernen von Gewebe ist ein Phänomen, das während einer Lumbalpunktion auftreten kann, bei der Gewebestücke durch die Nadel entfernt werden, wenn sie durch das Gewebe hindurchgeht und die Stücke im Subarachnoidalraum ablegt. Obwohl selten, können unerwünschte Folgen wie intraspinale iatrogene Epidermoidtumoren mit diesem Phänomen in Verbindung gebracht werden. Sharma et al. postulierten, dass die CSE-Technik weniger Epithelzellen in den Subarachnoidalraum einführt, verglichen mit der SSS ohne die Verwendung einer Einführhilfe. Diese Studie unterstützte die Hypothese jedoch nicht. Bei beiden Techniken kam es zu signifikanten Gewebestanzungen (CSE 88 % und SSS 96 %).
Infektiöse neurologische Komplikationen
Obwohl die Gesamtinzidenz von Infektionen und deren Folgen nach der Platzierung von CSE als äußerst gering angesehen wird, ist das relative Risiko im Vergleich zu einer spinalen oder epiduralen Technik allein nicht bekannt. In einer klassischen Studie berichteten Dripps und Vandam prospektiv über keine Fälle von Meningitis nach 10,098 Spinalanästhetika. Phillips et al. berichteten nach einer prospektiven Überprüfung von 10,440 solcher Fälle ebenfalls über keine Fälle. Diese Studien schlossen Patienten ein, die sich geburtshilflichen und urologischen Operationen unterziehen, von denen bekannt ist, dass sie mit perioperativer Bakteriämie assoziiert sind. Allerdings erschienen ab Mitte der 1990er Jahre Fallberichte über Meningitis nach CSE in den Fachzeitschriften.
Theoretisch wird angenommen, dass CSE mit einem erhöhten Meningitis-Risiko im Vergleich zur alleinigen Epiduralanästhesie verbunden ist, da die Dura (Schutzbarriere für das zentrale Nervensystem) während des CSE absichtlich punktiert wird und dann ein Fremdkörper, ein Epiduralkatheter, in der Nähe platziert wird. Der Epiduralkatheter kann nahe am Duralloch liegen und ist ein potenzieller Infektionsherd, insbesondere nach Bakteriämie. Eine Kontamination des Subarachnoidalraums kann durch Blutungen aufgrund eines Nadeltraumas bei einem bakteriämischen Patienten oder durch Versagen der aseptischen Technik erfolgen.
Mehrere Studien haben gezeigt, dass Gesichtsmasken die Ausbreitung von Organismen aus den oberen Atemwegen nach vorne und die Ausbreitung nach unten beim Sprechen und Drehen des Kopfes verhindern. Trotzdem ergab eine postalische Umfrage unter Mitgliedern der Obstetric Anesthetists Association im Vereinigten Königreich im Jahr 1996, dass mehr als die Hälfte der Befragten bei der Durchführung einer neuraxialen Anästhesie nicht routinemäßig Gesichtsmasken trugen. Im Jahr 2007 empfahl das Healthcare Infection Control Practices Advisory Committee (HICPAC) zum ersten Mal, dass bei Eingriffen an der Wirbelsäule chirurgische Masken getragen werden sollten, um Infektionen vorzubeugen. Diese Empfehlung wurde als Reaktion auf mehrere Berichte über Meningitis nach Myelographieverfahren ausgesprochen.
Im Jahr 2008 wurden dem Gesundheitsministerium des Staates New York drei Fälle von bakterieller Meningitis bei postpartalen Frauen gemeldet. Alle drei Frauen erhielten CSE für die Wehen. Streptococcus salivarius (ein normaler Kommensaler der Mundflora) wurde aus dem Liquor von zwei Patienten kultiviert. Der für alle drei Fälle zuständige Anästhesist berichtete von der routinemäßigen Verwendung von Masken bei neuroaxialen Eingriffen. Das Personal berichtete jedoch, dass es üblich sei, während dieser Verfahren entlarvte Besucher im Raum zu haben. Das Krankenhaus führte neue Richtlinien ein, um Besucher zu minimieren und Masken für alle Personen im Raum während neuroaxialer Analgesieverfahren zu verlangen. 2009 wurden dem Gesundheitsministerium von Ohio zwei ähnliche Fälle gemeldet. Der für diese beiden Fälle zuständige Anästhesist trug keine Maske. Liquorkulturen beider Patienten zeigten S. salivarius, und einer von ihnen starb an eitriger Meningoenzephalitis. Im Jahr 2009 berichteten Sankovsky et al. auch über einen Fall von S. salivarius-Meningitis im Anschluss an CSE für Wehen bei einer gesunden erstgeborenen Patientin. Der Anästhesist trug sterile Handschuhe und eine Maske, aber die Maske war bei früheren Eingriffen getragen worden. Diese Fälle unterstreichen die Bedeutung der Einhaltung etablierter Empfehlungen zur Infektionskontrolle während neuroaxialer Eingriffe, zu denen die Verwendung von Masken, das Waschen der Hände und die Einhaltung aseptischer Techniken gehören. Es ist wichtig, dass die Gesichtsmaske fest angebracht ist, um Mund und Nase zu bedecken, und nicht wiederverwendet wird.
Kopf- und Nackenschmerzen oder Nackensteifigkeit bei einem Patienten, der kürzlich eine Spinalanästhesie erhalten hat, wird häufig postduralem Punktionskopfschmerz (PDPH) zugeschrieben. Ein Fallbericht hob die Gefahren hervor, die mit einer versäumten Diagnose einer Meningitis verbunden sind. Bei der Patientin wurde fälschlicherweise eine Endometritis diagnostiziert, als sie 2 Tage lang nach einer unkomplizierten Epiduralanalgesie während der Wehen mit Kopfschmerzen, Erbrechen und Fieber auftrat. Ihr Zustand verschlechterte sich rapide und eine Meningitis wurde erst als zu spät diagnostiziert. Sie starb anschließend auf der Intensivstation.
Cauda Equina-Syndrom
Hyperbares Bupivacain wird während der CSE-Anästhesie häufig intrathekal verabreicht. Obwohl nach Verabreichung von Lidocain oder Mepivacain meistens über neurologische Probleme berichtet wird, wurden einige Fälle von Cauda-Equina-Syndrom nach intrathekaler Gabe von Bupivacain in einer CSE-Technik berichtet. Tariq berichtete über einen Fall eines 83-jährigen Mannes, der nach einer komplikationslosen CSE-Anästhesie für eine elektive Knieendoprothetik ein Cauda-Equina-Syndrom entwickelte.
Takasu et al. berichteten über eine 29-jährige Gebärende, die nach einer komplikationslosen CSE mit hyperbarem Bupivacain zur Kaiserschnittgeburt ein Cauda-Equina-Syndrom entwickelte. Kubina et al. beschrieben auch zwei Fälle von Cauda equina nach komplikationslosem CSE mit hyperbarem Bupivacain. Einer der Patienten litt jedoch an einer Spinalkanalstenose, was diese Komplikation erklären könnte. Kato et al. beschrieben einen Fall von Cauda-Equina-Syndrom nach CSE mit einer normalen Dosis von hyperbarem Bupivacain bei einem älteren Patienten ohne Spinalkanalstenose. Es wird angenommen, dass das Fehlen einer Schutzhülle in der Cauda equina, wenn die Spinalnerven und -wurzeln durch die Dura verlaufen, sie besonders anfällig für Verletzungen durch hohe Konzentrationen von Lokalanästhetika macht.
Postduralpunktionskopfschmerz
Die Inzidenz von PDPH nach CSE-Technik ist umstritten; Einige Autoren berichten von einer verringerten Inzidenz im Vergleich zur Epiduraltechnik allein, während andere von einer erhöhten Inzidenz berichten. Balestrieri berichtete, dass die Patienten, die eine konventionelle Epiduralanalgesie erhielten, mit größerer Wahrscheinlichkeit eine versehentliche Durapunktion erlitten (zweifache Zunahme; Epidural vs. CSE = 4.2 % vs. 1.7 %). Sie boten zwei mögliche Erklärungen für dieses Ergebnis an. Der erste Grund war, dass sie in der Regel CSE für Frauen wählten, die am häufigsten in frühen Wehen waren, und Epiduralanalgesie für Patientinnen in der schmerzhafteren aktiven Phase der Wehen reservierten. Daher war es wahrscheinlicher, dass sich die Patienten in der Epiduralgruppe während des Eingriffs bewegten und so einen „wet tap“ verursachten. Zweitens könnte während der CSE, wenn die Position der Epiduralnadel unsicher ist, die Spinalnadel eingeführt werden, um nach CSF zu suchen, und die Epiduralnadel könnte nicht weiter vorgeschoben werden, nachdem sie CSF in der Spinalnadel gesehen hat.
Andere Faktoren können auch das Auftreten von PDPH nach der CSE-Technik verringern. Es wurde gezeigt, dass die Verabreichung von intrathekalen Opioiden die Inzidenz von PDPH verringert. Die anschließende Infusion eines epiduralen Lokalanästhetikums erhöht den Subarachnoidaldruck und kann helfen, die Inzidenz von PDPH nach CSE zu verringern. Dunnet al. argumentierten, dass die mit der CSE-Technik verbundene absichtliche Duralpunktion das Risiko einer PDPH bei geburtshilflichen Patientinnen im Vergleich zur Epiduralanalgesie allein erhöhen würde. Die Verwendung von kleinen atraumatischen Spinalnadeln mit Bleistiftspitze (wie Whitacre, Pencan, Sprotte und Gertie Marx) wird die Inzidenz von PDPH bei Patienten, die CSE erhalten, stark reduzieren.
Chan und Paech berichteten über drei Fälle von anhaltendem CSF-Leck nach komplikationsloser CSE-Analgesie für die Wehen. Durch den β2-Transferrin-Immunfixationsassay wurde bestätigt, dass die austretende Flüssigkeit in zwei Fällen CSF war. Keiner der Patienten entwickelte PDPH oder andere Komplikationen. Howes und Lenz berichteten auch über eine CSF-Hautfistel bei zwei Patienten nach Epiduralanästhesie (nicht CSE) zur postoperativen Schmerzlinderung. Beide Patienten entwickelten PDPH erst nach Entfernung der Katheter und wurden erfolgreich mit Eigenblutpflaster behandelt.
Weitere Informationen finden Sie unter Postduralpunktionskopfschmerz.
Komplikationen im Zusammenhang mit Wehenanalgesie
Fötale Bradykardie
Berichte in der Literatur deuten auf eine erhöhte Häufigkeit nicht beruhigender Aufzeichnungen der fetalen Herzfrequenz (FHR) und fetaler Bradykardie im Zusammenhang mit CSE hin. Die Ätiologie der fötalen Bradykardie nach CSE bleibt schwer fassbar, kann aber mit einer akuten Verringerung der zirkulierenden mütterlichen Katecholaminspiegel nach dem fast sofortigen Einsetzen der Analgesie zusammenhängen. Darüber hinaus wurde postuliert, dass ein Ungleichgewicht zwischen Epinephrin- und Norepinephrinspiegeln (verringerte Epinephrinspiegel bei anhaltend hohen Norepinephrinspiegeln) ungehinderte α-Adrenozeptor-Effekte auf den Uterustonus mit erhöhtem Uterusgefäßwiderstand verursacht, was zu einem verringerten Uterusblutfluss führt.
Eine Metaanalyse von Mardirosoff und Kollegen ergab ein relatives Risiko von 1.81 für FHF-Anomalien, wenn intrathekale Opioide verwendet wurden. Das Risiko eines späteren Kaiserschnitts war jedoch nicht erhöht. Es gibt Hinweise auf eine Dosisbeziehung und ein häufigeres Auftreten besorgniserregender Herzfrequenzanomalien bei höheren Opioiddosen. Nicolet et al. führten eine prospektive Studie durch, um mütterliche Faktoren zu identifizieren, die an der fötalen Bradykardie nach CSE wegen Wehenschmerz beteiligt sind. Sie fanden heraus, dass die Höhe der mütterlichen Schmerzscores zum Zeitpunkt der Wehenanalgesie und das Alter der Mutter unabhängige Prädiktoren für fetale Bradykardie nach neuraxialer Analgesie für die Wehen waren.
Die daraus resultierende fetale Bradykardie war in der Regel nur von kurzer Dauer und klang in der Regel innerhalb von 5–8 Minuten ab. Eine retrospektive Studie mit 1240 Patientinnen, die regionale Wehenanalgesie (meist CSE) erhielten, und 1140 Patientinnen, die systemische Medikamente oder keine Analgesie erhielten, zeigte mit Raten von 1.3 % bzw. 1.4 % keinen signifikanten Unterschied in der Kaiserschnittrate. Diese Studie berichtete auch, dass bis zu 90 Minuten nach der intrathekalen Sufentanil-Verabreichung keine Notfall-Kaiserschnitte bei akutem fötalem „Distress“ erforderlich waren, wenn keine geburtshilflichen Indikationen vorlagen. Eine prospektive randomisierte Studie von Skupski et al. fand ebenfalls keinen Unterschied in der Rate der verlängerten Verzögerung zwischen der Epiduralanästhesie im Vergleich zu CSE für die Wehen (3.2 % vs. 6.2 %; p = 0.43).
AUSRÜSTUNG
Die CSE-Technik hat insbesondere in der Geburtshilfe an Popularität und Akzeptanz gewonnen. Spezielle Kits wurden für CSE hergestellt (z. B. B. Braun Medical Ltd., bestehend aus der standardmäßigen 16-Gauge-8-cm-Tuohy-Nadel mit einer 26-Gauge-Quincke-Spinalnadel). Verschiedene Bedenken bezüglich der CSE-Technik haben zu einigen Modifikationen der verwendeten Nadeln geführt.
Um den Epiduralkatheter von der Durapunktionsstelle wegzulenken, empfahlen Rawal et al., die Epiduralnadel nach der Durapunktion um 180° zu drehen. Bei diesem Manöver wird der Epiduralkatheter 2–2.5 mm von der Duralpunktionsstelle entfernt. Meikljohn demonstrierte jedoch unter Verwendung der postmortalen Dura Mater, dass die Drehung der Epiduralnadel die zum Durchstechen der Dura erforderliche Kraft signifikant verringerte und somit zu einem nassen Abstich führen könnte.
Kürzlich wurden CSE-Kits mit einer Öffnung in der hinteren Krümmung (hinteres Loch) der Epiduralnadel für den separaten Durchgang der Spinalnadel zur Verfügung gestellt (Figure 4). Diese Nadel und andere ähnliche können die Wahrscheinlichkeit einer Duralpassage des Epiduralkatheters verringern, indem sie den Katheter von der Durapunktionsstelle wegführen. Die Spinalnadel geht jedoch möglicherweise nicht immer durch die Spinalnadelöffnung und tritt möglicherweise durch die Huber-Spitze aus, wodurch der Vorteil des hinteren Lochs verloren geht (Figure 5).
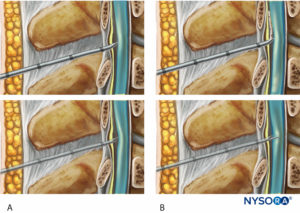
ABBILDUNG 4. Kombiniertes Spinal-Epidural-Kit mit einer Öffnung in der hinteren Krümmung für den separaten Durchgang der Spinalnadel.
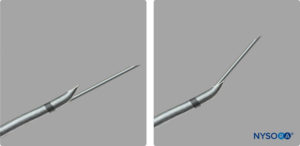
ABBILDUNG 5. Kombiniertes Spinal-Epidural-Kit mit aus dem hinteren Loch austretender Spinalnadel und der Huber-Spitze.
Joshi und McCarroll schlugen eine Technik vor, um den Austritt der Spinalnadel durch die Öffnung der Spinalnadel zu verbessern. Die modifizierte Technik bestand darin, zuerst die abgeschrägte Öffnung der Spinalnadel in die gleiche Richtung wie die Tuohy-Abschrägung auszurichten und dann die Spinalnadel um 10° in Richtung der Tuohy-Abschrägung zu biegen, während sie durch die Tuohy-Nadel vorgeschoben wurde. Diese Technik führt die Spitze der Spinalnadel zum Austritt durch das hintere Loch. Pan hat in einer prospektiven randomisierten Studie die Erfolgsrate der Spinalnadel, die durch die Spinalnadelöffnung austritt, in zwei allgemein erhältlichen CSE-Nadelkits mit einem Lumen und zwei Öffnungen bewertet. Bei den CSE-Kit-Studien handelte es sich zunächst um das Espocan CSE-Kit (Braun Medical Ltd.), das aus einer standardmäßigen 18-Gauge-Tuohy-Nadel mit einer 26-Gauge-Mantel-Quincke-Spinalnadel besteht, die 12 mm über die Spitze der Tuohy-Nadel durch das hintere Loch hinausragt . Die Hülse an der Spinalnadel wurde entwickelt, um die Spinalnadel zum Austritt durch das hintere Loch zu führen. Das zweite war das Espocan CSE-Kit (Braun Medical Ltd.), das aus der gleichen Epiduralnadel mit einer 27-Gauge-Sprotte-Spinalnadel ohne Hülse besteht, die 13 mm über die Spitze der Tuohy-Nadel durch das hintere Loch hinausragt. Sie führten 1600 Versuche durch, darunter die von Joshi und McCarroll beschriebene modifizierte Technik. Die modifizierte Technik verbesserte die Erfolgsrate des Austritts der Spinalnadel durch das hintere Loch von 67 % auf 94 % für das erste Kit und von 50 % auf 81 % für das zweite Kit; Die kraniale Ausrichtung der Tuohy-Nadelschräge verbesserte die Erfolgsrate weiter auf 96 % bzw. 91 %. Insgesamt hatte die gesleevte Spinalkanüle eine bessere Erfolgsquote als die ungesleevte Spinalkanüle.
Das Versäumnis der Spinalnadel, durch das hintere Loch auszutreten, kann auch zu einem Biegen der Spinalnadel und einem geringeren Vorstehen über die Spitze der Tuohy-Nadel hinaus führen. Dies kann zu der erhöhten Misserfolgsrate der Durapunktion beitragen. Die ideale Länge des Spinalnadelvorsprungs wird mit mindestens 12–13 mm angegeben. In einer prospektiven, randomisierten Studie mit 40 Patienten berichteten Joshi und McCarroll von einer 15 %igen Ausfallrate der CSF-Rückführung, wenn die Spinalnadel nur 10 mm über die Spitze der Tuohy-Nadel hinausragte, und von 0 % bei einem 13 mm-Vorsprung. Riley et al. berichteten über ähnliche Ergebnisse beim Vergleich von 24-Gauge-Sprotte (9 mm Vorsprung über die Tuhoy-Spitze hinaus und 17 % Ausfall der Liquorgewinnung) und Gertie Marx (17 mm Vorsprung und 0 % Ausfallrate). Die Anzahl der Patienten, die eine PDPH entwickelten und ein Blutpflaster benötigten, war bei Gertie Marx größer als bei der Sprotte-Nadel. Dieser Unterschied war jedoch statistisch nicht signifikant. Es ist möglich, dass die längere Spinalnadel auch den anterioren Teil der Dura durchstochen und somit ein größeres Liquorleck verursacht haben könnte. Höhere Raten von Parästhesien wurden auch (anekdotisch) mit der 127-mm-Nadel festgestellt, und die 124-mm-Gertie-Marx-Nadel wurde als ausgezeichneter Kompromiss vorgeschlagen.
Herbstman et al. verglichen vier Spinalnadeln mit Bleistiftspitze, die üblicherweise in der CSE-Technik verwendet werden, und berichteten, dass längere Spinalnadeln mit signifikant mehr vorübergehenden Parästhesien assoziiert waren (Gertie Marx 15-mm-Vorwölbung mit 29 % Inzidenz; Whitacre 10-mm-Vorwölbung mit 17 % Inzidenz ). Der Erfolg bei der Gewinnung von Liquor und das Auftreten von PDPH unterschieden sich nicht zwischen den vier Nadeln.
Die herkömmliche Spinalnadel im CSE-Kit, die nicht in der Epiduralnadel einrastet, kann während der Injektion von Spinalmedikamenten schwierig zu handhaben und zu stabilisieren sein. Die Verschiebung der Spinalnadel während der Aspiration des Liquors und der Injektion kann zu einem Fehlschlagen der Anästhesie führen oder die Spinalnadel tiefer drücken, was zu einer Nervenschädigung oder einer Perforation der vorderen Dura führen kann. Um dieses Problem zu lösen, schlug Simsa ein externes Fixierungsgerät vor. Diese Vorrichtung ist jedoch etwas umständlich zu handhaben.
Vor kurzem wurden Spinalnadeln mit einer einstellbaren Verriegelungsvorrichtung eingeführt (CSEcure und Adjustable Durasafe CSE-Nadel). Studien zu den arretierbaren Verlängerungen berichteten, dass sie sichere und stabile Bedingungen während der Platzierung der Spritze und der Injektion bieten. Beide Studien berichteten jedoch häufig, dass die Duraperforation mit den Verriegelungsnadeln nicht ertastet werden konnte (15.3 % mit CSFcure und 25 % mit Adjustable Durasafe). Dafür gab es keine eindeutige Erklärung.
Bei einer CSE-Technik kann der Epiduralkatheter manchmal nicht intravaskulär eingefädelt oder eingefädelt werden, nachdem die intrathekalen Medikamente injiziert wurden. Um dieses Problem zu lösen, wurde ein CSE-Kit mit zwei Lumen und zwei Öffnungen entwickelt, in das ein Epiduralkatheter eingeführt werden kann, bevor die Spinalnadel und das Medikament eingeführt werden. Dies ist möglich, weil es zwei getrennte Lumen für den Katheter und die Spinalnadel gibt (Figure 6). Kürzlich wurde in Europa eine zweilumige CSE-Nadel vermarktet (Epistar; Medimex, Deutschland).

ABBILDUNG 6. CSE-Kit mit zwei Lumen und zwei Öffnungen.
KONTROVERSE THEMEN IN DER CSE-TECHNIK
Testdosis
Die Frage, ob eine Testdosis bei der Verabreichung von Geburtsschmerzmitteln erforderlich ist, wird kontrovers diskutiert. Da häufig sehr verdünnte Lösungen von LA verwendet werden und die Aspiration oft diagnostisch ist, glauben einige Autoren, dass eine herkömmliche Testdosis unnötig ist. Da die Katheteraspiration jedoch nicht immer prädiktiv ist (insbesondere bei Verwendung eines Epiduralkatheters mit einer einzigen Öffnung), halten andere an der Bedeutung einer Testdosis fest, um die Erkennung der intrathekalen oder intravaskulären Platzierung eines Epiduralkatheters zu verbessern.
Ein Teil der Kontroverse um das Testen von Epiduralkathetern betrifft die Verwendung von Epinephrin. Es wurde gezeigt, dass Epinephrin bei Freiwilligen und chirurgischen Patienten eine zuverlässige Erhöhung der Herzfrequenz bewirkt, wenn die Epiduralanästhesie in einem Blutgefäß platziert wurde. Bei gebärenden Frauen kann jedoch die mütterliche Herzfrequenzvariabilität aufgrund des Schmerzes der Uteruskontraktionen die Interpretation der Herzfrequenzreaktion verwirren, und intravenöses Epinephrin kann schädliche Auswirkungen auf den Uterusblutfluss haben.
Mittel zur Verbesserung der Zuverlässigkeit einer Epinephrin-Testdosis umfassen das Injizieren der Dosis zwischen Uteruskontraktionen und das Wiederholen der Testdosis, wenn die Reaktion zweideutig ist. Der Mangel an Sensitivität und Spezifität der Testdosis stellt jedoch ihre Nützlichkeit als diagnostisches Instrument in Frage.
Leighton und Kollegen haben ein alternatives Mittel zum Testen eines Epiduralkatheters für die intravaskuläre Platzierung beschrieben. Sie befürworteten die Injektion von 1–2 ml Luft in den Epiduralkatheter, während sie mit dem mütterlichen externen Doppler-Monitor über das Präkordium auf Anzeichen von Luft abhörten.
Mit Berichten über die subarachnoidale Verabreichung von Chloroprocain ist es möglich, dass dieses Mittel in Zukunft zum Testen von Epiduralkathetern verwendet wird. Vorsicht ist jedoch geboten, da konservierungsmittelhaltiges Chloroprocain auch im Handel erhältlich ist. Wenn eine kontinuierliche Infusion eines verdünnten Lokalanästhetikums verabreicht wird und der Patient sich ohne motorische Blockade wohlfühlt, ist eine ordnungsgemäße Platzierung des Epiduralkatheters sehr wahrscheinlich. Das heißt, wenn der Epiduralkatheter intravaskulär wäre, sollte der Patient eine unzureichende Schmerzlinderung erfahren, und wenn der Katheter subarachnoidal wäre, würde sich eine solide motorische Blockade entwickeln. Obwohl Infusionen von ultraverdünnten Lokalanästhetika keine ernsthafte Gefahr darstellen, gilt dies nicht für konzentrierte Lokalanästhetika, die für operative Entbindungen verwendet werden. Einige Autoren haben vorgeschlagen, dass eine Testdosis für jede Gebärende, die eine Epiduralanästhesie erhält, unerlässlich ist. Unabhängig von der angewandten Technik schreibt die sichere Praxis der Verabreichung von Epiduralanästhesie bei Wehen eine anfängliche Katheteraspiration, inkrementelle Injektionen und eine kontinuierliche Überwachung auf Hinweise auf Toxizität des Lokalanästhetikums vor.
Positionierung für CSE
Neuraxiale Blockaden werden häufig bei sitzenden Patienten durchgeführt, insbesondere bei fettleibigen Personen, da die Mittellinie leicht erkennbar ist. Es hat sich gezeigt, dass die sitzende Position eine bessere Flexion der Wirbelsäule bei den Gebärenden ermöglicht. Zudem zeigte sich, dass der Hautabstand zum Epiduralraum bei der Epiduralpunktion in Seitenlage signifikant größer war als in sitzender Position. Diese Abstandsänderung kann zu einer Verschiebung des Katheters führen, wenn der Patient aus der sitzenden Position in die seitliche Position gedreht wird, was zu einer unzureichenden Analgesie führt.
Yun et al. verglichen die Wirkungen der Einleitung einer CSE-Anästhesie in sitzender gegenüber seitlicher Position bei gesunden Frauen, die sich einem elektiven Kaiserschnitt unterzogen. Der Schweregrad der Hypotonie, gemessen an der maximalen prozentualen Abnahme des systolischen Blutdrucks gegenüber der Kontrolle, sowie deren Dauer waren in der sitzenden Gruppe signifikant größer (p < 0.05). Patienten in der sitzenden Gruppe benötigten doppelt so viel Ephedrin zur Behandlung von Hypotonie als die in der seitlich liegenden Gruppe. Der Grund für den Unterschied in der Schwere der Hypotonie war nicht klar. Sie postulierten, dass dies mit einer langsameren Erholung von der venösen Ansammlung in den unteren Extremitäten zusammenhängt, wenn aus der anfänglichen Sitzposition eine Rückenlage eingenommen wird. Diese Autoren kamen zu dem Schluss, dass die zur Induktion von CSE verwendete Position in Fällen in Betracht gezogen werden sollte, die mit einem höheren mütterlichen oder fetalen Risiko durch Hypotonie verbunden sind.
Die traditionelle Lehre besagt, dass die Ausbreitung hyperbarer intrathekaler Lösungen der Schwerkraft folgt. Lewis et al. verglichen die Entwicklung von Wirbelsäulenblockaden in der linken Seitenlage mit einer Keillage in Rückenlage nach Durchführung des CSE in sitzender Position. Die intrathekale Medikation bestand aus 2 ml 0.5 % hyperbarem Bupivacain mit 15 μg Fentanyl. Die linke Seitenlage erzeugte keinen einseitigen Block. Die Linksseitenlage war mit einem langsameren Einsetzen der Blockade verbunden (p = 004), erzeugte aber schließlich eine Spinalblockade, die in ihren Eigenschaften derjenigen ähnelte, die in der Keillage in Rückenlage erhalten wurde. Es ist bekannt, dass die linke Seitenlage das mütterliche Herzzeitvolumen verbessert, und der mögliche Nutzen für den Fötus kann einen langsameren Beginn überwiegen.
ZUSAMMENFASSUNG
Die CSE-Technik ist eine etablierte Methode für verschiedene Arten von Operationen, insbesondere in der Geburtshilfe. In unserer Einrichtung ist die CSE-Technik die am häufigsten durchgeführte regionale Technik für Wehenanalgesie (97 %) sowie Kaiserschnittentbindung (54 %). CSE bietet viele Vorteile; es stellt ein Verfahren bereit, um eine neuraxiale Anästhesie und Analgesie in zahlreichen klinischen Situationen zu verabreichen.
Die CSE-Technik bietet die Vorteile sowohl der Spinal- als auch der Epiduraltechnik und hat daher eine hohe Erfolgsquote bei der Bereitstellung einer Regionalanästhesie. CSE bietet ein schnelles Einsetzen und die Fähigkeit, auf ein gewünschtes sensorisches Niveau zu titrieren, die Dauer der Blockade zu kontrollieren und postoperative Analgesie zu liefern. Ein weiterer Vorteil der CSE ist die Erleichterung des Eintritts der Spinalnadel in den Subarachnoidalraum. Die Tuohy-Nadel dient als Führung für die Spinalnadel bis fast zum Subarachnoidalraum. Dies ermöglicht die Verwendung kleinerer atraumatischer Spinalnadeln, bei denen die PDPH fehlt oder selten ist.
Die Nachteile der CSE bestehen darin, dass die kombinierte Technik potenzielle Nebenwirkungen wie PDPH, das erhöhte Risiko einer Kathetermigration in den Subarachnoidalraum und vorübergehende Parästhesien durch die Spinalnadel einführt. Obwohl das Risiko gering ist, wurden eine Reihe von Ausrüstungsmodifikationen vorgeschlagen und entwickelt, um ein Eindringen des Epiduralkatheters durch das von der Spinalnadel erzeugte Duralloch zu vermeiden.
Die ideale Länge des Überstands der Spinalnadel über die Spitze der Epiduralnadel wird mit mindestens 12–13 mm angegeben. Es wurde gezeigt, dass längere Spinalnadeln mit einer signifikant höheren Inzidenz von vorübergehenden Parästhesien assoziiert sind. Bei kürzeren Nadeln (< 10 mm Vorsprung) kann es unmöglich sein, Liquor durch die Spinalnadel zu erhalten, was zu einem Versagen der spinalen Komponente der Technik führen kann. CSE-Versagen hängt auch mit einer fehlerhaften Punktionsstelle oder Achsenabweichung während des Nadelvorschubs zusammen. Das Risiko von Infektionen, Hämatomen und neurologischen Schäden steigt mit mehreren Versuchen und mehreren Manipulationen der Nadeln, aber es ist nicht klar, ob die CSE-Technik diese Risiken erhöht.
Weiterlesen Epiduralanästhesie und Analgesie
REFERENZEN
- Rodgers A, Walker N, Schug S, et al. Reduktion der postoperativen Mortalität und Morbidität mit Epidural- oder Spinalanästhesie: Ergebnisse aus Übersicht randomisierter Studien. BMJ 2000;321:1493–1504.
- Buhre W, Rossaint R: Perioperatives Management und Monitoring in der Anästhesie. Lancet 2003;362:1839–1846.
- Kehlet H, Wilmore DW: Multimodale Strategien zur Verbesserung des chirurgischen Ergebnisses. Am J Surg 2002;183:630–641.
- Holmström B, Laugaland K, Rawal N, et al: Kombinierte spinale Epiduralblockade versus spinale und epidurale Blockade für orthopädische Chirurgie. Can J. Anesth 1993;40:601–606.
- Stienstra R, Dahan A, Alhadi ZRB, et al: Wirkmechanismus eines epiduralen Top-ups bei kombinierter spinaler Epiduralanästhesie. Anesth Analg 1996;83:382–386.
- Stienstra R, Dilrosun-Alhadi BZR, Dahan A, et al: The epidural top-up in kombinierter Spinal-Epidural-Anästhesie: The effect of volume versus dose. Anesth Analg 1999;88:810–814.
- Blanshard HJ, Cook TM: Verwendung der kombinierten Spinal-Epiduralanästhesie durch geburtshilfliche Anästhesisten. Anästhesie 2004;59(9):922–923.
- Norris MC. Sind kombinierte spinale Epiduralkatheter zuverlässig. Int J Obsted Anaesth 2000;9:3–6.
- Reynolds F: Schädigung des Conus medullaris nach Spinalanästhesie. Anästhesie 2001;56:238–247.
- Cook TM: Kombinierte Spinal-Epidural-Techniken. Anästhesie 2000; 55:42–64.
- Hughes D, Simmons SW, Brown J, Cyna AM: Kombinierte Spinalepidural- versus Epiduralanalgesie bei der Geburt. Cochrane Database Syst Rev 2003;(4):CD003401.
- Poulakka R, Pitkanen MT, Rosenberg PH: Vergleich der technischen und Blockeigenschaften verschiedener kombinierter Spinal- und Epiduralanästhesietechniken. Reg Anesth Pain Med 2001;26:17–23.
- Cherng YG, Wang YP, Liu CC, Shi JJ, Huang CC: Kombinierte Spinal- und Epiduralanästhesie zur abdominalen Hysterektomie bei einer Patientin mit Myotoner Dystrophie. Fallbericht. Reg Anesth 1994;19(1):69–72.
- Mane RS, Patil MC, Kedareshvara KS, Sanikop CS: Kombinierte spinale Epiduralanästhesie zur laparoskopischen Appendektomie bei Erwachsenen: Eine Fallserie. Saudi J Anaesth 2012;6:27–30.
- Browne IM, Birnbach DJ, Stein DJ, O'Gorman DA: Ein Vergleich von Espocan- und Tuohy-Nadeln für die kombinierte Spinal-Epidural-Technik zur Analgesie der Wehen. Anesth Analg 2005;101:535–540.
- Hermanides J, Hollmann MW, Stevens MF, Lirk P: Fehlgeschlagene Epiduralanästhesie: Ursachen und Management. Br. J. Anaesth 2012;109:144–154.
- Viscomi CM, Rathmell JP, Pace NL: Dauer der intrathekalen Wehenanalgesie. Frühe versus fortgeschrittene Wehen. Anesth Analg 1997;84:1108–1112.
- Collis RE, Davies DW, Aveling W: Randomisierter Vergleich der kombinierten spinalen Epidural- und Standard-Epiduralanalgesie in der Geburt. Lancet 1995;345:1413–1416.
- Palmer CM, Randall CC, Hays R, et al: The dose-response relation of intrathecal fentanyl for wehenanalgesia. Anesthesiology 1998;88:355–361.
- Campbell DC, Camann WR, Datta S, et al.: The addition of bupivacaine to intrathecal sufentanil for wehenanalgesie. Anesth Analg 1995;81:305–309.
- Sia AT, Chong JL, Chiu JW: Kombination von intrathekalem Sufentanil 10 mcg plus Bupivacain 2.5 mg zur Analgesie der Wehen. Reicht die halbe Dosis? Anesth Analg 1999;88:362–366.
- Hughes D, Hill D, Fee JP: Intrathekales Ropivacain oder Bupivacain mit Fentanyl für die Wehen. Br. J. Anaesth 2001;87:733–737.
- Vercauteren MP, Haus G, De Decker K, et al: Levobupivacain kombiniert mit Sufentanil zur intrathekalen Wehenschmerzlinderung: Ein Vergleich mit racemischem Bupivacain. Anesth Analg 2001;93:996–1000.
- Van de Velde, M., Dreelinck, R., Dubois, J., et al. Bestimmung der vollständigen Dosis-Wirkungs-Beziehung von intrathekalem Bupivacain, Levobupivacain und Ropivacain, kombiniert mit Sufentanil, zur Analgesie der Wehen. Anesthesiology 2007;106:149–156.
- Wilson MJ, MacArthur C, Cooper GM, Shennan A; COMET Study Group UK: Ambulation in Wehen- und Entbindungsmodus: Eine randomisierte kontrollierte Studie zur hochdosierten vs. mobilen Epiduralanalgesie. Anästhesie 2009;64:266–272.
- Tsen L, Thue B, Datta S, et al: Ist eine kombinierte Spinal-Epidural-Analgesie im Vergleich zu einer konventionellen Epidural-Analgesie mit einer schnelleren zervikalen Dilatation bei Nulliparapatienten verbunden? Anesthesiology 1999;91:920–925.
- Wong CA, Scavon BM, Peaceman AM, et al: Das Risiko einer Kaiserschnittentbindung mit neuraxialer Analgesie, die früh im Vergleich zu spät in der Wehen verabreicht wird. N. Engl. J. Med. 2005;352(7):655–665.
- Pascual-Ramirez J, Haya J, Pérez-López FR, et al: Wirkung der kombinierten spinalen Epiduralanalgesie im Vergleich zur Epiduralanalgesie auf Wehen und Entbindungsdauer. Int J Gynaecol Obstet 2011;114:246–250.
- Carrie LES, O'Sullivan GM: Subarachnoidales Bupivacain 0.5 % für den Kaiserschnitt. Eur J Anaesthesiol 1984;1:275–283.
- Crowhurst J, Birnbach DJ: Neuraxialer Block mit niedriger Dosis. Auf dem Weg ins neue Jahrtausend. Anesth Analg 2000;90:241–242.
- Blumgart CH, Ryall D, Dennison B, et al: Mechanismus der Verlängerung der Spinalanästhesie durch extradurale Injektion eines Lokalanästhetikums. Br. J. Anaesth 1992;169:457.
32. Kawasw H., Sumikura H., Kamada T., et al.: Fall einer externen kranialen Version unter kombinierter Spinal-Epiduralanästhesie, gefolgt von einer vaginalen Entbindung. Masui 2009;58:637–640. - Sullivan JT, Grobman WA, Bauchat JR, et al: Eine randomisierte kontrollierte Studie über die Wirkung einer kombinierten Spinal-Epidural-Analgesie auf den Erfolg der externen kranialen Version für Beckenendlage. Int J Obstet Anesth 2009;18:328–334.
- Pan PH, Bogard TD, Owen MD: Häufigkeit und Merkmale von Fehlern bei der geburtshilflichen neuraxialen Analgesie und Anästhesie: Eine retrospektive Analyse von 19,259 Geburten. Int J Obstet Anesth 2004;13(4):227–233.
- Eappen S, Blinn A, Segal S: Inzidenz des Ersatzes von Epiduralkathetern bei Gebärenden: Eine retrospektive Diagrammübersicht. Int J Obstet Anesth 1998;7:220–225.
- Choi DH, Park YD: Vergleich der kombinierten Spinal-Epiduralanästhesie und der Spinalanästhesie für den Kaiserschnitt. IMRAPT 2002;14:A129.
- Reyes M, Pan PH:. Sehr niedrig dosierte Spinalanästhesie für den Kaiserschnitt bei einem krankhaft adipösen Patienten mit Präeklampsie und ihre möglichen Auswirkungen. Int J Obstet Anesth 2004;13:99–102.
- Ranasinghe JS, Steadman J, Toyama T, Lai M: Die kombinierte Spinal-Epiduralanästhesie ist besser als die Spinal- oder Epiduralanästhesie allein für Kaiserschnittgeburten. Br. J. Anaesth 2003;91:299–300.
- Lim Y, Loo CC, Goh E: Ultraniedrig dosierte kombinierte Spinal- und Epiduralanästhesie für den Kaiserschnitt. Int J Obstet Anesth 2004;13:198–200.
- Peng PW, Chan VW, Perks A: Minimale wirksame Anästhesiekonzentration von hyperbarem Lidocain für die Spinalanästhesie. Can J. Anesth 1998;45:122–129.
- Urmey WF, Stanton J, Peterson M, et al: Kombinierte Spinal-Epiduralanästhesie für ambulante Operationen. Dosis-Wirkungs-Eigenschaften von intrathekalem isobarem Lidocain unter Verwendung einer 27-Gauge-Whitacre-Nadel. Anesthesiology 1995;83:528–534.
- Norris MC, Kombinierte Spinal-Epiduralanästhesie für urologische und vaskuläre Eingriffe an den unteren Extremitäten. Tech Reg Anaesth Pain Manag 1997;1:131–136.
- Patel NP, Armstrong SL, Fernando R, et al: Combined spinal epidural vs. epidural wehenanalgesie: Verringert die anfängliche intrathekale Analgesie die nachfolgende minimale lokale analgetische Konzentration von epiduralem Bupivacain? Anästhesie 2012;67:584–593.
- Takiguchi T, Okano T, Egawa H, et al: Die Wirkung der epiduralen Kochsalzinjektion auf den Analgetikaspiegel während einer kombinierten Spinal- und Epiduralanästhesie, bewertet klinisch und myelographisch. Anesth Analg 1997;85:1097–1100.
- Blumgart CH, Ryall D, Dennison B, et al: Mechanismus der Verlängerung der Spinalanästhesie durch extradurale Injektion eines Lokalanästhetikums. Br. J. Anaesth 1992;69:457–460.
- Loubert C, Hallworth S, Fernando R, et al: Epidurale Volumenerweiterung in kombinierter spinaler Epiduralanästhesie für elektiven Kaiserschnitt: eine randomisierte kontrollierte Studie. Anesth Analg 2011;113:811–817.
- Doganci N, Apan A, Tekin O, Kaymak C: Epidurale Volumenexpansion: Gibt es einen Deckeneffekt? Minerva Anestesiol 2010;76:334–339.
- Tyagi A, Kumar A, Sethi AK, Mohta M: Epidurale Volumenerweiterung und intrathekale Dosisanforderung: Reines versus hyperbares Bupivacain. Anesth Analg 2008;107:333–338.
- Tyagi A, Girotra G, Kumar A, et al: Single-Shot Spinalanästhesie, kombinierte Spinal-Epidural- und Epidural-Volumenerweiterung für elektiven Kaiserschnitt: Ein randomisierter Vergleich. Int J Obstet Anesth 2009; 18:231–236.
- Fan SZ, Suseti L, Wang YP, et al: Niedrig dosiertes intrathekales hyperbares Bupivacain in Kombination mit epiduralem Lidocain für den Kaiserschnitt – eine Balance-Block-Technik. Anesth Analg 1994;78:474–477.
- Macfarlane A, Pryn A, Litchfield K, et al: Randomisierte kontrollierte Studie von kombinierte spinale Epiduralanästhesie vs. Spinalanästhesie für elektiven Kaiserschnitt: Vasopressorbedarf und kardiovaskuläre Veränderungen. Eur J Anaesth 2009;26:47–51.
- Landau R, Giraud R, Morales M, Kern C, Trindade P: Sequentielle kombinierte Spinal-Epiduralanästhesie für den Kaiserschnitt bei einer Frau mit einem doppelten rechten Ventrikel. Acta Anaesthesiol Scand 2004; 48:922–926.
- Parneix M, Fanou L, Morau E, Colson P: Niedrig dosiertes vombined Spinalepidural Anästhesie für einen Kaiserschnitt bei einem Patienten mit Eisenmenger-Syndrom. Int. J. Obstet Anesth 2009;18:81–84.
- Agarwal A, Garg R, Joshi A, Verma S: Kombinierte spinale Epiduralanästhesie mit epiduraler Volumenerweiterungstechnik zur Hysterektomie bei Patienten mit nicht gelinderter zyanotischer Herzkrankheit – ein Fallbericht. Acta Anaesthesiol Belg 2010;61:159–161.
- Monat RC, Vaida SJ: Eine kombinierte Spinal-Epidural-Technik zur Wehenschmerzlinderung und symptomatischen Linderung bei zwei Gebärenden mit idiopathischer intrakranieller Hypertonie. Int J Obstet Anesth 2012;21:192–194.
- Thorén T., Holmström B., Rawal N. et al.: Sequentielle kombinierte spinale Epiduralblockade versus spinale Blockade bei Kaiserschnitt: Auswirkungen auf die mütterliche Hypotonie und die neurologische Verhaltensfunktion des Neugeborenen. Anesth Analg 1994;78:1087–1092.
- Simmons SW, Cyna AM, Dennis AT, Hughes D: Kombinierte Spinal-Epidural- versus Epiduralanalgesie bei der Geburt. Cochrane Database Syst Rev 2007;(3):CD003401.
- Van De Velde M: Kombinierte spinale Epiduralanalgesie für Wehen und Entbindung: Eine ausgewogene Sichtweise basierend auf Erfahrung und Literatur. Acta Anaesth Belg 2009;60:109–122.
- Hoffmann VL, Vercauteren MP, Vreugde JP, Hans GH, Coppejans HC, Adriaensen HA: Tiefe des hinteren Epiduralraums: Sicherheit des Widerstandsverlusts und hängender Tropfentechniken. Br. J. Anaesth 1999;83: 807–809.
- Han KR, Kim C, Park SK, Kim JS: Abstand zum zervikalen Epiduralraum des Erwachsenen. Reg Anesth Pain Med 2003;28:95–97.
- McAndrew CR, Harms P: Parästhesien während einer Nadel-durch-Nadel-Kombination an der Wirbelsäulen-Epiduralanästhesie im Vergleich zu einer Single-Shot-Wirbelsäulenanästhesie für einen elektiven Kaiserschnitt. Anaesth Intensive Care 2003;31:514–517
- Hoffmann VL, Vercauteren MP, Buczkowski PW, Vanspringel GL: Ein neuer kombinierter Spinal-Epidural-Apparat: Messung der Distanz zum Epidural- und Subarachnoidalraum. Anästhesie 1997;52:350–355.
- Cousins MJ, Bridenbaugh PO: Neuronale Blockade in der klinischen Anästhesie und Schmerzbehandlung, 3. Aufl. Lippincott-Raven, 1998, S. 252–255.
- Watts RW: Der Einfluss von Fettleibigkeit auf die Beziehung zwischen Body-Mass-Index und dem Abstand des Epiduralraums von der Haut. Anesth Intensive Care 1993;21;309–310.
- Lirk P, Moriggl B, Colvin J, et al: Die Inzidenz von lumbalen Ligamentum flavum-Mittellinienlücken. Anesth Analg 2004;98:1178–1180.
- Cook TM: Kombinierte Spinal-Epidural-Techniken. Anästhesie 2000;55: 42–64.
- Landau R: Kombinierte Spinal-Epidural-Analgesie bei Wehen: Durchbruch oder ungerechtfertigte Invasion? Semin Perinatol 2002;26:109–121.
- Rawal N, Holmstrom B: Die kombinierte Spinal-Epidural-Technik. Best Practise Res Clin Anaesthesiol 2003;17:347–364.
- Soresi AL: Episubduralanästhesie. Anesth Analg 1937;16:306–310.
- Curelaru I: Langzeit-Subarachnoidalanästhesie mit kontinuierlichem Epiduralblock. Prak Anaesth 1979;14:71–78.
- Brownridge P: Zentrale Neuralblockade und Kaiserschnitt, Teil 1. Review und Fallserie. Anaesth Intensive Care 1979;7:33–41.
- Brownridge P: Epidurale und subarachnoidale Analgesie für einen elektiven Kaiserschnitt. Anästhesie 1981;36:70.
- Coates MB: Kombinierte Subarachnoidal- und Epiduraltechniken. Anästhesie. 982;37:89–90.
- Mumtaz MH, Daz M, Kuz M: Eine weitere Single-Space-Technik für die orthopädische Chirurgie. Anästhesie 1982;37:90.
- Carrie LES, O'Sullivan GM: Subarachnoidales Bupivacain 0.5 % für den Kaiserschnitt. Eur J Anaesth 1984;1:275–283.
- Turner MA, Reifenberg NA. Kombinierte spinale Epiduralanalgesie. Die Single-Space-Double-Barrel-Technik. Int J Obstet Anesth 1995;55: 158–160.
- Cook TM: Eine neue kombinierte Spinal-Epidural-Technik. Int J Obstet Anesth 1999;55:3–6.
- Brownridge P: Epidural- und Subarachnoidalanalgesie bei elektivem Kaiserschnitt. Anästhesie 1981;55:70.
- Carrie LES: Epidural versus kombinierter spinaler Epiduralblock für Kaiserschnitt. Acta Anaesth Scand 1988;55:5956.
- Morris GN, Kinsella M, Thomas TA: Pencil-Point-Nadeln und kombinierter spinaler Epiduralblock. Warum Nadel durch Nadel? Anästhesie 1998;55: 1132.
- Kestin IG: Spinalanästhesie in der Geburtshilfe. Br. J. Anaesth 1991;55:663.
- Eldor J: Kombinierte Spinal-Epiduralanästhesie durch das Portex-Set. Anästhesie 1993;55:836.
- Soni AK, Sarna MC. Kombinierte spinale Epiduralanalgesie. Die Single-Space-Double-Barrel-Technik. Int J Obstet Anesth 1996;55:206–207.
- Sakuma N., Hori M., Suzuki H. et al.: Ein abgescherter und sequestrierter Epiduralkatheter: Ein Fallbericht. Masui 2004;53(2):198–200.
- Roberts E, Brighouse D: Kombinierte Spinal-Epiduralanästhesie für den Kaiserschnitt. Anästhesie 1992;55:1006.
- Cook TM: 201 kombinierte Spinal-Epiduralanästhesie mit separater Nadeltechnik. Eur J Anaesthesiol 2004;21:679–683.
- Levin A, Segal S, Datta S: Verändert die kombinierte Spinalepiduralanalgesie das Auftreten von Parästhesien während der Einführung eines Epiduralkatheters? Anesth Analg 1998;55:44551.
- Familton MJG, Morgan BM: „Nadel-durch-Nadel“-Technik für die kombinierte Spinal-Extradural-Anästhesie in der Geburtshilfe. Br J Anaesth 1992; 55:327.
- Patel M, Samsoon G, Swami A, Morgan B: Körperhaltung und die Ausbreitung von hyperbarem Bupivacain bei Gebärenden unter Verwendung der kombinierten Spinal-Epidural-Technik. Can J Anaesth 1993;55:943–946.
- McAndrew CR, Harms P: Parästhesien während einer Nadel-durch-Nadel-Kombination an der Wirbelsäulen-Epiduralanästhesie im Vergleich zu einer Single-Shot-Wirbelsäulenanästhesie für einen elektiven Kaiserschnitt. Anaesth Intensive Care 2003;31:514–517.
- Lyons G, Macdonald R, Mikl B: Kombinierte epiduralspinale Anästhesie für den Kaiserschnitt. Durch die Nadel oder in getrennten Räumen? Anästhesie 1992;55:199–201.
- Casati A, D'Ambrosio A, De Negri P, Fanelli G, Tageriello V, Tarantino F: Ein klinischer Vergleich zwischen Nadel-durch-Nadel- und Doppelsegmenttechniken für die kombinierte Spinal- und Epiduralanästhesie. Reg Anesth Pain Med 1998;55:3904.
- Rawal N., Van Zundert A., Holmström B., Crowhurst JA: Combined spinalepidural technique. Reg Anesth 1997;55:40623.
- Backe SK, Sheikh Z, Wilson R, Lyons GR: Kombinierte Epidural-/Spinalanästhesie: Nadel-durch-Nadel oder getrennte Räume? Eur J Anaesthesiol 2004;21:854–857.
- Sadashivaiah J., Wilson R., McLure H., Lyons G.: Kombinierte Spinal-Epidural-Technik mit doppeltem Raum für den elektiven Kaiserschnitt: Ein Rückblick auf 10 Jahre Erfahrung in einer britischen Mutterschaftslehranstalt. Int J Obstet Anesth 2010;19:183–187.
- Van den Berg AA, Ghatge S, Wang S: Der Verlust der Resistenz gegenüber Kochsalzlösung reduziert die Reaktionen, die das Einführen einer Spinalnadel während der Einführung einer kombinierten Spinal-Epidural-Analgesie „Nadel durch Nadel“ begleiten. Anaesth Intensive Care 2010;38:1013–1017.
- Grau T, Leipold RW, Fatehi s, Martin E, Motsch J: Echtzeit-Ultraschallbeobachtung der kombinierten Spinal-Epidural-Anästhesie. Eur J Anaesthesiol 2004;21:25–31.
- Tsui BC, Gupta S, Finucane B: Bestimmung der Epiduralkatheterplatzierung mittels Nervenstimulation bei geburtshilflichen Patienten. Reg Anesth 1999;24:17–23.
- Herman NL, Calicott R, Van Decar TK, et al: Bestimmung der Dosis-Wirkungs-Beziehung für intrathekales Sufentanil bei Wehen. Anesth Analg 1997;84:1256–1261.
- Herman NL, Choi KC, Affleck PJ, et al: Analgesie, Juckreiz und Ventilation treten bei Gebärenden auf, die intrathekales Fentanyl während der Wehen erhalten. Anesth Analg 1999;89:378–383.
- Palmer CM, Randall CC, Hays R, et al: The dose-response relation of intrathecal fentanyl for wehenanalgesia. Anesthesiology 1998;88:355–361.
- Honet JE, Arkoosh VA, Norris MC, et al: Vergleich zwischen intrathekalem Fentanyl, Meperidin und Sufentanil für Wehenanalgesie. Anesth Analg 1992;75:734–739.
- Jaffe RA, Rowe MA: Vergleich der lokalanästhetischen Wirkung von Meperidin, Fentanyl und Sufentanil auf Dorsalwurzelaxone. Anesth Analg 1996;83:776–781.
- Flanagan MT, Walker FO, Butterworth J: Versagen von Meperidin, den menschlichen Medianusnerv zu betäuben. Ein verblindeter Vergleich mit Lidocain und Kochsalzlösung. Reg Anesth 1997;22:73–79.
- Abouleish A, Abouleish E, Camann W: Kombinierte spinal-epidurale Analgesie bei fortgeschrittener Wehentätigkeit. Can J Anaesth 1994;41:575–578.
- Campbell DC, Camann WR, Datta S: Die Zugabe von Bupivacain zu intrathekalem Sufentanil zur Analgesie der Wehen. Anesth Analg 1995;81: 305–309.
- Sia ATH, Chong JL, Chiu JW: Kombination von intrathekalem Sufentanil 10 μg plus Bupivacain 2.5 mg zur Analgesie der Wehen: Reicht die halbe Dosis? Anesth Analg 1999;88:362–366.
- Stocks GM, Hallworth SP, Fernando R, et al: Minimale lokale analgetische Dosis von intrathekalem Bupivacain bei der Geburt und die Wirkung von intrathekalem Fentanyl. Anesthesiology 2001, 94:593–598.
- Whitty R, Goldszmidt E, Parkes RK, Carvalho JC: Bestimmung der ED95 für intrathekales reines Bupivacain in Kombination mit Fentanyl bei aktiver Wehentätigkeit. Int J Obstet Anesth 2007;16:341–345.
- Levin A, Datta S, Camann W: Intrathekales Ropivacain zur Analgesie der Wehen: Ein Vergleich mit Bupivacain. Anesth Analg 1998;87:624–627.
- Joshi GP, McCarroll SM: Bewertung der kombinierten Spinal-Epiduralanästhesie mit zwei verschiedenen Techniken. Reg Anaesth 1994;55:16974.
- Collis RE, Baxandall ML, Srikantharajah ID, Edge G, Kadim MY, Morgan BM: Kombinierte spinale Epiduralanalgesie mit Gehfähigkeit während der Wehen. Lancet 1993;55:7678.
- Hoffmann VLH, Vercauteran MP, Buczkowski PW, Vanspringel GLJ: Ein neuer kombinierter spinaler Epiduralapparat: Messung des Abstands zum Epidural- und Subarachnoidalraum. Anästhesie 1997;55:350–355.
- Holloway TE, Telford RJ: Beobachtungen zur absichtlichen Duralpunktion mit einer Touhy-Nadel: Tiefenmessung. Anästhesie 1991;46:722–724.
- Cousins MJ, Bridenbaugh PO: Neuronale Blockade in der klinischen Anästhesie und Schmerzbehandlung, 3. Aufl. Lippincott-Raven, 1998, S. 255.
Brighouse D, Wilkins A: Versagen von Spinalnadeln mit Bleistiftspitze beim Eindringen in den Subarachnoidalraum. Anästhesie 1994;55:176. - Meiklejohn BH: Die Wirkung der Drehung einer Epiduralnadel: Eine In-vitro-Studie. Anästhesie 1987;42:1180–1182.
- Husemeyer RP, White DC: Topographie des lumbalen Epiduralraums. Anästhesie 1980;55:7–11.
- Waldman SA, Liguori GA: Vergleich der Flussraten von 27-Gauge Whitacre- und Sprotte-Nadeln für die kombinierte Spinal- und Epiduralanästhesie. Reg Anesth 1996;55:378–379.
- Vandermeersch E: Kombinierte Spinal-Epiduralanästhesie. Ballieres Clin Anaesth 1993;7:691–708.
- Fukishige T, Sano T, Kano T: Deformation des lumbalen Duralsacks nach epiduraler Injektion. Anesthesiology 1998;55:A870.
- Norris MC, Grieco WM, Borkowski M, et al: Komplikationen der Wehenanalgesie: Epidural versus kombinierte spinale Epiduraltechniken. Anesth Analg 1994;55:529–537.
- Lesser P, Bembridge M, Lyons G, Macdonald R: Eine Bewertung einer 30-Gauge-Nadel für die Spinalanästhesie für den Kaiserschnitt. Anästhesie 1990;55:76–78.
- Dennison B: Kombinierter Subarachnoidal- und Epiduralblock für Kaiserschnitt. Can J Anaesth 1987;55:105.
- Patel M, Swami M: Kombinierte spinal-extradurale Anästhesie für den Kaiserschnitt. Anästhesie 1992;55:1005–1006.
- Robbins PM, Fernando R, Lim GH: Versehentliches intrathekales Einführen eines extraduralen Katheters während einer kombinierten spinal-extraduralen Anästhesie für einen Kaiserschnitt. Br. J. Anaesth 1995;75:355–357.
- Vucevic M, Russell IF: Spinalanästhesie für den Kaiserschnitt: 0.125 % reines Bupivacain 12 ml im Vergleich zu 0.5 % reines Bupivacain 3 ml. Br. J. Anaesth 1992;55:590–595.
- Ferguson DJM: Duralpunktion und Epiduralkatheter. Anästhesie 1992;55:272.
- Muranaka K, Tsutsui T: Vergleich der klinischen Nützlichkeit der beiden Arten von kombinierten spinalen Epiduralnadeln. Masui 1994;55:1714–1717.
- Angle P, Kronberg JE, Thompson DE, Duffin J, et al: Epiduralkatheter
Penetration von menschlichem Dura-Gewebe: In-vitro-Untersuchung. Anästhesiologie
2004;100(6);141–146. - Holtz D, Mollman M, Schymroszcyk B, Ebel C, Wendt M: Kein Risiko einer Metalltoxizität bei kombinierter Spinal-Epidural-Anästhesie. Anesth Analg 1999;88(2):393–397.
- Holmstrom B, Rawal N, Axelsson K, et al: Risiko einer Kathetermigration während einer kombinierten Studie mit spinaler epiduraler Blockade und perkutaner Epiduroskopie. Anesth Analg 1995;80:747–753.
- Leighton BL, Arkoosh VA, Huffnagle S, et al.: Die dermatomale Ausbreitung von epiduralem Bupivacain mit und ohne vorheriges intrathekales Sufentanil. Anesth Analg 1996;83:526–529.
- Stienstra R, Dilrosun-Alhadi BZ, Dahan A, van Kleef JW, Veering BT, Burm AG: Das epidurale „Top-up“ in der kombinierten Spinal-Epidural-Anästhesie: Die Wirkung von Volumen versus Dosis. Anesth Analg 1999;88:810–814.
- Suzuki N., Koganemaru M., Onizuka S., Takasaki M.: Die Duralpunktion mit einer 26G-Spinalnadel beeinflusst die Ausbreitung der Epiduralanästhesie. Anesth Analg 1996;82:1040–1042.
- Kamiya Y, Kikuchi T, Inagawa G, et al: Lidocain-Konzentration in der Zerebrospinalflüssigkeit nach epiduraler Verabreichung: Ein Vergleich zwischen Epidural- und kombinierter Spinal-Epidural-Anästhesie. Anesthesiology 2009;110:1127–1132.
- Leach A, Smith GB: Subarachnoidale Ausbreitung eines epiduralen Lokalanästhetikums nach einer Durapunktion. Anästhesie 1988;43:671–674.
- Gaiser RR, Lewin SB, Cheek TG, Gutsche BB: Auswirkungen der sofortigen Einleitung einer epiduralen Infusion in der kombinierten Spinal- und Epiduraltechnik bei Nulliparagebärenden. Reg Anesth Pain Med 2000;25:223–227.
- Beaubien G, Drolet P, Girard M, Grenier Y: Patientengesteuerte Epiduralanästhesie
Analgesie mit Fentanyl-Bupivacain: Einfluss einer vorangegangenen Durapunktion. Reg Anesth Pain Med 2000;25:254–258. - Hodgkinson R: Totaler spinaler Block nach epiduraler Injektion in einen Zwischenraum neben einer unbeabsichtigten Duraperforation. Anästhesiologie 1981;55:593–595.
- Eldor J, Guedj P, Levine S. Verzögerter Atemstillstand bei kombinierter Spinal-Epiduralanästhesie. Fallbericht. Reg Anesth 1994;19;418–422.
- Kuczkowski KM, Birnbach DJ, O'Gorman DA, Stein DJ, Santos AC: Erhöht eine Testdosis die Wahrscheinlichkeit, eine intrathekale Platzierung von Epiduralkathetern während der Analgesie der Wehen zu erkennen? Zusammenfassung wissenschaftlicher Arbeiten SOAP. Anästhesiologie 2000;A26.
- Goy RW, Sia AT. Sensomotorische Anästhesie und Hypotonie nach Subarachnoidalblock: Kombinierte Spinal-Epidural- versus Single-Shot-Spinaltechnik. Anesth Analg 2004;98(2):491–496.
- Goy RWL, Chee-Seng Y: Die mittlere effektive Dosis von intrathekalem hyperbarem Bupivacain ist bei der Single-Shot-Wirbelsäulentherapie größer als bei der kombinierten Spinal-Epidural-Technik. Anesth Analg 2005; 100: 1499–1502.
- Gaur V, Gupta RK, Agarwal A, et al: Luft oder Distickstoffoxid für den Widerstandsverlust
Epiduraltechnik? Can J Anaesth 2000;47:503–505. - Carpenter RL, Hogan QH, Liu SS, et al: Das Volumen der lumbosakralen Zerebrospinalflüssigkeit ist die primäre Determinante für das Ausmaß und die Dauer der sensorischen Blockade während der Spinalanästhesie. Anästhesiologie 1998;89:24–29.
- Rawal N., Schollin J., Wesström G.: Epidural versus kombinierter spinaler Epiduralblock für den Kaiserschnitt. Acta Anaesth Scand 1988;32: 61–66.
- Kumar C: Kombinierter Subarachnoidal- und Epiduralblock für Kaiserschnitt. Can J. Anesth 1987;34:329–330.
- Mandell GL, Jamnback L, Ramanathan S: Hämodynamische Wirkungen von subarachnoidalem Fentanyl bei Wehen. Reg Anesth 1995;21(2):103–111.
- Horlocker TT, McGregor DG, Matsushige DK, Schroeder DR, Besse JA: Eine retrospektive Überprüfung von 4767 aufeinanderfolgenden Spinalanästhetika: Komplikationen des zentralen Nervensystems. Anesth Analg 1997;55:578–584.
- Bigeleisen PE: Eine Nervenpunktion und offensichtliche intraneurale Injektion während einer ultraschallgeführten Axillarblockade führt nicht immer zu einer neurologischen Verletzung. Anesthesiology 2006;105:779–783.
- Simsa J: Verwendung von 29-G-Spinalnadeln und einer Fixiervorrichtung mit kombinierter spinaler Epiduraltechnik. Acta Anaesth Scand 1994;38:439–441.
- McAndrew CR, Harms P: Parästhesien während einer Nadel-durch-Nadel-Kombination an der Wirbelsäulen-Epiduralanästhesie im Vergleich zu einer Single-Shot-Wirbelsäulenanästhesie für einen elektiven Kaiserschnitt. Anaesth Intensive Care 2003;31(5):514–517.
- Holloway J, Seed PT, O'Sullivan G, Reynolds F: Parästhesien und Nervenschäden nach kombinierter spinaler Epidural- und Spinalanästhesie: Eine Pilotstudie. Int J Obstet Anesth 2000;9(3):151–155.
- Turner MA, Shaw M: Atraumatische Spinalnadeln [Brief]. Anästhesie 1993;48:452.
- Broadbent CR, Maxwell WB, Ferrie R, et al: Fähigkeit von Anästhesisten, einen markierten lumbalen Zwischenraum zu identifizieren. Anästhesie 2000;55:1106–1126.
- Eldor J: Metallfragmente und die kombinierte spinal-extradurale Technik. Br. J. Anaesth 1992;69:663.
- Sharma B, Gupta S, Jain N, Handoo A, Sood J: Zerebrospinalflüssigkeits-Zytologie bei Patienten, die sich einer kombinierten Spinal-Epidural- versus Spinalanästhesie ohne Einführhilfe unterziehen. Anaesth Intensivstation 2011; 39:914–918.
- Dripps Rd, Vandem LD: Langzeit-Follow-up von Patienten, die 10,098 Spinalanästhetika erhalten haben. JAMA 1954;156:1486–1491.
- Phillips OC, Ebner H, Melson AT, Black MH: Neurologische Komplikationen nach Spinalanästhesie mit Lidocain: Eine prospektive Überprüfung von 10,440 Fällen. Anästhesiologie 1969;30:284–289.
- Harding SA, Collis RE, Morgan BM: Meningitis nach kombinierter extraduraler Spinalanästhesie in der Geburtshilfe. Br. J. Anaesth 1994;73:545–547.
- Cascio M: Meningitis nach einer kombinierten Spinal-Epidural-Technik in einem Geburtstermin. Can J Anaesth 1996;43:399–402.
- Pinder AJ, Dresner M: Meningokokken-Meningitis nach kombinierter Spinalepiduralanästhesie
Analgesie. Int J Obstet Anesth 2003;12:183–187. - McLure HA, Talboys CA, Yentis SM, Azadian BS: Chirurgische Gesichtsmasken und Ausbreitung von Bakterien nach unten. Anästhesie 1998;53:624–626.
- Phillips BJ, Fergusson S, Armstrong P, Anderson FM, Wildsmith JAW: Chirurgische Gesichtsmasken reduzieren wirksam die bakterielle Kontamination, die durch die Ausbreitung aus den oberen Atemwegen verursacht wird. Br. J. Anaesth 1992;69:407–408.
- Burnstein R, Buckland R, Pickett JA: Eine Untersuchung der Epiduralanalgesie für die Arbeit im Vereinigten Königreich. Anästhesie 1999;54:634–650.
- Siegel J., Rhinehart E., Jackson M., Chiarello L.; und das Beratungskomitee für Praktiken der Infektionskontrolle im Gesundheitswesen. Richtlinie für Isolationsvorkehrungen: Verhinderung der Übertragung von Infektionserregern im Gesundheitswesen, Juni 2007. http://www.premierinc.com/safety/topics/guidelines/downloads/cdc-isolation-2007.pdf.
- Zentren für die Kontrolle und Prävention von Krankheiten. Bakterielle Meningitis nach Spinalanästhesie während der Wehen – Ohio und New York, 2008–2009. MMWR Morb Mortal Wkly Rep 2010;59:65–69.
- Sandkovsky U, Mihu MR, Adeyeye A, et al: Iatrogene Meningitis bei einer geburtshilflichen Patientin nach kombinierter Spinal-Epidural-Analgesie: Fallbericht und Literaturübersicht. South Med J 2009;102:287–290.
- Choy JC: Sterblichkeit durch peripartale Meningitis. Anaesth Intensive Care 2000;28:328–330.
- Tariq A: Neurologisches Defizit nach kombinierter Spinal-Epiduralanästhesie bei Knieendoprothetik. Mittlerer Osten J Anesthesiol 2010;20:759–762.
- Takasu, M, Okita M, Araki m, et al: Gadolinium-Verstärkung der Cauda equina nach kombinierter Spinal-Epidural-Anästhesie. Br. J. Radiol 2010;83:192–194.
- Kubina P, Gupta A Oscarsson A, et al: Zwei Fälle von Cauda-Equina-Syndrom nach Spinal-Epidural-Anästhesie. Reg Anesth 1997;22: 447–450.
- Kato J, Konishi J, Yoshida H, et al: Cauda equina-Syndrom nach kombinierter Spinal- und Epiduralanästhesie: Ein Fallbericht. Can J Anaesth 2011;58:638–641.
- Rawal N, Holmstrom B, Croehurst JA, Van Zundert A: Die kombinierte Spinal-Epidural-Technik. Anaesthsiol Clin North America 2000;18: 267–295.
- Dunn SM, Connelly NR, Parker RK: Postduralpunktionskopfschmerz (PDPH) und kombinierte Spinalanästhesie (CSE). Anesth Analg 2000;90: 1249–1250.
- Balestrieri PJ: Die Inzidenz von Kopfschmerzen nach Punktion und kombinierter Spinal-Epiduralanästhesie: Einige Gedanken. Int J Obstet Anesth 2003; 12(4):305–306.
- Brownridge P. Spinalanästhesie in der Geburtshilfe. Br. J. Anaesth 1991;67: 663–667.
- Geurts JW, Haanschoten MC, Van Wijk RM, Kraak H, Besse TC: Kopfschmerz nach Punktion bei jungen Patienten. Eine vergleichende Studie zwischen der Verwendung von 0.52 mm (25-Gauge) und 0.33 mm (29-Gauge) Spinalnadeln. Acta Anaesthesiol Scand 1990;34:350–353.
- Chan BO, Paech MJ: Anhaltender Austritt von Liquor cerebrospinalis: Eine Komplikation der kombinierten Spinal-Epidural-Technik. Anesth Analg 2004;98(3): 828–830.
- Reisinger PWM, Hochstrasser K: Die Diagnose von Liquorfisteln anhand des Nachweises von beta2-Transferrin durch Polyacrylamid-Gelelektrophorese und Immunoblot. J. Clin. Chem. Clin. Biochem. 1989; 27:169–172.
- Howes J, Lenz R: Liquor-Hautfistel – eine ungewöhnliche Komplikation der Epiduralanästhesie. Anästhesie 1994;49:221–222.
- Pan PH, Moore CH, Ross VH: Schwere mütterliche Bradykardie und Asystolie nach kombinierter spinal-epiduraler Wehenanalgesie bei einer krankhaft fettleibigen Gebärenden. J Clin Anesth 2004;16(6):461–464.
- Kuczkowski KM: Schwere anhaltende fötale Bradykardie nach subarachnoidaler Verabreichung von Fentanyl und Bupivacain zur Induktion einer kombinierten spinal-epiduralen Analgesie bei Wehenschmerzen. J Clin Anesth 2004;16(1):78–79.
- D'Angelo R, Eisenach JC: Schwere mütterliche Hypotonie und fetale Bradykardie nach einem CSE. Anesthesiology 1997;81:116–118.
- Mardirosoff C, Dumont L, Boulvain M, Tramèr MR: Fetale Bradykardie durch intrathekale Opioide zur Analgesie der Wehen: Eine systematische Übersicht. BJOG 2002;109:274–281.
- Van de Velde M: Neuraxiale Analgesie und fötale Bradykardie. Curr Opin Anaesthesiol 2005;18:253–256.
- Nocolet J, Miller A, Kaufman I, et al: Mütterliche Faktoren, die mit fötaler Bradykardie nach kombinierter spinaler Epiduralanästhesie bei Wehenschmerzen in Verbindung stehen. Eur J Anaesth 2008;25:721–725.
- Clarke VT, Smiley RM, Finster M: Uterine Hyperaktivität nach intrathekaler Injektion von Fentanyl zur Analgesie während der Wehen: Eine Ursache für fetale Bradykardie? Anesthesiology 1994;81:1083.
- Albright GA, Forster RM: Erhöht die kombinierte Spinal-Epidural-Analgesie mit Subarachnoidal-Sufentanil die Inzidenz von Notfall-Kaiserschnitten? Reg Anesth Pain Med 1997;22:400–405.
- Skupski DW, Abramovitz S, Samuels J, et al: Unerwünschte Wirkungen der kombinierten Spinal-Epiduralanästhesie im Vergleich zur traditionellen Epiduralanalgesie während der Wehen. Int. J. Gynecol Obstet 2009;106:242–245.
- Rawal N, Schollin J, Wesstrom G: Epidural versus kombinierter spinaler Epiduralblock für Kaiserschnitt. Acta Anaesthesiol Scand 1988;32: 61–66.
- Joshi GP, MaCarroll SM: Kombinierte Spinal-Epiduralanästhesie mit Nadel-durch-Nadel-Technik [Brief]. Anesthesiology 1993;78: 406–407.
- Pan PH: Laborbewertung von einlumigen kombinierten Spinal-Epidural-Nadeln mit zwei Öffnungen: Auswirkungen der Ausrichtung der Abschrägung und der modifizierten Technik. J Clin Anesth 1998;10(4):286–290.
- Riley ET, Hamilton CL, Ratner EF, Cohen S: Ein Vergleich der 24-Gauge-Sprotte- und Gertie-Marx-Spinalnadeln für die kombinierte Spinal-Epidural-Analgesie während der Wehen. Anesthesiology 2002;97:574–577.
- Herbstman CH, Jaffe JB, Tuman KJ, et al: Eine in vivo-Bewertung von vier Spinalnadeln, die für die kombinierte Spinal-Epidural-Technik verwendet werden. Anesth Analg 1998;86(3):520–522.
- Simsa J: Nadelfixation mit kombinierter Spinalepiduralanästhesie. Acta Anaesth Scand 1995;55:275.
- Stocks GM, Hallworth SP, Fernando R: Evaluation of a Spinal Needle Locking Device zur Verwendung mit der kombinierten spinalen Epiduraltechnik. Anästhesie 2000;55(12):1185–1188.
- Eldor J, Chaimsky G: Die kombinierte Spinal-Epiduralnadel von Eldor. Anästhesie 1993;48:173.
- Torrieri A, Aldrete JA: Kombinierte Spinal-Epidural-Nadel. Acts Anaesth Belg 1998;39:65–66.
- Birnbach DJ, Chestnut DH: Die epidurale Testdosis in der geburtshilflichen Praxis: Hat sie ausgedient? Anesth Analg 1999;88:971.
- Steffek M, Owczuk R, Szlyk-Augustin M, Lasinska-Kowara M, Wujtewicz M: Totale Spinalanästhesie als Komplikation der Lokalanästhesie-Testdosis-Verabreichung durch einen Epiduralkatheter. Acta Anaesthesiol Scand 2004;48(9):1211–1213.
- Norris MC, Ferrenbach D, Dalman H, et al: Verbessert Epinephrin die diagnostische Genauigkeit der Aspiration während der Epiduralanalgesie während der Wehen? Anesth Analg 1999;88;1073.
- Moore DC, Batra MS: Die Komponenten einer wirksamen Testdosis vor dem Epiduralblock. Anesthesiology 1981;55:693.
- Hood DD, Dewan DM, James FM III: Maternale und fötale Wirkung von Epinephrin bei trächtigen Mutterschafen. Anesthesiology 1986;64:610.
- Leighton BL, Norris MC, DeSimone CA, et al: Der Lufttest als klinisch nützlicher Indikator für intravenös platzierte Epiduralkatheter. Anesthesiology 1990;73:610.
- Kopacz DJ: Spinales 2-Chloroprocain: Minimale wirksame Dosis. Reg Anesth Pain Med 2005;30(1):36–42.
- Hamza J, Smida M, Benhamou D, Cohen SE: Die Potatur des Gebärenden während der Epiduralpunktion beeinflusst den Abstand von der Haut zum Epiduralraum. J Clin Anesth 1995;7:1–4.
- Yun EM, Marx GF, Santos AC: Die Auswirkungen der mütterlichen Position während der Einleitung einer kombinierten Spinal-Epiduralanästhesie für Kaiserschnittgeburten. Anesth Analg 1998;87:614–618.
- Lewis NL, Ritchie EL, Downer JP, Nel MR: Linke laterale vs. Rückenlage, Keilposition zur Entwicklung einer Blockade nach kombinierter Spinal-Epiduralanästhesie für einen Kaiserschnitt. Anästhesie 2004;59: 894–898.


