Honorio T. Benzon, Rasha S. Jabri et Tom C. Van Zundert
INTRODUCTION
L'hématome intra-rachidien est une affection relativement rare résultant de diverses causes. Les causes traumatiques comprennent la ponction lombaire et l'anesthésie neuraxiale. Il est plus susceptible de se produire chez les patients anticoagulés ou thrombocytopéniques, les patients atteints d'une maladie néoplasique ou chez ceux souffrant d'une maladie du foie ou d'alcoolisme. Environ un quart à un tiers de tous les cas sont associés à un traitement anticoagulant. Le risque de formation d'un hématome intrarachidien après l'administration d'une anesthésie et d'une analgésie neuraxiales est augmenté chez les patients qui ont reçu un traitement anticoagulant ou qui présentent un trouble de la coagulation. Pour cette raison, l'anesthésie neuraxiale est souvent contre-indiquée en présence d'une coagulopathie. D'autres facteurs de risque pour le développement d'un hématome épidural ou rachidien comprennent la difficulté technique (tentatives multiples) dans l'exécution des procédures neuraxiales en raison d'anomalies anatomiques de la colonne vertébrale et de ponctions multiples ou sanglantes.
L'incidence de l'hématome rachidien était à l'origine d'une péridurale sur 150,000 220,000 et d'une anesthésie rachidienne sur 2700 19,505. Des études épidémiologiques récentes ont montré que l'incidence des hématomes rachidiens était plus fréquente, allant d'un sur 1 à un sur 21,643 3800 épidurales. L'étude la plus récente a montré un risque global de 200,000 sur 315 XNUMX injections épidurales. Les personnes âgées (une sur XNUMX) courent un risque accru en raison d'anomalies dégénératives de la colonne vertébrale, d'ostéoporose et de maladies vasculaires périphériques. Les populations obstétricales semblent avoir une incidence plus faible d'hématome rachidien (un sur XNUMX XNUMX), probablement secondaire à l'état hypercoagulable de la grossesse, à la plus grande capacité de l'espace épidural chez les jeunes parturientes et à une pression intra-épidurale plus élevée. D'après une grande étude rétrospective récente, l'incidence de l'hématome épidural chez les patients présentant une coagulation anormale peut être aussi faible qu'un patient sur XNUMX.
L'introduction de l'héparine de bas poids moléculaire (HBPM) a été associée à une augmentation de l'incidence des hématomes rachidiens, entraînant un avertissement de la Food and Drug Administration (FDA) et l'introduction de la première déclaration de consensus sur l'anesthésie régionale chez les patients. sur les anticoagulants par l'American Society of Regional Anesthesia and Pain Medicine (ASRA) en 1998. Les recommandations étaient basées sur une revue approfondie de la littérature et de la pharmacologie des différents anticoagulants.
Des recommandations ont été faites sur le moment du bloc nerveux neuraxial, le retrait du cathéter péridural et l'administration ultérieure d'anticoagulants. En particulier, l'utilisation de faibles concentrations d'anesthésiques locaux pour la perfusion péridurale (pour préserver la force motrice pour une surveillance plus facile) et la surveillance neurologique subséquente ont été recommandées par l'ASRA. Les lignes directrices consensuelles, publiées en 1998 et mises à jour en 2003 et 2010, ont grandement aidé les cliniciens dans la prise de décision concernant l'utilisation des procédures neuraxiales dans le cadre d'un traitement anticoagulant. Deux autres séries de lignes directrices, publiées par la Société européenne d'anesthésiologie et la Société scandinave d'anesthésiologie et de médecine de soins intensifs, sont influentes en Europe.
Dans ce chapitre, nous discutons de l'importance des anticoagulants courants et espérons offrir au lecteur un guide dans la prise de décision concernant l'utilisation de l'anesthésie neuraxiale et des blocs nerveux périphériques (PNB) dans la pratique clinique. Nous aborderons également les nouveaux anticoagulants, des médicaments qui n'étaient pas suffisamment couverts par les dernières recommandations de l'ASRA et seulement partiellement couverts par les recommandations européennes et scandinaves. Suivez le lien pour en savoir plus sur Diagnostic et prise en charge de l'hématome des nerfs spinal et périphérique.
THÉRAPIE ANTIPLAQUETTAIRE
Les médicaments antiplaquettaires inhibent l'enzyme cyclooxygénase plaquettaire et empêchent la synthèse du thromboxane A2. Le thromboxane A2 est un puissant vasoconstricteur qui facilite l'agrégation plaquettaire secondaire et les réactions de libération. Le rôle des plaquettes dans la coagulation et l'hémostase est montré dans Chiffres 1 et 2. Les plaquettes des patients prenant ces médicaments ont une adhérence plaquettaire normale au sous-endothélium et une formation normale de bouchon hémostatique primaire. Un caillot adéquat, bien que potentiellement fragile, peut se former. Bien que de tels bouchons puissent constituer des barrières hémostatiques satisfaisantes pour les petites lésions vasculaires, ils peuvent ne pas assurer une formation adéquate de caillots hémostatiques périopératoires. La fonction plaquettaire chez les patients recevant des médicaments antiplaquettaires doit être supposée diminuée pendant 1 semaine avec l'aspirine et 1 à 6 jours avec les anti-inflammatoires non stéroïdiens (AINS). Cette hypothèse ne tient pas compte de la formation continue de nouvelles plaquettes fonctionnelles. La production continue de plaquettes fraîches fonctionnant normalement, combinée à la fonction résiduelle de plaquettes déjà en circulation, peut expliquer la sécurité relative des procédures neuraxiales chez ces patients.
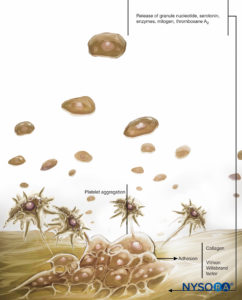
FIGURE 1. Rôle des plaquettes dans la coagulation. Les plaquettes jouent leur rôle dans l'hémostase à travers trois réactions fondamentales : l'adhésion, l'activation (et la sécrétion) et l'agrégation. Lorsque l'endothélium vasculaire est endommagé, les plaquettes se lient rapidement au sous-endothélium par un processus appelé adhésion.
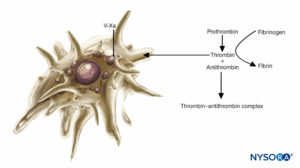
FIGURE 2. Rôle des plaquettes dans la coagulation : Les plaquettes soutiennent les réactions de coagulation du plasma. Lorsqu'elles sont activées, les plaquettes se lient à plusieurs complexes de protéines plasmatiques et sécrètent une forme activée du facteur V (facteur Va), qui se lie à la surface des plaquettes et au facteur Xa. Le facteur Xa lié aux plaquettes accélère alors la conversion de la prothrombine en thrombine.
Le risque d'hématome péridural et rachidien chez les patients sous traitement antiplaquettaire a été soulevé par un rapport de cas de formation spontanée d'hématome péridural en l'absence d'anesthésie rachidienne ou péridurale chez un patient ayant des antécédents d'ingestion d'aspirine. Vandermeulen et ses collègues ont impliqué un traitement antiplaquettaire dans 3 des 61 cas d'hématome rachidien survenant après une anesthésie rachidienne ou péridurale. D'autres études ont montré un risque relativement faible d'hématome rachidien chez les patients sous aspirine ou AINS subissant une procédure neuraxiale. Le groupe CLASP (Collaborative Low-dose Aspirin Study in Pregnancy) a inclus 1422 patientes obstétriques à haut risque qui ont reçu 60 mg d'aspirine par jour et ont subi une anesthésie péridurale sans aucune séquelle neurologique. Dans une étude rétrospective de 1013 anesthésiques rachidiens et périduraux dans lesquels des médicaments antiplaquettaires ont été pris par 39 % des patients, dont 11 % des patients qui prenaient plusieurs médicaments antiplaquettaires, aucun patient n'a développé de signes d'hématome rachidien.
Les patients prenant des médicaments antiplaquettaires, cependant, ont montré une incidence plus élevée d'aspiration de sang à travers l'aiguille spinale ou épidurale ou le cathéter. Une étude prospective ultérieure portant sur 1000 patients, dont 39 % ont déclaré un traitement antiplaquettaire préopératoire, a noté l'absence de complications hémorragiques. Par conséquent, le traitement antiplaquettaire préopératoire n'était pas un facteur de risque de placement sanglant d'une aiguille ou d'un cathéter. Le sexe féminin, l'âge avancé, les antécédents d'ecchymoses ou de saignements excessifs, la technique du cathéter continu, le gros calibre de l'aiguille, les tentatives multiples et le placement difficile de l'aiguille ont été notés comme des facteurs de risque importants. Les études cliniques chez les patients des cliniques de la douleur sont similaires à celles qui subissent une intervention chirurgicale. Les patients sous aspirine ou AINS qui ont subi des injections péridurales de stéroïdes n'ont pas développé de signes ou de symptômes d'hématome intrarachidien.
L'absence de corrélation entre les médicaments antiplaquettaires et le placement sanglant d'une aiguille ou d'un cathéter fournit des preuves que le traitement antiplaquettaire préopératoire ne représente pas un facteur de risque significatif pour le développement d'un dysfonctionnement neurologique à partir d'un hématome spinal chez les patients sous traitement antiplaquettaire. Il convient de noter qu'il y a eu des rapports de cas d'hématome intrarachidien chez des patients sous aspirine ou AINS, bien qu'il y ait eu des facteurs de complication dans ces rapports de cas. Ceux-ci comprenaient l'administration concomitante d'héparine, l'angiome veineux péridural coexistant et la difficulté technique à effectuer la procédure. Plus récemment, davantage de rapports de cas d'hématome rachidien ont été publiés en relation avec des procédures d'intervention sur la douleur, en particulier des placements de stimulation de la moelle épinière.
Sur la base des preuves disponibles, l'ASRA a formulé plusieurs recommandations concernant les médicaments antiplaquettaires. Le traitement antiplaquettaire préopératoire ne représente pas un facteur de risque significatif pour le développement d'un dysfonctionnement neurologique à partir d'un hématome rachidien chez les patients sous traitement antiplaquettaire. Le risque de complications hémorragiques, cependant, peut être augmenté chez les patients prenant plusieurs médicaments antiplaquettaires et l'utilisation concomitante d'autres médicaments affectant les mécanismes de coagulation, tels que les anticoagulants oraux, l'héparine standard et l'HBPM.
Conseils NYSORA
- Il est probablement sûr de faire des procédures d'anesthésie neuraxiale et régionale chez les patients sous aspirine et AINS.
- Les facteurs de risque d'augmentation des saignements et des hématomes rachidiens comprennent la prise par le patient de plusieurs médicaments antiplaquettaires et les tentatives multiples.
Procédures d'aspirine et de douleur interventionnelle
Il y a eu plusieurs rapports de cas d'hématome rachidien après l'injection péridurale de stéroïdes ou la mise en place ou le retrait d'un stimulateur de la moelle épinière chez des patients qui prenaient de l'aspirine seule, des AINS seuls ou lorsque les directives de l'ASRA étaient suivies. Ces événements peuvent être liés aux fréquentes anomalies de la colonne vertébrale trouvées chez ces patients, à la présence de fibrose après une chirurgie de la colonne vertébrale, à des aiguilles plus grosses utilisées pour le placement du stimulateur de la moelle épinière ou aux manipulations fréquentes (avancées et rétractions) des électrodes.
Les médicaments utilisés dans la gestion de la douleur provoquent également des saignements ; ceux-ci comprennent l'oxcarbazépine et les inhibiteurs sélectifs de la recapture de la sérotonine. Pour ces raisons, l'ASRA a collaboré avec la Société européenne d'anesthésie régionale et de thérapie de la douleur, l'Académie américaine de médecine de la douleur, la Société internationale de neuromodulation, la Société nord-américaine de neuromodulation et l'Institut mondial de la douleur pour formuler des lignes directrices spécifiques pour les procédures interventionnelles de la douleur. . Contrairement aux directives de l'ASRA sur l'anesthésie régionale, les directives multisociétés recommandaient d'arrêter l'aspirine pendant 4 à 6 jours avant les procédures interventionnelles contre la douleur.
Conseils NYSORA
Les lignes directrices sur les procédures interventionnelles de la douleur chez les patients sous antiagrégants plaquettaires et anticoagulants sont plus restrictives que celles sur l'anesthésie régionale.
Inhibiteurs de COX-2 et inhibiteurs de P2Y12
Les inhibiteurs de la cyclooxygénase-2 (COX-2) ont gagné en popularité en raison de leurs propriétés analgésiques et de l'absence d'effets plaquettaires et gastro-intestinaux, et des études ont montré leur propriété analgésique dans divers contextes périopératoires.
Les médicaments ont une toxicité gastro-intestinale (GI) minimale et sont idéaux pour les patients qui présentent un risque accru d'événements indésirables graves au niveau gastro-intestinal supérieur. Par rapport à l'aspirine ou aux AINS, l'effet des inhibiteurs de la COX-2 sur l'agrégation plaquettaire et les temps de saignement n'était pas différent du placebo. La perte de sang n'augmente pas pendant la chirurgie de fusion vertébrale lorsque des inhibiteurs de la COX-2 sont administrés en préopératoire. Les propriétés plaquettaires de ces médicaments les rendent idéaux pour une utilisation périopératoire lorsqu'une anesthésie neuraxiale est prévue. Malheureusement, le rofécoxib et le valdécoxib ont été retirés du marché en raison de leurs effets secondaires cardiovasculaires, ne laissant que le célécoxib disponible, mais à des doses inférieures à celles précédemment recommandées.
Les médicaments à base de thiénopyridine, la ticlopidine et le clopidogrel, n'ont aucun effet direct sur le métabolisme de l'acide arachidonique. Ces médicaments préviennent l'agrégation plaquettaire en inhibant l'activation plaquettaire médiée par les récepteurs de l'adénosine diphosphate (ADP). Ils modulent également le muscle lisse vasculaire, réduisant la contraction vasculaire. La ticlopidine est rarement utilisée car elle provoque une neutropénie, un purpura thrombocytopénique et une hypercholestérolémie.
Le clopidogrel est préféré en raison de son profil d'innocuité amélioré et de son efficacité prouvée. Il a été noté qu'il était meilleur que l'aspirine chez les patients atteints de maladie vasculaire périphérique. L'inhibition maximale de l'agrégation plaquettaire induite par l'ADP avec le clopidogrel se produit 3 à 5 jours après le début d'une dose standard (75 mg) mais dans les 4 à 6 heures après l'administration d'une dose de charge importante de 300 à 600 mg. Une dose de charge importante est généralement administrée aux patients avant qu'ils ne subissent une intervention coronarienne percutanée (ICP). Un cas d'hématome rachidien a été rapporté chez un patient sous ticlopidine. Bien qu'il n'y ait eu aucun cas d'hématome intrarachidien chez un patient sous clopidogrel seul, un cas de quadriplégie chez un patient sous clopidogrel, diclofénac et aspirine a été rapporté.
Pour les médicaments à base de thiénopyridine, il est recommandé d'arrêter la ticlopidine pendant 10 à 14 jours et le clopidogrel pendant 7 jours avant l'injection neuraxiale. Il y a eu des rapports de cas sur la sécurité de la rachianesthésie 5 jours après l'arrêt du clopidogrel. Une étude a montré que la plupart des patients présentaient une inhibition plaquettaire minimale 5 jours après l'arrêt du clopidogrel. Si une procédure neuraxiale doit être effectuée 5 à 6 jours après l'arrêt du clopidogrel, alors un test P2Y12, ou un autre test approprié, doit être effectué pour assurer une inhibition minimale ou nulle de l'activité plaquettaire.
Conseils NYSORA
- Les recommandations de l'ASRA recommandent un intervalle de 7 jours entre l'arrêt du clopidogrel et une intervention neuraxiale.
- Si une rachianesthésie ou une péridurale doit être effectuée est indiquée, un test de la fonction plaquettaire est recommandé pour s'assurer que l'inhibition plaquettaire résiduelle a disparu ou est négligeable.
Pour un essai de stimulation médullaire, un arrêt de 5 jours peut être observé puisque le patient sera hors clopidogrel pendant l'essai. Un test de la fonction plaquettaire (par exemple, le test VerifyNow P2Y12 ou la partie cartographie plaquettaire du Thrombelastograph [TEG]) doit être effectué pour garantir une activité plaquettaire adéquate.
Médicaments antiplaquettaires plus récents
Le clopidogrel est le médicament antiplaquettaire couramment utilisé dans la bithérapie antiplaquettaire, dans laquelle l'aspirine est associée à un inhibiteur du récepteur P2Y12, chez les patients atteints de syndromes coronariens aigus. Le prasugrel est un promédicament similaire au clopidogrel mais avec des caractéristiques salutaires par rapport au clopidogrel, et le ticagrélor est un inhibiteur direct des récepteurs P2Y12. Le délai médian jusqu'au pic d'effet est de 1 heure avec le prasugrel et de 4 heures avec le clopidogrel. Le temps moyen pour atteindre le pic de concentration plasmatique avec le prasugrel est de 30 minutes et sa demi-vie médiane est de 3.7 heures. Ces valeurs ne reflètent pas la durée de l'inhibition plaquettaire car l'inhibition du récepteur P2Y12 est irréversible. Il faut 7 jours pour que l'activité plaquettaire se normalise après l'arrêt du prasugrel.
Le prasugrel et le ticagrélor provoquent une inhibition de 90 % de la fonction plaquettaire contre 60 à 70 % pour le clopidogrel. Les patients ayant un faible indice de masse corporelle (IMC), ceux de plus de 75 ans et ceux ayant des antécédents d'accident vasculaire cérébral sont à risque de saignement. Contrairement au clopidogrel, le prasugrel est converti de manière fiable en son métabolite actif et n'a aucune interaction médicamenteuse. De plus, il n'est pas sensible aux polymorphismes génétiques.
Le ticagrélor se lie de manière réversible au récepteur P2Y12, bloquant l'activation du récepteur médiée par l'ADP. Contrairement aux thiénopyridines, le métabolite actif et le médicament parent présentent une activité antiplaquettaire, le médicament parent étant responsable de la majorité de l'inhibition plaquettaire in vivo. L'effet antiplaquettaire du ticagrélor est rapide ; le pic d'inhibition plaquettaire survient 2 à 4 heures après la prise contre 24 heures avec le clopidogrel. L'inhibition plaquettaire moyenne par le ticagrélor est de 93 % contre 58 % pour le clopidogrel. La récupération plaquettaire est rapide avec le ticagrelor ; l'activité plaquettaire est normale 5 jours après la dernière dose.
Délai entre l'arrêt/la reprise d'un médicament antiplaquettaire et l'injection neuraxiale
L'intervalle entre l'arrêt d'un médicament antiplaquettaire et l'injection neuraxiale est basé sur le pourcentage d'inhibition plaquettaire et le pourcentage de renouvellement plaquettaire. Le prasugrel et le ticagrelor provoquent une inhibition de 90 %. Dix à 15 % du pool de plaquettes en circulation se forment chaque jour, ce qui donne de nouvelles plaquettes représentant 50 à 75 % du pool de plaquettes en circulation 5 à 7 jours après l'arrêt du médicament. Un intervalle de 5 à 7 jours a été recommandé pour le ticagrelor et un intervalle de 7 à 10 jours pour le prasugrel. Ces recommandations sont appropriées car l'agrégation plaquettaire se normalise 7 jours après l'arrêt du prasugrel et 5 jours après le ticagrélor.
Les recommandations scandinaves notent qu'il est acceptable de reprendre les médicaments antiplaquettaires au moment du retrait du cathéter, alors que les recommandations de la Société européenne d'anesthésiologie recommandent un intervalle de 6 heures entre le retrait du cathéter péridural et la reprise du prasugrel ou du ticagrélor. D'autres revues ont recommandé la prudence lors du redémarrage du prasugrel et du ticagrélor en raison de leur effet rapide et de leur puissant inhibiteur antiplaquettaire. Un intervalle de 24 heures peut être plus approprié pour ces agents.
Conseils NYSORA
- Le prasugrel et le ticagrelor doivent être arrêtés respectivement 7 et 5 jours avant une rachianesthésie ou une péridurale.
- Les médicaments antiplaquettaires peuvent être redémarrés 6 à 24 heures après une procédure neuraxiale ou le retrait du cathéter.
Surveillance de la fonction plaquettaire
Le temps de saignement Ivy a été considéré comme un prédicteur fiable de saignement anormal chez les patients recevant des médicaments antiplaquettaires. Cependant, le temps de saignement post-aspirine n'est pas un indicateur fiable de la fonction plaquettaire. Il existe une grande variabilité intra- et inter-patients dans les résultats du test, et il n'y a aucune preuve suggérant que le temps de saignement puisse prédire la fonction hémostatique, car les études n'ont pas réussi à montrer une corrélation entre l'allongement du temps de saignement induit par l'aspirine et la perte de sang chirurgicale. .
Des tests spéciaux de la fonction plaquettaire sont désormais disponibles pour surveiller l'agrégation et la dégranulation des plaquettes. L'analyseur de la fonction plaquettaire (PFA) est un test de la fonction plaquettaire in vitro. C'est un bon test de dépistage de la maladie de von Willebrand et il surveille l'effet de l'administration de desmopressine. La PFA est prolongée après un traitement antiplaquettaire. Malheureusement, le PFA-100 n'est pas un test sensible pour surveiller la fonction antiplaquettaire des inhibiteurs de P2Y12 clopidogrel, prasugrel et ticagrelor. Cependant, le PFA-200, une mise à jour récente du PFA-100, semble être sensible aux effets des inhibiteurs de P2Y12. Cependant, les études au point de service sur ce nouveau test PFA font toujours défaut.
Les tests plus récents qui surveillent l'activité du récepteur P2Y12 comprennent le test de phosphoprotéine stimulée par un vasodilatateur (VASP), le test VerifyNow, le test d'aggrégométrie plaquettaire multiple (Multiplate) et le composant de cartographie plaquettaire du thromboélastographe (TEG). Le test VerifyNow peut surveiller les effets antiplaquettaires de l'aspirine et des inhibiteurs P2Y12. Le composant de cartographie plaquettaire du TEG est couramment utilisé en chirurgie et en anesthésiologie, tandis que VerifyNow est le test prédominant en cardiologie clinique. Une revue sur la surveillance de la fonction plaquettaire a été discutée par plusieurs revues et dépasse le cadre de ce chapitre.
ANTICOAGULANTS ORAUX
La warfarine exerce son effet anticoagulant en interférant avec la synthèse des facteurs de coagulation dépendant de la vitamine K (VII, IX, X et thrombine) (Figure 3). Il inhibe également les protéines anticoagulantes C et S. Le facteur VII a une demi-vie relativement courte (6 à 8 h) et le temps de prothrombine (TP) peut être prolongé dans la plage thérapeutique (1.5 à 2 fois la normale) en 24 à 36 heures. La protéine C anticoagulante a également une courte demi-vie (6 à 7 h). L'allongement initial du rapport international normalisé (INR) est le résultat des effets concurrents de la réduction du facteur VII et de la protéine C et de l'élimination des facteurs de coagulation existants. Pour cette raison, l'INR est imprévisible au cours de la phase initiale du traitement par la warfarine. Le facteur VII ne participe qu'à la voie extrinsèque et une anticoagulation adéquate n'est pas obtenue tant que les niveaux des facteurs biologiquement actifs II (demi-vie de 50 h) et X ne sont pas suffisamment abaissés. Cela nécessite 4 à 5 jours. Des doses de charge élevées de warfarine (15 mg) sont parfois utilisées pendant les 2 à 3 premiers jours de traitement, et l'effet anticoagulant souhaité est atteint dans les 48 à 72 heures. L'effet anticoagulant de la warfarine persiste pendant 4 à 6 jours après la fin du traitement, tandis que de nouveaux facteurs de vitamine K biologiquement actifs sont synthétisés. Les inconvénients du traitement par la warfarine comprennent la nécessité de surveiller son effet avec une surveillance en série de l'INR, son interaction avec d'autres médicaments et la nécessité de l'arrêter quelques jours avant la chirurgie. L'effet de la warfarine peut être inversé par la transfusion de plasma frais congelé et d'injections de vitamine K. Le concentré de complexe prothrombique (PCC) à 3 ou 4 facteurs peut être utilisé pour antagoniser la warfarine dans les situations d'urgence.
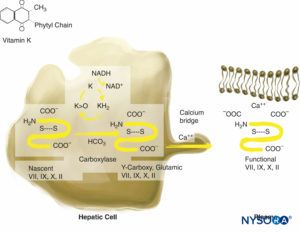
FIGURE 3. Synthèse du facteur de coagulation dépendant de la vitamine K. La vitamine K est nécessaire à la modification post-traductionnelle de la prothrombine ; protéines C et S; et les facteurs VII, IX et X. La vitamine K est stockée dans les hépatocytes.
Peu de données existent concernant le risque d'hématome rachidien chez les patients porteurs de cathéters rachidiens ou périduraux à demeure qui sont ensuite anticoagulés à la warfarine. Odoom et Sih ont réalisé 1000 anesthésies péridurales lombaires continues chez 950 patients ayant subi des interventions vasculaires et reçu des anticoagulants oraux préopératoires. Le thrombotest (un test de l'activité du facteur IX) a été diminué et le temps de thromboplastine partielle activée (aPTT) a été prolongé chez tous les patients avant la mise en place de la péridurale. De l'héparine a également été administrée en peropératoire. Les cathéters épiduraux sont restés en place pendant 48 heures après l'opération et il n'y a pas eu de complications neurologiques. Malheureusement, l'état de la coagulation des patients au moment du retrait du cathéter n'a pas été décrit. Bien que les résultats de cette étude soient rassurants, la nature désuète du thrombotest comme mesure de l'anticoagulation combinée à l'état de coagulation inconnu des patients au moment du retrait du cathéter limite l'utilité de l'étude.
L'utilisation d'un cathéter péridural ou intrathécal à demeure et le moment de son retrait chez un patient sous anticoagulation sont controversés. Bien que le traumatisme du placement de l'aiguille se produise avec les techniques de cathéter à dose unique et continue, la présence d'un cathéter à demeure peut entraîner des lésions supplémentaires des tissus et des structures vasculaires.
Étant donné que des hématomes intrarachidiens se sont produits après le retrait du cathéter, il est recommandé que les mêmes valeurs de laboratoire s'appliquent au placement et au retrait du cathéter péridural. Aucun hématome rachidien n'a été signalé chez 192 patients recevant une analgésie péridurale postopératoire en conjonction avec de la warfarine à faible dose après une arthroplastie totale du genou.
Dans cette étude, les patients ont reçu de la warfarine pour prolonger leur PT à 15.0-17.3 secondes. Les cathéters périduraux ont été laissés à demeure pendant 37 ± 15 heures (extrêmes 13–96 h). Le TP moyen au moment du retrait du cathéter péridural était de 13.4 ± 2 secondes (intervalle de 10.6 à 25.8 s). Cette étude et plusieurs études ultérieures ont documenté l'innocuité relative de l'anticoagulation à faible dose de warfarine chez les patients porteurs d'un cathéter péridural à demeure. Une autre étude a montré que des niveaux d'INR plus élevés (jusqu'à 1.9) sont acceptables pour le retrait des cathéters périduraux tant qu'il est effectué dans les 12 à 14 heures suivant la prise de warfarine. Une étude a montré l'absence d'hématome rachidien lorsque les cathéters périduraux ont été retirés 2 à 3 jours après la prise de warfarine, même avec des INR nettement élevés. La pratique consistant à retirer le cathéter péridural 3 jours après le début de la warfarine, lorsque les taux de facteurs de coagulation VII, IX et X sont faibles (les taux de facteur II peuvent encore être acceptables) doit être étudiée. C'est particulièrement le cas puisque les patients varient considérablement dans leur réponse à la warfarine, incitant certains auteurs à recommander une surveillance étroite de l'état de la coagulation pour éviter un allongement excessif du PT. Les facteurs responsables d'un TP et d'un PTT prolongés sont illustrés dans Chiffres 4 et 5.
L'ASRA a recommandé une valeur INR de 1.4 ou moins comme acceptable pour la performance des blocs nerveux neuraxiaux. Cette valeur est basée sur des études qui ont montré une excellente hémostase périopératoire lorsque la valeur de l'INR était ≤ 1.5. Des études sur les niveaux de facteurs de coagulation à différentes valeurs d'INR ont montré que la diminution de ces facteurs peut ne pas être significative à un INR de 1.5. À des valeurs d'INR de 1.5 à 2.0, les concentrations de facteur II ont été notées comme étant de 74 % à 82 % des valeurs initiales, tandis que les niveaux de facteur VII étaient de 27 % à 54 % des valeurs initiales.
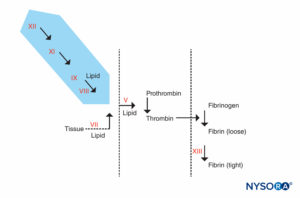
FIGURE 4. Réaction de coagulation. Les facteurs responsables d'un PTT prolongé sont dans la zone ombrée. Les patients qui ont un PTT anormal mais dont le PT et les autres tests sont normaux peuvent être divisés en 2 groupes : ceux qui sont sujets aux saignements et ceux qui ne le sont pas. Les patients qui ne saignent pas peuvent avoir un PTT extrêmement prolongé (90 secondes ou plus) mais n'ont pas d'antécédents de saignement. Ils auront une déficience en facteur XII, en prékalikréine ou en kininogène de haut poids moléculaire. Ces patients ne doivent pas se voir refuser une intervention chirurgicale ou une anesthésie péridurale. L'autre groupe, les patients qui saignent, ont à la fois un PTT prolongé et des antécédents de saignement. Ils auront un déficit en facteur VIII (hémophilie A), en facteur IX (hémophilie B ou maladie de Christmas) ou en facteur XI.
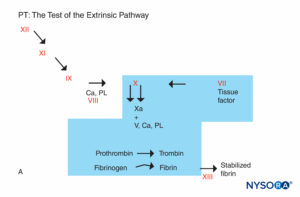
FIGURE 5A. Réaction de coagulation. Les facteurs impliqués dans le PT sont dans la zone ombrée. Le PT est réalisé en ajoutant une source de facteur tissulaire au plasma du patient avec du calcium ou des phospholipides. Le facteur tissulaire forme un complexe avec le facteur VII et l'active. (Ca, calcium ; PL, phospholipide.)
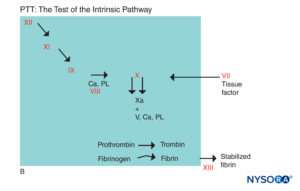
FIGURE 5B. Réaction de coagulation. Les facteurs impliqués dans le PTT sont dans la zone ombrée. Lors de l'évaluation du PTT, la coagulation est initiée par un agent qui active le complexe facteur Hageman-kininogène-prékalikréine. La plupart des facteurs de coagulation sont criblés par PTT, à l'exception des facteurs VII et XIII, la protéine qui stabilise les caillots de fibrine en les réticulant, et des composants du système fibrinolytique. (Ca, calcium ; PL, phospholipide.)
À des valeurs d'INR de 2.1 ± 1 pendant la phase initiale de l'administration de warfarine, les facteurs II et VII étaient de 65 ± 28 % et de 25 ± 20 % des valeurs témoins. Des activités de 40 % sont considérées comme adéquates pour une hémostase normale au moment d'une intervention chirurgicale majeure. Une autre étude a révélé qu'à des INR de 1.3 à 2, sous anticoagulation stable avec de la warfarine, les concentrations des facteurs de coagulation VII, IX et X étaient dans les limites normales.
Le clinicien doit être conscient de l'effet de la warfarine sur la cascade de la coagulation et du rôle de l'INR dans la surveillance de cet effet. Pour minimiser les risques de complications, l'ASRA recommande plusieurs précautions. Le traitement chronique par warfarine orale doit être arrêté et l'INR doit être mesuré avant la réalisation d'un bloc nerveux neuraxial. L'utilisation concomitante d'autres médicaments, tels que l'aspirine, les AINS et les héparines, qui affectent le mécanisme de coagulation, augmente le risque de complications hémorragiques sans affecter l'INR. Si une dose initiale de warfarine est administrée avant la chirurgie, l'INR doit être vérifié si la dose a été administrée plus de 24 heures plus tôt. Si les patients sont sous warfarine à faible dose (dose quotidienne moyenne d'environ 5 mg) pendant l'analgésie péridurale, l'INR doit être vérifié quotidiennement et avant le retrait du cathéter si la dose initiale a été administrée plus de 36 heures auparavant. Des doses quotidiennes plus élevées peuvent nécessiter une surveillance plus intensive. La dose de warfarine doit être maintenue ou réduite lorsque l'INR est> 3 chez les patients porteurs de cathéters neuraxiaux à demeure pour prévenir l'hématome épidural et l'hémarthrome. Pendant le traitement par warfarine, l'état neurologique du patient doit être vérifié régulièrement pendant la perfusion analgésique péridurale, ainsi que 24 heures après le retrait du cathéter. Des concentrations diluées d'anesthésique local doivent être utilisées pour minimiser le degré de blocage sensoriel et moteur. Le jugement clinique doit être exercé pour prendre des décisions concernant le retrait ou le maintien des cathéters neuraxiaux chez les patients présentant des niveaux thérapeutiques d'anticoagulation pendant la perfusion du cathéter neuraxial. La dose de warfarine doit être réduite chez les patients susceptibles d'avoir une réponse accrue au médicament, en particulier les personnes âgées. Chez les patients sous anticoagulation orale chronique, la warfarine doit être arrêtée et l'INR mesuré.
Conseils NYSORA
- Un INR de 1.4, en l'absence de meurtrissabilité facile et de fonction hépatique normale, est acceptable avant l'injection neuraxiale chez les patients devant subir des blocs nerveux neuraxiaux.
- L'INR doit être vérifié si le patient a pris de la warfarine plus de 24 heures auparavant.
- L'INR doit être normal 5 jours après l'arrêt de la warfarine avant une procédure neuraxiale
Héparine
Héparine intraveineuse
L'héparine est un polysaccharide complexe qui exerce son effet anticoagulant en se liant à l'antithrombine. Le changement conformationnel de l'antithrombine accélère sa capacité à inactiver les facteurs de thrombine Xa et IXa.
L'héparine non fractionnée libère l'inhibiteur de la voie du facteur tissulaire de l'endothélium, renforçant son activité contre le facteur Xa. L'effet anticoagulant de l'héparine sous-cutanée prend 1 à 2 heures, mais l'effet de l'héparine intraveineuse est immédiat. En fait, le temps de coagulation est prolongé de 2 à 4 fois le niveau de base 5 minutes après l'injection intraveineuse de 10,000 1.5 unités d'héparine. L'héparine a une demi-vie de 2 à 4 heures. La dose thérapeutique d'héparine cesse 6 à 1.5 heures après son administration. L'aPTT est utilisé pour surveiller l'effet de l'héparine ; l'anticoagulation thérapeutique est obtenue avec un allongement de l'aPTT supérieur à 0.2 fois la valeur initiale ou un taux d'héparine de 0.4 à XNUMX U/mL. L'aPTT n'est généralement pas prolongé par l'administration sous-cutanée de faibles doses d'héparine et n'est pas surveillé. La protamine neutralise l'effet de l'héparine administrée par voie intraveineuse.
L'héparine n'est pas l'anticoagulant idéal puisqu'il s'agit d'un mélange de molécules dont seule une fraction a une activité anticoagulante. Il se lie au facteur plaquettaire 4 et au facteur von Willebrand. Le complexe héparine-antithrombine n'est pas non plus très efficace pour neutraliser la thrombine liée au caillot. Enfin, l'héparine est associée à une thrombocytopénie immunologique et à une thrombose à médiation immunitaire. Pour les patients recevant une héparinothérapie standard, le risque de complications hémorragiques est accru en présence d'autres médicaments qui affectent d'autres mécanismes de coagulation, notamment l'aspirine, les AINS, les HBPM et les anticoagulants oraux. Plusieurs études ont démontré l'innocuité de l'anesthésie rachidienne ou péridurale suivie d'une héparinisation systémique si certaines précautions sont respectées. Rao et El-Etr n'ont rapporté aucun hématome rachidien chez plus de 4000 patients ayant subi une chirurgie vasculaire des membres inférieurs sous anesthésie rachidienne ou péridurale continue. Dans leur étude, les patients présentant des troubles de la coagulation préexistants ont été exclus, l'héparinisation s'est produite au moins 60 minutes après la pose du cathéter, le niveau d'anticoagulation a été soigneusement surveillé et les cathéters à demeure ont été retirés à un moment où l'activité de l'héparine était faible. La chirurgie a été annulée chez les patients lorsque du sang franc a été noté dans l'aiguille et réalisée le lendemain sous anesthésie générale. Les mêmes résultats ont été notés dans un rapport ultérieur dans la littérature neurologique. Ruff et Dougherty ont noté des hématomes rachidiens chez 7 des 342 (2%) patients ayant subi une ponction lombaire et une héparinisation ultérieure pour l'évaluation de l'ischémie cérébrale.
La présence de sang pendant la procédure, le traitement concomitant par aspirine et l'héparinisation dans l'heure qui suit ont été identifiés comme des facteurs de risque dans le développement d'un hématome rachidien. L'ASRA a formulé plusieurs recommandations lorsqu'une technique neuraxiale est utilisée en présence d'anticoagulation peropératoire. L'ASRA conseille d'éviter cette technique chez les patients atteints d'autres coagulopathies. Il doit y avoir un délai d'au moins 1 heure entre le placement de l'aiguille et l'administration de l'héparine. Le cathéter doit être retiré 1 à 2 heures après la dernière dose d'héparine et 4 heure avant l'administration suivante d'héparine. L'aPTT ou le temps de coagulation activé (ACT) doit être surveillé pour éviter un effet excessif de l'héparine. Le patient doit être suivi en postopératoire pour une détection précoce de la réapparition d'un bloc moteur. Des concentrations diluées d'anesthésiques locaux sont recommandées pour minimiser le bloc moteur.
Bien qu'il puisse y avoir un risque accru en cas de placement d'aiguille traumatique (sanglant) ou difficile, il n'existe aucune donnée pour justifier l'annulation obligatoire de la chirurgie. La décision de procéder doit être basée sur un jugement clinique approprié et une discussion approfondie avec le chirurgien et le patient.
Conseils NYSORA
- Il doit y avoir un délai d'au moins 1 heure entre une procédure neuraxiale et la réadministration d'héparine.
- Le cathéter peut être retiré 2 à 4 heures après la dernière dose d'héparine.
Des procédures neuraxiales sont parfois réalisées chez des patients qui subissent une circulation extracorporelle. Les précautions suivantes ont été recommandées pour prévenir le développement d'un hématome intrarachidien chez ces patients :
- Les procédures neuraxiales doivent être évitées chez les patients présentant une coagulopathie connue.
- La chirurgie doit être retardée de 24 heures chez les patients présentant une ponction traumatique.
- Le temps entre la procédure neuraxiale et l'héparinisation systémique doit dépasser 1 heure.
- L'héparinisation et l'inversion doivent être étroitement surveillées et contrôlées.
- Le cathéter péridural doit être retiré lorsque la coagulation normale est rétablie et le patient doit être étroitement surveillé pour détecter tout signe d'hématome spinal.
Héparine sous-cutanée
La base thérapeutique de l'héparine sous-cutanée à faible dose deux fois par jour (5000 unités toutes les 8 à 12 heures) est l'inhibition médiée par l'héparine du facteur X activé. De plus petites doses d'héparine sont nécessaires lorsqu'elles sont administrées en prophylaxie plutôt qu'en traitement de la maladie thromboembolique. Après l'injection intramusculaire ou sous-cutanée de 5000 40 unités d'héparine, l'effet anticoagulant maximal est observé en 50 à 4 minutes et revient à la valeur initiale en 6 à XNUMX heures. L'aPTT peut rester dans la plage normale et n'est souvent pas surveillé. Cependant, de grandes variations dans les réponses individuelles des patients à l'héparine sous-cutanée ont été rapportées. Les techniques neuraxiales ne sont pas contre-indiquées pendant la prophylaxie sous-cutanée (mini-dose), mais le risque de saignement peut être réduit en retardant l'administration d'héparine jusqu'après le bloc nerveux. Les saignements peuvent être augmentés chez les patients affaiblis ou après un traitement prolongé. La sécurité de l'anesthésie neuraxiale majeure en présence d'anticoagulation avec des doses sous-cutanées biquotidiennes d'héparine non fractionnée a été documentée par plusieurs études. Le régime d'héparine sous-cutanée deux fois par jour a été remplacé par un régime trois fois par jour dans la plupart des hôpitaux pour diminuer l'incidence de la thromboembolie veineuse postopératoire. Cependant, cette pratique a été associée à des hématomes spontanés. Pour cette raison, les dernières directives de l'ASRA déconseillent les procédures neuraxiales chez les patients suivant un régime trois fois par jour jusqu'à ce que davantage de données soient disponibles.
Conseils NYSORA
- Les procédures neuraxiales peuvent être réalisées chez les patients sous héparine sous-cutanée deux fois par jour.
- En raison du manque de données adéquates, l'ASRA recommande que les procédures neuraxiales ne soient pas effectuées chez les patients sous héparine sous-cutanée trois fois par jour.
Héparine de bas poids moléculaire
L'héparine non fractionnée est un mélange hétérogène de chaînes polysaccharidiques qui peuvent être séparées en fragments de différents poids moléculaires. L'effet anticoagulant de l'HBPM est similaire à celui de l'héparine non fractionnée ; il active l'antithrombine, accélérant l'interaction de l'antithrombine avec la thrombine et le facteur Xa. L'HBPM a une plus grande activité contre le facteur Xa, tandis que l'héparine non fractionnée a une activité équivalente contre la thrombine et le facteur Xa. La demi-vie plasmatique des HBPM varie de 2 à 4 heures après une injection intraveineuse et de 3 à 6 heures après une injection sous-cutanée ; la demi-vie d'une HBPM est de 2 à 4 fois celle de l'héparine standard. Il a une faible affinité pour les protéines plasmatiques, ce qui se traduit par une plus grande biodisponibilité. Les avantages de l'HBPM par rapport à l'héparine non fractionnée comprennent une biodisponibilité plus élevée et plus prévisible après administration sous-cutanée et une demi-vie biologique plus longue. De plus, la surveillance en laboratoire de la réponse anticoagulante de l'HBPM n'est pas nécessaire et l'ajustement de la dose en fonction du poids n'est pas nécessaire (bien qu'un surdosage puisse survenir chez les patients ayant un IMC bas). L'HBPM présente un effet antithrombotique dose-dépendant qui est précisément évalué par la mesure du niveau d'activité anti-Xa. La récupération de l'activité anti-facteur Xa après une injection sous-cutanée d'HBPM approche les 100 %, rendant la surveillance biologique inutile sauf chez les insuffisants rénaux ou ceux dont le poids corporel est inférieur à 50 kg ou supérieur à 80 kg. Le temps de réaction du thrombélastogramme semble corrélé à la concentration sérique anti-Xa.
Les trois HBPM disponibles dans le commerce aux États-Unis sont l'énoxaparine (Lovenox), la daltéparine (Fragmin) et la tinzaparine (Innohep), bien que cette dernière ait été abandonnée en raison de sa faible utilisation. L'énoxaparine est administrée une fois par jour ou toutes les 12 heures lorsqu'elle est utilisée en prophylaxie, et la daltéparine et la tinzaparine sont administrées une fois par jour. Les trois médicaments semblent avoir une efficacité comparable dans le traitement et la prévention de la thromboembolie veineuse. L'énoxaparine et la daltéparine ont une efficacité comparable dans la prévention du décès ou de l'infarctus du myocarde chez les patients souffrant d'angor instable.
La dose thromboprophylactique recommandée aux États-Unis est de 30 mg d'énoxaparine deux fois par jour, bien que certains cliniciens augmentent la dose chez les patients obèses (1.5 mg/kg par jour ou 1 mg/kg toutes les 12 heures). Le schéma posologique européen est l'énoxaparine 20 à 40 mg une fois par jour, et les patients reçoivent leur dose initiale 12 heures avant la chirurgie, une pratique non observée aux États-Unis.
De nombreux cas d'hématome neuraxial se sont produits aux États-Unis, ce qui a incité la FDA à émettre un avis de santé en décembre 1997 et à convoquer la première conférence de consensus de l'ASRA sur l'anticoagulation et l'anesthésie neuraxiale. Les directives de l'ASRA recommandent d'administrer la plus petite dose efficace d'HBPM. L'administration postopératoire de la thérapie HBPM doit être retardée aussi longtemps que possible, pendant un minimum de 12 heures et idéalement 24 heures après l'opération. Une rachianesthésie à dose unique peut être la technique neuraxiale la plus sûre chez les patients recevant une HBPM préopératoire. Il est recommandé d'attendre au moins 12 heures après la dose prophylactique d'HBPM avant d'effectuer une technique neuraxiale. Les patients qui reçoivent des doses plus élevées d'HBPM (p. ex., énoxaparine 1 mg/kg deux fois par jour) nécessitent des délais plus longs (24 h). Le cathéter doit être retiré lorsque l'activité anticoagulante est faible, au moins 12 heures après l'administration prophylactique d'HBPM et 4 heures avant la dose suivante. Une extrême vigilance quant à l'état neurologique du patient doit être observée si une thromboprophylaxie HBPM est mise en place pendant la perfusion d'une sonde à demeure. Une solution anesthésique locale diluée est recommandée afin que la fonction neurologique puisse être mieux surveillée. L'utilisation d'autres médicaments affectant l'hémostase, tels que les médicaments antiplaquettaires, l'héparine standard, le dextran ou les anticoagulants oraux, en association avec l'HBPM crée un risque supplémentaire de complications hémorragiques.
Conseils NYSORA
- Chez les patients recevant une dose prophylactique d'HBPM, un intervalle de 12 heures est recommandé avant une injection neuraxiale.
- Pour les patients recevant une dose thérapeutique d'HBPM, un intervalle de 24 heures est approprié.
- Un délai de 4 heures après le retrait du cathéter épidural avant la reprise de l'HBPM a été recommandé par la FDA.
THÉRAPIE THROMBOLYTIQUE
Les agents thrombolytiques dissolvent activement les caillots de fibrine déjà formés. Les activateurs de plasminogène exogènes tels que la streptokinase et l'urokinase non seulement dissolvent le thrombus mais affectent également le plasminogène circulant, entraînant une diminution des taux de plasminogène et de fibrine. L'activateur tissulaire recombinant du plasminogène (r-TPA), un agent endogène, est plus sélectif pour la fibrine et a moins d'effet sur les taux de plasminogène circulant. La lyse des caillots entraîne une élévation des produits de dégradation de la fibrine, qui ont un effet anticoagulant en inhibant l'agrégation plaquettaire.
Bien que la mise en place d'une aiguille péridurale ou rachidienne et d'un cathéter avec héparinisation ultérieure semble relativement sûre, le risque d'hématome rachidien chez les patients qui reçoivent un traitement thrombolytique n'est pas bien défini. Des cas d'hématome rachidien chez des patients porteurs de cathéters périduraux ou périduraux à demeure et ayant reçu des agents thrombolytiques ont été rapportés dans la littérature.
Les lignes directrices de l'ASRA formulent des recommandations concernant les procédures neuraxiales après un traitement thrombolytique ou fibrinolytique. L'utilisation concomitante d'héparine avec des médicaments fibrinolytiques ou thrombolytiques expose les patients à un risque élevé d'hémorragie neuraxiale indésirable pendant l'anesthésie rachidienne ou péridurale. Sauf dans des circonstances très inhabituelles, les patients recevant un traitement fibrinolytique ou thrombolytique doivent être mis en garde contre une anesthésie rachidienne ou péridurale. Il n'y a pas de données disponibles pour déterminer clairement la durée appropriée après l'arrêt de ces médicaments et la performance sûre d'une technique neuraxiale. Les directives européennes recommandent de laisser le cathéter épidural en place lorsqu'un patient reçoit un médicament thrombolytique, et de ne le retirer qu'une fois que l'effet du médicament a disparu. Les directives scandinaves recommandent un intervalle de 24 heures entre l'arrêt du médicament et la procédure neuraxiale. Une surveillance neurologique fréquente est recommandée pendant une durée appropriée chez les patients qui ont eu des blocs nerveux neuraxiaux après un traitement fibrinolytique ou thrombolytique. Si un patient reçoit une perfusion épidurale continue et a reçu un traitement fibrinolytique ou thrombolytique, des médicaments minimisant le blocage sensoriel et moteur doivent être utilisés. Il n'y a pas eu de recommandation définitive sur le moment du retrait des cathéters neuraxiaux chez les patients qui reçoivent de manière inattendue un traitement fibrinolytique ou thrombolytique. La mesure des niveaux de fibrinogène peut être utile pour orienter une décision concernant le retrait ou l'entretien du cathéter.
Phytothérapie
Les médicaments à base de plantes les plus couramment utilisés sont l'ail, le ginkgo et le ginseng. L'ail inhibe l'agrégation plaquettaire et son effet sur l'hémostase semble durer 7 jours. Le ginkgo inhibe le facteur d'activation plaquettaire et son effet dure 36 heures. Le ginseng a une variété d'effets : il inhibe l'agrégation plaquettaire in vitro et prolonge à la fois le temps de thrombine (TT) et l'aPTT chez les animaux de laboratoire ; son effet dure 24 heures. Malgré leur effet sur la fonction plaquettaire, les médicaments à base de plantes ne semblent pas présenter à eux seuls de risque significatif supplémentaire dans le développement d'un hématome rachidien chez les patients subissant une anesthésie péridurale ou rachidienne. L'arrêt obligatoire de ces médicaments, ou l'annulation de la chirurgie chez les patients chez qui ces médicaments ont été poursuivis, n'est pas étayé par les données cliniques disponibles. Cependant, l'utilisation concomitante d'autres médicaments qui affectent les mécanismes de coagulation, tels que les anticoagulants oraux ou l'héparine, peut augmenter le risque de complications hémorragiques chez ces patients. Il n'y a pas de test accepté pour évaluer l'adéquation de l'hémostase chez le patient qui a pris des médicaments à base de plantes. À l'heure actuelle, il ne semble pas y avoir de préoccupations spécifiques quant au moment du blocage du nerf neuraxial par rapport au dosage de la phytothérapie, à la surveillance postopératoire ou au moment du retrait du cathéter neuraxial.
Inhibiteurs de la thrombine
Les dérivés d'hirudine recombinants, y compris la désirudine et la bivalirudine, inhibent à la fois la thrombine libre et liée au caillot. L'argatroban, un dérivé de la l-arginine, a un mécanisme d'action similaire. Ces médicaments sont principalement utilisés dans le traitement de la thrombocytopénie induite par l'héparine. Il n'y a pas d'inversion pharmacologique de l'effet de ces médicaments. Aucun cas d'hématome rachidien lié à une anesthésie neuraxiale n'a été rapporté chez des patients ayant reçu un inhibiteur de la thrombine. Cependant, des saignements intracrâniens spontanés ont été rapportés. Selon les directives de l'ASRA, aucune déclaration concernant l'évaluation des risques et la prise en charge des patients ne peut être faite.
Fondaparinux
Le fondaparinux est un anticoagulant synthétique qui produit son effet antithrombotique par inhibition sélective du facteur Xa. Le médicament présente une cohérence dans son effet anticoagulant puisqu'il est synthétisé chimiquement. Il est 100% biodisponible. Rapidement absorbé, il atteint sa concentration maximale dans les 1.7 heures suivant l'administration. Sa demi-vie est de 17 à 21 heures.
Le fondaparinux est préconisé comme antithrombotique après une chirurgie orthopédique majeure et comme traitement initial de l'embolie pulmonaire. La demi-vie prolongée (environ 20 heures) permet une administration une fois par jour. La FDA a émis un avertissement de boîte noire pour le fondaparinux similaire à celui pour les HBPM et l'héparine.
Le risque réel d'hématome rachidien avec le fondaparinux est inconnu. Une étude n'a montré aucune complication chez les patients ayant reçu des injections neuraxiales. Dans cette étude, les cathéters ont été retirés 36 heures après la dernière dose de fondaparinux et le dosage a été retardé de 12 heures après le retrait du cathéter. Les patients étaient exclus de l'étude si des difficultés étaient rencontrées dans la réalisation de la procédure neuraxiale (plus de 3 tentatives nécessaires), si la procédure était compliquée par un saignement, s'ils nécessitaient des médicaments antiplaquettaires ou s'il était prévu de retirer le cathéter péridural le lendemain de la chirurgie. En raison des exigences irréalistes de la pratique clinique, l'ASRA déconseille l'utilisation du fondaparinux en présence d'un cathéter péridural à demeure. Leurs recommandations sont basées sur l'effet antithrombotique soutenu et irréversible du fondaparinux, le dosage postopératoire précoce et l'hématome rachidien rapporté lors des premiers essais cliniques du médicament. Une surveillance étroite de la littérature sur les facteurs de risque associés aux saignements chirurgicaux peut être utile dans l'évaluation des risques et le traitement des patients. L'exécution des techniques neuraxiales doit se produire dans les conditions utilisées dans les essais cliniques (passage d'une seule aiguille, placement atraumatique de l'aiguille, évitement des cathéters neuraxiaux à demeure). Si cela n'est pas possible, une autre méthode de prophylaxie doit être envisagée.
Résumé
L'intervalle de temps entre l'arrêt de l'anticoagulant et la procédure neuraxiale et entre le retrait du cathéter épidural et la reprise du médicament sont résumés dans Tableau 1.
TABLE 1. Intervalles de temps recommandés avant ou après la procédure neuraxiale et le retrait du cathéter péridural.
| Drogue | Temps avant neuraxial Procédure ou retrait du cathéter | Temps après neuraxial Procédure ou retrait du cathéter | Commentaires |
|---|---|---|---|
| Aspirine | Aucun | Aucun | |
| AINS | Aucun | Aucun | |
| Clopidogrel | 7 jours* | Après le retrait du cathéter | Selon les directives européennes et scandinaves |
| Le prasugrel | 7-10 jours | 6h | Selon les directives européennes |
| Ticagrelor | 5 jours | 6h | (Comme ci-dessus) |
| Warfarine | 5 jours (INR normal) | Après le retrait du caterier | |
| Héparine (IV) | 4-6 h | 1-2h | |
| Héparine | |||
| -(Sc, OFFRE) | Aucun | Aucun | |
| -(Sc, TID) | N'est pas applicable | Procédure neuraxiale | |
| HBPM | |||
| Prophylactique | 12 heures | 4 heures | Recommandation de la FDA |
| Thérapeutique | 24 heures | 4 heures | |
| Fondaparinux | 36 et 42 heures | 6 et 12 heures | Selon les directives européennes. L'ASRA a déconseillé les procédures neuraxiales chez les patients prenant le médicament. *Si une procédure neuraxiale doit être réalisée à 5 jours, un test de la fonction plaquettaire est recommandé (voir texte |
NOUVEAUX ANTICOAGULANTS
Une discussion sur les nouveaux anticoagulants dabigatran, rivaroxaban et apixaban implique un examen de certaines informations de base.
L'intervalle entre l'arrêt de l'anticoagulant et l'injection neuraxiale et entre la procédure neuraxiale ou Retrait du cathéter péridural et reprise de l'anticoagulant
Il a été recommandé que deux demi-vies constituent un compromis adéquat entre le risque de thromboembolie veineuse (TEV) et la prévention de l'hématome rachidien. Les recommandations européennes et scandinaves recommandent un intervalle de 2 demi-vies entre l'arrêt de l'anticoagulant et l'injection neuraxiale.
Cette décision a été prise parce que la TEV subclinique survient chez un bon pourcentage de patients immédiatement après la chirurgie et qu'une anticoagulation résiduelle pourrait prévenir cet événement. La présence d'anticoagulation résiduelle facilite la transition vers une anticoagulation complète après une procédure neuraxiale. Après 1, 2, 3, 4, 5 et 6 demi-vies, les pourcentages suivants de médicament restent dans la circulation : 50 %, 25 %, 12.5 %, 6.25 %,
3.125 % et 1.5625 %, respectivement (Tableau 2).Cependant, ces résultats sont basés sur des études chez de jeunes volontaires sains dans des études pharmacocinétiques à dose unique en l'absence d'autres anticoagulants. En revanche, dans la pratique clinique, les patients sont généralement plus âgés et présentent des comorbidités concomitantes.
TABLE 2. Intervalles de temps recommandés avant ou après la procédure neuraxiale et le cathéter épidural pour les nouveaux anticoagulants.
| Drogue | Demi-vie | Lignes directrices européennes | Directives scandinaves | Cinq demi-vies |
|---|---|---|---|---|
| Le dabigatran | 12-17h 28 heures (maladie rénale) | (Contre-indiqué par fabricant) | Données non disponibles | 85h (4j) 6d (malades rénaux) |
| Le rivaroxaban | 9-13h | 22-26h | 18h | 65h (3j) |
| L'apixaban | 15.2 +/-8.5h | 26-30h | Données non disponibles | 75h (3-4j) |
Chez les patients à risque de TEV, tels que ceux ayant des antécédents d'AVC, un intervalle de 2 ou 3 demi-vies peut être approprié, sachant qu'une hémostase adéquate n'est pas assurée. Pour les patients sans facteur de risque thrombotique, un intervalle de 4 à 6 demi-vies entre la dernière dose d'anticoagulant et l'injection neuraxiale assure une élimination plus complète du médicament et un moindre risque de saignement. Un compromis entre les recommandations conservatrices de 4 à 6 demi-vies et de 2 à 3 demi-vies est un intervalle de 5 demi-vies avec la thérapie de pont HBPM.
Concernant la reprise de l'anticoagulant après injection neuraxiale ou retrait du cathéter péridural, les recommandations scandinaves se basent sur la recommandation de Rosencher et al. de 8 heures moins le temps nécessaire à l'anticoagulant pour atteindre son effet maximal.
Huit heures ont été présumées suffisantes pour que le caillot se stabilise, une présomption étayée par l'efficacité des agents thrombolytiques à lyser un caillot s'ils sont administrés dans les 6 heures suivant la formation du caillot. Tertri et ses collègues ont également noté que l'administration d'énoxaparine dans les 24 à 48 heures suivant une hémorragie intracérébrale n'augmentait pas la taille de l'hématome, de sorte qu'un intervalle de 24 heures est probablement plus sûr. D'autres auteurs recommandent une approche plus conservatrice car la réintroduction d'un traitement antithrombotique dans les 24 heures suivant une intervention majeure pourrait augmenter le risque d'hémorragie péri-opératoire. Liew et Douketis recommandent un minimum de 24 heures chez les patients à faible risque de saignement et de 48 heures chez ceux à haut risque de saignement avant de reprendre le dabigatran, le rivaroxaban ou l'apixaban. Les options sont donc soit 8 heures ou 24 heures moins l'effet maximal du médicament.
Il y a probablement peu de différence entre ces deux options puisque les risques de TEV, d'AVC ou de syndrome coronarien aigu sont probablement les mêmes. De plus, le délai d'action et le délai d'effet maximal des nouveaux anticoagulants sont courts.
Le dabigatran
Le dabigatran etexilate est une prodrogue qui est hydrolysée par les estérases dans l'estomac en médicament actif. Le dabigatran etexilate a une biodisponibilité de 7.2 %. Le dabigatran est un inhibiteur direct de la thrombine qui bloque nerveusement l'interaction de la thrombine avec divers substrats. Les concentrations plasmatiques maximales sont atteintes 1.5 à 3 heures après la prise du promédicament. Il a une demi-vie de 14 à 17 heures. La clairance rénale représente 80 % de la clairance totale du dabigatran. En cas d'insuffisance rénale terminale, la demi-vie d'élimination double de 14 heures à 28 heures.
Le dabigatran est efficace dans le traitement de la TEV aiguë et dans la prévention des récidives de TEV. Chez les patients atteints de fibrillation auriculaire, le dabigatran réduit les taux d'accident vasculaire cérébral et d'embolie systémique à un degré similaire à celui de la warfarine. Le dabigatran ne s'est pas avéré cohérent dans la prévention de la TEV après une chirurgie articulaire totale. Des études ont montré qu'il était soit plus efficace, soit non inférieur, soit inférieur à l'énoxaparine. Une méta-analyse des essais n'a noté aucune différence entre le dabigatran et l'énoxaparine dans aucun des paramètres analysés. Le fabricant déclare que les cathéters périduraux ne doivent pas être placés chez les patients recevant du dabigatran. Un intervalle minimum de 2 heures entre le retrait du cathéter à demeure et l'administration de dabigatran a été recommandé par Levy et ses collègues. Cet intervalle semble être plus court que 6 heures, c'est-à-dire la différence entre 8 heures moins le temps de 2 heures pour atteindre l'effet maximal du médicament. Des saignements accrus ont été signalés après la prise de dabigatran. La Société d'hématologie d'Australie et de Nouvelle-Zélande a identifié 78 épisodes hémorragiques chez environ 7000 2 patients sur une période de XNUMX mois. Un audit de la FDA a toutefois conclu qu'il n'y avait pas d'augmentation absolue des saignements avec le dabigatran par rapport à la warfarine.
Le TCA est prolongé après le dabigatran, mais la relation est curviligne. Le temps de thrombine (TT), également connu sous le nom de temps de coagulation de la thrombine (TCT), est très sensible aux effets du dabigatran et est utilisé de manière plus appropriée pour détecter la présence de l'effet anticoagulant du dabigatran que pour quantifier l'effet du médicament. Un TT dilué présente une inérité pour les concentrations plasmatiques de dabigatran pharmacologiquement pertinentes. Le temps de coagulation de l'écarine (ECT), qui mesure directement la génération de thrombine, est prolongé de manière dose-dépendante par le dabigatran. C'est le test le plus sensible pour le dabigatran, mais peu d'institutions ont le test disponible. Le temps de prothrombine (TP) est le test le moins sensible. Le TT dilué et l'ECT sont les tests de choix pour le dabigatran.
À ce jour, il n'existe aucun antidote permettant d'inverser l'effet du dabigatran ou des autres nouveaux anticoagulants oraux. Le charbon actif empêche l'absorption du médicament, mais il doit être administré dans les 2 heures suivant l'ingestion de dabigatran. La dialyse pourrait accélérer l'élimination des médicaments. Des concentrés de complexes plasmatiques (PCC) contenant 3 (facteurs II, IX et X) ou 4 (facteurs II, VII, IX et X) facteurs de coagulation ont été suggérés, mais leur efficacité n'a pas été prouvée. L'idarucizumab, un fragment d'anticorps monoclonal qui se lie au dabigatran libre et lié à la thrombine, a récemment été approuvé par la FDA.
Conseils NYSORA
- Le dabigatran dépend principalement des reins pour son élimination, et sa demi-vie est doublée chez les patients atteints de maladie rénale.
- Un intervalle plus long entre l'arrêt du médicament et la procédure neuraxiale, probablement 6 jours, est recommandé chez ces patients.
Le rivaroxaban
Le rivaroxaban est un inhibiteur direct du facteur Xa. Les concentrations plasmatiques maximales sont observées dans les 2.5 à 4 heures, et l'inhibition maximale du facteur Xa (jusqu'à 68 %) survient 3 heures après l'administration et se maintient pendant au moins 12 heures, ou 24 à 48 heures lorsque des doses plus élevées sont administrées chez les personnes âgées. les patients. Le rivaroxaban a une demi-vie terminale de 5.7 à 9.2 heures, mais celle-ci peut atteindre 11 à 13 heures chez les patients âgés en raison du déclin de la fonction rénale lié à l'âge. Un tiers du médicament est éliminé par les reins, un tiers par voie fécale/biliaire et un tiers est transformé en métabolites inactifs. La concentration maximale n'est pas affectée par l'obésité (patients pesant ≥ 120 kg) mais est augmentée de 24 % chez les patients pesant ≤ 50 kg. La clairance rénale du rivaroxaban diminue avec l'augmentation de l'insuffisance rénale.
Le rivaroxaban est efficace dans le traitement des TEV symptomatiques et non inférieur à la warfarine dans la prévention des AVC emboliques au cours de la fibrillation auriculaire. L'ajout de rivaroxaban au traitement antiplaquettaire standard réduit le critère composite de décès par causes cardiovasculaires, infarctus du myocarde ou accident vasculaire cérébral chez les patients atteints d'un syndrome coronarien aigu récent. Le rivaroxaban s'est avéré aussi efficace ou supérieur à l'énoxaparine dans la prévention de la TEV après une chirurgie articulaire totale. Dans les études RECORD 1, 2, 3 et 4, le rivaroxaban était un agent thromboprophylactique plus efficace que l'énoxaparine, avec un profil de tolérance similaire. Rosencher et al. ont déclaré que les cathéters périduraux n'étaient pas retirés avant au moins 2 demi-vies après la dernière dose de rivaroxaban, et que la dose suivante de rivaroxaban était administrée 4 à 6 heures après le retrait du cathéter. Aucun des 1141 patients ayant reçu du rivaroxaban et ayant subi une anesthésie neuraxiale n'a développé d'hématome rachidien. Cependant, ce petit nombre de patients n'est pas suffisant pour tirer une conclusion ferme sur la sécurité périopératoire de ce régime.
Les recommandations européennes et scandinaves recommandent un intervalle de 2 demi-vies entre l'arrêt du rivaroxaban et la mise en place ou le retrait du cathéter péridural (18 heures dans les recommandations scandinaves et 22 à 26 heures dans les recommandations européennes). Ces lignes directrices recommandent également un intervalle de 4 à 6 heures avant la reprise de la dose suivante, car le rivaroxaban prend 2.5 à 4 heures pour atteindre son effet maximal.
Une corrélation linéaire a été observée entre les effets du rivaroxaban et le TP. Cependant, il existe une variabilité marquée dans la sensibilité des réactifs PT au rivaroxaban, il est donc recommandé que chaque laboratoire calibre son PT spécifiquement pour le rivaroxaban. L'aPTT manque de sensibilité suffisante pour déterminer l'effet du rivaroxaban. L'inhibition du facteur Xa peut également être un substitut des concentrations plasmatiques de rivaroxaban. Le TP et les anti-Xa sont les tests recommandés pour le suivi des effets du rivaroxaban.
L'utilisation de charbon actif a été recommandée pour éliminer le rivaroxaban, mais il doit être administré dans les 8 heures suivant la prise de rivaroxaban. Il a été démontré qu'un PCC à 4 facteurs inverse l'activité anticoagulante in vitro du rivaroxaban chez des volontaires sains. En raison de leur forte liaison aux protéines, le rivaroxaban et l'apixaban peuvent ne pas être dialysables.
L'apixaban
Apixaban est un inhibiteur hautement spécifique du facteur Xa. Il est rapidement absorbé et atteint des concentrations maximales en 1 à 2 heures. Des études ont montré que la demi-vie terminale d'apixaban était de 13.5 +/- 9.9 heures, soit 15.2 +/- 8.5 heures après une dose unique de 5 mg et 11.7 +/- 3.3 après plusieurs doses de 5 mg. La concentration plasmatique maximale est affectée par le poids corporel, avec des concentrations plus élevées d'apixaban chez les sujets de faible poids corporel. L'activité plasmatique anti–facteur Xa a montré une relation linéaire directe avec la concentration plasmatique d'apixaban.
Apixaban a une biodisponibilité orale de plus de 45 %. Après administration orale, il est éliminé par de multiples voies d'élimination ainsi que par excrétion rénale et intestinale directe. Vingt-quatre à 29 % de la dose est excrétée par les reins et 56 % de la dose est récupérée dans les selles. Plus de la moitié de l'apixaban est excrété sous forme inchangée, ce qui réduit le risque d'interactions métaboliques médicamenteuses Apixaban est efficace pour réduire les accidents vasculaires cérébraux ou les embolies systémiques sans augmenter le risque de saignement. Apixaban est supérieur à la warfarine dans la prévention des accidents vasculaires cérébraux ou des embolies systémiques chez les patients atteints de fibrillation auriculaire. Apixaban assure une thromboprophylaxie efficace dans l'arthroplastie totale du genou, comparable à l'énoxaparine ou à la warfarine. L'apixaban est aussi efficace que l'énoxaparine pour prévenir la TEV après une arthroplastie totale du genou (ATG) tout en ayant un taux d'hémorragie majeure inférieur ou similaire. L'apixaban est plus efficace que l'énoxaparine pour prévenir la TEV après prothèse totale de hanche (PTH) sans augmentation des saignements. Dans cet essai, « les dispositifs liés à une anesthésie intrathécale ou péridurale ont été retirés au moins 5 heures avant la première dose » d'apixaban. Dans toutes les études sur l'apixaban, le médicament a été commencé 12 à 24 heures après la chirurgie.
Comparé au rivaroxaban, l'apixaban a peu d'effet sur le TP lorsqu'il est administré aux doses approuvées. Le test PT dilué a une sensibilité améliorée par rapport au PT conventionnel. Il semble exister une corrélation linéaire entre l'activité anti-Xa et les concentrations plasmatiques d'apixaban. Le test anti-Xa s'est avéré plus sensible que le PT et aussi sensible que le test PT dilué et semble être le meilleur choix pour le suivi clinique de l'effet anticoagulant de l'apixaban. Le charbon actif, administré dans les 3 heures suivant l'ingestion, réduit l'absorption d'apixaban.
Andexanet est une protéine leurre recombinante modifiée du facteur Xa humain qui se lie et séquestre les inhibiteurs du facteur Xa. Des études chez des volontaires et chez des patients ont montré qu'andexanet vénère l'activité anticoagulante du rivaroxaban et de l'apixaban. Depuis 2016, andexanet n'est pas encore cliniquement disponible aux États-Unis.
Résumé des recommandations pour les nouveaux anticoagulants
Alors qu'un intervalle de 2 à 3 demi-vies peut être acceptable chez les patients à haut risque de TEV ou d'AVC, un intervalle de 4 à 6 demi-vies entre l'arrêt du médicament et l'injection neuraxiale est probablement plus sûr chez la plupart des patients à faible risque de thrombose. Un intervalle de 5 demi-vies en conjonction avec un traitement relais HBPM est une alternative chez la plupart des patients, comme le montre Tableau 2. Après une procédure neuraxiale ou le retrait d'un cathéter péridural, l'anticoagulant peut être repris 6 heures (8 heures moins le début/l'effet maximal du médicament, qui est généralement de 2 heures) plus tard. Les anticoagulants sont généralement repris dans les 24 à 48 heures chez la plupart des patients, mais ils peuvent être repris plus tôt chez les patients qui présentent un risque plus élevé de TEV ou d'AVC ; c'est-à-dire 24 heures moins le temps d'effet maximal du médicament. D'autres ont recommandé un intervalle de 24 heures (Tableau 3)
TABLE 3. Intervalles de temps recommandés pour la reprise du médicament après une procédure neuraxiale ou le retrait du cathéter.
| Drogue | Lignes directrices européennes | Directives scandinaves | Liew & Douketis (102); Connolly et Spyropoulos (98) |
|---|---|---|---|
| Le dabigatran | 6h | 6h | 24h |
| Le rivaroxaban | 4-6h | 6h | 24h |
| L'apixaban | 4-6h | 6h | 24h |
La surveillance en laboratoire de l'effet anticoagulant est appropriée dans certaines situations, et des agents d'inversion sont suggérés lorsqu'il est nécessaire de restaurer rapidement la fonction hémostatique.
Conseils NYSORA
- Pour les nouveaux anticoagulants, un intervalle de 5 demi-vies entre l'arrêt du médicament et la procédure neuraxiale est recommandé jusqu'à ce qu'il y ait plus d'expérience avec ces agents.
- Un intervalle de 8 ou 24 heures jusqu'à l'effet maximal du médicament est recommandé avant que le médicament ne soit repris après le retrait du cathéter ; un intervalle de 24 heures est probablement le plus sûr.
CARACTÉRISTIQUES CLINIQUES, DIAGNOSTIC ET GESTION DE L'HÉMATOME ÉPIDURAL
Les patients qui développent un hématome rachidien présentent généralement des douleurs dorsales soudaines, sévères et constantes avec ou sans composante radiculaire. La percussion sur la colonne vertébrale aggrave la douleur, tout comme les manœuvres qui augmentent la pression intraspinale, y compris la toux, les éternuements ou les efforts. De plus, le retour de la faiblesse motrice et/ou du déficit sensitif après la résolution apparente du bloc épidural ou rachidien est fortement évocateur de la formation d'un hématome épidural ou rachidien. Les résultats moteurs et sensoriels dépendent entièrement du niveau et de la taille de l'hématome, mais peuvent inclure une faiblesse, une parésie, une perte de la fonction intestinale ou vésicale et pratiquement tout déficit sensoriel. L'imagerie par résonance magnétique (IRM) est l'étude diagnostique de choix. Le diagnostic différentiel comprend un abcès spinal, un néoplasme épidural, une hernie discale aiguë et une hémorragie sous-arachnoïdienne spinale. La récupération sans chirurgie est rare et une consultation neurochirurgicale pour envisager une laminectomie décompressive urgente doit être obtenue dès qu'un hématome rachidien est suspecté. La récupération fonctionnelle est principalement liée à la durée pendant laquelle les symptômes sont présents avant la chirurgie. Les caractéristiques cliniques, le diagnostic, le diagnostic différentiel et le traitement d'un patient atteint d'un hématome rachidien sont discutés plus en détail dans Toxicité systémique des anesthésiques locaux.
RÉSUMÉ
Les praticiens doivent périodiquement mettre à jour leur base de connaissances sur les nouveaux médicaments anticoagulants, les protocoles d'anticoagulation, les recommandations actuelles des lignes directrices et les alertes de la FDA. Étant donné que l'hématome rachidien peut survenir même en l'absence de facteurs de risque identifiables, la vigilance dans la surveillance est essentielle pour une évaluation précoce du dysfonctionnement neurologique et une intervention rapide. La décision d'effectuer un bloc neuraxial et le moment du retrait du cathéter chez un patient recevant un traitement anticoagulant doivent être pris sur une base individuelle, en évaluant les avantages de l'anesthésie régionale par rapport au risque faible, bien que certain, d'hématome rachidien.
Anticoagulation et blocs nerveux périphériques
Le cas échéant, des blocs nerveux périphériques peuvent être réalisés chez les patients sous anticoagulants. Contrairement aux procédures neuraxiales en présence d'anticoagulants, il n'y a pas eu d'études prospectives sur les blocs nerveux périphériques en présence d'anticoagulants. L'ASRA recommande les mêmes directives pour les blocs nerveux périphériques que pour les procédures neuraxiales. Des cas de psoas et d'hématomes rétropéritonéaux ont été rapportés après des blocs nerveux du plexus lombaire et des blocs nerveux du compartiment psoas. Ces patients étaient soit sous énoxaparine, soit sous ticlopidine, soit sous clopidogrel. Dans certains cas, l'hématome est survenu malgré le respect des directives de l'ASRA.
Les symptômes de la formation d'un hématome après un bloc nerveux périphérique peuvent inclure des douleurs (douleurs au flanc ou paravertébrales, ou douleurs à l'aine dans les saignements du psoas), une sensibilité dans la région, une baisse constante de l'hémoglobine/hématocrite, une hypotension due à l'hypovolémie et un déficit sensitivo-moteur. Le diagnostic définitif est fait par tomographie informatisée (CT); l'échographie peut également être utilisée pour détecter la présence d'un hématome sous-capsulaire rénal après bloc nerveux du compartiment psoas. Le traitement peut inclure une consultation chirurgicale, l'inversion de l'anticoagulation, une transfusion sanguine si nécessaire et une attente sous surveillance par rapport au drainage chirurgical.
Il est probablement trop restrictif d'adapter les recommandations de l'ASRA sur les blocs nerveux neuraxiaux aux patients subissant des blocs nerveux périphériques. La Société européenne d'anesthésiologie a noté que les lignes directrices pour le bloc nerveux neuraxial ne s'appliquent pas systématiquement aux blocs nerveux périphériques. La Société autrichienne d'anesthésiologie, de réanimation et de soins intensifs, d'autre part, a suggéré que les blocs nerveux superficiels peuvent être réalisés en toute sécurité en présence d'anticoagulants. En raison de la possibilité d'hématome rétropéritonéal, les blocs du plexus lombaire et des nerfs paravertébraux méritent les mêmes recommandations que pour les injections neuraxiales. Les mêmes directives devraient également s'appliquer aux blocs nerveux sympathiques viscéraux. Les lignes directrices de l'ASRA peuvent donc s'appliquer aux blocs nerveux dans les zones vasculaires et non compressibles, tels que les blocs nerveux du plexus coeliaque, les blocs nerveux du plexus hypogastrique supérieur et les blocs nerveux du plexus lombaire. Les cliniciens doivent individualiser leur décision et discuter des risques et des avantages du bloc nerveux avec le patient et le chirurgien. Plus important encore, le clinicien doit suivre le patient de près après la mise en place du bloc nerveux.
Conseils NYSORA
- Les lignes directrices sur les injections neuraxiales devraient également s'appliquer aux blocs nerveux du plexus lombaire et aux blocs nerveux sympathiques viscéraux.
- Pour les blocs nerveux superficiels, des blocs nerveux régionaux échoguidés peuvent probablement être réalisés en présence d'anticoagulation résiduelle.
Références
- Horlocker TT, Wedel DJ : Anticoagulation et bloc nerveux neuraxial : perspective historique, implications anesthésiques et gestion des risques. Reg Anesth Pain Med 1998;23:129–134.
- Tryba M : [Anesthésie régionale péridurale et héparine de bas poids moléculaire : Pro]. Anasthesiol Intensivmed Notfallmed Schmerzther 1993;28:179–181.
- Pöpping DM, Zahn PK, Van Aken HK, Dasch B, Boche R, Pogatzki-Zahn EM : Efficacité et sécurité de la gestion de la douleur postopératoire : une enquête auprès de 18 925 patients consécutifs entre 1998 et 2006 (2e révision) : une analyse de base de données prospective données relevées. Br J Anaesth 2008;101:832–840.
- Moen V, Dahlgren N, Irestedt L : Complications neurologiques sévères après des blocs neuraxiaux centraux en Suède 1990–1999. Anesthésiologie 2004 ; 101 : 950–959.
- Volk T, Wolf A, Van Aken H, Bürkle H, Wiebalck A, Steinfeldt T : Incidence de l'hématome rachidien après ponction épidurale : analyse du réseau allemand pour la sécurité en anesthésie régionale. Eur J Anaesthesiol 2012;29:170–176.
- Ehrenfeld JM, Agarwal AK, Henneman JP, Sandberg WS : Estimation de l'incidence d'un hématome épidural suspecté et du coût d'imagerie caché du cathétérisme épidural : une étude rétrospective de 43,200 2013 cas. Reg Anesth Pain Med 38;409:414–XNUMX.
- Bateman BT, Mhyre JM, Ehrenfeld J, et al : Le risque et les résultats des hématomes épiduraux après un cathétérisme épidural périopératoire et obstétrical : un rapport du consortium de recherche multicentrique sur les résultats périopératoires. Anesth Analg 2013:116:1380–1385.
- Horlocker T, Kopp S : Hématome épidural après bloc épidural aux États-Unis : il ne s'agit plus seulement d'héparine de bas poids moléculaire après une chirurgie orthopédique. Anesth Analg 2013;116:1195–1197.
- Horlocker T : Bloc neuraxial chez les patients atteints de sténose rachidienne : entre le marteau et l'enclume. Anesth Analg 2010;110:1305.
- Gulur P, Tsui B, Pathak R, Koury KM, Lee H : analyse rétrospective de l'incidence de l'hématome péridural chez les patients porteurs de cathéters périduraux et de paramètres de coagulation anormaux. Br J Anaesth 2015;114:808–811.
- Heit JA, Horlocker TT (eds) : Anesthésie neuraxiale et anticoagulation. Reg Anesth Pain Med 1998;23:S129–S193.
- Horlocker TT, Wedel DJ, Benzon HT, et al : Anesthésie régionale chez le patient anticoagulé : Définir les risques (La deuxième conférence de consensus de l'ASRA sur l'anesthésie neuraxiale et l'anticoagulation). Reg Anesth Pain Med 2003;28:171–197.
- Horlocker TT, Wedel DJ, Rowlingson JC, et al : Anesthésie régionale chez le patient recevant un traitement antithrombotique ou un traitement thrombolytique : directives fondées sur des preuves de l'American Society of Regional Anesthesia and Pain Medicine (troisième édition). Reg Anesth Pain Med 2010;35:64–101.
- Gogarten W, Vandermeulen E, Van Aken H, Kozek S, Llau JV, Samama CM : Société européenne d'anesthésiologie. Anesthésie régionale et agents antithrombotiques : recommandations de la Société européenne d'anesthésiologie. Eur J Anaesthesiol 2010;27:999–1015.
- Breivik H, Bang U, Jalonen J, Vigfusson G, Alahuhta S, Lagerkranser M : Directives nordiques pour les blocs neuraxiaux dans l'hémostase perturbée de la Société scandinave d'anesthésiologie et de médecine de soins intensifs. Acta Anaesthesiol Scand 2010;54:16–41.
- Cronberg S, Wallmark E, Söderberg I : Effet sur l'agrégation plaquettaire de l'administration orale de 10 analgésiques non stéroïdiens à l'homme. Scand J Haematol 1984;33:155–159.
- Locke GE, Giorgio AJ, Biggers SL Jr, et al : hématome épidural spinal aigu secondaire à un saignement prolongé induit par l'aspirine. Surg Neurol 1976;5:293–296.
- Vandermeulen EP, Van Aken H, Vermylen J : Anticoagulants et anesthésie rachidienne-péridurale. Anesth Analg 1994;79:1165–1177.
- Groupe collaboratif CLASP (étude collaborative sur l'aspirine à faible dose pendant la grossesse). CLASP : un essai randomisé d'aspirine à faible dose pour la prévention et le traitement de la pré-éclampsie chez 9364 femmes enceintes. Lancet 1994;343:619–629.
- Horlocker TT, Wedel DJ, Offord KP : Le traitement antiplaquettaire préopératoire augmente-t-il le risque de complications hémorragiques associées à l'anesthésie régionale ? Anesth Analg 1990;70:631–634.
- Horlocker TT, Wedel DJ, Schroeder DR, et al : le traitement antiplaquettaire préopératoire n'augmente pas le risque d'hématome rachidien associé à l'anesthésie régionale. Anesth Analg 1995;80:303–309.
- Benzon HT, Brunner EA, Vaisrub N : Temps de saignement et blocs nerveux après l'aspirine. Reg Anesth 1984;9:86–90.
- Horlocker TT, Bajwa ZH, Ashraft Z, et al : évaluation du risque de complications hémorragiques associées aux médicaments anti-inflammatoires non stéroïdiens chez les patients ambulatoires de la clinique de la douleur subissant une injection épidurale de stéroïdes. Anesth Analg 2002;95 : 1691–1697.
- Benzon HT, Wong HY, Siddiqui T, et al : prudence lors de la réalisation d'injections péridurales chez les patients prenant plusieurs médicaments antiplaquettaires. Anesthésiologie 1999 ;91 :1558–1559.
- Benzon HT, Huntoon M : Avons-nous besoin de nouvelles lignes directrices pour les procédures interventionnelles contre la douleur chez les patients sous anticoagulants ? Reg Anesth Pain Med 2014;39:1–3.
- Giberson CE, Barbosa J, Brooks ES, et al : Hématomes épiduraux après le retrait des fils d'essai du stimulateur percutané de la moelle épinière : deux rapports de cas. Reg Anesth Pain Med 2014;39:73–77.
- Williams KN, Jackowski A, Evans PJD : Hématome épidural nécessitant une décompression chirurgicale à la suite d'injections répétées de stéroïdes périduraux cervicaux pour la douleur chronique. Douleur 1990 ; 42 : 197–199.
- Ain RJ, Vance MB : Hématome épidural après injection épidurale de stéroïdes chez un patient refusant l'énoxaparine conformément aux directives. Anesthésiologie 2005 ; 102 : 701–703.
- Buvanendran A, Young A : Hématome épidural spinal après le placement de la sonde d'essai d'un stimulateur de la moelle épinière chez un patient prenant de l'aspirine. Reg Anesth Pain Med 2014;39:70–72.
- Desai MJ, Dua S: Hématome périneural suite à une injection de stéroïde transforaminal lombaire provoquant une radiculopathie lombaire aiguë sur chronique: à propos d'un cas. Pratique de la douleur 2014 ; 14 : 271–277.
- Mahmoud J, Mathews M, Verna S, Basil B : Thrombocytopénie induite par l'oxcarbazépine. Psychosomatique 2006;47:73–74.
- Meijer WEE, Heerdink ER, Nolen WA, Herings RMC, Leufkens HGM, Egberts ACG. Association du risque de saignement anormal avec le degré d'inhibition de la recapture de la sérotonine par les antidépresseurs. Arch Intern Med 2004;164:2367–2370.
- Narouze S, Benzon HT, Provenzano DA, et al : Procédures interventionnelles de la colonne vertébrale et de la douleur chez les patients sous antiplaquettaires et anticoagulants : directives de l'American Society of Regional Anesthesia and Pain Medicine, de la European Society of Regional Anesthesia and Pain Therapy, de l'American Academy of Pain Medicine, l'International Neuromodulation Society, la North American Neuromodulation Society et l'Institut mondial de la douleur. Reg Anesth Pain Med 2015;40 : 182–212.
- Gajraj NM : inhibiteurs de la cyclooxygénase-2. Anesth Analg 2003;96 : 1720–1738.
- Buvanendran A, Kroin JS, Tuman KJ, et al : Effets de l'administration périopératoire d'un inhibiteur sélectif de la cyclooxygénase 2 sur la gestion de la douleur et la récupération de la fonction après une arthroplastie du genou : un essai contrôlé randomisé. JAMA 2003;290:2411–2418.
- Gajraj NM, Joshi GP : Rôle des inhibiteurs de la cyclooxygénase-2 dans la gestion de la douleur postopératoire. Anesthesiol Clin North America 2005;23:49–72.
- Desjardins PJ, Shu VS, Recker DP, et al : Une dose préopératoire unique de valdécoxib, un nouvel inhibiteur spécifique de la cyclooxygénase-2, soulage la douleur post-chirurgie orale ou oignonectomie. Anesthésiologie 2002 ; 97 : 565–573.
- Sinatra RS, Shen QJ, Halaszynski T, et al : suspension orale préopératoire de rofécoxib comme adjuvant analgésique après une chirurgie abdominale basse : les effets d'une douleur dépendante de l'effort et de la fonction pulmonaire. Anesth Analg 2003;98:135–140.
- Locataire PT, Hubbard RC, Karim A, et al : Effets du célécoxib, un nouvel inhibiteur de la cyclooxygénase-2, sur la fonction plaquettaire chez des adultes en bonne santé : un essai clinique randomisé. J Clin Pharmacol 2000;40:124–132.
- van Heeken H, Schwartz JI, Depre M, et al : activité inhibitrice comparative du rofécoxib, du méloxicam, du diclofénac, de l'ibuprofène et du naproxène sur la COX-2 par rapport à la COX-1 chez des volontaires sains. J Clin Pharmacol 2000;40:1109–1120.
- Greenberg H, Gottesdiener K, Huntington M, et al : Un nouvel inhibiteur de la cyclooxygénase-2, le rofécoxib (VIOXX) n'a pas modifié les effets antiplaquettaires de l'aspirine à faible dose chez des volontaires sains. J Clin Pharmacol 2000;40:1509–1515.
- Psaty BM, Furberg CD : Inhibiteurs de la Cox-2—Leçons sur la sécurité des médicaments. N Engl J Med 2005;352:1133–1135.
- Schror K : Médicaments antiplaquettaires : une revue comparative. Drogues 1995 ; 50 : 7–28.
- Yang LH, Fareed J : Action vasomodulatrice du clopidogrel et de la ticlopidine. Thromb Res 1997;86:479–491.
- Comité de pilotage CAPRIE : Essai randomisé en aveugle clopidogrel versus aspirine chez des patients à risque d'AVC ischémique (CAPRIE). Lancet 1996;348:1329–1339.
- Helft G, Osende JI, Worthley SG, et al : effet antithrombotique aigu d'un régime à charge frontale de clopidogrel chez les patients atteints d'athérosclérose sous aspirine. Arterioscler Thromb Vasc Biol 2000;29:2316–2321.
- Mayumi T, Dohi S : Hématome sous-arachnoïdien spinal après ponction lombaire chez un patient recevant un traitement antiplaquettaire. Anesth Analg 1983;62:777–779.
- Benzon HT, McCarthy R, Benzon HA, et al : Détermination de l'activité antiplaquettaire résiduelle du clopidogrel. Br J Anaesth 2011;107 : 966–971.
- Hall R, Mazer CD : Médicaments antiplaquettaires : un examen de leur pharmacologie et de leur gestion pendant la période périopératoire. Anesth Analg 2011;112 : 292–318.
- Wallentin L : inhibiteurs de P2Y(12) : différences de propriétés et de mécanismes d'action et conséquences potentielles pour l'utilisation clinique. Eur Heart J 2009;30:1964–1977.
- Capodanno D, Ferreiro JL, Angiolillo DJ : Thérapie antiplaquettaire : nouveaux agents pharmacologiques et changements de paradigmes. J Thromb Haemost 2013;11(Suppl 1):316–329.
- Brandt JT, Payne CD, Wiviott SD, et al : Une comparaison des doses de charge de prasugrel et de clopidogrel sur la fonction plaquettaire : l'ampleur de l'inhibition plaquettaire est liée à la formation de métabolites actifs. Am Heart J 2007;153:66.e9–16.
- Dobesh PP : Pharmacocinétique et pharmacodynamique du prasugrel, un inhibiteur de la thiénopyridine P2Y12. Pharmacothérapie 2009;29:1089–1102.
- Asai F, Jacubowski JA, Nagamura H, et al : Activité inhibitrice plaquettaire et pharmacocinétique du prasugrel (CS-747), un nouvel inhibiteur de la thiénopyridine P2Y12 : une étude à dose unique croissante chez des humains en bonne santé. Plaquettes 2006 ; 17 : 209–217.
- Wiviott SD, Trenk D, Frelinger AL, et al : Prasugrel comparé au clopidogrel à dose de charge et d'entretien élevée chez les patients ayant subi une intervention coronarienne percutanée planifiée : le prasugrel en comparaison avec le clopidogrel pour l'inhibition de l'activation et de l'agrégation plaquettaires - Thrombolyse dans l'infarctus du myocarde 44 essai. Diffusion 2007 ;116 : 2923–2932.
- Wiviott SD, Antman EM, Winters KJ, et al : comparaison randomisée du prasugrel (CS-747, LY640315), un nouvel antagoniste de la thiénopyridine P2Y12, avec le clopidogrel dans l'intervention coronarienne percutanée : résultats de l'utilisation conjointe de médicaments pour bloquer les plaquettes de manière optimale (JUMBO )-essai TIMI 26. Diffusion 2005 ;111 :3366–3373.
- Brandt JT, Close SL, Iturria SJ et al : les polymorphismes courants du CYP2C19 et du CYP2C9 affectent la réponse pharmacocinétique et pharmacodynamique au clopidogrel mais pas au prasugrel. J Thromb Haemost 2007;5:2429–2436.
- Mega JL, Close SL, Wiviott SD, et al : polymorphismes génétiques du cytochrome P450 et réponse au prasugrel : relation avec les résultats pharmacocinétiques, pharmacodynamiques et cliniques. Diffusion 2009 ;119 : 2553–2560.
- Teng R, Butler K : Pharmacocinétique, pharmacodynamique, tolérabilité et innocuité de doses uniques croissantes de ticagrelor, un antagoniste des récepteurs P2Y(12) oral à liaison réversible, chez des sujets sains. Eur J Clin Pharmacol 2010;66:487–496.
- Teng R, Oliver S, Hayes MA, Butler K : Absorption, distribution, métabolisme et excrétion du ticagrélor chez des sujets sains. Drug Metab Dispos 2010;38:1514–1521.
- Husted S, Emanuelsson H, Heptinstall S, Sandset PM, Wickens M, Peters G : Pharmacodynamique, pharmacocinétique et sécurité de l'antagoniste oral réversible P2Y12 AZD6140 avec de l'aspirine chez les patients atteints d'athérosclérose : une comparaison en double aveugle avec le clopidogrel avec de l'aspirine. Eur Heart J 2006;27:1038–1047.
- Gurbel PA, Bliden KP, Butler K, et al : évaluation randomisée en double aveugle de l'effet ONSET et OFFSET des effets antiplaquettaires du ticagrélor par rapport au clopidogrel chez les patients atteints d'une maladie coronarienne stable : l'étude ONSET/OFFSET. Diffusion 2009 ;120 : 2577–2585.
- George JN : Plaquettes. Lancet 2000;355:1531–1539.
- van Giezen J, Nilsson L, Berntsson P, et al : le ticagrelor se lie au P2Y(12) humain indépendamment de l'ADP, mais s'oppose à la signalisation des récepteurs induits par l'ADP et à l'agrégation plaquettaire. J Thromb Haemost 2009;7:1556–1565.
- Baron TH, Kamath PS, McBane RD : Gestion du traitement antithrombotique chez les patients subissant des procédures invasives. N Engl J Med 2013;368:2113–2124.
- Rodgers RPC, Levin J : Une réévaluation critique du temps de saignement. Semin Thromb Hemost 1990;16:1–20.
- Ferraris VA, Swanson E : Utilisation d'aspirine et perte de sang périopératoire chez les patients subissant des opérations inattendues. Surg Gynecol Obstet 1983;156:439–442.
- Mammen EF, Comp PC, Gossselin R, et al : système PFA-100. Une nouvelle méthode d'évaluation du dysfonctionnement plaquettaire. Semin Thromb Hemost 1998;24:195–202.
- Edwards A, Jakubowski JA, Rechner AR, Sugidachi A, Harrison P : Évaluation de la cartouche de test INNOVANCE PFA P2Y : sensibilité au bloc P2Y(12) et influence de l'anticoagulant. Plaquettes 2012 ;23 : 106–115.
- Gorog DA, Fuster V : Tests de la fonction plaquettaire en cardiologie clinique. J Am Coll Cardiol 2013;61:2115–2129.
- Bouman HJ, Parlak E, van Werkum JW, et al : Quel test de la fonction plaquettaire convient pour surveiller la réactivité au clopidogrel ? Une analyse pharmacocinétique sur le métabolite actif du clopidogrel. J Thromb Haemost 2010;8:482–488.
- van Werkum JW, Harmsze AM, Elsenberg EH, Bouman HJ, ten Berg JM, Hackeng CM : L'utilisation du système VerifyNow pour surveiller le traitement antiplaquettaire : un examen des preuves actuelles. Plaquettes 2008 ; 19 : 479–488.
- Mueller T, Dieplinger B, Poelz W, Haltmayer M : Utilité de l'instrument PFA-100 et du nouvel analyseur multiplaques pour l'évaluation des effets de la spirine et du clopidogrel sur la fonction plaquettaire chez les patients atteints de maladies cardiovasculaires. Clin Appl Thromb Hemost 2009;15:652–659.
- Scharbert G, Auer A, Kozek-Langenecker S : Évaluation du test de cartographie plaquettaire sur la thromboélastométrie rotationnelle ROTEM. Plaquettes 2009 ; 20 : 125–130.
- Malinin A, Pokov A, Swaim L, Kotob M, Serebruany V : Validation d'une cartouche VerifyNow-P2Y12 pour la surveillance de l'inhibition plaquettaire avec le clopidogrel. Méthodes Trouver Exp Clin Pharmacol 2006;28:315.
- Benzon HT, Avram J, Green D, Bonow RO : Nouveaux anticoagulants oraux et anesthésie régionale. Br J Anaesth 2013;111(Suppl 1):i96–i113.
- Kearon C, Hirsh J : Gestion de l'anticoagulation avant et après une chirurgie élective. N Engl J Med 1997;336:1506–1511.
- Harrison L, Johnston M, Massicote MP, et al : comparaison des doses de 5 mg et 10 mg lors de l'initiation du traitement par la warfarine. Ann Intern Med 1997;126:133–136.
- Benzon HT, Benzon HA, Kirby-Nolan M, Avram MJ, Nader A : Niveaux de facteur VII et facteurs de risque d'augmentation du rapport international normalisé dans la phase précoce du traitement par la warfarine. Anesthésiologie 2010 ;112 : 298–304.
- Schulman S, Lockner D, Bergstrom K, Blomback M : Anticoagulation orale initiale intensive et traitement à l'héparine plus court dans la thrombose veineuse profonde. Thromb Haemost 10984;52:276–280.
- Enneking FK, Benzon HT : Anticoagulants oraux et anesthésie régionale : une perspective. Reg Anesth Pain Med 1998;23:140–145.
- Odoom JA, Sih IL : Analgésie péridurale et traitement anticoagulant. Anesthésie 1983 ;38 : 254–259.
- Horlocker TT : Quand retirer un cathéter rachidien ou péridural chez un patient sous anticoagulation. Reg Anesth 1993;18:264–265.
- Horlocker TT, Wedel DJ, Schlichting JL : Analgésie épidurale postopératoire et traitement anticoagulant oral. Anesth Analg 1994;79:89–93.
- Wu CL, Perkins FM : Prophylaxie anticoagulante orale et retrait du cathéter épidural. Reg Anesth 1996;21:517–524.
- Liu SS, Buvanendran A, Viscusi ER, et al : Retrait simple des cathéters épiduraux chez 4365 1.4 patients présentant un rapport international normalisé supérieur à 2011 lors de l'initiation du traitement par la warfarine. Reg Anesth Pain Med 36;231:235–XNUMX.
- Weinstock DM, Chang P, Aronson DL, et al : Comparaison des concentrations plasmatiques de prothrombine et de facteur VII et de prothrombine F1 urinaire chez les patients sous traitement à long terme par la warfarine et ceux en phase initiale. Am J Hematol 1998;57:193–199.
- Jerkeman A, Astermark J, Hedner U, et al : Corrélation entre différentes intensités de traitement anti-vitamine K et paramètres de coagulation. Thromb Res 2000;98:467–471.
- Abildgaard U, Lindahl AK, Sandset PM : L'héparine nécessite à la fois l'antithrombine et un inhibiteur de la voie extrinsèque pour son effet anticoagulant dans le sang humain. Hémostase 1991;21:254–257.
- Murray DJ, Brodsnahan WJ, Pennell B, et al : détection de l'héparine par le temps de coagulation activé : une comparaison de la sensibilité des tests de coagulation et des dosages d'héparine. J Cardiothorac Vasc Anesth 1997; 11:24–28.
- Shapiro SS. Traiter la thrombose au 21ème siècle. N Engl J Med 2003;349:1762–1764.
- Rao TL, El-Etr AA : Anticoagulation suite à la mise en place de cathéters épiduraux et sous-arachnoïdiens : une évaluation des séquelles neurologiques. Anesthésiologie 1981 ; 55 : 618–620.
- Ruff DL, Dougherty JH : Complications de l'anticoagulation suivie d'anticoagulation. Accident vasculaire cérébral 1981;12:879–881.
- Liu SS, Mulroy MF : Anesthésie neuraxiale et analgésie en présence d'héparine standard. Reg Anesth Pain Med 1998;23:157–163.
- Chaney MA : Anesthésie et analgésie intrathécale et péridurale pour la chirurgie cardiaque. Anesth Analg 1997;84:1211–1221.
- Geerts WH, Bergqvist D, Pineo GF, et al : Prévention de la thromboembolie veineuse. American College of Chest Physicians Evidence-Based Clinical Practice Guidelines (8e édition). Poitrine 2008 ;133 : 381S–453S.
- King CS, Holley AB, Jackson JL, et al : Dosage d'héparine deux fois contre trois fois par jour pour la prophylaxie thromboembolique dans la population générale : une méta-analyse. Poitrine 2007 ; 131 : 507–516.
- Weitz JI. Traitement médicamenteux : héparines de bas poids moléculaire. N Engl J Med 1997;337:688–698.
- Horlocker TT, Heit JA : Héparine de bas poids moléculaire : biochimie, pharmacologie, régimes de prophylaxie périopératoire et lignes directrices pour la gestion de l'anesthésie régionale. Anesth Analg 1997;85:874–885.
- Bara L, Billaud E, Gramond G, et al : Pharmacocinétique comparative d'une héparine de bas poids moléculaire (PK 10 169) et d'une héparine non fractionnée après administration intraveineuse et sous-cutanée. Thromb Res 1985;39:631–636.
- Klein S, Slaughter T, Vail PT, et al : Thrombelastography comme mesure périopératoire de l'anticoagulation résultant de l'héparine de bas poids moléculaire : une comparaison avec les concentrations anti-Xa. Anesth Analg 2000;91:1091–1095.
- White RH : Héparines de bas poids moléculaire : sont-elles toutes identiques ? Br J Haematol 2003;121:12–20.
- Horlocker TT, Wedel DJ : Bloc neuraxial et héparine de bas poids moléculaire : équilibrer l'analgésie périopératoire et la thromboprophylaxie. Reg Anesth Pain Med 1998;23:164–177.
- Administration américaine des aliments et médicaments. Communication de la FDA sur la sécurité des médicaments : recommandations mises à jour pour réduire le risque de saignement de la colonne vertébrale et de paralysie chez les patients sous héparines de bas poids moléculaire. http://www.fda.gov/drugs/drugsafety/ucm373595.htm. Mis à jour le 19 janvier 2016. Consulté le 9 septembre 2015.
- Rosenquist RW, Brown DL : Saignement neuraxial : Fibrinolytiques/thrombolytiques. Reg Anesth Pain Med 1998;23S:152–156.
- Bauer KA : Fondaparinux : propriétés de base, efficacité et sécurité dans la prophylaxie de la thromboembolie veineuse. Am J Orthop 2002;31:4–10.
- Turpie AG, Bauer KA, Eriksson BL, et al : Fondaparinux vs énoxaparine pour la prévention de la thromboembolie veineuse en chirurgie orthopédique majeure : une méta-analyse de 4 études randomisées en double aveugle. Arch Intern Med 2002;162:1833–1840.
- Les enquêteurs de Matisse : fondaparinux sous-cutané versus héparine intraveineuse non fractionnée dans le traitement initial de l'embolie pulmonaire. N Engl J Med 2003;349:1695–1702.
- Singelyn FJ, Verheyen CC, Piovella F, Van Aken HK, Rosenceher N, enquêteurs de l'étude EXPERT : L'innocuité et l'efficacité de la thromboprophylaxie étendue avec le fondaparinux après une chirurgie orthopédique majeure du membre inférieur avec ou sans cathéter neuraxial ou nerveux périphérique profond : l'EXPERT Étude. Anesth Analg 2007;105:1540–1547.
- Rosencher N, Bonnet MP, Sessler DI : Nouveaux agents antithrombotiques sélectionnés et anesthésie neuraxiale pour la chirurgie orthopédique majeure : stratégies de gestion. Anesthésie 2007 ; 62 : 1154–1160.
- Greenblatt DJ : Demi-vie d'élimination des médicaments : valeur et limites. Ann Rev Med 985;36:421–427.
- Olesen JB, Lip GY, Hansen ML, et al : Validation des schémas de stratification des risques pour prédire les accidents vasculaires cérébraux et les thromboembolies chez les patients atteints de fibrillation auriculaire : étude de cohorte à l'échelle nationale. BMJ 2011;342:d124.
- Connolly G, Spyropoulos AC : Problèmes pratiques, limites et gestion périprocédurale des NOAC. J Thromb Thrombolysis 2013;36:212–222.
- Garcia D, Barrett YC, Ramaciotti E, Weitz JI : Évaluation en laboratoire des effets anticoagulants de la prochaine génération d'anticoagulants oraux. J Thromb Haemost 2013;11:245–252.
- Groupe de collaboration IST-3 : Les avantages et les inconvénients de la thrombolyse intraveineuse avec un activateur tissulaire du plasminogène recombinant dans les 6 heures suivant un AVC ischémique aigu (le troisième essai international sur les AVC [IST-3]) : un essai randomisé. Lancet 2012;379:2352–2363.
- Tertri S, Hakal J, Juvela S, et al : Sécurité de l'énoxaparine sous-cutanée à faible dose pour la prévention de la thromboembolie veineuse après une hémorragie intracérébrale primaire. Thromb Res 2008;123:206–212.
- Liew A, Douketis J : Prise en charge périopératoire des patients qui reçoivent un nouvel anticoagulant oral. Intern Emerg Med 2013;8:477–484.
- Blech S, Ebner T, Ludwig-Schwellinger E, Stangier J, Roth W : Le métabolisme et la disposition de l'inhibiteur direct de la thrombine par voie orale, le dabigatran, chez l'homme. Drug Metab Disposition 2008;36:386–399.
- Di Nisio M, Middeldorp S, Buller HR. Inhibiteurs directs de la thrombine. N Engl J Med 2005;353:1028–1040.
- Levy JH, Faraoni D, Spring JL, Douketis JD, Samana CM : Gestion des nouveaux anticoagulants oraux dans les unités de soins périopératoires et intensifs. Anesthésiologie 2013 ;118 :1466–1474.
- Stangier J, Clemens A : Pharmacologie, pharmacocinétique et pharmacodynamique du dabigatran etexilate, un inhibiteur direct de la thrombine par voie orale. Clin Appl Thromb Hemost 2009;15(S1):9S–16S.
- Stangier J, Stahle H, Rathgen K, Fuhr R : Pharmacocinétique et pharmacodynamique du dabigatran, un inhibiteur oral direct de la thrombine, chez des sujets âgés en bonne santé. Clin Pharmacokinet 2008;47:47–59.
- Eisert WG, Hauel N, Stangier J, Wienen W, Clemens A, Van Ryn J : Dabigatran : un nouvel inhibiteur non peptidique réversible puissant de la thrombine. Arterioscler Thromb Vasc Biol 2010;30:1885–1889.
- Stangier J, Rathgen K, Stahle H, Mazur D : Influence de l'insuffisance rénale sur la pharmacocinétique et la pharmacodynamique du dabigatran etexilate oral. Une étude ouverte, en groupes parallèles, monocentrique. Clin Pharmacokinet 2010;49:259–268.
- Ezekowitz MD, Reilly PA, Nehmiz G, et al. Dabigatran avec ou sans aspirine concomitante comparé à la warfarine seule chez les patients atteints de fibrillation auriculaire non valvulaire (étude PETRO). Am J Cardiol 2007;100 : 1419–1426.
- Ericksson BI, Dahl OE, Buller HR, et al ; Groupe d'étude BISTRO II : Un nouvel inhibiteur oral direct de la thrombine, le dabigatran etexilate, comparé à l'énoxaparine pour la prévention des événements thromboemboliques après une arthroplastie totale de la hanche ou du genou : l'essai randomisé BISTRO II. J Thromb Haemost 2005;3:103–111.
- Ericksson BI, Dahl OE, Rosencher N, et al ; Groupe d'étude RE-MODEL : Dabigatran etexilate oral vs énoxaparine sous-cutanée pour la prévention de la thromboembolie veineuse après prothèse totale de genou : l'essai randomisé RE-MODEL. J Thromb Haemost 2007;5:2178–2185.
- Ericksson BI, Dahl OE, Rosencher N, et al ; Groupe d'étude RE-NOVATE. Dabigatran etexilate versus énoxaparine pour la prévention de la thromboembolie veineuse après prothèse totale de hanche : un essai randomisé, en double aveugle, de non-infériorité. Lancet 2007;370:949–956.
- Comité de rédaction RE-MOBILIZE, Ginsberg JS, Davidson BL, Comp PC, et al : Inhibiteur oral de la thrombine dabigatran etexilate vs régime nord-américain d'énoxaparine pour la prévention de la thromboembolie veineuse après une arthroplastie du genou. J Arthroplastie 2009 ;24 : 1–9.
- Wolowacz SE, Roskell NS, Plumb JM, Caprini JA, Ericksson BI : Efficacité et innocuité du dabigatran étaxilate pour la prévention de la thromboembolie veineuse après une arthroplastie de la hanche ou du genou. Une méta-analyse. Thromb Haemost 2009;101:77–85.
- Harper P, Young L, Merriman E : Risque de saignement avec le dabigatran chez les personnes âgées fragiles. N Engl J Med 2012;366:864–866.
- Tripode A : Le laboratoire et les anticoagulants oraux directs. Sang 2013;121:4032–4035.
- Siegal DM, Cuker A : Inversion des nouveaux anticoagulants oraux chez les patients présentant des saignements majeurs. J Thromb Thrombolysis 2013;35:391–398.
- Miyares MA, Davis K : Nouveaux anticoagulants oraux : un examen des options de surveillance en laboratoire et des agents d'inversion chez le patient hémorragique. Am J Health Syst Pharm 2012;69:1473–1484.
- Baron TH, Kamath PS, McBane RD : Gestion du traitement antithrombotique chez les patients subissant des procédures invasives. N Engl J Med 2013;368:2113–2124.
- Breuer G, Weiss DR, Ringwald J : « Nouveaux » anticoagulants oraux directs dans le cadre périopératoire. Curr Opin Anaesthesiol 2014;27:409–419.
- Lévy S : Nouveaux antithrombotiques disponibles en clinique et leurs antidotes. J Interv Card Electrophysiol 2014;40:269–275.
- Laux V, Perzborn E, Kubitza D, Misselwitz F : Caractéristiques précliniques et cliniques du rivaroxaban : un nouvel inhibiteur oral direct du facteur Xa. Sem Thromb Hemost 2007;33:515–523.
- Kubitza D, Becka M, Wensing G, Voith B, Zuehlsdorf M : Innocuité, pharmacodynamie et pharmacocinétique de BAY 59-7939 - un inhibiteur oral direct du facteur Xa - après administration multiple chez des sujets masculins en bonne santé. Eur J Clin Pharmacol 2005;61:873–880.
- Jiang J, Hu Y, Zhang J, et al : Sécurité, pharmacocinétique et pharmacodynamique de doses uniques de rivaroxaban - un inhibiteur oral direct du facteur Xa - chez les sujets chinois âgés. Thromb Haemost 2010;103:234–241.
- Kubitza D, Becka M, Roth A, Mueck W : étude à dose croissante de la pharmacocinétique et de la pharmacodynamique du rivaroxaban chez des sujets âgés en bonne santé. Curr Med Res Opin 2008;24:2757–2765.
- Ericksson BI, Quinlan DJ, Weitz JI : Pharmacodynamique et pharmacocinétique comparatives de la thrombine directe orale et des inhibiteurs du facteur Xa en cours de développement. Clin Pharmacokinet 2009;48:1–22.
- Weitz JI, Eikelboom JW, Samama MM : nouveaux médicaments antithrombotiques. Poitrine 2012;141S:e120S–e151S.
- Kubitza D, Becka M, Mueck W, et al : Effets de l'insuffisance rénale sur la pharmacocinétique, la pharmacodynamique et l'innocuité du rivaroxaban, un inhibiteur direct du facteur Xa par voie orale. Br J Clin Pharmacol 2010;70:703–712.
- Patel MR, Mahaffey KW, Garg J, et al ; Chercheurs de ROCKET AF : Rivaroxaban versus warfarine dans la fibrillation auriculaire non valvulaire. N Engl J Med 2011;365:883–891.
- Eriksson BI, Borris LC, Friedman RJ, et al ; Groupe d'étude RECORD1 : Rivaroxaban versus énoxaparine pour la thromboprophylaxie après arthroplastie de la hanche. N Engl J Med 2008;358:2765–2775.
- Kakkar AK, Brenner B, Dahl O, et al ; Investigateurs RECORD2 : rivaroxaban à durée prolongée par rapport à l'énoxaparine à court terme pour la prévention de la thromboembolie veineuse après arthroplastie totale de la hanche : un essai contrôlé randomisé en double aveugle. Lancet 2008 ;372 : 31–39.
- Lassen MR, Ageno W, Borris LC, et al ; Enquêteurs RECORD3 : Rivaroxaban versus énoxaparine pour la thromboprophylaxie après arthroplastie totale du genou. N Eng J Med 2008;358:2776–2786.
- Turpie AG, Lassen MR, Davidson BL, et al; Investigateurs RECORD4 : Rivaroxaban versus énoxaparine pour la thromboprophylaxie après arthroplastie totale du genou (RECORD4) : un essai randomisé. Lancet 2009 ;373 : 1673–1680.
- Ericksson BI, Kakkar AK, Turpie AG, et al : rivaroxaban oral pour la prévention de la thromboembolie veineuse symptomatique après une arthroplastie élective de la hanche et du genou. J Bone Joint Surg Br 2009;91:636–644.
- Rosencher N, Liau JV, Mueck W, Loewe A, Berkowitz SD, Homering M : Incidence de l'hématome neuraxial après une chirurgie totale de la hanche ou du genou : programme RECORD (rivaroxaban vs énoxaparine). Acta Anaesthesiol Scand 2013;57:565–572.
- Samama MM : Quel test utiliser pour mesurer l'effet anticoagulant du rivaroxaban : le dosage anti-facteur Xa. J Thromb Haemost 2013;11:579–580.
- Raghavan N, Frost CE, Yu Z, et al : Métabolisme et pharmacocinétique de l'apixaban après administration orale à l'homme. Drug Metab Dispos 2009;37:74–81.
- Frost C, Wang J, Nepal S, et al : Apixaban, un inhibiteur oral direct du facteur Xa : innocuité d'une dose unique, pharmacocinétique, pharmacodynamique et effet alimentaire chez des sujets sains. Br J Pharmacol 2013;75:476–487.
- Frost C, Nepal S, Wang J, et al : sécurité, pharmacocinétique et pharmacodynamique de doses orales multiples d'apixaban, un inhibiteur du facteur Xa, chez des sujets sains. Br J Clin Pharmacol 2013;76:776–786.
- Zhang D, He K, Raghavan N, et al : Métabolisme comparatif de l'apixaban marqué au 14C chez la souris, le rat, le lapin, le chien et l'homme. Drug Metab Dispos 2009;37:1738–1748.
- Lassen MR, Davidson BL, Gallus A, Pineo G, Ansell J, Deitchman D : L'efficacité et l'innocuité de l'apixaban, un inhibiteur oral direct du facteur Xa, en tant que thromboprophylaxie chez les patients après une arthroplastie totale du genou. J Thromb Haemost 2007;5:2368–2375.
- Lassen MR, Rasskob GE, Gallus A, Pineo G, Chen D, Portman RJ : Apixaban ou énoxaparine pour la thromboprophylaxie après arthroplastie du genou. N Engl J Med 2009;361:594–604.
- Lassen MR, Raskob GE, Gallus A, Pineo G, Chen D, Hornick P ; Investigateurs ADVANCE-2 : Apixaban versus énoxaparine pour la thromboprophylaxie après arthroplastie du genou (ADVANCE-2) : un essai randomisé en double aveugle. Lancet 2010;375:807–815.
- Lassen MR, Gallus A, Raskob GE, Pineo G, Chen D, Ramirez LM ; Investigateurs ADVANCE-3 : Apixaban versus énoxaparine pour la thromboprophylaxie après une arthroplastie de la hanche. N Engl J Med 2010;363 : 2487–2498.
- Barrett YC, Wang Z, Frost C, Shenker A : mesure en laboratoire clinique des inhibiteurs directs du facteur Xa : le test anti Xa est préférable au test du temps de prothrombine. Thromb Haemost 2010;104:1263–1271.
- Kozek-Langenecker SA, Fries D, Gutl M, et al : Anesthésie locorégionale et inhibiteurs de la coagulation. Recommandations du groupe de travail sur la coagulation périopératoire de la Société autrichienne d'anesthésiologie et de médecine de soins intensifs. Anesthésiste 2005 ;54 :476–484.
- Siegal DM, Curnutte JT, Connolly SJ, et al. Andexanet alfa pour l'inversion de l'activité de l'inhibiteur du facteur Xa. N Engl J Med 2015;373 : 2413–242

