Honorio T. Benzon, Rasha S. Jabri e Tom C. Van Zundert
INTRODUÇÃO
O hematoma intraespinhal é uma condição relativamente rara resultante de uma variedade de causas. As causas traumáticas incluem punção lombar e anestesia neuraxial. É mais provável que ocorra em pacientes anticoagulados ou trombocitopênicos, pacientes com doença neoplásica ou naqueles com doença hepática ou alcoolismo. Aproximadamente um quarto a um terço de todos os casos estão associados à terapia anticoagulante. O risco de formação de hematoma intraespinhal após a administração de anestesia e analgesia neuroaxial é aumentado em pacientes que receberam terapia anticoagulante ou têm um distúrbio de coagulação. Por esse motivo, a anestesia neuraxial é frequentemente contraindicada na presença de uma coagulopatia. Outros fatores de risco para o desenvolvimento de hematoma epidural ou espinhal incluem dificuldade técnica (várias tentativas) na realização dos procedimentos do neuroeixo devido a anormalidades anatômicas da coluna e punções múltiplas ou sanguinolentas.
A incidência de hematoma espinhal foi originalmente relatada como sendo uma em 150,000 peridural e uma em 220,000 anestesias espinhais. Estudos epidemiológicos recentes mostraram que a incidência de hematoma espinhal é mais frequente, variando de uma em 2700 a uma em 19,505 epidurais. O estudo mais recente mostrou um risco geral de 1 em 21,643 injeções epidurais. Os idosos (um em 3800) estão em risco aumentado devido a anormalidades degenerativas da coluna, osteoporose e doença vascular periférica. Populações obstétricas parecem ter menor incidência de hematoma espinhal (uma em 200,000), provavelmente secundária ao estado de hipercoagulabilidade da gravidez, maior capacidade do espaço peridural em parturientes mais jovens e maior pressão intra-epidural. Com base em um grande estudo retrospectivo recente, a incidência de hematoma epidural em pacientes com coagulação anormal pode ser tão baixa quanto um em 315 pacientes.
A introdução da heparina de baixo peso molecular (HBPM) foi associada a um pico na incidência de hematoma espinhal, resultando em um alerta da Food and Drug Administration (FDA) e na introdução da primeira declaração de consenso sobre anestesia regional em pacientes sobre anticoagulantes pela Sociedade Americana de Anestesia Regional e Medicina da Dor (ASRA) em 1998. As diretrizes foram baseadas em uma extensa revisão da literatura e da farmacologia dos diferentes anticoagulantes.
Foram feitas recomendações quanto ao momento do bloqueio do nervo neuroaxial, remoção do cateter peridural e posterior administração de anticoagulantes. Em particular, o uso de baixas concentrações de anestésicos locais para infusão epidural (para preservar a força motora para facilitar o monitoramento) e o monitoramento neurológico subsequente foram recomendados pela ASRA. As diretrizes de consenso, publicadas em 1998 e atualizadas em 2003 e 2010, têm auxiliado muito os médicos na tomada de decisão com relação ao uso de procedimentos neuroaxiais no contexto da terapia de anticoagulação. Dois outros conjuntos de diretrizes, publicados pela Sociedade Europeia de Anestesiologia e pela Sociedade Escandinava de Anestesiologia e Medicina Intensiva, são influentes na Europa.
Neste capítulo, discutimos o significado dos anticoagulantes comuns e esperamos oferecer ao leitor um guia na tomada de decisão sobre o uso de anestesia neuroaxial e bloqueios de nervos periféricos (BNPs) na prática clínica. Também discutiremos os novos anticoagulantes, medicamentos que não foram adequadamente cobertos nas últimas diretrizes da ASRA e apenas parcialmente cobertos pelas diretrizes europeias e escandinavas. Acesse o link para saber mais sobre Diagnóstico e Manejo do Hematoma Espinhal e de Nervos Periféricos.
TERAPIA ANTIPLAQUETÓRIA
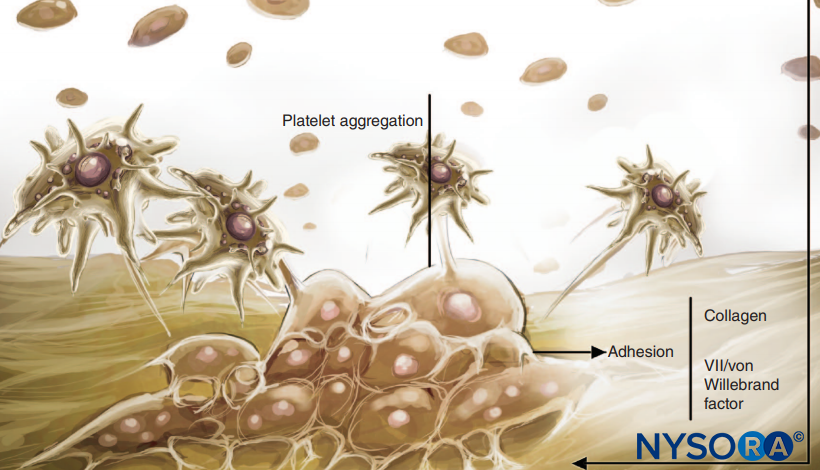
Os medicamentos antiplaquetários inibem a enzima ciclooxigenase plaquetária e impedem a síntese de tromboxano A2. O tromboxano A2 é um potente vasoconstritor que facilita a agregação plaquetária secundária e as reações de liberação. O papel das plaquetas na coagulação e hemostasia é mostrado em Figuras 1 e 2. As plaquetas de pacientes em uso desses medicamentos apresentam aderência plaquetária normal ao subendotélio e formação normal do tampão hemostático primário. Um coágulo adequado, embora potencialmente frágil, pode se formar. Embora esses tampões possam ser barreiras hemostáticas satisfatórias para lesões vasculares menores, eles podem não garantir a formação adequada de coágulos hemostáticos perioperatórios. A função plaquetária em pacientes que recebem medicamentos antiplaquetários deve ser considerada diminuída por 1 semana com aspirina e 1 a 6 dias com anti-inflamatórios não esteroides (AINEs). Essa suposição não leva em consideração a formação contínua de novas plaquetas funcionais. A produção contínua de plaquetas frescas e funcionando normalmente, combinada com a função residual de plaquetas já circulantes, pode explicar a relativa segurança da realização de procedimentos neuroaxiais nesses pacientes.
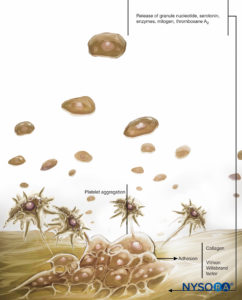
FIGURA 1. Papel das plaquetas na coagulação. As plaquetas desempenham seu papel na hemostasia por meio de três reações básicas: adesão, ativação (e secreção) e agregação. Quando o endotélio vascular é danificado, as plaquetas ligam-se rapidamente ao subendotélio por um processo denominado adesão.
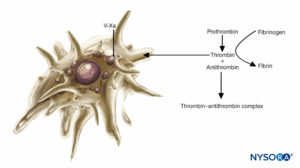
FIGURA 2. Papel das plaquetas na coagulação: As plaquetas suportam as reações de coagulação do plasma. Quando ativadas, as plaquetas ligam-se a vários complexos de proteínas plasmáticas e secretam uma forma ativada do fator V (fator Va), que se liga à superfície plaquetária e se liga ao fator Xa. O fator Xa ligado às plaquetas acelera então a conversão da protrombina em trombina.
O risco de hematoma epidural e espinhal em pacientes em terapia antiplaquetária foi aumentado por um relato de caso de formação espontânea de hematoma epidural na ausência de anestesia espinhal ou epidural em um paciente com histórico de ingestão de aspirina. Vandermeulen e colaboradores implicaram a terapia antiplaquetária em 3 dos 61 casos de hematoma espinhal ocorridos após raquianestesia ou peridural. Outros estudos mostraram um risco relativamente baixo de hematoma espinhal em pacientes em uso de aspirina ou AINEs submetidos a procedimento neuraxial. O grupo Collaborative Low-dose Aspirin Study in Pregnancy (CLASP) incluiu 1422 pacientes obstétricas de alto risco que receberam 60 mg de aspirina diariamente e foram submetidas à anestesia peridural sem sequelas neurológicas. Em um estudo retrospectivo de 1013 anestésicos espinhais e peridurais em que 39% dos pacientes tomaram drogas antiplaquetárias, incluindo 11% dos pacientes que estavam em uso de múltiplas medicações antiplaquetárias, nenhum paciente desenvolveu sinais de hematoma espinhal.
Já os pacientes em uso de antiplaquetários apresentaram maior incidência de aspiração de sangue pela agulha raquidiana ou peridural ou pelo cateter. Um estudo prospectivo subsequente em 1000 pacientes, 39% dos quais relataram terapia antiplaquetária pré-operatória, observou a ausência de complicações hemorrágicas. Portanto, a terapia antiplaquetária pré-operatória não foi um fator de risco para agulha sangrenta ou colocação de cateter. Sexo feminino, idade avançada, história de hematomas ou sangramento excessivos, técnica de cateter contínuo, calibre de agulha grande, múltiplas tentativas e colocação de agulha difícil foram considerados fatores de risco significativos. Os estudos clínicos em pacientes da clínica de dor são semelhantes aos submetidos à cirurgia. Pacientes em uso de aspirina ou AINEs que foram submetidos a injeções epidurais de esteróides não desenvolveram sinais ou sintomas de hematoma intraespinal.
A falta de correlação entre a medicação antiplaquetária e a colocação de agulha ou cateter com sangue fornece algumas evidências de que a terapia antiplaquetária pré-operatória não representa um fator de risco significativo para o desenvolvimento de disfunção neurológica por hematoma espinhal em pacientes em terapia antiplaquetária. Deve-se notar que houve relatos de casos de hematoma intraespinal em pacientes em uso de aspirina ou AINEs, embora houvesse fatores complicadores nesses relatos de casos. Estes incluíram administração concomitante de heparina, coexistência de angioma venoso epidural e dificuldade técnica na realização do procedimento. Mais recentemente, mais relatos de casos de hematoma espinhal foram publicados em relação a procedimentos intervencionistas da dor, especificamente colocações de estimulação da medula espinhal.
Com base nas evidências disponíveis, a ASRA fez várias recomendações sobre medicamentos antiplaquetários. A terapia antiplaquetária pré-operatória não representa um fator de risco significativo para o desenvolvimento de disfunção neurológica por hematoma espinhal em pacientes em terapia antiplaquetária. O risco de complicações hemorrágicas, no entanto, pode ser aumentado em pacientes em uso de vários medicamentos antiplaquetários e uso concomitante de outros medicamentos que afetam os mecanismos de coagulação, como anticoagulantes orais, heparina padrão e HBPM.
Dicas NYSORA
- Provavelmente é seguro realizar procedimentos de anestesia neuraxial e regional em pacientes em uso de aspirina e AINEs.
- Os fatores de risco para aumento do sangramento e hematoma espinhal incluem a ingestão de vários antiplaquetários pelo paciente e a realização de múltiplas tentativas.
Aspirina e Procedimentos Intervencionistas de Dor
Houve vários relatos de casos de hematoma espinhal após injeção peridural de esteróides ou colocação ou remoção de um estimulador da medula espinhal em pacientes que estavam tomando aspirina isoladamente, AINEs isoladamente ou quando as diretrizes da ASRA foram seguidas. Essas ocorrências podem estar relacionadas às frequentes anormalidades da coluna encontradas nesses pacientes, à presença de fibrose após a cirurgia da coluna, agulhas maiores utilizadas na colocação do estimulador medular ou às frequentes manipulações (avanços e retrações) dos eletrodos.
Medicamentos usados no tratamento da dor também causam sangramento; estes incluem a oxcarbazepina e os inibidores seletivos da recaptação da serotonina. Por essas razões, a ASRA entrou em contato com a Sociedade Europeia de Anestesia Regional e Terapia da Dor, a Academia Americana de Medicina da Dor, a Sociedade Internacional de Neuromodulação, a Sociedade Norte-Americana de Neuromodulação e o Instituto Mundial de Dor para formular diretrizes específicas para procedimentos intervencionistas de dor. . Em contraste com as diretrizes de anestesia regional da ASRA, as diretrizes da multisociedade recomendavam que a aspirina fosse interrompida por 4 a 6 dias antes dos procedimentos intervencionistas da dor.
Dicas NYSORA
As orientações sobre procedimentos intervencionistas de dor em pacientes em uso de antiplaquetários e anticoagulantes são mais restritivas do que as de anestesia regional.
Inibidores de COX-2 e Inibidores de P2Y12
Os inibidores da ciclooxigenase-2 (COX-2) ganharam popularidade por causa de suas propriedades analgésicas e falta de efeitos plaquetários e gastrointestinais, e estudos mostraram sua propriedade analgésica em uma variedade de cenários perioperatórios.
Os medicamentos têm toxicidade gastrointestinal (GI) mínima e são ideais para pacientes que apresentam risco aumentado de eventos adversos graves no trato GI superior. Comparado com aspirina ou AINEs, o efeito dos inibidores da COX-2 na agregação plaquetária e nos tempos de sangramento não foi diferente do placebo. A perda de sangue não aumenta durante a cirurgia de fusão espinhal quando os inibidores de COX-2 são administrados no pré-operatório. As propriedades plaquetárias dessas drogas as tornam ideais para uso perioperatório quando a anestesia neuraxial é planejada. Infelizmente, rofecoxib e valdecoxib foram retirados do mercado por causa de seus efeitos colaterais cardiovasculares, deixando apenas o celecoxib disponível, mas em dosagens inferiores às recomendadas anteriormente.
As drogas tienopiridinas ticlopidina e clopidogrel não têm efeito direto sobre o metabolismo do ácido araquidônico. Esses medicamentos previnem a agregação plaquetária inibindo a ativação plaquetária mediada pelo receptor de adenosina difosfato (ADP). Eles também modulam o músculo liso vascular, reduzindo a contração vascular. A ticlopidina é raramente usada porque causa neutropenia, púrpura trombocitopênica e hipercolesterolemia.
O clopidogrel é preferido devido ao seu perfil de segurança aprimorado e eficácia comprovada. Notou-se ser melhor do que a aspirina em pacientes com doença vascular periférica. A inibição máxima da agregação plaquetária induzida por ADP com clopidogrel ocorre 3 a 5 dias após o início de uma dose padrão (75 mg), mas dentro de 4 a 6 horas após a administração de uma grande dose de ataque de 300 a 600 mg. Uma grande dose de carga é geralmente administrada aos pacientes antes de serem submetidos à intervenção coronária percutânea (ICP). Houve um relato de caso de hematoma espinhal em um paciente em uso de ticlopidina. Embora não tenha havido nenhum caso de hematoma intraespinal em um paciente em uso de clopidogrel isolado, um caso de tetraplegia em um paciente em uso de clopidogrel, diclofenaco e aspirina foi relatado.
Para as drogas tienopiridinas, recomenda-se que a ticlopidina seja descontinuada por 10 a 14 dias e o clopidogrel por 7 dias antes da injeção neuraxial. Houve relatos de casos sobre a segurança da raquianestesia 5 dias após a interrupção do clopidogrel. Um estudo mostrou que a maioria dos pacientes apresentou inibição plaquetária mínima 5 dias após a interrupção do clopidogrel. Se um procedimento neuroaxial precisar ser realizado 5 a 6 dias após a descontinuação do clopidogrel, um ensaio de P2Y12 ou outro teste apropriado deve ser realizado para garantir mínima ou nenhuma inibição da atividade plaquetária.
Dicas NYSORA
- As diretrizes da ASRA recomendam um intervalo de 7 dias entre a descontinuação do clopidogrel e um procedimento neuroaxial.
- Se for indicada uma raquianestesia ou epidural, recomenda-se um teste de função plaquetária para garantir que a inibição plaquetária residual desapareceu ou é insignificante.
Para um teste de estimulação da medula espinhal, uma descontinuação de 5 dias pode ser observada, pois o paciente estará sem clopidogrel durante o teste. Um teste de função plaquetária (por exemplo, o teste VerifyNow P2Y12 ou a porção de mapeamento de plaquetas do Thrombelastograph [TEG]) deve ser realizado para garantir a atividade plaquetária adequada.
Medicamentos antiplaquetários mais recentes
O clopidogrel é o fármaco antiplaquetário comumente usado na terapia antiplaquetária dupla, em que a aspirina é combinada com um inibidor do receptor P2Y12, em pacientes com síndromes coronarianas agudas. O prasugrel é um pró-fármaco semelhante ao clopidogrel, mas com características salutares em relação ao clopidogrel, e o ticagrelor é um inibidor do receptor P2Y12 de ação direta. O tempo médio para o efeito máximo é de 1 hora com prasugrel e 4 horas com clopidogrel. O tempo médio para atingir o pico de concentração plasmática com prasugrel é de 30 minutos e sua meia-vida média é de 3.7 horas. Esses valores não refletem a duração da inibição plaquetária porque a inibição do receptor P2Y12 é irreversível. Leva 7 dias para a atividade plaquetária normalizar após a interrupção do prasugrel.
Prasugrel e ticagrelor causam 90% de inibição da função plaquetária em comparação com 60%–70% do clopidogrel. Pacientes com baixo índice de massa corporal (IMC), aqueles com mais de 75 anos de idade e aqueles com histórico de acidente vascular cerebral estão em risco de sangramento. Ao contrário do clopidogrel, o prasugrel é convertido de forma confiável em seu metabólito ativo e não possui interações medicamentosas. Além disso, não é suscetível a polimorfismos genéticos.
Ticagrelor liga-se reversivelmente ao receptor P2Y12, bloqueando a ativação do receptor mediado por ADP. Em contraste com as tienopiridinas, o metabólito ativo e o fármaco original exibem atividade antiplaquetária com o fármaco original responsável pela maior parte da inibição plaquetária in vivo. O efeito antiplaquetário do ticagrelor é rápido; o pico de inibição plaquetária ocorre 2 a 4 horas após a ingestão em comparação com 24 horas com clopidogrel. A inibição plaquetária média pelo ticagrelor é de 93% em comparação com 58% do clopidogrel. A recuperação plaquetária é rápida com ticagrelor; a atividade plaquetária é normal 5 dias após a última dose.
Tempo entre a descontinuação/retomada de um medicamento antiplaquetário e injeção neuroaxial
O intervalo entre a descontinuação de um medicamento antiplaquetário e a injeção neuraxial é baseado no percentual de inibição plaquetária e no percentual de renovação plaquetária. Prasugrel e ticagrelor causam 90% de inibição. Dez a 15 por cento do pool de plaquetas circulantes é formado todos os dias, resultando em novas plaquetas compreendendo 50-75% do pool de plaquetas circulantes 5-7 dias após a descontinuação da droga. Um intervalo de 5 a 7 dias tem sido recomendado para o ticagrelor e um intervalo de 7 a 10 dias para o prasugrel. Essas recomendações são apropriadas, pois a agregação plaquetária normaliza 7 dias após a interrupção do prasugrel e 5 dias após o ticagrelor.
As diretrizes escandinavas observam que é aceitável reiniciar as drogas antiplaquetárias no momento da remoção do cateter, enquanto as diretrizes da Sociedade Europeia de Anestesiologia recomendam um intervalo de 6 horas entre a remoção do cateter peridural e a retomada do prasugrel ou ticagrelor. Outras revisões recomendaram cautela ao reiniciar prasugrel e ticagrelor devido ao seu efeito rápido e potente inibição antiplaquetária. Um intervalo de 24 horas pode ser mais apropriado para esses agentes.
Dicas NYSORA
- Prasugrel e ticagrelor devem ser interrompidos 7 e 5 dias, respectivamente, antes de uma raquianestesia ou epidural.
- Os medicamentos antiplaquetários podem ser reiniciados 6 a 24 horas após um procedimento neuroaxial ou remoção do cateter.
Função de monitoramento das plaquetas
O tempo de sangramento de Ivy foi considerado um preditor confiável de sangramento anormal em pacientes que receberam drogas antiplaquetárias. No entanto, o tempo de sangramento pós-aspirina não é um indicador confiável da função plaquetária. Há grande variabilidade intra e interpaciente nos resultados do teste, e não há evidências que sugiram que o tempo de sangramento possa predizer a função hemostática, uma vez que os estudos falharam em mostrar uma correlação entre o prolongamento do tempo de sangramento induzido pela aspirina e a perda de sangue cirúrgica .
Ensaios especiais de função plaquetária estão agora disponíveis para monitorar a agregação e degranulação plaquetária. O analisador de função plaquetária (PFA) é um teste de função plaquetária in vitro. É um bom teste de triagem para a doença de von Willebrand e monitora o efeito da administração de desmopressina. O PFA é prolongado após terapia antiplaquetária. Infelizmente, o PFA-100 não é um teste sensível para monitorar a função antiplaquetária dos inibidores de P2Y12 clopidogrel, prasugrel e ticagrelor. No entanto, o PFA-200, uma atualização recente do PFA-100, parece ser sensível aos efeitos dos inibidores de P2Y12. No entanto, ainda faltam estudos no local de atendimento sobre esse novo teste de PFA.
Testes mais recentes que monitoram a atividade do receptor P2Y12 incluem o ensaio de fosfoproteína estimulada por vasodilatador (VASP), o ensaio VerifyNow, o teste de agregometria de múltiplas plaquetas (Multiplate) e o componente de mapeamento de plaquetas do Tromboelastógrafo (TEG). O teste VerifyNow pode monitorar os efeitos antiplaquetários da aspirina e dos inibidores de P2Y12. O componente de mapeamento de plaquetas do TEG é comumente usado em cirurgia e anestesiologia, enquanto o VerifyNow é o ensaio predominante em cardiologia clínica. Uma revisão sobre o monitoramento da função plaquetária foi discutida por várias revisões e está além do escopo deste capítulo.
ANTICOAGULANTES ORAIS
A varfarina exerce seu efeito anticoagulante ao interferir na síntese dos fatores de coagulação dependentes da vitamina K (VII, IX, X e trombina).Figura 3). Também inibe as proteínas anticoagulantes C e S. O fator VII tem uma meia-vida relativamente curta (6-8 h), e o tempo de protrombina (TP) pode ser prolongado dentro da faixa terapêutica (1.5-2 vezes o normal) dentro de 24-36 horas. A proteína C anticoagulante também tem uma meia-vida curta (6-7 h). O prolongamento inicial da razão normalizada internacional (INR) é o resultado de efeitos concorrentes da redução do fator VII e da proteína C e a eliminação dos fatores de coagulação existentes. Por isso, o INR é imprevisível durante a fase inicial do tratamento com varfarina. O fator VII participa apenas da via extrínseca, e a anticoagulação adequada não é alcançada até que os níveis dos fatores biologicamente ativos II (meia-vida de 50 h) e X estejam suficientemente deprimidos. Isso requer 4-5 dias. Altas doses de ataque de varfarina (15 mg) são ocasionalmente empregadas nos primeiros 2 a 3 dias de terapia, e o efeito anticoagulante desejado é alcançado em 48 a 72 horas. O efeito anticoagulante da varfarina persiste por 4 a 6 dias após o término da terapia, enquanto novos fatores biologicamente ativos da vitamina K são sintetizados. As desvantagens da terapia com varfarina incluem a necessidade de monitorar seu efeito com monitoração seriada do INR, sua interação com outras drogas e a necessidade de sua descontinuação alguns dias antes da cirurgia. O efeito da varfarina pode ser revertido pela transfusão de plasma fresco congelado e injeções de vitamina K. O concentrado de complexo de protrombina de 3 ou 4 fatores (PCC) pode ser usado para antagonizar a varfarina em situações de emergência.
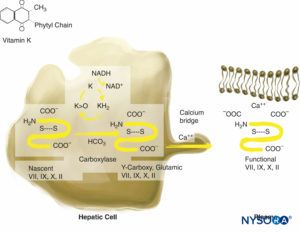
FIGURA 3. Síntese do fator de coagulação dependente da vitamina K. A vitamina K é necessária para a modificação pós-traducional da protrombina; proteínas C e S; e fatores VII, IX e X. A vitamina K é armazenada nos hepatócitos.
Existem poucos dados sobre o risco de hematoma espinhal em pacientes com cateteres raquidianos ou peridurais que são posteriormente anticoagulados com varfarina. Odoom e Sih realizaram 1000 anestesias peridural lombar contínua em 950 pacientes submetidos a procedimentos vasculares e receberam anticoagulantes orais no pré-operatório. O tromboteste (um teste da atividade do fator IX) foi diminuído e o tempo de tromboplastina parcial ativada (aPTT) foi prolongado em todos os pacientes antes da colocação epidural. A heparina também foi administrada no intraoperatório. Os cateteres peridurais permaneceram no local por 48 horas no pós-operatório e não houve complicações neurológicas. Infelizmente, o estado de coagulação dos pacientes no momento da retirada do cateter não foi descrito. Embora os resultados deste estudo sejam tranquilizadores, a natureza antiquada do tromboteste como medida de anticoagulação combinada com o estado de coagulação desconhecido dos pacientes no momento da retirada do cateter limita a utilidade do estudo.
O uso de um cateter peridural ou intratecal e o momento de sua remoção em um paciente anticoagulado são controversos. Embora o trauma da colocação da agulha ocorra com as técnicas de cateter de dose única e contínua, a presença de um cateter permanente pode resultar em lesão adicional aos tecidos e estruturas vasculares.
Como os hematomas intraespinhais ocorreram após a remoção do cateter, recomenda-se que os mesmos valores laboratoriais se apliquem à colocação e remoção do cateter epidural. Nenhum hematoma espinhal foi relatado em 192 pacientes que receberam analgesia epidural pós-operatória em conjunto com varfarina em baixa dose após artroplastia total do joelho.
Neste estudo, os pacientes receberam varfarina para prolongar o TP para 15.0–17.3 segundos. Os cateteres peridurais foram deixados por 37 ± 15 horas (intervalo de 13 a 96 h). O PT médio no momento da remoção do cateter peridural foi de 13.4 ± 2 segundos (variação de 10.6 a 25.8 s). Este e vários estudos subsequentes documentaram a relativa segurança da anticoagulação com varfarina em baixas doses em pacientes com cateter peridural permanente. Outro estudo mostrou que níveis mais elevados de INR (até 1.9) são aceitáveis para a remoção de cateteres peridurais desde que seja feita dentro de 12 a 14 horas após a ingestão de varfarina. Um estudo mostrou a ausência de hematoma espinhal quando os cateteres peridurais foram removidos 2-3 dias após a ingestão de varfarina, mesmo com INRs acentuadamente elevados. A prática de retirar o cateter peridural 3 dias após o início da varfarina, quando os níveis de fatores de coagulação VII, IX e X estão baixos (os níveis de fator II ainda podem ser aceitáveis) precisa ser estudado. Este é especialmente o caso, uma vez que os pacientes variam muito em sua resposta à varfarina, levando alguns autores a recomendar o monitoramento rigoroso do estado de coagulação para evitar o prolongamento excessivo do PT. Os fatores responsáveis por um PT e PTT prolongados são ilustrados em Figuras 4 e 5.
A ASRA recomendou um valor de INR de 1.4 ou menos como aceitável para a realização de bloqueios de nervos neuroaxiais. Esse valor é baseado em estudos que mostraram excelente hemostasia perioperatória quando o valor de INR foi ≤1.5. Estudos sobre os níveis de fatores de coagulação em diferentes valores de INR mostraram que o declínio desses fatores pode não ser significativo em um INR de 1.5. Em valores de INR de 1.5–2.0, as concentrações do fator II foram observadas em 74%–82% da linha de base, enquanto os níveis do fator VII foram de 27%–54% dos valores da linha de base.
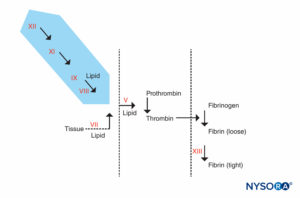
FIGURA 4. Reação de coagulação. Os fatores responsáveis por um PTT prolongado estão na área sombreada. Os pacientes que apresentam PTT anormal, mas cujo PT e outros exames são normais, podem ser divididos em 2 grupos: aqueles que são propensos a sangramento e aqueles que não são. Os pacientes que não sangram podem ter um PTT extremamente prolongado (90 segundos ou mais), mas não têm histórico de sangramento. Eles terão uma deficiência no fator XII, pré-calicreína ou cininogênio de alto peso molecular. A esses pacientes não se deve negar cirurgia ou anestesia peridural. O outro grupo, pacientes que sangram, têm PTT prolongado e história de sangramento. Eles terão uma deficiência de fator VIII (hemofilia A), fator IX (hemofilia B ou doença de Christmas) ou fator XI.
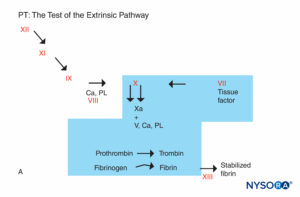
FIGURA 5A. Reação de coagulação. Os fatores envolvidos no PT estão na área sombreada. O TP é realizado pela adição de uma fonte de fator tecidual ao plasma do paciente juntamente com cálcio ou fosfolipídio. O fator tecidual forma um complexo com e ativa o fator VII. (Ca, cálcio; PL, fosfolipídio.)
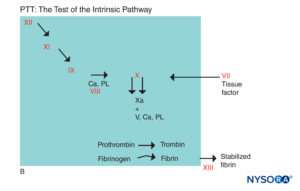
FIGURA 5B. Reação de coagulação. Os fatores envolvidos no PTT estão na área sombreada. Na avaliação do PTT, a coagulação é iniciada por um agente que ativa o complexo fator de Hageman-cininogênio-precalicreína. A maioria dos fatores de coagulação é rastreada por PTT, exceto os fatores VII e XIII, a proteína que estabiliza os coágulos de fibrina por meio de sua ligação cruzada, e componentes do sistema fibrinolítico. (Ca, cálcio; PL, fosfolipídio.)
Em valores de INR de 2.1 ± 1 durante a fase inicial de administração de varfarina, os fatores II e VII foram 65 ± 28% e 25 ± 20% dos valores de controle. Atividades de 40% são consideradas adequadas para a hemostasia normal no momento da cirurgia de grande porte. Outro estudo descobriu que em INRs de 1.3-2, sob anticoagulação estável com varfarina, as concentrações dos fatores de coagulação VII, IX e X estavam dentro dos limites normais.
O clínico deve estar ciente do efeito da varfarina na cascata de coagulação e do papel do INR na monitorização deste efeito. Para minimizar o risco de complicações, a ASRA recomenda várias precauções. A terapia oral crônica com varfarina deve ser interrompida e o INR medido antes que um bloqueio do nervo neuroaxial seja realizado. O uso concomitante de outros medicamentos, como aspirina, AINEs e heparinas, que afetam o mecanismo de coagulação, aumenta o risco de complicações hemorrágicas sem afetar o INR. Se uma dose inicial de varfarina for administrada antes da cirurgia, o INR deve ser verificado se a dose foi administrada mais de 24 horas antes. Se os pacientes estiverem em tratamento com baixa dose de varfarina (dose média diária de aproximadamente 5 mg) durante a analgesia epidural, o INR deve ser verificado diariamente e antes da remoção do cateter se a dose inicial tiver sido administrada há mais de 36 horas. Doses diárias mais altas podem precisar de monitoramento mais intensivo. A dose de varfarina deve ser mantida ou reduzida quando o INR for >3 em pacientes com cateteres neuroaxiais permanentes para prevenir hematoma e hemartroma epidural. Durante a terapia com varfarina, o estado neurológico do paciente deve ser verificado rotineiramente durante a infusão analgésica epidural, bem como 24 horas após a remoção do cateter. Concentrações diluídas de anestésico local devem ser utilizadas para minimizar o grau de bloqueio sensorial e motor. O julgamento clínico deve ser exercido na tomada de decisões sobre a remoção ou manutenção de cateteres neuroaxiais em pacientes com níveis terapêuticos de anticoagulação durante a infusão de cateter neuroaxial. A dose de varfarina deve ser reduzida para pacientes que provavelmente terão uma resposta aumentada ao medicamento, especialmente os idosos. Para pacientes em anticoagulação oral crônica, a varfarina deve ser interrompida e o INR medido.
Dicas NYSORA
- Um INR de 1.4, na ausência de hematomas fáceis e função hepática normal, é aceitável antes da injeção neuroaxial em pacientes planejados para bloqueios nervosos neuroaxiais.
- O INR deve ser verificado se o paciente tomou varfarina mais de 24 horas antes.
- O INR deve ser normal 5 dias após a interrupção da varfarina antes de um procedimento neuroaxial
HEPARINA
Heparina intravenosa
A heparina é um polissacarídeo complexo que exerce seu efeito anticoagulante ligando-se à antitrombina. A mudança conformacional da antitrombina acelera sua capacidade de inativar os fatores de trombina Xa e IXa.
A heparina não fracionada libera o inibidor da via do fator tecidual do endotélio, aumentando sua atividade contra o fator Xa. O efeito anticoagulante da heparina subcutânea leva de 1 a 2 horas, mas o efeito da heparina intravenosa é imediato. De fato, o tempo de coagulação é prolongado 2 a 4 vezes o nível basal 5 minutos após a injeção intravenosa de 10,000 unidades de heparina. A heparina tem uma meia-vida de 1.5 a 2 horas. A dose terapêutica de heparina cessa 4-6 horas após a sua administração. O TTPa é usado para monitorar o efeito da heparina; a anticoagulação terapêutica é alcançada com um prolongamento do TTPa superior a 1.5 vezes o valor basal ou um nível de heparina de 0.2–0.4 U/mL. O TTPa geralmente não é prolongado pela administração subcutânea de baixas doses de heparina e não é monitorado. A protamina neutraliza o efeito da heparina administrada por via intravenosa.
A heparina não é o anticoagulante ideal, pois é uma mistura de moléculas, das quais apenas uma fração tem atividade anticoagulante. Liga-se ao fator plaquetário 4 e ao fator von Willebrand. O complexo heparina-antitrombina também não é muito eficaz na neutralização da trombina ligada ao coágulo. Finalmente, a heparina está associada à trombocitopenia imunológica e à trombose imunomediada. Para pacientes que recebem terapia padrão com heparina, o risco de complicações hemorrágicas aumenta na presença de outros medicamentos que afetam outros mecanismos de coagulação, incluindo aspirina, AINEs, HBPMs e anticoagulantes orais. Vários estudos demonstraram a segurança da raquianestesia ou peridural seguida de heparinização sistêmica, desde que observadas certas precauções. Rao e El-Etr não relataram hematomas espinhais em mais de 4000 pacientes submetidos à cirurgia vascular de membros inferiores sob raquianestesia contínua ou peridural. Em seu estudo, os pacientes com distúrbios de coagulação preexistentes foram excluídos, a heparinização ocorreu pelo menos 60 minutos após a colocação do cateter, o nível de anticoagulação foi cuidadosamente monitorado e os cateteres de demora foram removidos em um momento em que a atividade da heparina era baixa. A cirurgia foi cancelada em pacientes quando foi observado sangue franco na agulha e realizada no dia seguinte sob anestesia geral. Os mesmos achados foram observados em um relatório subsequente na literatura neurológica. Ruff e Dougherty observaram hematomas espinhais em 7 de 342 (2%) pacientes submetidos à punção lombar e posterior heparinização para avaliação de isquemia cerebral.
A presença de sangue durante o procedimento, terapia concomitante com aspirina e heparinização em 1 hora foram identificados como fatores de risco para o desenvolvimento de hematoma espinhal. A ASRA fez várias recomendações para quando uma técnica neuroaxial é usada na presença de anticoagulação intraoperatória. A ASRA aconselha que a técnica deve ser evitada em pacientes com outras coagulopatias. Deve haver um atraso de pelo menos 1 hora entre a colocação da agulha e a administração da heparina. O cateter deve ser removido 2 a 4 horas após a última dose de heparina e 1 hora antes da administração subsequente de heparina. O TTPa ou tempo de coagulação ativado (ACT) deve ser monitorado para evitar o efeito excessivo da heparina. O paciente deve ser acompanhado no pós-operatório para detecção precoce de recorrência do bloqueio motor. Concentrações diluídas de anestésicos locais são recomendadas para minimizar o bloqueio motor.
Embora possa haver um risco aumentado no caso de uma colocação de agulha traumática (sangrenta) ou difícil, não há dados para apoiar o cancelamento obrigatório da cirurgia. A decisão de prosseguir deve ser baseada no julgamento clínico apropriado e na discussão completa com o cirurgião e o paciente.
Dicas NYSORA
- Deve haver um atraso de pelo menos 1 hora entre um procedimento neuroaxial e a readministração de heparina.
- O cateter pode ser removido 2 a 4 horas após a última dose de heparina.
Procedimentos neuroaxiais são ocasionalmente realizados em pacientes submetidos à circulação extracorpórea. As seguintes precauções foram recomendadas para prevenir o desenvolvimento de hematoma intraespinal nesses pacientes:
- Procedimentos neuroaxiais devem ser evitados em pacientes com coagulopatia conhecida.
- A cirurgia deve ser adiada 24 horas em pacientes com punção traumática.
- O tempo do procedimento neuroaxial até a heparinização sistêmica deve ultrapassar 1 hora.
- A heparinização e a reversão devem ser monitoradas e controladas rigorosamente.
- O cateter epidural deve ser removido quando a coagulação normal for restaurada e o paciente deve ser monitorado de perto quanto a sinais de hematoma espinhal.
Heparina Subcutânea
A base terapêutica da heparina subcutânea em dose baixa duas vezes ao dia (5000 unidades a cada 8–12 horas) é a inibição do fator X ativado mediada pela heparina. Doses menores de heparina são necessárias quando administradas como profilaxia e não como tratamento para doença tromboembólica. Após a injeção intramuscular ou subcutânea de 5000 unidades de heparina, o efeito anticoagulante máximo é observado em 40 a 50 minutos e retorna à linha de base em 4 a 6 horas. O TTPa pode permanecer na faixa normal e muitas vezes não é monitorado. No entanto, foram relatadas grandes variações nas respostas individuais dos pacientes à heparina subcutânea. As técnicas neuroaxiais não são contraindicadas durante a profilaxia subcutânea (minidose), mas o risco de sangramento pode ser reduzido atrasando a administração de heparina até após o bloqueio do nervo. O sangramento pode aumentar em pacientes debilitados ou após terapia prolongada. A segurança da anestesia neuroaxial maior na presença de anticoagulação com doses subcutâneas duas vezes ao dia de heparina não fracionada foi documentada por vários estudos. O regime de heparina subcutânea duas vezes ao dia foi substituído por um regime de três vezes ao dia na maioria dos hospitais para diminuir a incidência de tromboembolismo venoso pós-operatório. No entanto, essa prática tem sido associada a hematomas espontâneos. Por esse motivo, as diretrizes mais recentes da ASRA recomendam contra procedimentos neuraxiais em pacientes em regime de três vezes ao dia até que mais dados estejam disponíveis.
Dicas NYSORA
- Procedimentos neuroaxiais podem ser realizados em pacientes com heparina subcutânea duas vezes ao dia.
- Devido à falta de dados adequados, a ASRA recomenda que procedimentos neuraxiais não sejam realizados em pacientes em uso de heparina subcutânea três vezes ao dia.
Heparina de baixo peso molecular
A heparina não fracionada é uma mistura heterogênea de cadeias de polissacarídeos que podem ser separadas em fragmentos de vários pesos moleculares. O efeito anticoagulante da HBPM é semelhante ao da heparina não fracionada; ativa a antitrombina, acelerando a interação da antitrombina com a trombina e o fator Xa. A HBPM tem maior atividade contra o fator Xa, enquanto a heparina não fracionada tem atividade equivalente contra a trombina e o fator Xa. A meia-vida plasmática das LMWHs varia de 2 a 4 horas após uma injeção intravenosa e 3 a 6 horas após uma injeção subcutânea; a meia-vida de uma HBPM é de 2 a 4 vezes a da heparina padrão. Possui baixa afinidade para a proteína plasmática, resultando em maior biodisponibilidade. As vantagens da LMWH sobre a heparina não fracionada incluem uma biodisponibilidade maior e mais previsível após a administração subcutânea e uma meia-vida biológica mais longa. Além disso, o monitoramento laboratorial da resposta anticoagulante da HBPM não é necessário, e o ajuste da dose para o peso não é necessário (embora uma superdosagem possa ocorrer em pacientes com IMC baixo). A LMWH exibe um efeito antitrombótico dose-dependente que é avaliado com precisão pela medição do nível de atividade anti-Xa. A recuperação da atividade antifator Xa após injeção subcutânea de HBPM aproxima-se de 100%, tornando desnecessária a monitorização laboratorial, exceto em pacientes com insuficiência renal ou com peso corporal inferior a 50 kg ou superior a 80 kg. O tempo de reação do tromboelastograma parece correlacionar-se com a concentração sérica de anti-Xa.
As três LMWHs comercialmente disponíveis nos Estados Unidos são enoxaparina (Lovenox), dalteparina (Fragmin) e tinzaparina (Innohep), embora esta última tenha sido descontinuada devido ao baixo uso. A enoxaparina é administrada uma vez ao dia ou a cada 12 horas quando usada como profilaxia, e a dalteparina e a tinzaparina são administradas uma vez ao dia. As três drogas parecem ter eficácia comparável no tratamento e prevenção do tromboembolismo venoso. A enoxaparina e a dalteparina têm eficácia comparável na prevenção de morte ou infarto do miocárdio em pacientes com angina instável.
A dose tromboprofilática recomendada nos Estados Unidos é de 30 mg de enoxaparina duas vezes ao dia, embora alguns médicos aumentem a dose em pacientes obesos (1.5 mg/kg diariamente ou 1 mg/kg a cada 12 horas). O esquema posológico europeu é de 20 a 40 mg de enoxaparina uma vez ao dia, e os pacientes recebem sua dose inicial 12 horas antes da cirurgia, uma prática não observada nos Estados Unidos.
Numerosos casos de hematoma neuroaxial ocorreram nos Estados Unidos, levando a FDA a emitir um aviso de saúde em dezembro de 1997 e a convocação da primeira conferência de consenso da ASRA sobre anticoagulação e anestesia neuroaxial. As diretrizes da ASRA recomendam que a menor dose efetiva de HBPM seja administrada. A administração pós-operatória da terapia com HBPM deve ser adiada o máximo possível, por um mínimo de 12 horas e idealmente 24 horas após a cirurgia. Um anestésico espinhal de dose única pode ser a técnica neuroaxial mais segura em pacientes que recebem HBPM pré-operatória. Aguardar pelo menos 12 horas após a dose profilática de HBPM é recomendado antes de realizar uma técnica neuroaxial. Pacientes que recebem doses mais altas de HBPM (por exemplo, enoxaparina 1 mg/kg duas vezes ao dia) requerem atrasos mais longos (24 h). O cateter deve ser removido quando a atividade de anticoagulação for baixa, pelo menos 12 horas após a administração profilática de HBPM e 4 horas antes da próxima dose. Extrema vigilância do estado neurológico do paciente deve ser observada se a tromboprofilaxia HBPM for implementada durante a infusão de um cateter de demora. Solução anestésica local diluída é recomendada para que a função neurológica possa ser melhor monitorada. O uso de outros medicamentos que afetam a hemostasia, como antiplaquetários, heparina padrão, dextrana ou anticoagulantes orais, em combinação com HBPM cria um risco adicional de complicações hemorrágicas.
Dicas NYSORA
- Em pacientes em dose profilática de HBPM, é recomendado um intervalo de 12 horas antes de uma injeção no neuroeixo.
- Para pacientes em uma dose terapêutica de HBPM, um intervalo de 24 horas é apropriado.
- Um atraso de 4 horas após a remoção do cateter peridural antes que a HBPM seja retomada foi recomendado pelo FDA.
TERAPIA TROMBOLÍTICA
Os agentes trombolíticos dissolvem ativamente os coágulos de fibrina já formados. Ativadores exógenos do plasminogênio, como a estreptoquinase e a uroquinase, não apenas dissolvem o trombo, mas também afetam o plasminogênio circulante, levando à diminuição dos níveis de plasminogênio e fibrina. O ativador de plasminogênio tipo tecido recombinante (r-TPA), um agente endógeno, é mais seletivo para a fibrina e tem menos efeito sobre os níveis de plasminogênio circulante. A lise do coágulo leva a uma elevação dos produtos de degradação da fibrina, que têm um efeito anticoagulante ao inibir a agregação plaquetária.
Embora a colocação de agulha e cateter peridural ou espinhal com heparinização subsequente pareça relativamente segura, o risco de hematoma espinhal em pacientes que recebem terapia trombolítica não está bem definido. Casos de hematoma espinhal em pacientes que tiveram cateter peridural ou peridural de demora e que receberam agentes trombolíticos foram relatados na literatura.
As diretrizes da ASRA fazem recomendações com relação a procedimentos neuraxiais após terapia trombolítica ou fibrinolítica. O uso concomitante de heparina com drogas fibrinolíticas ou trombolíticas coloca os pacientes em alto risco de sangramento adverso no neuroeixo durante anestesia raquidiana ou peridural. Exceto em circunstâncias altamente incomuns, os pacientes que recebem terapia fibrinolítica ou trombolítica devem ser advertidos contra a raquianestesia ou anestesia epidural. Não há dados disponíveis para determinar claramente o período de tempo apropriado após a descontinuação desses medicamentos e o desempenho seguro de uma técnica neuraxial. As diretrizes europeias recomendam deixar o cateter peridural no lugar quando o paciente recebe um medicamento trombolítico, removendo-o apenas quando o efeito do medicamento desaparece. As diretrizes escandinavas recomendam um intervalo de 24 horas entre a descontinuação da droga e o procedimento neuroaxial. O monitoramento neurológico frequente é recomendado por um período de tempo apropriado em pacientes que tiveram bloqueios do nervo neuroaxial após terapia fibrinolítica ou trombolítica. Se um paciente recebe infusão peridural contínua e recebeu terapia fibrinolítica ou trombolítica, devem ser usados medicamentos que minimizem o bloqueio sensorial e motor. Não houve recomendação definitiva sobre o momento da remoção de cateteres neuroaxiais em pacientes que recebem inesperadamente terapia fibrinolítica ou trombolítica. A medição dos níveis de fibrinogênio pode ser útil para orientar uma decisão sobre a remoção ou manutenção do cateter.
Terapia à base de plantas
Os medicamentos fitoterápicos mais comumente usados são alho, ginkgo e ginseng. O alho inibe a agregação plaquetária e seu efeito na hemostasia parece durar 7 dias. Ginkgo inibe o fator ativador de plaquetas e seu efeito dura 36 horas. O ginseng tem uma variedade de efeitos: inibe a agregação plaquetária in vitro e prolonga o tempo de trombina (TT) e o TTPa em animais de laboratório; seu efeito dura 24 horas. Apesar de seu efeito sobre a função plaquetária, os medicamentos fitoterápicos por si só parecem não apresentar risco significativo adicional no desenvolvimento de hematoma espinhal em pacientes submetidos à anestesia peridural ou espinhal. A descontinuação obrigatória desses medicamentos, ou o cancelamento da cirurgia em pacientes nos quais esses medicamentos foram continuados, não é suportado pelos dados clínicos disponíveis. No entanto, o uso concomitante de outros medicamentos que afetam os mecanismos de coagulação, como anticoagulantes orais ou heparina, pode aumentar o risco de complicações hemorrágicas nesses pacientes. Não há teste aceito para avaliar a adequação da hemostasia no paciente que tomou medicamentos fitoterápicos. Neste momento, parece não haver preocupações específicas quanto ao momento do bloqueio do nervo neuroaxial em relação à dosagem da fitoterapia, monitoramento pós-operatório ou o momento da remoção do cateter neuroaxial.
Inibidores de Trombina
Derivados de hirudina recombinantes, incluindo desirudina e bivalirudina, inibem a trombina livre e ligada ao coágulo. O argatroban, um derivado da l-arginina, tem um mecanismo de ação semelhante. Esses medicamentos são usados principalmente no tratamento da trombocitopenia induzida pela heparina. Não há reversão farmacológica para o efeito dessas drogas. Não houve relatos de casos de hematoma espinhal relacionado à anestesia neuraxial em pacientes que receberam um inibidor de trombina. No entanto, sangramento intracraniano espontâneo foi relatado. De acordo com as diretrizes da ASRA, nenhuma declaração sobre avaliação de risco e gerenciamento de pacientes pode ser feita.
fondaparinux
O fondaparinux é um anticoagulante sintético que produz seu efeito antitrombótico através da inibição seletiva do fator Xa. A droga apresenta consistência em seu efeito anticoagulante, uma vez que é sintetizada quimicamente. É 100% biodisponível. Rapidamente absorvido, atinge a concentração máxima dentro de 1.7 horas após a administração. Sua meia-vida é de 17 a 21 horas.
O fondaparinux é recomendado como agente antitrombótico após cirurgia ortopédica de grande porte e como tratamento inicial para embolia pulmonar. A meia-vida estendida (aproximadamente 20 horas) permite a dosagem uma vez ao dia. O FDA emitiu um aviso de caixa preta para fondaparinux semelhante ao de LMWHs e heparina.
O risco real de hematoma espinhal com fondaparinux é desconhecido. Um estudo não mostrou complicações em pacientes que receberam injeções neuroaxiais. Neste estudo, os cateteres foram retirados 36 horas após a última dose de fondaparinux e a dosagem foi adiada por 12 horas após a retirada do cateter. Os pacientes foram excluídos do estudo se houvesse dificuldades na realização do procedimento neuroaxial (necessidade de mais de 3 tentativas), o procedimento fosse complicado por sangramento, necessitassem de antiagregantes plaquetários ou o plano fosse retirar o cateter peridural no dia seguinte à cirurgia. Devido aos requisitos irreais na prática clínica, a ASRA não recomenda o uso de fondaparinux na presença de um cateter peridural de demora. Suas recomendações são baseadas no efeito antitrombótico sustentado e irreversível do fondaparinux, na dosagem pós-operatória precoce e no hematoma espinhal relatado durante os ensaios clínicos iniciais da droga. O monitoramento cuidadoso da literatura para fatores de risco associados ao sangramento cirúrgico pode ser útil na avaliação de risco e no tratamento do paciente. A execução de técnicas neuroaxiais deve ocorrer em condições usadas em ensaios clínicos (passagem única da agulha, colocação atraumática da agulha, evitar cateteres neuroaxiais permanentes). Se isso não for viável, um método alternativo de profilaxia deve ser considerado.
Sumário
O intervalo de tempo entre a descontinuação do anticoagulante e o procedimento neuroaxial e entre a retirada do cateter peridural e a retomada da droga estão resumidos em tabela 1.
TABELA 1. Intervalos de tempo recomendados antes ou após o procedimento neuroaxial e a remoção do cateter peridural.
| Droga | Tempo antes do neuroaxial Procedimento ou Remoção do Cateter | Tempo após neuroaxial Procedimento ou Remoção do Cateter | Comentários |
|---|---|---|---|
| Aspirina | nenhum | nenhum | |
| AINEs | nenhum | nenhum | |
| Clopidogrel | 7 dias * | Após a remoção do cateter | De acordo com as diretrizes europeias e escandinavas |
| Prasugrel | dias 7-10 | 6h | Por Diretrizes Europeias |
| Ticagrelor | 5 dias | 6h | (Como acima) |
| Varfarina | 5 dias (INR normal) | Após a remoção do cateter | |
| Heparina (IV) | 4-6 h | 1-2h | |
| Heparina | |||
| -(Sc, BID) | nenhum | nenhum | |
| -(Sc, TID) | Não aplicável | Procedimento neuroaxial | |
| HBPM | |||
| Profilático | 12 horas | 4 horas | Recomendação da FDA |
| Terapêutico | 24 horas | 4 horas | |
| fondaparinux | 36-42 horas | 6-12 horas | De acordo com as diretrizes europeias. ASRA recomendado contra procedimentos neuraxiais em pacientes com a droga. *Se o procedimento neuroaxial tiver que ser realizado em 5 dias, um teste de função plaquetária é recomendado (ver texto |
NOVOS ANTICOAGULANTES
Uma discussão sobre os novos anticoagulantes dabigatrana, rivaroxabana e apixabana envolve a revisão de algumas informações básicas.
O intervalo entre a descontinuação do anticoagulante e a injeção neuroaxial e entre o procedimento neuroaxial ou Remoção do Cateter Epidural e Retomada do Anticoagulante
Tem sido recomendado que duas meias-vidas sejam um compromisso adequado entre o risco de tromboembolismo venoso (TEV) e a prevenção de hematoma espinhal. As diretrizes europeias e escandinavas recomendaram um intervalo de 2 meias-vidas entre a descontinuação do anticoagulante e a injeção no neuroeixo.
Essa decisão foi tomada porque o TEV subclínico ocorre em uma boa porcentagem de pacientes imediatamente após a cirurgia e ter anticoagulação residual pode evitar essa ocorrência. A presença de anticoagulação residual facilita a transição para anticoagulação total após um procedimento neuroaxial. Após 1, 2, 3, 4, 5 e 6 meias-vidas, os seguintes percentuais de droga permanecem na circulação: 50%, 25%, 12.5%, 6.25%,
3.125% e 1.5625%, respectivamente (tabela 2). No entanto, esses achados são baseados em estudos em voluntários jovens e saudáveis em estudos farmacocinéticos de dose única na ausência de outros anticoagulantes. Por outro lado, na prática clínica, os pacientes geralmente são mais velhos e apresentam comorbidades concomitantes.
TABELA 2. Intervalos de tempo recomendados antes ou após procedimento neuroaxial e cateter peridural para os novos anticoagulantes.
| Droga | Meia-vida | Diretrizes Europeias | Diretrizes escandinavas | Cinco meias-vidas |
|---|---|---|---|---|
| Dabigatran | 12-17h 28 horas (doença renal) | (Contra-indicado pelo fabricante) | Dados não disponíveis | 85h (4d) 6d (pacientes renais) |
| Rivaroxaban | 9-13h | 22-26h | 18 horas | 65h (3d) |
| Apixaban | 15.2 +/-8.5h | 26-30h | Dados não disponíveis | 75h (3-4d) |
Em pacientes com risco de TEV, como aqueles com história prévia de acidente vascular cerebral, um intervalo de 2 ou 3 meias-vidas pode ser apropriado, reconhecendo que a hemostasia adequada não está garantida. Para pacientes sem fatores de risco trombóticos, um intervalo de 4 a 6 meias-vidas entre a última dose do anticoagulante e a injeção no neuroeixo garante uma eliminação mais completa do fármaco e menor risco de sangramento. Um compromisso entre as recomendações conservadoras de 4-6 meias-vidas e 2-3 meias-vidas é um intervalo de 5 meias-vidas com terapia de ponte de HBPM.
Em relação à retomada do anticoagulante após injeção neuroaxial ou retirada do cateter peridural, as diretrizes escandinavas são baseadas na recomendação de Rosencher et al. de 8 horas menos o tempo que leva para o anticoagulante atingir o efeito máximo.
Presume-se que oito horas sejam suficientes para a estabilização do coágulo, uma presunção apoiada pela eficácia dos agentes trombolíticos para lisar um coágulo se administrados dentro de 6 horas após a formação do coágulo. Tertri e colegas também observaram que dar enoxaparina dentro de 24 a 48 horas após a hemorragia intracerebral não aumentou o tamanho do hematoma, portanto, um intervalo de 24 horas é provavelmente mais seguro. Outros autores recomendam uma abordagem mais conservadora, pois a reinstituição da terapia antitrombótica em até 24 horas após um procedimento de grande porte pode aumentar o risco de sangramento periprocedimento. Liew e Douketis recomendam um mínimo de 24 horas em pacientes com baixo risco de sangramento e 48 horas naqueles com alto risco de sangramento antes de retomar dabigatrana, rivaroxabana ou apixabana. As opções, portanto, são 8 horas ou 24 horas menos o efeito de pico da droga.
Provavelmente, há pouca diferença entre essas duas opções, pois os riscos de TEV, acidente vascular cerebral ou síndrome coronariana aguda são provavelmente os mesmos. Além disso, o início e os tempos para o efeito máximo dos novos anticoagulantes são curtos.
Dabigatran
O etexilato de dabigatrana é um pró-fármaco que é hidrolisado por esterases no estômago para o fármaco ativo. O etexilato de dabigatrana tem uma biodisponibilidade de 7.2%. A dabigatrana é um inibidor direto da trombina que bloqueia a interação da trombina com vários substratos. As concentrações plasmáticas máximas são atingidas 1.5 a 3 horas após a ingestão do pró-fármaco. Tem meia-vida de 14 a 17 horas. A depuração renal é responsável por 80% da depuração total da dabigatrana. Nos casos de doença renal terminal, a meia-vida de eliminação dobra de 14 horas para 28 horas.
A dabigatrana é eficaz no tratamento de TEV agudo e na prevenção de TEV recorrente. Em pacientes com fibrilação atrial, a dabigatrana reduz as taxas de acidente vascular cerebral e embolia sistêmica em um grau semelhante ao da varfarina. A dabigatrana não demonstrou ser consistente na prevenção de TEV após cirurgia articular total. Estudos mostraram que ela é mais eficaz, não inferior ou inferior à enoxaparina. Uma meta-análise dos ensaios não observou diferenças entre dabigatrana e enoxaparina em nenhum dos desfechos analisados. O fabricante afirma que cateteres peridurais não devem ser colocados em pacientes recebendo dabigatrana. Um intervalo mínimo de 2 horas entre a remoção do cateter de demora e a administração da dabigatrana foi recomendado por Levy e colegas. Esse intervalo parece ser menor que 6 horas, ou seja, a diferença entre 8 horas menos o tempo de 2 horas para atingir o pico do efeito da droga. Houve relatos de sangramento aumentado após tomar dabigatrana. A Hematology Society of Australia and New Zealand identificou 78 episódios de sangramento em aproximadamente 7000 pacientes em um período de 2 meses. Uma auditoria do FDA, no entanto, concluiu que não houve aumento absoluto de sangramento com dabigatrana em relação à varfarina.
O TTPa é prolongado após a dabigatrana, mas a relação é curvilínea. O tempo de trombina (TT), também conhecido como tempo de coagulação da trombina (TCT), é altamente sensível aos efeitos da dabigatrana e é mais apropriado para detectar a presença do efeito anticoagulante da dabigatrana do que para quantificar o efeito da droga. Um TT diluído tem inaridade em todas as concentrações plasmáticas de dabigatrana farmacologicamente relevantes. O tempo de coagulação da ecarina (ECT), que mede diretamente a geração de trombina, é dependente da dose prolongado pela dabigatrana. É o ensaio mais sensível para dabigatrana, mas poucas instituições têm o teste disponível. O tempo de protrombina (TP) é o teste menos sensível. O TT diluído e a ECT são os testes de escolha para a dabigatrana.
Até o momento, não há antídoto para reverter o efeito da dabigatrana ou de outros novos anticoagulantes orais. O carvão ativado impede a absorção do fármaco, mas deve ser administrado em até 2 horas após a ingestão da dabigatrana. A diálise pode acelerar a eliminação da droga. Concentrados de complexos plasmáticos (PCCs) que contêm 3 (fatores II, IX e X) ou 4 (fatores II, VII, IX e X) fatores de coagulação foram sugeridos, mas sua eficácia não foi comprovada. O idarucizumab, um fragmento de anticorpo monoclonal que se liga ao dabigatrano livre e ligado à trombina, foi recentemente aprovado pelo FDA.
Dicas NYSORA
- A dabigatrana depende principalmente dos rins para eliminação e sua meia-vida é dobrada em pacientes com doença renal.
- Um intervalo maior entre a interrupção da droga e o procedimento neuroaxial, provavelmente 6 dias, é recomendado nesses pacientes.
Rivaroxaban
A rivaroxabana é um inibidor direto do fator Xa. As concentrações plasmáticas máximas são observadas dentro de 2.5 a 4 horas, e a inibição máxima do fator Xa (até 68%) ocorre 3 horas após a administração e é mantida por pelo menos 12 horas, ou 24 a 48 horas quando doses mais altas são administradas em idosos pacientes. A rivaroxabana tem meia-vida terminal de 5.7 a 9.2 horas, mas pode chegar a 11 a 13 horas em pacientes idosos devido ao declínio da função renal relacionado à idade. Um terço do fármaco é eliminado pelos rins, um terço pela via fecal/biliar e um terço é transformado em metabólitos inativos. A concentração máxima não é afetada pela obesidade (pacientes com peso ≥120 kg), mas é aumentada em 24% em pacientes com peso ≤50 kg. A depuração renal da rivaroxabana diminui com o aumento da insuficiência renal.
Rivaroxabana é eficaz no tratamento de TEV sintomático e não inferior à varfarina na prevenção de acidente vascular cerebral embólico durante fibrilação atrial. A adição de rivaroxabana à terapia antiplaquetária padrão reduz o desfecho composto de morte por causas cardiovasculares, infarto do miocárdio ou acidente vascular cerebral em pacientes com síndrome coronariana aguda recente. A rivaroxabana foi relatada como eficaz ou superior à enoxaparina na prevenção de TEV após cirurgia articular total. Nos estudos RECORD 1, 2, 3 e 4, a rivaroxabana foi um agente tromboprofilático mais eficaz que a enoxaparina, com perfil de segurança semelhante. Rosencher et ai. afirmaram que os cateteres peridurais não eram removidos até pelo menos 2 meias-vidas após a última dose de rivaroxabana, e a próxima dose de rivaroxabana era administrada 4-6 horas após a remoção do cateter. Nenhum dos 1141 pacientes que receberam rivaroxabana e tiveram anestesia neuraxial desenvolveu hematoma espinhal. No entanto, esse pequeno número de pacientes não é adequado para uma conclusão firme sobre a segurança perioperatória desse regime.
As diretrizes europeias e escandinavas recomendam um intervalo de 2 meias-vidas entre a descontinuação da rivaroxabana e a colocação ou remoção do cateter peridural (18 horas nas diretrizes escandinavas e 22 a 26 horas nas diretrizes europeias). Essas diretrizes também recomendam um intervalo de 4 a 6 horas antes da retomada da próxima dose, pois a rivaroxabana leva de 2.5 a 4 horas para atingir o efeito máximo.
Foi observada uma correlação linear entre os efeitos da rivaroxabana e do PT. No entanto, existe uma variabilidade acentuada na sensibilidade dos reagentes de PT ao rivaroxabano, pelo que se recomenda que cada laboratório calibre o seu PT especificamente para o rivaroxabano. O TTPa não tem sensibilidade suficiente para determinar o efeito da rivaroxabana. A inibição do fator Xa também pode ser um substituto para as concentrações plasmáticas de rivaroxabana. O PT e o anti-Xa são os testes recomendados para monitorar os efeitos da rivaroxabana.
O uso de carvão ativado tem sido recomendado para remover a rivaroxabana, mas deve ser administrado dentro de 8 horas após a ingestão da rivaroxabana. Foi demonstrado que um PCC de 4 fatores reverte a atividade anticoagulante in vitro da rivaroxabana em voluntários saudáveis. Devido à sua alta ligação às proteínas, a rivaroxabana e a apixabana podem não ser dialisáveis.
Apixaban
Apixabana é um inibidor do fator Xa altamente específico. É rapidamente absorvido e atinge concentrações máximas em 1-2 horas. Estudos demonstraram que a meia-vida terminal do apixabano é de 13.5 +/− 9.9 horas, ou 15.2 +/− 8.5 horas após uma dose única de 5 mg e 11.7 +/− 3.3 após múltiplas doses de 5 mg. A concentração plasmática máxima é afetada pelo peso corporal, com concentrações mais altas de apixabana em indivíduos com baixo peso corporal. A atividade anti-fator Xa do plasma mostrou uma relação linear direta com a concentração plasmática de apixabana.
Apixabana tem uma biodisponibilidade oral de mais de 45%. Após administração oral, é eliminado por múltiplas vias de eliminação, bem como por excreção renal e intestinal direta. Vinte e quatro a 29% da dose é excretada pelos rins e 56% da dose é recuperada nas fezes. Mais da metade da apixabana é excretada inalterada, diminuindo o risco de interações medicamentosas metabólicas A apixabana é eficaz na redução de acidente vascular cerebral ou embolia sistêmica sem aumentar o risco de sangramento. A apixabana é superior à varfarina na prevenção de acidente vascular cerebral ou embolia sistêmica em pacientes com fibrilação atrial. A apixabana fornece tromboprofilaxia eficaz na artroplastia total do joelho, comparável à enoxaparina ou varfarina. A apixabana é igualmente eficaz com a enoxaparina na prevenção de TEV após artroplastia total do joelho (TKR), enquanto apresenta uma taxa menor ou semelhante de sangramento maior. A apixabana é mais eficaz que a enoxaparina na prevenção de TEV após artroplastia total de quadril (ATQ) sem aumento do sangramento. Neste estudo, “os dispositivos relacionados à anestesia intratecal ou epidural foram removidos pelo menos 5 horas antes da primeira dose” de apixabana. Em todos os estudos de apixabana, a droga foi iniciada 12 a 24 horas após a cirurgia.
Comparado ao rivaroxabano, o apixabano tem pouco efeito na TP quando administrado em doses aprovadas. O ensaio de PT diluído melhorou a sensibilidade em relação ao PT convencional. Parece haver uma correlação linear entre a atividade anti-Xa e as concentrações plasmáticas de apixabana. O ensaio anti-Xa mostrou-se mais sensível que o PT e tão sensível quanto o ensaio PT diluído e parece ser a melhor escolha para o monitoramento clínico do efeito anticoagulante do apixabano. O carvão ativado, administrado em até 3 horas após a ingestão, reduz a absorção do apixabano.
Andexanet é uma proteína decoy do fator Xa humano modificado recombinante que se liga e sequestra os inibidores do fator Xa. Estudos em voluntários e em pacientes mostraram que o andexanet reverte a atividade anticoagulante da rivaroxabana e da apixabana. A partir de 2016, andexanet ainda não está clinicamente disponível nos Estados Unidos.
Resumo das Recomendações para os Novos Anticoagulantes
Enquanto um intervalo de 2-3 meias-vidas pode ser aceitável em pacientes com alto risco de TEV ou acidente vascular cerebral, um intervalo de 4-6 meias-vidas entre a interrupção do medicamento e a injeção neuraxial é provavelmente mais seguro na maioria dos pacientes com baixo risco de trombose. Um intervalo de 5 meias-vidas em conjunto com uma terapia de ponte de HBPM é uma alternativa na maioria dos pacientes, conforme mostrado em tabela 2. Após um procedimento neuroaxial ou remoção de um cateter peridural, o anticoagulante pode ser retomado 6 horas (8 horas menos o início/efeito de pico da droga, que geralmente é de 2 horas) depois. Os anticoagulantes são normalmente retomados dentro de 24 a 48 horas na maioria dos pacientes, mas podem ser retomados mais cedo em pacientes com maior risco de TEV ou acidente vascular cerebral; isto é, 24 horas menos o tempo para o efeito máximo da droga. Outros recomendaram um intervalo de 24 horas (tabela 3)
TABELA 3. Intervalos de tempo recomendados para retomada da droga após procedimento neuroaxial ou remoção do cateter.
| Droga | Diretrizes Europeias | Diretrizes escandinavas | Liew & Douketis (102); Connolly e Spyropoulos (98) |
|---|---|---|---|
| Dabigatran | 6h | 6h | 24 horas |
| Rivaroxaban | 4-6h | 6h | 24 horas |
| Apixaban | 4-6h | 6h | 24 horas |
A monitorização laboratorial do efeito anticoagulante é adequada em algumas situações, sendo sugeridos agentes de reversão quando há necessidade de restaurar rapidamente a função hemostática.
Dicas NYSORA
- Para os novos anticoagulantes, recomenda-se um intervalo de 5 meias-vidas entre a descontinuação do medicamento e o procedimento neuroaxial até que haja mais experiência com esses agentes.
- Recomenda-se um intervalo de 8 ou 24 horas até o pico do efeito do medicamento antes que o medicamento seja retomado após a remoção do cateter; um intervalo de 24 horas é provavelmente o mais seguro.
CARACTERÍSTICAS CLÍNICAS, DIAGNÓSTICO E TRATAMENTO DO HEMATOMA EPIDURAL
Os pacientes que desenvolvem hematoma espinhal geralmente apresentam dor nas costas súbita, intensa e constante, com ou sem componente radicular. A percussão sobre a coluna agrava a dor, assim como as manobras que aumentam a pressão intraespinhal, incluindo tosse, espirro ou esforço. Além disso, o retorno da fraqueza motora e/ou déficit sensorial após a aparente resolução do bloqueio epidural ou espinhal é altamente sugestivo de formação de hematoma epidural ou espinhal. Os achados motores e sensoriais dependem inteiramente do nível e tamanho do hematoma, mas podem incluir fraqueza, paresia, perda da função intestinal ou da bexiga e praticamente qualquer déficit sensorial. A ressonância magnética (RM) é o exame diagnóstico de escolha. O diagnóstico diferencial inclui abscesso espinhal, neoplasia epidural, hérnia discal aguda e hemorragia subaracnóidea espinhal. A recuperação sem cirurgia é rara, e a consulta neurocirúrgica para consideração de laminectomia descompressiva emergente deve ser obtida assim que houver suspeita de hematoma espinhal. A recuperação funcional está relacionada principalmente ao período de tempo em que os sintomas estão presentes antes da cirurgia. As características clínicas, diagnóstico, diagnóstico diferencial e tratamento de um paciente com hematoma espinhal são discutidos com mais detalhes em Toxicidade Sistêmica Anestésica Local.
RESUMO
Os profissionais devem atualizar periodicamente sua base de conhecimento sobre novos medicamentos anticoagulantes, protocolos de anticoagulação, recomendações atuais de diretrizes e alertas da FDA. Como o hematoma espinhal pode ocorrer mesmo na ausência de fatores de risco identificáveis, a vigilância no monitoramento é fundamental para avaliação precoce da disfunção neurológica e intervenção imediata. A decisão de realizar o bloqueio neuroaxial e o momento da remoção do cateter em um paciente recebendo terapia anticoagulante deve ser feita individualmente, pesando os benefícios da anestesia regional contra o pequeno, embora definitivo, risco de hematoma espinhal.
Anticoagulação e Bloqueios de Nervos Periféricos
Se apropriado, bloqueios de nervos periféricos podem ser realizados em pacientes em uso de anticoagulantes. Ao contrário dos procedimentos neuroaxiais na presença de anticoagulantes, não há estudos prospectivos sobre bloqueios de nervos periféricos na presença de anticoagulantes. A ASRA recomenda as mesmas diretrizes para bloqueios de nervos periféricos e procedimentos neuraxiais. Casos de hematomas do psoas e retroperitoneais foram relatados após bloqueios dos nervos do plexo lombar e do compartimento do psoas. Esses pacientes estavam em uso de enoxaparina, ticlopidina ou clopidogrel. Em alguns casos, o hematoma ocorreu apesar da adesão às diretrizes da ASRA.
Os sintomas de formação de hematoma após bloqueio de nervo periférico podem incluir dor (dor no flanco ou paravertebral, ou dor na virilha no sangramento do psoas), sensibilidade na área, um declínio constante da hemoglobina/hematócrito, hipotensão devido à hipovolemia e déficit sensório-motor. O diagnóstico definitivo é feito por tomografia computadorizada (TC); a ultrassonografia também pode ser usada para detectar a presença de hematoma subcapsular renal após bloqueio do nervo do compartimento do psoas. O tratamento pode incluir consulta cirúrgica, reversão da anticoagulação, transfusão de sangue, se necessário, e espera vigilante versus drenagem cirúrgica.
Provavelmente é muito restritivo adaptar as diretrizes da ASRA sobre bloqueios de nervos neuroaxiais para pacientes submetidos a bloqueios de nervos periféricos. A Sociedade Europeia de Anestesiologia observou que as diretrizes para bloqueio de nervo neuroaxial não se aplicam rotineiramente a bloqueios de nervo periférico. A Sociedade Austríaca de Anestesiologia, Ressuscitação e Terapia Intensiva, por outro lado, sugeriu que bloqueios nervosos superficiais podem ser realizados com segurança na presença de anticoagulantes. Devido à possibilidade de hematoma retroperitoneal, os bloqueios do plexo lombar e dos nervos paravertebrais merecem as mesmas recomendações das injeções neuroaxiais. As mesmas diretrizes também devem ser aplicadas aos bloqueios nervosos simpáticos viscerais. As diretrizes da ASRA podem, portanto, ser aplicáveis a bloqueios nervosos em áreas vasculares e não compressíveis, como bloqueios nervosos do plexo celíaco, bloqueios nervosos do plexo hipogástrico superior e bloqueios nervosos do plexo lombar. Os médicos devem individualizar sua decisão e discutir os riscos e benefícios do bloqueio nervoso com o paciente e o cirurgião. Mais importante ainda, o clínico deve acompanhar o paciente de perto após a colocação do bloqueio do nervo.
Dicas NYSORA
- As diretrizes sobre injeções neuraxiais também devem ser aplicadas aos bloqueios dos nervos do plexo lombar e aos bloqueios dos nervos simpáticos viscerais.
- Para bloqueios nervosos superficiais, bloqueios nervosos regionais guiados por ultrassom provavelmente podem ser realizados na presença de anticoagulação residual.
REFERÊNCIAS
- Horlocker TT, Wedel DJ: Anticoagulação e bloqueio do nervo neuroaxial: perspectiva histórica, implicações anestésicas e gerenciamento de risco. Reg Anesth Pain Med 1998;23:129–134.
- Tryba M: [Anestesia regional peridural e heparina de baixo peso molecular: Pro]. Anasthesiol Intensivmed Notfallmed Schmerzther 1993;28:179–181.
- Pöpping DM, Zahn PK, Van Aken HK, Dasch B, Boche R, Pogatzki-Zahn EM: Eficácia e segurança do manejo da dor pós-operatória: uma pesquisa com 18 pacientes consecutivos entre 925 e 1998 (2006ª revisão): uma análise de banco de dados de dados levantados. Br J Anaesth 2;2008:101–832.
- Moen V, Dahlgren N, Irestedt L: Complicações neurológicas graves após bloqueios neuroaxiais centrais na Suécia 1990-1999. Anestesiologia 2004;101:950–959.
- Volk T, Wolf A, Van Aken H, Bürkle H, Wiebalck A, Steinfeldt T: Incidência de hematoma espinhal após punção peridural: análise da rede alemã para segurança em anestesia regional. Eur J Anesthesiol 2012;29:170–176.
- Ehrenfeld JM, Agarwal AK, Henneman JP, Sandberg WS: Estimando a incidência de suspeita de hematoma epidural e o custo de imagem oculto do cateterismo epidural: uma revisão retrospectiva de 43,200 casos. Reg Anesth Pain Med 2013;38:409–414.
- Bateman BT, Mhyre JM, Ehrenfeld J, et al: O risco e os resultados de hematomas epidurais após cateterismo peridural perioperatório e obstétrico: um relatório do consórcio de pesquisa multicêntrico do grupo de resultados perioperatórios. Anesth Analg 2013:116:1380–1385.
- Horlocker T, Kopp S: Hematoma epidural após bloqueio epidural nos Estados Unidos: Não é mais apenas heparina de baixo peso molecular após cirurgia ortopédica. Anesth Analg 2013;116:1195–1197.
- Horlocker T: Bloqueio neuroaxial em pacientes com estenose espinhal: entre uma pedra e um lugar duro. Anesth Analg 2010;110:1305.
- Gulur P, Tsui B, Pathak R, Koury KM, Lee H: Análise retrospectiva da incidência de hematoma epidural em pacientes com cateteres epidural e parâmetros anormais de coagulação. Br J Anaesth 2015;114:808–811.
- Heit JA, Horlocker TT (eds): Anestesia neuroaxial e anticoagulação. Reg Anesth Pain Med 1998;23:S129–S193.
- Horlocker TT, Wedel DJ, Benzon HT, et al: Anestesia regional no paciente anticoagulado: Definindo os riscos (A segunda conferência de consenso da ASRA sobre anestesia neuraxial e anticoagulação). Reg Anesth Pain Med 2003;28:171–197.
- Horlocker TT, Wedel DJ, Rowlingson JC, et al: Anestesia regional no paciente recebendo terapia antitrombótica ou terapia trombolítica: Diretrizes baseadas em evidências da Sociedade Americana de Anestesia Regional e Medicina da Dor (terceira edição). Reg Anesth Pain Med 2010;35:64–101.
- Gogarten W, Vandermeulen E, Van Aken H, Kozek S, Llau JV, Samama CM: Sociedade Europeia de Anestesiologia. Anestesia regional e agentes antitrombóticos: recomendações da Sociedade Europeia de Anestesiologia. Eur J Anesthesiol 2010;27:999–1015.
- Breivik H, Bang U, Jalonen J, Vigfusson G, Alahuhta S, Lagerkranser M: Diretrizes nórdicas para bloqueios neuroaxiais em hemostasia perturbada da Sociedade Escandinava de Anestesiologia e Medicina Intensiva. Acta Anesthesiol Scand 2010;54:16–41.
- Cronberg S, Wallmark E, Söderberg I: Efeito na agregação plaquetária da administração oral de 10 analgésicos não esteróides a humanos. Scand J Haematol 1984;33:155–159.
- Locke GE, Giorgio AJ, Biggers SL Jr, et al: Hematoma epidural espinhal agudo secundário a sangramento prolongado induzido por aspirina. Surg Neurol 1976; 5:293-296.
- Vandermeulen EP, Van Aken H, Vermylen J: Anticoagulantes e anestesia raqui-peridural. Anesth Analg 1994;79:1165–1177.
- CLASP (Estudo Colaborativo de Aspirina de Baixa Dose na Gravidez) Grupo Colaborativo. CLASP: um estudo randomizado de aspirina em baixas doses para a prevenção e tratamento da pré-eclâmpsia entre 9364 mulheres grávidas. Lancet 1994;343:619-629.
- Horlocker TT, Wedel DJ, Offord KP: A terapia antiplaquetária pré-operatória aumenta o risco de complicações hemorrágicas associadas à anestesia regional? Anesth Analg 1990;70:631–634.
- Horlocker TT, Wedel DJ, Schroeder DR, et al: A terapia antiplaquetária pré-operatória não aumenta o risco de hematoma espinhal associado à anestesia regional. Anesth Analg 1995;80:303–309.
- Benzon HT, Brunner EA, Vaisrub N: Tempo de sangramento e bloqueios nervosos após aspirina. Reg Anesth 1984; 9:86-90.
- Horlocker TT, Bajwa ZH, Ashraft Z, et al: Avaliação do risco de complicações hemorrágicas associadas a medicamentos antiinflamatórios não esteroides em pacientes ambulatórios de dor submetidos à injeção peridural de esteroides. Anesth Analg 2002;95: 1691–1697.
- Benzon HT, Wong HY, Siddiqui T, et al: Cuidado ao realizar injeções peridurais em pacientes em uso de vários medicamentos antiplaquetários. Anestesiologia 1999;91:1558–1559.
- Benzon HT, Huntoon M: Precisamos de novas diretrizes para procedimentos intervencionistas de dor em pacientes em uso de anticoagulantes? Reg Anesth Pain Med 2014;39:1–3.
- Giberson CE, Barbosa J, Brooks ES, et al: Hematomas epidurais após remoção de eletrodos de estimulação percutânea da medula espinhal: relato de dois casos. Reg Anesth Pain Med 2014;39:73–77.
- Williams KN, Jackowski A, Evans PJD: Hematoma epidural requerendo descompressão cirúrgica após repetidas injeções de esteroides peridurais cervicais para dor crônica. Dor 1990;42:197-199.
- Ain RJ, Vance MB: Hematoma peridural após injeção peridural de esteróide em paciente sem enoxaparina de acordo com as diretrizes. Anestesiologia 2005;102:701–703.
- Buvanendran A, Young A: Hematoma epidural espinhal após a colocação do eletrodo de teste do estimulador da medula espinhal em um paciente tomando aspirina. Reg Anesth Pain Med 2014;39:70–72.
- Desai MJ, Dua S: Hematoma perineural após injeção de esteróide transforaminal lombar causando radiculopatia lombar aguda-crônica: relato de caso. Prática da Dor 2014;14:271–277.
- Mahmoud J, Mathews M, Verna S, Basil B: trombocitopenia induzida por oxcarbazepina. Psicossomática 2006;47:73–74.
- Meijer WEE, Heerdink ER, Nolen WA, Herings RMC, Leufkens HGM, Egberts ACG. Associação de risco de sangramento anormal com grau de inibição da recaptação de serotonina por antidepressivos. Arch Intern Med 2004;164:2367–2370.
- Narouze S, Benzon HT, Provenzano DA, et al: Procedimentos intervencionistas da coluna e dor em pacientes em uso de medicamentos antiplaquetários e anticoagulantes: diretrizes da Sociedade Americana de Anestesia Regional e Medicina da Dor, da Sociedade Europeia de Anestesia Regional e Terapia da Dor, da Academia Americana of Pain Medicine, a International Neuromodulation Society, a North American Neuromodulation Society e o World Institute of Pain. Reg Anesth Pain Med 2015;40: 182–212.
- Gajraj NM: Inibidores da ciclooxigenase-2. Anesth Analg 2003;96: 1720–1738.
- Buvanendran A, Kroin JS, Tuman KJ, et al: Efeitos da administração perioperatória de um inibidor seletivo da ciclooxigenase 2 no controle da dor e recuperação da função após a substituição do joelho: um estudo controlado randomizado. JAMA 2003;290:2411–2418.
- Gajraj NM, Joshi GP: Papel dos inibidores da ciclooxigenase-2 no manejo da dor pós-operatória. Anesthesiol Clin North America 2005;23:49–72.
- Desjardins PJ, Shu VS, Recker DP, et al: Uma única dose pré-operatória de valdecoxib, um novo inibidor específico da ciclooxigenase-2, alivia a dor pós-cirurgia oral ou bunionectomia. Anestesiologia 2002;97:565–573.
- Sinatra RS, Shen QJ, Halaszynski T, et al: Suspensão oral pré-operatória de rofecoxib como adjuvante analgésico após cirurgia abdominal baixa: os efeitos de uma dor dependente de esforço e função pulmonar. Anesth Analg 2003;98:135–140.
- Arrendatário PT, Hubbard RC, Karim A, et al: Efeitos do celecoxib, um novo inibidor da ciclooxigenase-2, na função plaquetária em adultos saudáveis: um ensaio clínico randomizado. J Clin Pharmacol 2000;40:124–132.
- van Heeken H, Schwartz JI, Depre M, et al: Atividade inibitória comparativa de rofecoxib, meloxicam, diclofenaco, ibuprofeno e naproxeno em COX-2 versus COX-1 em voluntários saudáveis. J Clin Pharmacol 2000;40:1109-1120.
- Greenberg H, Gottesdiener K, Huntington M, et al: Um novo inibidor da ciclooxigenase-2, rofecoxib (VIOXX) não alterou os efeitos antiplaquetários da aspirina em baixas doses em voluntários saudáveis. J Clin Pharmacol 2000;40:1509–1515.
- Psaty BM, Furberg CD: Inibidores de Cox-2—Lições sobre segurança de medicamentos. N Engl J Med 2005;352:1133–1135.
- Schror K: Drogas antiplaquetárias: uma revisão comparativa. Drogas 1995; 50:7-28.
- Yang LH, Fareed J: Ação vasomoduladora do clopidogrel e da ticlopidina. Thromb Res 1997;86:479–491.
- CAPRIE Steering Committee: Um estudo cego randomizado de clopidogrel versus aspirina em pacientes com risco de acidente vascular cerebral isquêmico (CAPRIE). Lancet 1996;348:1329-1339.
- Helft G, Osende JI, Worthley SG, et al: Efeito antitrombótico agudo de um regime de clopidogrel em pacientes com aterosclerose em uso de aspirina. Arterioscler Thromb Vasc Biol 2000;29:2316–2321.
- Mayumi T, Dohi S: Hematoma subaracnóideo espinhal após punção lombar em paciente recebendo terapia antiplaquetária. Anesth Analg 1983;62:777–779.
- Benzon HT, McCarthy R, Benzon HA, et al: Determinação da atividade antiplaquetária residual do clopidogrel. Br J Anaesth 2011;107: 966–971.
- Hall R, Mazer CD: Antiplaquetários: uma revisão de sua farmacologia e manejo no período perioperatório. Anesth Analg 2011;112: 292–318.
- Inibidores de Wallentin L: P2Y(12): diferenças nas propriedades e mecanismos de ação e potenciais consequências para uso clínico. Eur Heart J 2009;30:1964–1977.
- Capodanno D, Ferreiro JL, Angiolillo DJ: Terapia antiplaquetária: novos agentes farmacológicos e mudança de paradigmas. J Thromb Haemost 2013;11(Suppl 1):316–329.
- Brandt JT, Payne CD, Wiviott SD, et al: Uma comparação das doses de carga de prasugrel e clopidogrel na função plaquetária: a magnitude da inibição plaquetária está relacionada à formação de metabólitos ativos. Am Heart J 2007;153:66.e9–16.
- Dobesh PP: Farmacocinética e farmacodinâmica do prasugrel, um inibidor de tienopiridina P2Y12. Farmacoterapia 2009;29:1089–1102.
- Asai F, Jacubowski JA, Nagamura H, et al: Atividade inibidora de plaquetas e farmacocinética de prasugrel (CS-747) um novo inibidor tienopiridina P2Y12: um estudo de dose única ascendente em humanos saudáveis. Plaquetas 2006;17:209–217.
- Wiviott SD, Trenk D, Frelinger AL, et al: Prasugrel comparado com clopidogrel em altas doses de carga e manutenção em pacientes com intervenção coronária percutânea planejada: o Prasugrel em comparação com clopidogrel para inibição da ativação e agregação plaquetárias-trombólise no infarto do miocárdio 44 tentativas. Circulação 2007; 116: 2923-2932.
- Wiviott SD, Antman EM, Winters KJ, et al: Comparação randomizada de prasugrel (CS-747, LY640315), um novo antagonista tienopiridínico P2Y12, com clopidogrel em intervenção coronária percutânea: resultados da utilização conjunta de medicamentos para bloquear plaquetas de forma otimizada (JUMBO )-TIMI 26 julgamento. Circulação 2005;111:3366–3373.
- Brandt JT, Close SL, Iturria SJ, et al: Polimorfismos comuns de CYP2C19 e CYP2C9 afetam a resposta farmacocinética e farmacodinâmica ao clopidogrel, mas não ao prasugrel. J Thromb Haemost 2007;5:2429–2436.
- Mega JL, Close SL, Wiviott SD, et al: Polimorfismos genéticos do citocromo P450 e a resposta ao prasugrel: relação com resultados farmacocinéticos, farmacodinâmicos e clínicos. Circulação 2009;119:2553–2560.
- Teng R, Butler K: Farmacocinética, farmacodinâmica, tolerabilidade e segurança de doses únicas ascendentes de ticagrelor, um antagonista do receptor P2Y(12) oral de ligação reversível, em indivíduos saudáveis. Eur J Clin Pharmacol 2010;66:487–496.
- Teng R, Oliver S, Hayes MA, Butler K: Absorção, distribuição, metabolismo e excreção de ticagrelor em indivíduos saudáveis. Drug Metab Dispos 2010; 38:1514-1521.
- Husted S, Emanuelsson H, Heptinstall S, Sandset PM, Wickens M, Peters G: Farmacodinâmica, farmacocinética e segurança do antagonista P2Y12 oral reversível AZD6140 com aspirina em pacientes com aterosclerose: uma comparação duplo-cega com clopidogrel com aspirina. Eur Heart J 2006;27:1038–1047.
- Gurbel PA, Bliden KP, Butler K, et al: Avaliação randomizada duplo-cega do ONSET e OFFSET dos efeitos antiplaquetários do ticagrelor versus clopidogrel em pacientes com doença arterial coronariana estável: o estudo ONSET/OFFSET. Circulação 2009;120:2577–2585.
- George JN: Plaquetas. Lancet 2000;355:1531–1539.
- van Giezen J, Nilsson L, Berntsson P, et al: Ticagrelor liga-se ao P2Y(12) humano independentemente do ADP, mas antagoniza a sinalização do receptor induzida pelo ADP e a agregação plaquetária. J Thromb Haemost 2009;7:1556–1565.
- Baron TH, Kamath PS, McBane RD: Manejo da terapia antitrombótica em pacientes submetidos a procedimentos invasivos. N Engl J Med 2013;368:2113–2124.
- Rodgers RPC, Levin J: Uma reavaliação crítica do tempo de sangramento. Semin Thromb Hemost 1990;16:1–20.
- Ferraris VA, Swanson E: Uso de aspirina e perda de sangue perioperatória em pacientes submetidos a operações inesperadas. Surg Gynecol Obstet 1983;156:439–442.
- Mammen EF, Comp PC, Gosselin R, et ai: sistema PFA-100. Um novo método para avaliação da disfunção plaquetária. Semin Thromb Hemost 1998;24:195–202.
- Edwards A, Jakubowski JA, Rechner AR, Sugidachi A, Harrison P: Avaliação do cartucho de teste INNOVANCE PFA P2Y: sensibilidade ao bloqueio P2Y(12) e influência do anticoagulante. Plaquetas 2012;23: 106–115.
- Gorog DA, Fuster V: Testes de função plaquetária em cardiologia clínica. J Am Coll Cardiol 2013;61:2115–2129.
- Bouman HJ, Parlak E, van Werkum JW, et al: Qual teste de função plaquetária é adequado para monitorar a resposta ao clopidogrel? Uma análise farmacocinética do metabólito ativo do clopidogrel. J Thromb Haemost 2010;8:482–488.
- van Werkum JW, Harmsze AM, Elsenberg EH, Bouman HJ, ten Berg JM, Hackeng CM: O uso do sistema VerifyNow para monitorar a terapia antiplaquetária: uma revisão das evidências atuais. Plaquetas 2008;19:479–488.
- Mueller T, Dieplinger B, Poelz W, Haltmayer M: Utilidade do instrumento PFA-100 e do novo analisador multiplaca para a avaliação dos efeitos da espirina e do clopidogrel na função plaquetária em pacientes com doença cardiovascular. Clin Appl Thromb Hemost 2009;15:652–659.
- Scharbert G, Auer A, Kozek-Langenecker S: Avaliação do ensaio de mapeamento de plaquetas em ROTEM de tromboelastometria rotacional. Plaquetas 2009;20:125–130.
- Malinin A, Pokov A, Swaim L, Kotob M, Serebruany V: Validação de um cartucho VerifyNow-P2Y12 para monitorar a inibição plaquetária com clopidogrel. Métodos Encontre Exp Clin Pharmacol 2006;28:315.
- Benzon HT, Avram J, Green D, Bonow RO: Novos anticoagulantes orais e anestesia regional. Br J Anaesth 2013;111(Supl 1):i96–i113.
- Kearon C, Hirsh J: Manejo da anticoagulação antes e após cirurgia eletiva. N Engl J Med 1997;336:1506–1511.
- Harrison L, Johnston M, Massicote MP, et al: Comparação de doses de 5 mg e 10 mg no início da terapia com varfarina. Ann Intern Med 1997;126:133–136.
- Benzon HT, Benzon HA, Kirby-Nolan M, Avram MJ, Nader A: Níveis de fator VII e fatores de risco para aumento da razão normalizada internacional na fase inicial da terapia com varfarina. Anestesiologia 2010;112:298–304.
- Schulman S, Lockner D, Bergstrom K, Blomback M: Anticoagulação oral inicial intensiva e tratamento mais curto com heparina na trombose venosa profunda. Thromb Haemost 10984;52:276–280.
- Enneking FK, Benzon HT: Anticoagulantes orais e anestesia regional: uma perspectiva. Reg Anesth Pain Med 1998;23:140–145.
- Odoom JA, Sih IL: Analgesia epidural e terapia anticoagulante. Anestesia 1983;38:254–259.
- Horlocker TT: Quando remover um cateter raquidiano ou peridural em um paciente anticoagulado. Reg Anesth 1993;18:264–265.
- Horlocker TT, Wedel DJ, Schlichting JL: Analgesia peridural pós-operatória e terapia anticoagulante oral. Anesth Analg 1994;79:89–93.
- Wu CL, Perkins FM: Profilaxia com anticoagulante oral e remoção de cateter epidural. Reg Anesth 1996;21:517–524.
- Liu SS, Buvanendran A, Viscusi ER, et al: Remoção descomplicada de cateteres peridurais em 4365 pacientes com razão normalizada internacional maior que 1.4 durante o início da terapia com varfarina. Reg Anesth Pain Med 2011;36:231–235.
- Weinstock DM, Chang P, Aronson DL, et al: Comparação das concentrações plasmáticas de protrombina e fator VII e protrombina F1 na urina em pacientes em terapia de longo prazo com varfarina e aqueles em fase inicial. Am J Hematol 1998;57:193-199.
- Jerkeman A, Astermark J, Hedner U, et al: Correlação entre diferentes intensidades de tratamento anti-vitamina K e parâmetros de coagulação. Thromb Res 2000;98:467–471.
- Abildgaard U, Lindahl AK, Sandset PM: A heparina requer antitrombina e inibidor da via extrínseca para seu efeito anticoagulante no sangue humano. Hemostasia 1991;21:254–257.
- Murray DJ, Brodsnahan WJ, Pennell B, et al: Detecção de heparina pelo tempo de coagulação ativado: Uma comparação da sensibilidade de testes de coagulação e ensaios de heparina. J Cardiothorac Vasc Anesth 1997; 11:24-28.
- Shapiro SS. Tratamento da trombose no século XXI. N Engl J Med 21;2003:349–1762.
- Rao TL, El-Etr AA: Anticoagulação após colocação de cateteres peridural e subaracnóideo: uma avaliação das sequelas neurológicas. Anestesiologia 1981;55:618-620.
- Ruff DL, Dougherty JH: Complicações da anticoagulação seguida de anticoagulação. AVC 1981;12:879-881.
- Liu SS, Mulroy MF: Anestesia neuroaxial e analgesia na presença de heparina padrão. Reg Anesth Pain Med 1998;23:157–163.
- Chaney MA: Anestesia e analgesia intratecal e epidural para cirurgia cardíaca. Anesth Analg 1997;84:1211–1221.
- Geerts WH, Bergqvist D, Pineo GF, et al: Prevenção de tromboembolismo venoso. Diretrizes de Prática Clínica Baseada em Evidências do American College of Chest Physicians (8ª edição). Baú 2008;133: 381S–453S.
- King CS, Holley AB, Jackson JL, et al: Dosagem de heparina duas vezes versus três vezes ao dia para profilaxia de tromboembolismo na população geral: uma meta-análise. Peito 2007;131:507–516.
- Weitz JI. Terapia medicamentosa: heparinas de baixo peso molecular. N Engl J Med 1997;337:688–698.
- Horlocker TT, Heit JA: Heparina de baixo peso molecular: bioquímica, farmacologia, regimes de profilaxia perioperatória e diretrizes para manejo anestésico regional. Anesth Analg 1997;85:874–885.
- Bara L, Billaud E, Gramond G, et al: Farmacocinética comparativa de uma heparina de baixo peso molecular (PK 10 169) e heparina não fracionada após administração intravenosa e subcutânea. Thromb Res 1985;39:631–636.
- Klein S, Slaughter T, Vail PT, et al: Trombelastografia como medida perioperatória de anticoagulação resultante de heparina de baixo peso molecular: comparação com concentrações de anti-Xa. Anesth Analg 2000;91:1091–1095.
- Branco RH: Heparinas de baixo peso molecular: são todas iguais? Br J Haematol 2003;121:12–20.
- Horlocker TT, Wedel DJ: Bloqueio neuroaxial e heparina de baixo peso molecular: equilibrando analgesia perioperatória e tromboprofilaxia. Reg Anesth Pain Med 1998;23:164–177.
- Administração de Alimentos e Medicamentos dos EUA. Comunicação de Segurança de Medicamentos da FDA: recomendações atualizadas para diminuir o risco de sangramento e paralisia da coluna vertebral em pacientes em uso de heparinas de baixo peso molecular. http://www.fda.gov/drugs/drugsafety/ucm373595.htm. Atualizado em 19 de janeiro de 2016. Acessado em 9 de setembro de 2015.
- Rosenquist RW, Brown DL: Sangramento neuroaxial: Fibrinolíticos/trombolíticos. Reg Anesth Pain Med 1998;23S:152–156.
- Bauer KA: Fondaparinux: propriedades básicas e eficácia e segurança na profilaxia do tromboembolismo venoso. Am J Orthop 2002;31:4–10.
- Turpie AG, Bauer KA, Eriksson BL, et al: Fondaparinux vs enoxaparina para a prevenção de tromboembolismo venoso em cirurgia ortopédica de grande porte: uma meta-análise de 4 estudos randomizados duplo-cegos. Arch Intern Med 2002;162:1833–1840.
- Os investigadores de Matisse: fondaparinux subcutâneo versus heparina não fracionada intravenosa no tratamento inicial da embolia pulmonar. N Engl J Med 2003;349:1695–1702.
- Singelyn FJ, Verheyen CC, Piovella F, Van Aken HK, Rosenceher N, EXPERT Investigadores do estudo: A segurança e eficácia da tromboprofilaxia estendida com fondaparinux após cirurgia ortopédica de grande porte do membro inferior com ou sem um cateter neuroaxial ou de nervo periférico profundo: o EXPERT Estudar. Anesth Analg 2007;105:1540–1547.
- Rosencher N, Bonnet MP, Sessler DI: Novos agentes antitrombóticos selecionados e anestesia neuraxial para cirurgia ortopédica de grande porte: estratégias de manejo. Anestesia 2007;62:1154–1160.
- Greenblatt DJ: Meia-vida de eliminação das drogas: valor e limitações. Ann Rev Med 985;36:421–427.
- Olesen JB, Lip GY, Hansen ML, et al: Validação de esquemas de estratificação de risco para prever acidente vascular cerebral e tromboembolismo em pacientes com fibrilação atrial: estudo de coorte nacional. BMJ 2011;342:d124.
- Connolly G, Spyropoulos AC: questões práticas, limitações e gestão periprocedimento dos NOACs. J Thromb Thrombolysis 2013;36:212–222.
- Garcia D, Barrett YC, Ramaciotti E, Weitz JI: Avaliação laboratorial dos efeitos anticoagulantes da próxima geração de anticoagulantes orais. J Thromb Haemost 2013;11:245–252.
- IST-3 Collaborative Group: Os benefícios e malefícios da trombólise intravenosa com ativador de plasminogênio tecidual recombinante dentro de 6 h de acidente vascular cerebral isquêmico agudo (o terceiro estudo internacional de acidente vascular cerebral [IST-3]): um estudo randomizado. Lancet 2012;379:2352–2363.
- Tertri S, Hakal J, Juvela S, et al: Segurança de enoxaparina subcutânea de baixa dose para a prevenção de tromboembolismo venoso após hemorragia intracerebral primária. Thromb Res 2008;123:206–212.
- Liew A, Douketis J: Manejo perioperatório de pacientes que estão recebendo um novo anticoagulante oral. Estagiário Emerg Med 2013;8:477–484.
- Blech S, Ebner T, Ludwig-Schwellinger E, Stangier J, Roth W: O metabolismo e a disposição do inibidor oral direto da trombina, dabigatrana, em humanos. Disposição de Metab de Drogas 2008; 36:386-399.
- Di Nisio M, Middeldorp S, Buller HR. Inibidores diretos da trombina. N Engl J Med 2005;353:1028–1040.
- Levy JH, Faraoni D, Spring JL, Douketis JD, Samana CM: Gerenciando novos anticoagulantes orais no ambiente perioperatório e unidade de terapia intensiva. Anestesiologia 2013;118:1466–1474.
- Stangier J, Clemens A: Farmacologia, farmacocinética e farmacodinâmica do etexilato de dabigatrana, um inibidor oral direto da trombina. Clin Appl Thromb Hemost 2009;15(S1):9S–16S.
- Stangier J, Stahle H, Rathgen K, Fuhr R: Farmacocinética e farmacodinâmica do inibidor oral direto da trombina dabigatrano em idosos saudáveis. Clin Pharmacokinet 2008;47:47–59.
- Eisert WG, Hauel N, Stangier J, Wienen W, Clemens A, Van Ryn J: Dabigatran: um romance oral potente inibidor reversível não peptídico da trombina. Arterioscler Thromb Vasc Biol 2010;30:1885–1889.
- Stangier J, Rathgen K, Stahle H, Mazur D: Influência da insuficiência renal na farmacocinética e farmacodinâmica do etexilato de dabigatrana oral. Um estudo aberto, de grupos paralelos e de centro único. Clin Pharmacokinet 2010;49:259–268.
- Ezekowitz MD, Reilly PA, Nehmiz G, et al. Dabigatrana com ou sem aspirina concomitante em comparação com varfarina isolada em pacientes com fibrilação atrial não valvar (Estudo PETRO). Am J Cardiol 2007;100: 1419-1426.
- Ericksson BI, Dahl OE, Buller HR, et al; Grupo de Estudo BISTRO II: Um novo inibidor oral direto da trombina, etexilato de dabigatrana, comparado com enoxaparina para prevenção de eventos tromboembólicos após artroplastia total de quadril ou joelho: o estudo randomizado BISTRO II. J Thromb Haemost 2005;3:103–111.
- Ericksson BI, Dahl OE, Rosencher N, et ai; RE-MODEL Grupo de estudo: etexilato de dabigatrana oral versus enoxaparina subcutânea para a prevenção de tromboembolismo venoso após artroplastia total do joelho: o estudo randomizado RE-MODEL. J Thromb Haemost 2007;5:2178–2185.
- Ericksson BI, Dahl OE, Rosencher N, et ai; Grupo de Estudos RE-NOVATE. Etexilato de dabigatrana versus enoxaparina para prevenção de tromboembolismo venoso após artroplastia total do quadril: um estudo randomizado, duplo-cego e de não inferioridade. Lancet 2007;370:949–956.
- RE-MOBILIZE Comitê de Redação, Ginsberg JS, Davidson BL, Comp PC, et al: Inibidor oral da trombina dabigatrana etexilato vs regime norte-americano de enoxaparina para prevenção de tromboembolismo venoso após cirurgia de artroplastia do joelho. J Artroplastia 2009;24:1–9.
- Wolowacz SE, Roskell NS, Plumb JM, Caprini JA, Ericksson BI: Eficácia e segurança do etaxilato de dabigatrana para a prevenção de tromboembolismo venoso após artroplastia de quadril ou joelho. Uma meta-análise. Thromb Haemost 2009;101:77–85.
- Harper P, Young L, Merriman E: Risco de sangramento com dabigatrana em idosos frágeis. N Engl J Med 2012;366:864–866.
- Tripodi A: O laboratório e os anticoagulantes orais diretos. Sangue 2013;121:4032–4035.
- Siegal DM, Cuker A: Reversão de novos anticoagulantes orais em pacientes com sangramento maior. J Thromb Thrombolysis 2013;35:391–398.
- Miyares MA, Davis K: Novos anticoagulantes orais: uma revisão das opções de monitoramento laboratorial e agentes de reversão no paciente hemorrágico. Am J Health Syst Pharm 2012;69:1473–1484.
- Baron TH, Kamath PS, McBane RD: Manejo da terapia antitrombótica em pacientes submetidos a procedimentos invasivos. N Engl J Med 2013;368:2113–2124.
- Breuer G, Weiss DR, Ringwald J: 'Novos' anticoagulantes orais diretos no ambiente perioperatório. Curr Opin Anesthesiol 2014;27:409–419.
- Lévy S: Novos antitrombóticos clinicamente disponíveis e seus antídotos. J Interv Card Electrophysiol 2014;40:269–275.
- Laux V, Perzborn E, Kubitza D, Misselwitz F: Características pré-clínicas e clínicas da rivaroxabana: um novo inibidor oral do fator Xa direto. Sem Thromb Hemost 2007;33:515–523.
- Kubitza D, Becka M, Wensing G, Voith B, Zuehlsdorf M: Segurança, farmacodinâmica e farmacocinética de BAY 59-7939 - um inibidor oral direto do fator Xa - após dosagem múltipla em indivíduos saudáveis do sexo masculino. Eur J Clin Pharmacol 2005;61:873-880.
- Jiang J, Hu Y, Zhang J, et al: Segurança, farmacocinética e farmacodinâmica de doses únicas de rivaroxabana – um inibidor oral direto do fator Xa – em idosos chineses. Thromb Haemost 2010;103:234–241.
- Kubitza D, Becka M, Roth A, Mueck W: Estudo de aumento de dose da farmacocinética e farmacodinâmica da rivaroxabana em idosos saudáveis. Curr Med Res Opin 2008;24:2757–2765.
- Ericksson BI, Quinlan DJ, Weitz JI: Farmacodinâmica comparativa e farmacocinética da trombina direta oral e inibidores do fator Xa em desenvolvimento. Clin Pharmacokinet 2009;48:1–22.
- Weitz JI, Eikelboom JW, Samama MM: Novas drogas antitrombóticas. Baú 2012;141S:e120S–e151S.
- Kubitza D, Becka M, Mueck W, et al: Efeitos da insuficiência renal na farmacocinética, farmacodinâmica e segurança da rivaroxabana, um inibidor oral direto do fator Xa. Br J Clin Pharmacol 2010;70:703-712.
- Patel MR, Mahaffey KW, Garg J, et ai; Investigadores ROCKET AF: Rivaroxabana versus varfarina na fibrilação atrial não valvar. N Engl J Med 2011;365:883–891.
- Eriksson BI, Borris LC, Friedman RJ, et al; RECORD1 Grupo de Estudo: Rivaroxabana versus enoxaparina para tromboprofilaxia após artroplastia de quadril. N Engl J Med 2008;358:2765–2775.
- Kakkar AK, Brenner B, Dahl O, et ai; RECORD2 Investigadores: Rivaroxabana de longa duração versus enoxaparina de curta duração para a prevenção de tromboembolismo venoso após artroplastia total do quadril: um estudo controlado randomizado, duplo-cego. Lancet 2008;372:31–39.
- Lassen MR, Ageno W, Borris LC, et ai; RECORD3 Investigadores: Rivaroxabana versus enoxaparina para tromboprofilaxia após artroplastia total do joelho. N Eng J Med 2008;358:2776–2786.
- Turpie AG, Lassen MR, Davidson BL, et ai; RECORD4 Investigadores: Rivaroxabana versus enoxaparina para tromboprofilaxia após artroplastia total do joelho (RECORD4): um estudo randomizado. Lancet 2009; 373: 1673-1680.
- Ericksson BI, Kakkar AK, Turpie AG, et al: Rivaroxabana oral para a prevenção de tromboembolismo venoso sintomático após artroplastia eletiva de quadril e joelho. J Bone Joint Surg Br 2009;91:636–644.
- Rosencher N, Liau JV, Mueck W, Loewe A, Berkowitz SD, Homering M: Incidência de hematoma neuroaxial após cirurgia total de quadril ou joelho: programa RECORD (rivaroxabana vs, enoxaparina). Acta Anesthesiol Scand 2013;57:565–572.
- Samama MM: Qual teste usar para medir o efeito anticoagulante da rivaroxabana: o ensaio anti-fator Xa. J Thromb Haemost 2013;11:579–580.
- Raghavan N, Frost CE, Yu Z, et al: Metabolismo e farmacocinética do apixabano após administração oral a humanos. Drug Metab Dispos 2009;37:74–81.
- Frost C, Wang J, Nepal S, et al: Apixabana, um inibidor oral direto do fator Xa: segurança de dose única, farmacocinética, farmacodinâmica e efeito alimentar em indivíduos saudáveis. Br J Pharmacol 2013;75:476–487.
- Frost C, Nepal S, Wang J, et al: Segurança, farmacocinética e farmacodinâmica de múltiplas doses orais de apixabana, um inibidor do fator Xa, em indivíduos saudáveis. Br J Clin Pharmacol 2013;76:776-786.
- Zhang D, He K, Raghavan N, et al: Metabolismo comparativo de apixabano marcado com 14C em camundongos, ratos, coelhos, cães e humanos. Drug Metab Dispos 2009;37:1738–1748.
- Lassen MR, Davidson BL, Gallus A, Pineo G, Ansell J, Deitchman D: A eficácia e segurança do apixabano, um inibidor oral direto do fator Xa, como tromboprofilaxia em pacientes após artroplastia total do joelho. J Thromb Haemost 2007;5:2368–2375.
- Lassen MR, Rasskob GE, Gallus A, Pineo G, Chen D, Portman RJ: Apixabana ou enoxaparina para tromboprofilaxia após artroplastia de joelho. N Engl J Med 2009;361:594–604.
- Lassen MR, Raskob GE, Gallus A, Pineo G, Chen D, Hornick P; Investigadores ADVANCE-2: Apixabana versus enoxaparina para tromboprofilaxia após artroplastia de joelho (ADVANCE-2): um estudo randomizado duplo-cego. Lancet 2010;375:807–815.
- Lassen MR, Gallus A, Raskob GE, Pineo G, Chen D, Ramirez LM; Investigadores ADVANCE-3: Apixabana versus enoxaparina para tromboprofilaxia após artroplastia de quadril. N Engl J Med 2010;363: 2487–2498.
- Barrett YC, Wang Z, Frost C, Shenker A: Medição laboratorial clínica de inibidores diretos do fator Xa: o ensaio anti Xa é preferível ao ensaio do tempo de protrombina. Thromb Haemost 2010;104:1263–1271.
- Kozek-Langenecker SA, Fries D, Gutl M, et al: Anestesia locorregional e inibidores de coagulação. Recomendações do Grupo de Trabalho sobre Coagulação Perioperatória da Sociedade Austríaca de Anestesiologia e Medicina Intensiva. Anestesista 2005;54:476–484.
- Siegal DM, Curnutte JT, Connolly SJ, et al. Andexanet alfa para a reversão da atividade do inibidor do fator Xa. N Engl J Med 2015;373: 2413–242