Vivian HY Ip y Ban CH Tsui
INTRODUCCIÓN
La anestesia regional se ha convertido en un lugar común en muchas prácticas en todo el mundo debido a la creciente evidencia de los beneficios para el paciente, como la reducción de las complicaciones pulmonares y tromboembólicas, la reducción del consumo de opiáceos, así como la reducción del dolor y el tiempo hasta el alta y una mejor calidad de vida en el entorno inmediato. período postoperatorio. La creciente popularidad de la anestesia regional ha resultado en avances en técnicas y equipos. La práctica ha evolucionado desde el uso de la parestesia para la localización de los nervios hasta la estimulación nerviosa eléctrica y, actualmente, la ecografía. Este capítulo ofrece una descripción general del equipo disponible en la práctica de bloqueos de nervios periféricos. También describe el equipo necesario en varias etapas del procedimiento de anestesia regional para garantizar que se realice de manera eficiente y segura. La práctica de la anestesia regional comprende el equipo, los protocolos y las habilidades necesarias para garantizar que el bloqueo se realice de la manera más segura y sin problemas posible, antes, durante y después de administrar el bloqueo.
PREPARACIÓN Y MONTAJE DEL BLOQUE REGIONAL
Área y Monitoreo
Un ambiente tranquilo con todo el equipamiento necesario para realizar actividades regionales. anestesia, junto con medicamentos y equipos de reanimación a nuestro alcance, es de suma importancia. Una ubicación ideal es una sala de inducción donde se puede monitorear al paciente, premedicarlo y realizar el bloqueo regional antes de trasladarlo al quirófano. Se puede utilizar un área de bloque designada para proporcionar un entorno de procedimiento adecuado y monitoreado y al mismo tiempo optimizar la eficiencia del quirófano.
Al realizar el bloqueo, debe estar presente un asistente capacitado en anestesia regional para preparar y manejar el equipo y ayudar con el inyectado. El asistente también debe estar capacitado para realizar la reanimación si es necesario.
Independientemente del lugar donde se realice el bloqueo, es fundamental contar con todos los equipos, medicamentos y monitoreo disponibles. La mejor manera de reunir todo el equipo y los medicamentos necesarios es la instalación de un carro de almacenamiento (Figura 1), que debe estar bien etiquetado con los suministros fácilmente identificables.
Consejos NYSORA
- Un carro de equipo debe contener todos los medicamentos, agujas y catéteres necesarios para la anestesia regional, así como los medicamentos y el equipo de reanimación.
Zona de Bloques Equipamiento General
Los artículos de uso común deben almacenarse en el carro de almacenamiento y rellenarse cuando sea necesario. El carro de almacenamiento debe contener lo siguiente:
- Solución estéril para la preparación de la piel, esponjas/gasas, campo, rotulador, regla para la identificación de puntos de referencia, gel de ultrasonido, agujas hipodérmicas para la infiltración de la piel y extracción de dextrosa al 5 % (dextrosa al 5 % en agua, D5W).
- Una selección de sedantes, por ejemplo, midazolam (0.5 a 3 mg IV) y opioides de acción corta como fentanilo (50 a 100 μg IV) y propofol (20 a 100 mg IV) para bloqueos nerviosos que son más incómodos y requieren una sedación más profunda (p. ej., bloqueo del tobillo).
- Anestésicos locales y solución salina normal para la dilución del fármaco si es necesario. Los anestésicos locales se almacenan idealmente en un compartimento separado de los medicamentos intravenosos para evitar errores de medicación.
- Cánulas intravenosas. Todos los pacientes deben tener una cánula intravenosa insertada en caso de toxicidad del anestésico local.
- Apósitos para cánulas intravenosas, apósitos transparentes para cubrir el transductor de ultrasonido utilizado en bloqueos nerviosos de un solo disparo, cubierta de transductor, gel y apósitos para la inserción de catéteres de bloqueo nervioso.
Medicamentos de emergencia y equipo de reanimación
El uso de ultrasonido permite la visualización del inyectado y, por lo tanto, ha reducido significativamente, pero no eliminado, el riesgo de toxicidad sistémica severa por anestésicos locales (LAST). Sin embargo, el equipo de reanimación y los medicamentos siempre deben estar disponibles de inmediato en el área de bloqueo.
Equipo de reanimación
- Suministro de oxígeno, vías respiratorias nasales y máscaras de O2
- Vías aéreas orales de diferentes tamaños, máscaras laríngeas y tubos endotraqueales
- Laringoscopios (hojas Macintosh y Miller)
- Dispositivo de ventilación bolsa-mascarilla
- Succión
- Selección de cánulas intravenosas de varios tamaños
- Desfibrilador
Medicamentos de reanimación y dosis sugeridas por vía intravenosa
- Atropina (300–600 μg).
- Epinefrina (10–100 μg).
- Suxametonio (40–100 mg).
- Efedrina (5–15 mg).
- Fenilefrina (100–200 μg).
- Glicopirrolato (200–400 μg).
- Intralípido® 20 % (1.5 ml/kg durante 1 a 2 minutos como bolo inicial, que se puede repetir dos o tres veces para la asistolia persistente. Después del bolo, se puede iniciar una infusión a 0.25 ml/kg/min durante 30 a 60 minutos ; aumentar la velocidad de infusión para la hipotensión refractaria). Idealmente, Intralipid debe mantenerse en un recipiente con un protocolo de uso y equipo para preparar el medicamento.
Consejos NYSORA
- Durante el bloqueo de nervios periféricos guiado por ecografía, la visualización de la propagación del inyectado puede minimizar el riesgo de inyección intravascular. Nunca se debe inyectar la dosis completa de anestésico local sin ver la propagación del inyectado en la ecografía, ya que esto sugiere una inyección intravenosa.
Documentación
Una lista de verificación previa al bloqueo es fundamental para garantizar la ejecución correcta del bloqueo en el sitio apropiado del cuerpo del paciente e incluye la documentación de las condiciones preoperatorias (p. ej., déficits neurológicos y comorbilidades relevantes) y la discusión de los riesgos y beneficios y la obtención del consentimiento adecuado. En la mayoría de los países, se han establecido protocolos de documentación médica estandarizados para la inducción y el mantenimiento de la anestesia general. Esta documentación incluye información sobre la presión arterial, la frecuencia cardíaca, la oxigenación y detalles de los procedimientos comunes, como el mantenimiento del estado de las vías respiratorias y la intubación endotraqueal. Asimismo, existen pautas estándar similares para documentar la anestesia neuroaxial, que incluyen información sobre el nivel de bloqueo; provisiones de esterilidad; equipo y técnica utilizada; la incidencia de líquido cefalorraquídeo, sangre o parestesia; e inyección de anestésico local. Por el contrario, no existen tales directrices para documentar los bloqueos de nervios periféricos, aunque se utilizan de forma rutinaria en la práctica clínica y tienen las mismas implicaciones médico-legales que la anestesia general y neuroaxial. Una limitación de la falta de un protocolo de documentación para los bloqueos de nervios periféricos es la relativa escasez de información disponible para aquellos que deseen revisar retrospectivamente un procedimiento regional por motivos legales, de investigación o de control de calidad. Un ejemplo de documentación de bloque se ve en Figura 2 y XNUMX.
Se aborda más información sobre el seguimiento y la documentación de los PNB en “Monitoreo, Documentación y Consentimiento para Procedimientos de Anestesia Regional".
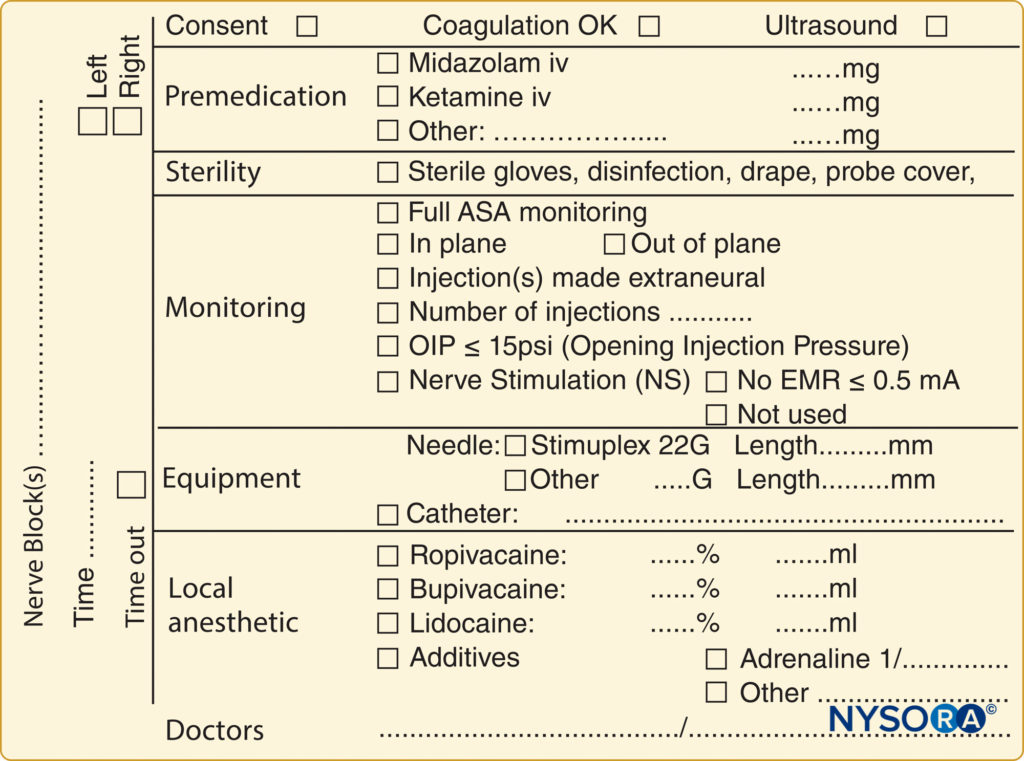
FIGURA 2. Un ejemplo de documentación en bloque como se usa en NYSORA-Europe CREER (Centro de Investigación, Educación y Recuperación Mejorada) en ZOL (Ziekenhuis Oost-Limburg, Genk, Bélgica).
EQUIPOS PARA INDUCCIÓN DE ANESTESIA REGIONAL
Agujas para bloqueos nerviosos de un solo disparo
Actualmente, hay muchos tipos diferentes de agujas de bloqueo de nervios periféricos en el mercado. Las agujas aisladas se usan comúnmente con la estimulación nerviosa. Con la introducción de la ecografía, las agujas ecogénicas se han utilizado ampliamente para una mejor visualización. Las agujas disponibles en el mercado para bloqueos nerviosos de una sola inyección generalmente vienen con un tubo de extensión preinstalado para facilitar la aspiración y la inyección de D5W o anestésicos locales y cuentan con un accesorio hembra para la conexión a un estimulador nervioso. Se debe tener en cuenta que el cierre Luer para el tubo adjunto puede estar ocasionalmente suelto, lo que puede provocar una fuga del anestésico local inyectado, así como también del aire en la aspiración.
Diseño de punta de aguja
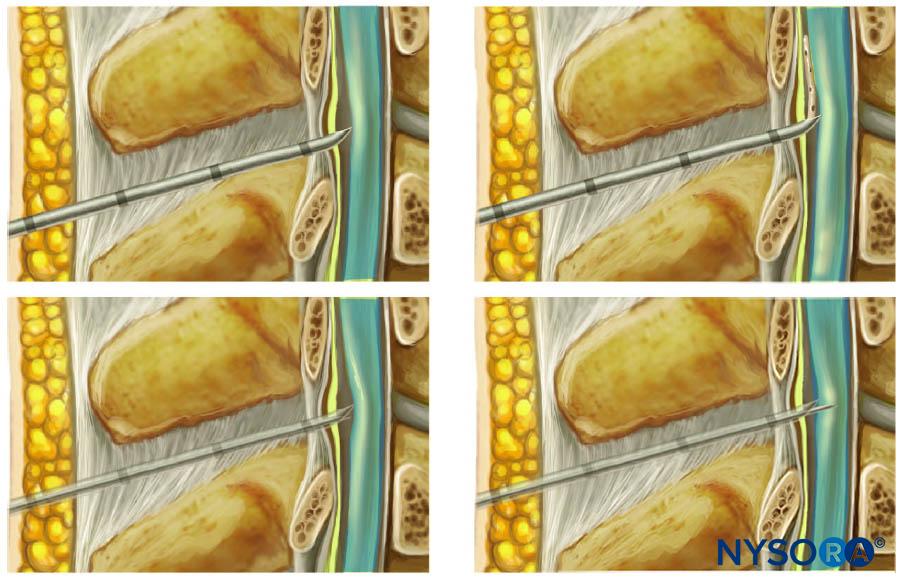
La lesión del nervio puede ser causada por la penetración directa del nervio o por el contacto forzado de la aguja con el nervio. El bisel de la aguja puede tener un impacto en la extensión del daño en la inserción de la aguja cerca de un nervio. Agujas de bisel corto (Figura 3 y XNUMX) puede tener la ventaja de reducir el daño nervioso causado por el corte o la penetración del nervio, mientras que se ha demostrado que las agujas de bisel largo (14°) tienen más probabilidades de penetrar el perineuro y causar lesión fascicular que las agujas de bisel corto (45°). aguja, especialmente cuando se orienta transversalmente a las fibras nerviosas. Por otro lado, las agujas de bisel corto pueden causar una lesión mayor en el caso de penetración de nervios o fasciculares. Las agujas romas que no cortan y las agujas Tuohy brindan una mejor retroalimentación y una mayor sensación del "chasquido" que se produce al perforar la fascia. Sin embargo, una aguja demasiado desafilada puede dificultar la punción de la fascia, lo que da como resultado una mayor presión aplicada y un posible "exceso" después de la punción de la fascia. Las agujas de punta de lápiz y Tuohy también pueden causar una mayor inflamación postraumática, daño a la mielina y hematoma intraneural.
Los bloqueos neuroaxiales se pueden realizar con agujas de diferentes estilos de punta. A pesar de su descripción como agujas atraumáticas, Whitacre o Sprotte (Figura 4 y XNUMX) puede ser traumático para los tejidos al entrar, con desgarro y ruptura severa de las fibras de colágeno (ver “Anatomía ultraestructural de las meninges espinales y estructuras relacionadas“). Esto contrasta con la aguja de Quincke, la llamada aguja de corte (Figura 4 y XNUMX), también utilizado para bloqueos neuroaxiales. Sin embargo, el consenso general es que los bloqueos neuroaxiales realizados con una aguja atraumática se asocian con un menor riesgo de cefalea pospunción dural.

FIGURA 4. Diferentes agujas para anestesia espinal: Whitacre (arriba), Sprotte (centro) y Quincke (abajo).
Longitud de la aguja
La elección de la longitud de la aguja depende del bloque específico. Por ejemplo, los bloqueos más profundos, como el bloqueo del nervio ciático, requerirán agujas más largas (p. ej., 100 a 120 mm). El uso de ultrasonido puede ayudar a determinar la distancia de la trayectoria hacia el nervio objetivo. Una aguja demasiado corta no alcanzará el sitio objetivo, mientras que una aguja larga puede ser difícil de maniobrar y puede avanzar demasiado. Las agujas deben tener marcas de profundidad (Figura 5 y XNUMX) para controlar la profundidad de penetración en el tejido. La longitud correcta de la aguja (la más corta posible) permitirá un mejor manejo y manipulación.

FIGURA 5. Aguja de bloqueo nervioso que muestra marcas en centímetros que se pueden usar como ejemplo para monitorear la profundidad de penetración. Los reflectores de piedra angular para ayudar en la visualización bajo ultrasonido también se pueden ver en el extremo distal.
Medidor de aguja
En general, las agujas aisladas de calibre 22 probablemente se utilicen más comúnmente para bloqueos de nervios periféricos de una sola inyección. Con el tamaño de la aguja, se debe buscar un equilibrio entre la comodidad del paciente y la flexión de la aguja a medida que perfora la piel. Debido a que las agujas más largas tienden a doblarse más fácilmente durante el avance y son más difíciles de manejar durante bloqueos profundos, es posible que se requiera una aguja de mayor calibre, ya que las agujas de menor calibre carecen de rigidez y se doblan más fácilmente. Las agujas de calibre más grande deben usarse con precaución, ya que se asocian con una mayor gravedad de la lesión tisular y el hematoma, mientras que las agujas de calibre más pequeño conllevan un riesgo más grave de que la punta se inserte intrafascicular. Además, la resistencia tiende a aumentar en la inyección con agujas de calibre más pequeño, y también lleva más tiempo aspirar la sangre si la punta es intravascular.
Agujas ecogénicas
Desde la introducción de los bloqueos de nervios periféricos guiados por ultrasonido, ha habido un esfuerzo por fabricar agujas con visibilidad mejorada en el ultrasonido. Las agujas ecogénicas reflejan los haces de ultrasonido a través de una variedad de mecanismos, incluido un recubrimiento especial que atrapa microburbujas de aire, ranuras cerca de la punta de la aguja o "puntos" ecogénicos hechos por reflectores de "piedra angular" (ver el extremo distal de la aguja en Figura 5 y XNUMX). Las agujas con ecogenicidad mejorada pueden reducir el tiempo de visualización durante los procedimientos guiados por ultrasonido. Una aguja ecogénica, con o sin dirección del haz de ultrasonido, se visualiza mejor en comparación con una aguja no ecogénica en ángulos de inserción de 60°–70°. Por el contrario, la aguja no ecogénica con dirección de haz fue más visible en un ángulo de inserción de 40° en comparación con la aguja ecogénica.
Conjuntos de catéteres continuos
La infusión continua de anestésico local ha demostrado ser eficaz para proporcionar analgesia posoperatoria a largo plazo en una variedad de entornos. Los catéteres de bloqueo de nervios periféricos también permiten la titulación de la medicación en alícuotas de dosis pequeñas. El equipo para bloqueos nerviosos periféricos continuos se analiza en detalle en “Equipos para Bloqueo Continuo de Nervios Periféricos“. Los conjuntos de catéter sobre aguja han ido ganando popularidad para administrar anestesia y analgesia regionales continuas y se analizan brevemente en este capítulo.
Históricamente, se ha reconocido bien que los catéteres perineurales están asociados con fugas y migración. Sin embargo, el diseño del sistema de catéter sobre aguja puede reducir estos obstáculos y ha renovado el interés en las técnicas regionales continuas. La diferencia entre este conjunto y los conjuntos tradicionales de catéter a través de la aguja es también la posición de la aguja en relación con el catéter, ya sea dentro o alrededor del catéter (Figura 6 y XNUMX). Con los conjuntos de catéter a través de la aguja, se deja un espacio entre la piel y el catéter al retirar la aguja. Por el contrario, la retirada de la aguja en el conjunto de catéter sobre aguja no afecta al ajuste perfecto del catéter en la piel porque la aguja está alojada dentro del catéter.
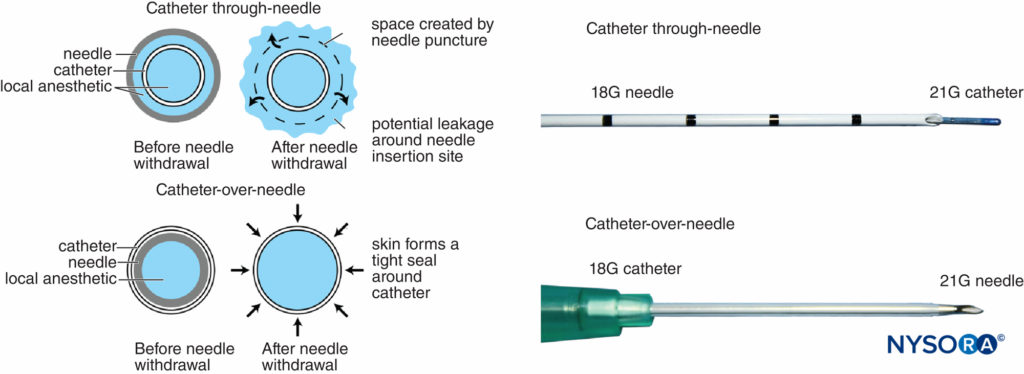
FIGURA 6. A la izquierda, esquema que muestra la diferencia entre los diseños tradicionales de catéter a través de la aguja (arriba) y catéter sobre aguja (abajo) con respecto al riesgo de fuga desde el sitio de punción de la piel. En el primero, el diámetro del orificio de la aguja es mayor que el diámetro del catéter, lo que deja espacio para que el anestésico local se filtre cuando se inyecta. En este último, el orificio de punción es más pequeño que el diámetro del catéter, lo que permite que la piel circundante sostenga firmemente el catéter. A la derecha, extremos distales diferentes de los conjuntos de catéter a través de la aguja (arriba) y catéter sobre aguja (abajo).
Hay algunas variaciones en este diseño que son comercializadas por diferentes marcas. Por ejemplo, el diseño de Contiplex (B-Braun Medical, Melsungen, Alemania) presenta el catéter sobre la aguja como una sola unidad (Figura 7 y XNUMX).

FIGURA 7. R: El conjunto de catéter sobre aguja Contiplex (B-Braun Medical, Melsungen, Alemania), que presenta una aguja larga cubierta por el catéter y un clip que se puede mover a lo largo de la aguja para facilitar la manipulación de la unidad. B: Componentes del catéter sobre aguja B. Braun: aguja con extensiones para estimulación nerviosa e inyección (arriba) y catéter con marcas de centímetros (abajo).
Otra variación es el kit E-Cath recientemente presentado (Pajunk MEDIZINTECHNOLOGIE GmbH, Geisingen, Alemania) con un diseño de "catéter dentro del catéter", que presenta dos componentes, la vaina exterior del catéter y el catéter interior flexible, que crean una unidad que no se dobla. (Figura 8 y XNUMX). El dispositivo inicial se asemeja a una cánula intravenosa, con una aguja dentro del catéter externo, que se inserta proximal al nervio objetivo bajo guía ecográfica. El extremo distal de la aguja sobresale por su propiedad de conducción eléctrica. Una vez en su lugar, la aguja se retira de la unidad, dejando el catéter externo in situ, y se inserta un catéter interno en el catéter externo para reemplazar la aguja y se bloquea con Luer en el lugar para la inyección (Figura 8 y XNUMX). El catéter interno reemplaza literalmente a la aguja, y la punta del catéter interno está esencialmente en el lugar exacto donde estaba la punta de la aguja antes de retirar la aguja.
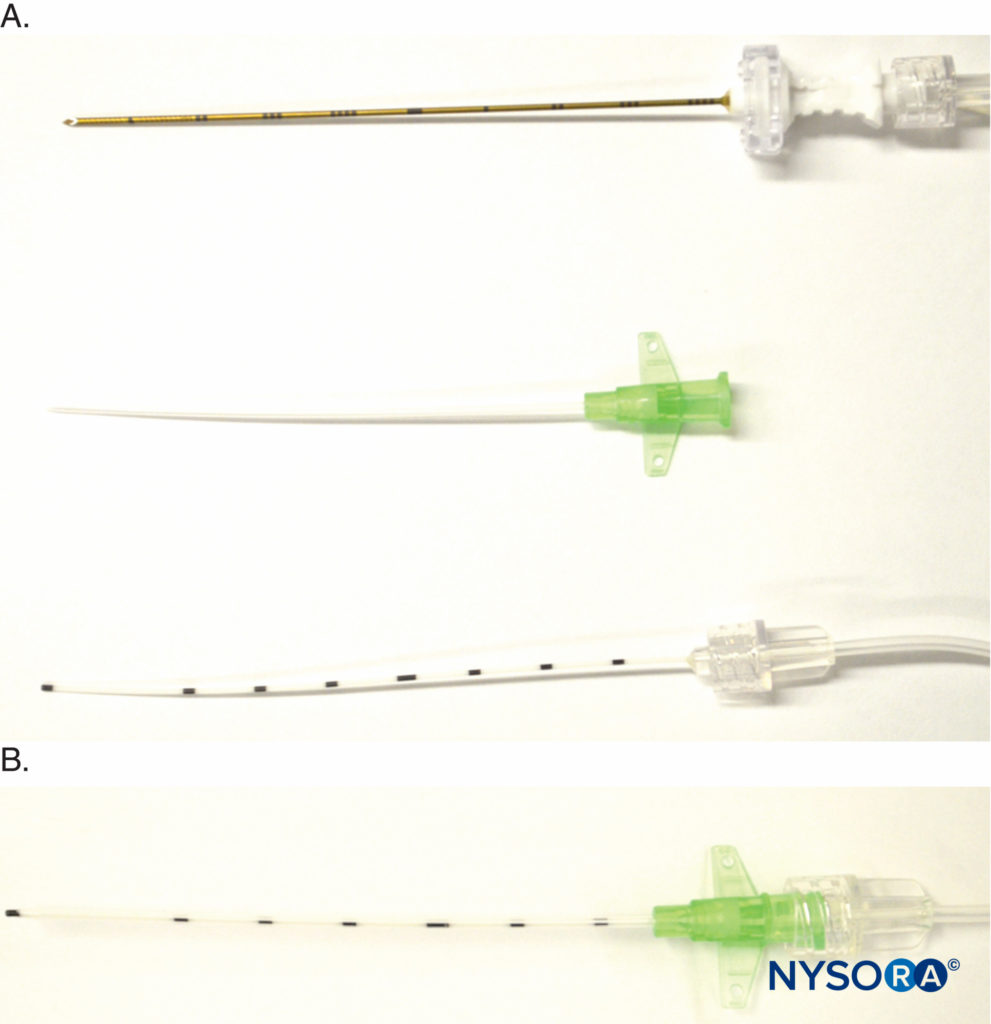
FIGURA 8. Detalle de componentes de catéter sobre aguja E-Cath (Pajunk MEDIZINTECHNOLOGIE GmbH, Geisingen, Alemania. A: Arriba, aguja con tubo de extensión para estimulador nervioso y un equipo de administración de fluidos; en el medio, el catéter se coloca sobre la aguja para crear un solo unidad que se inserta cerca del nervio objetivo; abajo, el catéter interno se inserta en el catéter externo luego de retirar la aguja una vez que la unidad de catéter sobre aguja está en la posición deseada. B: cierre Luer que mantiene unidos los catéteres interno y externo.
Varias ventajas del diseño de catéter sobre aguja incluyen el potencial:
- Fácil de usar con una técnica de inserción en comparación con la de un bloqueo nervioso de un solo disparo
- Menos fugas desde el sitio de inserción del catéter, por ejemplo, durante una cirugía de hombro cuando el paciente está sentado con posibilidad de contaminación del campo quirúrgico
- Menos riesgo de rotura del adhesivo del apósito
- Menos pasos y menos riesgo de desalojo
- Fácil visualización del catéter, especialmente de la punta del catéter
Dispositivos de localización de nerviosEstimuladores de nervios periféricos
Los estimuladores de nervios periféricos fueron el principal dispositivo de búsqueda de nervios en las décadas anteriores al uso generalizado de la guía por ultrasonido. El uso combinado de ultrasonido y estimulación nerviosa crea un método más objetivo para lograr bloqueos precisos y seguros al mismo tiempo que permite monitorear y visualizar la aguja de bloqueo y los objetivos en tiempo real. Con la introducción de la ecografía, el papel de los estimuladores nerviosos ha cambiado de la búsqueda de nervios a la monitorización del contacto de la aguja con el nervio o la colocación de la punta de la aguja intraneural. Además, la estimulación nerviosa se puede utilizar como técnica de confirmación y guía en la colocación de catéteres epidurales mediante la prueba de estimulación epidural eléctrica (Tsui). Las propiedades clave de los estimuladores nerviosos disponibles comercialmente se destacan brevemente a continuación (Figura 9 y XNUMX).
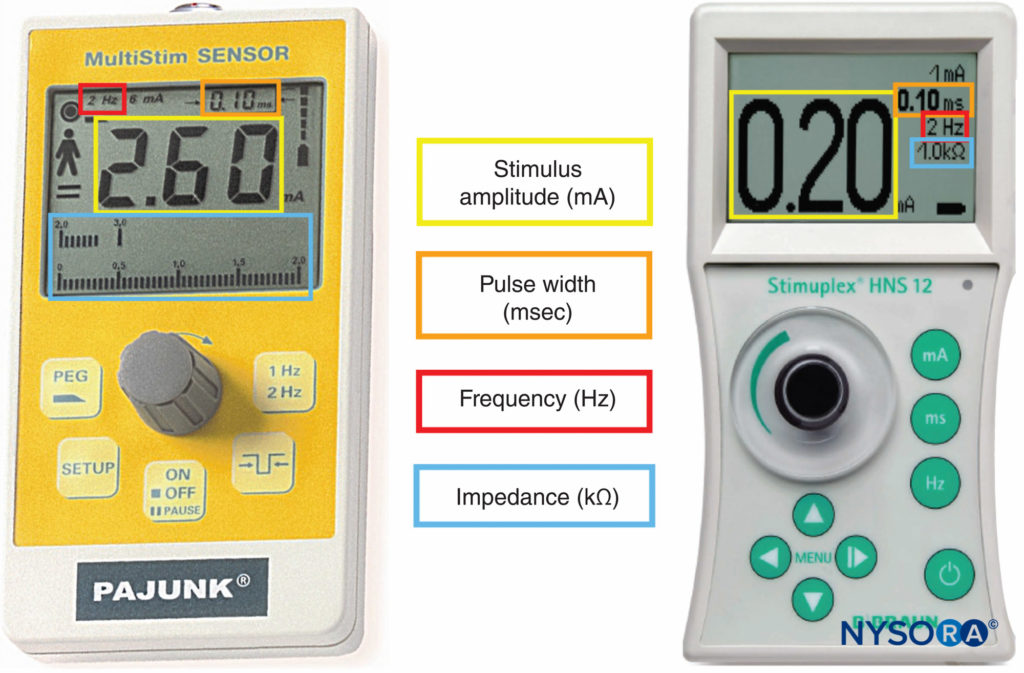
FIGURA 9. Estimuladores de nervios periféricos que permiten medir la amplitud del estímulo, el ancho del pulso, la frecuencia y la impedancia eléctrica.
Pantalla y salida de corriente constante
La mayoría de los modelos modernos ahora entregan corriente constante y la salida de corriente se puede configurar en frecuencia, ancho de pulso y miliamperios (mA) de corriente. La principal ventaja de un estimulador nervioso de salida de corriente constante es su capacidad para proporcionar una salida de corriente estable en presencia de resistencias variadas.
Pantalla
Una pantalla digital clara con una precisión de dos decimales es una característica importante del estimulador nervioso eléctrico. Esta pantalla debe indicar la corriente real suministrada al paciente y no simplemente el ajuste de corriente objetivo. Algunos estimuladores nerviosos están equipados con rangos de salida baja (hasta 6 mA) y alta (hasta 80 mA). El rango más bajo se usa principalmente para alertar sobre la posible colocación de una aguja intraneural, mientras que el rango más alto se usa principalmente para la prueba de estimulación epidural (1–10 mA).
Ancho de pulso variable
Los anchos de pulso cortos (es decir, 0.04 ms) son un mejor indicador de la distancia entre la aguja y el nervio, según los cambios en la corriente. Por el contrario, con anchos de pulso largos (es decir, 1 ms), hay poca diferencia en la corriente necesaria para estimular el nervio, independientemente de si la aguja estimulante está en contacto directo con el nervio oa 1 cm de distancia. Con un ancho de pulso de 0.04 ms, existe una gran diferencia en la corriente de estimulación necesaria cuando se compara el contacto directo con el nervio frente a una distancia de 1 cm.
El ancho de pulso también tiene un papel en el uso exitoso de la prueba de estimulación epidural eléctrica. Se debe utilizar el ancho de pulso adecuado para las diferentes aplicaciones de la prueba, ya sea un bloqueo periférico o neuroaxial. Tabla 1 resume el ancho de pulso apropiado para diferentes aplicaciones.
TABLA 1. Anchos de pulso para diferentes aplicaciones durante el bloqueo de nervios periféricos y el bloqueo neuroaxial.
| Ancho de pulso | Solicitud | Rango de umbral típico |
|---|---|---|
| 0.1 ms | Nervio periférico motor | Evitar < 0.3 mA |
| 0.2 ms | Espacio epiduralEspacio intratecal | 1–15 mA < 1 mA |
| 1 ms | Espacio epidural | 6 mA |
Polaridad claramente marcada de los electrodos
La polaridad de la aguja afectará su capacidad para estimular el nervio a una corriente determinada y debe estar claramente marcada. El cátodo (negro) se selecciona como electrodo estimulante porque es de tres a cuatro veces más efectivo que el ánodo para despolarizar la membrana nerviosa.
Frecuencia de pulso variable
La mayoría de los estimuladores nuevos tienen una opción para cambiar la frecuencia a la que se entrega el pulso eléctrico. Aunque algunos estimuladores de nervios periféricos disponibles comercialmente pueden permitir un ajuste de frecuencia de hasta 5 Hz, la frecuencia óptima del pulso eléctrico está entre 0.5 y 4 Hz. La mayoría de los usuarios seleccionan una frecuencia de 2 Hz. Cuando se utiliza una frecuencia más baja, como 1 Hz (un estímulo por segundo), la aguja debe avanzar lentamente para evitar perder el nervio entre estímulos.
Indicadores de desconexión y mal funcionamiento
La desconexión y el mal funcionamiento de los estimuladores nerviosos deben ser fácilmente detectables, y es esencial una indicación de la carga de la batería. La mayoría de los estimuladores nerviosos usan un cambio de tono o luz para advertir cuando el circuito no está completo y si no se puede administrar la corriente de pulso. El valor del cambio de tono/luz en la desconexión del circuito se demostró recientemente con un uso novedoso para un estimulador de nervios periféricos al guiar una aguja aislada con una punta no aislada en la luz traqueal para la topicalización de las vías respiratorias. El cambio de tono/luz indicaba si la punta estaba en contacto con el tejido (circuito cerrado) o suspendida en la tráquea llena de aire (circuito abierto) (Figura 10 y XNUMX).
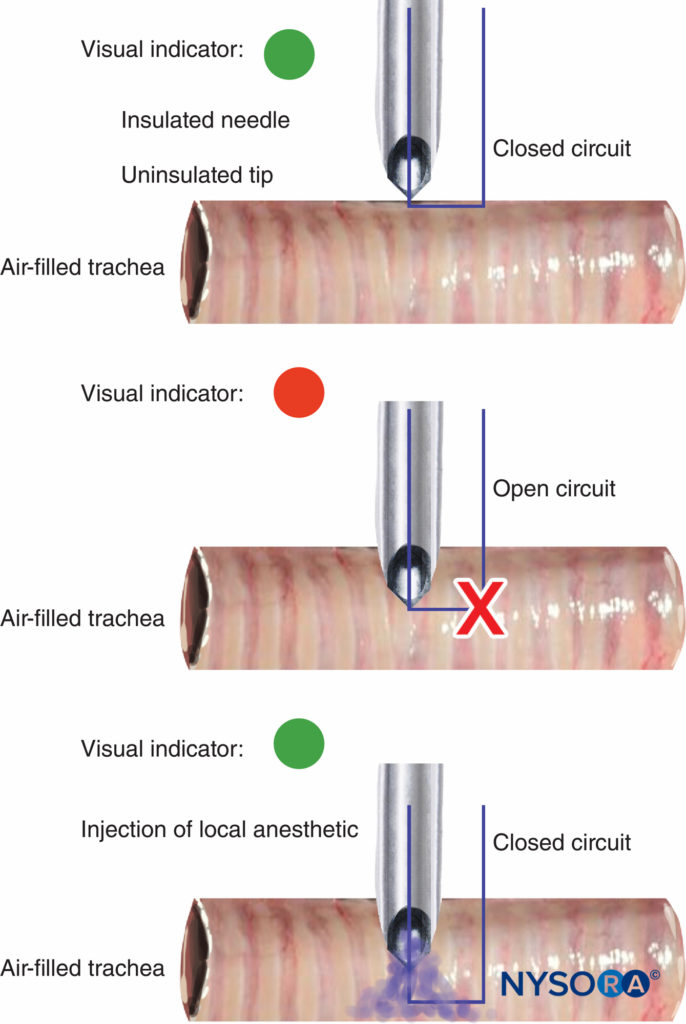
FIGURA 10. Cambio en la luz del estimulador de nervios periféricos y la señal de tono en la entrada de la punta de la aguja no aislada en la luz traqueal durante la topicalización de las vías respiratorias (superior y central). Con la inyección de anestesia local, la corriente eléctrica se cierra, provocando otro cambio de señal de luz/tono (abajo).
Impedancia eléctrica
Algunos estimuladores nerviosos modernos muestran la impedancia total entre la punta de la aguja y el electrodo de tierra. La importancia de esta propiedad en la monitorización de la colocación de la punta de la aguja intraneural se analiza en la sección sobre dispositivos de monitorización de este capítulo.
Otros Accesorios
Se puede usar una sonda para realizar la guía de electrodos percutáneos durante el mapeo de nervios de superficie (Figura 11 y XNUMX). Un pequeño control remoto de mano o pedal permite que un solo operador ajuste la salida de corriente de un estimulador nervioso sin un asistente, aunque esto rara vez se usa clínicamente (Figura 12 y XNUMX).

FIGURA 12. Dispositivos remotos controlados con la mano (izquierda) y con el pie (derecha) para ajustar la salida de corriente del estimulador nervioso.
Ultrasonido.
La introducción de la tecnología de ultrasonido ha revolucionado el campo de la anestesia regional, permitiendo visualizar estructuras nerviosas, agujas y otros objetos subcutáneos en tiempo real. El ultrasonido, sin duda, puede mejorar la seguridad y facilidad de realizar bloqueos nerviosos; sin embargo, esto depende en gran medida del operador.
Hay una serie de máquinas de ultrasonido portátiles disponibles en el mercado que son adecuadas para la anestesia regional (Figura 13 y XNUMX). Estas máquinas se pueden transportar fácilmente y la calidad y resolución de imagen son equivalentes o similares a las de las máquinas de ultrasonido estacionarias. El transductor (o sonda) es el elemento más importante de la máquina de ultrasonido; Los transductores de varias huellas y planos de haz están disponibles, lo que permite al usuario escanear la mayoría de las superficies en individuos con diferentes hábitos corporales. La calidad de las máquinas de ultrasonido mejora constantemente, con mejores opciones ergonómicas y facilidad de uso, una resolución más alta con transductores mejorados, portabilidad mejorada y reducción de costos.
Dispositivos de monitorización Monitorización para el paciente
Es importante aplicar un seguimiento de rutina a los pacientes sometidos a anestesia regional con o sin sedación. La toxicidad de la sobredosis de anestésico local y la inyección intravascular y la sobresedación son complicaciones potenciales de la anestesia regional. Por lo tanto, se debe estar atento con respecto a la monitorización del paciente. También se debe tener en cuenta que la toxicidad del anestésico local puede ocurrir dentro de la primera media hora después de la inyección del medicamento debido al pico de concentración plasmática (típicamente 20 a 30 minutos). La toxicidad sistémica de los anestésicos locales se analiza en detalle en otra parte.
El control general del paciente incluye examinar lo siguiente:
- Electrocardiograma
- Presión arterial no invasiva.
- Oximetría de pulso.
- Para la ventilación: La adecuación de la ventilación para la anestesia regional sin sedación se puede realizar mediante un seguimiento clínico cualitativo. Sin embargo, para los pacientes que requieren sedación, se debe usar la capnografía a menos que el paciente, el procedimiento o el equipo lo impidan.
Monitoreo de parestesia por inyección intraneural
Antes de la introducción de la tecnología de estimulación nerviosa, la parestesia era el único medio de localización nerviosa. Sin embargo, ha surgido evidencia que sugiere que la parestesia dolorosa puede provocar síntomas neurológicos persistentes y neuropatía. Por lo tanto, la mayoría de los médicos no solo abandonan la búsqueda de parestesia, sino que también, con pacientes despiertos o ligeramente sedados, utilizan la parestesia como una señal para advertir sobre la proximidad del nervio de la aguja.
Estimulación nerviosa eléctrica
El papel del estimulador nervioso ha cambiado desde la introducción del ultrasonido. En la mayoría de los casos, la estimulación nerviosa ya no se usa como herramienta principal para la localización de nervios, sino que se usa para monitorear y minimizar la inyección intraneural. Los estimuladores nerviosos permiten al usuario controlar dos propiedades electrofisiológicas durante la ejecución del bloqueo nervioso: el umbral de estimulación nerviosa y la impedancia eléctrica.
- Umbral de estimulación nerviosa: Un umbral de estimulación nerviosa de menos de 0.2 mA puede sugerir una ubicación intraneural de la punta de la aguja o un contacto entre la aguja y el nervio. Cuando se usa sola, la estimulación nerviosa carece de sensibilidad y, por lo tanto, debe usarse junto con otra monitorización, como se describe en esta sección. La observación de una respuesta motora indica la proximidad del nervio de la aguja con un umbral de corriente bajo; sin embargo, la falta de respuesta motora a un umbral de 0.2 mA o menos con un ancho de pulso de 0.1 ms no siempre descarta la colocación de la aguja intraneural.
- Impedancia eléctrica: Muchos estimuladores nerviosos modernos son capaces de medir la impedancia. En un circuito eléctrico, la corriente continua (DC) es el flujo de carga eléctrica en una sola dirección, mientras que la corriente alterna (AC) describe el flujo de carga eléctrica que invierte la dirección periódicamente. En la estimulación nerviosa, se utiliza CC pulsante. Debido a que la CC pulsante comparte características de las formas de onda de CA y CC, la resistencia eléctrica del circuito de estimulación nerviosa a menudo se denomina impedancia. La impedancia es muy sensible a la composición del tejido y varía según el contenido de agua del tejido. Debido a que existe una variación en el contenido de agua y lípidos entre los espacios intraneural y extraneural, teniendo el primero una cantidad considerablemente mayor de lípidos no conductores y menor contenido de agua, se ha demostrado una diferencia significativa en la impedancia intraneural y extraneural. Un estudio reciente en pacientes adultos también mostró que un aumento de la impedancia superior al 4.3 % puede indicar la colocación de una aguja intraneural. Además, la discriminación entre el tejido nervioso y otros tipos de tejidos se ha mejorado mediante la combinación de varias variables de impedancia en múltiples frecuencias de medición para aumentar la precisión. La impedancia eléctrica también cambia con la inyección intravascular y perineural de D5W. Por lo tanto, un cambio en la impedancia puede advertir contra la inyección en un lugar que podría causar daño a los nervios u otras secuelas.
Consejos NYSORA
- Un cambio repentino en la impedancia puede indicar que la aguja está ingresando a diferentes tejidos.
Imagen de ultrasonido
Con la creciente popularidad de la guía por ultrasonido para bloqueos de nervios periféricos, ha habido un malentendido común de que el ultrasonido puede ayudar a evitar la inyección intraneural. Para mejorar el margen de seguridad, la punta de la aguja debe visualizarse en todo momento durante el avance de la aguja durante una aproximación en el plano; sin embargo, esto puede ser un desafío, incluso en manos experimentadas. Además, existe una curva de aprendizaje significativa asociada con el uso de ultrasonido en anestesia regional, tanto con enfoques en el plano como fuera del plano. Cuando se usa un enfoque fuera del plano, el eje de la aguja podría confundirse con la punta, que estaría más abajo del haz de ultrasonido. Durante la inyección, la hinchazón del nervio como resultado de la inyección intraneural también puede ser difícil de notar en tiempo real. Además, cuando se nota la inflamación del nervio, puede ser demasiado tarde para prevenir la lesión del nervio, ya que solo se necesita un volumen minúsculo de anestésico local para romper el perineurio cuando la aguja se coloca intrafascicular. Finalmente, la resolución de ultrasonido actual no es lo suficientemente alta para reconocer la inyección intrafascicular, el evento más severo en términos de daño nervioso. Como tal, se siguen informando lesiones nerviosas con bloqueos de nervios periféricos a pesar del uso de ultrasonido. Se estima que la tasa de parestesia residual o entumecimiento después del bloqueo de nervios periféricos guiado por ecografía es del 0.18 % al 16 %. Por lo tanto, el ultrasonido no debe usarse como el único dispositivo de guía, sino que debe usarse junto con otras modalidades de monitoreo para minimizar el riesgo de inyección intraneural.
Supervisión de la presión de inyección
El control de la presión de la inyección puede ayudar a distinguir la ubicación de la punta de la aguja en el tejido perineural frente al contacto entre la aguja y el nervio o la colocación de la aguja intrafascicular (es decir, perineural frente a intraneural-intrafascicular). Los resultados de varios estudios sugieren que la inyección a alta presión en el espacio intraneural, incluso con volúmenes pequeños, puede contribuir de manera importante a la lesión mecánica del tejido neurológico durante los bloqueos de los nervios periféricos. La justificación y la base del daño a los nervios por la inyección de alta presión son probablemente una combinación de lesión mecánica por ruptura del perineuro, lo que provoca interferencia con la microcirculación endoneural, y lesión química por la neurotoxicidad de los anestésicos locales.
Usando modelos caninos, se demostró que la alta presión de inyección (>20 psi) puede provocar daño neurológico persistente indicativo de inyección intrafascicular. Sin embargo, no todas las inyecciones intraneurales dan como resultado una presión de inyección alta y un déficit neurológico posterior. Esto podría deberse a una inyección extrafascicular intraneural oa que la punta de la aguja biselada no está completamente dentro del nervio. En estos casos, el inyectado puede empujar el nervio fuera del camino, evitando una inyección de alta presión. Sin embargo, generalmente no se recomienda la inyección intraneural. También se ha demostrado que el contacto y el desplazamiento forzados entre la aguja y el nervio provocan cambios inflamatorios en los nervios. Dado que un estudio reciente demostró que la presión de inyección de apertura alta (≥15 psi), la presión que debe superarse antes de que pueda comenzar la inyección, puede ser indicativa de la colocación de una aguja intraneural, es importante monitorear cuidadosamente la presión de inyección durante la inyección del anestésico local. Además, la alta presión de inyección también puede causar una extensión neuroaxial no deseada durante ciertos bloqueos regionales cerca del neuroeje, por ejemplo, bloqueo del plexo lumbar o bloqueo del plexo braquial.
Consejos NYSORA
- Se ha sugerido que la presión de inyección de apertura debe mantenerse por debajo de 15 psi para mejorar la seguridad. La presión de apertura no depende del tamaño de la aguja, el tipo de aguja, la velocidad de inyección y el tamaño de la jeringa.
Los métodos para monitorear la presión de inyección incluyen lo siguiente: sensación de jeringa, manómetro de presión en línea y técnica de inyección de aire comprimido (CAIT).
- Sensación de jeringa. Tradicionalmente en la práctica clínica, se ha utilizado una técnica subjetiva de "sensación de jeringa" para evaluar la resistencia a la inyección de anestésico local y la realiza el anestesiólogo o el asistente mientras el anestesiólogo mantiene la posición correcta de la aguja. No hace falta decir que este enfoque subjetivo no es fiable y depende del operador. Las diferentes longitudes de aguja, diámetros y tipos de jeringas también afectan la sensación.
- manómetro de presión en línea. Dispositivos desechables objetivos disponibles comercialmente para medir la presión de inyección, como BSmart™ (B-Braun Medical, Melsungen, Alemania) (Figura 14 y XNUMX), muestra continuamente la presión durante la inyección, lo que permite a los médicos cuantificar la información de la presión de inyección, que se puede documentar. El manómetro está codificado por colores, de modo que cuando la presión es de 20 psi o más, el indicador estará rojo para advertir al operador. El monitor de presión en línea se coloca proximal a la aguja y en línea con el tubo no distensible. El otro extremo del monitor de presión se conecta directamente a la jeringa. El principio es el mismo que el de los sensores de presión en línea en dispositivos como las bombas de jeringa para el control continuo de la presión. El principio principal detrás del uso de un monitor de presión de inyección es que debe alcanzarse una cierta cantidad de presión de inyección (presión de apertura) antes de que pueda comenzar la inyección (el flujo del anestésico). La presión de apertura crítica necesaria para inyectar anestésico local cuando la aguja está en contacto con el nervio o es intrafascicular se ha estimado en varios estudios en más de 15 psi. Por lo tanto, si se detiene la inyección antes de alcanzar la presión de apertura y se inicia el flujo de anestésico, se puede evitar la inyección en una interacción vulnerable entre la aguja y el nervio.
- Técnica de inyección de aire comprimido. Esta es la aplicación clínica de la ley de Boyle (Presión × Volumen = Constante). A una temperatura constante, un volumen determinado de gas (aire) varía inversamente con la presión; por ejemplo, si el volumen del gas se reduce en un 50%, la presión aumentará de 1 atmósfera a 2 atmósferas. Esta técnica, diseñada por Tsui, consiste en aspirar una cantidad determinada de aire por encima de un volumen de inyectado dentro de una jeringa. Durante la inyección, el volumen de aire se comprime y se mantiene en un determinado porcentaje (Figura 15 y XNUMX).
Con una compresión de aire del 50%, la presión de inyección fue de 760 mm Hg o menos, muy por debajo del umbral de menos de 25 psi (1293 mm Hg). CAIT es una forma sencilla y práctica de estandarizar las presiones de inyección de anestésicos locales en tiempo real, asegurando que la presión de inyección esté constantemente por debajo del umbral y minimizando el riesgo de lesión nerviosa clínicamente significativa. Este método también reduce inevitablemente la velocidad de la inyección, lo que a su vez disminuye el riesgo de inyección intrafascicular o de desvío del anestésico local a planos de tejido no deseados. Las presiones generadas por CAIT también se mantienen constantemente estables durante todo el período de inyección, a diferencia de la técnica de sensación de jeringa, que produce picos de presión elevados. Esto probablemente se deba al efecto de "amortiguación" del volumen de aire, que amortigua la alta presión inicial.

FIGURA 14. Dispositivo de control de presión en línea desechable disponible en el mercado para controlar la presión de inyección durante el bloqueo de nervios periféricos (BSmart, BBraun Medical, Melsungen, GE).
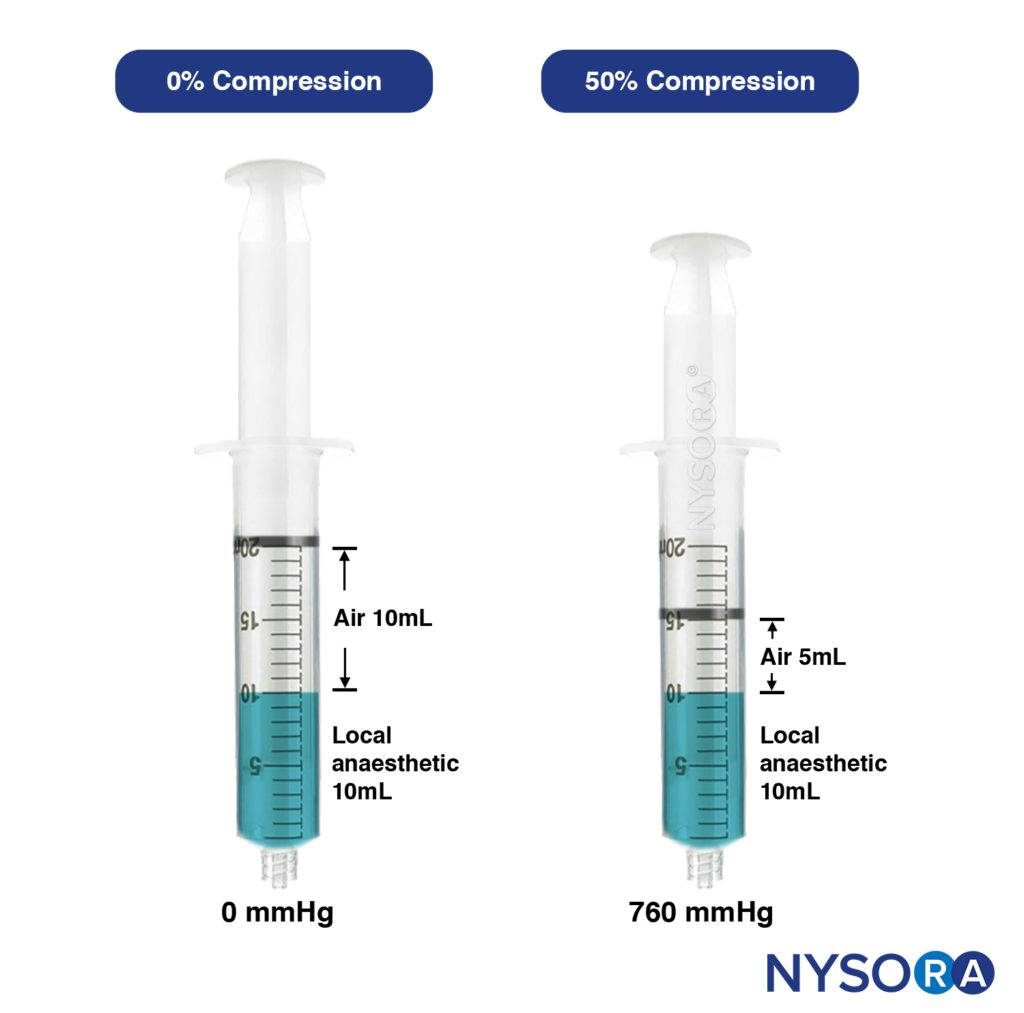
FIGURA 15. Jeringa izquierda: sin comprimir, que contiene 10 ml de aire y 10 ml de anestésico local. Jeringa derecha: El aire comprimido en un 50 % da como resultado una presión ejercida de 760 mmHg (aproximadamente 15 psi).
Consejos NYSORA
- En la era de los bloqueos de nervios periféricos guiados por ultrasonido, es importante no descartar el valor del estimulador nervioso y el control de la presión de inyección para minimizar el potencial de lesión nerviosa.
- Es importante utilizar una combinación de monitores para minimizar el riesgo de inyección intraneural, intrafascicular y traumatismo del nervio de la aguja.
EQUIPOS PARA LA GESTIÓN DE POSTblock
Herramientas de evaluación de bloques
Varias herramientas y técnicas están disponibles para monitorear el progreso de un bloque regional (Figura 16 y XNUMX). Idealmente, la herramienta o dispositivo de monitoreo debe ser lo más objetivo posible, pero debido a las diferencias fisiológicas entre las personas que reciben un bloqueo, esto rara vez ocurre. Hasta la fecha, no existe un consenso sobre cuál es el método más eficaz. Sin embargo, la mayoría de las herramientas de monitoreo de bloques generalmente ofrecen una interpretación aceptable de cuándo se logra la anestesia quirúrgica. De manera similar, las herramientas y escalas utilizadas para evaluar el bloqueo sensorial y motor varían mucho y ofrecen información subjetiva sobre el grado en que un bloqueo nervioso está logrando el objetivo deseado. Comúnmente, las escalas o puntajes de dolor se usan para indicar el nivel de comodidad de un paciente; Al igual que con las herramientas de monitoreo de bloques, estas escalas y puntajes brindan un medio más objetivo y reproducible para evaluar la gravedad del dolor.

FIGURA 16. Selección de equipo de monitoreo de bloqueo nervioso, incluidos dispositivos para medir el umbral de percepción actual (arriba a la izquierda), monofilamentos e hisopos con alcohol para percepción sensorial (abajo a la izquierda), dispositivo de escaneo infrarrojo (abajo a la derecha) y transductores de fuerza con capacidad de recopilación de datos inalámbrica (arriba Correcto).
Pruebas sensoriales (dermatomas)
Las herramientas de evaluación del bloqueo regional se basan en la suposición de que el paciente no podrá percibir un estímulo en el área bloqueada. Estos estímulos generalmente se basan en la temperatura (hielo, hisopo con alcohol), pero también se puede usar un filamento graduado para medir la disminución y el retorno de la sensación cutánea. En el caso de bloqueos troncales/neuraxiales, estos métodos pueden ayudar a determinar y seguir la propagación del bloqueo observando qué dermatomas responden al estímulo.
Grabación de temperatura/infrarrojos
Recientemente, la imagen térmica infrarroja también se ha probado como un medio para monitorear la progresión del bloqueo. Esta prueba se basa en el conocimiento de que la temperatura de la piel en los dedos aumenta después del bloqueo del plexo braquial. Los estudios mostraron que la termografía infrarroja de los dedos tenía un alto valor predictivo positivo para el éxito del bloqueo después de la anestesia del plexo braquial.
Umbral de percepción actual
El umbral de percepción de corriente (CPT) es un medio de aplicar corriente eléctrica a través de un electrodo percutáneo conectado a un generador de corriente especializado (por ejemplo, un neurómetro) para probar el nivel sensorial. Este método se ha utilizado para cuantificar los grados de neuropatía en condiciones como la diabetes mellitus. Recientemente, la reproducibilidad de este método se probó en voluntarios con resultados aceptables usando un estimulador de nervio periférico común. En este estudio, se utilizó un estimulador de nervios periféricos (consulte la discusión anterior) para aplicar un estímulo eléctrico en el área bloqueada; si la corriente necesaria para provocar una respuesta sensorial era mayor a lo largo del tiempo que la corriente de la línea de base (prebloqueo o región desbloqueada), esto era un indicador de la progresión del bloqueo. De hecho, un estudio posterior demostró que la CPT puede ser una herramienta objetiva y confiable para monitorear el inicio del bloqueo en escenarios clínicos.
Evaluación del dolor
Existen numerosas escalas de calificación del dolor validadas, siendo las más populares las variaciones en la escala de 0 a 10, donde 0 indica "ningún dolor en absoluto" y 10 indica "el peor dolor de todos". La escala de calificación numérica (NRS) y la escala analógica visual (VAS) son dos ejemplos de este tipo. Otras escalas de calificación del dolor, como la Escala de calificación del dolor de defensa y veteranos (DVPRS), presentan notas sobre cómo el dolor afecta la vida cotidiana que se pueden usar para definir con mayor precisión la gravedad del dolor. El DVPRS también presenta caricaturas faciales que se pueden usar para obtener comentarios sobre la gravedad del dolor de personas con capacidad de comunicación limitada. Para pacientes de edad avanzada, la Lista de verificación de evaluación del dolor para personas mayores con capacidad limitada para comunicarse (PACSLAC) se puede usar para evaluar el dolor en personas con demencia o deterioro cognitivo y que tienen problemas para comunicarse. Para los niños, hay disponible una variedad de escalas de dolor que se pueden usar para diferentes grupos de edad y habilidades de comunicación.
Evaluación del bloque motor
La herramienta de evaluación motora más común es la puntuación de Bromage, una escala de 4 puntos que va de 0 (movimiento completo) a 3 (bloqueo completo/sin movimiento). La puntuación de Bromage original se aplicó para los casos de bloqueo de las extremidades inferiores, pero también puede adaptarse a la evaluación del bloqueo de las extremidades superiores. Otro método más objetivo que puede evaluar el inicio y la recuperación de un bloqueo nervioso es la prueba de fuerza. Esto se puede realizar con un transductor de fuerza portátil: se le pide al paciente que ejerza fuerza contra el transductor con la extremidad o parte del cuerpo que ha sido bloqueada (p. ej., extensión del codo para evaluar la función del nervio radial).
Algunos transductores de fuerza modernos vienen equipados con una memoria de bus serie universal (USB) que, junto con una computadora portátil, permite recopilar datos de fuerza de forma inalámbrica en tiempo real (Figura 16 y XNUMX).
Mantenimiento de Anestesia Regional
La práctica de la anestesia regional se ha basado en bombas de infusión para proporcionar un suministro continuo de anestésico local a través de un catéter perineural. Este método sigue siendo el método más popular de anestesia regional continua, pero los nuevos desarrollos en la tecnología y la práctica han permitido flexibilidad en la analgesia posoperatoria. Los métodos convencionales para bloqueos nerviosos continuos se analizan con más detalle en “Bloqueos nerviosos periféricos continuos: soluciones anestésicas locales y estrategias de infusión y Equipos para Bloqueo Continuo de Nervios Periféricos“; los nuevos desarrollos se tratan aquí brevemente.
Bolo intermitente
Además del régimen tradicional de infusión continua, se ha vuelto cada vez más popular el uso de bolos intermitentes para el manejo continuo del bloqueo nervioso periférico. Con su capacidad para apuntar a las estructuras nerviosas con precisión, la tecnología de catéter sobre aguja (consulte la discusión anterior) reduce en gran medida el riesgo de migración o desplazamiento del catéter. Una ventaja de los bolos intermitentes es que también se reduce el riesgo de toxicidad del anestésico local porque se evita la administración constante de anestésico local y, por lo general, se reduce la dosis total. Un régimen de bolo intermitente se puede lograr mediante un enfoque preprogramado o controlado por el paciente.
Consejos NYSORA
- Se deben considerar y seleccionar bombas que permitan la administración de bolos intermitentes así como la infusión continua.
- Debido a que las bombas de infusión serán mantenidas y transportadas por el paciente si son móviles, la bomba debe ser portátil y fácil de usar.
Avances futuros
Recientemente, se describió la emocionante perspectiva de controlar la infusión de anestésicos locales por control remoto. En este sistema, las bombas se configuraron para ajustarse a las necesidades del paciente en función de las respuestas a las preguntas sobre su control del dolor y, en caso de que fuera necesario cambiar la configuración, los médicos podían acceder a la información de la bomba a través de un servidor seguro de forma remota, evitando la necesidad de que una enfermera o un médico estén físicamente presentes.
CONCLUSIÓN
Con las mejoras en la tecnología y el equipo, la anestesia regional ha pasado de ser un “arte” practicado por unos pocos a una “ciencia” que, con la capacitación y la experiencia adecuadas, puede ser practicada por muchos. Independientemente de quién realice el bloqueo o dónde se realice, existen varias pautas clave que deben seguirse para garantizar una anestesia regional segura y eficaz. Es esencial que haya un área designada para realizar bloqueos nerviosos y que todos los medicamentos y equipos estén fácilmente disponibles. La documentación cuidadosa del procedimiento de bloque debe ser el estándar de cada institución. La monitorización adecuada del paciente es esencial y debe incluir la monitorización estándar de ASA, así como la monitorización objetiva de la presión de inyección y el estimulador de nervios por ultrasonido para ayudar a prevenir lesiones en los nervios. El uso del equipo adecuado, incluida la longitud y el calibre adecuados de la aguja, resultará en una punción más fácil y precisa. Si se desea un bloqueo continuo, los nuevos conjuntos de catéter sobre aguja pueden ayudar a mitigar los problemas de los diseños tradicionales de catéter a través de aguja, y los desarrollos recientes en los métodos de administración de anestésicos locales a largo plazo, incluidos los bolos intermitentes y el control remoto, representan opciones valiosas. .
En resumen, la práctica actual de la anestesia regional depende de numerosas herramientas, métodos y equipos de monitorización. Aunque se necesita tiempo para adquirir la competencia adecuada con algunos de estos métodos y herramientas, son fundamentales para garantizar que el bloqueo regional se realice de la manera más segura y eficaz posible durante cada etapa del procedimiento.
Referencias
- van Lier F, van der Geest PJ, Hoeks SE, et al: La analgesia epidural se asocia con mejores resultados de salud de pacientes quirúrgicos con enfermedad pulmonar obstructiva crónica. Anestesiología 2011;115:315–3121.
- Davies J, Fernando R: Efecto de la ropivacaína sobre la función plaquetaria. Anestesia 2001;56:709–710.
- Richman JM, Liu SS, Courpas G, et al: ¿El bloqueo nervioso periférico continuo proporciona un mejor control del dolor que los opioides? Un meta-análisis. Anesth Analg 2006;102:248–257.
- Salviz EA, Xu D, Frulla A, et al: Bloqueo interescalénico continuo en pacientes sometidos a cirugía ambulatoria de reparación del manguito rotador: un ensayo prospectivo aleatorizado. Anesth Analg 2013;117:1485–1492.
- Sitios BD, Taenzer AH, Herrick MD, et al: Incidencia de toxicidad sistémica anestésica local y síntomas neurológicos posoperatorios asociados con 12,668 bloqueos nerviosos guiados por ultrasonido: un análisis de un registro clínico prospectivo. Reg Anesth Pain Med 2012;37(5):478–482.
- Cave G, Harvey M: Emulsión lipídica intravenosa como antídoto más allá de la toxicidad del anestésico local: una revisión sistemática. Acad Emerg Med 2009;16:815–824.
- Weinberg G, Ripper R, Feinstein DL, Hoffman W: La infusión de emulsión de lípidos rescata a los perros de la toxicidad cardíaca inducida por la bupivacaína. Reg Anesth Pain Med 2003;28:198–202.
- Weinberg, G: Regímenes de tratamiento. 2015. http://www.lipidrescue.org/.
- Abbal B, Choquet O, Gourari A, et al: Mejora de la agudeza visual con agujas ecogénicas en el bloqueo del plexo braquial axilar guiado por ultrasonido: un estudio aleatorizado, comparativo, observador ciego. Minerva Anestesiol 2015;81:369–378.
- Selander D, Dhuner KG, Lundborg G: lesión del nervio periférico debido a las agujas de inyección utilizadas para la anestesia regional. Un estudio experimental de los efectos agudos del traumatismo por punta de aguja. Acta Anaesthesiol Scand 1977;21:182–188.
- Selander D: Lesión del nervio periférico causada por agujas de inyección. Hermano J Anaesth 1993;71:323–325.
- Selander DE: Conferencia Labat 2006. Anestesia regional: Aspectos, pensamientos y algo de ética honesta; sobre biseles de agujas y lesiones nerviosas, y dolor de espalda después de la anestesia espinal. Reg Anesth Pain Med 2007;32:341–350.
- Mackinnon SE, Hudson AR, Llamas F, et al: lesión del nervio periférico por inyección de quimopapaína. J Neurosurg 1984;61:1–8.
- Steinfeldt T, Graf J, Schneider J, et al: Consecuencias histológicas del contacto entre la aguja y el nervio después de la estimulación nerviosa en un modelo porcino. Anesthesiol Res Pract 2011;2011:591851.
- Steinfeldt T, Werner T, Nimphius W, et al: Análisis histológico después de la punción del nervio periférico con punta de lápiz o punta de aguja Tuohy. Anesth Analg 2011;112:465–470.
- Reina MA, de Leon-Casasola OA, Lopez A, et al: Estudio in vitro de lesiones durales producidas por agujas Quincke y Whitacre calibre 25 evaluadas por microscopía electrónica de barrido. Reg Anesth Pain Med 2000;25:393–402.
- Castrillo A, Tabernero C, Garcia-Olmos LM, et al: Dolor de cabeza pospunción dural: impacto del tipo de aguja, un ensayo aleatorizado. Columna J 2015;15:1571–1576.
- Hammond ER, Wang Z, Bhulani N, et al: tipo de aguja y el riesgo de dolor de cabeza posterior a la punción lumbar en la clínica de neurología para pacientes ambulatorios. J Neurol Sci 2011;306:24–28.
- Uppal V, Sondekoppam RV, Ganapathy S: Efecto de la dirección del haz en la visibilidad de agujas ecogénicas y no ecogénicas: un estudio de laboratorio. Can J Anaesth 2014;61:909–915.
- Ip VH, Tsui BC: El conjunto de catéter sobre aguja facilita la administración de un segundo bolo de anestésico local para prolongar el bloqueo del plexo braquial supraclavicular sin pasos de cateterización que consumen mucho tiempo: un estudio controlado aleatorio. Can J Anaesth 2013;60:692–699.
- Tsui BC, Tsui J: Menos fugas y desplazamientos con un abordaje de catéter sobre aguja versus catéter a través de aguja para el bloqueo de nervios periféricos: un estudio ex vivo. Can J Anaesth 2012;59:655–661.
- Ip VH, Rockley MC, Tsui BC: El conjunto de catéter sobre aguja ofrece una mayor estabilidad y menos fugas en comparación con la contraparte tradicional en los bloqueos nerviosos interescalénicos continuos: un estudio aleatorizado y ciego del paciente. Can J Anaesth 2013;60:1272–1273.
- Ip V, Bouliane M, Tsui B: Contaminación potencial del sitio quirúrgico causada por fuga de un catéter interescalénico con el paciente en posición sentada: informe de un caso. Can J Anaesth 2012;59:1125–1129.
- Tsui BC, Ip VH: el método de catéter sobre aguja reduce el riesgo de dislocación del catéter perineural. Hermano J Anaesth 2014;112:759–760.
- Ip V, Tsui B. La seguridad de una técnica de catéter sobre aguja interescalénico. Anestesia 2013;68:774–775.
- Tsui BC, Gupta S, Finucane B: Confirmación de la colocación del catéter epidural mediante estimulación nerviosa. Can J Anaesth 1998;45:640–644.
- Green JS, Tsui BC: Uso de un estimulador nervioso para ayudar a la punción de la membrana cricotiroidea durante la topicalización de las vías respiratorias difíciles. Can J Anaesth 2015;62:1126–1127.
- Becker DE, Reed KL: Fundamentos de la farmacología anestésica local. Anesth Prog 2006;53:98–108.
- Bigeleisen PE, Moayeri N, Groen GJ: Umbrales de estimulación extraneural versus intraneural durante el bloqueo supraclavicular guiado por ecografía. Anestesiología 2009;110:1235–1243.
- Robards C, Hadzic A, Somasundaram L, et al: inyección intraneural con estimulación de baja corriente durante el bloqueo del nervio ciático poplíteo. Anesth Analg 2009;109:673-677.
- Chan VW, Brull R, McCartney CJ, et al: Un estudio ultrasonográfico e histológico de inyección intraneural y estimulación eléctrica en cerdos. Anesth Analg 2007;104:1281–1284, tablas.
- Byrne K, Tsui BC: conceptos prácticos en estimulación nerviosa: impedancia y otros avances recientes. Int Anesthesiol Clin 2011;49:81–90.
- Tsui BC, Pillay JJ, Chu KT, Dillane D: Impedancia eléctrica para distinguir la colocación intraneural de la aguja extraneural en los nervios porcinos durante la exposición directa y la guía por ultrasonido. Anestesiología 2008;109:479–483.
- Bardou P, Merle JC, Woillard JB, et al: Impedancia eléctrica para detectar punciones nerviosas accidentales durante bloqueos de nervios periféricos guiados por ecografía. Can J Anaesth 2013;60:253–258.
- Kalvoy H, Sauter AR: Detección de colocación de aguja intraneural con monitoreo de bioimpedancia de frecuencia múltiple: un método novedoso. J Clin Monit Comput 2106;30(2):185–192.
- Chin J, Tsui BC: Sin cambios en la impedancia tras la inyección intravascular de D5W. Can J Anaesth 2010;57:559–564.
- Cohen JM, Gray AT: Déficits funcionales después de la inyección intraneural durante el bloqueo interescalénico. Reg Anesth Pain Med 2010;35:397–399.
- Reiss W, Kurapati S, Shariat A, Hadzic A: Lesión nerviosa que complica el bloqueo del plexo braquial supraclavicular guiado por ultrasonido/electroestimulación. Reg Anesth Pain Med 2010;35:400–401.
- Hara K, Sakura S, Yokokawa N, Tadenuma S: Incidencia y efectos de la inyección intraneural no intencional durante el bloqueo del nervio ciático subglúteo guiado por ecografía. Reg Anesth Pain Med 2012;37:289–293.
- Sitios BD, Taenzer AH, Herrick MD, et al: Incidencia de toxicidad sistémica anestésica local y síntomas neurológicos posoperatorios asociados con 12,668 bloqueos nerviosos guiados por ultrasonido: un análisis de un registro clínico prospectivo. Reg Anesth Pain Med 2012;37:478–482.
- Liu SS, YaDeau JT, Shaw PM, et al: Incidencia de inyección intraneural no intencional y complicaciones neurológicas posoperatorias con bloqueos nerviosos interescalénicos y supraclaviculares guiados por ecografía. Anestesia 2011;66:168–174.
- Widmer B, Lustig S, Scholes CJ, et al: Incidencia y gravedad de las complicaciones debidas a bloqueos del nervio femoral realizados para cirugía de rodilla. Rodilla 2013;20:181–185.
- Bilbao Ares A, Sabate A, Porteiro L, et al: Complicaciones neurológicas asociadas al bloqueo interescalénico y supraclavicular ecoguiado en cirugía electiva de hombro y brazo. Estudio observacional prospectivo en un hospital universitario. Rev Esp Anestesiol Reanim 2013;60:384–391.
- Brull R, Hadzic A, Reina MA, Barrington MJ: Fisiopatología y etiología de la lesión nerviosa después del bloqueo del nervio periférico. Reg Anesth Pain Med 2015;40(5):479–490.
- Neal JM, Barrington MJ, Brull R, et al: El segundo aviso de práctica de ASRA sobre complicaciones neurológicas asociadas con anestesia regional y analgésicos: Resumen ejecutivo 2015. Reg Anesth Pain Med 2015;40(5):401–430.
- 46. Gadsden J, Latmore M, Levine DM, Robinson A: La presión de inyección de apertura alta se asocia con el contacto entre la aguja y el nervio y entre la aguja y la fascia durante el bloqueo del nervio femoral. Reg Anesth Pain Med 2016;41(1):50–55.
- Gadsden JC, Choi JJ, Lin E, Robinson A: La presión de apertura de la inyección detecta constantemente el contacto entre la aguja y el nervio durante el bloqueo del plexo braquial interescalénico guiado por ecografía. Anestesiología 2014;120(5):1246–1253.
- Hadzic A, Dilberovic F, Shah S, et al: La combinación de inyección intraneural y alta presión de inyección conduce a lesiones fasciculares y déficits neurológicos en perros. Reg Anesth Pain Med 2004;29:417–423.
- Kapur E, Vuckovic I, Dilberovic F, et al: Resultado neurológico e histológico después de inyecciones intraneurales de lidocaína en nervios ciáticos caninos. Acta Anaesthesiol Scand 2007;51:101–107.
- Gentili F, Hudson A, Kline DG, Hunter D: Lesión por inyección de nervio periférico: un estudio experimental. Neurocirugía 1979;4:244–253.
- Gentili F, Hudson AR, Hunter D, Kline DG: Lesión por inyección nerviosa con agentes anestésicos locales: un estudio con microscopia óptica y electrónica, microscopia fluorescente y peroxidasa de rábano picante. Neurocirugía 1980;6:263–272.
- Myers RR, Kalichman MW, Reisner LS, Powell HC. Neurotoxicidad de los anestésicos locales: Alteración de la permeabilidad perineural, edema y lesión de fibras nerviosas. Anestesiología 1986;64:29–35.
- Selander D, Brattsand R, Lundborg G, et al: Anestésicos locales: importancia del modo de aplicación, concentración y adrenalina para la aparición de lesiones nerviosas. Un estudio experimental de la degeneración axonal y el daño de la barrera después de la inyección intrafascicular o la aplicación tópica de bupivacaína (Marcain). Acta Anaesthesiol Scand 1979;23:127–136.
- Bigeleisen PE: la punción del nervio y la aparente inyección intraneural durante el bloqueo axilar guiado por ecografía no invariablemente resultan en una lesión neurológica. Anestesiología 2006;105:779–783.
- Steinfeldt T, Wiesmann T, Nimphius W, et al: El hematoma perineural puede provocar inflamación nerviosa y daño a la mielina. Reg Anesth Pain Med 2014;39(6):513–519.
- Steinfeldt T, Poeschl S, Nimphius W, et al: avance forzado de la aguja durante el contacto entre la aguja y el nervio en un modelo porcino: resultado histológico. Anesth Analg 2011;113(2):417–420.
- Gadsden JC, Lindenmuth DM, Hadzic A, et al: El bloqueo del plexo lumbar con inyección de alta presión conduce a la propagación contralateral y epidural. Anestesiología 2008;109:683–688.
- Orebaugh SL, Mukalel JJ, Krediet AC, et al: Inyección en la raíz del plexo braquial en un modelo de cadáver humano: distribución de la inyección y efectos en el neuroeje. Reg Anesth Pain Med 2012;37:525–529.
- Claudio R, Hadzic A, Shih H, et al: Presiones de inyección realizadas por anestesiólogos durante el bloqueo nervioso periférico simulado. Reg Anesth Pain Med 2004;29(3):201–205.
- Theron PS1, Mackay Z, Gonzalez JG, Donaldson N, Blanco R. Un modelo animal de "sensación de jeringa" durante el bloqueo de nervios periféricos. Reg Anesth Pain Med 2009;34(4):330–332.
- Tsui BC, Li LX, Pillay JJ: Técnica de inyección de aire comprimido para estandarizar las presiones de inyección en bloque. Can J Anaesth 2006;53: 1098–1102.
- Asghar S, Bjerregaard LS, Lundstrom LH, et al: termografía infrarroja distal y temperatura de la piel después del bloqueo del plexo braquial interescalénico guiado por ultrasonido: un estudio observacional prospectivo. Eur J Anaesthesiol 2014;31:626–634.
- Asghar S, Lundstrom LH, Bjerregaard LS, Lange KH: Bloqueo infraclavicular lateral guiado por ultrasonido evaluado por termografía infrarroja y temperatura de la piel distal. Acta Anaesthesiol Scand 2014;58:867–874.
- Masson EA, Veves A, Fernando D, Boulton AJ: Umbrales de percepción actuales: un método nuevo, rápido y reproducible para la evaluación de la neuropatía periférica en la diabetes mellitus. Diabetología 1989; 32:724–728.
- Matsutomo R, Takebayashi K, Aso Y: Evaluación de la neuropatía periférica mediante la medición del umbral de percepción actual con el neurómetro en pacientes con diabetes mellitus tipo 2. J Int Med Res 2005; 33:442–453.
- Nather A, Keng LW, Aziz Z, et al: Evaluación de la neuropatía sensorial en pacientes con problemas de pie diabético. Pie Diabético Tobillo 2011;2:6367. doi:10.3402/dfa.v2i0.6367
- Tsui BC, Shakespeare TJ, Leung DH, et al: Reproducibilidad del umbral de percepción actual con el Neurometer((R)) frente al estimulador de nervios periféricos Stimpod NMS450 en voluntarios sanos: un estudio observacional. Can J Anaesth 2013;60:753–760.
- Gaudreault F, Drolet P, Fallaha M, Varin F: La confiabilidad del umbral de percepción actual en voluntarios y su aplicabilidad en un entorno clínico. Anesth Analg 2015;120:678–683.
- Huskisson EC: escalas analógicas visuales. En Melczak R (ed): Medición y evaluación del dolor. Raven Press, 1983, págs. 33–37.
- Buckenmaier CC III, Galloway KT, Polomano RC, et al: Validación preliminar de la Escala de calificación del dolor de veteranos y defensa (DVPRS) en una población militar. Pain Med 2013;14:110–123.
- Fuchs-Lacelle S, Hadjistavropoulos T: Desarrollo y validación preliminar de la lista de verificación de evaluación del dolor para personas mayores con capacidad limitada para comunicarse (PACSLAC). Enfermeras de manejo del dolor 2004;5:37–49.
- Bromage PR. Analgesia epidural. Saunders, 1978.
- Byeon GJ, Shin SW, Yoon JU, et al: Métodos de infusión para el bloqueo interescalénico continuo del plexo braquial para el control del dolor posoperatorio después de la reparación artroscópica del manguito rotador. Korean J Pain 2015;28:210–216.
- Patkar CS, Vora K, Patel H, et al: Una comparación de la infusión continua y la administración en bolo intermitente de ropivacaína al 0.1 % con fentanilo al 0.0002 % para la analgesia epidural durante el trabajo de parto. J Anaesthesiol Clin Pharmacol 2015;31:234–238.
- Spencer AO, Tsui BC: Bolo intermitente a través de un catéter en el nervio infraclavicular utilizando una técnica de catéter sobre aguja en un paciente pediátrico. Can J Anaesth 2014;61:684–685.
- Macaire P, Nadhari M, Greiss H, et al: control remoto por Internet de la configuración de la bomba para bloqueos nerviosos periféricos continuos posoperatorios: un estudio de viabilidad en 59 pacientes. Ann Fr Anesth Reanim 2014;33:e1–e7.