INTRODUCTION
Le syndrome de loge est une urgence orthopédique. Il s'agit d'une affection aiguë des membres dans laquelle la pression de compartiments musculaires isolés ou groupés peu compliants augmente considérablement et limite la perfusion locale des tissus mous jusqu'au point d'atteinte motrice et sensorielle et de nécrose ischémique neuronale et tissulaire. Bien que l'on pense souvent que l'anesthésie régionale retarde le diagnostic et le traitement du syndrome aigu du compartiment (SCA), il n'existe que des rapports de cas isolés et un manque d'informations factuelles pour guider la pratique clinique.
Quoi qu'il en soit, les praticiens doivent être conscients des facteurs de risque du patient, de la présentation clinique et de la prise en charge de cette affection potentiellement menaçante pour les membres. Les structures musculo-squelettiques des membres sont enfermées dans des compartiments créés en investissant des couches fasciales avec une capacité limitée à s'étirer. Ces compartiments renferment les muscles squelettiques ainsi que les structures neurovasculaires qui traversent les compartiments. S'il n'est pas pris en compte, le syndrome des loges peut être une condition potentiellement mortelle.
Le syndrome des loges est plus fréquent dans la partie inférieure de la jambe et l'avant-bras, bien qu'il puisse également survenir dans la main, le pied, la cuisse et le haut du bras. En théorie, les muscles de la jambe supérieure présentent un risque de blessure plus faible que les muscles plus petits de la jambe inférieure, car les muscles de la cuisse peuvent dissiper les forces importantes d'un traumatisme direct, provoquant moins de blessures musculaires et d'œdème qui en résulte. Le syndrome du compartiment aigu survient plus fréquemment dans l'un des quatre petits compartiments de la partie inférieure de la jambe.
Les conséquences de pressions intra-compartimentales constamment élevées ont été décrites pour la première fois par Richard von Volkmann, qui a documenté des lésions nerveuses et des contractures musculaires tardives dues au syndrome des loges après une fracture supracondylienne de l'humérus distal. Jepson a décrit des contractures ischémiques dans les pattes postérieures du chien, résultant d'une hypertension des membres après une obstruction veineuse induite expérimentalement. Ce n'est qu'après environ 40 ans (depuis les années 1970) que l'importance de mesurer les pressions compartimentales est devenue évidente.
Étiologie
Toute condition pouvant réduire le volume du compartiment ou augmenter la taille du contenu du compartiment peut entraîner un syndrome de compartiment aigu. Des exemples de facteurs menant à ces changements sont présentés dans Tableau 1.
Physiopathologie
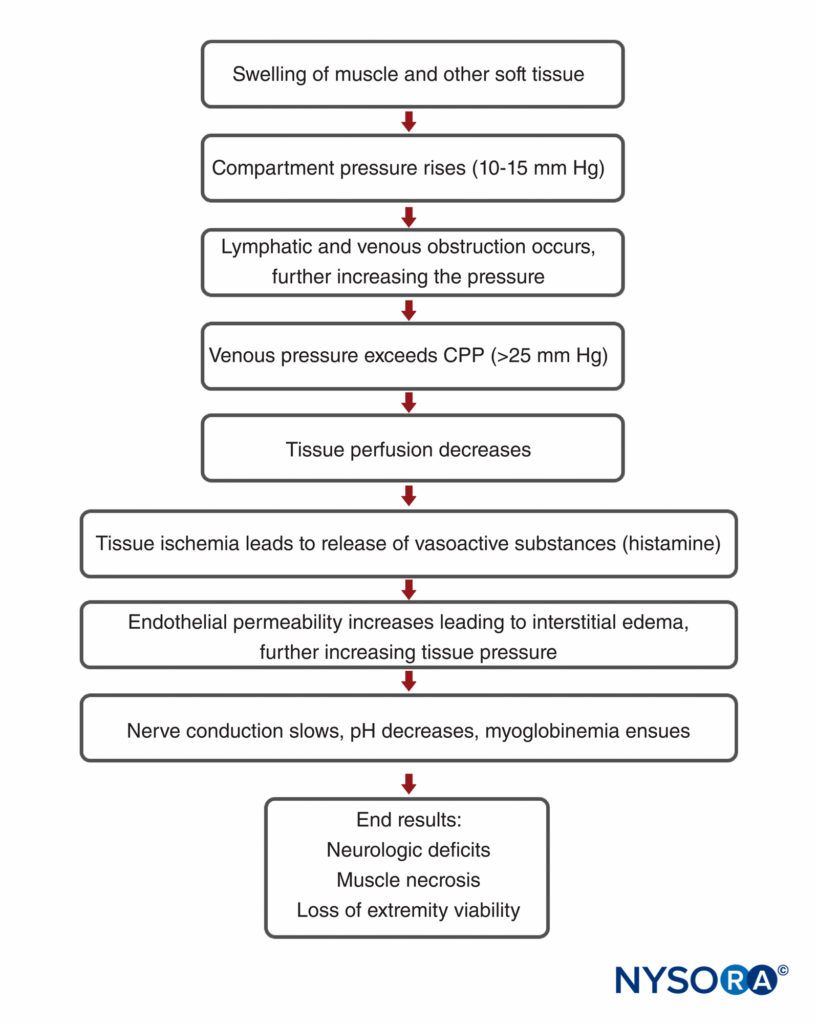
Le syndrome de loge est essentiellement une ischémie des tissus mous, généralement associée à un traumatisme, une fracture avec plâtre ultérieur, un malpositionnement prolongé pendant la chirurgie ou une lésion de reperfusion. Cependant, l'ensemble du mécanisme du syndrome des loges n'est pas clair. Étant donné que divers compartiments ostéofasciaux ont un volume relativement fixe, l'introduction d'un excès de liquide ou d'une constriction externe augmente la pression à l'intérieur du compartiment et diminue la perfusion tissulaire (Figure 1). Lorsque la pression compartimentale augmente, l'hypoperfusion tissulaire entraîne une hypoxie tissulaire entravant le métabolisme cellulaire. Si des lésions prolongées et permanentes du tissu myoneural se produisent. Dans des circonstances physiologiques, la pression veineuse dépasse celle de la pression du tissu interstitiel, soutenant l'écoulement veineux. Cependant, à mesure que la pression tissulaire augmente, la pression luminale veineuse extrinsèque est dépassée, entraînant un collapsus veineux. La pression à laquelle cela se produit n'est pas connue; cependant, il est généralement admis que les pressions compartimentales supérieures à 30 mm Hg nécessitent une intervention urgente car l'ischémie est imminente. Les lésions hypoxiques amènent les cellules à libérer des radicaux libres, ce qui augmente la perméabilité endothéliale. Ceci, à son tour, conduit à un cercle vicieux de perte continue de liquide, augmentant encore la pression tissulaire et les blessures. La diminution du flux sanguin vers les nerfs locaux se manifeste d'abord par des changements sensoriels.
TABLE 1. Facteurs conduisant au syndrome des loges.
| Conditions qui augmentent le volume du compartiment |
| • Traumatisme direct des tissus mous avec ou sans os long fracture (incidence de 10 % à 20 % après une fracture fermée) • Fractures fermées de la diaphyse tibiale (40 %) et avant-bras fermés fractures (12 %) • Lésions par écrasement des tissus mous sans fractures chez 23 % des cas de syndrome des loges5,6 • Les fractures ouvertes, qui devraient théoriquement décompresser les compartiments adjacents, peut conduire à compartiment syndrome7 • Hémorragie : lésion vasculaire, coagulopathie • Traitement anticoagulant8 • Revascularisation du membre après ischémie • Traumatisme à haute énergie, à partir d'un véhicule à moteur à grande vitesse accident ou blessure par écrasement • Augmentation de la perméabilité capillaire après brûlures (surtout circonférentiel) • Perfusions ou injections à haute pression (p. ex., blocs, pistolets à peinture) • Extravasations de liquide arthroscopique (p. ex., après arthroscopie du genou9) • Reperfusion après des périodes prolongées d'ischémie • Utilisation de stéroïdes anabolisants, entraînant une hypertrophie musculaire10 • Diminution de l'osmolarité sérique (p. ex., syndrome néphritique11) • Exercice intense, en particulier chez les personnes précédemment sédentaires personnes |
| Conditions qui entraînent une réduction du volume de Compartiments à tissus |
| • Pansements circonférentiels serrés (p. ex., peuvent survenir avec rembourrage en coton moulé seul) • Fermeture des défauts fasciaux12 • Plâtre ou attelle, surtout s'il est placé avant le retrait du garrot chirurgical • Compression prolongée des membres, comme dans Trendelenburg et positions de décubitus latéral6,13 ou chez les patients obnubilés de l'abus d'alcool ou de drogues • Traction excessive sur les membres fracturés14 |
Les paresthésies se développent dans les 30 minutes suivant le début de l'ischémie. Les lésions nerveuses irréversibles commencent après 12 à 24 heures d'ischémie totale. Des changements irréversibles dans les muscles commencent après seulement 4 à 8 heures, entraînant la mort des fibres musculaires et une myocontracture tardive.
DIAGNOSTIC DU SYNDROME DES COMPARTIMENTS
Le syndrome de loge est souvent un diagnostic basé principalement sur la variation des signes cliniques et des symptômes du patient lors d'examens séquentiels. Une douleur disproportionnée par rapport à la blessure, en particulier avec un étirement passif des muscles du compartiment ou du membre suspect, est l'un des indicateurs les plus significatifs.
Une extrémité palpable tendue par rapport au membre non blessé est également une découverte importante.
Cependant, aucun de ces signes avant-coureurs ne s'est avéré fiable. Les autres P classiques de pâleur, d'absence de pouls et de parésie ont une très faible valeur prédictive. En fait, la pâleur et l'absence de pouls sont rarement présentes dans le syndrome des loges, et au moment où la parésie se manifeste, les dommages sont en grande partie irréversibles. D'autre part, des accès douloureux paroxystiques chez un patient avec un bloc continu qui fonctionnait bien auparavant peuvent être un signe avant-coureur d'un SCA.
Perle clinique
• Une douleur disproportionnée par rapport à la blessure est un symptôme important.
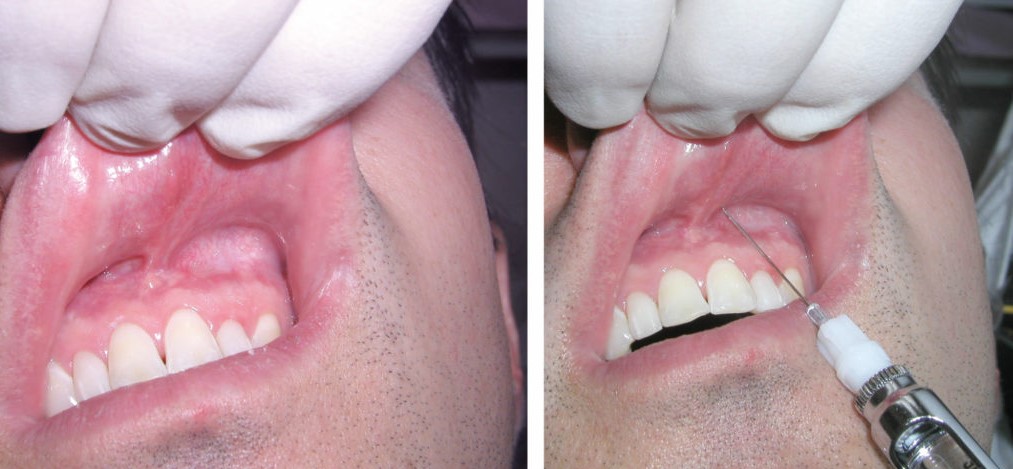
En général, l'établissement du diagnostic basé sur le seul jugement clinique peut être difficile. Au lieu de cela, le diagnostic doit être étayé par une mesure objective des pressions compartimentales à l'aide d'une aiguille et d'un transducteur de ligne artérielle ou d'autres appareils de mesure de la pression. En supposant que le bon compartiment est identifié, la mesure des pressions des tissus interstitiels reste la seule méthode de référence objective pour le diagnostic du SCA et est particulièrement utile chez le patient insensible, obnubilé ou anesthésié (Chiffres 2 et 3).
Une valeur absolue supérieure à 30 mm Hg chez le patient normotendu est compatible avec un syndrome des loges.
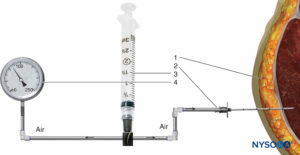
FIGURE 2. Mesure de la pression intramusculaire par la technique de Whiteside. (1) Aiguille intramusculaire, calibre 18. (2) Ligne de perfusion.(3) Seringue de 20 ml. (4) Manomètre à mercure.
Cette valeur est diminuée chez le patient hypotendu car la pression artérielle plus faible rend les membres encore plus sensibles aux lésions ischémiques. La spectroscopie proche infrarouge est une autre méthode non invasive suggérée pour surveiller la saturation en oxygène de l'hémoglobine et de la myoglobuline dans les tissus à risque (Figure 4). Plus récemment, la surveillance du pH intramusculaire a été introduite comme outil de diagnostic supplémentaire afin d'identifier avec précision le SCA.
Le membre supérieur
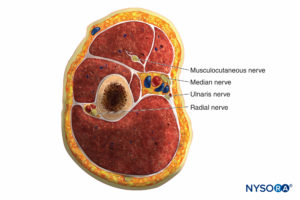
Il existe plusieurs compartiments du membre supérieur qui, lorsqu'ils sont blessés, peuvent entraîner un syndrome des loges nécessitant une fasciotomie du bras, de l'avant-bras ou de la main. Le bras a deux compartiments : antérieur et postérieur (Figure 5).
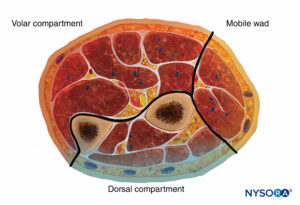
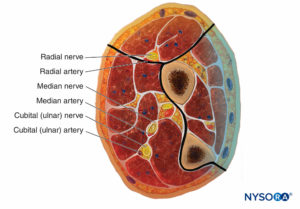
L'avant-bras comporte trois compartiments : les compartiments palmaire et dorsal et le compartiment contenant les muscles de la bourre mobile. Moubarak et al. ont démontré que ces compartiments sont interconnectés, contrairement aux compartiments de la jambe (Chiffres 6 et 7).
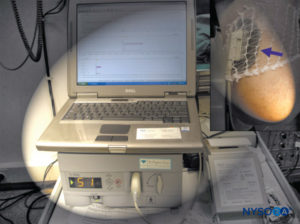
FIGURE 3. La spectroscopie proche infrarouge est une méthode non invasive pour surveiller la saturation en oxygène de l'hémoglobine et de la myoglobuline.
Par conséquent, la décompression du compartiment palmaire seul peut diminuer la pression dans les deux autres compartiments. Quoi qu'il en soit, la fasciotomie du compartiment dorsal doit toujours être effectuée si le compartiment dorsal reste tendu après la décompression palmaire. Les muscles du compartiment palmaire de l'avant-bras comprennent les fléchisseurs digitaux et du poignet et les pronateurs de l'avant-bras. Ces muscles sont testés par extension passive des doigts et du poignet et par supination de l'avant-bras.
Le compartiment dorsal de l'avant-bras contient les extenseurs des articulations métacarpo-phalangiennes du pouce et des doigts, les extenseurs ulnaires du poignet et les supinateurs de l'avant-bras et est testé par la flexion passive des doigts, du pouce et du poignet et par la pronation de l'avant-bras. La bourre mobile comprend le brachioradial et les deux extenseurs radiaux du poignet et est testée en flexion passive du poignet.
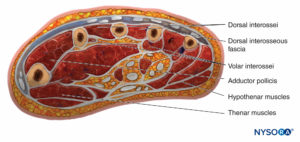
Il y a 10 compartiments dans la main, les plus importants étant les compartiments interosseux dorsal et palmaire, dont il y a respectivement quatre et trois (Figure 8). Les autres compartiments sont l'hypothénar, le thénar et l'adducteur. Le compartiment contenant le muscle adducteur du pouce est souvent négligé lors des fasciotomies. Des études utilisant le colorant Renografin n'ont montré aucune connexion entre les interosseux dorsaux et les autres compartiments, montrant que chaque compartiment doit être décomprimé séparément.
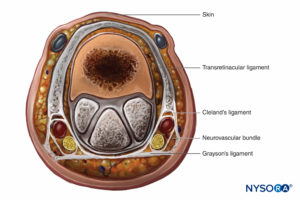
Le doigt est enfermé dans un fascia d'investissement serré et est compartimenté par le fascia et la peau palmaire au niveau du pli fléchisseur. Bien qu'aucun ventre musculaire ne soit éloigné des articulations métacarpo-phalangiennes, l'ischémie et l'engorgement peuvent entraîner une perte de tissu (Figure 9).
Le membre inférieur
Cuisse
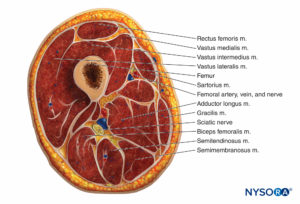
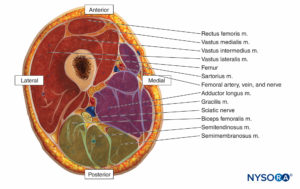
Les muscles de la cuisse sont divisés en trois compartiments investis par un fascia épais : l'antérieur, le médial et le postérieur (Chiffres 10 et 11). Parce que le syndrome du compartiment de la cuisse est rare, il peut passer inaperçu. Des antécédents d'utilisation d'anticoagulants sont fréquents chez les patients atteints du syndrome du compartiment de la cuisse.
Les signes et symptômes comprennent des antécédents de gonflement de la cuisse et/ou d'hématome et de douleur après une blessure mineure chez un patient sous anticoagulation. Bien que rare, le syndrome de la cuisse peut également survenir chez les patients après une chirurgie de remplacement articulaire. La combinaison d'un traumatisme mineur et d'une anticoagulation produit des saignements dans les espaces musculaires et tissulaires, entraînant une augmentation de la pression du compartiment. La douleur varie de légère à sévère et peut être déclenchée uniquement lorsque la hanche et le genou sont fléchis et étendus. Les autres signes d'occlusion vasculaire - perte de pouls, pâleur, paresthésies et paralysie - sont souvent absents.
Partie inférieure de la jambe
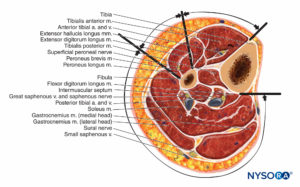
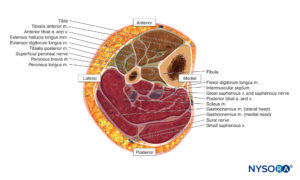
Le bas de la jambe contient quatre compartiments, chacun investi par un fascia inélastique (Chiffres 12 et 13). Chaque loge contient un nerf majeur : le péronier profond dans la loge antérieure, le péronier superficiel dans la loge latérale, le saphène dans la loge postérieure superficielle et le tibial dans la loge postérieure profonde. Un gonflement du compartiment latéral ou antérieur peut comprimer les nerfs péroniers profonds et superficiels contre le col du péroné.
Le nerf péronier superficiel se situe généralement dans l'intervalle entre les deux muscles péroniers sur une courte distance, puis émerge en avant du court péronier. Il perce le fascia de la loge latérale à la jonction du tiers moyen et distal de la jambe.
L'anatomie des loges postérieures superficielles et profondes est quelque peu variable, mais les deux loges, et en particulier la loge profonde, sont fréquemment impliquées dans le syndrome des loges.
Pied
Le pied a de nombreux compartiments liés de manière rigide, et même un léger saignement dans ces espaces peut augmenter considérablement les pressions (Figure 14). Selon Manoli et Weber, il y a neuf compartiments dans le pied. Trois compartiments courent sur toute la longueur du pied (médial, latéral et superficiel).
Cinq compartiments sont contenus dans l'avant-pied (adducteur et quatre interosseux). La loge calcanéenne est confinée à l'arrière-pied mais communique avec la loge postérieure de la jambe. Ce compartiment contient le muscle carré et le faisceau neurovasculaire plantaire latéral. Les compartiments les plus pertinents sur le plan clinique sont les compartiments médial, central, latéral et interosseux.
Un large éventail de blessures peut entraîner le syndrome des loges du pied, les plus probables étant les blessures par écrasement, en particulier celles associées à de multiples fractures métatarsiennes.
Souvent, la seule méthode fiable de diagnostic est la suspicion clinique et la mesure des pressions intracompartimentales.
La perte du pouls tibial postérieur ou dorsal pédiatrique est notoirement peu fiable dans le diagnostic précoce du syndrome des loges. Les signes cliniques les plus précoces sont une ischémie musculaire et nerveuse et des douleurs. Bien que cette douleur puisse être confondue avec la douleur de la blessure elle-même, elle peut être exacerbée par une dorsiflexion douce et passive des orteils, qui étire les muscles intrinsèques du pied.
L'absence de sensation est généralement acceptée comme un signe important d'ischémie nerveuse, mais elle n'est pas fiable par rapport à une discrimination en deux points et un toucher léger sur la face plantaire du pied et des orteils.
Perle clinique
• La mesure de la pression des loges est le seul test objectif et précis pour diagnostiquer et surveiller le syndrome des loges.
La mesure de la pression des loges est le seul test objectif et précis pour diagnostiquer et enregistrer le syndrome des loges, en particulier parce que les changements de pression des loges peuvent précéder les signes cliniques du syndrome des loges.
Le compartiment central peut être mesuré en passant une aiguille entre le métatarsien et le muscle abducteur de l'hallux à la base du premier métatarsien. Le compartiment interosseux est mesuré dans deux positions en introduisant l'aiguille à travers les espaces intermétatarsiens, de préférence entre les deuxième et quatrième espaces de toile pour éviter les perforations de la dorsalis pedis dans la première région intermétatarsienne.
Le compartiment calcanéen ou quadratus est mesuré en insérant l'aiguille à 5 cm en distal et 2 cm en dessous de la malléole médiale et en avançant à travers le muscle de l'abducteur.
Syndrome de compartiment aigu et anesthésie régionale
Il existe un aspect médico-légal important du SCA et de son issue dans la pratique clinique ; dans 50 % de tous les cas et réclamations liés au SCA, les données montrent que les décisions sont rendues en faveur du plaignant (le patient). Plusieurs rapports de cas et séries de cas suggèrent que l'anesthésie régionale peut avoir retardé le diagnostic de SCA. En revanche, il existe également un certain nombre de cas et de revues suggérant que l'anesthésie régionale peut ne pas masquer un diagnostic rapide et, en fait, peut même faciliter la détection du SCA. Par conséquent, l'utilisation d'une technique d'anesthésie locorégionale face aux facteurs de risque de SCA reste controversée.
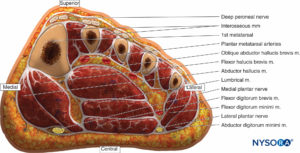
FIGURE 14. Coupe coronale du pied à travers la base des métatarsiens représentant les compartiments médial, central, latéral et interosseux.
Dans la littérature récente, des « règles de bonnes pratiques » ont été suggérées pour réduire le risque de manquer un syndrome de loge chez les enfants subissant une intervention chirurgicale avec anesthésie régionale périopératoire ; ces règles peuvent également s'appliquer aux adultes. Il convient de noter que bien que ces recommandations semblent succinctes, il s'agit en grande partie de considérations théoriques pour aider à guider la prise de décision clinique ; ils n'ont pas été mis à l'épreuve dans la pratique clinique.
Perle clinique
Lorsqu'une analgésie régionale est envisagée pour traiter les douleurs réfractaires chez les patients présentant un risque de syndrome des loges :
• Réduire la concentration des anesthésiques locaux (0.1 % à 0.25 % de bupivacaïne, lévobupivacaïne ou ropivacaïne) car des concentrations plus faibles sont moins susceptibles de masquer la douleur ischémique.
• Pour les perfusions continues de bupivacaïne, de lévobupivacaïne ou de ropivacaïne, les concentrations doivent être limitées à 0.1 %.
• Dans les chirurgies à haut risque de syndrome des loges (p. ex., chirurgie du compartiment tibial), il est conseillé de limiter à la fois le volume et la concentration.
• Les patients doivent faire l'objet d'un suivi attentif par les services de traitement de la douleur aiguë afin de permettre une détection précoce des signes et symptômes potentiels (h).
• Si un SCA est cliniquement suspecté, la mesure de la pression du compartiment sans délai est obligatoire.
TRAITEMENT DU SYNDROME DES COMPARTIMENTS
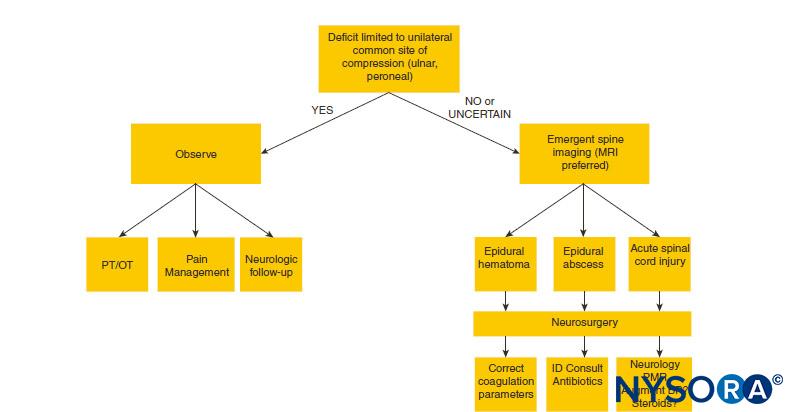
La fasciotomie d'urgence reste le traitement définitif pour un diagnostic de syndrome des loges en raison de ses résultats bien documentés qui sauvent les membres. Il est universellement accepté comme étant la meilleure chance de guérison complète et de prévention d'une nécrose tissulaire ultérieure. Le traitement repose principalement sur le tableau clinique associé à des mesures de pression compartimentale corroborantes (Figure 15). Le chirurgien doit procéder d'urgence à une fasciotomie de décompression lorsqu'elle est cliniquement indiquée, car la pression exacte à laquelle la fasciotomie doit être effectuée reste controversée. La plupart des études ont montré que la fasciotomie est indiquée lorsque la pression du compartiment atteint 30 mm Hg. La fasciotomie est également recommandée lorsque la pression du compartiment est inférieure à 30 mm Hg de la pression diastolique du patient.
Après une fasciotomie complète, il y a rarement un besoin de libérations supplémentaires. Les incisions de fasciotomie sont toujours laissées ouvertes et la fermeture de la plaie est retardée d'au moins 5 jours. Le patient est suivi cliniquement sauf s'il est anesthésié ou obnubilé, auquel cas des mesures régulières de la pression du compartiment doivent être effectuées.
Perle clinique
• La fasciotomie d'urgence reste le traitement définitif du syndrome des loges.
• Ses résultats en matière de préservation des membres en font une solution universellement acceptée comme la meilleure chance de guérison complète et de prévention d'une nécrose tissulaire ultérieure.
• La fasciotomie est indiquée lorsque la pression du compartiment atteint 30 mm Hg.
• Après la réalisation d'une fasciotomie complète, une libération supplémentaire est rarement nécessaire.
RÉSUMÉ
Une intervention chirurgicale prolongée, en particulier chez les patients subissant des interventions en position de Trendelenburg ou en décubitus latéral, présente un risque de syndrome des loges. La position de Trendelenburg nécessite
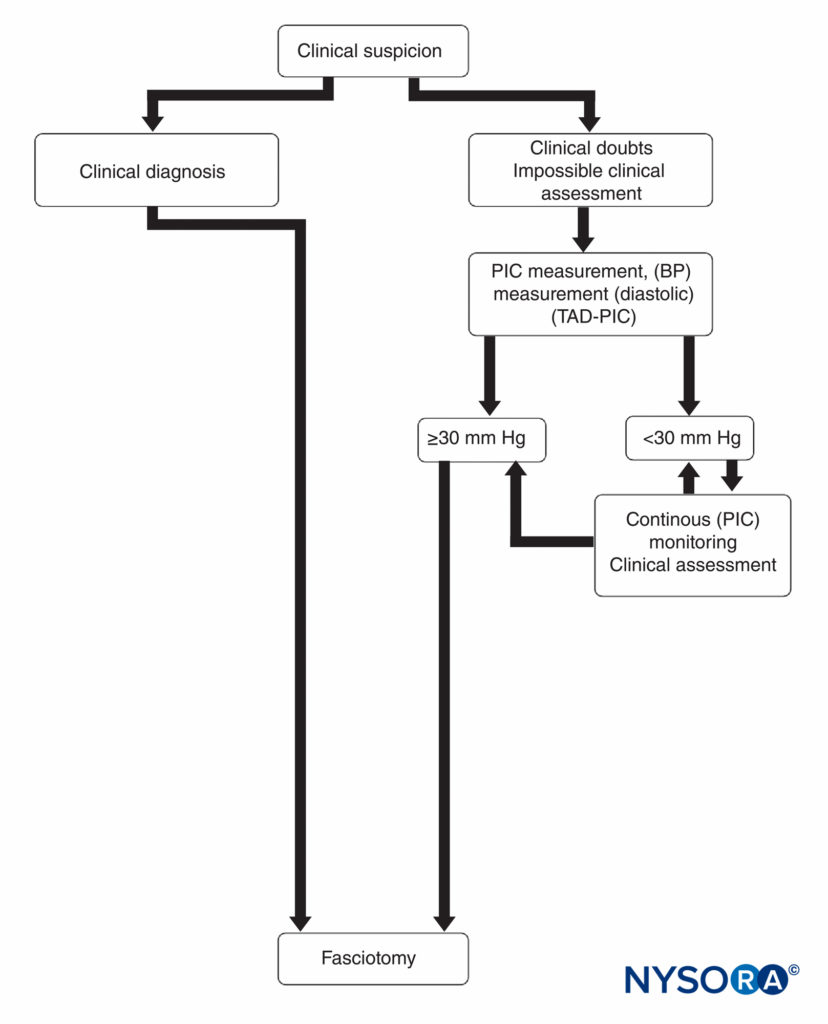
FIGURE 15. Diagnostic et prise en charge du syndrome des loges. TA, tension artérielle ; PIC, pression à l'intérieur du compartiment ; TAD-PIC, tension artérielle diastolique.
que les jambes sont sanglées à un niveau plus élevé que le cœur. Ceci peut être évité en repositionnant et redrapant les jambes, ou, si cela n'est pas possible, la position d'inclinaison tête en bas doit être inversée toutes les 2 heures afin que la reperfusion des membres inférieurs puisse se produire. En décubitus latéral, le bras en bas et la jambe en bas doivent être bien rembourrés pour éviter une compression excessive.
Lors d'une analyse récente des facteurs de risque, l'âge semble être un facteur prédictif important de développer un SCA (P < 0.001), avec la prévalence la plus élevée entre 12 et 19 ans et entre 20 et 29 ans. La profession et le type d'implant étaient les seuls autres facteurs qui restaient significatifs après ajustement pour l'âge.
Les patients sous anticoagulants ont tendance à présenter un risque élevé de syndrome du compartiment de la cuisse, même en cas de traumatisme relativement mineur ou d'interventions chirurgicales. Ce scénario clinique doit être abordé avec un indice de suspicion élevé.
En conclusion, l'utilisation de l'anesthésie régionale chez les patients à risque de syndrome des loges est controversée. Par conséquent, les blocs régionaux doivent être réalisés en concertation avec le patient et avec l'équipe chirurgicale. Lorsqu'elle est jugée bénéfique pour les soins aux patients, l'anesthésie régionale peut être utilisée lorsqu'elle est indiquée pour soulager une douleur intense; cependant, une gestion astucieuse, une surveillance des tissus du compartiment et peut-être des concentrations et des volumes plus faibles d'anesthésiques locaux doivent être envisagés.
Continuer la lecture: Complications et prévention des lésions neurologiques avec les blocs nerveux périphériques
Références
- Matsen F, Winquist R, Krugmire R : Diagnostic et prise en charge des syndromes de loge. J Bone Joint Surg 1980;62A:286.
- Schwartz J, Brumback R, Lakatos R : Syndrome aigu du compartiment de la cuisse : un spectre de blessures. J Bone Joint Surg 1989;71:392–400.
- von Volkmann R : Die ischamischen Kontakturen. Zentralbl Chir 1881 ; 8 : 801.
- Jepson P : Contracture ischémique, étude expérimentale. Ann Surg 1926; 68A:820.
- Matsen F : Syndrome compartimental. Un concept unifié. Clin Orthop 1975;113:8–14.
- Botte M, Santi M, Prestianni C, Abrams R : Contracture ischémique du pied et de la cheville : Principes de prise en charge et de prévention. Orthopédie 1996;19:235–244.
- Ziv I, Mosheiff R, Zeligowski A, et al : Blessures par écrasement du pied avec syndrome des loges : gestion immédiate en une étape. Cheville du pied 1989 ; 9 : 185–189.
- Whitesides T, Harada H, Morimoto K : La réponse du muscle squelettique à l'ischémie temporaire : Une étude expérimentale. J Bone Joint Surg 1971;53A : 1027–1028.
- McQueen M, Gaston P, Court-Brown C : Syndrome aigu des loges : qui est à risque ? J Bone Joint Surg 2000;82B:200–203.
- Ulmer T : Le diagnostic clinique du syndrome des loges du bas
jambe : les résultats cliniques sont-ils prédictifs de la maladie ? J Orthop Traumatologie
2002; 16: 572-577. - Shuler FD, Dietz MJ : capacité du médecin à détecter manuellement les
élévations de la pression intracompartimentale de la jambe. J Bone Joint Surg Am
2010; 92: 361-367. - Mc Queen MM. Syndrome aigu des loges. Dans : Bucholz RW, Court-Brown CM, Heckman JD, Tornetta P 3rd (eds) : Rockwood and Green's Fractures in Adults, 7th ed. Philadelphie : Lippincott Williams & Wilkins ; 2010 :689–708.
- Tighe PJ, Elliott CE, Lucas SD, et al : saturation en oxygène des tissus non invasifs déterminée par spectroscopie dans le proche infrarouge après un bloc nerveux périphérique. Acta Anesth Scand 2011;55:1239–1246.
- Elliott KG : Le pH intramusculaire comme nouvel outil de diagnostic pour les maladies aiguës
syndrome des loges : une étude clinique prospective [mémoire].
Aberdeen, Écosse : Université d'Aberdeen ; 2007. uk.bl.ethos.485671. - Gelberman R, Zakaib G, Mubarak S, et al : Décompression de l'avant-bras
compartiments. Clin Orthop 1978;134:225–229. - Allen M, Steingold R, Kotecha M : L'importance du compartiment palmaire
dans les blessures par écrasement à l'avant-bras. Blessure 1985;16:173–175. - Choyce A, Chan V, Middleton W, et al : Quelle est la relation entre
paresthésie et stimulation nerveuse pour bloc axillaire du plexus brachial ? Reg
Anesth Pain Med 2001 ; 26 : 100-104. - An H, Simpson M, Gale S, Jackson W : Syndrome aigu du compartiment antérieur de la cuisse : à propos d'un cas et revue de la littérature. J Orthop Trauma 1987;1:180–183.
- Manoli A II, Weber T : Fasciotomie du pied : Une étude anatomique avec
référence particulière à la libération du compartiment calcanéen. Cheville du pied
1990;10(6):267–275. - Sarraffian S : Anatomie du pied et de la cheville. Philadelphie : JB Lippincott, 1983.
- Myerson M : Décompression expérimentale du compartiment fascial du pied : la base de la fasciotomie dans les syndromes aigus du compartiment. Cheville du pied 1988 ; 8 : 308–314.
- Dunwoody J, Reichert CC, Brown KL : Syndrome de compartiment associé à la bupivacaïne et à l'analgésie péridurale au fentanyl en orthopédie pédiatrique. J Pediatr Orthop 1997;17:285–328.
- Hyder N, Kessler S, Jennings A, et al : Syndrome de compartiment dans une fracture de la tige tibiale manqué en raison d'un bloc nerveux local. Chirurgie de l'articulation osseuse J
1996 ; 78-B : 499-500. - Tang W, Chiu K : Syndrome du compartiment silencieux compliquant une arthroplastie totale du genou. J Arthroplasty 2000;15:241–243.
- Walker BJ, Noonan KJ, Bosenberg AT : Syndrome évolutif des loges
non masqué par un bloc nerveux continu. Reg Anesth Pain Med
2012; 3: 393-397. - Mar GJ, Barrington MJ, McGuirk BR : Syndrome aigu du compartiment du membre inférieur et effet de l'analgésie postopératoire sur le diagnostic. Br J Anaesth 2009;102:3–11.
- Cometa MA, Esch AT, Boezaart AP : Le blocage continu des nerfs fémoral et sciatique a-t-il obscurci le diagnostic ou retardé le traitement du syndrome aigu du compartiment inférieur de la jambe ? Un rapport de cas. Pain Med 2011;12:823–828.
- Kucera TJ, Boezaart AP : L'anesthésie régionale ne bloque pas systématiquement la douleur ischémique : deux autres cas et revue de la littérature. Douleur Médicale
2014; 15: 316-319. - Rauf J, Iohom G, O'Donnell B : Syndrome aigu du compartiment et anesthésie régionale - à propos d'un cas. Rom J Anaesth Int Care 2015;22 :
51-54. - Sermeus L, Boeckx S, Camerlynck HP, et al : syndrome du compartiment post-chirurgical de l'avant-bras chez un enfant. Acta Anaesthesiol Belg 2015;66 : 29–32.
- Aguirre JA, Gresch D, Ropovici A, et al : Scénario de cas : Syndrome de compartiment de l'avant-bras chez un patient avec cathéter infraclaviculaire. Anesthésiologie 2013 ;118 :1198–1205.
- Ivani G, Suresh S, Ecoffey C, et al : La Société européenne d'anesthésie régionale et de thérapie de la douleur et la Société américaine d'anesthésie régionale et de médecine de la douleur Conseil sur la pratique du comité consultatif sur les sujets controversés en anesthésie régionale pédiatrique. Reg Anesth Pain Med 2015;40:526–532.
- Mubarak S, Owen C : syndrome de compartiment et sa relation avec le syndrome d'écrasement : un spectre de maladies - un examen de 11 cas de compression prolongée des membres. Clin Orthop 1975;113:81–89.
- Whitesides T, Haney T, Morimoto K : Mesures de la pression tissulaire en tant que déterminant de la nécessité d'une fasciotomie. Clin Orthop 1975;113:43–51.
- Staudt JM, Smeulders MJ, van der Horst CM : Pressions normales du compartiment inférieur de la jambe chez les enfants. J Bone Joint Surg Br 2008;90 : 215–219.
- McQueen MM, Duckworth AD, Aitken SA, et al : prédicteurs du syndrome des loges après une fracture du tibia. J Orthop Trauma 2015;29 : 451–455.