Rishi M.Diwan
MANEJO DEL DOLOR AGUDO
INTRODUCCIÓN
El tratamiento y alivio del dolor constituye un derecho humano básico que existe independientemente de la edad. El dolor se define como una experiencia sensorial y emocional desagradable asociada con daño tisular real o potencial. La experiencia previa y el manejo del dolor, incluso desde etapas muy tempranas de la vida, alteran las respuestas y el comportamiento hacia más experiencias y eventos "dolorosos". Por lo tanto, no hay dos personas que experimenten el dolor de la misma manera, lo que se suma a la complejidad del manejo del dolor.
Desafortunadamente, incluso cuando el dolor es evidente, los niños con frecuencia no reciben tratamiento o reciben un tratamiento inadecuado para el dolor y los procedimientos dolorosos. Los recién nacidos y los niños gravemente enfermos son especialmente vulnerables a no recibir tratamiento o recibir un tratamiento insuficiente. La noción convencional de que los niños no responden ni recuerdan las experiencias dolorosas en la misma medida que los adultos es inexacta. Muchas de las vías nerviosas esenciales para la transmisión y percepción del dolor están presentes y funcionando entre las 24 y 29 semanas de gestación. La investigación en animales recién nacidos ha revelado que la falta de analgesia para el dolor da como resultado un "recableado" de las vías nerviosas responsables de la transmisión del dolor en el asta dorsal de la médula espinal, lo que resulta en una mayor percepción del dolor de futuras agresiones dolorosas. Esto confirma la investigación de recién nacidos humanos que encontró que la falta de anestesia o analgesia para la circuncisión del recién nacido resultó no solo en perturbaciones fisiológicas a corto plazo sino también en cambios de comportamiento a más largo plazo.
Tradicionalmente, a las enfermeras se les enseña o se les advierte que desconfíen de las órdenes de los médicos y de las solicitudes de control del dolor de los pacientes. La orden de prescripción más común para analgésicos potentes, "dar según sea necesario" (pro re nata, PRN), en realidad significa "dar con la menor frecuencia posible". La orden PRN también significa que el paciente debe saber o recordar pedir medicamentos para el dolor o que la enfermera debe poder identificar cuándo un paciente tiene dolor. Ningún requisito puede ser cumplido por niños con dolor. Los niños menores de 3 años y los niños gravemente enfermos pueden ser incapaces de verbalizar adecuadamente cuando sienten dolor o dónde les duele. Además, pueden tener miedo de informar su dolor. Varios estudios han documentado la incapacidad de enfermeras, médicos y padres/tutores para identificar y tratar correctamente el dolor, incluso en pacientes pediátricos postoperatorios.
Los temores sociales a la adicción a los opioides y la falta de apoyo también son factores causales en el tratamiento insuficiente del dolor pediátrico. A diferencia de los pacientes adultos, el manejo del dolor en los niños a menudo depende de la capacidad de los padres/tutores para reconocer y evaluar el dolor y de su decisión de tratarlo o no. Por lo tanto, los conceptos erróneos de los padres sobre la evaluación y el manejo del dolor también pueden dar como resultado un tratamiento inadecuado del dolor. Incluso en pacientes hospitalizados, la mayor parte del dolor que experimentan los niños es manejado por sus padres/tutores. Los padres/tutores pueden no informar el dolor porque no pueden evaluarlo o temen las consecuencias de la terapia del dolor. En un estudio, las creencias falsas sobre la adicción y el uso adecuado del paracetamol y otros analgésicos dieron como resultado que no se proporcionara analgesia a los niños. En otro, la creencia de que el dolor era útil o que las dosis repetidas de analgésicos provocaban un bajo rendimiento de la medicación hizo que los padres/tutores no proporcionaran o solicitaran los analgésicos prescritos para tratar el dolor de sus hijos. La educación de los padres/tutores es, por lo tanto, esencial si los niños van a recibir un tratamiento adecuado para el dolor.
Todos estos factores convierten a los niños en un grupo extremadamente vulnerable. Afortunadamente, en los últimos 25 años se han visto avances sustanciales en la investigación y el interés en el manejo del dolor pediátrico y en el desarrollo de servicios de dolor pediátrico, principalmente bajo la dirección de anestesiólogos pediátricos. Los equipos de servicios del dolor brindan tratamiento del dolor agudo, posoperatorio, terminal, neuropático y dolor crónico. Sin embargo, la evaluación y el tratamiento del dolor en los niños son aspectos importantes de la atención pediátrica, independientemente de quién la brinde. No proporcionar un control adecuado del dolor equivale a una práctica médica deficiente y poco ética.
EVALUACIÓN DEL DOLOR
La percepción del dolor es una experiencia subjetiva, consciente; operativamente, puede definirse como “lo que el paciente dice que duele” y existente “cuando el paciente dice que lo hace”. Los bebés, los niños preverbales y los niños de 2 a 7 años de edad pueden ser incapaces de describir su dolor o sus experiencias subjetivas. Esto ha llevado a muchos a concluir incorrectamente que los niños no experimentan el dolor de la misma manera que los adultos. Claramente, los niños no tienen que saber (o ser capaces de expresar) el significado de una experiencia para tener una experiencia. Por lo tanto, debido a que el dolor es esencialmente una experiencia subjetiva, cada vez es más claro que la perspectiva del dolor del niño es una faceta indispensable del manejo del dolor pediátrico y un elemento esencial en el estudio especializado del dolor infantil. A veces hay una confianza excesiva en las evaluaciones objetivas del dolor, ya sea de un profesional de la salud o de la evaluación de los padres o tutores. Esta evaluación objetiva, aunque a veces importante, debería seguir siendo solo un socio menor en la evaluación y el manejo del dolor, ya que las evaluaciones objetivas también están sujetas a sesgos y nociones preconcebidas. De hecho, la evaluación y el manejo del dolor son interdependientes, y uno es esencialmente inútil sin el otro. El objetivo de la evaluación del dolor es proporcionar datos precisos sobre la ubicación y la intensidad del dolor, así como la eficacia de las medidas utilizadas para aliviarlo o erradicarlo.
Actualmente existen instrumentos para evaluar el dolor en niños de todas las edades. De hecho, la sensibilidad y la especificidad de estos instrumentos han sido ampliamente debatidas y han dado lugar a una gran cantidad de estudios para validar su fiabilidad y validez. Los instrumentos más utilizados miden la calidad y la intensidad del dolor y son "medidas de autoinforme" que utilizan imágenes o descriptores de palabras para describir el dolor. La intensidad o severidad del dolor se puede medir en niños desde los 3 años de edad usando la escala de Oucher (desarrollada por Judith E. Beyer, RN, PhD; Antonia M. Villarreal, RN, PhD; y Mary J. Denyes, RN , PhD)—una escala de dos partes que incluye tanto una escala numérica (de 0 a 100) como una escala fotográfica de seis fotografías del rostro de un niño pequeño que expresa grados crecientes de incomodidad—o una escala analógica visual—una línea de 10 cm con un rostro angustiado y lloroso en un extremo y un rostro sonriente en el otro. La escala analógica visual ha sido validada tanto por sexo como por raza. En nuestra práctica, utilizamos la escala de calificación de dolor Wong-Baker FACES de seis caras (desarrollada por la Dra. Donna Wong y Connie M. Baker), principalmente debido a su simplicidad (Figura 1 y XNUMX). Esta escala se adjunta al registro de signos vitales y se instruye a las enfermeras para que la usen o una medida de autoinforme más apropiada para la edad siempre que se tomen los signos vitales.
Consejos NYSORA
- La evaluación regular utilizando las herramientas adecuadas de evaluación del dolor, involucrando al paciente y a los cuidadores en la toma de decisiones, y siendo lo más flexible posible a las necesidades del paciente, juegan un papel vital para lograr un resultado exitoso.

FIGURA 1. La escala de calificación del dolor Wong-Baker FACES de seis caras. (Fundación CARAS Wong-Baker (2015). CARAS Wong-Baker® Escala de valoración del dolor. Consultado el 28 de enero de 2017 con permiso de http://www.WongBakerFACES.or.)
La evaluación del dolor en niños preverbales plantea desafíos, ya que no pueden autoinformarse. Hay muchas herramientas de evaluación del dolor disponibles en este grupo de edad, pero ninguna es ideal. La escala de dolor CRIES se usa con frecuencia para calificar el dolor en los recién nacidos (Tabla 1). Los niños con retraso en el desarrollo, necesidades complejas o en cuidados intensivos necesitan herramientas especiales de evaluación del dolor para monitorear el dolor. La mayoría de estas herramientas incorporan parámetros fisiológicos para el estrés (cardíaco, respiratorio y endocrino) con cambios de comportamiento asociados con el dolor (expresiones faciales, llanto, movimientos corporales y de las extremidades). En nuestra institución se encuentra disponible una escala de evaluación del dolor separada llamada Pediatric Pain Profile (PPP) para uso en niños con necesidades complejas. Lo utilizan principalmente los padres/tutores para medir el dolor de su hijo e incorpora la puntuación de los cambios de comportamiento antes mencionados. Independientemente de la herramienta de evaluación del dolor utilizada en estos grupos de pacientes, es importante que los profesionales de la salud entiendan qué causa el dolor, aprecien que los pacientes pediátricos perciben el dolor y tengan una variedad de métodos de evaluación y tratamientos en su arsenal para lograr un control efectivo del dolor.
TABLA 1. Escala de dolor CRIES para bebés a partir de las 32 semanas de edad gestacional.
| 0 | 1 | 2 | |
|---|---|---|---|
| Llanto El grito característico de dolor es agudo. | No hay llanto o llanto que no sea agudo | Llanto agudo pero el bebé es consolable | Llanto agudo y el bebé está inconsolable |
| Requiere O2 para mantener SaO2 > 95 Considere otros cambios en la oxigenación | No | Requiere O2 < 30% | Requiere O2 > 30% |
| Aumento de los signos vitales Tome la PA en último lugar, ya que esto puede causar dificultades con otras evaluaciones. | FC y PA +/– 10 % del valor inicial | Aumento del 10 % al 20 % en la PA o la FC | > 20% de aumento en FC o PA |
| expresión Mueca caracterizada por abultamiento de la frente, ojos cerrados, boca abierta, surco nasolabial más profundo | Neutro | Mueca | mueca/gruñido |
| Insomnio Basado en el estado durante la hora anterior a la evaluación | No | Se despierta con frecuencia | constantemente despierto |
| Contiene: pescado (Tilapia). Cada una de las cinco categorías recibe una puntuación de 0, 1 o 2, lo que da como resultado una puntuación total entre 0 y 10. | |||
EL MANEJO DEL DOLOR
El tratamiento del dolor pediátrico agudo se caracteriza cada vez más por un enfoque multimodal o "equilibrado" en el que se administran dosis más pequeñas de analgésicos opioides y no opioides, como los medicamentos antiinflamatorios no esteroideos (AINE), los anestésicos locales, los antagonistas del N-metil-D-aspartato (NMDA) , y agonistas adrenérgicos α2, se combinan para maximizar el control del dolor y minimizar los efectos secundarios adversos inducidos por fármacos. El manejo del dolor también incluye el manejo de las expectativas del paciente y de los padres/tutores y ser informado, abierto y franco sobre qué esperar durante el transcurso de los períodos posoperatorio y de rehabilitación. Debe reconocerse que ciertos procedimientos “duelen” más que otros y que, a pesar de nuestros mejores esfuerzos, no siempre es posible lograr “no dolor”, aunque ese siempre debe ser el objetivo. Al mismo tiempo, la discusión preoperatoria de las diversas estrategias analgésicas disponibles y la seguridad de que el paciente "será atendido" contribuyen en gran medida a lograr un resultado satisfactorio para todos los involucrados. Además, un enfoque multimodal también utiliza terapias de medicina alternativa, complementaria y no farmacológica. Estas técnicas incluyen distracción, imágenes guiadas, estimulación nerviosa transcutánea, acupuntura, masaje terapéutico, entre otras.
Consejos NYSORA
- El objetivo del tratamiento del dolor agudo es proporcionar un período perioperatorio cómodo y sin dolor para facilitar la deambulación y la rehabilitación tempranas.
- Las discusiones preoperatorias con el paciente y sus padres/tutores que detallan el resultado alcanzable, el curso esperado y las diversas modalidades de manejo del dolor disponibles juegan un papel importante para lograr un resultado satisfactorio para todos los involucrados.
- Un enfoque multimodal para el manejo del dolor logra los mejores resultados.
- Si es posible, la anestesia/analgesia regional debe ser parte integrante de cualquier régimen de analgesia multimodal.
Consejos NYSORA
Terapia del dolor de medicina alternativa:
- Distracción
- Imágenes guiadas
- Estimulación nerviosa transcutánea
- Acupuntura
- Masaje TERAPEUTICO
El dolor de procedimiento es a menudo un aspecto olvidado e ignorado del manejo del dolor en los niños ingresados en el hospital. Diversas intervenciones y procedimientos, algunos de los cuales se realizan repetidamente, pueden infligir dolor o un niño ansioso los percibe como dolorosos (p. ej., canulación, flebotomía, punción lumbar y vendaje y limpieza de heridas). Es fundamental practicar cómo explicar los procedimientos y cómo preparar y tranquilizar al niño y a los padres/tutores. Las técnicas simples, como las cremas anestésicas locales y la terapia de juego/distracción, pueden ayudar en muchas situaciones. Algunos pacientes también pueden necesitar intervención y apoyo psicológico formal o ayudas farmacológicas como sedación u óxido nitroso (N2O), todo lo cual requiere tiempo y planificación. Por último, si se requiere sedación consciente o N2O, se debe disponer de inmediato de equipo de emergencia y monitoreo adecuado, incluidos oxígeno, succión y personal apropiado. (p. ej., acetaminofén/paracetamol, AINE y opioides “más suaves” como codeína o tramadol, si es necesario). Deben evitarse los opioides “fuertes”, aunque no están contraindicados. La anestesia regional guiada por ultrasonido es cada vez más popular y proporciona una anestesia regional más segura y eficaz.
Consejos NYSORA
Estrategias de manejo del dolor para cirugía ambulatoria:
- Infiltración de anestésico local
- Anestesia regional
- Analgésicos no opioides (paracetamol, AINE)
- Opiáceos suaves (codeína, tramadol) cuando sea necesario
- Se deben evitar los opioides más potentes cuando sea posible, pero no están contraindicados
Los anestesiólogos deben trabajar en estrecha colaboración con los colegas quirúrgicos para identificar las cirugías ambulatorias adecuadas y desarrollar vías de atención al paciente con planes estándar de manejo de la analgesia para procedimientos específicos.
Para cirugía mayor, además de todos los analgésicos mencionados anteriormente, pueden ser necesarias infusiones de opioides y/o anestésicos locales. Estos pueden complementarse con otras modalidades de tratamiento que incluyen ketamina, clonidina o diazepam para el espasmo muscular después de cirugías ortopédicas; gabapentina para el dolor agudo; magnesio intraoperatorio; y la adición de dexametasona sistémicamente oa un anestésico local para bloqueos nerviosos.
Analgésicos con actividad antipirética o analgésicos no opioides ("más débiles")
Los analgésicos “más débiles” o más leves con actividad antipirética, de los cuales el paracetamol, el ibuprofeno, el naproxeno y el diclofenaco son los ejemplos clásicos, conforman un grupo heterogéneo de AINE que son analgésicos no opioides (Tabla 2).
Proporcionan alivio del dolor principalmente al bloquear la producción de prostaglandinas periféricas y centrales mediante la inhibición de la ciclooxigenasa tipo I y II. Estos agentes analgésicos se administran principalmente por vía enteral por vía oral o rectal y son particularmente útiles para el dolor inflamatorio, óseo y reumático. El paracetamol administrado por vía parenteral y los AINE, como el ketorolaco, están disponibles para su uso en niños en quienes las vías de administración oral o rectal no son posibles. Desafortunadamente, independientemente de la dosis, los analgésicos no opiáceos alcanzan un "efecto techo", por encima del cual el dolor no puede aliviarse con estos fármacos por sí solos. Debido a esto, estos analgésicos más débiles se consideran los componentes básicos de un enfoque terapéutico multimodal y, a menudo, se administran en formas combinadas con opioides como codeína, oxicodona, hidrocodona o tramadol. La aspirina se ha abandonado en gran medida en la práctica pediátrica debido a su posible papel en el síndrome de Reye, sus efectos sobre la función plaquetaria y sus propiedades irritantes gástricas.
Consejos NYSORA
- Los analgésicos no opiáceos tienen un “efecto techo”, por encima del cual el dolor no se puede aliviar con estos fármacos por sí solos, independientemente de la dosis.
- Los analgésicos no opiáceos se consideran los componentes básicos de un enfoque terapéutico multimodal y, a menudo, se administran en formas combinadas con opiáceos como la codeína, la oxicodona, la hidrocodona o el tramadol.
El analgésico no opioide más utilizado en la práctica pediátrica sigue siendo el paracetamol. A diferencia de los AINE, el paracetamol funciona principalmente de forma central y tiene una actividad antiinflamatoria mínima, si es que tiene alguna. Cuando se administra en dosis normales (10–15 mg · kg–1, PO), el paracetamol es extremadamente seguro y tiene muy pocos efectos secundarios graves. Es un antipirético y, como todos los AINE administrados por vía enteral, tarda unos 30 minutos en proporcionar una analgesia eficaz. Varios investigadores han informado que cuando se administra por vía rectal, el paracetamol debe administrarse en dosis significativamente más altas que las sugeridas por las recomendaciones anteriores. Sin embargo, este autor no utiliza dosis de carga de paracetamol cuando el fármaco se administra por vía rectal. Independientemente de la vía de administración, para prevenir la hepatotoxicidad, la dosis máxima diaria de paracetamol en recién nacidos prematuros, recién nacidos a término y niños mayores es de 30, 60 y 80 mg/kg, respectivamente.Tabla 3). La dosis máxima para adultos es de 4 g/día.
El descubrimiento de al menos dos isoenzimas de ciclooxigenasa (COX), denominadas COX-1 y COX-2, ha aumentado nuestro conocimiento sobre los AINE. Estas dos isoenzimas COX comparten similitudes estructurales y enzimáticas, pero están reguladas de manera única a nivel molecular y pueden distinguirse por sus funciones. Las prostaglandinas protectoras, que preservan la integridad del revestimiento del estómago y mantienen la función renal normal en un riñón comprometido, son sintetizadas por la COX-1. COX-2 es una isoforma inducible. Los estímulos inductores incluyen citoquinas proinflamatorias y factores de crecimiento, lo que implica un papel para la COX-2 tanto en la inflamación como en el control del crecimiento celular. Además de la inducción de COX-2 en las lesiones inflamatorias, la COX-2 está presente de manera constitutiva en el cerebro y la médula espinal, donde puede estar involucrada en la transmisión nerviosa, particularmente para el dolor y la fiebre.
TABLA 2. Pautas de dosificación para analgésicos no opioides de uso común (las pautas institucionales o nacionales pueden variar).
| Recién nacidos prematuros (32 a 36 semanas Edad posmenstruala) | Recién nacidos a término (> 36–44 semanas Edad posmenstruala) | Lactantes y niños (> 44 semanas Edad posmenstruala y hasta 50 kg) | > 12 Años (y Peso > 50 kgb) | |
|---|---|---|---|---|
| Acetaminofén (paracetamol) | ||||
| Acetaminofén (paracetamol) | 15 mg/kg PO/PR cada 8 horas (máx. 60 mg/kg/día) | 15 mg/kg PO/PR cada 6 horas (máx. 60 mg/kg/día) | 15–20 mg/kg VO/PRbc cada 4-6 horas (máx. 90 mg/kg/día) | 1 g VO/PR cada 4-6 horas (máx. 4 g/día) |
| acetaminofén intravenoso | 7.5 mg/kg IV cada 8 horas (máx. 25 mg/kg/día) | 7.5 mg/kg IV cada 6 horas (máx. 30 mg/kg/día) | 15 mg/kg IVb cada 6 horas (máximo 60mg/kg/día) | 15 mg/kg IV (máximo 1 g) cada 6 horas |
| Medicamentos antiinflamatorios no esteroides (AINE) Prescribir un solo medicamento. | ||||
| Ibuprofen | No recomendado | No recomendado | Menos de 3 meses de edad: 5 mg/kg VO cada 8 horas A partir de los 3 meses de edad: 10 mg/kg VO (máximo 400 mg) cada 8 horas (máximo 30 mg/kg/día) | 400 mg VO cada 8 horas |
| Diclofenac | No recomendado | No recomendado | A partir de los 6 meses de edad: 1 mg/kg VO/PR cada 8 horas | 50 mg VO/PR cada 8 horas |
| Naproxeno | No recomendado | No recomendado | 5 mg/kg cada 12 horas | 5 mg/kg cada 12 horas (máx. 1 g/día) |
bEs posible que sea necesario reducir las dosis basadas en el peso en pacientes obesos o en función de la edad en pacientes con bajo peso para evitar una sobredosis.
cPuede usarse una dosis mayor de paracetamol 20 mg/kg VO/PR cada 6 horas cuando el dolor no se controla con la dosis estándar (15 mg/kg) cuando no existen contraindicaciones. Esta dosis debe revisarse cada 24 horas. No se recomiendan dosis de carga para minimizar la posibilidad de error.
Las prostaglandinas producidas por COX-2 también son importantes en la ovulación y en el proceso de nacimiento. El descubrimiento de la COX-2 ha hecho posible el diseño de fármacos que reducen la inflamación sin eliminar las prostaglandinas protectoras del estómago y los riñones producidas por la COX-1. De hecho, el desarrollo de un inhibidor COX-2 más específico ha sido un objetivo importante de gran parte de la investigación farmacológica porque esta clase de fármacos tiene todas las propiedades antiinflamatorias y analgésicas que uno desea en un fármaco sin ninguno de los efectos secundarios gastrointestinales y antiplaquetarios. . Desafortunadamente, la creciente controversia con respecto a los posibles riesgos cardiovasculares adversos del uso prolongado de inhibidores de la COX-2 ha apagado gran parte del entusiasmo por estos medicamentos y ha llevado a que el fabricante retire el rofecoxib del mercado. Otros AINE, especialmente el diclofenaco, ahora enfrentan un escrutinio similar. Muchos cirujanos ortopédicos también están preocupados por el efecto negativo de todos los AINE sobre el crecimiento y la cicatrización de los huesos. Si bien algunos cirujanos ortopédicos pediátricos han recomendado que estos medicamentos no se usen en sus pacientes en el período posoperatorio, la opinión de este autor es que, a pesar de las controversias, los AINE siguen siendo medicamentos efectivos y útiles en el tratamiento del dolor agudo pediátrico cuando se usan con prudencia y por períodos breves. duración.
TABLA 3. Pautas de dosificación inicial de analgésicos opioides (las pautas institucionales o nacionales pueden variar).
| Dosis equianalgésica (mg) | Intervalo y dosis IV inicial habitual | Intervalo y dosis oral inicial habitual | |||||
|---|---|---|---|---|---|---|---|
| Droga | IV, IM, SC | Oral | < 50 kg | > 50 kg | Proporción IV/oral | < 50 kg | > 50 kg |
| Codeína | 120 | 200 | NR | NR | 1:2 | 0.5-1a mg/kg cada 4-6 horas | 0.5-1a mg/kg cada 4-6 horas |
| El Fentanilo | 0.1 | NAb | Bolo: 0.5–1 mcg/kg, 0.5–2 h (máx. 50 mcg) NCA/PCA (concentración de fármaco: 1 mcg/kg/ml, máx. 50 mcg/ml) ANC: Bolo: 0.5–1 mcg/kg, 30 min–1 h; infusión: 0.5-1 mcg/kg/h ACP: Bolo: 0.5 mcg/kg, 10 min–1 h; infusión: 0.5-1 mcg/kg/h | NA | NA | NA | |
| La hidrocodona | NA | 10-20 | NA | NA | NA | 0.1 mg/kg cada 3-4 horas | 5–10 mg cada 3–4 horas |
| La hidromorfona | 1.5-2 | 3-5c | Bolo: 0.02 mg/kg, 0.5–2 h; infusión: 0.004 mg/kg/h | Bolo: 1 mg, 0.5–2 h; infusión: 0.3 mg/h | 1:2 | 0.03–0.08 mg/kg cada 4 horas | 2–4 mg cada 4 horas |
| Metadona | 10 | 10-20 | 0.1 mg/kg cada 4-8 horas | 5–10 mg cada 4–8 horas | 1:2 | 0.2 mg/kg cada 4-8 horas | 10 mg cada 4 a 8 horas |
| Morfina | 10 | 30-50 | Bolo: 0.03–0.1 mg/kg, 0.5–2 h (máx. 10 mg) NCA/PCA (concentración de fármaco 20 mcg/kg/ml, máx. 1 mg/ml)d ANC: Bolo: 20 mcg/kg, 15 min–1 h; infusión: 20 mcg/kg/h ACP: Bolo: 20 mcg/kg (máx. 1 mg), 5 min; infusión: 4 mcg/kg/h | 1: 2 – 3 | 0.2–0.3 mg/kg cada 4–6 horas Liberación sostenida: 0.4–0.5 mg/kg cada 8-12 horas | 15 mg/kg cada 4-6 horas Liberación sostenida: 30 mg cada 8-12 horas |
|
| Oxicodona | NA | 10-20 | NA | NA | NA | 0.1 mg/kg cada 3-4 horas | 5-10 mg cada 3-4 horase |
bVía transmucosa oral disponible: dosis 10-15 mcg/kg.
cLa dosis oral equianalgésica y la relación dosis parenteral/oral no están bien establecidas.
dPara recién nacidos y lactantes menores de 13 semanas, la concentración del fármaco debe reducirse a la mitad: bolo de 5 mcg/kg, 1 h; infusión 5-10 mcg/kg/h.
eSe encuentra disponible una preparación de liberación sostenida.
Selección de fármacos opioides
Se tienen en cuenta muchos factores al decidir cuál es el analgésico opioide apropiado para administrar a un paciente pediátrico con dolor. Estos incluyen la intensidad del dolor, la edad del paciente, la enfermedad coexistente, las interacciones farmacológicas potenciales, el historial de tratamiento, la preferencia del médico, la preferencia del paciente y la vía de administración. Se prefieren algunos opioides a otros, y es posible que algunos no estén disponibles según la institución, el país o el continente, por razones que no se comprenden del todo. La idea de que algunos opioides son "débiles" (por ejemplo, la codeína) y otros "fuertes" (por ejemplo, la morfina) está desactualizada. Todos son capaces de tratar el dolor independientemente de su intensidad si la dosis se ajusta adecuadamente (Tabla 4). En dosis equipotentes, la mayoría de los opioides tienen efectos y efectos secundarios similares. La meperidina (petidina) en una dosis equianalgésica tiene el mismo perfil de efectos secundarios que la morfina; sin embargo, ya no se prescribe comúnmente.
TABLA 4. Pautas de dosificación máxima de anestésicos locales.
| Droga | Dosis mg/kg Sin epinefrina | Dosis mg/kg con epinefrina | Duración en horas | Contraindicaciones | Comentarios |
|---|---|---|---|---|---|
| Bupivacaínaa | 2.5 | 3 | 3-6 | Reducir la dosis en un 50% en neonatos | |
| Cloroprocaínab | 8 | 10 | 1 | Deficiencia de colinesterasa plasmática | Metabolismo rápido y de acción corta, útil en recién nacidos y posiblemente en pacientes con convulsiones o enfermedad hepática |
| Lidocaína | 5 | 7 | 1 | ||
| Ropivacaínac | 3 | nunca mezclado | 3 - 6 | Menos cardiotoxicidad que la bupivacaína |
bEn infusión continua epidural neonatal: 10-15 mg/kg/h.c La tasa de infusión es de 0.5 mg/kg para pacientes pediátricos mayores de 4-6 meses de edad.
Opioides orales de uso común: codeína, oxicodona, hidrocodona, morfina y tramadol
La codeína, la oxicodona y la hidrocodona son opioides que se usan con frecuencia para tratar el dolor en niños y adultos, en particular el dolor menos intenso y cuando los pacientes están cambiando de opioides parenterales a enterales (ver Tabla 3). La morfina se usa comúnmente en regímenes para el dolor crónico (p. ej., cáncer). La codeína, la oxicodona y la hidrocodona se administran con mayor frecuencia en forma oral, generalmente en combinación con paracetamol o aspirina. Desafortunadamente, se han realizado muy pocos estudios farmacocinéticos o dinámicos en niños, si es que se ha realizado alguno, y la mayoría de las pautas de dosificación se basan en anécdotas. En dosis equipotentes, la codeína, la oxicodona, la hidrocodona y la morfina son iguales como analgésicos y depresores respiratorios (ver Tabla 3). Además, estos fármacos comparten efectos comunes sobre el sistema nervioso central con otros opioides, incluida la sedación, la depresión respiratoria y la estimulación de la zona de activación de los quimiorreceptores en el tronco encefálico, este último en particular en el caso de la codeína. Hay menos efectos secundarios de náuseas y vómitos con oxicodona e hidrocodona. La codeína, la hidrocodona y la oxicodona tienen una biodisponibilidad de aproximadamente el 60 % después de la ingestión oral. Los efectos analgésicos ocurren tan pronto como 20 minutos después de la ingestión y alcanzan un máximo después de 60 a 120 minutos. La semivida plasmática de eliminación es de 2.5 a 4 horas. La codeína sufre un metabolismo casi completo en el hígado antes de su excreción final en la orina. Aproximadamente el 10% de la codeína se metaboliza en morfina (CYP2D6), y es este 10% el responsable del efecto analgésico de la codeína. Curiosamente, aproximadamente el 10% de la población y la mayoría de los recién nacidos no pueden metabolizar la codeína en morfina y, en estos pacientes, la codeína produce poca o ninguna analgesia.
La codeína necesita una mención especial, ya que su uso ha sido objeto de un mayor escrutinio en el momento de escribir este capítulo. Se han informado algunos casos de muertes y episodios potencialmente mortales de depresión respiratoria en niños que son "metabolizadores ultrarrápidos" del citocromo P450 CYP2D6 y recibieron codeína después de una amigdalectomía o adenoidectomía en el tratamiento de la apnea obstructiva del sueño. La enzima CYP2D6 está sujeta a polimorfismo genético. Al tener múltiples copias de genes, algunos pacientes metabolizan la codeína más rápidamente (y por lo tanto se los denomina “metabolizadores ultrarrápidos”) y, por lo tanto, tienen un mayor riesgo de experimentar toxicidad por morfina, es decir, depresión respiratoria. La prevalencia de esto varía según el origen étnico, desde un 0% a un 2% en los asiáticos hasta un 10% a un 16% en los etíopes y los árabes saudíes.
La posición actual sobre el uso de codeína es la siguiente. La Administración Federal de Medicamentos (FDA) de EE. UU., el Comité de Evaluación de Riesgos de Farmacovigilancia (PRAC) de la Agencia Europea de Medicamentos (EMA) y la Agencia Reguladora de Medicamentos y Productos Sanitarios (MHRA) del Reino Unido han recomendado restricciones en el uso de codeína en niños. . Estos incluyen lo siguiente:
- Restringir el uso de codeína a niños mayores de 12 años (EMA y MHRA)
- Evitar el uso de codeína en pacientes menores de 18 años sometidos a amigdalectomía o adenoidectomía, especialmente por apnea obstructiva del sueño (EMA y FDA).
- En todos los demás casos, use codeína solo si es necesario. Debe prescribirse solo "según sea necesario", con una dosis restringida a 0.5 mg/kg (máximo 30 mg) cada 6 horas y con una duración limitada del tratamiento.
- El paciente que recibe codeína debe ser monitoreado de cerca por depresión respiratoria; Se debe advertir a las enfermeras y a los padres/tutores que estén atentos a los signos de sobredosis de morfina.
Durante muchos años, la codeína se ha utilizado de manera más o menos universal en la práctica pediátrica para el alivio del dolor moderado, como medicamento de reducción y como medicamento para llevar a casa al momento del alta. Los posibles dilemas incluyen los siguientes:
- Debido a su uso generalizado, existen varias preparaciones y formulaciones "aptas para niños" que brindan sistemas de administración versátiles para todas las edades. Sin embargo, los desarrollos recientes pueden haber desalentado el desarrollo de formulaciones versátiles de otros opioides de "potencia" similar. Por lo tanto, muchos países se quedan con alternativas limitadas o no adecuadas a la codeína.
- La concesión de licencias y el uso de drogas alternativas está rezagada en ciertos países. Por ejemplo, el tramadol no está autorizado en el Reino Unido para pacientes menores de 12 años.
- Hay pocos datos para determinar si alguna de las alternativas disponibles es tan efectiva como la codeína.
- Aunque la morfina es la alternativa más lógica a la codeína, los temas de preocupación incluyen las regulaciones de drogas controladas en ciertos países, las prácticas institucionales y locales, y la renuencia de algunos profesionales de la salud a recetar morfina oral debido a preocupaciones sociales y al potencial percibido de abuso.
- Para las instituciones y los países donde se encuentran disponibles otras formulaciones seguras, efectivas y versátiles de alternativas a la codeína, como tramadol, oxicodona y buprenorfina, es posible que sea necesario acordar pautas provisionales locales (con o sin el uso continuo de codeína) para para continuar brindando analgesia segura y efectiva a la población pediátrica.
- Estos problemas pueden alentar a las compañías farmacéuticas a desarrollar productos analgésicos más "apropiados para los niños" y alentar investigaciones similares de otros opioides para validar su eficacia en los niños.
- Estas preocupaciones también pueden conducir al desarrollo de genotipado de pacientes comercialmente viable.
Al igual que la codeína y la oxicodona, la morfina es muy eficaz cuando se administra por vía oral, pero solo alrededor del 40 % de una dosis oral de morfina llega a la circulación sistémica. En el pasado, esto llevó a muchos a concluir de manera inapropiada que la morfina no es efectiva cuando se administra por vía oral; en cambio, la falta de eficacia fue simplemente el resultado de una dosificación oral inadecuada. Por lo tanto, al convertir la dosis de morfina intravenosa requerida de un paciente a una dosis de mantenimiento oral, se debe multiplicar la dosis intravenosa por un factor de 2 a 3.
Consejos NYSORA
- Al convertir la dosis de morfina intravenosa requerida de un paciente a una dosis de mantenimiento oral, multiplique la dosis intravenosa por un factor de 2 a 3.
Mientras que la morfina oral se receta sola, la codeína oral, la hidrocodona, la oxicodona y el tramadol generalmente se recetan en combinación con paracetamol o aspirina. El paracetamol potencia la analgesia producida por la codeína (y otros opiáceos) y permite el uso de una dosis menor del opiáceo con una analgesia satisfactoria. En todas las “preparaciones combinadas”, tenga cuidado de no administrar inadvertidamente una dosis hepatotóxica de paracetamol al aumentar las dosis de opioides para el dolor incontrolable. Debido a esta preocupación, se prefiere prescribir el opioide y el paracetamol (o ibuprofeno) por separado. Aunque es un analgésico eficaz cuando se administra por vía parenteral, la codeína intramuscular no tiene ventajas sobre la morfina o cualquier otro opioide; por lo tanto, se desaconseja su uso. Al igual que la codeína, el tramadol se usa para tratar el dolor de moderado a intenso. Aunque el tramadol a menudo se clasifica como un agonista del receptor μ, tiene múltiples mecanismos de acción propuestos. También es un liberador de serotonina, un inhibidor de la recaptación de norepinefrina y un antagonista del receptor NMDA. La edad de autorización del tramadol varía según el país, pero se ha estudiado en niños de hasta 1 año. Tramadol se prescribe a dosis de 1-2 mg/kg cada 6 horas hasta un máximo de 400 mg/día (dividido en 4 tomas para pacientes de más de 50 kg).
La hidrocodona se prescribe en una dosis de 0.05 a 0.1 mg/kg. Hay un elixir disponible en 2.5 mg/5 ml combinado con acetaminofeno 167 mg/5 ml. Como tableta, está disponible en dosis de hidrocodona entre 2.5 mg y 10 mg, combinada con 500 a 650 mg de acetaminofén. La oxicodona se prescribe en una dosis de 0.05 a 0.1 mg/kg. Desafortunadamente, un elixir no está disponible en la mayoría de las farmacias. Cuando lo es, se prepara como 1 mg/mL o 20 mg/mL. Obviamente, esto puede dar lugar a errores de dispensación catastróficos. En forma de comprimidos, la oxicodona suele estar disponible en comprimidos de 5 mg o como Tylox (500 mg de acetaminofeno y 5 mg de oxicodona) o Percocet (325 mg de acetaminofeno y 5 mg de oxicodona). La oxicodona también está disponible sin paracetamol en una tableta de liberación sostenida para usar en el dolor crónico. Como muchas otras tabletas de liberación prolongada, no debe triturarse y, por lo tanto, no puede administrarse a través de una sonda gástrica. Romper la tableta da como resultado la liberación inmediata de una gran cantidad de oxicodona. Al igual que la morfina de liberación sostenida (ver a continuación), la oxicodona de liberación sostenida solo se usa en pacientes tolerantes a los opioides con dolor crónico, no para el dolor posoperatorio de rutina. Además, tenga en cuenta que en pacientes con tránsito gastrointestinal rápido, es posible que las preparaciones de liberación sostenida no se absorban en absoluto (la metadona líquida puede ser una alternativa).
La morfina oral está disponible en forma líquida en varias concentraciones (hasta 20 mg/mL), en tabletas (p. ej., MSIR [sulfato de morfina de liberación inmediata], disponible en tabletas de 15 y 30 mg), y en forma de liberación sostenida. preparación. Debido a que está tan concentrado, el líquido es particularmente fácil de administrar a niños y pacientes severamente debilitados. De hecho, en pacientes terminales que no pueden tragar, la morfina líquida proporciona analgesia cuando simplemente se deja caer en la boca del paciente.
Analgesia controlada por el paciente y los padres/enfermera
Entre las muchas razones del tratamiento insuficiente del dolor pediátrico se encuentra la falta de familiaridad de los médicos (y enfermeras) con los fármacos, las dosis y las vías de administración adecuados. Cuando los medicamentos se administran a pedido (PRN), existe un desfase entre el momento de la solicitud del paciente y la respuesta de la enfermera y la preparación y administración de la analgesia. Sin embargo, en el dolor moderado a intenso, la administración en intervalos de administración las 4 horas del día (p. ej., cada 1 horas) tampoco es siempre la respuesta, debido a la gran variación individual en la percepción del dolor y el metabolismo de los opioides. De hecho, las dosis fijas y los intervalos de tiempo tienen poco sentido. Según la farmacocinética de los opioides, debe quedar claro que es posible que sea necesario administrar bolos intravenosos de morfina a intervalos de 2 a XNUMX horas para evitar marcadas fluctuaciones en los niveles plasmáticos del fármaco. Las infusiones intravenosas continuas pueden proporcionar niveles analgésicos estables, son preferibles a las intramusculares inyecciones, y se han utilizado con gran seguridad y eficacia en niños. Sin embargo, no son una panacea porque la percepción y la intensidad del dolor no son constantes. Por ejemplo, un paciente posoperatorio puede estar muy cómodo descansando en la cama y requerir pocos ajustes en el manejo del dolor. Pero este mismo paciente puede experimentar un dolor insoportable al toser, orinar o levantarse de la cama. Por lo tanto, el manejo racional del dolor requiere alguna forma de titulación cada vez que se administra cualquier opioide. Se han desarrollado dispositivos para dar a los pacientes (en algunos casos enfermeras y, en raras ocasiones, padres/tutores) alguna medida de control sobre la terapia del dolor, la analgesia a demanda o la analgesia controlada por el paciente (PCA). Estos dispositivos son bombas impulsadas por un microprocesador con un botón que el paciente presiona para autoadministrarse una pequeña dosis de opioide.
Los dispositivos PCA permiten a los pacientes administrar pequeñas cantidades de un analgésico cada vez que sienten la necesidad de aliviar más el dolor. El opioide, generalmente morfina, hidromorfona o fentanilo, se administra por vía intravenosa o subcutánea. La dosis de opioide (con o sin infusión de fondo), la cantidad de bolos por hora y el intervalo de tiempo entre los bolos (el "período de bloqueo") son programados en el equipo por el médico o la enfermera del servicio del dolor para permitir la máxima flexibilidad del paciente y un sensación de control con un riesgo mínimo de sobredosis. Generalmente, cuando los pacientes mayores saben que si tienen un dolor intenso, pueden obtener alivio inmediato, muchos prefieren regímenes de dosificación que produzcan un dolor leve a moderado a cambio de menos efectos secundarios, como náuseas o prurito. Por lo general, se prescribe morfina, 20 mcg/kg por bolo (o 3 a 4 mcg/kg/h de hidromorfona o 0.5 mcg/kg/h de fentanilo), con un intervalo de bloqueo de 5 a 15 minutos entre cada bolo. Las variaciones incluyen bolos más grandes o más pequeños, intervalos de tiempo más cortos o más largos y una infusión de fondo variable; estos tienden a basarse en la práctica y las preferencias institucionales. La computadora de la bomba PCA almacena en su memoria la cantidad de bolos que el paciente ha recibido, así como la cantidad de intentos que el paciente ha hecho para recibir bolos. Esto le permite al médico evaluar qué tan bien el paciente entiende el uso de la bomba y brinda información para programar la bomba de manera más eficiente. La mayoría de las unidades de ACP permiten infusiones continuas bajas de "fondo" (p. ej., 2 a 30 mcg/kg/h de morfina, 3 a 4 mcg/kg/h de hidromorfona, 0.5 a 1 mcg/kg/h de fentanilo) además de los bolos autoadministrados . Una infusión de fondo continua es particularmente útil por la noche y, a menudo, proporciona un sueño más reparador al evitar que el paciente se despierte con dolor. Sin embargo, también aumenta el potencial de sobredosis. Aunque la literatura de adultos sobre el dolor no apoya el uso de infusiones de base continuas, nuestra experiencia ha sido que las infusiones continuas son esenciales para un buen manejo del dolor en el paciente pediátrico. De hecho, en nuestra práctica, casi siempre usamos infusiones de fondo continuas cuando prescribimos PCA o analgesia controlada por enfermeras (NCA).
PCA requiere un paciente con suficiente inteligencia, destreza manual y fuerza para operar la bomba. Así, inicialmente estos dispositivos estaban limitados a los adolescentes, pero el límite inferior de edad en el que se puede utilizar esta modalidad de tratamiento sigue descendiendo (actualmente en torno a los 5-6 años). Las contraindicaciones para el uso de PCA incluyen la incapacidad para presionar el botón del bolo, la incapacidad para entender cómo usar la máquina y el deseo del paciente de no asumir la responsabilidad de su cuidado. pacientes con necesidades complejas, la práctica de permitir que sustitutos, como enfermeras, inicien un bolo PCA se denomina analgesia controlada por enfermeras (NCA). Esta es una práctica estándar en nuestra institución. Se ha demostrado que las enfermeras y, en casos excepcionales, los padres pueden estar capacitados para iniciar bolos PCA y usar esta tecnología de manera segura en niños, incluso en los menores de 1 año de edad, siendo similar la incidencia de efectos secundarios comunes inducidos por opioides. a la observada en pacientes mayores. Los NCA tienden a tener una tasa de infusión de fondo ligeramente más alta y un período de bloqueo más prolongado que los PCA. Para neonatos y lactantes de 1 a 3 meses utilizamos morfina NCA: una infusión de fondo de 5 o 10 mcg/kg/h, respectivamente, con un bolo de 5 mcg/kg y un bloqueo de 60 minutos.
Curiosamente, la depresión respiratoria es muy rara, pero ocurre, lo que refuerza la necesidad de una estrecha vigilancia y protocolos de enfermería establecidos. Las dificultades con PCA incluyen su mayor costo, las limitaciones de edad del paciente y los obstáculos burocráticos (protocolos, educación de enfermería, arreglos de almacenamiento) que deben superarse antes de su implementación.
Fentanilo transmucoso, intranasal y transdérmico
Debido a que el fentanilo es extremadamente lipofílico, puede absorberse fácilmente a través de cualquier membrana biológica, incluida la piel. Por lo tanto, se puede administrar sin dolor por nuevas vías de administración de fármacos no intravenosas, incluidas las vías transmucosa (nariz y boca) y transdérmica. La vía transmucosa de administración de fentanilo es extremadamente eficaz para el alivio del dolor agudo. Cuando se administra por vía intranasal (2 mcg/kg), produce una analgesia rápida equivalente al fentanilo administrado por vía intravenosa.
Alternativamente, el fentanilo se ha fabricado en una matriz de caramelo (Actiq) adherida a un aplicador de plástico (parece una piruleta) para la absorción transoral/transmucosa. A medida que el niño chupa el caramelo, el fentanilo se absorbe a través de la mucosa bucal y se absorbe rápidamente (durante 10 a 20 minutos) en la circulación sistémica. Si se produce una sedación excesiva, el aplicador elimina el fentanilo de la boca del niño. Este método es más eficiente que la administración intestinal oral-gástrica ordinaria porque la absorción transmucosa evita el metabolismo hepático de primer paso eficiente del fentanilo que ocurre después de la absorción enteral en la circulación portal. Actiq ha sido aprobado por la FDA para su uso en niños como premedicación antes de la cirugía y para el dolor relacionado con el procedimiento (p. ej., punción lumbar, aspiración de médula ósea). También es útil en el tratamiento del dolor del cáncer y como complemento del fentanilo transdérmico. Cuando se administra por vía transmucosa, el fentanilo se administra en dosis de 10 a 15 mcg/kg, es efectivo en 20 minutos y dura aproximadamente 2 horas. Se absorbe aproximadamente del 25% al 33% de la dosis administrada. Así, cuando se administra en dosis de 10 a 15 mcg/kg, se alcanzan niveles en sangre equivalentes a 3 a 5 mcg/kg de fentanilo IV. El principal efecto secundario, náuseas y vómitos, ocurre en aproximadamente 20 a 33 % de los pacientes que lo reciben.
La vía transdérmica se utiliza con frecuencia para administrar fármacos de administración crónica, como escopolamina, clonidina y nitroglicerina. Muchos factores, como el sitio del cuerpo, la temperatura de la piel, el daño de la piel, el grupo étnico y la edad, afectan la absorción de los medicamentos administrados por vía transdérmica. Colocado en un parche de membrana semipermeable selectivo, un reservorio de fármaco proporciona una absorción lenta y constante del fármaco a través de la piel. El parche se adhiere a la piel mediante un adhesivo de contacto, que a menudo causa irritación de la piel. El uso de fentanilo transdérmico ha revolucionado el tratamiento del dolor del cáncer en adultos. Dado que el fentanilo se absorbe sin dolor a través de la piel, una cantidad sustancial se almacena en las capas superiores de la piel, que luego actúa como un reservorio secundario. La presencia de un depósito en la piel tiene varias implicaciones: amortigua las fluctuaciones del efecto del fentanilo, debe llenarse razonablemente antes de que ocurra una absorción vascular significativa y contribuye a una concentración plasmática residual prolongada de fentanilo después de retirar el parche. De hecho, la cantidad de fentanilo que queda en el sistema y en el depósito de la piel después de retirar el parche es considerable. Al final de un período de 24 horas, aproximadamente el 30 % de la dosis total liberada del parche permanece en el depósito de la piel. Por lo tanto, quitar el parche no detiene la absorción continua de fentanilo en el cuerpo.
Debido al tiempo de inicio prolongado, la incapacidad para ajustar rápidamente la administración del fármaco y la vida media de eliminación prolongada, el uso de fentanilo transdérmico para el tratamiento del dolor agudo es controvertido. Como se indicó anteriormente, la seguridad de este sistema de administración de medicamentos se ve comprometida aún más porque el fentanilo continúa absorbiéndose de la grasa subcutánea durante casi 24 horas después de retirar el parche. De hecho, el uso de este sistema de administración de fármacos para el dolor agudo ha resultado en la muerte de un paciente por lo demás sano. El fentanilo transdérmico generalmente se reserva para pacientes con dolor crónico (p. ej., cáncer) y aquellos que son tolerantes a los opioides. Incluso cuando el fentanilo transdérmico es apropiado, el vehículo impone sus propias limitaciones. El “parche” de fentanilo de dosis más baja administra 25 mcg de fentanilo por hora; los otros entregan 50, 75 y 100 mcg de fentanilo por hora. Los parches no se pueden cortar físicamente en pedazos más pequeños para administrar menos fentanilo. Esto a menudo limita la utilidad en pacientes con pesos corporales más bajos y, al igual que con otros opioides, este sistema de administración de fármacos no ha sido probado ni aprobado para su uso en niños.
Un nuevo método no invasivo de PCA transdérmico está en el horizonte. Usando iontoforesis (electrotransporte), se pueden autoadministrar pequeñas dosis de fentanilo (40 mcg) a través de la piel (E-Trans, Alza Corporation). La PCA transdérmica puede ofrecer ventajas logísticas para los pacientes y el personal de enfermería al eliminar la necesidad de acceso venoso, tubos intravenosos y bombas especializadas.
Complicaciones
Independientemente del método de administración, todos los opioides producen efectos secundarios no deseados comunes, como prurito, náuseas y vómitos, estreñimiento, retención urinaria, deterioro cognitivo, tolerancia y dependencia. De hecho, muchos pacientes sufren innecesariamente un dolor agonizante porque prefieren sufrir dolor que experimentar estos efectos secundarios inducidos por los opioides. Además, los médicos suelen ser reacios a recetar opioides debido a estos efectos secundarios y por temor a otros efectos secundarios menos comunes, pero más graves, como la depresión respiratoria. Varios estudios clínicos y de laboratorio han demostrado que las infusiones de naloxona en dosis bajas (0.25 a 1 mcg/kg/h) pueden tratar o prevenir los efectos secundarios inducidos por opioides sin afectar la calidad de la analgesia o los requisitos de opioides.
Algunos opioides, cuando se administran concomitantemente con inhibidores selectivos de la recaptación de serotonina (ISRS), inhibidores de la monoaminooxidasa (IMAO) o inhibidores de la recaptación de serotonina y norepinefrina (IRSN), se han asociado con el síndrome serotoninérgico; estos incluyen fentanilo, oxicodona, hidrocodona y tramadol.
Transición a la medicación oral
La transición exitosa de los analgésicos intravenosos (o epidurales) a la medicación oral depende de la capacidad del médico para proporcionar una terapia alternativa que sea agradable al paladar, aceptable y, sobre todo, igualmente eficaz para tratar el dolor. Hay muchas ventajas en la administración de analgésicos por vía oral. La terapia enteral consiste en una vía de administración de fármacos menos invasiva y permite que los niños vuelvan más rápidamente a sus vidas normales. Además, los medicamentos orales son más fáciles y menos costosos de administrar que los medicamentos intravenosos y epidurales. Ciertos criterios son esenciales para la transición exitosa a la medicación oral. La función gastrointestinal normal debe estar presente antes de intentar la terapia enteral. Por lo tanto, el niño debe poder beber y/o comer (o tener un tubo gástrico en funcionamiento). Un niño que tiene náuseas o vomita después de comer simplemente no tolerará los analgésicos orales. En segundo lugar, el dolor intenso es difícil, si no imposible, de controlar solo con analgésicos orales. Por lo tanto, los analgésicos orales deben reservarse para el tratamiento del dolor leve a moderado durante la última parte del proceso de recuperación. La evaluación del grado de dolor y las modalidades de tratamiento existentes son pasos que ayudan en el proceso de transición. Tercero, debe estar disponible una formulación oral que sea apetecible y apropiada. Finalmente, se debe convertir la dosificación parenteral actual de opioides en una dosis oral más o menos equianalgésica.
Esta conversión es bastante sencilla incluso cuando los pacientes reciben múltiples formas y dosis de opioides parenterales. Como primer paso, convierta la dosis diaria completa de opioides administrados en equivalentes de morfina IV (Ejemplo 1). Luego, convierta esa dosis de morfina en una dosis equianalgésica de morfina oral (1:2) u otro opioide oral, si lo desea. Esta fórmula en realidad subestima la bioequivalencia de los medicamentos, pero se usa para minimizar el riesgo de sobredosis durante la transición.
Ejemplo
Un niño de 5 años y 20 kg fue víctima de un accidente automovilístico y sufrió una fractura pélvica. Ha estado tomando morfina IV PCA durante 2 semanas y será dado de alta para continuar con la terapia ambulatoria y la recuperación. Recibe morfina 2 mg/h y promedia un bolo de 0.5 mg de morfina cada hora. No puede tragar pastillas.
Paso 1: 2 mg/h durante 24 horas = 48 mg morfina/24 horas
Paso 2: 0.5 mg/bolo para 24 bolos/día = 12 mg de morfina
Paso 3: Morfina total de 24 horas = 48 mg + 12 mg = 60 mg
Paso 4: 60 mg de morfina IV = 120 mg de morfina PO (en realidad, esto representa una disminución del 25 % al 40 % en la bioequivalencia)
Paso 5: Prescribir morfina oral 20 mg cada 4 horas y un analgésico con actividad antipirética (p. ej., paracetamol o ibuprofeno).
Paso 6: Detenga la infusión de opioides basales (PCA) inmediatamente o junto con la dosis oral; aumente la dosis oral en un 20-25% si el alivio del dolor se considera inadecuado. Si el requerimiento de opiáceos es alto, la PCA se puede usar para proporcionar bolos de "rescate" solo durante el período de transición o para reducir las dosis de infusión/PCA de fondo a dosis orales más manejables.
Anestésicos locales
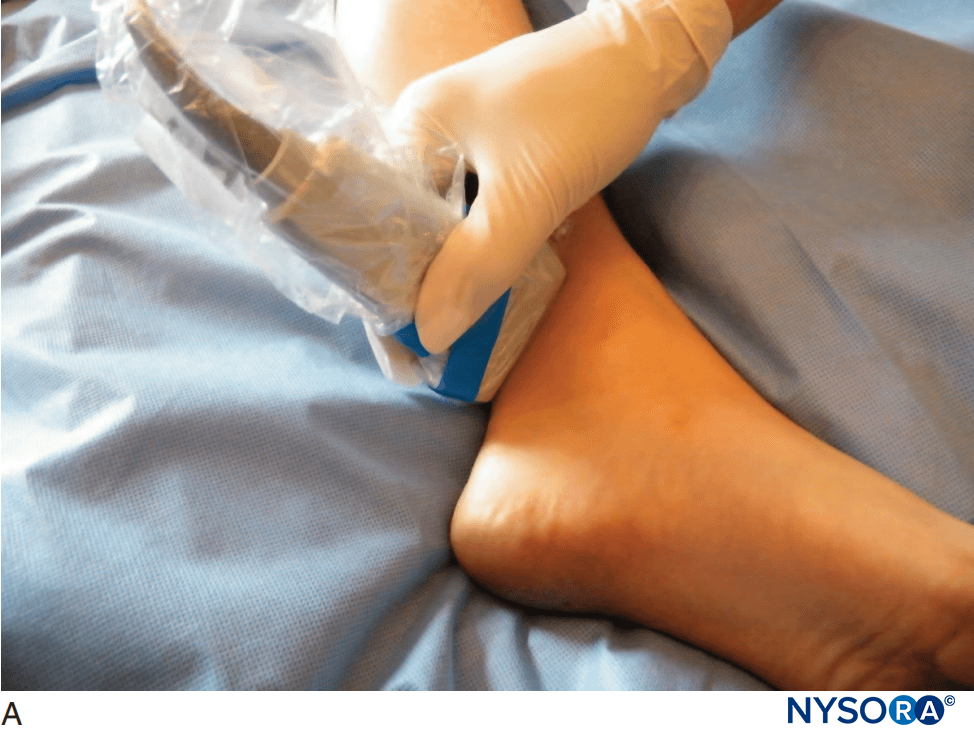
Durante los últimos 25 años, el uso de anestésicos locales y técnicas anestésicas regionales en la práctica pediátrica ha sufrido un cambio dramático. A diferencia de la mayoría de los fármacos utilizados en la práctica médica, los anestésicos locales deben depositarse físicamente en su sitio de acción mediante aplicación directa. Esto requiere la cooperación del paciente y el uso de agujas y equipos especializados; Debido a esto, durante mucho tiempo se consideró que los niños eran malos candidatos para las técnicas de anestesia regional debido a su abrumador miedo a las agujas. Sin embargo, una vez que se reconoció que la anestesia regional podía usarse como un complemento y no como un reemplazo de la anestesia general, su uso aumentó exponencialmente. La anestesia regional ofrece muchos beneficios al anestesiólogo y al especialista en dolor. Modifica la respuesta al estrés neuroendocrino, proporciona un profundo alivio del dolor posoperatorio, asegura una recuperación más rápida y puede acortar la estancia hospitalaria. Además, debido a que los catéteres colocados en la epidural, en las extremidades superiores o inferiores, o en el plexo lumbar pueden usarse durante días o meses, los anestésicos locales se usan cada vez más no solo para el alivio del dolor posoperatorio sino también para fines médicos (p. ej., crisis vasooclusiva de células falciformes), Alivio del dolor neuropático y terminal. Estas técnicas van desde la simple infiltración de anestésicos locales hasta bloqueos neuroaxiales (p. ej., analgesia espinal y epidural). Con el uso de la guía por ultrasonido, la anestesia regional en la población pediátrica ha ganado mayor popularidad. Los bloqueos de nervios periféricos también pueden proporcionar un alivio significativo del dolor después de muchos procedimientos pediátricos comunes y tienen el potencial de reemplazar o proporcionar una alternativa al tratamiento epidural "estándar de oro". Esto es particularmente cierto en la población neonatal donde el bloqueo paravertebral para una toracotomía o un bloqueo del plano transverso del abdomen (TAP) para una laparotomía pueden reemplazar una epidural para aliviar el dolor de manera efectiva y evitar los riesgos asociados con el bloqueo neuroaxial. Para utilizarlos de forma segura, es necesario un conocimiento práctico de la anatomía, las limitaciones de la técnica y las diferencias en la forma en que se metabolizan los anestésicos locales en lactantes y niños. Todos los aspectos de los anestésicos locales se analizan en detalle en los capítulos anteriores.
Otros adyuvantes en un régimen de analgesia multimodal
La gabapentina
La gabapentina está bien establecida en el tratamiento del dolor crónico. Algunos estudios han demostrado que la gabapentina perioperatoria reduce el consumo de opiáceos en el posoperatorio agudo en pacientes que se someten a una variedad de cirugías, incluido el bypass de la arteria coronaria y la artroplastia de rodilla. En un estudio, se demostró que la gabapentina reduce el uso perioperatorio de opioides pero no los efectos secundarios relacionados con los opioides en pacientes pediátricos sometidos a fusión espinal posterior. La dosificación varía desde una sola dosis perioperatoria hasta el tratamiento durante 1 a 2 semanas. En nuestra institución, usamos gabapentina para cirugías de fusión espinal y cirugías seleccionadas donde el alivio del dolor posoperatorio se considera un desafío. Normalmente administramos gabapentina a dosis de 5-10 mg/kg cada 8 horas durante 5 días. Para pacientes con necesidades complejas, es posible que sea necesario reducir las dosis, ya que en algunos casos, la gabapentina puede producir una sedación o somnolencia notables.
Ketamina
La ketamina es un anestésico bien conocido que produce anestesia disociativa pero también proporciona una analgesia de muy buena calidad a dosis muy bajas a través de su actividad antagonista del receptor NMDA. Sin embargo, los profesionales de la salud desconfían de la ketamina debido a su desagradable efecto secundario de alucinaciones y su reciente implicación en la neuroapoptosis en el cerebro en desarrollo. Estas preocupaciones ahora han llevado a evitar el uso de ketamina en pacientes menores de 1 año y también han disminuido la popularidad de la ketamina como aditivo en bloqueos caudales y epidurales.
Sin embargo, en niños mayores y adolescentes, la ketamina todavía se usa ampliamente con buenos resultados. La ketamina también se puede agregar a la morfina PCA en una proporción de 1:1. En nuestra institución, una sola dosis baja de ketamina (0.1-0.25 mg/kg) forma parte de un régimen analgésico intraoperatorio equilibrado para adenoamigdalectomía y cirugías mayores. La infusión de ketamina también se usa como analgésico intravenoso de segunda línea para afecciones complejas y dolorosas y en casos de dolor agudo o crónico en los que otros tratamientos no han logrado producir una analgesia eficaz. La dosis de infusión de ketamina utilizada es de 0.05-0.2 mg/kg/h (utilizando una concentración de fármaco de 0.1 mg/kg/ml, hasta un máximo de 250 mg en 50 ml).
Magnesio
El magnesio se usa en una variedad de emergencias médicas y tratamientos. Se ha informado que el uso intravenoso de magnesio mejora la analgesia posoperatoria. Aunque el mecanismo de acción aún no se comprende por completo, se cree que las propiedades analgésicas del magnesio se deben a la regulación de la entrada de calcio en la actividad antagonista del receptor de NMDA y la célula. Sin embargo, la evidencia ha sido equívoca y, aunque es relativamente seguro, el magnesio tiene efectos secundarios. Un metanálisis reciente concluyó que el magnesio intravenoso perioperatorio reduce el consumo de opiáceos y, en menor medida, las puntuaciones de dolor, en las primeras 24 horas posteriores a la operación sin que se hayan informado efectos adversos graves. El uso de magnesio, ya sea en bolo o en infusión (a dosis de 30-50 mg/kg), para cirugías mayores, particularmente fusiones espinales, y para otras cirugías ortopédicas mayores y generales, es una práctica estándar en nuestra institución.
MANEJO DEL DOLOR CRÓNICO
LA TRANSICIÓN DEL DOLOR AGUDO AL CRÓNICO
El dolor agudo ha evolucionado como un mecanismo de defensa vital, que alerta al animal sobre lesiones y daños físicos para detener la exposición a la lesión, como con el reflejo del dolor o para señalar la necesidad de descansar para permitir que se produzca la curación. El dolor crónico, sin embargo, no cumple ninguna función protectora. El dolor crónico se considera dolor que se extiende más allá del período esperado de curación. Cada vez hay más estudios en la literatura para adultos que demuestran el desarrollo de dolor crónico posoperatorio, que luego se asocia con consecuencias negativas significativas para el individuo, en términos de salud física y mental, y para la sociedad en general, en términos económicos. y la carga de los recursos sanitarios. La incidencia de dolor posoperatorio crónico varía según el tipo de cirugía, con estimaciones entre el 5% y el 50% en los procedimientos quirúrgicos más comunes, incluida la reparación de hernias, el reemplazo de cadera y la colecistectomía, frente a hasta el 85% en las amputaciones. Aunque la literatura sobre el desarrollo de dolor crónico posoperatorio es escasa en rangos de edad pediátrica, los estudios comienzan a indicar que sí ocurre, aunque su incidencia puede ser menor que en la población adulta.
Fortier estudió a 113 niños entre 2 y 17 años que habían sido sometidos a cirugía urológica u ortopédica general y encontró que el 13.3% reportaba dolor crónico como resultado de la cirugía. Las cirugías más relacionadas con el desarrollo de dolor crónico fueron las ortopédicas. Más de una cuarta parte informó interferencia en los patrones de sueño y actividades extracurriculares, y 1 de cada 6 informó interferencia en las actividades escolares. El dolor crónico en adultos después de la cirugía inguinal tiene una incidencia informada de 5 a 35%; sin embargo, en los niños, los estudios sugieren que la incidencia puede ser menor. Una cirugía particular en adolescentes asociada con una alta incidencia de dolor persistente es la escoliosis, donde se informan estimaciones del 50%. Un estudio realizado por Wong demostró una tendencia a que aquellos que experimentaron un dolor posoperatorio más severo tuvieran una mayor tendencia a desarrollar dolor persistente; solo el 39 % de las personas con dolor posoperatorio leve desarrollaron dolor persistente en comparación con el 74 % de las personas con dolor posoperatorio intenso. Los estudios han indicado que el dolor persistente puede ser una complicación hasta 12 meses después de la cirugía; sin embargo, la toracotomía en la infancia se ha asociado con dolor que persiste en la edad adulta hasta 30 años después. Este riesgo parece menor cuando la cirugía se realiza a una edad más temprana y aumenta con la edad a la que se realiza la cirugía. Aunque los mecanismos para la transición del dolor agudo al crónico son complejos, algunos factores de riesgo identificados en la literatura de adultos (en ausencia de muchos estudios en niños) también pueden ser relevantes para la población pediátrica. Estos incluyen la presencia de dolor preoperatorio, la gravedad del dolor posoperatorio agudo y la cirugía abierta versus laparoscópica. Por lo tanto, un buen manejo multimodal del dolor posoperatorio juega un papel importante en los esfuerzos para prevenir el desarrollo subsiguiente de dolor persistente en los niños.
Consejos NYSORA
- El dolor crónico puede ser una complicación postoperatoria en la población pediátrica.
- El dolor crónico tiene un impacto negativo en el sueño, las actividades, la asistencia a la escuela y el rendimiento escolar.
- Los riesgos para el desarrollo de dolor crónico incluyen el dolor preoperatorio, la gravedad del dolor posoperatorio agudo y la cirugía abierta versus laparoscópica.
EL MANEJO DEL DOLOR AGUDO SOBRE CRÓNICO
El manejo de pacientes sometidos a cirugía con dolor crónico preoperatorio puede ser problemático, y la presencia de dolor preoperatorio aumenta la percepción del dolor posoperatorio. Una buena preparación y planificación preoperatorias son importantes, incorporando educación tanto para el niño como para los padres/tutores e involucrándolos en la toma de decisiones. Las intervenciones psicológicas, como la terapia cognitiva conductual y la descatastrofización, pueden ser una preparación beneficiosa. Los pacientes que experimentan dolor preoperatorio pueden estar tomando medicamentos analgésicos adyuvantes, algunos de los cuales no deben suspenderse abruptamente, como los anticonvulsivos (p. ej., gabapentina). Otros medicamentos pueden tener interacciones significativas con los analgésicos de uso común; por ejemplo, la combinación de amitriptilina y tramadol ha dado lugar al síndrome serotoninérgico. Hay un pequeño número de pacientes pediátricos que se presentan para cirugía con opiáceos a largo plazo, y no todos estos pacientes serán paliativos. Las administraciones prolongadas de opioides pueden ocurrir en niños en unidades de cuidados intensivos, aquellos que requieren cirugía frecuente y repetida (p. ej., por quemaduras), aquellos con exacerbaciones frecuentes de la enfermedad (p. ej., células falciformes), adolescentes que usan opioides ilícitamente y en un pequeño número de niños con dolor médicamente inexplicable. Las recomendaciones para el manejo de tales pacientes se extrapolan principalmente de la literatura para adultos debido a la falta de evidencia en niños (Tabla 5).
TABLA 5. Consideraciones para el manejo perioperatorio de niños con opioides a largo plazo.
| Educar e involucrar al niño y sus padres/tutores en la planificación preoperatoria. |
| Continuar con los opioides de mantenimiento o considerar la conversión a opioides parenterales |
| Puede ser necesaria la suplementación con opioides sistémicos (orales o intravenosos) si se utiliza una técnica neuroaxial. |
| Valore los opioides en el posoperatorio. |
| Es posible que la dosis deba ser entre un 30 % y un 100 % mayor que la de los pacientes que no han recibido nunca opioides. |
| Usar terapia multimodal, incluidos medicamentos adyuvantes (p. ej., ketamina) y técnicas no farmacológicas. |
| Utilice técnicas de anestesia regional cuando sea posible. |
| Al pasar de los opioides parenterales a la administración oral, calcule la dosis total necesaria durante 24 horas. Administre el 50% de la dosis oral estimada como acción prolongada y el resto como avance. |
| Disminuya gradualmente los opioides orales a las dosis preoperatorias, durante un período de 2 a 4 semanas. - En las primeras 24 horas del postoperatorio, reducir la dosis en un 20-40%. - Transcurridas las primeras 24 horas del postoperatorio, reducir la dosis entre un 5-20% (utilizar un ritmo más lento en presencia de signos de abstinencia). |
| Asegúrese de que el servicio de dolor crónico participe en la transición al manejo del dolor a largo plazo. |
RESUMEN
Los últimos 25 años han visto una explosión en la investigación y el interés en el manejo del dolor pediátrico. En esta breve revisión hemos intentado consolidar de forma exhaustiva algunos de los agentes y técnicas más utilizados en la práctica actual.
Referencias
- Schechter NL, Berde CB, Yaster M: Dolor en bebés, niños y adolescentes, 2.ª ed. Filadelfia: Lippincott Williams & Wilkins; 2003.
- Yaster M, Krane EJ, Kaplan RF, et al: Manual de sedación y manejo del dolor pediátrico. Maryland Heights, MI: Mosby; 1997.
- Merskey H, Albe-Fessard DG, Bonica JJ: Términos de dolor: una lista con definiciones y notas sobre el uso. Recomendado por el Subcomité de Taxonomía de IASP. Dolor 1979;6:249–252.
- Anand KJ, Hickey PR: El dolor y sus efectos en el recién nacido y el feto humano. N Engl J Med 1987;317:1321–1329.
- Stevens B, Gibbins S, Franck LS: Tratamiento del dolor en la unidad de cuidados intensivos neonatales. Pediatr Clin North Am 2000;47:633–650.
- Fitzgerald M: Neurobiología del dolor fetal y neonatal. En: Wall PD, Melzack R (eds): Textbook of Pain, 3ra ed. Londres: Churchill Livingstone; 1994: 153–164.
- Lee SJ, Ralston HJ, Drey EA, et al: Dolor fetal: una revisión multidisciplinaria sistemática de la evidencia. JAMA 2005;294:947–954.
- Taddio A, Katz J, Ilersich AL, Koren G: Efecto de la circuncisión neonatal en la respuesta al dolor durante la vacunación de rutina posterior. Lancet 1997;349:599–603.
- Taddio A, Katz J: Los efectos de la experiencia temprana del dolor en los recién nacidos sobre las respuestas al dolor en la infancia y la niñez. Pediatr Drugs 2005;7:245–257.
- Adelante SP, Brown TL, McGrath PJ: Actitudes y comportamiento de las madres hacia la medicación del dolor de los niños. Dolor 1996;67:469–474.
- Finley GA, McGrath PJ, Forward SP, et al: Manejo del dolor de los niños por parte de los padres después de una cirugía 'menor'. Dolor 1996;64:83–87.
- Varni JW, Thompson KL, Hanson V: El cuestionario de dolor pediátrico de Varni/Thompson. I. Dolor musculoesquelético crónico en la artritis reumatoide juvenil. Dolor 1987; 28: 27–38.
- Thompson KL, Varni JW: Un enfoque cognitivo-bioconductual del desarrollo para la evaluación del dolor pediátrico. Dolor 1986; 25: 283–296.
- Beyer JE, Wells N: La evaluación del dolor en niños. Pediatr Clin North Am 1989;36:837–854.
- Beyer JE, Denyes MJ, Villarruel AM: La creación, validación y desarrollo continuo del Oucher: una medida de la intensidad del dolor en los niños. J Pediatr Nurs 1992;7:335–346.
- Wong DL, Baker CM: Dolor en niños: comparación de escalas de evaluación. Pediatr Nurs 1988;14:9–17.
- Franck LS, Greenberg CS, Stevens B: Evaluación del dolor en bebés y niños. Pediatr Clin North Am 2000;47:487–512.
- Anthony KK, Schanberg LE: Síndromes de dolor pediátrico y manejo del dolor en niños y adolescentes con enfermedad reumática. Pediatr Clin North Am 2005;52:611–639, vii.
- Krecher SW, Bildner J. CRIES: una puntuación de medición del dolor postoperatorio neonatal. Pruebas iniciales de validez y confiabilidad. Pediatr Anaesth 1995;5:53–65.
- Cunliffe M, Roberts SA: Manejo del dolor en niños. Curr Anaesth Crit Care 2004;15:272–283.
- Hunt A, Goldman A, Seers K, et al: Validación clínica del perfil de dolor pediátrico. Dev Med Child Neurol 2004;46(1):9–18.
- Rusy LM, Weisman SJ: Terapias complementarias para el manejo del dolor pediátrico agudo. Pediatr Clin North Am 2000;47:589–599.
- Berde CB, Sethna NF: Analgésicos para el tratamiento del dolor en niños. N Engl J Med 2002;347:1094–1103.
- Yaster M: Medicamentos antiinflamatorios no esteroideos. En: Yaster M, Krane EJ, Kaplan RF (eds): Manual de sedación y manejo del dolor pediátrico. Maryland Heights, MI: Mosby; 1997: 19–28.
- Tobias JD: Analgésicos débiles y agentes antiinflamatorios no esteroideos en el tratamiento de niños con dolor agudo. Pediatr Clin North Am 2000;47:527–543.
- Maunuksela EL, Kokki H, Bullingham RE: Comparación de ketorolaco intravenoso con morfina para el dolor posoperatorio en niños. Clin Pharmacol Ther 1992;52:436–443.
- Birmingham PK, Tobin MJ, Henthorn TK, et al: Farmacocinética de veinticuatro horas del paracetamol rectal en niños: un fármaco antiguo con nuevas recomendaciones. Anestesiología 1997;87:244–252.
- Rusy LM, Houck CS, Sullivan LJ, et al: Una evaluación doble ciego de ketorolaco trometamina versus paracetamol en amigdalectomía pediátrica: analgesia y sangrado. Anesth Analg 1995;80:226–229.
- Vane JR, Botting RM: Mecanismo de acción de los fármacos antiinflamatorios no esteroideos. Am J Med 1998;104:2S–8S; discusión 21S–2.
- Vane JR, Botting RM: Mecanismo de acción de los fármacos similares a la aspirina. Semin Arthritis Rheum 1997;26:2–10.
- Jouzeau JY, Terlain B, Abid A, et al: Cyclo-oxygenase isoenzymes. Cómo los hallazgos recientes afectan el pensamiento sobre los medicamentos antiinflamatorios no esteroideos. Drogas 1997;53:563–582.
- Cashman JN: Los mecanismos de acción de los AINE en la analgesia. Drugs 1996;52(Suplemento 5):13–23.
- Vane JR, Bakhle YS, Botting RM: Ciclooxigenasas 1 y 2. Annu Rev Pharmacol Toxicol 1998;38:97–120.
- Johnsen SP, Larsson H, Tarone RE, et al: Riesgo de hospitalización por infarto de miocardio entre usuarios de rofecoxib, celecoxib y otros AINE: un estudio de casos y controles basado en la población. Arch Intern Med 2005; 165:978–984.
- Levesque LE, Brophy JM, Zhang B: El riesgo de infarto de miocardio con inhibidores de la ciclooxigenasa-2: un estudio poblacional de adultos mayores. Ann Intern Med 2005;142:481–489.
- Dahners LE, Mullis BH: Efectos de los fármacos antiinflamatorios no esteroideos sobre la formación ósea y la cicatrización de los tejidos blandos. J Am Acad Orthop Surg 2004;12:139–143.
- Simon AM, Manigrasso MB, O'Connor JP: La función de ciclooxigenasa 2 es esencial para la curación de fracturas óseas. J Bone Miner Res 2002;17:963–976.
- Einhorn TA: Cox-2: ¿Dónde estamos en 2003? El papel de la ciclooxigenasa-2 en la reparación ósea. Arthritis Res Ther 2003;5:5–7.
- Radnay PA, Duncalf D, Novakovic M, Lesser ML: Cambios en la presión del conducto biliar común después de fentanilo, morfina, meperidina, butorfanol y naloxona. Anesth Analg 1984;63:441–444.
- Krane EJ, Yaster M: Transición a una terapia menos invasiva. En: Yaster M, Krane EJ, Kaplan RF, et al (eds): Manual de sedación y manejo del dolor pediátrico. Maryland Heights, MI: Mosby; 1997: 147–162.
- Ciszkowski C, Madadi P. Codeína, genotipo de metabolismo ultrarrápido y muerte posoperatoria. N Engl J Med 2009;361(8):827–828.
- Kelly LE, Rieder M, van den Anker J, et al. Más muertes por codeína después de la amigdalectomía en niños norteamericanos. Pediatría 2012;129(5): e1343–1347. doi: 10.1542/peds.2011-2538.
- Ingelman-Sundberg M, Oscarson M, McLellan RA. Enzimas polimórficas del citocromo P450 humano: una oportunidad para el tratamiento farmacológico individualizado. Tendencias Pharmacol Sci 1999;20(8):342–349.
- Administración de Drogas y Alimentos de los Estados Unidos (FDA). Comunicaciones de seguridad de medicamentos: actualización de la revisión de seguridad del uso de codeína en niños; nuevo recuadro de advertencia y contraindicación de uso después de amigdalectomía y/o adenoidectomía. http://www.fda.gov/downloads/Drugs/DrugSafety/UCM339116.pdf. Publicado el 20 de febrero de 2013. Consultado el 26 de febrero de 2013.
- Agencia Europea de Medicamentos (EMA). PRAC recomienda restringir el uso de codeína cuando se usa para aliviar el dolor en niños. http://www.ema.europa.eu/docs/en_GB/document_library/Press_release/2013/06/WC500144444.pdf. Publicado el 14 de junio de 2013. Consultado el 18 de junio de 2013.
- Tremlett M, Anderson BJ, Wolf A. Debate a favor y en contra: ¿es la codeína un fármaco que todavía tiene un papel útil en la práctica pediátrica? Pediatr Anaesth 2010;20(2):183–194.
- Heubi JE, Barbacci MB, Zimmerman HJ: Desventuras terapéuticas con paracetamol: hepatotoxicidad después de múltiples dosis en niños. J Pediatr 1998;132:22–27.
- Viitanen H, Annila P: Eficacia analgésica de tramadol 2 mg kg–1 para adenoidectomía pediátrica ambulatoria. Br. J. Anaesth 2001;86(4):572–575.
- Berde CB, Lehn BM, Yee JD, Sethna NF, Russo D: Analgesia controlada por el paciente en niños y adolescentes: una comparación prospectiva aleatoria con la administración intramuscular de morfina para la analgesia posoperatoria. J Pediatr 1991;118:460–466.
- Yaster M, Billett C, Monitto C: Analgesia intravenosa controlada por el paciente. En: Yaster M, Krane EJ, Kaplan RF, et al (eds): Manual de sedación y manejo del dolor pediátrico. Maryland Heights, MI: Mosby; 1997: 89–112.
- Monitto CL, Greenberg RS, Kost-Byerly S, et al: La seguridad y eficacia de la analgesia controlada por padres/enfermeros en pacientes menores de seis años. Anesth Analg 2000;91:573–579.
- Galinkin JL, Fazi LM, Cuy RM, et al: Uso de fentanilo intranasal en niños sometidos a miringotomía y colocación de sonda durante la anestesia con halotano y sevoflurano. Anestesiología 2000;93:137–383.
- Schechter NL, Weisman SJ, Rosenblum M, et al: El uso de citrato de fentanilo transmucoso oral para procedimientos dolorosos en niños. Pediatría 1995;95:335–339.
- Goldstein-Dresner MC, Davis PJ, Kretchman E, et al: Comparación doble ciego de citrato de fentanilo transmucoso oral con meperidina oral, diazepam y atropina como medicación preanestésica en niños con cardiopatía congénita. Anestesiología 1991;74:28–33.
- Streisand JB, Stanley TH, Hague B, et al: Premedicación oral transmucosa con citrato de fentanilo en niños. Anesth Analg 1989;69:28–34.
- Stanley TH, Hague B, Mock DL, et al: Premedicación oral transmucosa con citrato de fentanilo (piruleta) en voluntarios humanos. Anesth Analg 1989;69:21–27.
- Ashburn MA, Lind GH, Gillie MH, et al: Citrato de fentanilo transmucoso oral (OTFC) para el tratamiento del dolor posoperatorio. Anesth Analg 1993;76:377–381.
- Streisand JB, Varvel JR, Stanski DR, et al: Absorción y biodisponibilidad del citrato de fentanilo transmucoso oral. Anestesiología 1991;75:223–229.
- Dsida RM, Wheeler M, Birmingham PK, et al: Premedicación de pacientes con amigdalectomía pediátrica con citrato de fentanilo transmucoso oral. Anesth Analg 1998;86:66–70.
- Portenoy RK, Payne R, Coluzzi P, et al: Citrato de fentanilo transmucoso oral (OTFC) para el tratamiento del dolor irruptivo en pacientes con cáncer: un estudio de titulación de dosis controlada. Dolor 1999;79:303–312.
- Epstein RH, Mendel HG, Witkowski TA, et al: La seguridad y eficacia del citrato de fentanilo transmucoso oral para la sedación preoperatoria en niños pequeños. Anesth Analg 1996;83:1200–1205.
- Grond S, Radbruch L, Lehmann KA: Farmacocinética clínica de los opioides transdérmicos: Centrarse en el fentanilo transdérmico. Clin Pharmacokinet 2000;38:59–89.
- Chelly JE, Grass J, Houseman TW, et al: La seguridad y eficacia de un sistema transdérmico de fentanilo controlado por el paciente para la analgesia posoperatoria aguda: un ensayo multicéntrico controlado con placebo (tabla). Anesth Analg 2004;98:427–433.
- Yaster M, Kost-Byerly S, Maxwell LG: Agonistas y antagonistas de opioides. En: Schechter NL, Berde CB, Yaster M (eds: Pain in Infants, Children, and Adolescents, 2nd ed. Philadelphia: Lippincott Williams & Wilkins; 2003:181–224.
- Watcha MF, White PF: Náuseas y vómitos postoperatorios. Su etiología, tratamiento y prevención. Anestesiología 1992;77:162–184.
- Gan TJ, Ginsberg B, Glass PS, et al: Efectos ahorradores de opioides de una infusión de dosis baja de naloxona en sulfato de morfina administrado al paciente. Anestesiología 1997;87:1075–1081.
- Maxwell LG, Kaufmann SC, Bitzer S, et al: Los efectos de una infusión de naloxona en dosis pequeñas sobre los efectos secundarios inducidos por opioides y la analgesia en niños y adolescentes tratados con analgesia intravenosa controlada por el paciente: un estudio doble ciego, prospectivo, aleatorizado, estudio controlado. Anesth Analg 2005;100:953–958.
- Dalens B: Anestesia regional en niños. Anesth Analg 1989;68:654–672.
- Giaufre E, Dalens B, Gombert A: Epidemiología y morbilidad de la anestesia regional en niños: una encuesta prospectiva de un año de la Sociedad de Anestesiólogos Pediátricos de Lengua Francesa. Anesth Analg 1996;83:904–912.
- Yaster M, Maxwell LG: Anestesia regional pediátrica. Anestesiología 1989;70:324–338.
- Ross AK, Eck JB, Tobias JD: Anestesia regional pediátrica: más allá de la caudal. Anesth Analg 2000;91:16–26.
- Golianu B, Krane EJ, Galloway KS, Yaster M: Manejo del dolor agudo pediátrico. Pediatr Clin North Am 2000;47:559–587.
- Dauri M, Faria S, Gatti A, et al: Gabapentina y pregabalina para el manejo del dolor posoperatorio agudo. Una revisión sistémica-narrativa de evidencias clínicas recientes. Curr Drug Targets 2009;10:716–733.
- Ucak A, Onan B, Sen H, Selcuk I, Turan A, Yilmaz AT: Los efectos de la gabapentina en el dolor posoperatorio agudo y crónico después de la cirugía de injerto de derivación de la arteria coronaria. J Cardiothorac Vasc Anaesth 2011;25:824–829.
- Clarke H, Pereira S, Kennedy D, et al: La gabapentina disminuye el consumo de morfina y mejora la recuperación funcional después de la artroplastia total de rodilla. Pain Res Manag 2009;14:217–222.
- Rusy LM, Hainswork KR, Nelson TJ, et al. Uso de gabapentina en pacientes pediátricos con fusión espinal: un ensayo aleatorizado, doble ciego y controlado. Anesth Analg 2010;110:1393–1398.
- Green SM, Cote CJ: Ketamina y neurotoxicidad: perspectiva clínica e implicaciones para la medicina de emergencia. Ann Emerg Med 2009;54:181–190.
- Bambrink AM, Evers AS, Avidan MS, et al: Ketamina inducida por neuroapoptosis en el cerebro del macaco rhesus fetal y neonatal. Anestesialogía 2012;116: 372–384.
- Iseri LT, francés JH. Magnesio: bloqueador de calcio fisiológico de la naturaleza. Am Heart J 1984; 108: 188–193.
- Woolf CJ, Thompson SW. La inducción y el mantenimiento de la sensibilización central dependen de la activación del receptor del ácido N-metil-D-aspártico: implicaciones para el tratamiento de los estados de hipersensibilidad al dolor posteriores a la lesión. Dolor 1991;44:293–299.
- Albrecht E, Kirkham KR, Liu SS, Brull R: Administración intravenosa perioperatoria de sulfato de magnesio y dolor posoperatorio: un metanálisis. Anestesia 2013;68:79–90.
- Turk, DC, Okifuji A. Dolor y términos y taxonomías. En: Loeser D, Butler SH, Chapman JJ, et al. Manejo del dolor de Bonica, 3ª ed. Filadelfia: Lippincott Williams & Wilkins; 2001: 18–25.
- Fortier MA, Chou J, Muarer EL, Kain ZN. Dolor postoperatorio agudo a crónico en niños: hallazgos preliminares. J Ped Surg 2011;46:1700–1705.
- Wong GTC, Yuen VMY, Chow BFM, Irwin MG. Dolor persistente en pacientes después de la cirugía de escoliosis. Eur Spine J 2007;18:1551–1556.