1. INTRODUCTION
Étant capable d'une large gamme de mouvements articulés et de rotation, le coude est intrinsèquement prédisposé aux blessures aiguës et aux changements dégénératifs. Bien que l'examen clinique et la radiographie de routine soient essentiels pour évaluer les troubles du coude, l'échographie est devenue de plus en plus importante dans l'investigation diagnostique de plusieurs anomalies affectant les tendons et les muscles, les articulations, les ligaments, les nerfs et d'autres structures des tissus mous autour de l'articulation du coude. Après l'examen américain, une tomodensitométrie et une IRM peuvent être nécessaires pour examiner plus en détail l'état de la cavité articulaire, du cartilage articulaire et de l'os.
2. ANATOMIE CLINIQUE
Une brève description de l'anatomie complexe du coude en mettant l'accent sur les caractéristiques anatomiques se prêtant à l'examen américain, y compris les articulations et les complexes ligamentaires, les muscles et les tendons, les structures neurovasculaires et les bourses, est incluse ici.
3. COMPLEXES ARTICULAIRES ET LIGAMENTAIRES
Le coude est composé de trois articulations - radiocapitellaire, radio-ulnaire proximale et trochlée-ulna - partageant une cavité articulaire commune et stabilisées par un certain nombre de structures de tissus mous, y compris les ligaments collatéraux latéral et médial et la partie antérieure de l'articulation capsule.
4. COUDE
Les structures osseuses autour de l'articulation du coude comprennent les extrémités proximales de l'ulna et du radius et l'extrémité distale de l'humérus (Fig. 1). La tête radiale s'articule avec le capitellum huméral en mode pivot et le cubitus avec la trochlée humérale en mode charnière. L'articulation radio-ulnaire proximale est composée de la tête radiale qui s'articule dans l'échancrure sigmoïde (radiale) de l'ulna permettant les mouvements de pronation-supination. Ces articulations coopèrent lors de mouvements articulaires complexes permettant un large degré de flexion, d'extension et de rotation axiale. La congruence des surfaces articulaires apposées varie selon les positions du coude et est maximale avec le coude fléchi à 90° et l'avant-bras à mi-chemin entre la pronation complète et la supination complète. La trochlée humérale, l'échancrure trochléenne de l'ulna et la tête radiale, à l'exception de sa partie antérolatérale, sont recouvertes d'un cartilage articulaire d'environ 2 mm d'épaisseur.
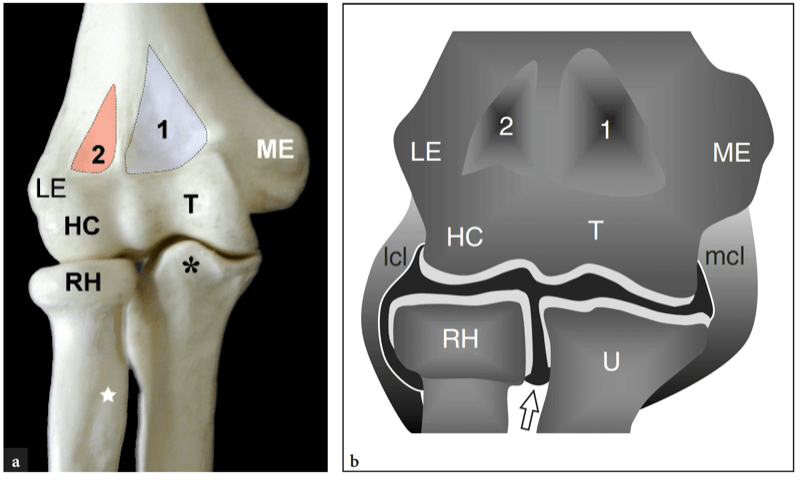
Figures 1a,b. Articulation du coude. Anatomie articulaire. a La face antérieure des os du coude illustre les relations de la trochlée (T) et du capitellum (HC) de l'humérus distal avec le processus coronoïde de l'ulna (astérisque) et la tête radiale (RH). Le capitellum de l'humérus s'articule avec la facette supérieure de la tête radiale formant l'articulation radio-capitellaire, et la trochlée de l'humérus s'articule avec l'échancrure trochléenne de l'ulna, formant l'articulation huméro-ulnaire. Observer les épicondyles médial (ME) et latéral (LE) et les fosses coronoïde (1) et radiale (2) de l'humérus. Étoile, tubérosité radiale. b Le dessin schématique d'une vue coronale à travers le coude montre l'extension de la cavité articulaire (en noir). Notez les ligaments collatéraux latéral (lcl) et médial (mcl) qui délimitent la cavité articulaire de chaque côté et la poche (flèche) de l'articulation du coude entre le radius et le cubitus formant l'articulation radio-ulnaire supérieure.
Le coude est l'une des articulations les plus stables du corps. Dans des états normaux, le mouvement de l'articulation du coude varie approximativement de 0° à 150° de flexion et de 75° en pronation à 85° en supination. L'extension du coude est limitée par le contact de l'olécrane dans la fosse humérale postérieure et le resserrement de la bande antérieure du ligament collatéral médial, de la capsule articulaire et des muscles fléchisseurs. En revanche, l'encombrement des muscles antérieurs du bras, la tension du triceps et le contact de l'apophyse coronoïde dans la fosse humérale antérieure limitent la flexion du coude. Les mouvements de pronation et de supination sont principalement limités par des contraintes musculaires passives plutôt que par des ligaments.
La capsule articulaire investit tout le coude. En avant, il est attaché à la diaphyse humérale juste au-dessus des fosses coronoïde et radiale, à la face antérieure du processus coronoïde et au ligament annulaire. Il est tendu en extension du coude et lâche en flexion du coude. En arrière, la capsule s'insère sur la face postérieure de l'humérus au-dessus de la fosse olécrânienne et jusqu'aux bords supérieurs de l'olécrâne. Le volume antérieur du muscle brachial, le volume postérieur du triceps et, de chaque côté, les ligaments collatéraux médial et latéral renforcent la capsule. La membrane synoviale de l'articulation du coude enveloppe la surface interne de la capsule et le ligament annulaire (Fig. 1b). Il se replie entre le radius et le cubitus et produit trois principaux évidements synoviaux. Le plus grand renfoncement est le renfoncement olécrânien (huméral postérieur) qui comprend une poche supérieure, médiale et latérale (Fig. 2). Sur le coude antérieur, l'évidement coronoïde (huméral antérieur) s'étend sur les fosses coronoïde et radiale de l'humérus, tandis que l'évidement annulaire (périradial) entoure le collet radial. Deux petits évidements supplémentaires sont situés en profondeur des ligaments collatéraux médial et latéral. Certains coussinets adipeux se situent entre la capsule fibreuse et la membrane synoviale dans un emplacement extrasynovial mais intra-articulaire. Les plus grands remplissent les fosses coronoïde et radiale de l'humérus sous le muscle brachial, et la fosse olécrânienne profonde jusqu'au muscle triceps (Fig. 2). Tout processus expansible intra-articulaire provoque le déplacement et l'élévation de ces coussinets graisseux. Un pli synovial en croissant, communément appelé « frange synoviale latérale », peut être retrouvé au niveau de l'articulation radiocapittelaire. Semblable au plicae du genou, cette frange représente un vestige septal (Clarke 1988) et peut provoquer des symptômes, tels que le blocage et le claquement du coude, secondaires à son piégeage dans l'articulation radio-capitelle. D'autres plicae synoviaux peuvent se projeter dans le récessus huméral antérieur à partir du coussinet adipeux antérieur et dans le récessus olécrânien à partir du coussinet adipeux postérieur, cette dernière localisation étant plus souvent associée à des symptômes cliniques (verrouillage du coude). Ils peuvent rarement imiter un corps lâche intra-articulaire (Awaya et al. 2001).
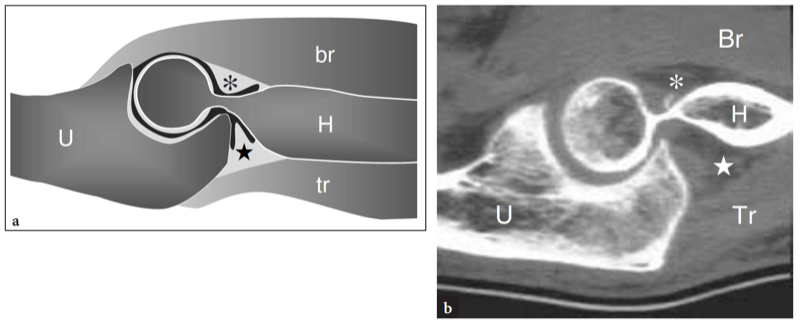
Figures 2a,b. Articulation du coude. Anatomie articulaire. a Dessin schématique d'une vue sagittale médiane à travers un coude étendu avec une corrélation de tomodensitométrie b montrant la relation articulaire entre la trochlée de l'humérus (H) et la rainure trochléaire de l'ulna (U), entraînant des mouvements de flexion et d'extension des articulations. Les coussinets adipeux extrasynoviaux antérieur (astérisque) et postérieur (étoile) sont étroitement appliqués à l'extrémité distale de l'humérus et se situent juste à la surface de l'espace articulaire (en noir). Notez l'insertion des muscles brachial (Br) et triceps (tr), qui sont respectivement les principaux muscles fléchisseurs et extenseurs du coude.
5. LIGAMENT COLLATÉRAL MÉDIAL
Le complexe ligamentaire collatéral médial, également appelé ligament collatéral ulnaire, est composé de trois bandes en continuité entre elles : antérieure, postérieure et oblique (Fig. 3a). La bande antérieure est la plus visible et s'étend de l'épicondyle médial à la face médiale du processus coronoïde, fournissant la contrainte majeure au stress en valgus. La bande postérieure provient de la face postérieure de l'épicondyle médial et s'insère dans le bord médial de l'olécrâne. La bande oblique, communément appelée «ligament de Cooper», est la plus faible et relie les insertions des bandes antérieure et postérieure sur l'ulna.
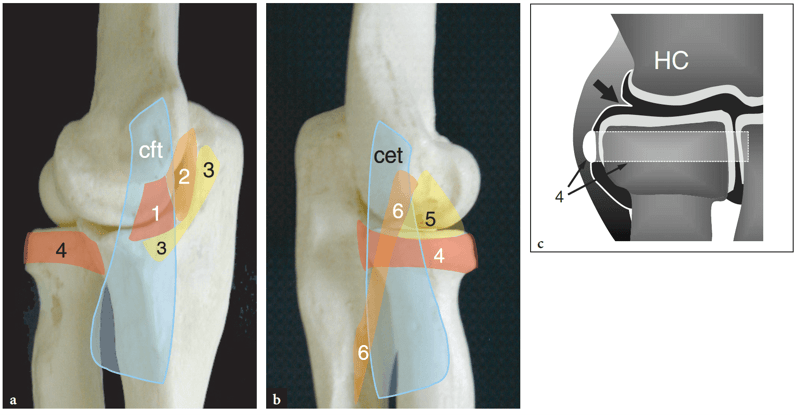
Fig. 3a–c. Ligaments collatéraux du coude. a Vue médiale des os du coude montrant la position du ligament collatéral médial, y compris sa bande antérieure (1), sa bande postérieure (2) et son ligament transverse (3). Notez que l'origine du tendon fléchisseur commun (cft) se situe juste en surface des structures ligamentaires médiales. La face médiale du ligament annulaire (4) est également représentée. b Vue latérale du coude montrant la position du complexe ligamentaire collatéral latéral, comprenant le ligament annulaire (4), le ligament collatéral radial (5) et le ligament collatéral ulnaire latéral (6) par rapport à l'origine du tendon extenseur commun (cet) . En a et b, on voit le ligament annulaire (4) encerclant la tête radiale et s'attachant aux bords de l'échancrure radiale de l'ulna. c Le dessin schématique d'une vue coronale du coude latéral illustre la position du ligament annulaire (4) par rapport aux structures articulaires et à la cavité articulaire (en noir). Notez la frange synoviale latérale (flèche) contiguë à la ligne articulaire. HC, capitule de l'humérus distal.
6. LIGAMENT COLLATÉRAL LATÉRAL
Le complexe ligamentaire collatéral latéral est plus variable que le complexe médial. Il se compose du ligament collatéral radial, du ligament annulaire, du ligament collatéral ulnaire latéral et du ligament collatéral latéral accessoire (Fig. 3b). Le ligament collatéral radial est une bande épaisse de tissu fibreux qui provient de l'épicondyle latéral et s'insère sur l'échancrure radiale de l'ulna, se confondant avec les fibres du ligament annulaire. Le ligament annulaire est un ligament solide qui entoure la tête radiale et la maintient en contact avec l'ulna en s'insérant sur les bords antérieur et postérieur de l'échancrure radiale de ce dernier os (Fig. 3). Dans son petit axe, le ligament annulaire présente un profil en forme de croissant d'aspect interne lisse et est recouvert d'une membrane synoviale (Fig. 3c). Proxicalement, les fibres du ligament annulaire se confondent avec la capsule articulaire et avec le ligament collatéral radial adjacent. Le ligament annulaire maintient la tête radiale en contact étroit avec le cubitus empêchant son retrait ou son déplacement inférieur hors de son alvéole. Le ligament collatéral ulnaire latéral provient de l'épicondyle latéral et se confond avec les fibres du ligament annulaire jusqu'à l'origine du tendon extenseur commun (Fig. 3b). Il reste tendu dans toute la gamme des mouvements de flexion-extension du coude et joue un rôle essentiel de stabilisateur latéral de l'articulation trochlée-cubitus.

Fig. 3a–c. Ligaments collatéraux du coude. a Vue médiale des os du coude montrant la position du ligament collatéral médial, y compris sa bande antérieure (1), sa bande postérieure (2) et son ligament transverse (3). Notez que l'origine du tendon fléchisseur commun (cft) se situe juste en surface des structures ligamentaires médiales. La face médiale du ligament annulaire (4) est également représentée. b Vue latérale du coude montrant la position du complexe ligamentaire collatéral latéral, comprenant le ligament annulaire (4), le ligament collatéral radial (5) et le ligament collatéral ulnaire latéral (6) par rapport à l'origine du tendon extenseur commun (cet) . En a et b, on voit le ligament annulaire (4) encerclant la tête radiale et s'attachant aux bords de l'échancrure radiale de l'ulna. c Le dessin schématique d'une vue coronale du coude latéral illustre la position du ligament annulaire (4) par rapport aux structures articulaires et à la cavité articulaire (en noir). Notez la frange synoviale latérale (flèche) contiguë à la ligne articulaire. HC, capitule de l'humérus distal.
7. MUSCLES ET TENDONS
Les muscles et les tendons autour du coude peuvent être subdivisés selon leur position en antérieur, médial, latéral et postérieur.
8. COUDE ANTÉRIEUR
Le groupe antérieur de muscles et de tendons comprend le biceps brachial et le brachial qui se situent dans la région cubitale entre le muscle brachioradialis latéralement et le muscle rond pronateur médialement. Le muscle biceps brachial est situé à la surface du brachial et possède un long tendon distal qui n'est pas entouré de muscle, ce qui le rend plus susceptible aux blessures que le brachial (Fig. 4). Le tendon distal du biceps est un tendon aplati qui dérive de l'union des deux ventres musculaires, les têtes longue et courte, du muscle biceps brachial qui se rejoignent dans la partie inférieure du bras. Il mesure environ 7 cm de long et s'incurve latéralement et en profondeur avant de s'insérer sur la face médiale de la tubérosité radiale. Il présente également une expansion aponévrotique aplatie, communément appelée «lacertus fibrosus», qui s'étend de la jonction myotendineuse au fascia profond médial de l'avant-bras. Cette aponévrose recouvre le nerf médian et l'artère brachiale et contribue à maintenir le tendon du biceps situé dans la bonne position (Fig. 4b, c). La partie distale du tendon du biceps est recouverte d'un paraténon extrasynovial et est séparée de la tubérosité radiale par une bourse intermédiaire, la bourse bicipitoradiale, qui n'est normalement pas visible à l'échographie à moins qu'elle ne soit distendue par un épanchement liquidien. Le biceps est un puissant fléchisseur du coude ; lorsque l'avant-bras est en supination, il agit également comme un supinateur. Au plus profond du biceps brachial, le muscle brachial naît de la surface antérieure de la moitié distale de l'humérus et des septa intermusculaires médial et latéral adjacents et s'étend le long de la capsule articulaire antérieure pour s'insérer sur la surface antérieure du processus coronoïde et de la tubérosité ulnaire. . Son tendon est plus fin que le tendon du biceps et est entouré par les ventres musculaires jusqu'à son insertion. Le brachial agit essentiellement comme un fléchisseur du coude quelle que soit la position de l'avant-bras.
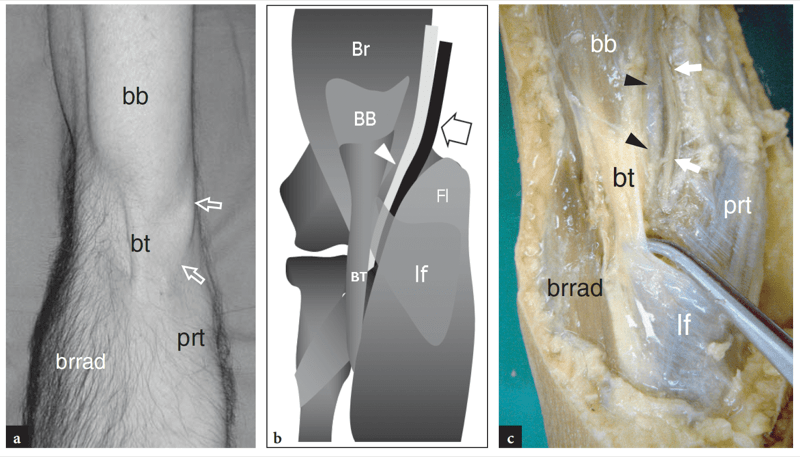
Fig. 4a–c. Anatomie de la fosse cubitale. a Photographie de la face antérieure du coude chez un jeune homme montrant les principales caractéristiques de surface visibles lors de la contraction résistée du muscle biceps en gardant le coude tendu et la main en supination. Au cours de cette action, le tendon distal (bt) du muscle biceps brachial (bb) devient proéminent sur la peau et peut être palpé lors de son passage à travers la fosse mi-antécubitale située entre les masses des muscles extenseurs - représentés par le brachioradial ( brrad) – et les muscles fléchisseurs – représentés par le rond pronateur (prt). Notez la proéminence de la veine basilique (flèches) par rapport au tendon distal du biceps. b Le dessin schématique d'une vue coronale du coude illustre la position du tendon du biceps (bt) et du lacertus fibrosus (lf) par rapport au groupe de muscles fléchisseurs-pronateurs (fl ), l'artère brachiale (tête de flèche) et le nerf médian (La Flèche). br, muscle brachial. c La dissection grossière du coude antérieur révèle la fosse cubitale délimitée par les muscles brachioradialis (brrad) et pronator teres (prt). Observez que l'artère brachiale (têtes de flèches) et le nerf médian (flèches) cheminent le long du muscle biceps (bb) et du tendon (bt) puis profondément jusqu'au lacertus fibrosus (of).
9. COUDE MEDIAL
Le compartiment médial comprend le rond pronateur et les muscles fléchisseurs superficiels du poignet et de la main qui découlent de l'épicondyle médial en tant que « tendon fléchisseur commun ». Le rond pronateur est le plus superficiel et le plus antérieur des muscles médiaux. Il a deux attaches proximales : l'une (tête humérale) immédiatement proximale à l'épicondyle médial et au tendon fléchisseur commun, l'autre (tête ulnaire) à la face médiale du processus coronoïde. Distalement, le rond pronateur s'insère le long de la surface latérale de l'arbre radial à travers un tendon plat (Fig. 5a). Le nerf médian passe entre les deux ventres du rond pronateur et est séparé de l'artère ulnaire par la tête ulnaire de ce muscle (Fig. 5). Lors de la pronation de l'avant-bras, le rond pronateur travaille avec le carré pronateur. Il existe quatre muscles fléchisseurs superficiels de la main et du poignet qui découlent du tendon fléchisseur commun, disposés de manière médiale ou latérale comme le fléchisseur radial du carpe, le long palmaire, le fléchisseur superficiel des doigts et le fléchisseur ulnaire du carpe. Le fléchisseur profond des doigts a une origine plus distale distincte de la face antéro-médiale de l'ulna, du processus coronoïde et de la surface antérieure de la membrane interosseuse. Les muscles fléchisseurs superficiels et profonds sont les principaux fléchisseurs du poignet et des doigts. De plus, le tendon fléchisseur commun fournit un soutien dynamique au ligament collatéral ulnaire sous-jacent pour résister au stress en valgus.
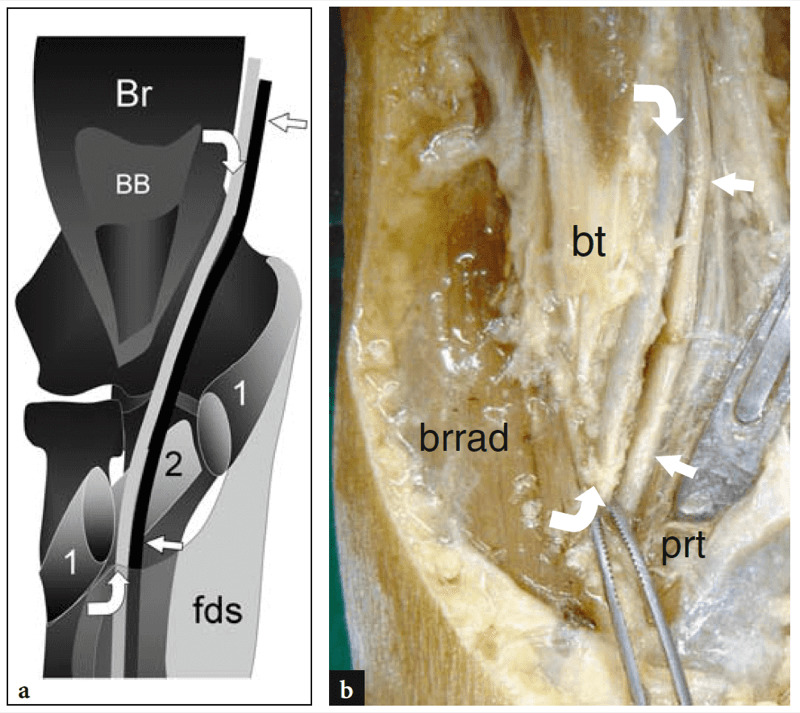
Figures 5a,b. Artère brachiale et nerf médian. a Même dessin schématique que la Fig. 8.4b après ablation du tendon distal du biceps et du ventre huméral superficiel du muscle rond pronateur (1) révèle le trajet de l'artère brachiale (têtes de flèches) et du nerf médian adjacent (flèches droites) dans le zone pronatrice et sous le « pont sublimis » (flèche courbée) du muscle fléchisseur superficiel des doigts (fds). Br, muscle brachial ; BB, muscle biceps ; 2, ventre profond (ulnaire) du muscle rond pronateur. b La dissection grossière de la fosse cubitale montre l'artère brachiale (flèches courbes) et le nerf médian (flèches droites) lorsqu'ils se replient dans l'espace entre les muscles brachioradialis (brrad) et pronator teres (prt). Le tendon distal du biceps (bt) a été précédemment retiré.
10. COUDE LATÉRAL
La loge latérale du coude comprend les muscles extenseurs du poignet et de la main qui naissent de l'épicondyle latéral en tant que « tendon extenseur commun », le brachioradialis, le long extensor carpi radialis longus et les muscles supinateurs. Le tendon extenseur commun est un tendon aplati qui prend naissance sur la face antérolatérale de l'épicondyle latéral. Il reçoit des contributions de fibres de quatre muscles extenseurs superficiels : extensor carpi radialis brevis, extensor digitorum communis, extensor digiti minimi et extensor carpi ulnaris. L'extensor carpi radialis brevis constitue la plupart des fibres articulaires profondes, tandis que l'extensor digitorum contribue à la partie superficielle du tendon extenseur commun (Connell et al. 2001). L'extenseur digiti minimi et le carpi ulnaris ne fournissent que des composants mineurs au tendon extenseur commun. Globalement, ces muscles jouent le rôle d'extenseurs du poignet et/ou des doigts et jouent également un rôle dans la déviation radiale (extensor carpi radialis brevis) et ulnaire (extensor carpi ulnaris) du poignet. L'origine du tendon extenseur commun est séparée de la capsule articulaire par le ligament collatéral ulnaire latéral. Crânien et séparément du tendon extenseur commun, les muscles brachioradialis (antérieur) et extensor carpi radialis longus (postérieur) naissent de la crête supracondylienne de l'humérus et du septum intermusculaire latéral. Le supinateur est le plus profond des muscles latéraux. Il possède deux têtes entre lesquelles passe le nerf interosseux postérieur, branche motrice du nerf radial, pour atteindre le coude postérieur (Fig. 6a). La tête superficielle naît de l'épicondyle latéral, des ligaments collatéraux et annulaires latéraux et de l'arrière de la crête supinatrice et de la fosse de l'ulna ; la tête profonde provient de la fosse supinatrice de l'ulna. Ce muscle dans son ensemble s'enroule autour du collet radial pour s'insérer dans la face proximale de la diaphyse radiale (Fig. 6b). Chez jusqu'à 35 % des individus, l'origine de la tête superficielle s'unit pour former un arc fibreux, communément appelé "arcade de Frohse" (Fig. 6c). Le muscle supinateur agit en synergie avec le biceps pour supiner l'avant-bras lorsque le coude est en extension.
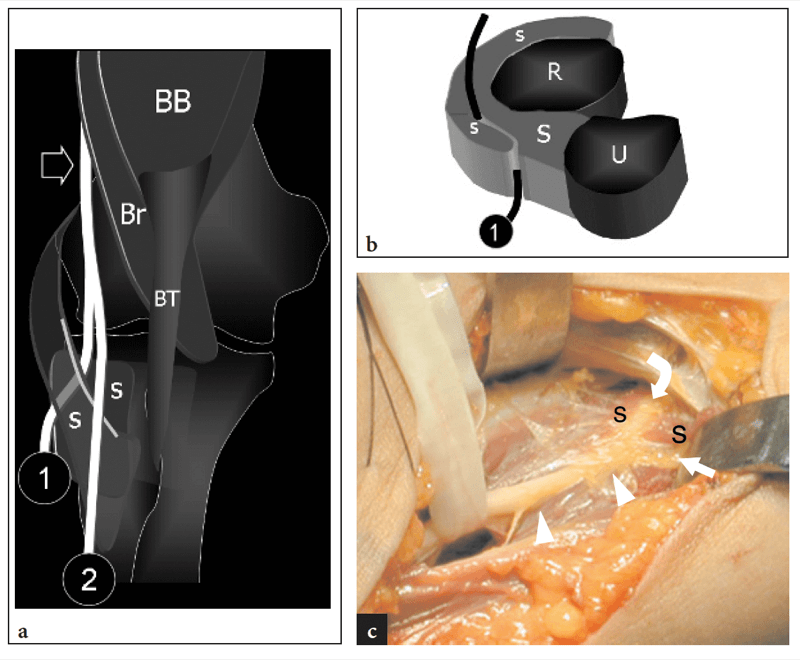
Fig. 6a–c. Nerf radial et nerf interosseux postérieur. un dessin schématique d'une vue coronale du coude montre le trajet du tronc principal du nerf radial (flèche) qui se trouve latéralement au muscle brachial (br) et se divise ensuite en ses branches terminales, le nerf interosseux postérieur (1) et la branche sensorielle superficielle (2). Au niveau du col radial, le nerf interosseux postérieur traverse le ou les muscles supinateurs pour atteindre la loge postérieure du coude. bb, muscle biceps ; bt, tendon du biceps. b Le dessin d'une coupe transversale à travers l'avant-bras proximal montre les ventres du ou des muscles supinateurs et le nerf interosseux postérieur (1) qui passe entre eux. U, cubitus ; R, rayon. c Aspect opératoire brut de la zone supinatrice. Remarquez le nerf radial (têtes de flèches) qui se divise en nerf sensitif cutané (flèche courbe) et en nerf interosseux postérieur (flèche droite) juste avant que ce dernier n'entre dans le(s) muscle(s) supinateur(s).
11. COUDE POSTÉRIEUR
La loge postérieure comprend les muscles triceps et anconé. Le triceps est un gros muscle composé de trois têtes - médiale, latérale et longue - dont il tire son nom. Les ventres musculaires convergent en un seul tendon épais qui s'attache sur la face postérieure du processus olécrânien. Pour augmenter la force d'extension de l'articulation du coude, le tendon du triceps ne s'insère pas sur la pointe de l'olécrane, mais à environ 1 cm en aval de celle-ci. Sur la face latérale de l'olécrâne, à l'opposé du tunnel cubital, le muscle anconé est un petit muscle triangulaire qui naît de la face postérieure de l'épicondyle latéral pour s'insérer plus distalement sur la face postérolatérale supérieure de la diaphyse de l'ulna. Il contribue à la masse des tissus mous dorsolatéral du coude, assiste le triceps dans l'extension du coude et fournit un soutien dynamique au ligament collatéral ulnaire latéral sous-jacent pour résister au stress varus.
L'épitrochléaire anconé est un petit muscle accessoire (prévalence allant de 1 % à 34 %) qui forme le toit du tunnel cubital, remplace le rétinaculum d'Osborne et relie la face postérieure de l'épicondyle médial à la face médiale de l'olécrâne. Ce muscle est souvent bilatéral et peut provoquer une neuropathie ulnaire en occupant de l'espace dans le tunnel cubital et en diminuant son volume libre lors de la flexion complète du coude. Quelque peu équivalente à l'épitrochléaire anconé, une jonction myotendineuse anormale du triceps peut également être proéminente sur le côté postéro-médial du tunnel cubital.
12. STRUCTURES NEUROVASCULAIRES
Le coude est traversé par les nerfs cubital, médian et radial qui traversent respectivement ses faces postéro-médiale, antérieure et latérale. Au niveau du coude, le nerf médian est accompagné de l'artère brachiale, le nerf radial dégage une branche motrice principale, le nerf interosseux postérieur, et le nerf cubital traverse un tunnel ostéofibreux, le tunnel cubital.
13. NERF MÉDIAN ET ARTÈRE BRACHIALE
Dans la fosse cubitale, le nerf médian passe derrière le lacertus fibrosus et superficiel par rapport au muscle brachial. Plus distalement, il s'approfondit progressivement pour passer entre les têtes ulnaire et humérale du muscle rond pronateur chez plus de 80 % des individus. Au coude, le nerf médian donne de petites branches musculaires au rond pronateur, au long palmaire, au fléchisseur radial du carpe et au fléchisseur ulnaire du carpe. Ensuite, il chemine en profondeur jusqu'au pont tendineux reliant les têtes huméro-ulnaire et radiale du muscle fléchisseur superficiel des doigts, le pont dit sublimis.
Au coude, l'artère brachiale est superficielle et longe le bord médial du muscle biceps et du tendon recouvrant le brachial. Ensuite, il passe entre le nerf médian (médial) et le tendon du biceps (latéral) sous l'aponévrose bicipitale pour se diviser, au niveau de l'avant-bras proximal, en artères radiale et ulnaire.
14. NERF RADIAL ET NERF INTEROSSE POSTERIEUR
Au niveau du coude proximal, le nerf radial est situé entre le brachial et les muscles brachioradiaux antérieurs à l'épicondyle latéral. Il se divise en une branche profonde purement motrice, le nerf interosseux postérieur et une branche sensorielle superficielle. Le nerf interosseux postérieur traverse le muscle supinateur en passant entre ses parties superficielle et profonde pour accéder à la loge postérieure du coude. Au bord proximal du muscle supinateur, un arc fibreux reliant le nerf, communément appelé «arcade de Frohse», peut provoquer un conflit nerveux.
15. NERF ULNAIRE
Dans son passage autour de la face postéro-médiale du coude, le nerf ulnaire se situe dans la rainure condylienne, un anneau ostéofibreux formé entre le processus olécranien et l'épicondyle médial relié par une feuille fasciale, le rétinaculum du tunnel cubital, également appelé rétinaculum d'Osborne. (Fig. 7). Le plancher de ce tunnel est formé par la bande postérieure du ligament collatéral médial. Environ 1 cm en aval de ce tunnel, le nerf cubital pénètre dans le tunnel cubital approprié, un hiatus entre les têtes ulnaire et humérale du muscle fléchisseur ulnaire du carpe qui sont reliées par un arc aponévrotique, le "ligament arqué" (Fig. 7). Ce ligament représente une expansion distale du rétinaculum d'Osborne. Dans le sillon cubital, le nerf cubital est très superficiel et peut être palpable immédiatement en arrière de la pointe de l'épicondyle. Lors de la flexion et de l'extension du coude, le tunnel cubital change de forme (de légèrement ovoïde à elliptique) et de volume, du fait de l'origine excentrée du rétinaculum. Il faut considérer que, lorsque le nerf cubital se courbe sur l'épicondyle médial, un aplatissement et un allongement du nerf liés à la traction se produisent normalement lorsque le coude fléchit ; de plus, jusqu'à 55 % de diminution de la section transversale du nerf et une multiplication par six de la pression interstitielle du tunnel cubital se produisent en raison de l'augmentation de la tension du rétinaculum et du gonflement du ligament collatéral médial (Gelberman et al. 1998 ). Il est concevable que ces conditions puissent prédisposer le nerf à toute compression extrinsèque à ce niveau. Dans le tunnel cubital, la petite artère et les veines récurrentes ulnaires postérieures cheminent entre le nerf ulnaire et l'olécrâne. En général, ces vaisseaux sont beaucoup plus petits que le nerf.
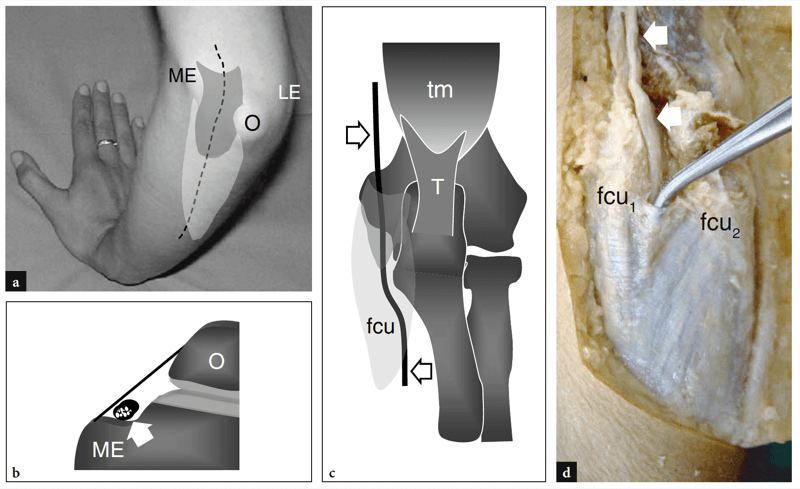
Fig. 7a–d. Nerf cubital et tunnel cubital. une photographie de la face postéro-médiale du coude illustre le trajet du nerf cubital (ligne noire pointillée) entre les proéminences osseuses de l'épicondyle médial (ME) et de l'olécrâne (O) recouvertes par le rétinaculum du tunnel cubital (gris foncé) et, plus caudalement, par l'aponévrose et le ventre du muscle fléchisseur ulnaire du carpe (gris clair). LE, épicondyle latéral. b Le dessin schématique du tunnel cubital sur une vue en coupe révèle les relations du nerf cubital (flèche) avec l'épicondyle médial (ME) et l'olécrâne (O). Notez le rétinaculum d'Osborne qui recouvre le tunnel cubital comme un toit. c Le dessin schématique de la face postérieure d'un coude étendu montre le nerf ulnaire (flèches) lors de son passage dans le tunnel cubital, sous le rétinaculum d'Osborne (gris foncé) et le muscle fléchisseur ulnaire du carpe (fcu, gris clair). tm, muscle triceps ; T, tendon distal du triceps. d La dissection grossière du tunnel cubital montre le ligament arqué triangulaire qui unit les têtes humérale (fcu1) et ulnaire (fcu2) du muscle fléchisseur ulnaire du carpe. La pince soulève le ligament en rendant visible le trajet du nerf (flèches).
16. BOURSE
Plusieurs bourses synoviales autour de l'articulation du coude réduisent la friction entre les os et la peau et les tissus mous sus-jacents. Les plus importantes sont la bourse olécrânienne et la bourse bicipitoradiale. La bourse olécrânienne est une grande bourse sous-cutanée qui s'interpose entre la peau et le processus olécranien sur la face postérieure du coude. La bourse bicipitoradiale (bourse cubitale) se situe profondément dans la loge antérieure du coude, entre le tendon distal du biceps et la tubérosité radiale, pour réduire les frottements entre eux, en particulier lors de la pronation de l'avant-bras (Skaf et al. 1999). En effet, la tubérosité radiale tourne vers l'arrière lors de la pronation et enroule le tendon autour de la corticale radiale. Au cours de ce mouvement, la bourse est tracée entre le tendon et l'os (Fig. 8). Lorsqu'elle est distendue par du liquide, la bourse bicipitoradiale peut entourer complètement le tendon du biceps et provoquer un effet de masse sur les branches adjacentes du nerf radial.
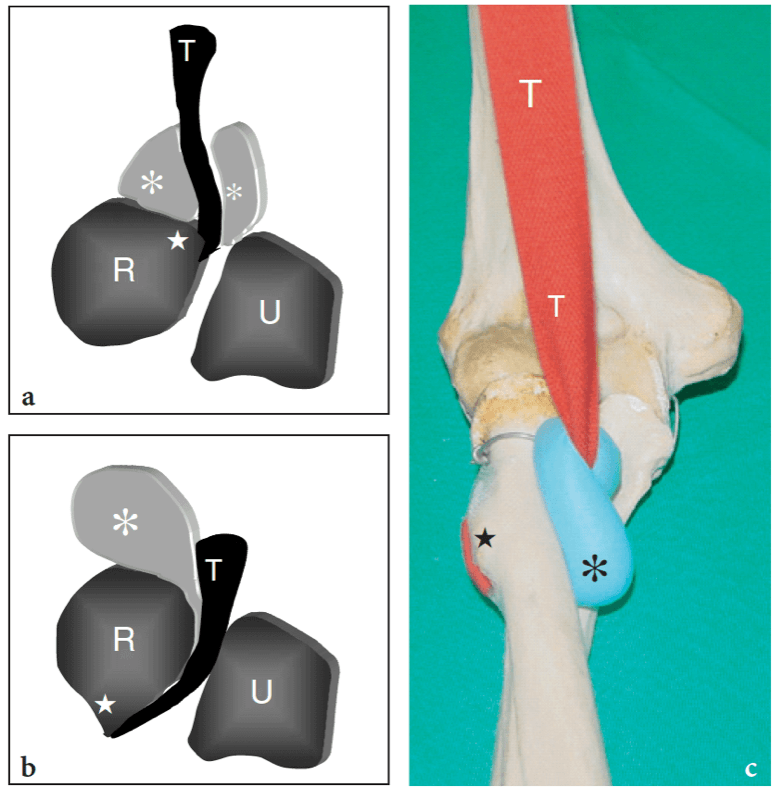
Fig. 8a–c. Bourse bicipitoradiale. a,b Des dessins schématiques illustrent la position de la bourse bicipitoradiale (astérisques) par rapport au tendon distal du biceps (T) lors d'une supination et d'une pronation b. En pronation, le grand axe du radius (R) et la tubérosité radiale (étoile) tournent en comprimant la bourse entre le tendon distal du biceps (T) et l'os. U, cubitus. (Dessins modifiés par Skaf et al. 1999.) c Modèle squelettique montrant la relation entre la bourse bicipitoradiale (astérisque) et le tendon distal du biceps (T) en pronation complète. Notez la position postérieure et latérale de la tubérosité radiale (étoile) sur laquelle s'insère le tendon du biceps.
17. ÉLÉMENTS ESSENTIELS DES ANTÉCÉDENTS CLINIQUES ET DE L'EXAMEN PHYSIQUE
Dans l'histoire du patient se plaignant de douleur ou de dysfonctionnement du coude, l'examinateur doit envisager d'éventuelles maladies articulaires systémiques (polyarthrite rhumatoïde et affections similaires), des troubles professionnels (maladies de forage pouvant provoquer une arthrose articulaire) et des traumatismes (des fractures manquées de la tête radiale peuvent être un cause d'inconfort durable), même si elles ont été subies dans le passé. Les activités sportives sont également une partie essentielle de l'histoire : la pratique du tennis et du golf peut provoquer des microtraumatismes et des lésions de surmenage aux origines communes des tendons extenseurs et fléchisseurs avec l'apparition de syndromes cliniques clairement définis. Avec des symptômes chroniques, il est important d'analyser aussi précisément que possible comment la douleur rayonne et où elle est localisée, ainsi que ses facteurs déclenchants, car ces caractéristiques peuvent aider à orienter l'examen échographique et suggérer le bon diagnostic.
le bon diagnostic. Lors de l'examen physique, l'amplitude de mouvement du coude et le point final du mouvement doivent être étudiés au niveau des articulations radio-capitellare et trochlée-ulnaire (flexion/extension) ainsi qu'au niveau de l'articulation radio-ulnaire proximale (pronation /supination). Ensuite, les radiographies standard précédentes, le cas échéant, doivent être revues avant de commencer l'examen échographique afin d'exclure les anomalies osseuses qui peuvent être négligées ou mal interprétées à l'échographie, telles que les érosions articulaires, les modifications arthrosiques et les calcifications hétérotopiques. Dans un contexte post-traumatique, un examen attentif des radiographies doit être obtenu avant l'examen américain pour exclure les fractures subtiles, en particulier impliquant la tête radiale, qui peuvent être négligées à la première observation.
18. ANOMALIES TENDONIENNES
Lorsqu'une lésion tendineuse est suspectée, des mouvements résistants spécifiques doivent être vérifiés. En raison de sa position superficielle, le tendon distal du biceps peut être facilement palpé pendant la flexion contre résistance tout en gardant le coude fléchi à 90° et en supination. La rupture de ce tendon est généralement associée à une rétraction du muscle dans le bras, où elle peut être appréciée comme une masse. Néanmoins, le ventre musculaire rétracté peut être difficile à détecter chez les patients obèses ou lorsque le gonflement local et la douleur limitent un examen physique approprié. Le tendon distal du triceps peut également être palpé sans difficulté sur le coude postérieur avec l'articulation fléchie à 90°. Son intégrité peut être évaluée en demandant au patient d'étendre le coude contre résistance : une déchirure complète du tendon distal du triceps entraîne une perte complète de la puissance d'extension. Dans le cas d'un patient suspecté d'épicondylite latérale, l'examinateur doit immobiliser le coude du patient d'une main tout en comprimant l'origine du tendon extenseur commun avec les doigts sur l'épicondyle latéral. Dans l'épicondylite latérale, cette manœuvre provoque une douleur irradiant de la région épicondylienne jusqu'à l'avant-bras. La douleur est généralement exacerbée par l'extension du poignet contre la résistance. Dans l'épicondylite médiale, la douleur peut être provoquée par une pression ferme sur le tendon commun médian ou par une résistance à la flexion du poignet.
19. INSTABILITÉ LIGAMENTAIRE
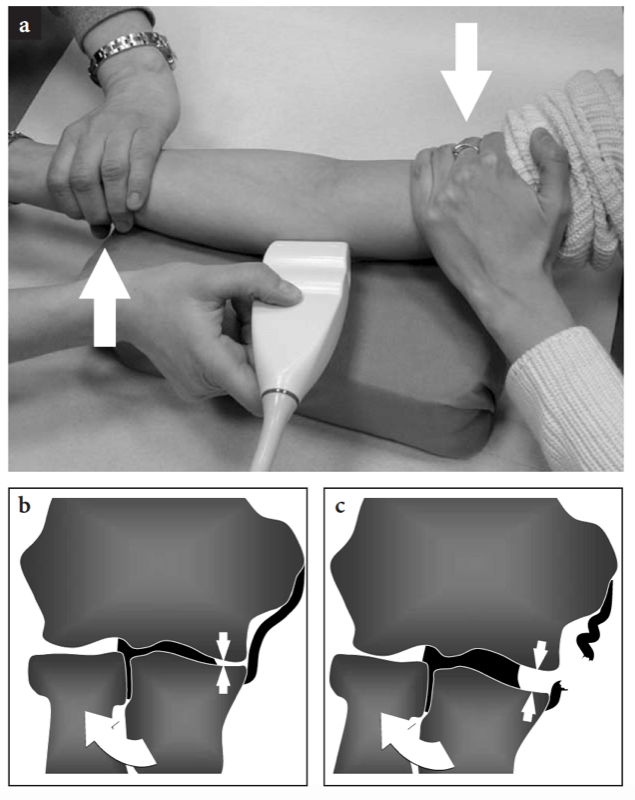
Des tests cliniques spécifiques peuvent être utiles dans le cadre de l'instabilité ligamentaire. Pour évaluer l'intégrité des ligaments collatéraux latéral et médial, l'examinateur peut saisir la face postérieure du coude du patient d'une main et le poignet du patient de l'autre. Lors du verrouillage du coude, une contrainte de valgus ou de varus est appliquée pour évaluer respectivement l'intégrité des ligaments collatéraux médial et latéral. Ces manœuvres cliniques sont effectuées de manière plus fiable en plaçant la sonde sur le ligament afin de démontrer un élargissement même mineur de l'espace articulaire lors de la sollicitation (Fig. 9).
20. SYNDROME DU TUNNEL CUBITAL
Une manœuvre clinique utile pour évaluer l'état du nerf cubital est le « test de Froment ». On demande au patient de pincer une feuille de papier entre le pouce et l'index. En cas de neuropathie ulnaire manifeste, le patient saisit le papier en fléchissant le pouce (activation du long fléchisseur innervé médian du pouce en compensation de la faiblesse des muscles interosseux dorsaux). Chez les patients atteints du syndrome du tunnel cubital, la palpation du nerf cubital au niveau du tunnel cubital peut être douloureuse et peut reproduire les symptômes.
21. ANATOMIE PAR ULTRASONS ET TECHNIQUE DE BALAYAGE
D'une manière générale, le coude est considéré comme l'une des articulations les plus faciles à examiner par échographie, même pour les débutants (Vanderschueren et al. 1998). La principale exigence technique est la disponibilité d'un transducteur linéaire moderne avec une bande de fréquences allant de 5 à 15 MHz. Les transducteurs adéquats ne doivent pas être excessivement larges pour permettre le balayage autour du coude à divers degrés de flexion sans limiter l'accessibilité autour des os saillants. Plus que dans d'autres sites des membres, les structures anatomiques du coude sont intrinsèquement prédisposées aux effets anisotropes lorsque la sonde balaie les fosses osseuses, les surfaces curvilignes et les proéminences osseuses. Cela nécessite une technique de numérisation minutieuse, en particulier lors de l'examen des tendons, des ligaments et des nerfs. Par défaut, le champ de vision de l'image US et la zone focale doivent être ajustés pour l'examen de petites parties superficielles, à peu près égaux à ceux actuellement utilisés pour l'examen du poignet. À l'exception de l'insertion du tendon distal du biceps et de la bourse bicipito-radiale, la plupart des structures des tissus mous du coude sont très superficielles et nécessitent une échelle de grossissement élevée. Lors de l'examen du tunnel cubital, un tampon de séparation ou une quantité généreuse de gel peut aider à améliorer le contact du transducteur avec la peau.
En général, l'examen échographique du coude doit être adapté directement à la structure appropriée, comme indiqué par les résultats cliniques. Concentrer l'examen américain sur une région définie du coude au lieu d'un examen complet du coude réduit le temps d'examen et améliore l'efficacité de l'étude. En conséquence, dans ce chapitre, nous avons arbitrairement subdivisé le coude en une approche à quatre quadrants, comprenant ses aspects antérieur, latéral, médial et postérieur. Dans la plupart des cas, l'examen du côté opposé n'est ni demandé ni exigé sauf pour comparer la taille d'une structure pathologique avec celle saine. Néanmoins, cela peut être utile pour les débutants (et en particulier dans les cas d'épicondylite latérale légère) pour établir si des modifications subtiles de l'épaisseur et de l'échogénicité du tendon ou du ligament sont réelles ou non.
L'examen dynamique est particulièrement utile pour l'examen des ligaments collatéraux car il peut montrer un élargissement de l'articulation lors des manœuvres d'effort en valgus et varus, confirmant ainsi les résultats obtenus en imagerie statique. L'examen de la fosse cubitale pendant la pronation et la supination peut mettre en évidence des changements survenant dans la bourse bicipitoradiale. L'instabilité antérieure du nerf cubital peut être facilement évaluée sur des coupes échographiques transversales obtenues lors de la flexion progressive du coude. Dans l'instabilité nerveuse, le nerf cubital peut être vu subluxer au-dessus de l'apex de l'épicondyle médial ou se disloquer à l'extérieur du tunnel. Lorsqu'ils sont associés à un épanchement synovial, les corps lâches intra-articulaires peuvent être mieux évalués lors des mouvements articulaires et de l'application de pression sur différents aspects de l'articulation dans le but de déplacer le liquide intra-articulaire. Cela peut entraîner des changements de position des fragments lâches et permet un diagnostic plus sûr.
22. COUDE ANTÉRIEUR
L'examen échographique du coude antérieur peut être réalisé avec le patient face à l'examinateur, le coude en extension reposant sur une table (Barr et Babcock 1991). Une légère inclinaison du corps du patient vers le côté examiné facilite la supination complète et l'évaluation de certaines structures de la loge antérieure, telles que le tendon distal du biceps. Une extension complète du coude peut être obtenue en plaçant un oreiller sous l'articulation. Élever la table peut également être utile et permet un examen plus confortable pour le patient et l'examinateur. Si le patient n'est pas en mesure d'obtenir une extension complète du coude, les balayages longitudinaux peuvent être difficiles à réaliser, en particulier lors de l'utilisation de sondes de grande taille. Comme alternative chez les personnes âgées ou pour les patients gravement traumatisés, la face antérieure du coude peut également être examinée avec le patient en décubitus dorsal tenant son bras le long du corps.
Les principales structures antérieures susceptibles d'examen échographique sont : le muscle brachial, le muscle et le tendon du biceps distal, l'artère brachiale, les nerfs médian et radial, le récessus synovial antérieur avec le coussinet adipeux antérieur et les articulations radio-capitellaire et trochlée-cubitus. . Des images échographiques transversales sont d'abord obtenues en balayant la sonde d'environ 5 cm au-dessus à 5 cm en dessous de l'articulation trochlée-cubitus, perpendiculairement à la diaphyse humérale. Les images échographiques crâniennes de la région supracondylienne révèlent les deux muscles principaux de la face antérieure du bras distal : le muscle biceps superficiel et le muscle brachial profond (Fig. 10a). Le biceps se trouve juste en profondeur du tissu sous-cutané entouré par le fascia brachial. Il a un aspect bipenné avec une couche centrale hyperéchogène reflétant l'aponévrose. Le muscle brachial est situé entre le biceps et le cortex osseux huméral et est beaucoup plus gros que le biceps. L'artère brachiale et le trajet du nerf médian le long de ces muscles : l'artère se trouve généralement latéralement au nerf (Fig. 10b). En déplaçant le transducteur plus distalement, le tendon distal du biceps apparaît comme une structure hyperéchogène qui recouvre le muscle brachial (Fig. 10b, c). Une technique de numérisation minutieuse est nécessaire pour imager ce tendon. Le tendon distal du biceps est mieux examiné sur des plans longitudinaux avec l'avant-bras du patient en supination maximale pour mettre en évidence l'insertion du tendon sur la tubérosité radiale (Fig. 11) (Miller et Adler 2000). En raison d'un parcours oblique de la surface à la profondeur, des portions de ce tendon peuvent apparaître artificiellement hypoéchogènes si la sonde n'est pas maintenue parallèle à celui-ci (Figures 12a,c). En conséquence, la moitié distale de la sonde doit être doucement poussée contre la peau du patient pour assurer le parallélisme entre le faisceau US et le tendon distal du biceps, permettant ainsi une visualisation complète de son schéma fibrillaire échogène (Figures 12b,d). Dans les gros coudes épais, cependant, la partie distale de ce tendon peut être difficile à examiner en raison de sa localisation profonde. En général, les plans transversaux sont moins utiles pour examiner la partie distale du tendon du biceps car de légers changements dans l'orientation du transducteur peuvent produire une variation spectaculaire de l'échogénicité du tendon, ce qui crée une confusion entre le tendon et les structures environnantes. Dans des conditions d'anisotropie maximale, le tendon et l'artère peuvent présenter la même taille et le même schéma échogène sur les coupes transversales (Fig. 12e, f).
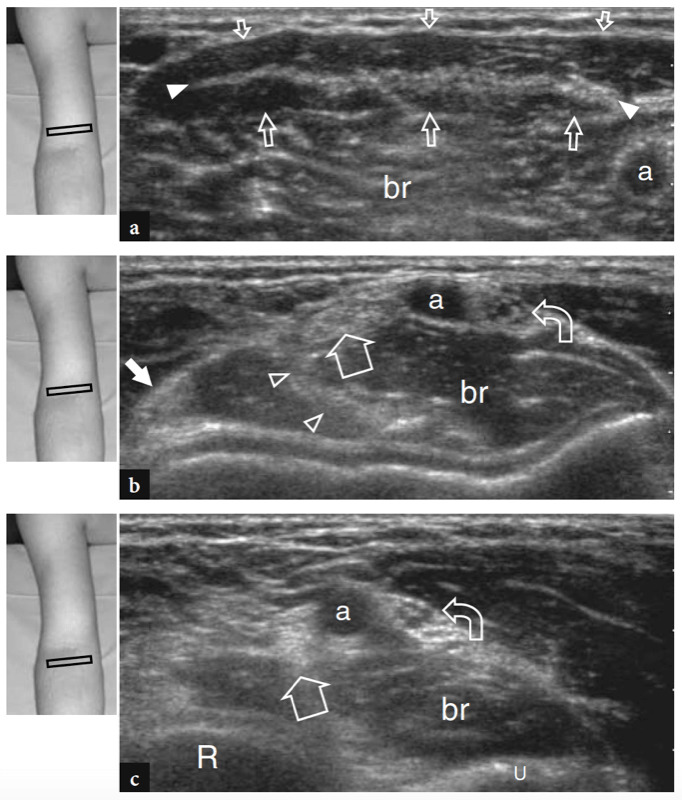
Fig. 10a–c. Tendon distal normal du biceps. Des images échographiques transversales 12−5 MHz obtenues sur le coude antérieur chez un sujet sain montrent le tendon distal du biceps : a à la jonction myotendineuse, b au niveau de la trochlée humérale et c sous l'interligne articulaire, juste avant son insertion. En a, le tendon distal du biceps prend son origine dans une large aponévrose échogène (têtes de flèches) située au centre du muscle (flèches). Notez le muscle brachial (br) qui se trouve profondément au biceps. a, artère brachiale. En b et c, le tendon distal du biceps (grande flèche) apparaît comme une structure ovale hyperéchogène superficielle au brachial (br). Près de son côté médial, l'artère brachiale (a) et le nerf médian (flèche courbe) sont visibles, tandis que le nerf radial (petite flèche) se situe plus latéralement entre les muscles brachial et brachioradial. Notez l'aponévrose (pointes de flèche) du brachial R, radius ; u, cubitus. Les inserts en haut à gauche des figures indiquent le positionnement de la sonde.
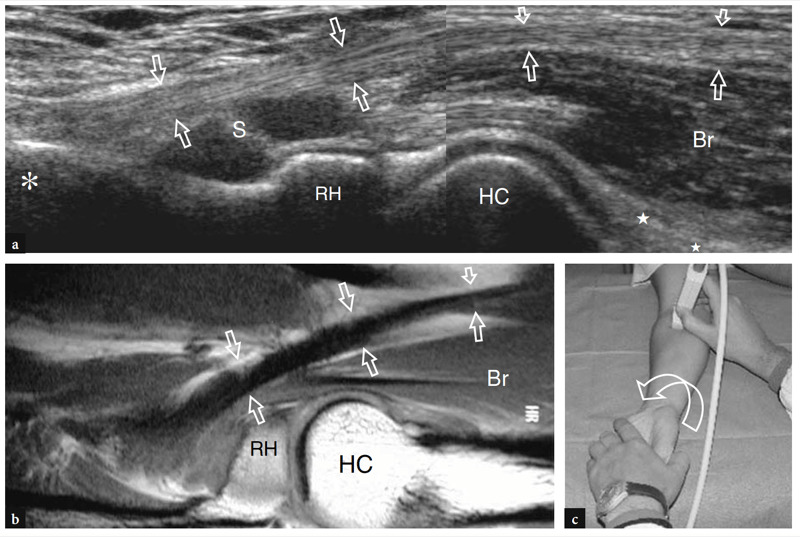
Fig. 11a–c. Tendon distal normal du biceps. a Image échographique grand axe 12−5 MHz du coude antérieur avec une corrélation d'imagerie SE IRM sagittale pondérée en T1 (T1w) montrant l'aspect incurvé du tendon distal du biceps (flèches) qui s'insère sur la tubérosité bicipitale (astérisque) du rayon. Le tendon a un aspect fibrillaire et des trajets superficiels par rapport aux muscles brachial (Br) et supinateur (S). Observez l'aspect carré de la tête radiale (RH), du capitellum huméral arrondi (HC) recouvert d'une bande de cartilage hypoéchogène et du coussinet adipeux antérieur (étoiles). c Photographie illustrant la technique de numérisation pour imager la partie distale du tendon du biceps. L'avant-bras du patient est maintenu en supination maximale (flèche courbe) et le bord inférieur du transducteur est poussé contre la peau du patient.
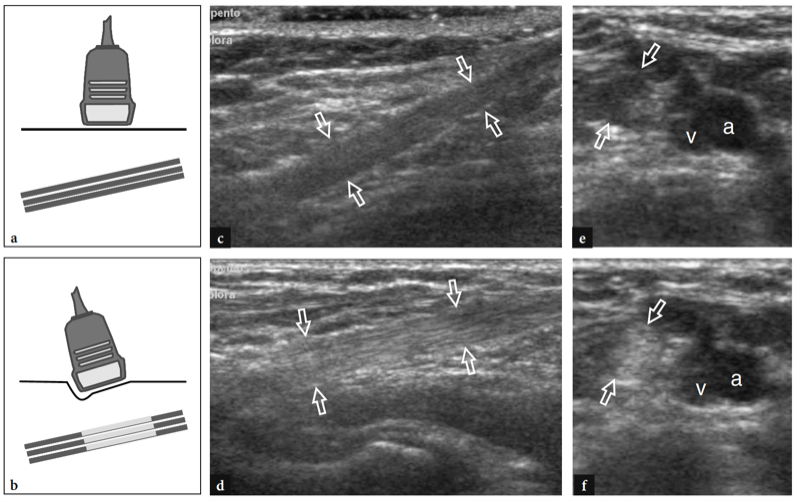
Fig.12a–f. Tendon distal du biceps normal et anisotropie. a,b Dessins schématiques et c,d images échographiques 12-5MHz grand axe correspondantes du tendon du biceps obtenues avec une incidence oblique (a,c) ou perpendiculaire (b,d) du faisceau échographique. e,f Balayages respectifs à petit axe. En c et e, une mauvaise orientation du faisceau échographique conduit à un aspect hypoéchogène du tendon (flèches) par rapport à la graisse environnante par anisotropie. Lorsqu'il est mal visualisé, le tendon peut difficilement être distingué de l'artère brachiale adjacente (a) et de la veine cubitale (v) car toutes semblent hypoéchogènes.
Comme indiqué précédemment, le nerf médian passe du côté interne de l'artère brachiale, tandis que le nerf radial peut être apprécié entre le muscle brachioradial et le muscle brachial (Figues. 10b,c ; 13). La fosse coronoïde apparaît comme une concavité de la face antérieure de l'humérus remplie de tissu hyperéchogène lié au coussinet adipeux antérieur (Fig. 14). Le coussinet adipeux a une forme triangulaire avec sa base située en avant, au plus profond du muscle brachial. À ce niveau, la capsule antérieure est imagée de manière incohérente avec l'échographie (Miles et Lamont 1989). Dans des états normaux, une petite quantité de liquide peut être reconnue entre le coussinet adipeux et l'humérus (Fig. 14). Sur les coupes échographiques transversales, la face antérieure de l'épiphyse humérale distale apparaît comme une ligne hyperéchogène ondulée recouverte d'une fine couche (2 mm d'épaisseur) de cartilage articulaire hypoéchogène (Fig. 15). Son tiers latéral correspond au capitellum huméral qui présente une forme convexe typique et s'articule avec la tête radiale. Les deux tiers médiaux de l'épiphyse humérale se rapportent à la trochlée humérale qui s'articule avec l'ulna. La trochlée ressemble à un sillon délimité par des facettes médiales et latérales (Fig. 15a, b). Sur les images longitudinales obtenues plus latéralement, la tête radiale présente un aspect carré. Sa facette articulaire est recouverte d'un mince bourrelet de cartilage. Dans les coupes antérieures mi-sagittales, le processus coronoïde de l'ulna apparaît comme une structure hyperéchogène triangulaire proéminente sur laquelle la partie crânienne du tendon brachial s'insère (Fig. 16).
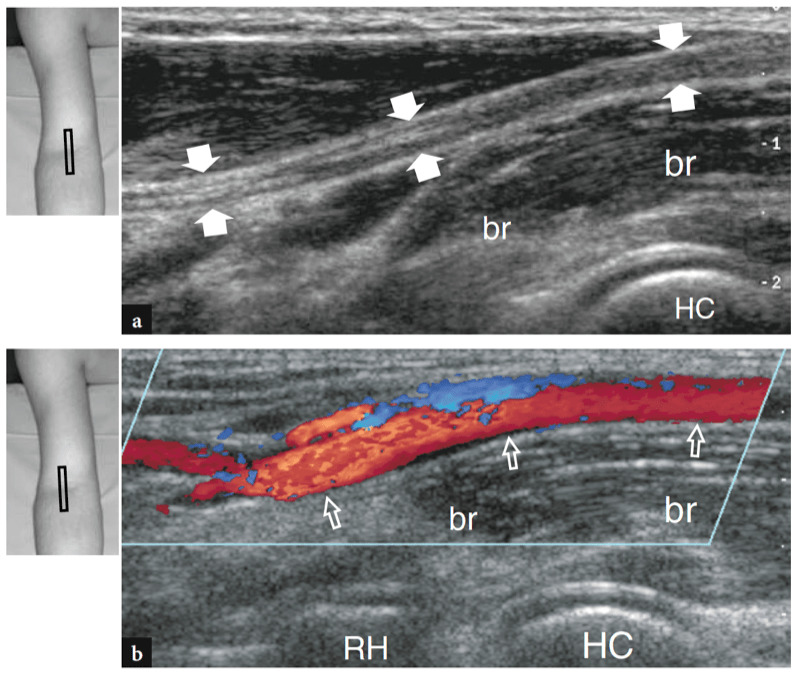
Figures 13a,b. Nerf médian et artère brachiale. Les images américaines longitudinales en échelle de gris (a) et Doppler couleur (b) 12 à 5 MHz sur la fosse antécubitale démontrent l'aspect normal du nerf médian (flèches blanches en a) et de l'artère brachiale (flèches ouvertes en b). Les deux sont superficiels par rapport au muscle brachial (br). Notez le capitellum huméral (HC) et la tête radiale (RH). Les inserts en haut à gauche des figures indiquent le positionnement de la sonde.
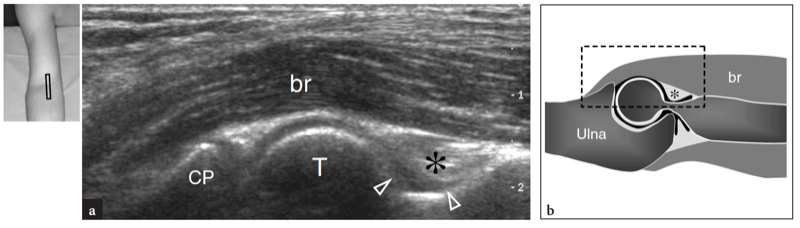
Figures 14a,b. Evidement articulaire antérieur. une image longitudinale 12−5 MHz US à la face antérieure du coude avec une corrélation de diagramme b identifie l'évidement articulaire antérieur (têtes de flèches) crânien aux surfaces osseuses hyperéchogènes du processus coronoïde (CP) et de la trochlée (T) et profondément à la muscle brachial (br). Notez le coussinet adipeux antérieur (astérisque) comme un tissu hyperéchogène délimitant cette cavité antérieurement. L'insert en haut à gauche de la figure indique le positionnement de la sonde.
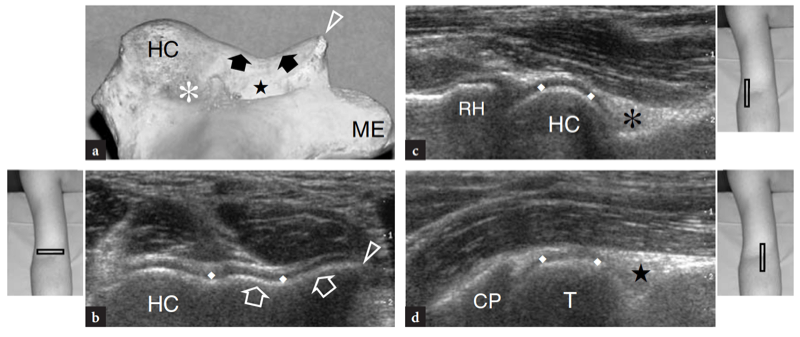
Fig. 15a–d. Anatomie échographique des os. une vue axiale de la face antérieure de l'humérus distal donne une projection du capitellum (HC) et de la trochlée (flèches) visualisés en échographie. Observez l'extrémité médiale abrupte (tête de flèche) de la trochlée et les fosses radiale (astérisque) et coronoïde (étoile), qui se trouvent juste à proximité des surfaces articulaires de l'humérus. ME, épicondyle médial. b L'image US transversale 12−5 MHz correspondante du coude antérieur révèle l'humérus distal antérieur comme une ligne hyperéchogène continue ondulée recouverte d'une couche hypoéchogène de cartilage (losanges) dans laquelle le capitellum (HC) et la trochlée (flèches) peuvent facilement être distingué. c,d Les images échographiques sagittales 12−5 MHz au-dessus des fosses radiale (c) et coronoïde (d) montrent le coussinet adipeux antérieur hyperéchogène (astérisque et étoile) remplissant ces dépressions. Notez l'aspect carré de la tête radiale (RH) en c et la forme pointue de l'apophyse coronoïde (CP) en d. T, trochlée. Les inserts placés à côté des figures indiquent le positionnement de la sonde.
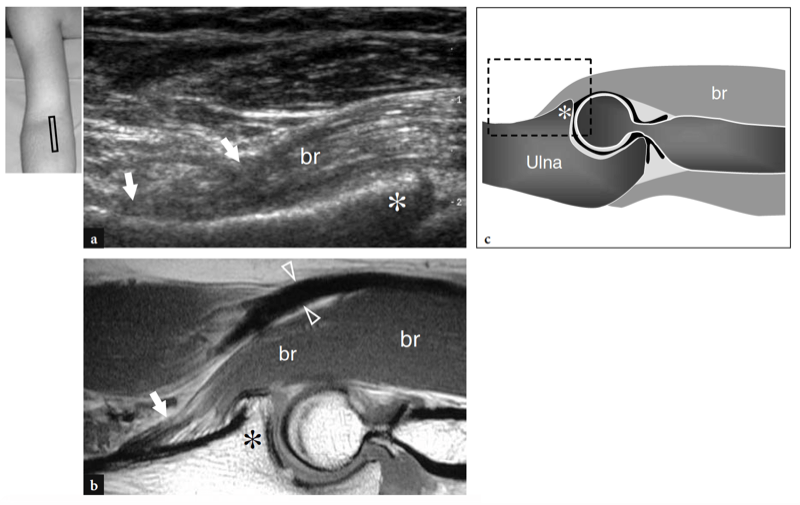
Figure 16a,c. Tendon brachial. une image US mi-sagittale 12−5 MHz de la fosse antécubitale avec imagerie IRM b T1w SE et corrélation du diagramme c montre le tendon brachial (flèche) comme une structure courte et épaisse qui s'insère sur l'ulna antérieur, juste caudale à l'apex (astérisque ) du processus coronoïde. br, muscle brachial ; pointes de flèches, tendon distal du biceps. L'insert en haut à gauche de la figure indique le positionnement de la sonde.
23. COUDE MEDIAL
La face médiale du coude est examinée coude en extension, en appui sur une table. Ensuite, le patient est invité à se pencher vers le côté avec l'avant-bras en rotation externe forcée (Barr et Babcock 1991). Du côté médial du coude, il existe deux structures principales susceptibles d'être évaluées par échographie : le tendon fléchisseur commun et le ligament collatéral médial.
Le tendon fléchisseur commun est mieux examiné dans les plans longitudinaux. Il apparaît plus court que l'origine du tendon extenseur commun et s'insère sur la face médiale de l'épitrochlée (Fig. 17a). Au plus profond de ce tendon, le faisceau antérieur du ligament collatéral médial apparaît comme une structure en forme de cordon qui relie l'épitrochlée à la partie la plus crânienne de l'ulna, appelée tubercule sublimis (Fig. 17a, b). Le positionnement correct pour l'examen du faisceau antérieur du ligament collatéral médial est obtenu avec le patient en décubitus dorsal en gardant l'épaule en abduction et en rotation externe et le coude à 90° de flexion (Ward et al. 2003). À l'examen américain, le composant antérieur du ligament collatéral médial a un motif fibrillaire et une forme en éventail (Ward et al. 2003). Il semble hyperéchogène : cependant, l'échogénicité ligamentaire peut varier en fonction du positionnement du patient et de la sonde (Fig. 17a, b). Le coude du patient en position d'extension allongé sur la table d'examen, il apparaît généralement hypoéchogène par rapport au tendon fléchisseur sus-jacent. Dans une récente étude américaine avec une corrélation cadavérique, l'épaisseur du ligament a été rapportée comme allant d'environ 2.6 à 4 mm, sans différences significatives dans la déviation, l'application du stress ou la dominance de la main (Ward et al. 2003). Les autres composants de ce ligament, à savoir les faisceaux postérieur et transverse, ne sont pas représentés aussi précisément que le antérieur à l'examen échographique, même avec des transducteurs à haute résolution. Cependant, ces dernières portions sont une source de morbidité moins fréquente et jouent un rôle mineur dans la stabilisation du coude contre le stress en valgus.
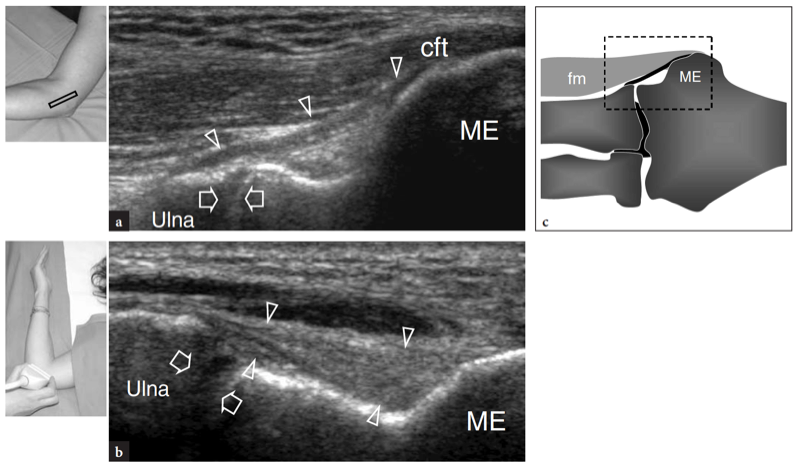
Fig. 17a–c. Bande antérieure du ligament collatéral médial. a,b Images échographiques grand axe 12−5 MHz obtenues coude en extension (a) et à 90° de flexion (b) selon le positionnement reporté dans les encarts en haut à gauche des figures, avec corrélation du diagramme c. La bande antérieure du ligament collatéral médial (têtes de flèches) est représentée comme une structure allongée traversant l'articulation trochlée-cubitus (flèches). Coude fléchi, le ligament est tendu et son schéma fibrillaire est mieux apprécié. Dans des états normaux, le ligament a une épaisseur et une échotexture uniformes. ME, épicondyle médial ; cft, tendon fléchisseur commun ; fm, muscles fléchisseurs.
24. COUDE LATÉRAL
La face latérale du coude est mieux examinée avec les deux coudes en extension, les pouces vers le haut, les paumes des mains jointes (Barr et Babcock 1991). Lors de l'examen du ligament collatéral radial et de la capsule, le coude doit être étendu en gardant la main en pronation. Le long du coude latéral, l'échographie haute résolution peut montrer le tendon extenseur commun, le ligament collatéral ulnaire latéral, le nerf radial avec ses branches superficielles et profondes (nerf interosseux postérieur) et l'articulation radio-capitellaire.
L'origine du tendon extenseur commun est mieux visualisée dans les plans longitudinaux comme une structure hyperéchogène en forme de bec située entre le tissu sous-cutané et le ligament collatéral ulnaire latéral (Fig. 18). Profondément à ce tendon, l'épicondyle latéral apparaît comme une structure hyperéchogène lisse en pente descendante. Les contributions individuelles des muscles extenseurs au tendon extenseur commun ne peuvent pas être discriminées avec l'échographie car elles sont entrelacées les unes avec les autres. Les fibres tendineuses profondes relatives au court extenseur radial du carpe recouvrent le ligament collatéral ulnaire latéral et ne peuvent pas facilement en être séparées. En fait, ces structures sont intimement liées et, bien qu'elles s'étendent dans une direction légèrement différente, elles ont le même aspect fibrillaire (Connell et al. 2001). Sur les images échographiques transversales, l'origine du tendon extenseur commun a une forme ovale en coupe transversale et est située juste à la surface de l'épicondyle latéral. Immédiatement en aval de la jonction myotendineuse, les ventres musculaires de l'extensor carpi radialis brevis, de l'extensor digitorum, de l'extensor digiti minimi et de l'extensor carpi ulnaris apparaissent généralement comme un seul bloc.
En avant de l'épicondyle latéral, le tronc principal du nerf radial chemine entre les muscles brachial et brachioradial. Il est examiné de manière fiable au moyen d'images échographiques transversales obtenues entre ces muscles sous la forme d'une petite structure arrondie composée de quelques points hypoéchogènes dispersés reflétant les faisceaux (Fig. 19a) (Bodner et al. 2002). L'artère radiale récurrente peut être vue adjacente au nerf et ne doit pas être confondue avec l'un de ses faisceaux. L'imagerie Doppler couleur peut être utile pour l'identifier avec précision. L'échographie haute résolution permet de visualiser le nerf radial lorsqu'il se divise en la branche sensorielle cutanée superficielle et le nerf interosseux postérieur (Fig. 19b, c). Les faisceaux de ces derniers nerfs sont très petits et une technique de balayage méticuleuse basée sur le suivi du faisceau nerveux selon son petit axe est nécessaire pour leur visualisation. Au niveau du coude latéral, l'échographie peut visualiser le nerf interosseux postérieur lorsqu'il perce le muscle supinateur et pénètre dans l'arcade de Frohse, en passant entre les parties superficielle et profonde de ce muscle (Fig. 20). À travers le supinateur, le nerf se déplace vers la loge postérieure. En conséquence, une technique de balayage appropriée doit inclure le repositionnement du patient avec le coude en semi-flexion, en plaçant l'avant-bras vers l'avant et orienté plus transversalement au-dessus de la table d'examen. Au cours de la pronation, le nerf peut prendre une trajectoire angulée au bord proximal de l'arcade de Frohse. Il ne faut pas confondre cette apparence avec une découverte pathologique. À l'intérieur ou juste après avoir quitté le muscle supinateur, le nerf interosseux postérieur peut être vu se subdiviser davantage en quelques branches subtiles dirigées vers les muscles de l'avant-bras postérieur. Ces dernières branches sont difficiles à examiner car leur taille se rapproche de la capacité de résolution spatiale de l'équipement américain actuel. Une fois dégagée en avant de l'épicondyle latéral, la branche sensorielle cutanée superficielle du nerf radial se poursuit dans l'avant-bras antérieur. Au niveau de l'avant-bras proximal, il rejoint l'artère radiale et peut être démontré cheminant entre le long extenseur radial du carpe et le brachioradial.
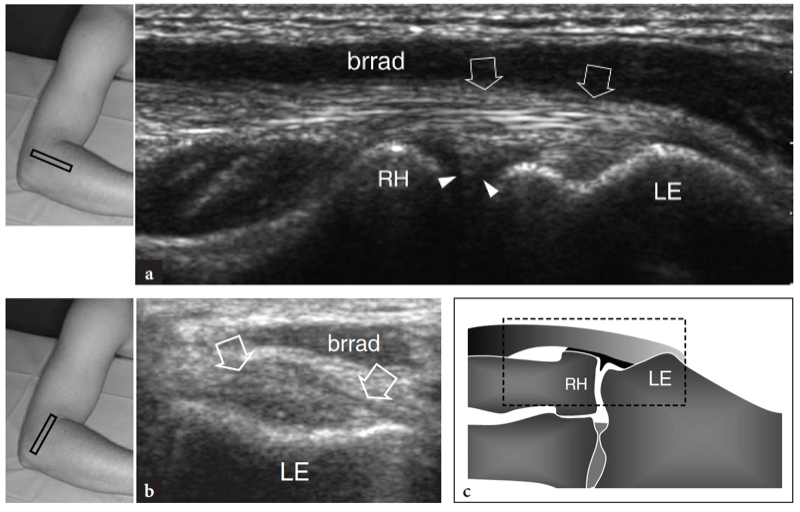
Fig. 18a–c. Tendon extenseur commun normal. une image US grand axe 12−5 MHz obtenue sur le coude latéral révèle une origine normale du tendon extenseur commun (flèches) caractérisée par un motif fibrillaire uniforme. Le tendon est situé en profondeur du muscle brachioradial (brrad) et en surface de l'articulation radio-capitellaire et des inserts sur l'épicondyle latéral (LE). La frange synoviale latérale (tête de flèche) est représentée comme une structure hyperéchogène triangulaire s'intercalant entre le capitulum et la tête radiale (RH). Notez l'aspect lisse et descendant du cortex de l'épicondyle latéral et de la tête radiale. b L'image US à axe court de 12 à 5 MHz sur l'épicondyle latéral (LE) montre la forme en coupe ovale de l'origine normale de l'extenseur commun (flèches). Brrad, muscle brachioradial. c Corrélation des diagrammes. Les inserts en haut à gauche des figures indiquent le positionnement de la sonde.
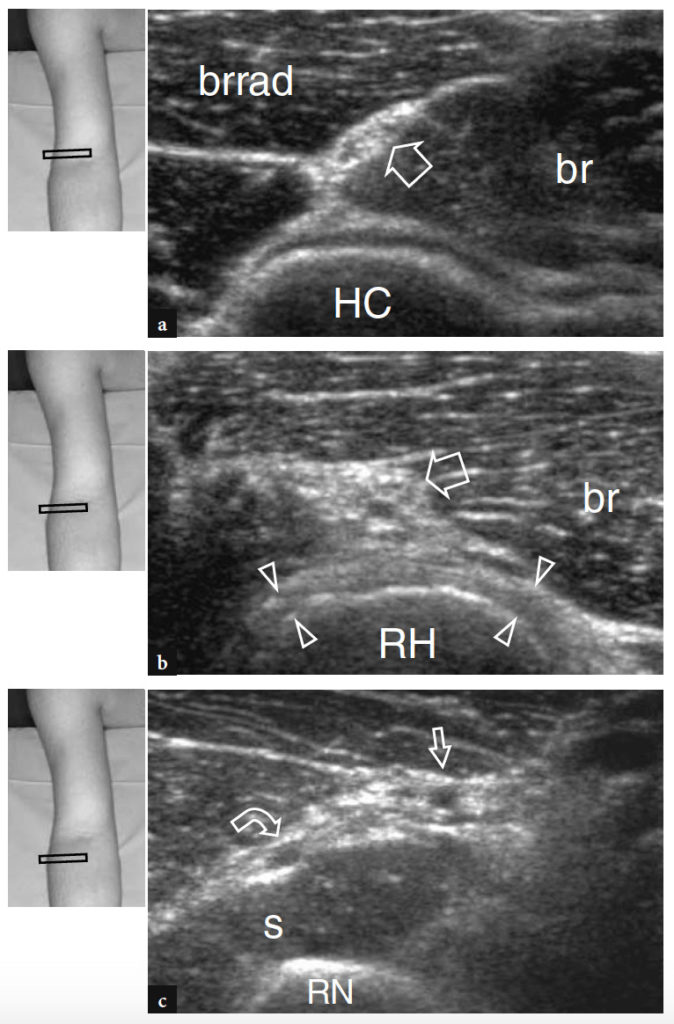
Fig. 19a–c. Nerf radial. Les images échographiques transversales 12−5 MHz obtenues sur le coude antérolatéral montrent le nerf radial normal et ses branches divisionnaires au niveau du capitellum huméral (a), de la tête radiale (b) et du col radial (c). En a, le tronc principal du nerf (flèche) se situe dans l'espace hyperéchogène entre les muscles brachial (br) et brachioradial (brrad), superficiel au capitellum huméral (HC). En b, le nerf radial (flèche) passe au-dessus de la tête radiale (RH) en relation étroite avec le ligament annulaire (têtes de flèches). Typiquement, ce ligament se présente sous la forme d'une bande hyperéchogène incurvée qui recouvre la tête radiale comme une ceinture. En c, la branche sensorielle cutanée (flèche droite) et le nerf interosseux postérieur (flèche courbe) peuvent être appréciés au-dessus du ou des muscles supinateurs grâce à la bifurcation du tronc principal du nerf. RN, col radial. Les inserts en haut à gauche des figures indiquent le positionnement de la sonde.
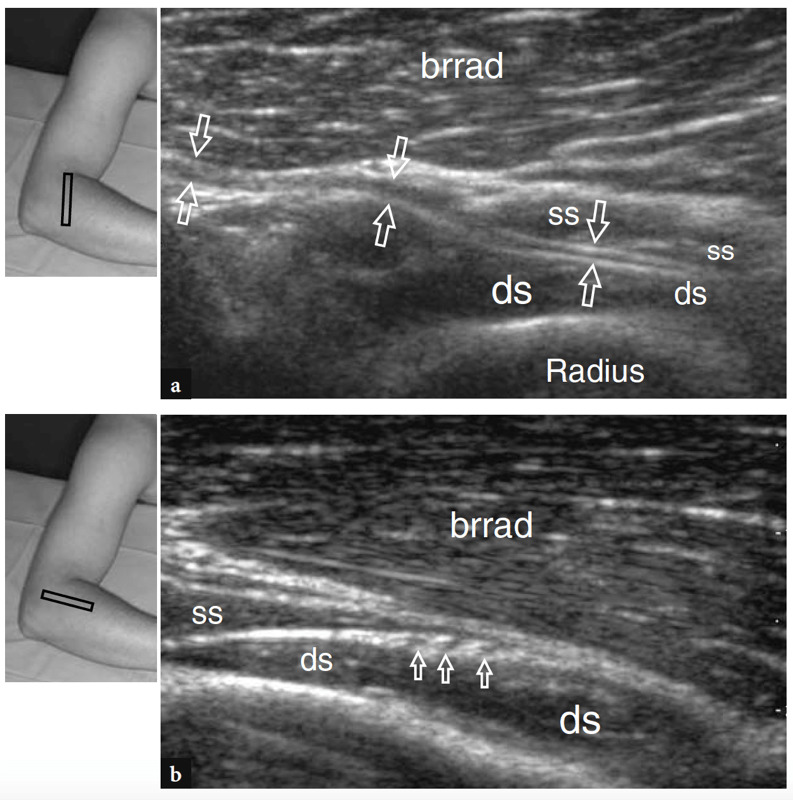
Figure 20a,b. Nerf interosseux postérieur. a Les images américaines grand axe et b petit axe 12−5 MHz obtenues au niveau de l'avant-bras proximal sur le muscle brachioradial (brrad) montrent le nerf interosseux postérieur normal lorsqu'il traverse le muscle supinateur. Au sein des ventres du supinateur (ss, partie superficielle du muscle supinateur ; ds, partie profonde du muscle supinateur), le nerf apparaît comme une fine structure hypoéchogène composée de quelques faisceaux (flèches) enchâssés dans un plan graisseux hyperéchogène. Les inserts en haut à gauche des figures indiquent le positionnement de la sonde.
L'aspect latéral de l'articulation radio-capitellar peut être clairement délimité par US (Fig. 18a). Une structure hyperéchogène triangulaire est généralement observée remplissant la partie périphérique du rebord articulaire entre les deux surfaces osseuses. Cette structure correspond à une saillie synoviale, un peu semblable à un ménisque (frange synoviale latérale) (Fig. 18a). L'aspect de la tête radiale varie avec différents degrés de rotation de l'avant-bras : en pronation, la tête radiale a un aspect plus carré, alors qu'en supination elle a tendance à adopter un contour plus lisse. L'échographie dynamique peut être utile pour évaluer l'état de la tête radiale et exclure d'éventuelles fractures occultes non déplacées. Superficiel, le ligament annulaire est visible sous la forme d'une structure hyperéchogène homogène en forme de ceinture (Fig. 19b). Il est mieux visualisé au moyen de transducteurs à haute résolution. Avec la sonde placée au-dessus de la tête radiale, les mouvements passifs de supination et de pronation de l'avant-bras permettent une meilleure différenciation du ligament annulaire fixe de la tête radiale rotative. Au niveau de la métaphyse radiale, le récessus annulaire n'est visualisé à l'échographie que s'il est distendu par du liquide.
25. COUDE POSTÉRIEUR
La face postérieure du coude peut être examinée en gardant l'articulation fléchie à 90°, la paume reposant sur la table (Barr et Babcock 1991). Cette position permet une démonstration aisée des principales structures du coude postérieur : le tunnel cubital et le nerf cubital, le muscle et le tendon du triceps, la fosse postérieure avec le coussinet adipeux postérieur et la bourse olécrânienne.
Crânien à l'olécrâne, l'échographie révèle les ventres hypoéchogènes du muscle triceps et son tendon situé de manière excentrée et légèrement médiale par rapport à la ligne médiane (Fig. 21). Le tendon distal du triceps apparaît hyperéchogène et présente généralement des stries lorsqu'il se déploie vers son insertion sur l'olécrâne, un schéma quelque peu similaire au quadriceps. Ces stries, avec alternance de bandes hypo et hyperéchogènes, sont plus vraisemblablement dues à une interposition de graisse entre les fibres tendineuses et ne doivent pas être interprétées à tort comme une tendinose ou une déchirure (Fig. 22). S'il est examiné en extension complète du coude, le tendon distal du triceps peut également apparaître ondulé, imitant éventuellement une rupture. La laxité tendineuse est particulièrement évidente chez les personnes âgées et représente un résultat normal (Rosenberg et al. 1997). De plus, les fibres préinsertionnelles de ce tendon peuvent apparaître hypoéchogènes du fait de leur trajet oblique (Fig. 22). Les changements d'orientation de la sonde permettent une correction adéquate des effets anisotropes dans cette zone. La partie la plus distale du tendon du triceps doit toujours être évaluée avec soin pour exclure les calcifications de l'enthèse.
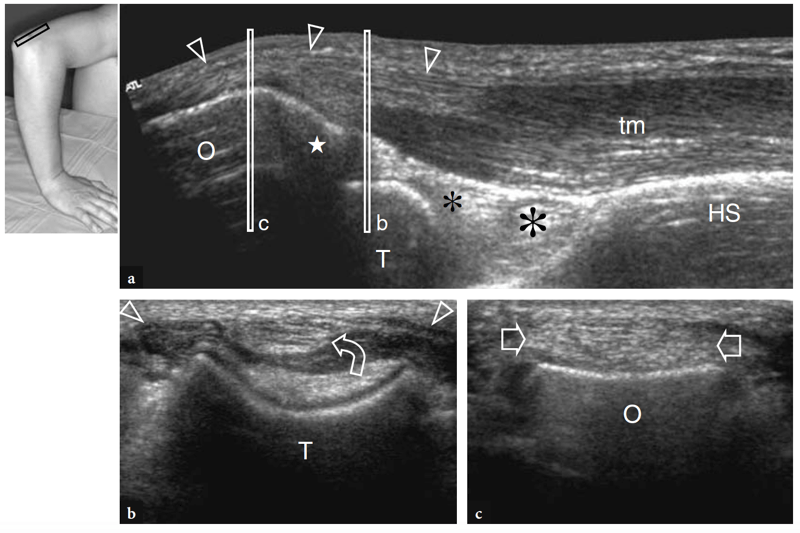
Fig. 21a–c. Tendon distal du triceps et fosse olécrânienne normaux. une image US à champ de vision étendu 12−5 MHz mi-sagittal obtenue avec le coude fléchi sur le processus olécrânien (O) et la face postérieure de l'humérus distal. Le tendon distal du triceps (têtes de flèches) apparaît comme une structure hyperéchogène en forme de bec en continuité avec les ventres hypoéchogènes du muscle triceps ™ qui s'insère à environ 1 cm en aval de l'apex (étoile) de l'olécrâne. Au plus profond du triceps, la fosse olécrânienne est délimitée par le contour en cuillère hyperéchogène de l'humérus et le coussinet adipeux postérieur échogène (astérisques). Notez l'aspect arrondi postérieur de la trochlée (T) et le profil rectiligne de la diaphyse humérale (HS) juste au-dessus de la fosse postérieure. b,c Images US transversales 12−5 MHz obtenues aux niveaux (barres blanches verticales) indiqués en a. En b, l'aspect en coupe de la jonction myotendineuse distale du triceps est visible sur la trochlée postérieure (T). Observez que le tendon (flèche incurvée) se pose légèrement excentriquement par rapport à la ligne médiane et au muscle distal (têtes de flèches). En c, la forme ovale en coupe transversale du tendon distal du triceps (flèches) est visible au-dessus de l'olécrâne (O). L'insert en haut à gauche de la figure indique le positionnement de la sonde.
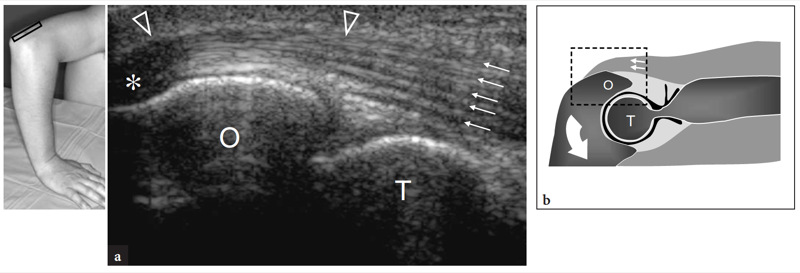
Figure 22a,b. Tendon distal du triceps : aspect normal mimant la maladie. une image US à axe long 12−5 MHz du tendon distal du triceps (têtes de flèches) avec corrélation du diagramme b révèle un motif intratendineux strié composé de bandes alternées hypo- et hyperéchogènes (flèches) qui sont liées à des brins de tissu adipeux intervenant entre les fibres tendineuses . Notez également l'aspect hypoéchogène artéfactuel (astérisque) du tendon lorsqu'il dévie pour s'insérer dans le processus olécrânien (O). Cela est dû à l'anisotropie. T, trochlée. L'insert en haut à gauche de la figure indique le positionnement de la sonde.
La fosse olécrânienne apparaît comme une concavité large et profonde de la face postérieure de la diaphyse humérale remplie du coussinet adipeux postérieur hyperéchogène (Fig. 21a) (Miles et Lamont 1989). De part et d'autre de cette fosse, la face postérieure des épicondyles médial et latéral est visible sur les coupes transversales. Lors de l'examen de l'articulation à 45° de flexion, le liquide intra-articulaire a tendance à migrer de l'espace synovial antérieur vers le récessus olécrânien, facilitant ainsi le repérage des petits épanchements intra-articulaires. Un léger mouvement de balancement du coude du patient pendant l'examen peut être utile pour déplacer le liquide de l'articulation du coude dans la cavité olécrânienne. Plus distalement, le processus olécrânien est représenté comme une structure curviligne hyperéchogène qui est séparée de la peau sus-jacente par une fine couche de tissu conjonctif lâche contenant la bourse synoviale olécrânienne. En raison de ses parois minces et de l'absence de contenu liquidien, la bourse olécrânienne normale n'est pas visible à l'échographie. Des précautions doivent être prises pour ne pas appliquer une pression excessive avec la sonde lors de l'évaluation de cette bourse, car de petits épanchements de bourse peuvent être expulsés.
Pour l'évaluation de la face postéro-médiale de l'articulation, y compris le tunnel cubital et le nerf cubital, le coude du patient doit être placé en rotation externe forcée pour permettre la visualisation et la palpation de l'épicondyle médial et de l'olécrâne. Celle-ci peut être obtenue soit avec le patient assis et le coude en extension et en hyperpronation avec sa face dorsale face à l'examinateur soit, au moins pour le côté droit, avec le patient en décubitus dorsal et le bras en abduction en rotation externe maximale, suspendu à la table (Martinoli et al. 2000 ; Jacobson et al. 2001).
Pour examiner le tunnel cubital, la sonde doit être placée dans le plan transversal avec une extrémité sur l'olécrâne et l'autre sur l'épicondyle médial (Jacobson et al. 2001). Semblable à la situation dans d'autres sites, les repères osseux fonctionnent bien dans la pratique de routine pour sélectionner le positionnement correct de la sonde. Parce que le nerf traverse un espace étroit délimité par des os proéminents, les petits transducteurs sont supérieurs pour évaluer cette région. Les scanners grand axe sont moins utiles que les plans petit axe pour suivre le nerf cubital (Fig. 23). Le balayage systématique dans des plans à petit axe commence à la face interne de la partie supérieure du bras, où le nerf cubital chemine dans une position superficielle par rapport au triceps. Au niveau du sillon huméral, le nerf cubital est situé près de la pente interne de l'épicondyle médial. Il apparaît généralement comme une structure ovoïde proche du cortex osseux hyperéchogène de l'épicondyle (Fig. 24a, b). Dans la partie distale du tunnel, le nerf ulnaire est visible entre les têtes humérale et ulnaire du muscle fléchisseur ulnaire du carpe (Fig. 24c, d). Dans des états normaux, la section transversale du nerf cubital est légèrement plus grande au niveau de l'épicondyle (6.8 mm2) qu'au niveau du bras distal (5.7 mm2) et de l'avant-bras proximal (6.2 mm2) (Chiou et al. 1998) . Il faut faire attention à ne pas confondre cette augmentation normale de la taille du nerf à l'intérieur du tunnel cubital avec un signe de neuropathie ulnaire. Certaines divergences existent dans la littérature sur la façon dont la taille du nerf cubital doit être considérée comme normale. Une section transversale de 7.5 mm2 a été initialement indiquée comme valeur seuil pour le syndrome du tunnel cubital (Chiou et al. 1998). Plus récemment, 7.9 mm2 a été trouvé comme valeur moyenne pour le nerf cubital normal au niveau du tunnel cubital (Jacob et al. 2004). Ces écarts semblent, au moins en partie, liés aux différences entre les races et à la conception des études. Dans le tunnel cubital, l'artère et les veines récurrentes ulnaires peuvent être facilement distinguées du nerf adjacent sur l'imagerie Doppler couleur. En cas d'engorgement, ces veines se dilatent et peuvent imiter des fascicules nerveux individuels enflés. L'imagerie Doppler peut aider à éviter cet écueil. Le rétinaculum du tunnel cubital et le ligament arqué sont constitués d'un fascia mince et, du moins dans les états normaux, ils ne sont pas visualisés par échographie, même en utilisant des transducteurs échographiques à très haute fréquence. L'imagerie dynamique du tunnel cubital est réalisée tout au long de la flexion complète du coude pour évaluer la position du nerf cubital et de la tête médiale du muscle triceps par rapport à l'épicondyle médial (Fig. 25). Pour cela, la sonde est placée dans le plan transversal au-dessus de l'épicondyle tandis que le patient est invité à fléchir lentement le coude (Jacobson et al. 2001). Lors de cette manœuvre, il convient de souligner que l'application d'une pression ferme sur la peau avec le transducteur doit être évitée car elle peut empêcher la luxation du nerf du tunnel.
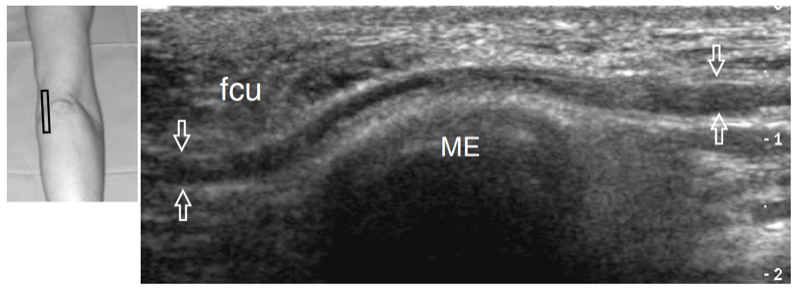
Fig. 23. Nerf ulnaire normal. Image échographique grand axe 12−5 MHz du nerf cubital normal obtenue au-dessus du tunnel cubital avec le coude en extension. Les relations du nerf (flèches) avec l'épicondyle médial (ME) et le muscle fléchisseur ulnaire du carpe (fcu) sont montrées. Le nerf ulnaire présente un aspect hypoéchogène et une épaisseur assez uniforme dans tout le tunnel. L'insert en haut à gauche de la figure indique le positionnement de la sonde.
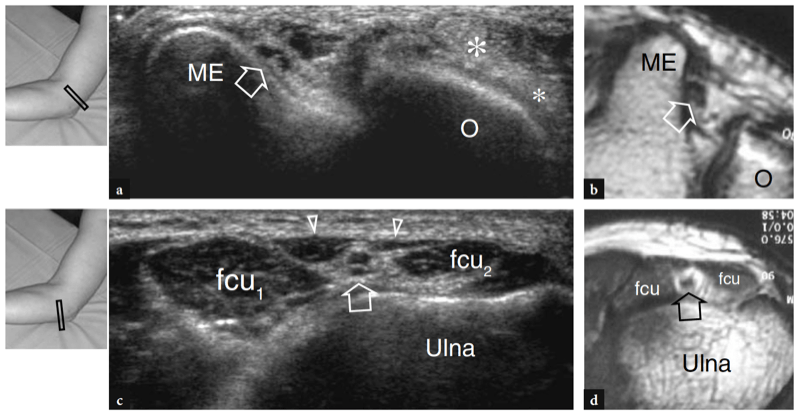
Fig. 24a–d. Tunnel cubital normal. Une image US transversale 12−5 MHz au niveau du tunnel cubital proximal (rainure condylienne) avec une corrélation d'imagerie b T1w SE MR montre la relation normale du nerf ulnaire (flèche) avec l'épicondyle médial (ME). Observez le tendon distal du triceps (astérisques) au-dessus de l'olécrâne (O). c Image US transversale 12−5 MHz au niveau du tunnel cubital distal (tunnel cubital approprié) avec d T1w SE La corrélation d'imagerie IRM montre le nerf (flèche) sous le ligament arqué (têtes de flèches) qui relie l'humérus (fcu1) et l'ulnaire (fcu2 ) chefs du muscle fléchisseur ulnaire du carpe. Les inserts en haut à gauche des figures indiquent le positionnement de la sonde.
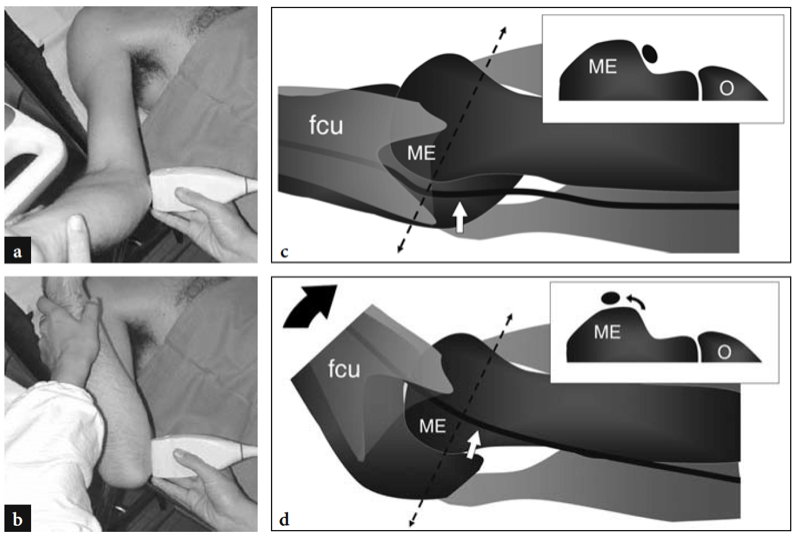
Fig. 25a–d. a,b Photographies illustrant la technique de balayage pour évaluer la position du nerf cubital droit par rapport à l'épicondyle médial avec extension du coude (a) et pendant les degrés progressifs de flexion du coude (b). Notez que la sonde reste stabilisée sur le plan transversal entre l'épicondyle médial et l'olécrâne pendant le mouvement complet du coude. c,d Les dessins schématiques du coude médial examiné en extension c et en flexion d illustrent le mécanisme de l'instabilité du nerf ulnaire au niveau du tunnel cubital. Notez l'absence du rétinaculum d'Osborne (voir pour comparaison Fig. 8.7c). Lorsque le coude est en extension, le nerf cubital (flèche blanche) est contenu dans le tunnel. La flexion du coude (flèche noire) luxe le nerf cubital en avant de l'épicondyle médial (ME). fcu, muscle fléchisseur ulnaire du carpe. Ligne pointillée, positionnement approprié de la sonde pendant le balayage.
26. PATHOLOGIE DU COUDE
Une variété de troubles peut impliquer les tissus mous du coude. Plusieurs conditions liées à des sites anatomiques spécifiques peuvent présenter des symptômes qui se chevauchent et sont facilement confondues cliniquement.
27. PATHOLOGIE ANTÉRIEURE DU COUDE : DÉCHIRURE DISTAL DU TENDON DU BICEPS
L'une des causes les plus fréquentes de douleur aiguë antérieure du coude est la rupture du tendon distal du biceps. Ces déchirures représentent moins de 5 % de toutes les lésions du tendon du biceps, les lésions proximales étant beaucoup plus fréquentes (Agins et al. 1988). Ils surviennent généralement après 40 ans (55 ans en moyenne) chez les travailleurs manuels qui tentent de soulever un objet lourd (ou chez les haltérophiles et les culturistes) ou lors d'une contraction excentrique vigoureuse du biceps contre résistance. Les déchirures distales du tendon du biceps peuvent survenir soit avec une avulsion du tendon par la tubérosité radiale (plus fréquemment), soit avec une déchirure ou une blessure à mi-substance à sa jonction myotendineuse. Semblable à d'autres tendons, il existe une zone relativement hypovasculaire dans le tendon distal du biceps, à environ 10 mm de son insertion sur la tubérosité radiale (Seiler et al. 1995). Le contact répétitif de cette zone entre le radius et le cubitus lors des mouvements de pronation semble être un facteur prédisposant à déclencher le processus dégénératif de la substance tendineuse (Seiler et al. 1995). Dans la plupart des cas, la rupture du tendon distal du biceps est associée à une déchirure du lacertus fibrosus, mais cette dernière structure peut également rester intacte. Cliniquement, une déchirure complète du tendon se présente avec une douleur et un défaut palpable avec une masse proximale dans la face antérieure du bras liée au muscle rétracté (Fig. 26). Bien qu'affaiblie, la flexion du coude est conservée du fait de la forte action du muscle brachial ; au contraire, la supination de l'avant-bras est plus sévèrement compromise en raison de la force limitée du petit muscle supinateur. Dans la plupart des cas, le diagnostic clinique est simple et ne nécessite pas d'examen d'imagerie supplémentaire. Néanmoins, les ruptures occultes sont plus fréquentes qu'on ne le pensait et, dans la pratique quotidienne, elles sont de plus en plus diagnostiquées avec l'US même quelque temps après le traumatisme. Un diagnostic clinique tardif survient principalement en l'absence de rétraction musculaire significative en raison d'un lacertus fibrosus intact, ou lorsque le muscle rétracté est caché à la palpation avec un œdème et une hémorragie environnants.
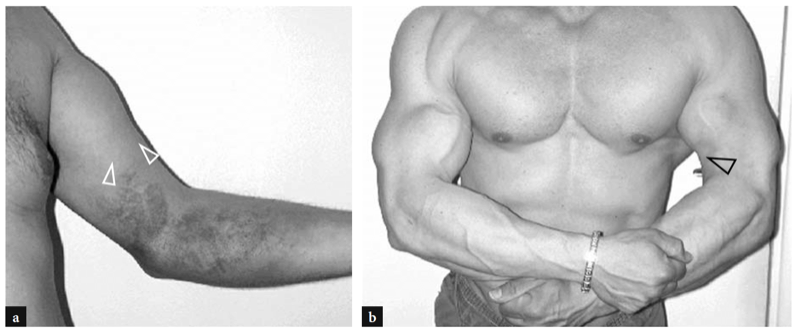
Figure 26a,b. Déchirure distale du tendon du biceps : constatations physiques. Photographies de deux patients différents ayant subi une rupture complète subaiguë et b chronique du tendon distal du biceps. En a, le patient s'est blessé au tendon gauche en tentant de soulever un objet lourd. Il s'est présenté avec une peau hémorragique sur le coude médial et l'avant-bras proximal et avec une masse proximale (têtes de flèches) dans la face antérieure du bras liée au muscle rétracté. En b, le patient était un culturiste de compétition qui refusait la réparation chirurgicale du tendon rompu. Notez le défaut (pointe de flèche) du bras antérieur gauche dû au muscle rétracté par rapport au côté droit.
Un diagnostic précoce de rupture du tendon distal du biceps est important car le résultat chirurgical est amélioré chez les patients traités dans les premières semaines après un traumatisme avant l'apparition d'adhérences tendineuses, de modifications dégénératives et d'infiltrations musculaires graisseuses. Les principales caractéristiques échographiques d'une rupture complète du tendon distal du biceps incluent la non-visualisation du tendon distal, qui apparaît rétracté en proximal (jusqu'à plus de 10 cm de la tubérosité radiale), et la détection d'un liquide hypoéchogène dans le lit tendineux lié à un hématome (Fig. 27) (Lozano et Alonso 1995 ; Miller et Adler 2000). L'épanchement est mieux reconnu autour du moignon tendineux (Fig. 28). Avec des transducteurs à haute résolution, l'échographie n'est pas suffisamment sensible pour représenter le lacertus fibrosus normal comme une bande fibrillaire très fine sur le rond pronateur. L'état du lacertus fibrosus n'est cependant pas un problème critique car il n'est pas systématiquement impliqué dans la réparation chirurgicale d'un tendon distal du biceps déchiré. De plus, rien ne prouve que le degré de rétraction du tendon soit en soi prédictif de l'état du lacertus fibrosus (Fig. 29) (Miller et Adler 2000). En cas de rupture, cependant, l'échographie peut reconnaître le liquide périfascial autour des aspects antérieur et latéral du groupe de muscles fléchisseurs-pronateurs et une rétraction tendineuse plus frappante (Fig. 29b).
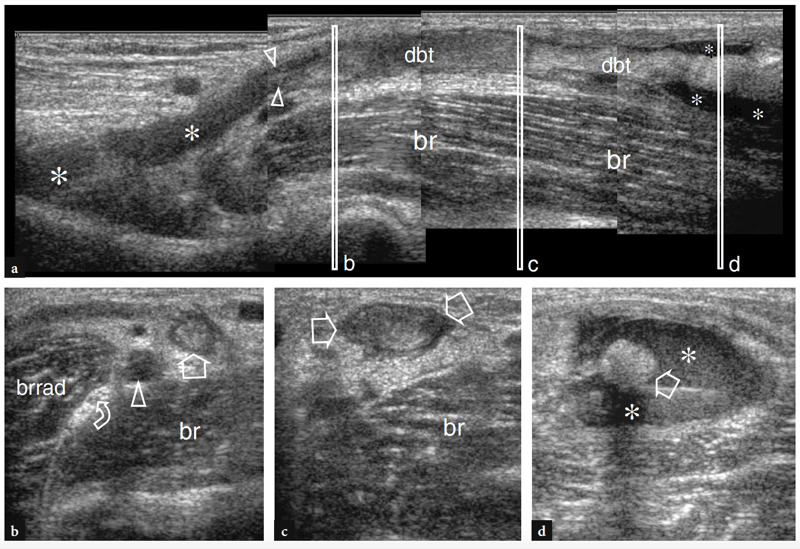
Fig. 27a–d. Rupture complète du tendon distal du biceps. une image US à axe long 12−5 MHz sur le muscle brachial (br) montre un liquide hypoéchogène (astérisques) remplissant le lit distal du tendon du biceps distal rétracté (dbt) et entourant sa jonction myotendineuse. Dans ce cas particulier, le bord du tendon (têtes de flèches) est distal par rapport à la ligne articulaire. b−d Les images US à axe court 12−5 MHz obtenues aux niveaux (barres blanches verticales) indiquées dans a montrent l'extrémité du tendon déchiré et rétracté (flèches droites) entourée d'un hématome hypoéchogène (astérisques). Les relations du tendon déchiré avec l'artère brachiale (tête de flèche), le nerf radial (flèche incurvée), les muscles brachialis (br) et brachioradialis (brrad) sont illustrées.
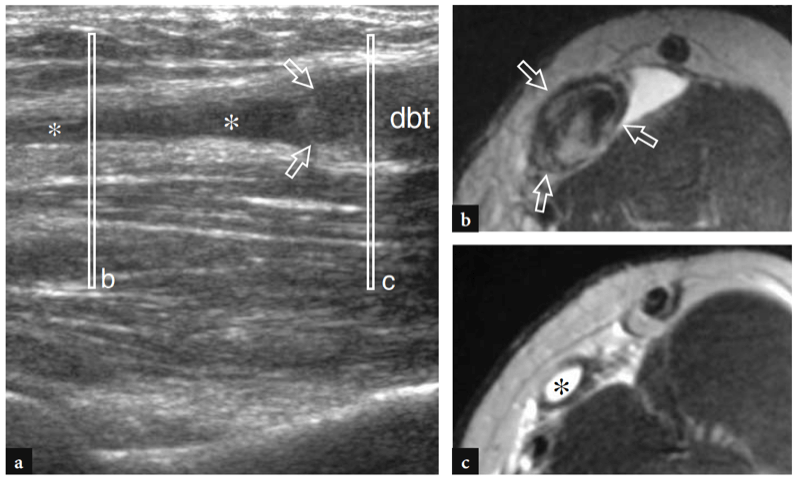
Figures 28a–c. Rupture complète du tendon distal du biceps. a Image échographique grand axe 12−5 MHz obtenue à proximité de l'articulation du coude avec b,c images transversales corrélatives T2w SE MR acquises aux niveaux (barres blanches verticales) indiqués dans un montrent le bord rétracté (flèches) du tendon distal du biceps (dbt) avec un liquide hypoéchogène (astérisques) remplissant l'espace.
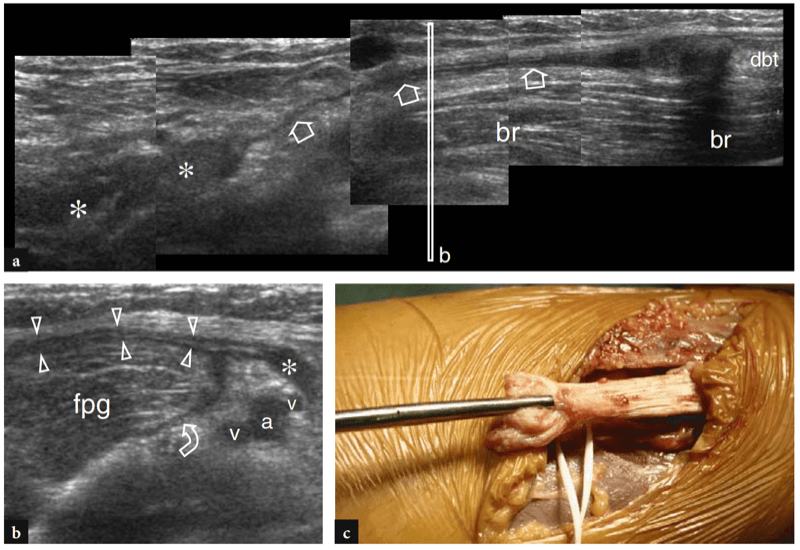
Figures 29a–c. Rupture aiguë complète du tendon distal du biceps associée à une déchirure de l'aponévrose bicipitale. une image US à axe long 12−5 MHz sur le muscle brachial (br) montre un bord de tendon nettement rétracté (dbt), l'hématome au site de rupture (astérisques) et l'absence de tendon (flèches). b L'image US à axe court 12−5 MHz obtenue au niveau (barre blanche verticale) indiqué dans a révèle du liquide (têtes de flèches et flèche incurvée) dans les tissus mous entourant le groupe fléchisseur-pronateur (fpg) des muscles, suggérant une blessure coïncidente du lacertus fibrosus. Dans ce cas, la lésion de l'aponévrose bicipitale a été confirmée chirurgicalement. a, artère brachiale ; v, veines cubitale. c Vue macroopératoire du même cas.
La tendinite et les déchirures partielles moins courantes du tendon distal du biceps se présentent avec une douleur et une sensibilité localisées au niveau de la fosse antécubitale. Ces conditions font généralement suite à des microtraumatismes répétés ou à une activation forcée du biceps. La douleur peut être exacerbée lors d'une résistance à la flexion du coude ou à la supination de la main et est aggravée par la palpation directe du tendon. À l'échographie, les déchirures partielles apparaissent comme un épaississement ou un amincissement hypoéchogène du tendon et comme des irrégularités de contour ou une ondulation sans discontinuité du tendon (Fig. 30) (Miller et Adler 2000). Le bilan de ces ruptures peut être difficile à l'échographie du fait de l'anisotropie liée au trajet oblique du tendon et à sa position profonde. L'aspect américain de la tendinite du biceps est très similaire à celui des déchirures partielles et la précision diagnostique de l'échographie pour différencier ces affections repose sur la disponibilité d'un transducteur de haute qualité ainsi que sur l'expérience globale de l'examinateur. Dans les cas douteux, l'IRM est un moyen précis de confirmer le diagnostic de déchirures partielles (Falchook et al. 1994).
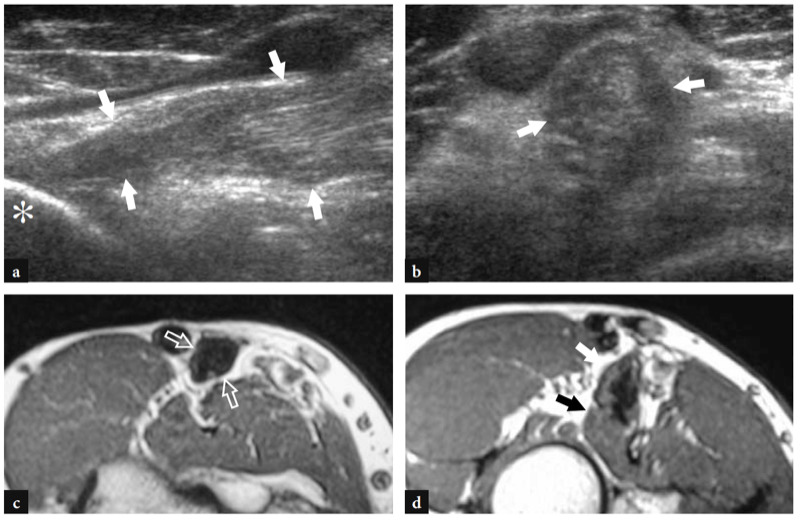
Fig. 30a–d. Rupture partielle du tendon distal du biceps. a Les images US grand axe et b petit axe 12−5 MHz obtenues au niveau distal de l'articulation du coude avec c, d images transversales corrélatives T1w SE MR montrent un tendon épaissi et hétérogène (flèches) s'insérant sur la tubérosité radiale (astérisque) .
Le traitement chirurgical des ruptures tendineuses complètes comprend la réparation et le rattachement du tendon rétracté à la tubérosité radiale ou, alternativement, au muscle brachial ou à la tubérosité ulnaire. La première technique donne de meilleurs résultats dans la restauration de la supination mais présente un risque significativement plus élevé de lésion du nerf radial. Après chirurgie, le tendon apparaît épaissi et hypoéchogène avec des images hyperéchogènes linéaires internes liées aux sutures (Fig. 31).
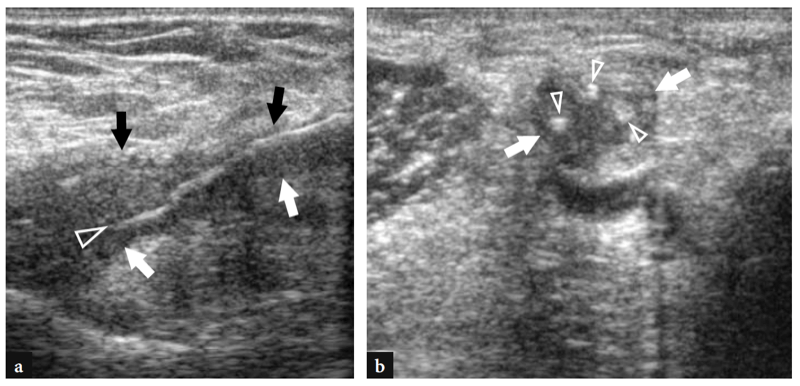
Figure 31a,b. Tendon distal du biceps postopératoire. Après réparation chirurgicale, une échographie grand axe et b petit axe 12−5 MHz révèle un tendon distal du biceps épaissi et ondulé (flèches). Des adhérences et des irrégularités dans les tissus péritendineux sont également observées. Observez les sutures, qui apparaissent comme des échos brillants (pointes de flèches) dans la substance du tendon.
28. BURSITE BICIPITORADIALE (CUBITALE)
Le tendon distal du biceps n'est pas investi par une gaine synoviale mais il est recouvert d'un paraténon. Juste en amont de l'insertion du tendon, il est en contact avec la bourse bicipitoradiale (cubitale). Cette bourse est située entre le tendon distal du biceps et la tubérosité radiale pour réduire les frottements lors de la pronation de l'avant-bras (Skaf et al. 1999). La bursite bicipitoradiale est une affection rare qui peut résulter de plusieurs causes (infection, arthropathie inflammatoire, amylose, etc.) mais elle est le plus souvent secondaire à des traumatismes mécaniques répétitifs ainsi qu'à des tendinoses et déchirures du biceps distal. Sur le plan clinique, le gonflement de la bourse bicipitoradiale peut être apprécié comme une masse non spécifique dans la fosse antécubitale souvent associée à une douleur antécubitale, en particulier lors du mouvement du coude et de la rotation de l'avant-bras. Étant donné que le tableau clinique de la bursite est similaire à celui de la tendinite et que la localisation profonde de la bourse rend la palpation difficile, un diagnostic définitif de bursite cubitale repose principalement sur les résultats de l'imagerie.
Lorsque la bourse bicipitoradiale n'est que légèrement distendue, l'échographie peut avoir des difficultés à la distinguer du tendon distal du biceps adjacent qui semble hypoéchogène en raison de l'anisotropie (Miller et Adler 2000). Habituellement, les coupes transversales avec l'avant-bras en supination permettent de mieux délimiter la forme de la bourse. À l'US, la bursite bicipitoradiale apparaît comme une masse hypoéchogène située à proximité du tendon distal du biceps (Liessi et al. 1996). Il peut avoir des cloisons, des parois épaisses et un contenu échogène. Des corps de riz ont été décrits dans cette bourse avec US (Spence et al. 1998). Lorsqu'elle est distendue par une grande quantité de liquide, la bourse bicipitoradiale peut entourer complètement la partie distale du tendon distal du biceps, imitant ainsi une ténosynovite (Fig. 32). La bursite bicipitoradiale doit être différenciée des kystes synoviaux et ganglionnaires et des autres masses des tissus mous. Les ganglions proviennent généralement de la capsule antérieure et peuvent s'étendre à une distance variable de l'articulation, disséquant les tissus mous de l'avant-bras (Steiner et al. 1996). La visualisation d'un pédicule qui relie le kyste à la cavité articulaire du coude peut aider au diagnostic. Une bursite calcifiée peut être rencontrée chez les patients atteints d'ostéodystrophie rénale (Fig. 33). Pour la bursite asymptomatique, aucun traitement n'est nécessaire, alors que la plupart des patients symptomatiques sont traités avec succès avec du repos, de la physiothérapie et des médicaments anti-inflammatoires.
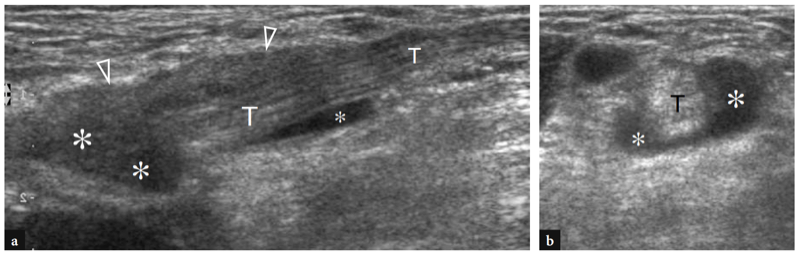
Figure 32a,b. Bursite bicipitoradiale. a Les images américaines longitudinales et b transversales à 12−5 MHz sur la fosse antécubitale au niveau distal de la ligne articulaire montrent une distension liquidienne de la bourse bicipitoradiale (astérisques) qui entoure presque complètement le tendon distal normal adjacent du biceps (T), imitant ainsi une ténosynovite processus.
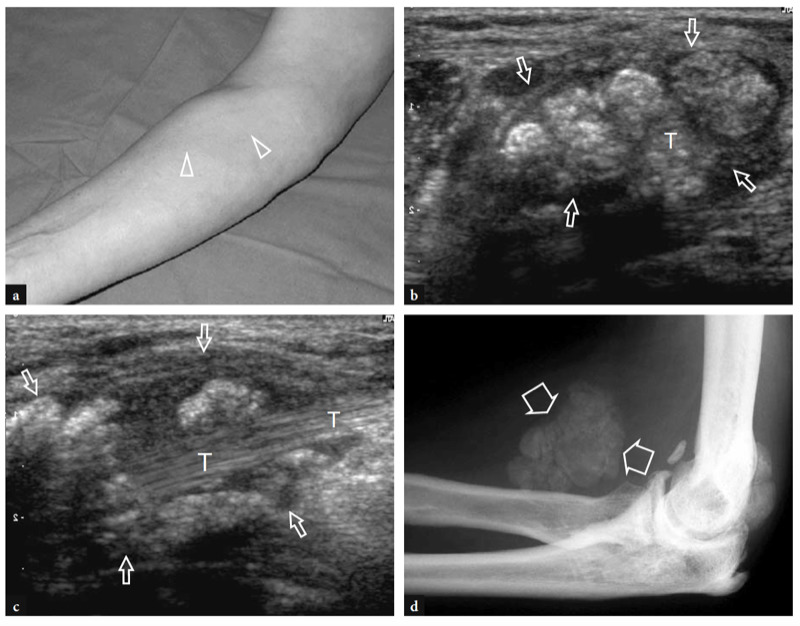
Fig. 33a–d. Bursite bicipitoradiale calcifiée chez une femme atteinte d'insuffisance rénale chronique qui présentait une masse palpable dans la fosse antécubitale et des difficultés de pronation. a La photographie montre un gonflement focal des tissus mous (têtes de flèches) sur l'avant-bras proximal antérieur. b Les images américaines transversales et c longitudinales à 12−5 MHz révèlent des dépôts hyperéchogènes étendus (flèches) avec de faibles ombres acoustiques postérieures liées à des calcifications avec la bourse bicipitoradiale. La bourse présente des parois épaissies et la partie distale du tendon du biceps (T) est complètement entourée de calcifications. d La radiographie latérale corrélative montre l'essentiel des calcifications (flèches) dans la fosse antécubitale.
29. PATHOLOGIE DU COUDE MÉDIAL : ÉPICONDYLITE MÉDICALE (ÉPITROCHLÉITE)
L'épicondylite médiale, communément appelée « coude du golfeur », « coude du tennis médial » ou « coude du lanceur », survient beaucoup moins fréquemment que l'épicondylite latérale et se manifeste généralement par une douleur et une sensibilité sur la face antérieure de l'épicondyle médial qui est renforcée par la préhension et par pronation résistée de l'avant-bras. Certaines activités sportives nécessitant un effort répétitif en valgus au niveau de l'articulation du coude, telles que le golf, le lancer de javelot et le squash, peuvent prédisposer à cette condition. L'épicondylite médiale est produite par la dégénérescence et la déchirure du tendon fléchisseur commun par rapport à la surutilisation du groupe de muscles fléchisseurs-pronateurs. Une enthésopathie est fréquemment observée à la place d'une tendinopathie. Dans cette condition, l'épanchement articulaire est absent et le coude conserve une gamme complète de mouvements. L'aspect américain de l'épicondylite médiale est similaire à l'aspect des autres tendinopathies dégénératives qui impliquent l'attachement des tendons à l'os et comprend des modifications hypoéchogènes de la substance tendineuse secondaires à une tendinose ou à des déchirures d'épaisseur partielle (Fig. 34) (Ferrare et Marcelis 1997). La rupture complète du tendon fléchisseur commun est rare. Dans ce contexte clinique, l'échographie peut aider à distinguer une tendinopathie d'une lésion du ligament collatéral médial sous-jacent. La neuropathie ulnaire peut être associée à une tendinose du tendon fléchisseur commun.
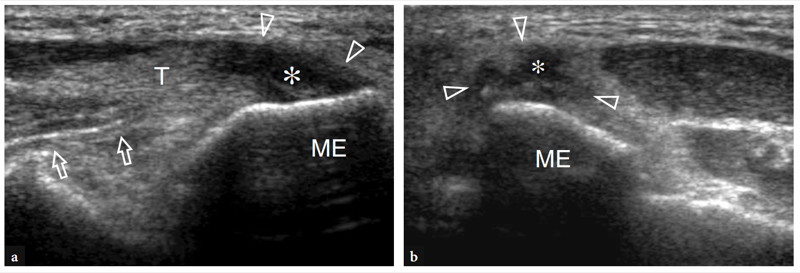
Figure 34a,b. Épicondylite médiale. a Les images échographiques longitudinales et b transversales à 12−5 MHz du coude médial chez un joueur de golf souffrant de douleurs chroniques au coude révèlent un tendon fléchisseur commun enflé (têtes de flèches) avec une zone hypoéchogène de pleine épaisseur (astérisque) compatible avec une tendinose sévère. Un ligament collatéral médial d'apparence normale (flèches) sous-tend l'origine anormale du tendon. ME, épicondyle médial ; T, partie proximale du tendon fléchisseur commun.
30. BLESSURE DU LIGAMENT COLLATÉRAL MÉDIAL
Le ligament collatéral médial est plus fort que le ligament collatéral latéral. Sa dégénérescence et sa déchirure avec ou sans lésion du tendon fléchisseur commun adjacent peuvent être secondaires à un sur-étirement aigu ou chronique répété en valgus lors des phases d'accélération du lancer ou résulter d'une chute ou d'une luxation postérieure du coude. Le lancer de baseball est l'activité sportive la plus souvent associée aux lésions du ligament collatéral médial et à l'instabilité de l'articulation médiale. Lorsque la bande antérieure est blessée, l'échographie haute résolution révèle un ligament hypoéchogène épaissi avec un épanchement environnant légèrement postérieur et profond à l'épicondyle médial (Vanderschueren et al. 1998 ; Jacobson et van Holsbeeck 1998 ; Ward et al. 2003). Les calcifications peuvent également être associées à des déchirures ligamentaires (Nazarian et al. 2003). En cas de rupture complète, l'examen échographique peut montrer soit une lacune, soit des zones hypoéchogènes focales dans la partie proximale et distale du ligament (Fig. 35) (de Smet et al. 2002). Pour améliorer la confiance diagnostique, l'examen échographique à haute fréquence peut fournir une évaluation dynamique du degré de laxité articulaire médiale dans les positions de stress neutre et valgus (de Smet et al. 2002). Dans une série de lanceurs de baseball asymptomatiques, l'espace articulaire médial du coude du bras lanceur était significativement plus large pendant la sollicitation en valgus que l'espace articulaire du coude du bras non lanceur (Nazarian et al. 2003). Chez les patients symptomatiques, l'élargissement de l'articulation trochlée-cubitus et la chute des tissus mous dans l'espace articulaire distrait suggèrent une lésion du ligament collatéral médial (de Smet et al. 2002). L'échographie dynamique peut être particulièrement utile en cas de déchirure de demi-épaisseur, où le ligament est continu mais relâché. L'examen du coude non blessé doit être obtenu pour comparer la quantité d'élargissement de l'articulation qui se produit pendant la sollicitation en valgus.
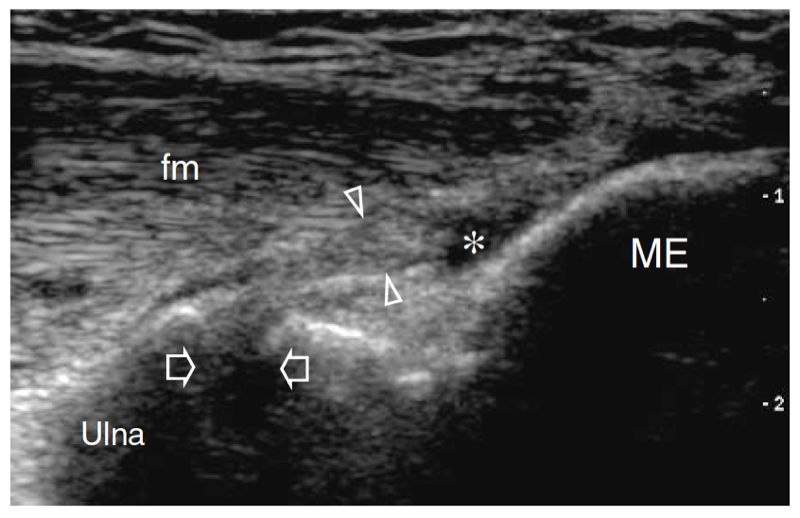
Fig. 35. Lésion du ligament collatéral médial. L'image longitudinale 12-5 MHz US obtenue avec une contrainte de valgus sur la bande antérieure du ligament collatéral médial (têtes de flèches) montre une zone hypoéchogène focale dans le ligament proximal et un léger élargissement de l'articulation du coude (flèches) compatible avec une lésion ligamentaire. ME, épicondyle médial ; fm, muscles fléchisseurs.
31. LYMPHADÉNOPATIES ÉPITROCHLÉAIRES
Juste à proximité du coude et adjacents à l'épicondyle médial et au faisceau neurovasculaire médial, de petits ganglions lymphatiques peuvent grossir à la suite d'une inflammation réactive ou septique (Barr et Kirks 1993). L'une des principales causes d'adénopathies régionales épitrochléaires médiales est la maladie des "griffes de chat", une infection causée par une bactérie gram-négative, Bartonella henselae, généralement transmise par des égratignures de la main par un animal (la plupart des patients ont des antécédents d'exposition à un chat!). Cependant, les ganglions lymphatiques hypertrophiés dans la région épitrochléaire peuvent également être impliqués par d'autres troubles, y compris les formes bénignes et malignes. L'échographie révèle l'apparition de ganglions lymphatiques réactifs constitués de masses hypoéchogènes ovales avec un hile échogène, souvent hypervasculaires au Doppler couleur (Fig. 36). Cet aspect est typique et fonctionne bien pour exclure d'autres masses des tissus mous, telles que les tumeurs neurogènes ou les sarcomes. L'examen échographique doit être étendu jusqu'à la région axillaire afin d'exclure la coexistence éventuelle d'adénopathies axillaires. Dans la maladie des griffes du chat, les adénopathies peuvent être multiples et contiguës. Cliniquement, ils s'accompagnent d'un gonflement douloureux des tissus mous et de symptômes systémiques, tels que fièvre et malaise. Les ganglions impliqués ont un schéma hypervasculaire à l'imagerie Doppler couleur et puissance et ont tendance à développer une nécrose centrale et une liquéfaction (Carcía et al. 2000 ; Gielen et al. 2003). L'infiltration hyperéchogène de la graisse périnodale due à la cellulite est une constatation caractéristique (Fig. 37a). Les ganglions lymphatiques hypertrophiés régressent le plus souvent au fil des semaines, voire des mois. Quelle que soit la cause des lymphadénopathies épitrochléaires, l'échographie peut exclure une masse locale des tissus mous, évitant ainsi la nécessité d'une biopsie ou d'une résection de cette pseudotumeur (Gielen et al. 2003). Avec le temps depuis le processus aigu, et en particulier chez les personnes âgées, les ganglions réactifs peuvent subir une infiltration adipeuse diffuse et massive conduisant à une médulla large et hyperéchogène et à une atrophie progressive du cortex externe (Fig. 37b). Dans ces cas, l'examinateur doit veiller à ne pas confondre ces ganglions atrophiques avec des lipomes ou d'autres masses hyperéchogènes des tissus mous. La détection d'un mince bourrelet hypoéchogène continu lié au cortex atrophique du ganglion peut aider au diagnostic (Fig. 37b).
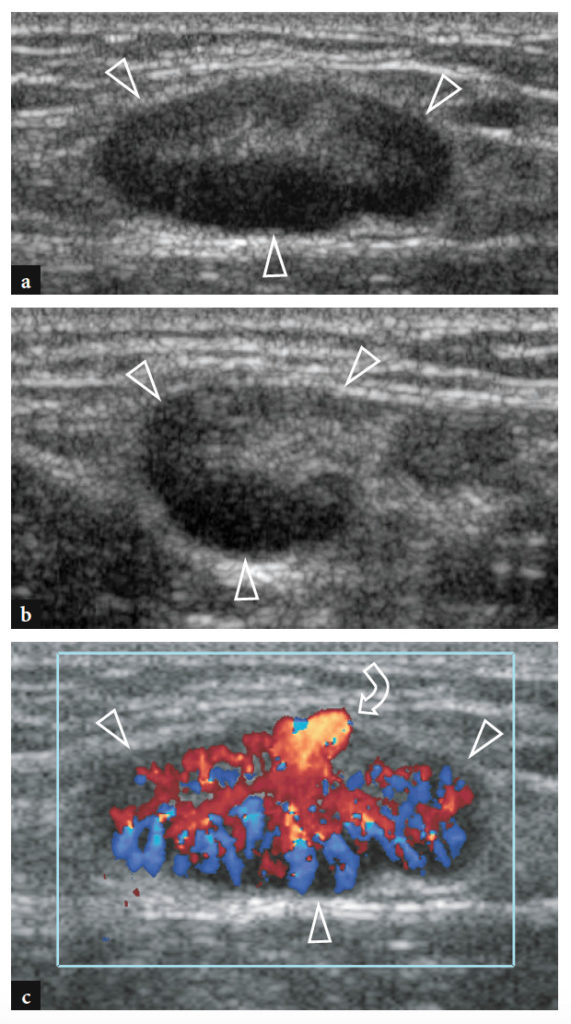
Figures 36a–c. Adénopathie épitrochléaire. a Images échographiques grand axe et b petit axe 12−5 MHz au-dessus du coude médial chez un patient présentant une masse palpable douloureuse associée à l'épicondyle médial. L'échographie identifie une masse ovale hypoéchogène avec un hile échogène compatible avec un ganglion lymphatique superficiel (têtes de flèches). c L'imagerie Doppler couleur révèle un schéma hypervasculaire du nœud avec un pédicule vasculaire (flèche) qui pénètre dans le hile et se ramifie à travers le cortex hypoéchogène. Ce ganglion lymphatique a régressé 2 semaines après le traitement médical.
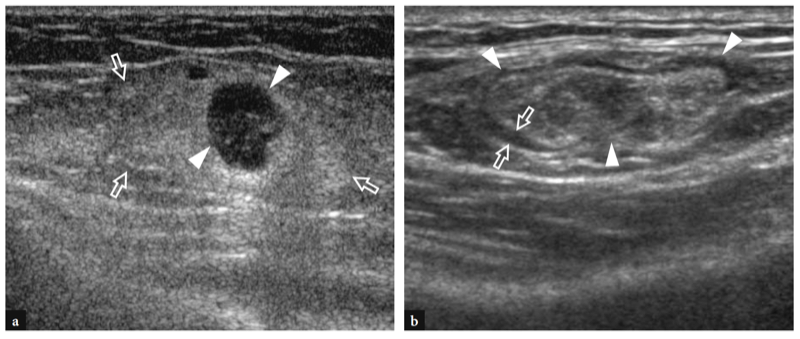
Figure 37a,b. Adénopathies épitrochléaires chez deux individus différents avec une maladie des griffes du chat active et b sans signes d'anomalies infectieuses ou inflammatoires. En a, le ganglion enflammé est complètement hypoéchogène (têtes de flèches) avec perte de définition du hile échogène et apparaît entouré d'une graisse anormalement hyperéchogène (flèches) due à une cellulite périnodale. En b, une infiltration adipeuse massive s'est produite dans un ganglion épitrochléaire (têtes de flèches) aboutissant à une large médullaire hyperéchogène. La portion corticale est nettement réduite en épaisseur et apparaît comme un mince rebord hypoéchogène périphérique (flèches).
32. PATHOLOGIE LATÉRALE DU COUDE
Le trouble le plus fréquent impliquant le coude latéral est l'épicondylite latérale, également appelée « coude de tennis », causée par une traction répétitive sur l'attache ostéotendineuse du tendon extenseur commun (Regan et al. 1992). Cette affection peut être la conséquence de microtraumatismes chroniques secondaires à un surmenage répétitif lié à des activités professionnelles ou récréatives entraînant une dégénérescence progressive et/ou des déchirures partielles du tendon extenseur commun (tendinopathie) ou une atteinte de l'insertion osseuse (enthésopathie). L'extensor carpi radialis brevis est le composant le plus fréquemment affecté du tendon extenseur commun. Bien que l'épicondylite latérale survienne généralement chez les joueurs de tennis qui blessent ce tendon - en particulier lors du coup de revers, dans lequel les extenseurs sont soumis à une plus grande tension - cette affection est beaucoup plus fréquente chez les non-athlètes. Dans la tendinopathie, les patients rapportent une douleur localisée sur le tendon extenseur commun pendant ou juste après l'activation musculaire répétitive, alors que dans l'enthésopathie, la douleur est confinée à la zone d'insertion du tendon. L'examen physique révèle une sensibilité localisée sur la face latérale du coude irradiant vers l'avant-bras proximal ou bien localisée sur la face latérale de l'épicondyle respectivement. L'épanchement intra-articulaire n'est pas un signe associé. Dans les maladies chroniques de longue date, on peut noter des douleurs au repos et une limitation de l'extension articulaire.
Le diagnostic est généralement basé sur les résultats cliniques et ne nécessite pas d'études d'imagerie. L'échographie peut être utile pour confirmer le diagnostic clinique dans les cas douteux ou réfractaires, pour révéler l'étendue et la gravité de la maladie et pour surveiller la réponse au traitement. Les principales caractéristiques échographiques de l'épicondylite latérale sont un gonflement hypoéchogène préinsertionnel du tendon avec des zones focales ou diffuses de réflectivité réduite dans la substance tendineuse et la perte du motif fibrillaire lié à la tendinose, du liquide adjacent au tendon commun et des marges tendineuses mal définies (Figues. 38, 39) (Maffulli et al. 1990 ; Connell et al. 2001 ; Miller et al. 2002d ; Levin et al. 2005). Dans une série récente, la taille moyenne des zones hypoéchogènes focales était de 8.7 mm (gamme de 3 à 15 mm) (Connell et al. 2001). Bien que les anomalies tendineuses précoces puissent être confinées aux fibres superficielles (Fig. 38a, b), l'atteinte des fibres profondes du composant extensor carpi radialis brevis est plus fréquente et peut même s'étendre jusqu'à la capsule articulaire (Fig. 38c, d). De même, la partie antérolatérale et médiane du tendon extenseur commun est plus souvent atteinte, alors que la partie postérieure reste généralement non affectée (Fig. 38b) (Connell et al. 2001). Dans les tendinoses de haut grade, l'infiltration angiofibroblastique basée sur la migration des fibroblastes et du tissu de granulation vasculaire dans la substance tendineuse provoque un schéma hypervasculaire frappant des zones hypoéchogènes intratendineuses à l'imagerie Doppler couleur et puissance (Fig. 39b). Un éperon au niveau de l'insertion du tendon extenseur commun et des irrégularités corticales à la surface antérolatérale de l'épicondyle latéral peuvent également être reconnus, bien que les modifications osseuses ne soient pas corrélées à l'activité de la maladie. Les calcifications intratendineuses peuvent également être considérées comme faisant partie des maladies de dépôt de cristaux (Fig. 40). Dans les ruptures partielles, le tendon extenseur commun peut apparaître aminci par rapport au côté opposé. En pratique, la discrimination des zones focales de tendinose et de déchirures partielles peut être difficile et l'échographie n'est fiable pour reconnaître une déchirure partielle que lorsque des plans de clivage anéchoïques discrets sans fibres intactes sont visibles dans la substance tendineuse (Connell et al. 2001). Ces déchirures apparaissent généralement sous forme de fentes longitudinales orientées distalement à partir de l'insertion osseuse (Fig. 41). Un épaississement des tissus mous péritendineux et une fine couche de liquide superficiel sur le tendon extenseur sont également plus souvent observés avec des déchirures partielles. Dans les déchirures complètes, l'échographie identifie un espace rempli de liquide séparant le tendon de son site d'attache osseux (Fig. 42) (Jacobson et van Holsbeeck 1998 ; Connell et al. 2001). Dans l'ensemble, l'échographie s'est avérée aussi spécifique mais pas aussi sensible que l'IRM pour évaluer l'épicondylite (Miller et al. 2002). En revanche, l'échographie du tendon extenseur commun a une sensibilité élevée mais une faible spécificité dans la détection des cas symptomatiques (Levin et al. 2005).
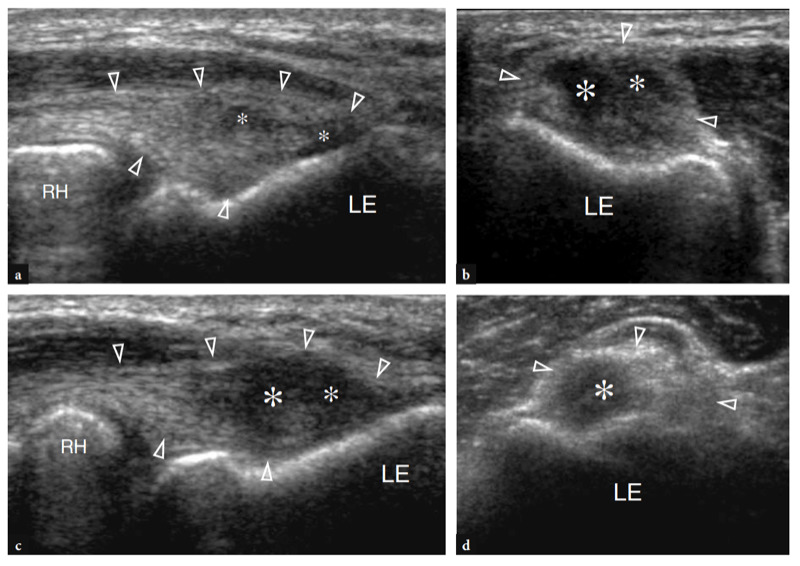
Figures 38a–d. Épicondylite latérale : spectre des apparitions échographiques chez un haltérophile souffrant de douleurs latérales bilatérales au coude. a Les images américaines à axe long et b à axe court 12−5 MHz sur l'origine du tendon extenseur commun droit révèlent un foyer hypoéchogène (astérisques) de tendinose dans les fibres superficielles d'un tendon d'apparence normale (têtes de flèches). c Les images américaines à axe long et à axe court 12−5 MHz sur l'origine du tendon extenseur commun gauche montrent une grande zone hypoéchogène (astérisques) affectant à la fois les fibres superficielles et profondes du tendon (têtes de flèches), indiquant une tendinopathie sévère. En coupe, on observe des zones hypoéchogènes anormales avec perte d'échotexture fibrillaire (astérisques) impliquant toute l'épaisseur de la moitié antérieure du tendon (têtes de flèches). Dans les deux coudes, observez l'intégrité des fibres les plus profondes par rapport au ligament collatéral latéral. LE, épicondyle latéral ; RH, tête radiale.
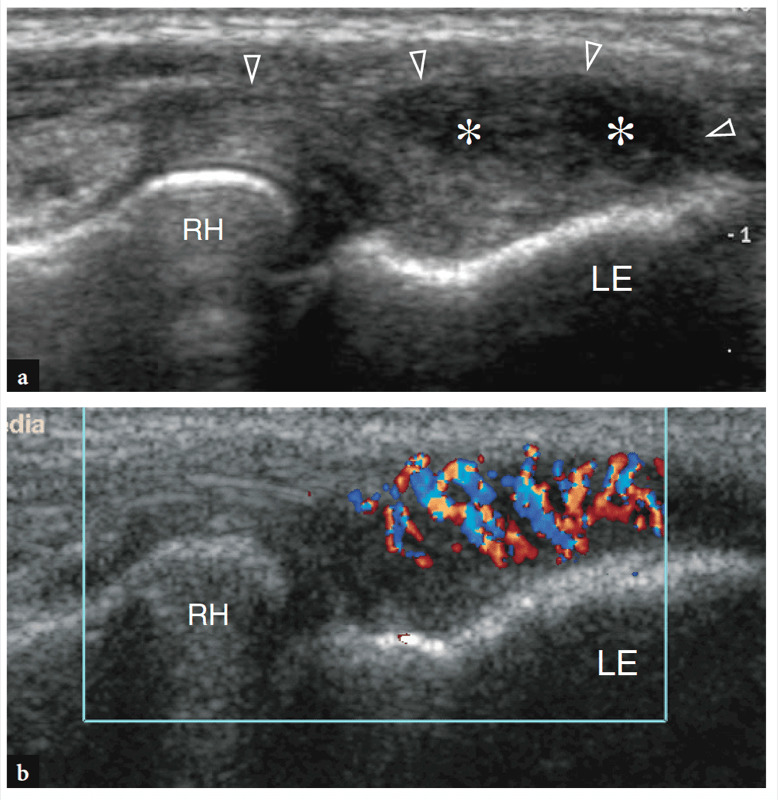
Figure 39a,b. Épicondylite latérale chez un joueur de tennis professionnel ayant des antécédents de douleur chronique du coude latéral droit. une image US à échelle de gris 12−5 MHz à axe long révèle un foyer hypoéchogène (astérisques) dans les fibres les plus superficielles de l'origine du tendon extenseur commun (têtes de flèches), alors que les fibres profondes sont préservées. b L'imagerie Doppler couleur montre un motif hypervasculaire frappant composé d'une série de minuscules vaisseaux dans les zones hypoéchogènes intratendineuses, caractéristique de la tendinose. LE, épicondyle latéral ; RH, tête radiale.
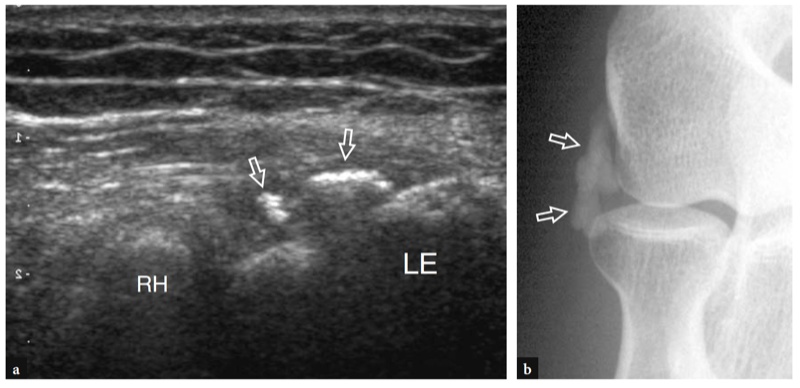
Figure 40a,b. Épicondylite latérale calcifiante. Une image US à axe long 12−5 MHz avec corrélation radiographique b chez un patient atteint d'une maladie de dépôt de cristaux de pyrophosphate de calcium et d'apparition récente de douleurs latérales au coude montre de grands foyers calcifiés (flèches) à l'origine du tendon extenseur commun. LE, épicondyle latéral ; RH, tête radiale.
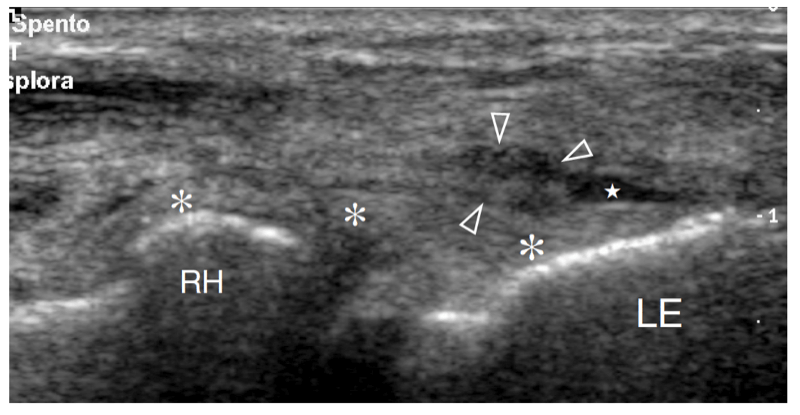
Fig. 41. Rupture d'épaisseur partielle du tendon extenseur commun. L'image US à axe long 12−5 MHz chez un travailleur manuel qui s'est présenté avec un début aigu de douleur latérale au coude révèle une scission hypoéchogène linéaire (étoile) s'étendant de l'épicondyle latéral (LE) à travers la substance de l'origine du tendon extenseur commun. Les fibres profondes déchirées (têtes de flèches) sont rétractées juste en aval de la zone hypoéchogène. Notez l'intégrité du ligament collatéral cubital latéral sous-jacent (astérisques). RH, tête radiale.
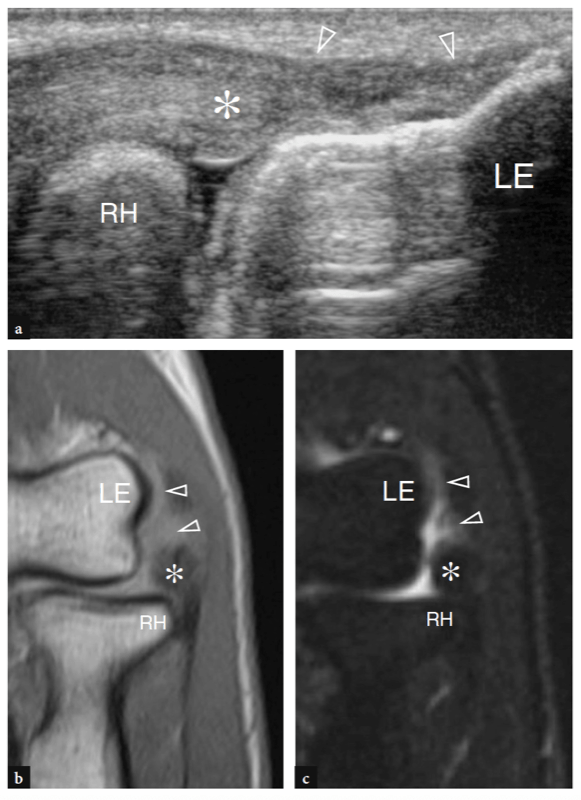
Figures 42a–c. Rupture complète du tendon extenseur commun. Une image US à axe long de 12 à 5 MHz chez un joueur de golf qui se plaignait de douleurs au coude de longue date avec une corrélation d'imagerie coronale b T1w SE et c T2w SE avec suppression de la graisse montre un tendon extenseur commun rétracté. Notez l'écart (têtes de flèches) lié à la déchirure qui sépare le bord du tendon avulsé (astérisque) de l'épicondyle latéral (LE). RH, tête radiale.
Un traitement conservateur avec repos, anti-inflammatoires, kinésithérapie et injections locales de stéroïdes donne des résultats satisfaisants dans la plupart des cas d'épicondylite latérale. Une intervention chirurgicale avec excision du tissu dégénéré, résection du tendon extenseur commun et débridement de l'origine du tendon extenseur avec libération du ligament annulaire peut être préconisée dans les cas réfractaires. La confirmation de la maladie et l'exclusion d'autres causes de douleur latérale du coude qui peuvent imiter ou accompagner l'épicondylite latérale, telles que le piégeage du nerf interosseux postérieur ou les lésions du ligament collatéral latéral, doivent cependant être vérifiées avec des modalités d'imagerie, et éventuellement avec des échographies, avant de soumettre le patient à la chirurgie.
33. BLESSURE LIGAMENTAIRE COLLATÉRALE LATÉRALE
Dans l'épicondylite latérale, le complexe ligamenteux latéral du coude, et en particulier le ligament collatéral ulnaire latéral, doit être systématiquement évalué car ce ligament est souvent blessé en association avec des déchirures du tendon extenseur commun en raison des mêmes forces ou mécanismes de surutilisation sur les structures adjacentes. (Bredella et al. 1999). Une déchirure insoupçonnée de ce ligament peut être à l'origine d'un échec du traitement conservateur chez un patient atteint d'épicondylite latérale. De plus, lorsque le ligament collatéral ulnaire latéral déchiré n'est pas reconnu en préopératoire, la libération opératoire du tendon extenseur commun peut être responsable d'une aggravation des symptômes et de la survenue d'une instabilité rotatoire postéro-latérale du coude.
Lorsque le court extenseur radial du carpe, plus superficiel, est déchiré, le ligament collatéral ulnaire latéral profond se distingue plus clairement avec l'échographie sous la forme d'une structure fibrillaire en forme de cordon située au-dessus de l'espace articulaire. Une déchirure ligamentaire isolée apparaît comme une discontinuité des fibres les plus profondes de l'origine du tendon extenseur, tandis que les déchirures impliquant à la fois le ligament et le tendon extenseur commun provoquent une interruption de pleine épaisseur des fibres sur la face latérale de l'articulation radiocapitellaire et un hématome des tissus mous autour de la marge proximale du capitule (Connell et al. 2001). Un balayage dynamique lors d'une sollicitation soigneuse en varus peut révéler une lésion du ligament collatéral ulnaire latéral en décrivant un élargissement de l'espace articulaire du coude latéral par rapport au coude normal opposé (Fig. 43).
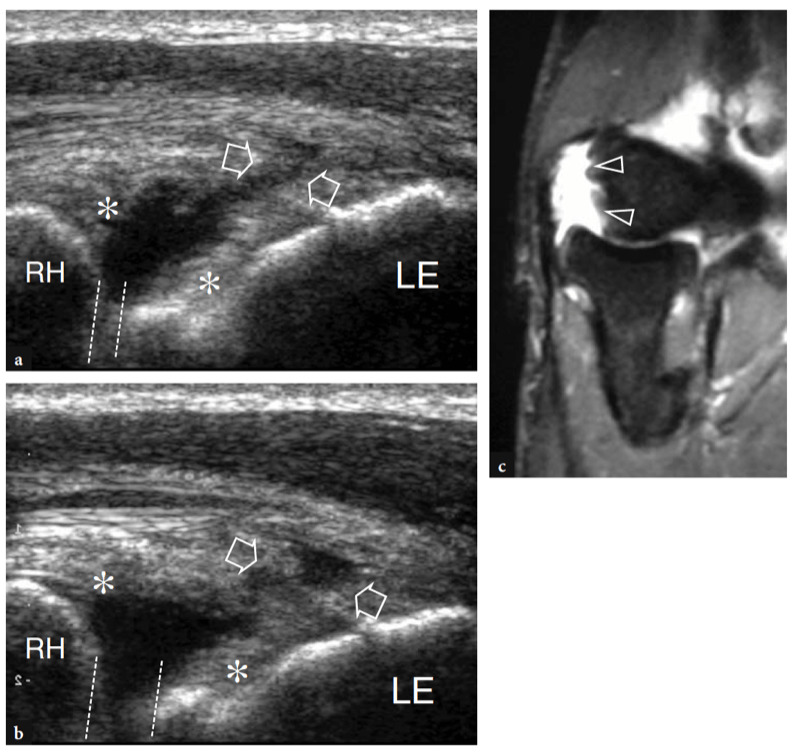
Figures 43a–c. Déchirure complète du tendon extenseur commun et du ligament collatéral ulnaire latéral. a, b Images échographiques longitudinales 12−5 MHz obtenues sur l'origine du tendon extenseur commun a en position neutre et b avec une contrainte en varus. En a, l'échographie identifie une grande fente hypoéchogène horizontale dans toute l'épaisseur de l'origine du tendon extenseur commun (flèches) et du ligament collatéral ulnaire latéral (astérisques). En b, l'effort en varus du coude montre un élargissement de l'espace articulaire radio-capiteller (lignes pointillées). RH, tête radiale ; LE, épicondyle latéral. c L'image corrélative STIR MR confirme la rupture complète des deux structures (têtes de flèches).
Dans le «coude tiré», une blessure courante chez les enfants due au glissement du ligament annulaire sur la tête radiale suite à une pronation forcée, l'échographie est en mesure de décrire une distance accrue entre la tête radiale et le capitellum huméral probablement due à l'impact de l'annulaire ligament (Kosuwon et al. 1993).
34. SYNDROME SUPINATEUR (NEUROPATHIE INTEROSSEUSE POSTERIEURE)
Le syndrome supinateur, également appelé « syndrome interosseux postérieur » ou « syndrome du tunnel radial », est une neuropathie de compression rare du membre supérieur affectant le nerf interosseux postérieur juste à côté ou derrière le muscle supinateur (Spinner 1968). Ce nerf est vulnérable aux lésions du bord proximal du ventre superficiel du muscle supinateur qui forme une arche libre, forte et fibreuse, « l'arcade de Frohse ». À ce site, le nerf interosseux postérieur peut être attaché et piégé par des bandes fibreuses, des vaisseaux radiaux récurrents en forme d'éventail ou par l'étanchéité du passage dans les couches superficielles et profondes du supinateur. De plus, il peut être comprimé par une variété de masses de tissus mous, telles que les lipomes paraostés et les ganglions profonds. Les fractures de la tête radiale et du cou, y compris les fractures-luxations de Monteggia, peuvent également déplacer et envelopper le nerf interosseux postérieur par un callus lors de son passage dans le tunnel du supinateur. Cliniquement, la neuropathie interosseuse postérieure produit un tableau clinique distinct d'une lésion du nerf radial du bras. En fait, le patient a un « doigt tombant » plutôt que le « poignet tombant » caractéristique d'une neuropathie radiale, car la faiblesse musculaire épargne l'extenseur radial du carpe (Fig. 44). L'extension des doigts au niveau des articulations métacarpo-phalangiennes est altérée et il existe un déficit d'abduction et d'extension du pouce. De plus, la neuropathie interosseuse postérieure peut provoquer une douleur brûlante et une sensibilité au niveau du coude latéral, imitant éventuellement une « épicondylite latérale résistante ».
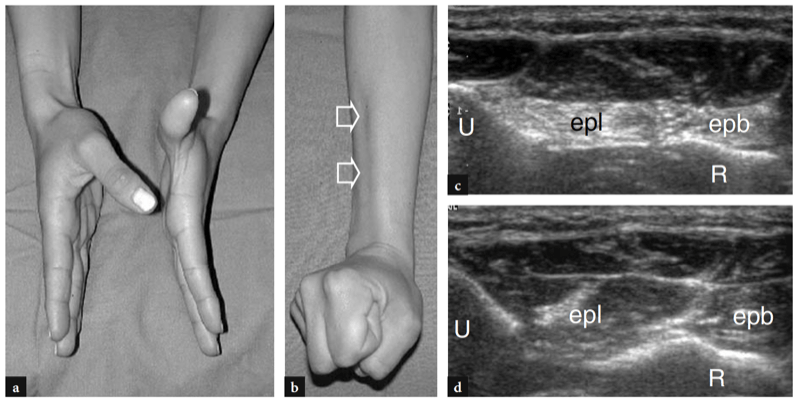
Figures 44a–d. Syndrome du nerf interosseux postérieur chez une jeune femme présentant une faiblesse intense dans l'extension des doigts droits, impliquant notamment des mouvements du pouce, et une dépression cutanée longitudinale (flèche) sur le dos de l'avant-bras suite à une contusion du coude latéral. c L'image US transversale 12−5 MHz au niveau de l'avant-bras dorsal moyen révèle une perte de volume et un aspect hyperéchogène des muscles extenseur du pouce long (epl) et extenseur du pouce court (epb) par rapport à l'atrophie graisseuse. La chirurgie a confirmé la lésion traumatique du nerf interosseux postérieur. d Côté controlatéral normal. U, cubitus ; R, rayon.
L'échographie haute résolution est capable d'identifier le conflit du nerf interosseux postérieur dans la zone supinatrice. Le nerf comprimé apparaît généralement gonflé et hypoéchogène à proximité ou à l'intérieur du muscle supinateur (Bodner et al. 2002). Dans les contextes post-traumatiques, le nerf peut sembler déplacé par une tête radiale mal alignée et peut présenter des segments épaissis et amincis alternés entre les ventres superficiel et profond du muscle supinateur en raison possible d'une blessure par étirement (Fig. 45). De plus, le nerf peut être vu enveloppé par du tissu cicatriciel hypoéchogène suite à une fracture radiale (Fig. 46).
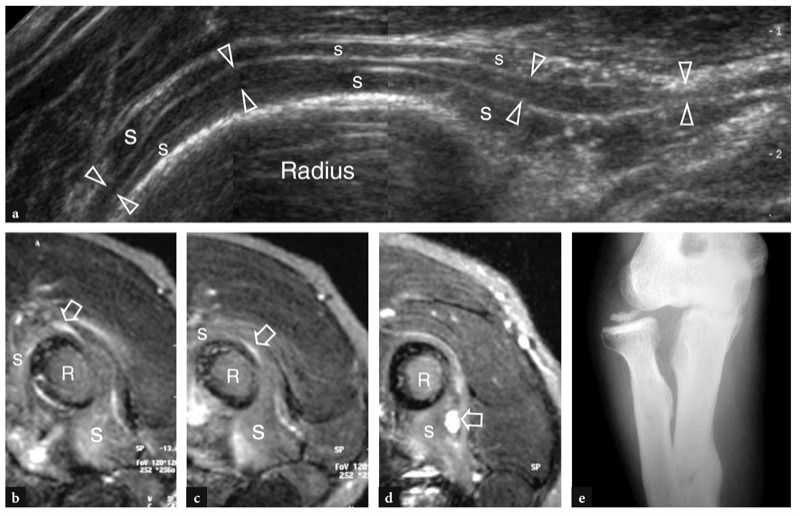
Fig. 45a–e. Syndrome du nerf interosseux postérieur chez un patient atteint d'une fracture-luxation de Monteggia mal alignée (type IV). une image US à champ de vision étendu 12−5 MHz reconstruite selon l'axe longitudinal du tunnel supinateur montre le nerf interosseux postérieur (têtes de flèches) qui alterne des parties épaissies et amincies lorsqu'il traverse le ou les muscles supinateurs. b–d Les images IRM en série T2*GRE révèlent une légère hyperintensité dans le(s) muscle(s) supinateur(s) due à un œdème de dénervation. Le nerf (flèches) apparaît nettement en hypersignal. R, rayon. e La radiographie montre le désalignement du radius, qui apparaît subluxé antérolatéralement.
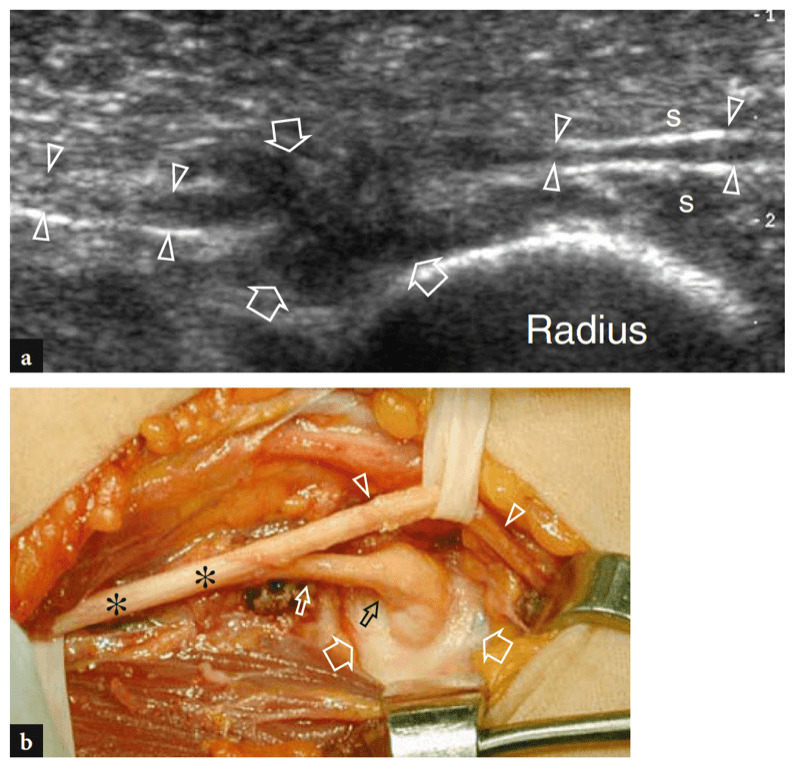
Figure 46a,b. Syndrome du nerf interosseux postérieur. une image US transversale de 12 à 5 MHz obtenue sur la zone du supinateur chez un patient ayant déjà subi une fracture de la tête radiale et un déficit du nerf radial montre le nerf interosseux postérieur (têtes de flèches) emprisonné dans une cicatrice hypoéchogène (flèches) dans la zone du muscle supinateur (s ). b La vue opératoire macroscopique montre le tronc principal du nerf radial (astérisques) lorsqu'il se divise en la branche sensorielle cutanée superficielle (têtes de flèches) et le nerf interosseux postérieur profond (flèches étroites). Ce dernier nerf est irrégulièrement gonflé lors de son passage sur l'os (grosses flèches) du fait de l'enrobage cicatriciel visible en a.
La chirurgie décompressive du nerf interosseux postérieur est indiquée en cas d'aggravation continue ou d'absence de récupération de la fonction après quelques mois.
35. PATHOLOGIE POSTÉRIEURE DU COUDE : DÉCHIRURE DISTAL DU TENDON DU TRICEPS
La déchirure distale du tendon du triceps est une affection rare qui survient principalement au niveau ou à proximité du processus olécrânien de l'ulna, souvent associée à une tache osseuse attachée au tendon rétracté à la suite d'une fracture par avulsion (Fig. 47). Le mécanisme implique soit une flexion forcée du coude contre un triceps qui se contracte, comme cela se produit lors d'une chute sur un bras tendu, soit un coup direct sur le processus olécrânien. L'injection locale de stéroïdes dans la bourse olécrânienne, l'abus de stéroïdes anabolisants et une tendinose préexistante peuvent également jouer un rôle dans la rupture du tendon. En règle générale, les déchirures complètes surviennent plus fréquemment que les déchirures partielles, alors que la perturbation des ventres musculaires ou de la jonction myotendineuse est rare. La rupture complète du tendon distal du triceps se présente cliniquement avec une incapacité totale à étendre le coude, étant donné l'absence d'autres muscles qui peuvent aider à ce mouvement. Dans la phase aiguë, cependant, le diagnostic clinique peut être entravé par un gonflement local des tissus mous, un œdème inflammatoire et des douleurs qui limitent l'examen physique. Dans de tels cas, l'échographie peut être utile à la fois pour confirmer la lésion du tendon et pour différencier les déchirures complètes qui nécessitent une intervention chirurgicale immédiate pour éviter la rétraction du tendon et les déchirures partielles qui peuvent être traitées de manière conservatrice. Dans les ruptures aiguës complètes, l'échographie montre que le tendon distal du triceps est ondulé, rétracté et entouré de liquide (Fig. 48) (Kaempffe et Lerner 1996). L'échographie est également fiable pour délimiter le degré de rétraction du tendon et peut aider au diagnostic des ruptures atypiques, comme dans les cas de déchirures survenant à la jonction myotendineuse (Fig. 49). En raison de la relation anatomique étroite du tendon du triceps distal avec l'épicondyle médial et le tunnel cubital, un syndrome aigu de compression du nerf ulnaire peut survenir secondairement à une déchirure du tendon du triceps distal (Duchow et al. 2000). La tendinose dégénérative peut être appréciée comme un tendon hypoéchogène épaissi.
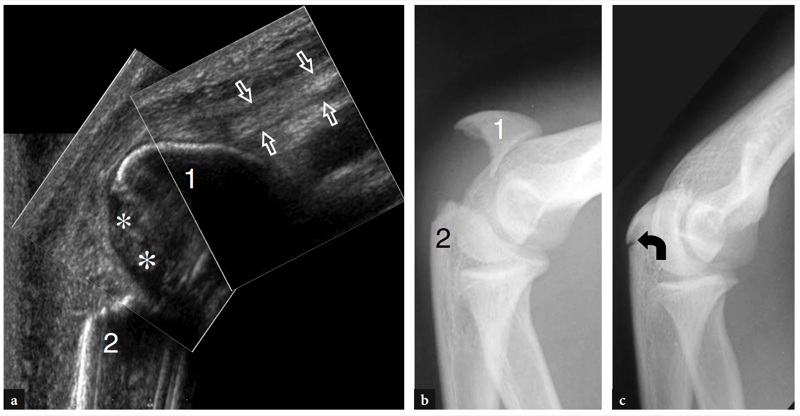
Figures 47a–c. Fracture-avulsion de l'olécrâne chez un garçon suite à un accident de vélo. a Une image US 12−5 MHz sagittale médiane reconstruite sur le coude postérieur avec une corrélation radiographique b latérale montre la fracture par avulsion du processus olécranien (1) à partir de la diaphyse ulnaire (2) due à un mécanisme de traction par le tendon distal du triceps (flèches). Notez l'avulsion coexistante de la plaque de croissance cartilagineuse (astérisques). c La radiographie de profil du côté sain opposé montre une ossification incomplète (flèche courbe) entre l'olécrâne et la diaphyse ulnaire.
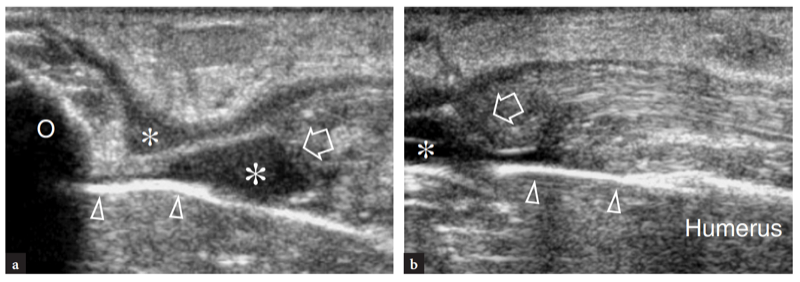
Figure 48a,b. Rupture complète du tendon distal du triceps chez un patient ayant subi une ostéosynthèse pour une fracture sus-condylienne de l'humérus. Les images échographiques 12-5 MHz médio-sagittales sur le coude postérieur obtenues en extension et en flexion légère b montrent un large défaut (astérisques) dans le tendon distal du triceps (flèche) qui semble rétracté à la suite d'une désinsertion de l'olécrâne (O). La déchirure résultait du bord inférieur de la plaque de fixation interne (têtes de flèches) qui faisait saillie dans la fosse postérieure, provoquant un conflit avec le tendon sus-jacent.
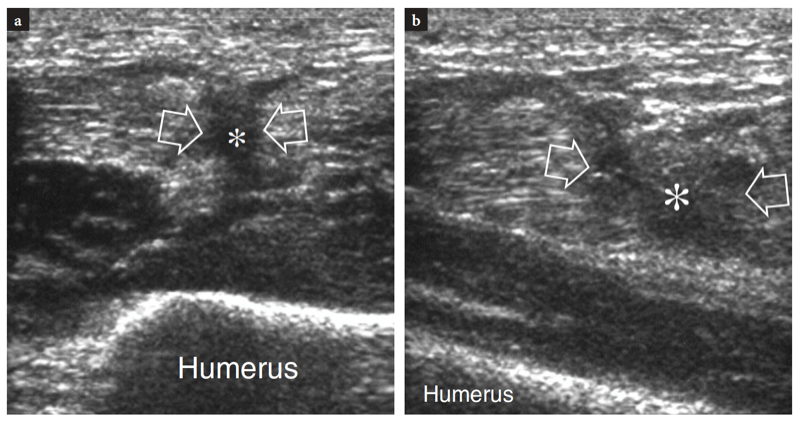
Figure 49a,b. Déchirure partielle à la jonction myotendineuse distale du triceps. Les images américaines 12−5 MHz à grand axe obtenues avec le coude étendu (a) et légèrement fléchi (b) montrent un espace (flèches) dans les fibres postérieures du triceps rempli d'hématome hypoéchogène (astérisque). L'écart hypoéchogène s'élargit à mesure que le coude fléchit.
36. BURSITE OLÉCRANIENNE
La bursite olécrânienne, la bursite superficielle la plus courante dans le corps, apparaît cliniquement comme une masse recouvrant le processus olécranien en raison d'une distension liquidienne ou d'une hypertrophie de la membrane synoviale. La cause la plus fréquente de bursite olécrânienne est une contusion locale répétitive (coude de l'étudiant, coude du mineur) qui entraîne une tuméfaction locale indolore recouverte de peau normale. L'enthésopathie calcifiante du tendon distal du triceps est un facteur prédisposant. Cependant, la distension de la bourse peut être appréciée dans une variété de troubles systémiques, tels que la polyarthrite rhumatoïde, la goutte, les maladies de dépôt d'hydroxyapatite et de pyrophosphate de calcium, ainsi que dans les conditions septiques (par exemple Staphylococcus, tuberculose) ; les patients sous hémodialyse chronique peuvent également présenter occasionnellement une bursite olécrânienne. Lorsque la bursite est secondaire à une infection ou à la goutte, le gonflement de la bourse est généralement douloureux et associé à une chaleur cutanée et à un érythème dus à des changements inflammatoires locaux. Parce que les signes systémiques sont souvent absents dans la bursite septique, la probabilité d'une bourse infectée doit toujours être gardée à l'esprit. De même, lorsque le patient a des antécédents de maladie tuberculeuse, une étiologie spécifique de bursite doit d'abord être suspectée.
L'échographie montre une bursite olécrânienne sous la forme d'une accumulation localisée de liquide et/ou d'une hypertrophie de la paroi synoviale dans le tissu sous-cutané immédiatement postérieur à l'olécrâne (Fig. 50). L'hyperémie des tissus mous est souvent reconnue par l'imagerie Doppler couleur et puissance comme résultat d'accompagnement (Lin et al. 2000). Le schéma hypervasculaire se distribue généralement selon un schéma péribursal en forme de jante. Dans les maladies de dépôt de cristaux, l'apparence américaine du liquide de la bourse est plus probablement hyperéchogène et associée à des parois épaissies et échogènes de la bourse (Fig. 51). Dans les bursites hémorragiques et septiques, le liquide peut se traduire par un aspect complexe : œdème des tissus mous environnants et cellulite sont fréquemment associés (Fig. 52). Cependant, ces caractéristiques sont trop subtiles pour permettre un diagnostic définitif basé sur les seuls résultats américains, et l'aspiration à l'aiguille du liquide, éventuellement obtenue sous la direction des États-Unis, est généralement nécessaire pour l'analyse et la culture. Dans les cas extrêmes, la prolifération synoviale chronique et la fibrose peuvent rendre la bourse indiscernable d'une tumeur solide. Une bursite calcifiée peut survenir chez les patients souffrant d'insuffisance rénale chronique (Fig. 53). Dans la polyarthrite rhumatoïde, le liquide de la bourse peut parfois être observé en train de disséquer les tissus mous superficiels de l'avant-bras après la rupture de la bourse. Chez ces patients, des nodules sous-cutanés peuvent être observés dans la région olécrânienne et le long de l'ulna proximal. Ces nodules doivent être pris en compte dans le diagnostic différentiel car ils peuvent imiter une bursite olécrânienne ou un néoplasme solide Distal par rapport à la bourse olécrânienne, une petite bourse sous-olécrânienne supplémentaire peut exister à la face postérieure de la diaphyse ulnaire proximale. Dans de rares cas, cette bourse peut être impliquée par les mêmes processus affectant le plus grand olécrâne (Fig. 54).
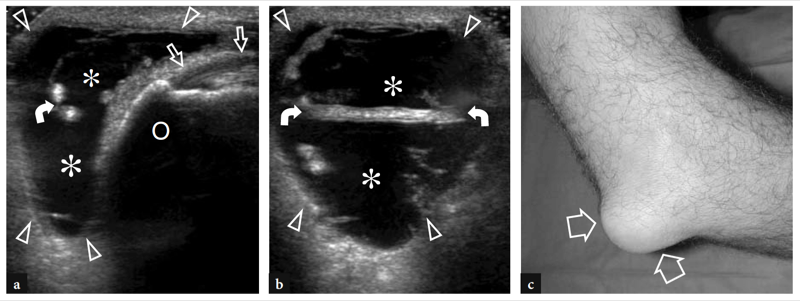
Figures 50a–c. Bursite olécrânienne chronique traumatique chez un ouvrier qui s'était récemment blessé plusieurs fois à l'arrière du coude droit. a Les images américaines 12−5 MHz transversales médianes et b transversales sur le processus olécrânien (O) montrent une bourse olécrânienne nettement distendue (têtes de flèches) contenant des septa épais (flèches courbes) et un épanchement anéchoïque (astérisques). Flèches droites, tendon distal du triceps. c Photographie montrant la masse de la bourse (flèches) sur le coude postérieur.
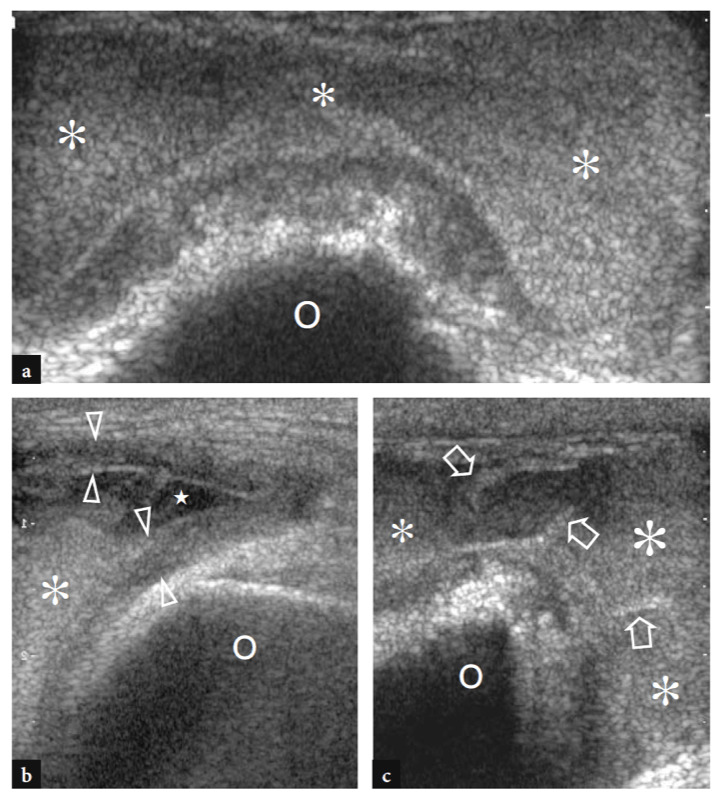
Figures 51a–c. Bursite olécrânienne à l'hydroxyapatite. a Transversale et b,c longitudinale 12−5 MHz US images d'une masse douloureuse des tissus mous sur l'olécrâne (O) montrent la bourse olécrânienne remplie de liquide homogène hautement échogène (astérisques) que l'on peut voir fluctuer pendant la compression de la sonde. La bourse présente des parois épaissies (pointes de flèches) et des cloisons (flèches). Dans ce cas, l'aspiration à l'aiguille du liquide de la bourse a révélé une solution de lait de calcium.
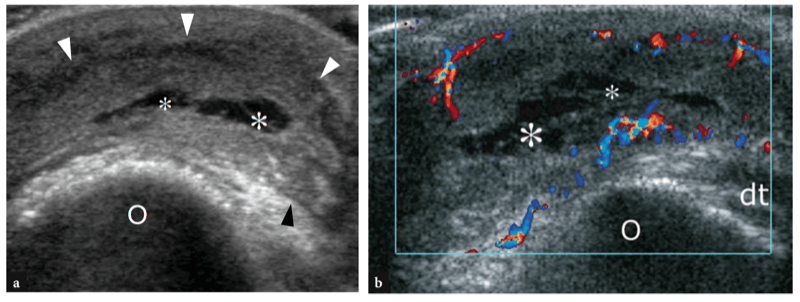
Figure 52a,b. Bursite olécrânienne tuberculeuse. a Images échographiques longitudinales en échelle de gris et b couleur Doppler 12−5 MHz chez un patient présentant un gonflement douloureux des tissus mous sur la partie postérieure du coude. La bourse olécrânienne (têtes de flèches) présente un épaississement irrégulier de la paroi et des marges mal définies en raison d'une cellulite péribursale coexistante. Seule une petite quantité de liquide intrabursal est visible (astérisques). dt, tendon du triceps distal ; O, olécrâne.
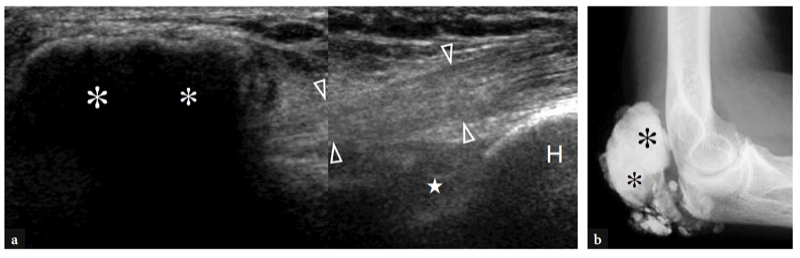
Figure 53a,b. Bursite olécranienne calcifiante chez un patient atteint d'ostéodystrophie rénale. a Image échographique médiane postérieure sagittale 12−5 MHz avec b corrélation radiographique latérale montre une grande calcification (astérisques) qui se trouve superficielle à l'insertion du tendon distal du triceps (têtes de flèches) reflétant une bourse largement calcifiée. Notez la relation de la masse avec la fosse olécrânienne postérieure (étoile) et la diaphyse humérale (H).
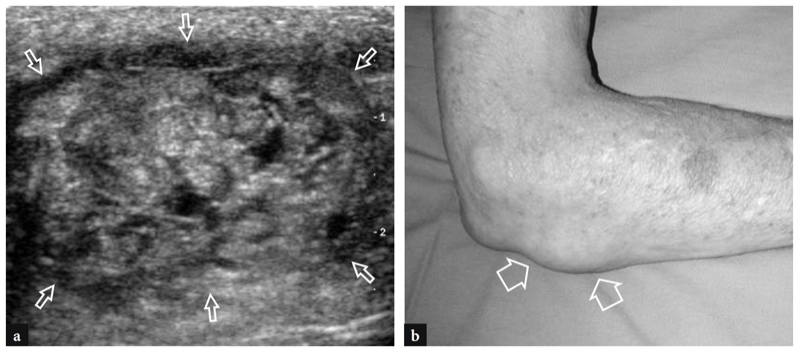
Figure 54a,b. Nodule de bursite sous-olécrânienne chez un patient atteint de polyarthrite rhumatoïde sévère. une image US transversale 12−5 MHz révèle une masse hétérogène indolore des tissus mous (flèches) avec une échotexture mixte située dans le tissu sous-cutané au-dessus de l'ulna postérieur proximal, compatible avec une bursite sous-olécrânienne. b Photographie du même cas illustré en a.
37. SYNDROME DU TUNNEL CUBITAL
La compression du nerf cubital à l'intérieur du tunnel cubital, deuxième syndrome de compression du membre supérieur après le syndrome du canal carpien, peut survenir soit au niveau de la gouttière condylienne, soit au bord du ligament arqué (tunnel cubital proprement dit). Il existe plusieurs causes de lésions du nerf cubital, y compris la compression extrinsèque directe du nerf contre une rainure condylienne peu profonde, des anomalies osseuses (cubitus valgus, déformations de fractures antérieures du coude, arthrose avec ostéophytes médiaux et corps lâches, ossification hétérotopique) et une variété d'espace - occupant des lésions des tissus mous, y compris un épaississement de la capsule et du ligament collatéral médial, des ganglions et des muscles accessoires (muscle anconeus epitrochlearis) (Stewart 1993). Cliniquement, le piégeage du nerf cubital au niveau du coude se manifeste insidieusement par une douleur médiale du coude et un éventail de plaintes allant des symptômes sensoriels de l'annulaire et de l'auriculaire à la faiblesse des muscles innervés ulnaires de la main. L'atrophie des muscles de la main est mieux appréciée au niveau du premier espace interosseux et de l'éminence hypothénar et provoque une déformation typique en semi-flexion de l'annulaire et des petits doigts communément appelée «main en griffe» (Fig. 55). De plus, le petit doigt peut rester légèrement en abduction (signe de Wartenberg).
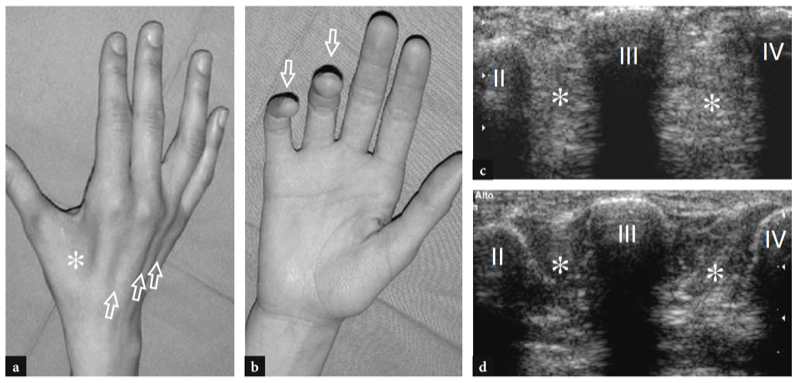
Figures 55a–d. Difformité en griffe de la main droite d'un jeune patient atteint de neuropathie ulnaire sévère au niveau du tunnel cubital. a Une photographie de la face dorsale de la main révèle une perte en masse des muscles interosseux dorsaux (flèches) situés dans les espaces intermétacarpiens. L'atrophie des muscles de la main à innervation ulnaire est plus évidente au niveau du premier espace intermétacarpien (astérisque). b La photographie de la face palmaire de la main montre les quatrième et cinquième doigts étendus au niveau de l'articulation métacarpo-phalangienne et fléchis au niveau des articulations interphalangiennes. c L'image US transversale 12−5 MHz sur la face dorsale de la main montre un aspect hyperéchogène des muscles interosseux dorsaux (astérisques) lié à une atrophie graisseuse neurogène. d Côté sain controlatéral. II–III–IV, métacarpiens.
Le diagnostic repose essentiellement sur des études électrophysiologiques. L'échographie démontre généralement un rétrécissement brutal et un déplacement du nerf dans le tunnel, éventuellement en association avec un rétinaculum épaissi ou une lésion encombrante (Fig. 56) (Puig et al. 1999 ; Martinoli et al. 2000 ; Okamoto et al. 2000). À sa proximité, le nerf comprimé apparaît gonflé avec perte du schéma fasciculaire et, dans certains cas, hypervascularisation à l'imagerie Doppler couleur. Comme évalué par analyse quantitative avec échographie, la section transversale du nerf au niveau de l'épicondyle est significativement plus grande chez les patients atteints du syndrome du tunnel cubital que chez les sujets sains ou dans le coude normal opposé (Okamoto et al. 2000 ; Chiou et al. 1998). Une zone du nerf cubital ≥7.5 mm2 au niveau de l'épicondyle a été indiquée comme valeur seuil pour le syndrome du tunnel cubital (Chiou et al. 1998). Ces données sont quelque peu contradictoires avec un article plus récent qui indique 7.9 mm2 comme surface de section transversale moyenne pour le nerf cubital normal au niveau du coude (Jacob et al. 2004). Outre l'évaluation du nerf cubital, un large éventail de causes extrinsèques de compression nerveuse peuvent également être reconnues par l'échographie, y compris des anomalies congénitales telles qu'un muscle anconé épitrochléaire accessoire (Fig. 57), et une maladie acquise qui à son tour entraîne une augmentation du contenu, c'est-à-dire un lipome (Fig. 58) – ou une taille réduite – c'est-à-dire des résidus de fracture (Fig. 59)–du tunnel.
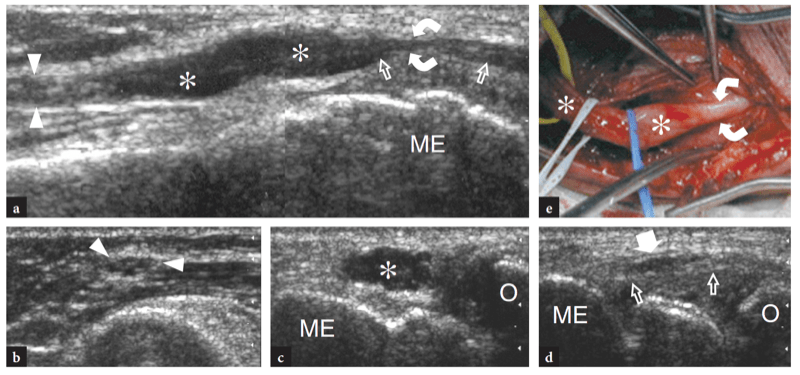
Figures 56a–e. Syndrome du tunnel cubital. une image américaine à axe long 12−5 MHz du tunnel cubital chez un patient atteint de cubitus valgus montre le nerf ulnaire (têtes de flèches), qui apparaît de plus en plus enflé et hypoéchogène avec un motif fasciculaire absent (astérisques) à mesure qu'il progresse vers le point de compression (courbe La Flèche). Observez le plancher surélevé du tunnel par rapport à l'épaississement de la capsule médiale et du complexe ligamentaire médial (flèches). b–d Les images échographiques transversales 12−5 MHz montrent b un nerf cubital d'apparence normale (têtes de flèches) au niveau du bras distal, c un nerf gonflé et hypoéchogène (astérisques), juste en amont du tunnel, et d un rétrécissement abrupt dans la coupe transversale zone du nerf cubital (flèche blanche) sous le rétinaculum d'Osborne et superficielle au plancher épaissi (flèches vides) du tunnel. ME, épicondyle médial ; O, olécrâne. e Vue macroopératoire du même cas.
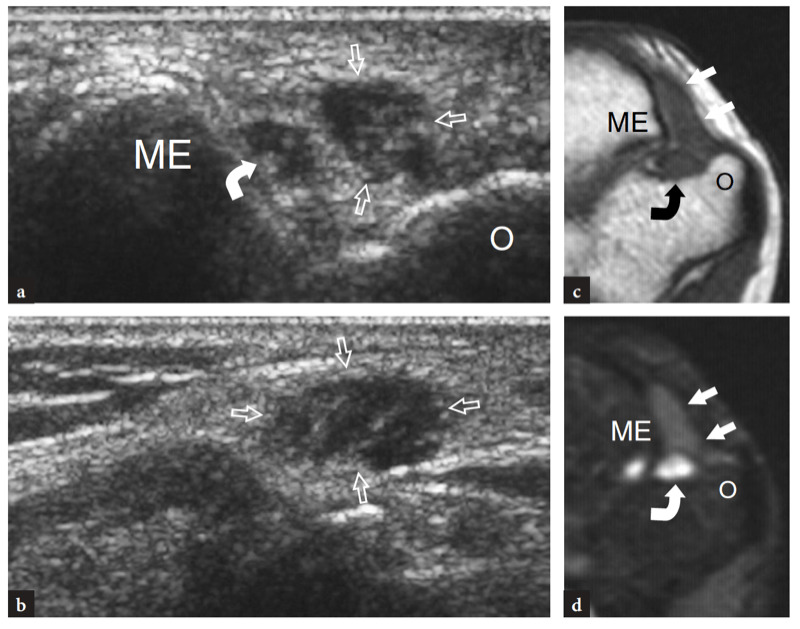
Figures 57a–d. Syndrome du tunnel cubital chez un patient présentant un muscle épitrochléaire anconé. a Les images US petit axe et b grand axe 12−5 MHz du tunnel cubital révèlent le muscle épitrochléaire anconé (flèches droites) qui se situe entre l'épicondyle médial (ME) et l'olécrâne (O) en relation étroite avec un ulnaire enflé nerf (flèche courbe). Les images IRM transversales corrélatives c T1w SE et d T2w SE avec suppression de la graisse montrent le muscle aberrant (flèches droites) dans le tunnel cubital. En d, le nerf cubital (flèche courbe) apparaît nettement en hypersignal à la suite d'une neuropathie compressive. ME, épicondyle médial ; O, olécrâne.
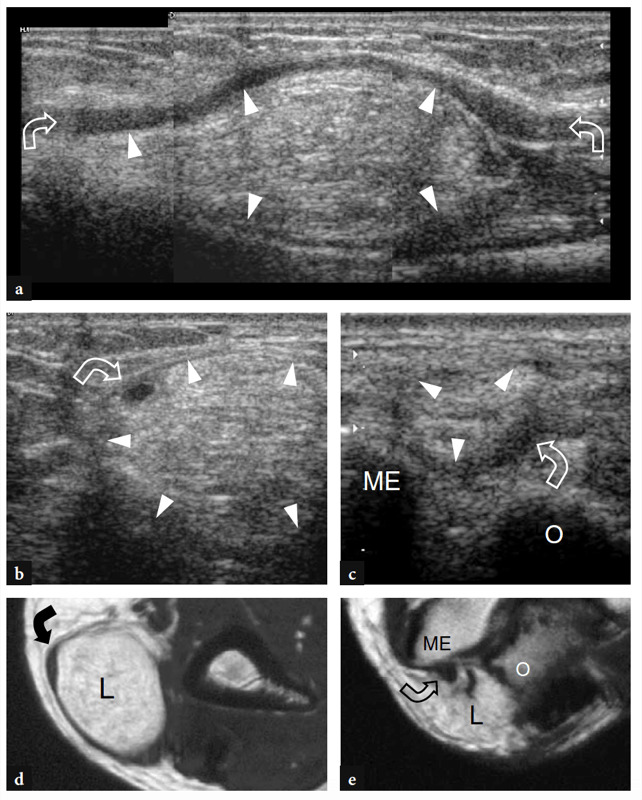
Figures 58a–e. Syndrome du tunnel cubital chez un patient présentant une masse superficielle des tissus mous sur le coude postéro-médial. a Les images américaines longitudinales et b transversales reconstruites à 12−5 MHz obtenues juste à proximité du tunnel cubital montrent le nerf cubital (flèche incurvée) qui montre une courbure sur une lésion hyperéchogène solide ovale (têtes de flèches) avec des marges bien définies, compatibles avec un lipome. Notez la relation étroite de la masse avec le nerf. c L'image US transversale 12−5 MHz obtenue au niveau du tunnel cubital montre le lipome (têtes de flèches) qui se replie dans le tunnel conduisant à la compression du nerf ulnaire (flèche courbe). ME, épicondyle médial ; O, olécrâne. d,e Les images IRM transversales T1w SE corrélatives obtenues d au niveau du bras distal et e au niveau du tunnel cubital confirment le caractère lipomateux de la lésion volumineuse (L). Flèche courbe, nerf cubital ; ME, épicondyle médial ; O, olécrâne.
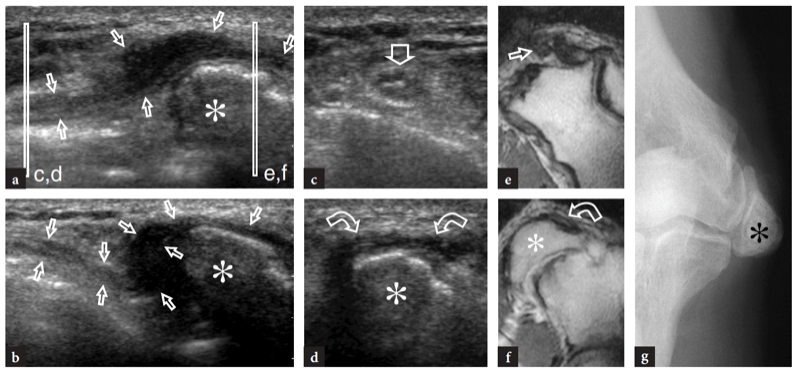
Fig. 59a–g. Syndrome du tunnel cubital chez un patient présentant des symptômes récents liés à une neuropathie ulnaire droite ayant subi une fracture de l'épicondyle médial à l'adolescence. a,b Images échographiques longitudinales 12−5 MHz du tunnel cubital obtenues a en flexion et b en extension complète du coude. a Avec la flexion du coude, un os anormal (astérisque) peut être apprécié comme une image hyperéchogène renflée dans le tunnel et déplaçant un nerf cubital gonflé et hypoéchogène (flèches). b Avec l'extension du coude, le nerf (flèches) forme une boucle anormale crânienne à l'os anormal (astérisque) et apparaît aplati et comprimé contre sa face superficielle. c,d Les images US transversales 12−5 MHz avec corrélation d'imagerie e,f T1w SE IRM obtenues c, e au niveau du bras distal et d, f au niveau de l'épicondyle médial avec le coude en extension révèlent un nerf d'apparence normale (flèche droite ) crânien au point de compression et un nerf hypoéchogène aplati (flèches courbes) sur l'os anormal (astérisque). g La radiographie simple montre une fracture ancienne de l'épicondyle médial (astérisque) avec le fragment déplacé vers l'interligne articulaire.
La décompression chirurgicale du nerf cubital au niveau du coude peut inclure l'incision du fascia d'Osborne et de l'aponévrose du fléchisseur ulnaire du carpe en laissant le nerf à l'intérieur du tunnel cubital. Alternativement, le nerf peut être transposé hors du sillon condylien et du tunnel cubital, en avant de l'épicondyle médial et en surface des muscles fléchisseurs (Fig. 60). Cette option chirurgicale est privilégiée en cas de neuropathies ulnaires causées par des maladies osseuses et articulaires. Après transposition chirurgicale, les symptômes persistants sont généralement liés à une angulation excessive du nerf cubital lors de son passage en profondeur du ligament arqué ou à une stabilisation incomplète du nerf dans sa nouvelle position. L'échographie est capable d'identifier le tissu cicatriciel le long du trajet du nerf chez les patients présentant des symptômes récurrents ou une rechute de causes compressives (Fig. 61).
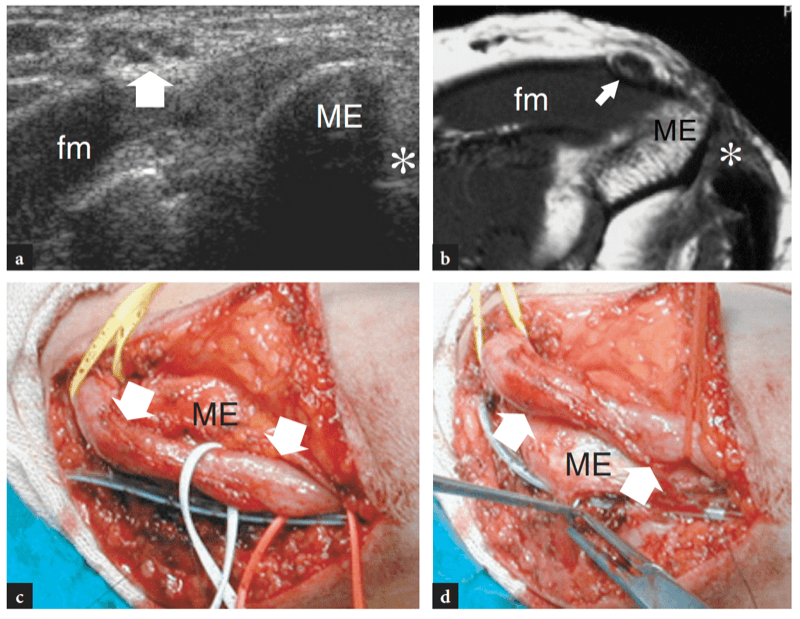
Figures 60a–d. Nerf cubital postopératoire. a Image US transversale 12−5 MHz sur le coude médial avec corrélation d'imagerie b T1w SE MR montre une transposition antérieure du nerf ulnaire (flèche) par rapport à l'épicondyle médial (ME). Le nerf est sous-cutané et repose sur les muscles fléchisseurs (fm). Notez le sillon condylien vide (astérisque). c,d Vues opératoires macroscopiques obtenues c avant et d après transposition antérieure du nerf cubital (flèches) par rapport à l'épicondyle médial (ME).
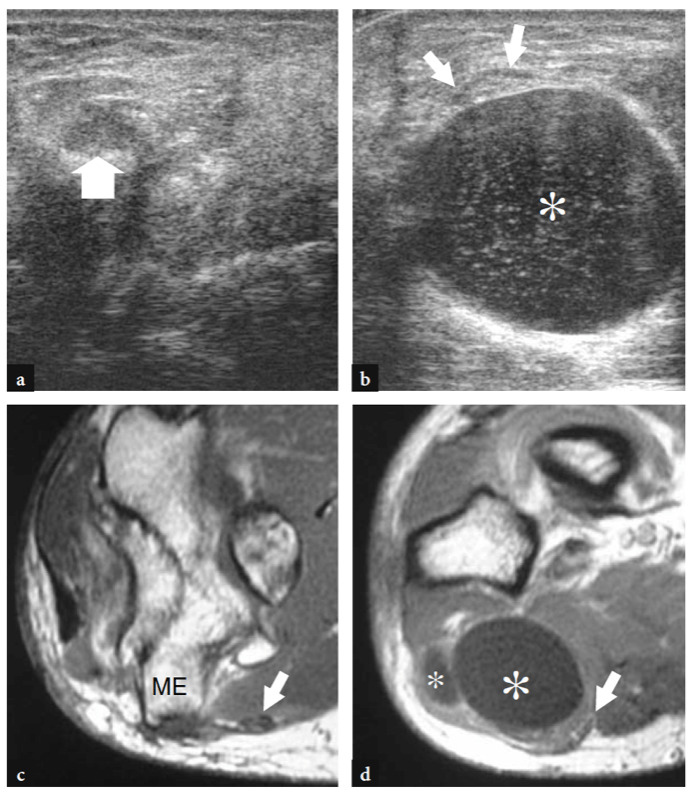
Fig. 61a–d. Patient postopératoire avec récidive des symptômes après chirurgie décompressive du nerf cubital au niveau du tunnel cubital pour un kyste ganglionnaire. a,b Les images US transversales 12−5 MHz obtenues a au niveau du tunnel cubital et b au niveau de l'avant-bras proximal avec corrélation d'imagerie c,d T1w SE MR montrent un kyste récidivant (astérisques) qui contracte le nerf ulnaire transposé (flèche). Le patient a de nouveau été opéré et l'évolution postopératoire s'est finalement déroulée sans incident. ME, épicondyle médial.
38. INSTABILITÉ DU NERF ULNAIRE
En cas d'absence congénitale partielle ou totale du rétinaculum du tunnel cubital, le nerf ulnaire peut subluxer au-dessus de la pointe de l'épicondyle ou se disloquer en avant de celui-ci avec une sensation de claquement transitoire lors de la flexion du coude, pour revenir à l'intérieur du tunnel lorsque l'articulation est en extension . L'instabilité du nerf cubital au niveau du tunnel cubital peut être considérée comme une variante normale, rapportée chez 16 % à 47 % des personnes en bonne santé asymptomatiques, la subluxation étant la forme la plus courante (Childress 1975 ; Okamoto et al. 2000). La condition est bilatérale dans près des trois quarts des cas et asymptomatique à la fois à l'examen clinique et aux études de conduction nerveuse. Les patients peuvent parfois se plaindre d'un léger inconfort avec des picotements et des paresthésies lorsque le coude fléchi heurte une surface ferme telle que le bord d'un bureau. Dans de rares cas, cependant, un microtraumatisme chronique du nerf sur l'épicondyle médial dû à une luxation répétitive peut provoquer une névrite de friction avec des symptômes et des signes d'atteinte du nerf ulnaire. Dans de tels cas, l'instabilité nerveuse doit être traitée par transposition chirurgicale du nerf afin d'éviter des lésions plus graves.
l'instabilité du nerf ulnaire lors de la flexion progressive du coude, pour reconnaître les anomalies nerveuses liées à la névrite de friction ainsi que pour établir si la neuropathie ulnaire est produite par des causes compressives ou une instabilité en raison du chevauchement des résultats cliniques (Jacobson et van Holsbeeck 1998 ; Jacobson et al. 2001). En subluxation, le nerf se déplace au-dessus de l'apex de l'épicondyle médial pendant la flexion active complète du coude, mais pas plus loin. En cas de luxation, le nerf peut être vu sortir complètement du tunnel cubital et migrer vers l'origine du tendon fléchisseur commun (Fig. 62). Pendant le balayage dynamique, la sensation de claquement peut être ressentie par l'examinateur à travers le transducteur. Une technique de numérisation minutieuse est nécessaire pour éviter une pression excessive avec la sonde sur l'épicondyle, ce qui peut empêcher le nerf de se disloquer. En cas de névrite de friction symptomatique, le nerf cubital apparaît nettement gonflé et hypoéchogène avec perte de l'échotexture fasciculaire, reflétant probablement un œdème intraneural localisé et des modifications fibrotiques (Fig. 63). Cependant, ces anomalies peuvent également être rencontrées occasionnellement chez des sujets sains, sans aucune implication de maladie.
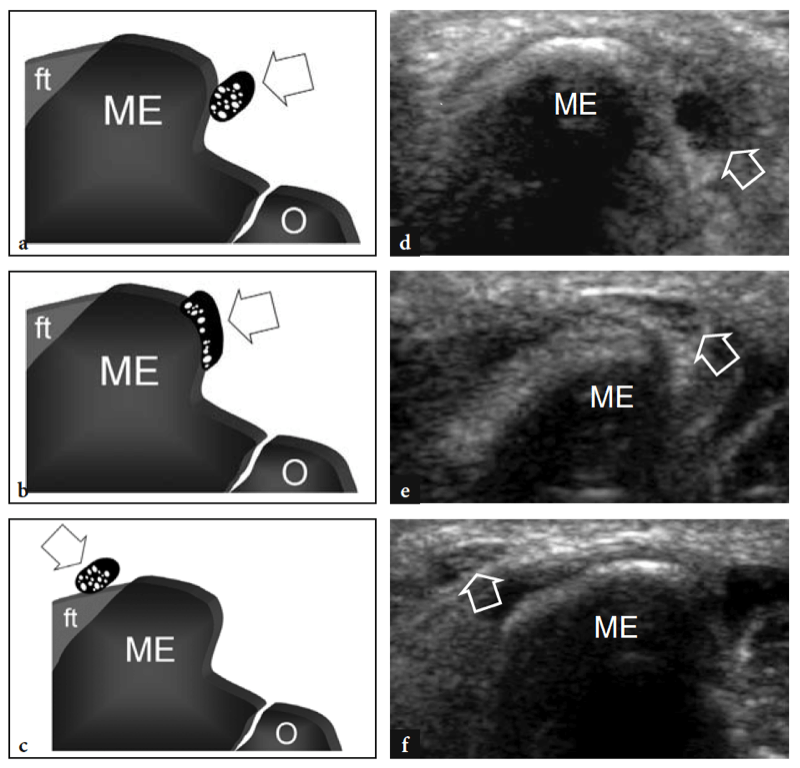
Fig. 62a–f. Etude dynamique du tunnel cubital dans la luxation du nerf ulnaire. a–c Dessins schématiques et d–f séries respectives d'images échographiques transversales 12−5 MHz obtenues a,d coude en extension et pendant les degrés progressifs de flexion du coude (b,e et c,f). Lorsque le coude est en extension, le nerf cubital (flèche) est contenu dans le tunnel. La flexion du coude pousse progressivement le nerf sur l'épicondyle médial (ME) jusqu'à ce qu'il sorte complètement du tunnel cubital pour se trouver superficiel par rapport à l'origine du tendon fléchisseur commun (ft). O, olécrâne.
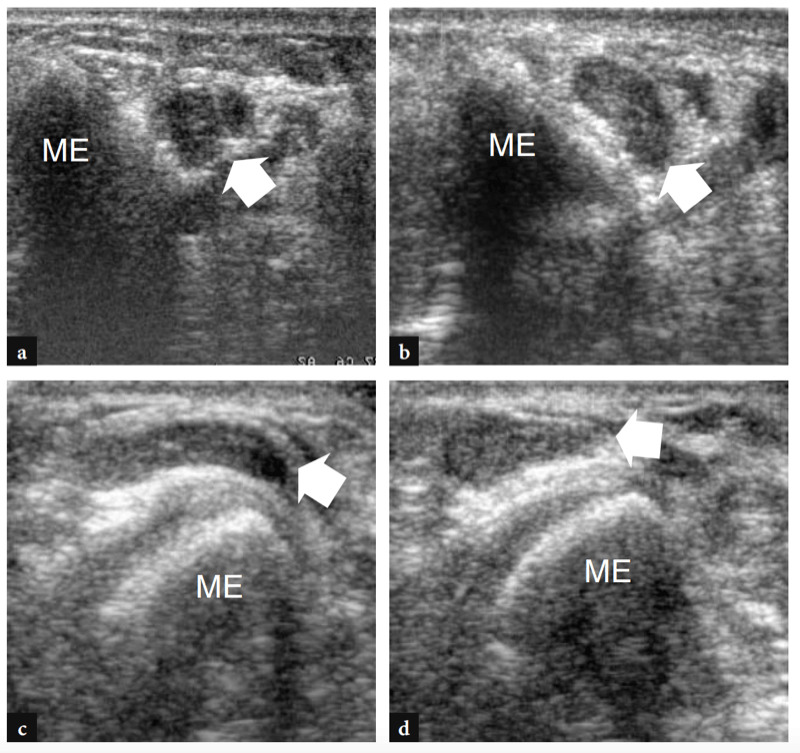
Figures 63a–d. Étude dynamique du tunnel cubital chez un patient présentant une luxation récurrente du nerf ulnaire et des symptômes cliniques de neuropathie ulnaire. a–d Une série d'images US transversales 13−8 MHz acquises a avec le coude étendu et b–d tout au long de la flexion du coude montre un nerf nettement enflé et hypoéchogène (flèche) qui s'aplatit et se disloque sur l'épicondyle médial (EM) pendant la flexion du coude. Chez le patient symptomatique, cette découverte est évocatrice d'une neuropathie ulnaire basée sur un mécanisme de friction.
39. SYNDROME DU TRICEPS CROQUANT
Avec la flexion du coude, une luxation antérieure du chef médial du muscle triceps par rapport à l'épicondyle médial peut se produire en combinaison avec une luxation du nerf cubital. Dans cette condition, appelée «syndrome du triceps cassant», la luxation du muscle entraîne une luxation concomitante du nerf cubital adjacent car ces structures sont contiguës (Fig. 64). Deux "claquements" palpables sont généralement appréciés sur le coude médial, le premier reflétant la luxation du nerf cubital et le second, la luxation de la tête médiale du muscle triceps. La présentation clinique de ce syndrome est variable et peut inclure une douleur médiale du coude, une sensation de claquement, une neuropathie ulnaire ou une combinaison de ces symptômes (Spinner et Goldner 1998). Un peu similaire à la luxation isolée du nerf cubital, le triceps claquant peut cependant rester asymptomatique et probablement méconnu dans la plupart des cas. Bien que la cause du claquement du triceps soit encore inconnue, certaines conditions congénitales et acquises possibles ont été préconisées pour expliquer ce syndrome, comme un muscle triceps hypertrophié, un tendon accessoire du triceps et une anomalie de la tête médiale du muscle triceps, ainsi que des troubles post-traumatiques. anomalies osseuses. La différenciation entre le syndrome de claquement du triceps et la luxation isolée du nerf ulnaire comme causes de claquement médial du coude est importante chez les sujets symptomatiques car les traitements chirurgicaux diffèrent. À cette fin, l'échographie dynamique est précise en permettant une visualisation directe de la luxation transitoire des deux structures lors de la flexion et de l'extension actives du coude (Fig. 65) (Jacobson et al. 2001).
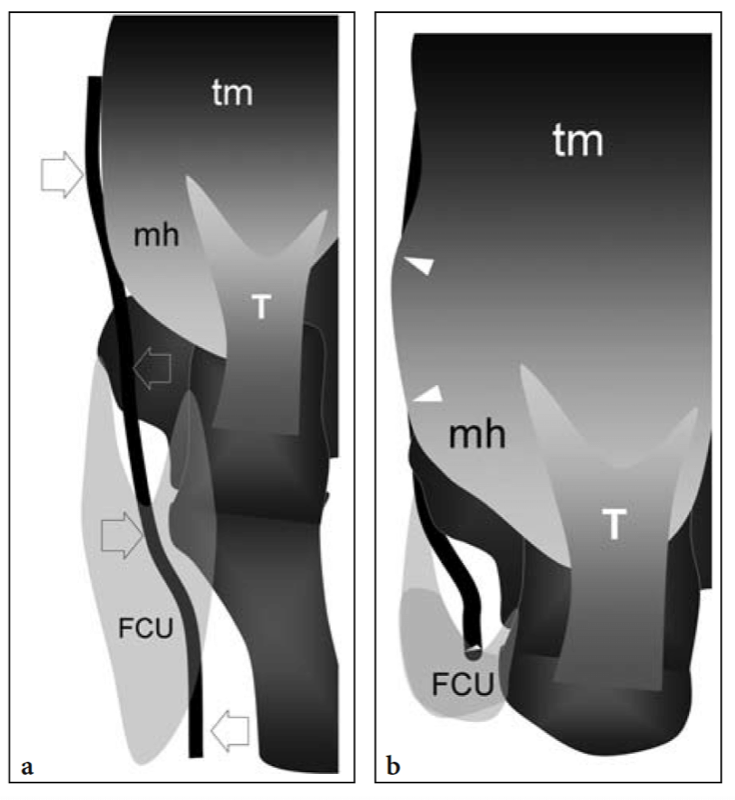
Figure 64a,b. Le syndrome du triceps qui claque. Des dessins schématiques de la face postérieure du coude en extension et b flexion à 90° montrent le nerf cubital (flèches) lors de son passage dans le tunnel cubital et une tête médiale proéminente (mh) du muscle triceps ™. Notez l'absence du rétinaculum d'Osborne par rapport à la Fig. 7c. Avec la flexion du coude, le bord médial du triceps (têtes de flèches) et le nerf cubital se déplacent en avant de la pointe de l'épicondyle. T, tendon distal du triceps ; fcu, fléchisseur ulnaire du carpe.
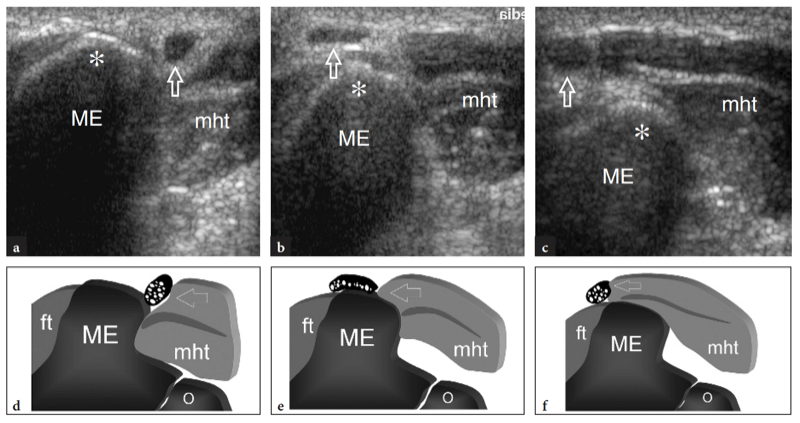
Figures 65a–f. Etude dynamique du tunnel cubital dans le syndrome du triceps cassant. a–c Série d'images US transversales 12−5 MHz avec schémas corrélatifs d–f obtenus (a,d) avec le coude en extension et (b,e et c,f) tout au long de la flexion du coude. Avec le coude étendu, le nerf cubital (flèche) et le chef médial du muscle triceps (mht) sont contenus dans le tunnel cubital. Au cours des degrés progressifs de flexion du coude, le triceps pousse le nerf cubital sur la pointe (astérisque) de l'épicondyle médial (ME) jusqu'à ce qu'il sorte du tunnel. Ensuite, les triceps se détachent aussi. ft, origine du tendon fléchisseur commun ; O, olécrâne.
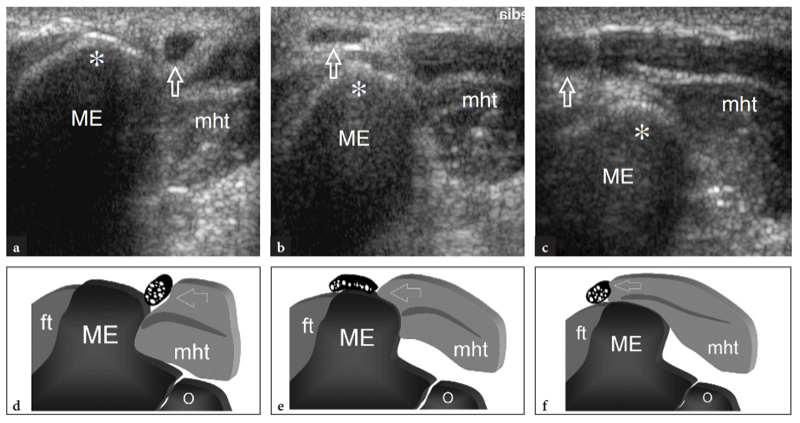
Figure 66a,b. Épanchement articulaire du coude. un dessin schématique d'une vue sagittale médiane à travers un coude étendu montre du liquide dans les parties antérieure (1) et postérieure (2) de l'articulation. Au plus profond des muscles brachial (br) et triceps (tr), les coussinets adipeux antérieur (astérisque) et postérieur (étoile) sont surélevés par le liquide intra-articulaire. b Une radiographie latérale chez un patient présentant un épanchement articulaire abondant révèle une élévation des coussinets adipeux antérieurs (astérisque) et postérieurs (étoile) de la surface de l'humérus, conduisant à un « signe de coussinet adipeux positif » et à une densité accrue (flèches) au niveau de l'humérus. niveau des récessus antérieur et postérieur, traduisant une synovite.
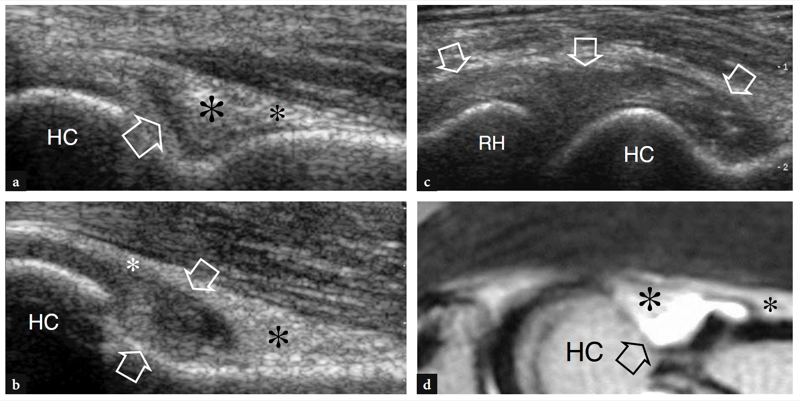
Figures 67a–d. Synovite de l'articulation du coude : évidement articulaire antérieur. Images échographiques longitudinales 12−5 MHz sur le récessus coronoïdien antérieur a à l'état normal et b,c dans deux cas de synovite articulaire présentant une distension b légère et c marquée des espaces synoviaux antérieurs par une synoviale fluide et hypertrophiée. Dans des conditions normales, une fine couche de liquide (flèche) peut être rencontrée dans le récessus coronoïde antérieur, en profondeur jusqu'au coussinet adipeux antérieur (astérisques). C'est un constat normal. Lorsque le liquide articulaire se dilate dans les espaces articulaires antérieurs, le coussinet adipeux antérieur (astérisques) s'élève pour prendre une apparence typique en forme de croissant ou de "voile". Dans les articulations nettement distendues, le renflement antérieur de la cavité articulaire est plus visible et peut s'étendre jusqu'au niveau de l'articulation. HC, capitellum huméral ; RH, tête radiale. d Image MR T2w SE correspondante du cas illustré en b.
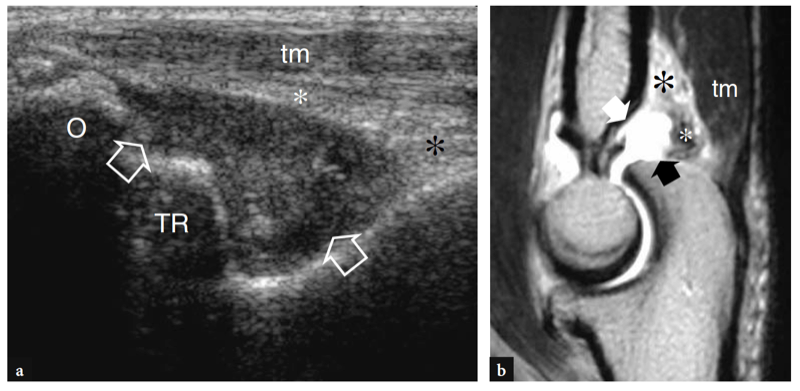
Figure 68a,b. Synovite de l'articulation du coude : récessus articulaire postérieur. a Image échographique longitudinale 12−5 MHz sur le récessus olécrânien postérieur avec corrélation d'imagerie IRM b T2w SE chez un patient atteint de polyarthrite rhumatoïde présentant un coude douloureux et une perte d'extension. L'échographie montre une masse de pannus synovial hypoéchogène remplissant l'évidement (flèches). Au plus profond du muscle triceps ™, le coussinet adipeux postérieur (astérisques) est surélevé par le pannus. Notez la proéminence de la pointe de l'olécrâne (O) et de la trochlée humérale (TR) renflée dans l'évidement.
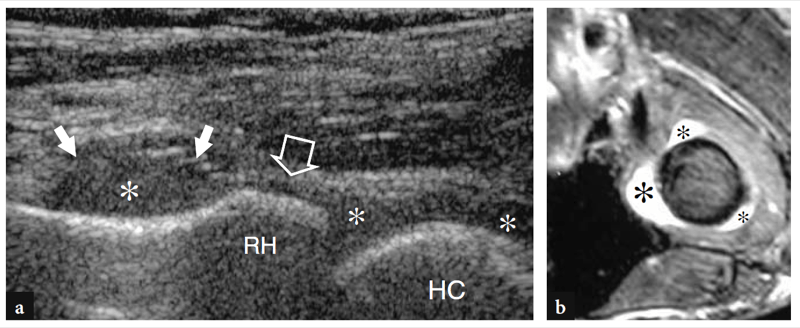
Figure 69a,b. Synovite de l'articulation du coude : évidement annulaire (périradial). a Image échographique longitudinale 12−5 MHz sur la face antérieure de l'articulation radio-capitellar avec b corrélation d'imagerie IRM transversale T2w SE chez un patient atteint de polyarthrite rhumatoïde révèle le remplissage de l'évidement annulaire (flèches blanches) par du liquide synovial hypoéchogène (astérisques). L'évidement annulaire se situe autour de la métaphyse radiale et communique avec la cavité articulaire par un mince passage (flèche ouverte) profond jusqu'au ligament annulaire. Notez le profil arrondi du capitellum huméral (HC) et le profil carré de la tête radiale (RH).
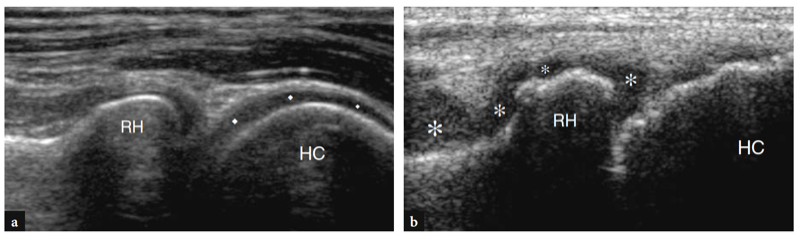
Figure 70a,b. La polyarthrite rhumatoïde. a,b Images échographiques longitudinales 12−5 MHz sur la face antérieure de l'articulation radio-capitellaire a chez un sujet normal et b chez un patient atteint de polyarthrite rhumatoïde sévère de longue date. En a, notez le cartilage articulaire (losanges) et le profil régulier de l'os sous-chondral du capitellum huméral (HC) et de la tête radiale (RH). En b, il y a perte complète de la couche cartilagineuse et la surface des os apparaît irrégulièrement diffuse, reflétant les érosions. Le pannus synovial (astérisques) peut être vu dans l'espace articulaire et distendre l'évidement annulaire.
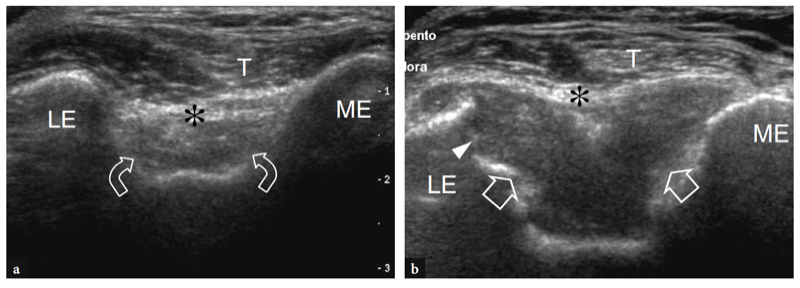
Figure 71a,b. Synovite de l'articulation du coude : écueil. a,b Images échographiques transversales 12−5 MHz sur le récessus olécrânien postérieur a chez un sujet normal et b chez un patient atteint de polyarthrite rhumatoïde et un récessus olécrânien (flèches) apparaît nettement distendu par le liquide. En a, la graisse hypoéchogène normale contenue. En b, la fosse olécrânienne, entre les épicondyles latéral (LE) et médial (ME), ne doit pas être confondue avec le processus de synovite illustré en b. Dans les cas douteux, un examen dynamique soigneux avec des mouvements de flexion et d'extension du coude peut être utile pour le diagnostic. Notez l'érosion (tête de flèche) sur la face postéro-médiale de l'épicondyle latéral. T, tendon distal du triceps.
41. ARTHROSE ET DOMMAGES OSTEOCHONDRAUX
L'arthrose du coude est essentiellement de nature post-traumatique. Il est généralement observé chez les patients de sexe masculin ayant des antécédents de travail manuel (outils de vibration), de surutilisation liée au sport ou de désalignement de fracture. Le membre dominant est plus fréquemment atteint. Compte tenu de l'attitude physiologique de l'articulation du coude en valgus, le compartiment radio-capitellar externe est le plus souvent atteint. Les signes cliniques sont liés au processus dégénératif lui-même (raideur et perte de mouvement, généralement en extension, liées à l'éperon, gonflement dû à la synovite, douleur locale), à la compression du nerf cubital à l'intérieur du tunnel cubital (douleur et sensibilité locales, fourmillements des annulaire et auriculaire et, en compression chronique, atrophie des muscles intrinsèques de la main ulnaire-innervés) ainsi que des corps lâches intra-articulaires (blocage articulaire intermittent et épanchement).
Les corps lâches intra-articulaires migrent généralement dans les parties dépendantes de l'articulation et dans les dépressions humérales au-dessus de la ligne articulaire, en particulier la fosse olécrânienne, entraînant des symptômes mécaniques tels qu'un blocage intermittent et une perte d'extension. Chez les patients sans épanchement synovial, la localisation intra-articulaire d'un fragment peut être établie en le mettant en évidence entre le cartilage articulaire et les coussinets adipeux intracapsulaires antérieur et postérieur. Le petit évidement annulaire radial est rarement impliqué par des corps étrangers. L'examen dynamique effectué pendant la flexion et l'extension du coude peut être utile pour mobiliser le liquide articulaire et les petits corps lâches ainsi que pour les différencier de l'ossification hétérotopique locale et de l'éperon (Fig. 72) (Bianchi et Martinoli 2000). Dans la chondromatose synoviale primaire, plusieurs corps lâches chondraux ou ostéochondraux présentent généralement une taille presque égale et peuvent varier en nombre de quelques à des centaines (Fig. 73). Une maladie avancée peut entraîner une désintégration des surfaces articulaires. Comme déjà décrit dans d'autres sites anatomiques, dans la phase initiale de la maladie, le traitement comprend l'ablation des corps étrangers et une synovectomie pour prévenir les récidives. Semblable à un corps lâche, l'os supratrochleare dorsale est un osselet intra-articulaire situé dans la fosse olécrânienne qui peut être associé à des douleurs et à une perte progressive de l'extension du coude avec des symptômes de blocage (Obermann et Loose 1983). On pense généralement que cet osselet accessoire est le résultat d'une anomalie congénitale plutôt que la conséquence d'un traumatisme antérieur et peut provoquer un approfondissement et un remodelage de la fosse olécrânienne à mesure qu'elle augmente en taille. La différenciation entre un os supratrochleare dorsale et un corps libre n'est cliniquement pas pertinente car les deux fragments sont traités par ablation chirurgicale.
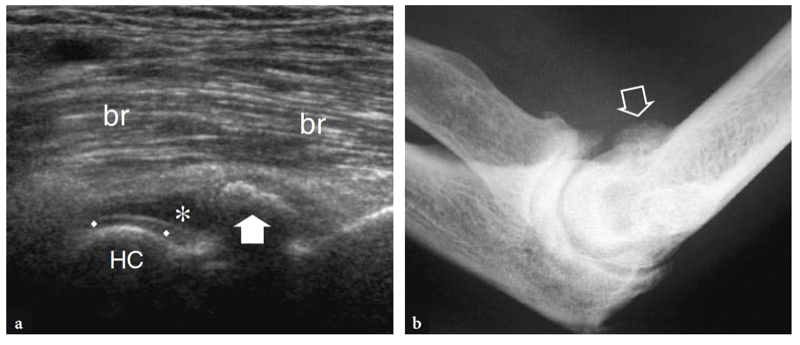
Figure 72a,b. Éperon antérieur imitant un corps lâche. une image longitudinale 12−5 MHz US avec b corrélation radiographique latérale montre un éperon proéminent (flèche) au-dessus de la fosse coronoïde de l'humérus. L'éperon est intracapsulaire et apparaît bordé de liquide (astérisque). Pendant les mouvements du coude, il est resté immobile. Notez la fine couche hypoéchogène de cartilage articulaire (losanges) qui recouvre le capitellum huméral (HC). Br, muscle brachial.
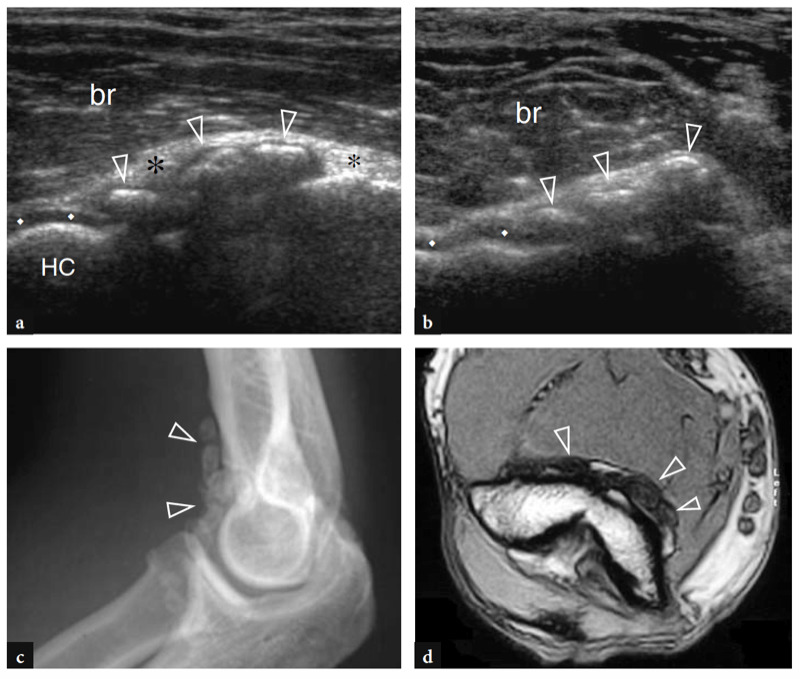
Figure 73a−d. Chondromatose synoviale primitive. a Les images américaines longitudinales et b transversales à 12−5 MHz sur l'évidement coronoïde antérieur montrent de multiples corps lâches intra-articulaires sous forme de fragments hyperéchogènes (têtes de flèches) de taille similaire avec une ombre acoustique postérieure située à l'intérieur de l'évidement. Notez l'élévation du coussinet adipeux antérieur (astérisques) sur les fragments et la fine couche hypoéchogène de cartilage articulaire (losanges) qui recouvre le capitellum huméral (HC). br, muscle brachial. c Radiographie latérale et d Imagerie transversale T1w GRE IRM du même cas montrant les corps étrangers (têtes de flèches).
Chez les adolescents, l'échographie est également capable de reconnaître les déformations du capitellum huméral dans l'ostéochondrite disséquante (Takahara et al. 1998, 2000a,b). Cette condition survient généralement chez les 13 à 16 ans, principalement à la suite d'une impaction latérale chronique ou d'un stress répétitif en valgus. La surface articulaire antérolatérale du capitellum est généralement impliquée dans l'aplatissement localisé de l'os sous-chondral et la fragmentation et le relâchement ultérieurs des fragments osseux (Takahara et al. 2000a). L'examen échographique est mieux réalisé avec une approche antérieure tout en gardant le coude étendu (pour voir les parties proximale et médiane du capitellum antérieur) et avec une approche postérieure tout en gardant le coude fléchi (pour voir les parties médiane et distale du capitellum antérieur) (Takahara et al. 2000b). Des fragments osseux détachés sont représentés comme des foyers échogènes dans le défaut ostéochondral. L'échographie s'est également avérée précise pour déterminer si la lésion est stable ou instable (fragments desserrés), avec un bon (89 %) accord avec les résultats chirurgicaux et l'IRM (Takahara et al. 2000b). Chez ces patients, un retard dans la prise en charge appropriée peut être évité par un examen échographique précoce. Des anomalies similaires peuvent être rencontrées dans la maladie de Panner, une affection liée à la nécrose avasculaire du centre d'ossification du capitellum qui survient chez les enfants de 5 à 11 ans suite à des blessures traumatiques. Assez comparable à la maladie de Legg-Calvé-Perthes de la hanche, cette dernière affection a une évolution bénigne sans déformation résiduelle du capitellum et absence de formation de corps lâche (Vanderschueren et al. 1998).
42. FRACTURES OCCULTES
En raison de la complexité anatomique de l'articulation du coude, certaines fractures non déplacées, telles que celles impliquant la tête et le cou radiaux et le processus coronoïde, peuvent rester occultes radiographiquement, même lorsque des projections supplémentaires sont effectuées. Lorsque l'immobilisation plâtrée n'est pas utilisée comme mesure prophylactique pour éviter le surtraitement, la douleur persistante et l'invalidité peuvent amener le médecin traitant à acquérir un examen américain pour exclure toute éventuelle anomalie des tissus mous autour du coude. Grâce à une technique de numérisation minutieuse, l'échographie haute résolution est capable d'identifier les fractures aiguës du coude sur la base de la détection d'une déformation en escalier ou d'une discontinuité focale de la ligne corticale hyperéchogène (Fig. 74). Dans ces cas, cependant, des études radiographiques ou d'imagerie par résonance magnétique supplémentaires doivent toujours être obtenues pour confirmer le diagnostic américain. Un balayage dynamique lors d'une pronation et d'une supination passives assistées soigneuses de l'avant-bras avec la sonde placée dans le plan transversal au-dessus de la tête radiale peut être utile pour exclure toute fracture à ce niveau. Dans les cas douteux, des signes échographiques associés, tels qu'un épanchement articulaire, peuvent être facilement détectés dans les fractures intra-articulaires et peuvent suggérer une analyse plus détaillée du contour osseux (Major et Crawford 2002). D'autre part, l'absence d'épanchement dans les lésions du coude avec des radiographies simples négatives peut rendre inutile une exploration osseuse supplémentaire avec l'IRM (Kessler et al. 2002). Plus que chez l'adulte, l'échographie semble avoir un rôle potentiel dans l'évaluation des fractures du coude chez l'enfant. En fait, il est difficile d'évaluer les anomalies osseuses autour du coude chez les patients au squelette immature à l'aide de radiographies standard en raison de l'absence de centres secondaires d'ossification (Fig. 75). Lorsqu'un signe radiographique d'épanchement articulaire est présent mais qu'une fracture n'est pas visualisée, l'échographie peut aider à distinguer la séparation de l'épiphyse humérale distale (Dias et al. 1988 ; Ziv et al. 1996) de la luxation du coude chez les nouveau-nés, ainsi que dans la détection ou l'exclusion de la tête radiale (Lazar et al. 1998) et des fractures supracondyliennes (Davidson et al. 1994 ; Brown et Eustace 1997).
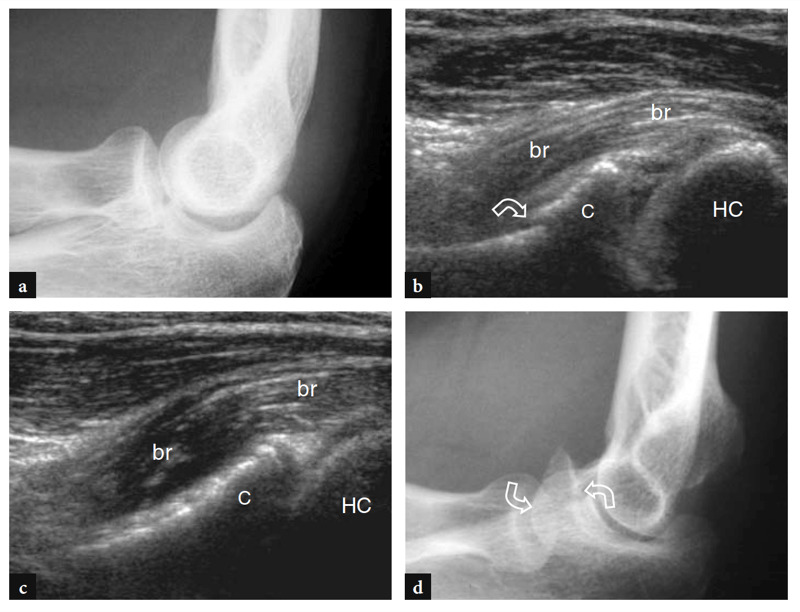
Figures 74a–d. Fracture occulte du processus coronoïde droit chez une femme suite à un accident de ski. a Le patient a eu un examen radiographique négatif effectué peu de temps après la blessure. b Deux semaines plus tard, elle a été soumise à un examen américain en raison d'une douleur persistante au coude et d'une perte d'extension. L'échographie a identifié une interruption (flèche courbe) du profil cortical hyperéchogène du processus coronoïde (C), juste crânien à l'insertion du brachial (br). Un léger épanchement intra-articulaire était associé. HC, capitellum huméral. c Côté sain gauche pour comparaison. d Une vue oblique supplémentaire du coude droit confirme la fracture.
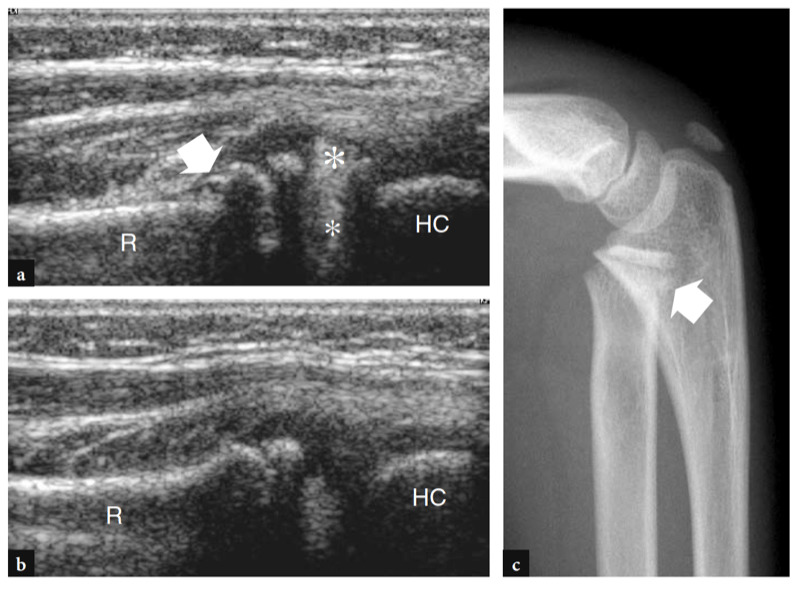
Figures 75a–c. Fracture radiale chez un enfant de 5 ans présentant des douleurs latérales du coude gauche et un handicap après une chute. une image longitudinale 12−5 MHz US au niveau du coude antérolatéral montre une distance accrue entre le capitellum huméral (HC) et l'épiphyse radiale liée à un épanchement articulaire hyperéchogène (astérisques). Notez le point hyperéchogène (têtes de flèches) dans l'épiphyse radiale représentant le centre d'ossification. Au niveau de la métaphyse radiale, l'échographie révèle une irrégularité focale de la ligne corticale hyperéchogène (flèche) évoquant une fracture. R, rayon. b Côté sain controlatéral pour comparaison. c La radiographie de profil du coude gauche confirme le diagnostic de fracture radiale (flèche).
43. BLESSURE DE LUXATION POSTÉRIEURE ET INSTABILITÉ
La luxation du coude est plus fréquente chez les enfants de moins de 10 ans et représente 5 à 8 % de toutes les fractures et luxations chez les adultes, juste derrière l'épaule. Habituellement, le cubitus et le radius se disloquent postérieurement suite à un mécanisme d'hyperextension, comme lors d'une chute sur la main tendue. La translation postérieure peut provoquer des fractures par impact (c.-à-d. processus coronoïde, capitellum huméral) et une variété de lésions des tissus mous, impliquant les articulations et les ligaments, les vaisseaux et les nerfs. Dans de tels cas, une échographie peut parfois être nécessaire pour démontrer des complications des tissus mous, telles qu'une ossification hétérotopique, une contusion du muscle brachial et des lésions de l'artère brachiale et des nerfs médian et ulnaire (Figues. 76, 77). Après une luxation, une instabilité de l'articulation du coude peut survenir suite à une rupture progressive du ligament collatéral ulnaire latéral (instabilité rotatoire postéro-latérale), une déchirure de la capsule articulaire antérieure et postérieure puis une rupture du complexe ligamentaire collatéral médial (instabilité multidirectionnelle).
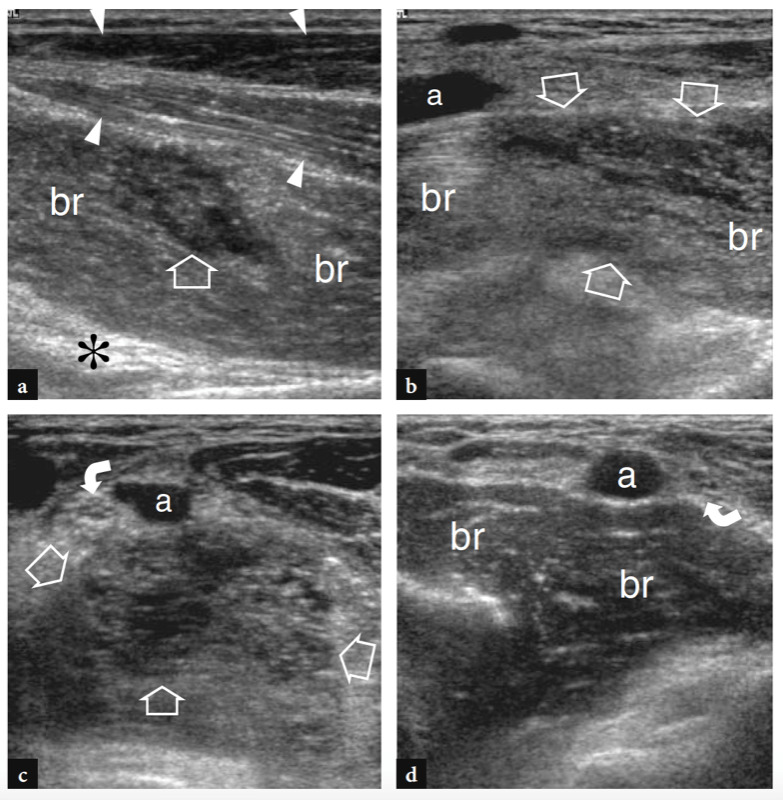
Figures 76a–d. Déchirure partielle du muscle brachial consécutive à une luxation postérieure. a,b Les images échographiques longitudinales et c transversales 12−5 MHz du coude antérieur obtenues dans la région supracondylienne montrent un large défect hypoéchogène (grosses flèches) dans la substance du muscle brachial (br) lié à un hématome. Le tissu musculaire déchiré est entouré d'espaces anéchoïques. Notez la relation entre le brachial blessé et le muscle biceps distal normal (têtes de flèches), l'artère brachiale (a) et le nerf médian (flèche incurvée). d Côté sain controlatéral. L'image US transversale 12−5 MHz correspondante montrée en c révèle un brachial intact.
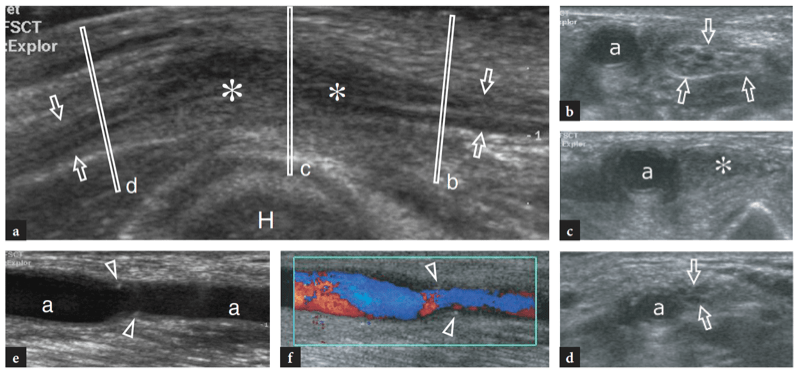
Figures 77a–f. Lésion traumatique du nerf médian et de l'artère brachiale après luxation postérieure du coude. Le patient a reçu une réparation chirurgicale primaire. une image US à axe long 12−5 MHz sur la trochlée (H) montre un gonflement fusiforme avec une surface externe indistincte et des modifications hypoéchogènes (astérisques) du nerf médian (flèches) par rapport à un névrome fusiforme post-traumatique. b – d Images américaines à axe court 12−5 MHz obtenues au niveau (barre blanche verticale) indiqué dans un élargissement du nerf révélateur et perte du motif fasciculaire interne (astérisque) au site de la blessure (b) par rapport à plus proximal ( niveaux a) et distal (c). Notez la relation étroite du nerf avec l'artère brachiale adjacente (a). e,f Échelle de gris grand axe e et Doppler couleur f 12−5 MHz Les images US de l'artère brachiale lésée montrent le site de la reconstruction vasculaire (têtes de flèches).
44. MASSES DU COUDE
Des masses solides et kystiques peuvent être rencontrées dans les tissus mous du coude en tant que découvertes fortuites. La plupart sont bénignes et ont un comportement indolent, comme les lipomes, les ganglions et les tumeurs neurales, et peuvent être facilement diagnostiquées avec l'échographie sur la base des critères décrits précédemment (Figues. 78, 79). Ce n'est qu'occasionnellement que les masses du coude peuvent provoquer des douleurs et des symptômes spécifiques liés à leur relation anatomique spécifique avec les structures du coude, notamment une atteinte articulaire et une compression nerveuse. Dans de tels cas, l'exérèse chirurgicale est toujours indiquée pour assurer la récupération de la fonction. De plus, l'échographie peut être utile pour distinguer les résultats normaux qui peuvent simuler une maladie. Au coude, cela survient le plus souvent chez les femmes jeunes qui consultent en raison d'une masse indolore située en avant de l'épicondyle médial qui est mieux appréciée avec une extension complète de l'articulation. Cette pseudomasse est due à la proéminence antérieure de la partie médiale de l'épicondyle qui devient évidente chez les femmes avec des articulations hyperlaxes lors de l'extension du coude> 180 °. Dans ces cas, l'US peut facilement exclure toute masse locale occupant de l'espace.
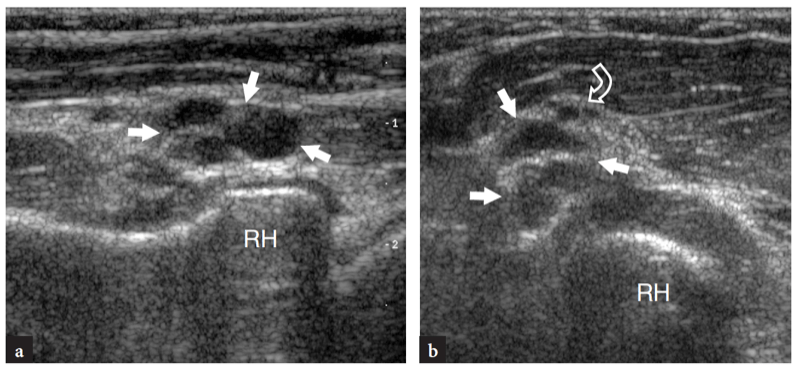
Figure 78a,b. Kyste ganglionnaire du coude chez un patient qui se plaignait de légères paresthésies irradiant sur la face dorsale du pouce. a Les images américaines longitudinales et b transversales à 12−5 MHz au-dessus de la tête radiale (RH) révèlent une petite masse remplie de liquide anéchoïque lobulée (flèches droites) compatible avec un ganglion, adjacente au nerf radial (flèche courbe). Le ganglion présentait un pédicule fin en liaison avec l'articulation radio-capitelleuse, confirmant son extension articulaire.
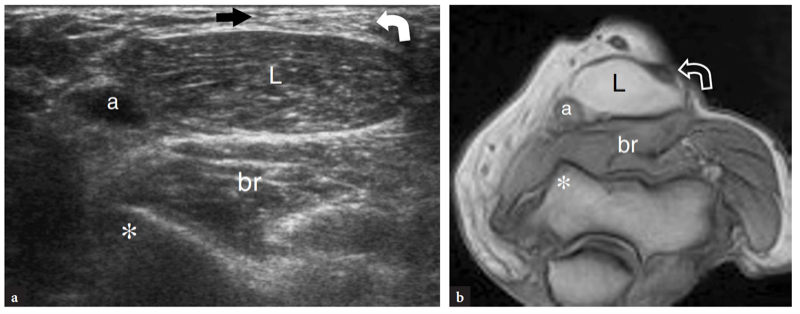
Figure 79a,b. Lipome chez un patient présentant un gonflement indolore des tissus mous sur la partie antérieure du coude. a Une image US transversale à 10-5 MHz sur l'humérus distal avec une corrélation d'imagerie b T1w GRE MR démontre une masse hypoéchogène ovale des tissus mous (L) située à la surface du muscle brachial (br) qui déplace l'artère brachiale (a) et l'artère distale tendon du biceps (flèches). Dans ce cas particulier, l'échotexture du lipome est assez similaire à celle du brachial sous-jacent et ne doit pas être interprétée comme un muscle normal. Astérisque, bord médial de la trochlée humérale.