Steven L. Orebaugh 和 Kyle R. Kirkham
引言
1990 年代中期,维也纳大学的麻醉师首次探索超声检查(US)作为引导周围神经阻滞(PNB)的手段。 尽管放射科医师已经利用超声技术引导穿刺针进行活检,但这种成像方式在 PNB 中的应用在当时还是很新颖的。 证明了超声在促进包括臂丛神经和股骨阻滞在内的一系列区域麻醉技术中的实用性。 十年后,加拿大多伦多大学的同事开始接受这项技术,进一步展示了它的实用性,并详细描述了臂丛神经的超声解剖结构。 与此同时,一些技术进步发生了,包括更小、更移动的超声平台、更高的分辨率和针头识别软件,所有这些都累积起来,增加了麻醉师对超声的床边实用性。
超声引导的优势
以前使用的基于表面解剖学的技术,例如神经刺激、标志性触诊、筋膜“咔哒”声、感觉异常和经动脉入路,无法监测局部麻醉剂注射液的配置。 然而,超声引导为神经阻滞提供了许多重要的实际优势。 超声波允许对感兴趣区域的解剖结构进行可视化。 这允许对针头路径到目标的更明智的指导,同时避免可能被针头损坏的结构。 超声波还允许在针尖穿过组织时对其进行可视化,从而确认与预期路径的对齐,再次降低针头意外损伤非预期结构的可能性。 也许最重要的是,实时超声成像允许持续可视化局部麻醉剂溶液的输送,以确保正确分布,并可以根据需要调整针尖位置以优化局部麻醉剂分布。
在区域内引入超声引导 麻醉 导致了许多神经阻滞技术的改进、PNB 的广泛使用以及外科同事和患者的更大接受度。
超声和超声解剖学
超声引导的 PNB 可以分解为两个基本方面:包括目标神经在内的截面平面中的成像结构和引导针。 理解和识别二维图像上的三维解剖结构需要在技术和超声解剖模式识别方面的培训。表1).
表1。 优化超声解剖可视化。
| 选择合适的换能器/频率 了解潜在的解剖关系 使用传感器施加不同程度的压力 将换能器与下面的神经目标对齐 旋转传感器以微调图像 倾斜换能器以优化图像 |
由于解剖识别对于放置块仍然至关重要,即使有实时视觉指导,专业协会培训住院医师和研究员的指南继续强调解剖解剖和大体解剖训练作为学习超声引导区域麻醉 (UGRA) 的固有组成部分的重要性。 在一项为期 1 个月的区域麻醉轮换研究中,住院医师使用超声成像显着改善了对几个不同 PNB 部位相关结构的识别。 在对超声引导下肌间沟阻滞教学的评估中,住院医师表现出随着他们在旋转过程中经验的增加,他们的声波解剖识别效率不断提高。
更多创新的培训方法也显示出了希望。 将解剖程序集成到床边超声机的软件中已被证明可以提高解剖学笔试的分数。 在接受多媒体解剖演示后,住院医师和社区麻醉师在后测中展示了对超声解剖学知识的增加,尽管他们无法在真人模型上进行的超声解剖学实践考试中提高分数。 然而,解剖知识与超声二维解剖模式识别之间的最佳联系尚未得到充分探索。
优化超声图像的某些基本原则适用于所有神经阻滞。 例如,超声检查需要了解力学和人体工程学。 新手容易出现探头疲劳、探头方向反转、设备准备不足等错误。 为了优化超声图像,建议使用助记符 PART(压力、对齐、旋转、倾斜)。 压力是必要的,以尽量减少与目标的距离并压缩皮下脂肪组织。 对齐是指将换能器放置在四肢(或躯干)上方的位置,在该位置上,潜在的神经预计会在视野中。 旋转允许微调目标结构的视图。 倾斜有助于使探头的表面与下面的目标垂直排列,以最大限度地增加返回回波的数量,从而提供最佳图像(图1)。 关于优化超声成像的深入讨论在“优化超声图像“。
NYSORA 小贴士
- 为了优化超声图像,建议使用助记符 PART:压力、对齐、旋转、倾斜。
- 识别和理解声波解剖需要了解基本的三维解剖。
- 目标神经的最佳可视化需要适当的换能器压力、与神经对齐以及探头的旋转和倾斜以微调图像。
使用超声临床场景优化神经和针头成像
神经成像可以在短轴(探针面垂直于神经轴)或长轴(探针面平行于神经轴)位置进行(图2).
使用短轴成像通常更容易识别圆形、通常是高回声的神经元,尤其是对于初学者。 因为大多数神经阻滞是在四肢进行的,所以这种定向导致换能器位置是横向的,穿过手臂或腿的长轴。 一般来说,根据大体解剖学知识了解神经的走向,可以使换能器垂直于神经走向对齐和旋转,然后如前所述调整倾斜度以优化图像。
一旦确定了神经和周围的解剖结构,就可以选择针路径,以便在平面内(针平行于探头的长轴)或平面外(针垂直于探头的长轴)对超声波束进行成像。 虽然这两种方法在阻滞成功或患者安全方面均未显示出优越性,但首选方法可能因解剖或技术考虑而异。 然而,通过平面内成像,可以保持包括尖端在内的整个针头的图像,尽管将针头完全保持在换能器的观察平面内可能具有挑战性。 这种方法在教学期间特别有用,因为当针尖穿过组织时,主管可以持续观察针尖。
在平面外成像过程中,观察者只能看到针的横截面,它在整个长度的任何平面上都显示为一个小的高回声点,因此区分针尖和针杆要困难得多.
然而,在将整个针头保持在成像平面内的同时将针尖引导至目标可能具有挑战性(表2).
表2。 使用超声波优化针头成像。
| 如果可能,使用较浅的接近角 “跟”换能器,使面部更平行于 针 旋转传感器以确保看到整个针头 根据需要倾斜换能器 选择“回声”针 应用针识别软件(如果有) “液压定位”可能有助于确定针尖位置 |
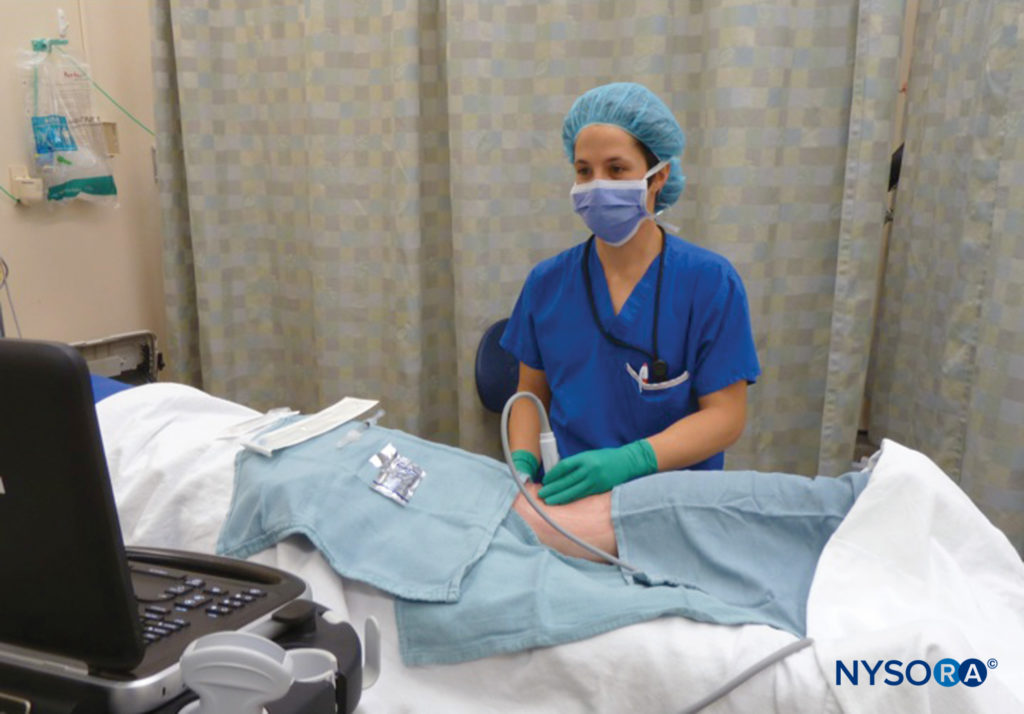
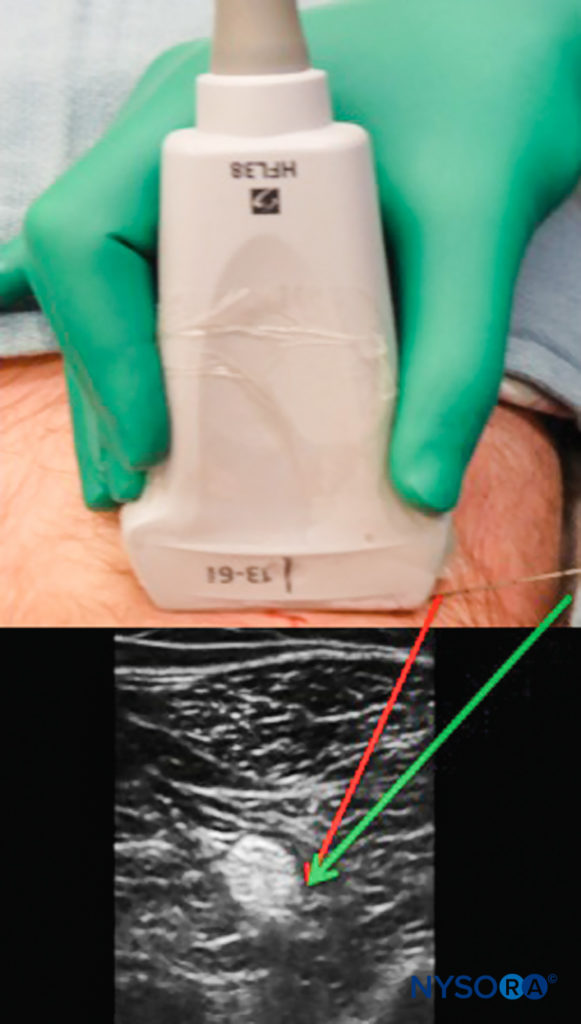
适当调整床的高度和符合人体工程学的超声波放置,使操作者的眼睛可以轻松快速地从图像转移到现场(图3),其中可以确保针与探头的长轴对齐,这是有益的。 当一个人的视线固定在超声屏幕上时,换能器很容易偏离针的平面。 如果操作员使探针和针垂直于他或她自己的观察轴对齐,而不是将针和探针与观察轴对齐,则更有可能发生这种情况。
在对学习 UGRA 基础知识的新医科学生进行的一项研究中,Speer 等人发现受试者定位目标所需的时间更少,并且能够更好地保持针在超声图像上的平面可视化, 和观看屏幕对齐。 尽管在血管通路方面已经完成了更多的工作,但导针器还可以在接近目标期间改进针的成像。 导针器的一个缺点是它们将针的运动限制在一个平面上,这可能并不总是理想的。
短轴神经的外观在某种程度上取决于它们与神经轴的接近程度。 尽管在大多数区域神经是圆形的,但它们可能呈现梭形,例如近臂的肌皮神经,或椭圆形,例如臀下区的坐骨神经。 与脊柱密切相关的神经和神经根主要由神经组织组成,结缔组织最少。 由于神经组织在超声成像上呈低回声,而束间的结缔组织呈高回声,靠近神经轴的神经呈黑色结节。
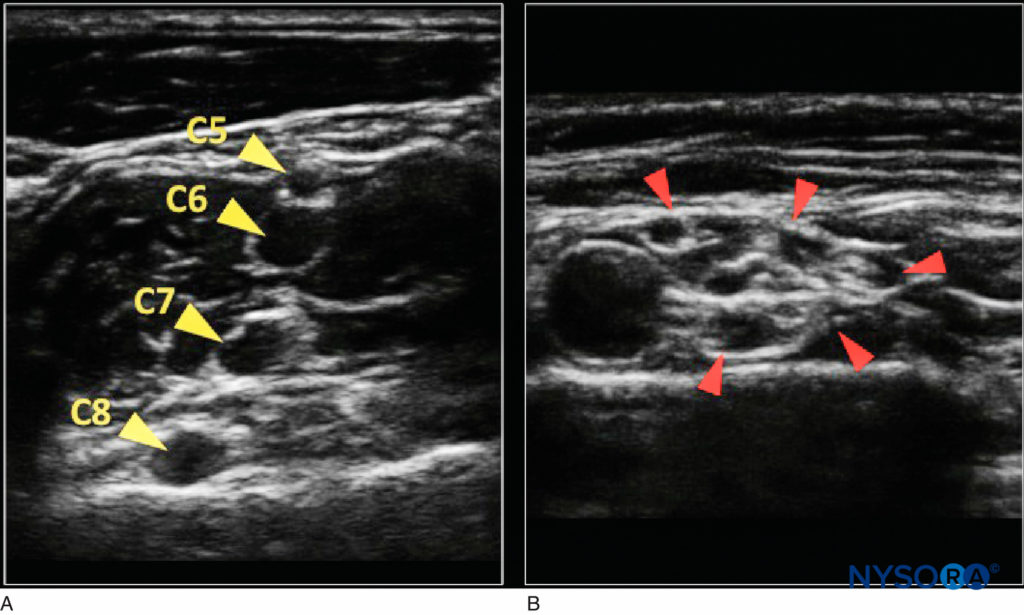
随着神经向周围走行,神经束的数量增加,尽管它们的大小减小了,而结缔组织的数量也增加了。 这些变化导致超声在短轴观察中出现越来越复杂的“蜂窝状”外观。图4)。 不幸的是,由于当前超声机器的技术限制,可能无法准确描绘周围神经内束的数量和排列。
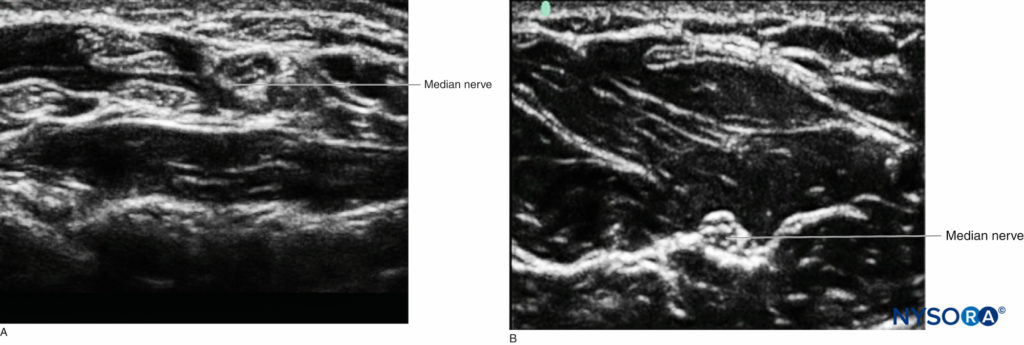
虽然不同的组织在超声上具有特征性的外观,但在短轴上观察两者时,可能不容易将神经与肌腱区分开来。 然而,使用解剖学知识,操作员可以遵循头尾结构的过程来确定成像结构的性质。 肌腱最终会消失在原始肌肉中或插入骨骼中。 一个很好的例子是腕部的正中神经,那里很难从腕管中的许多肌腱中辨别神经结构,而前臂中部的神经在视觉上更加明显,因为它位于两层之间肌肉,周围没有肌腱(图5).
为阻滞做准备的一个重要方面是在规划针路路径的同时获得首选的成像平面。 操作者应确保在计划过程中没有脆弱的结构,例如血管、胸膜或敏感结构,例如骨膜。
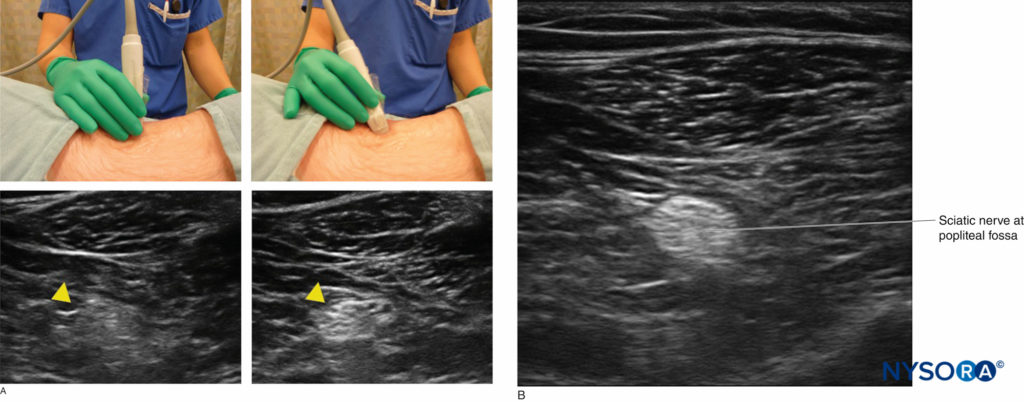
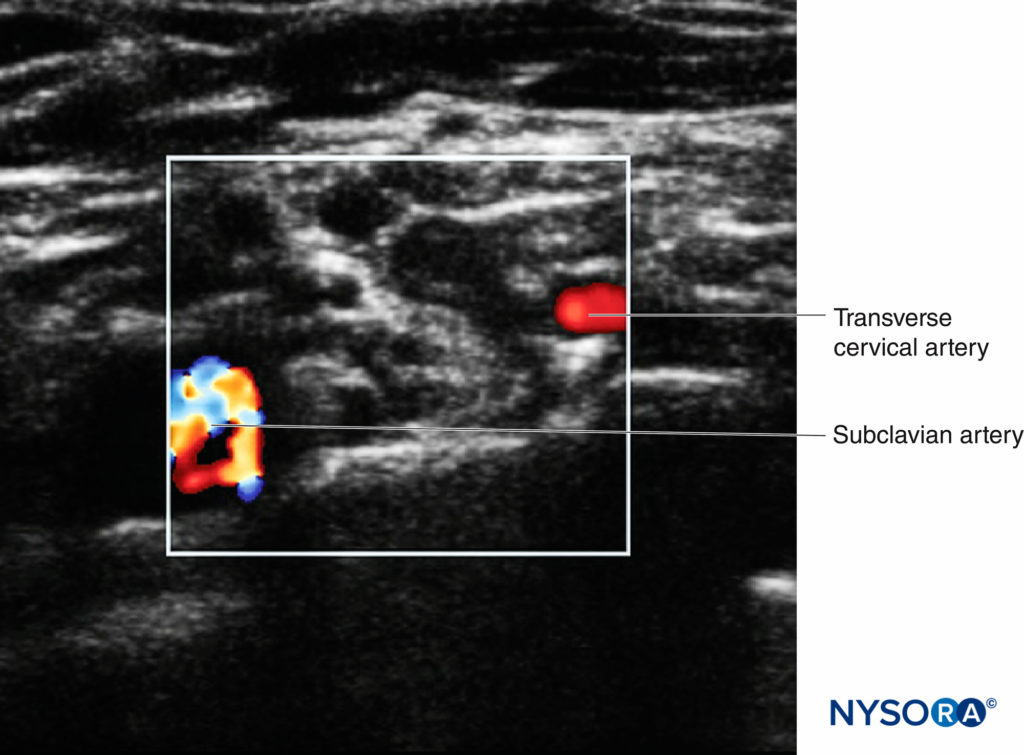
这个过程被称为“预块扫描”,它有助于患者安全和块成功。 除了二维成像外,还应使用彩色多普勒设置来识别小血管,当从短轴上观察时,这些小血管很容易与神经结构(尤其是根)混淆。图6).
为了保持针尖和针杆的视野,可以使用多种技术。 针与探头表面的平行度越高,传回换能器的回波就越多,从而获得更好的图像。 这可以通过在针插入部位轻轻压入皮肤或将插入部位远离探头移动来实现,从而降低插入的锐角(图7)。 这种方法的局限性在于可能需要更长的针头,并且在到达目标的途中要穿过更多的组织。
另一种称为倾斜的技术涉及压入与针插入侧相对的换能器边缘,这导致探头面与针更平行对齐。 此外,针头本身的结构可能会被改变以增加其回声性; 这些“回声针”的市售版本通常在轴的表面上蚀刻有交叉线,以产生更大程度的超声波束散射。
如所指出的,针引导器可用于改进针成像,尽管以限制运动为代价。 还创建了激光制导系统以改善对准,并取得了一些成功。 一种新颖的靶向针放置和局部麻醉剂输送的替代方法利用 GPS 引导系统,当由于针角陡峭而难以成像时,该系统可能特别有用。 用于陡角针头定位的专有软件利用空间复合成像,它结合了不同角度的声波图像。 这导致使用标准和回声阻滞针增强针成像。 最后,针尖的定位可以通过“液压定位”来完成,其中注射少量的葡萄糖溶液或局部麻醉剂以观察组织内的扩散,这通常揭示针尖的位置。
NYSORA 小贴士
• 几种不同的技术可用于通过超声成像保持针的可视化,包括使用浅接近角、“倾斜”换能器、市售的回声针以及物理测量,如换能器的旋转和倾斜。
• 此外,在困难的情况下,可以使用带有少量流体注射的液压定位来促进针的定位。
• 针头应在持续观察的情况下推进以避免损伤解剖结构。
• 预块扫描,包括使用彩色多普勒功能,有助于规划针的路线。
• 针尖穿过与神经相邻的筋膜平面时应以切线方式进行,以避免筋膜“释放”针头时刺穿神经。
使用超声波进行安全导针
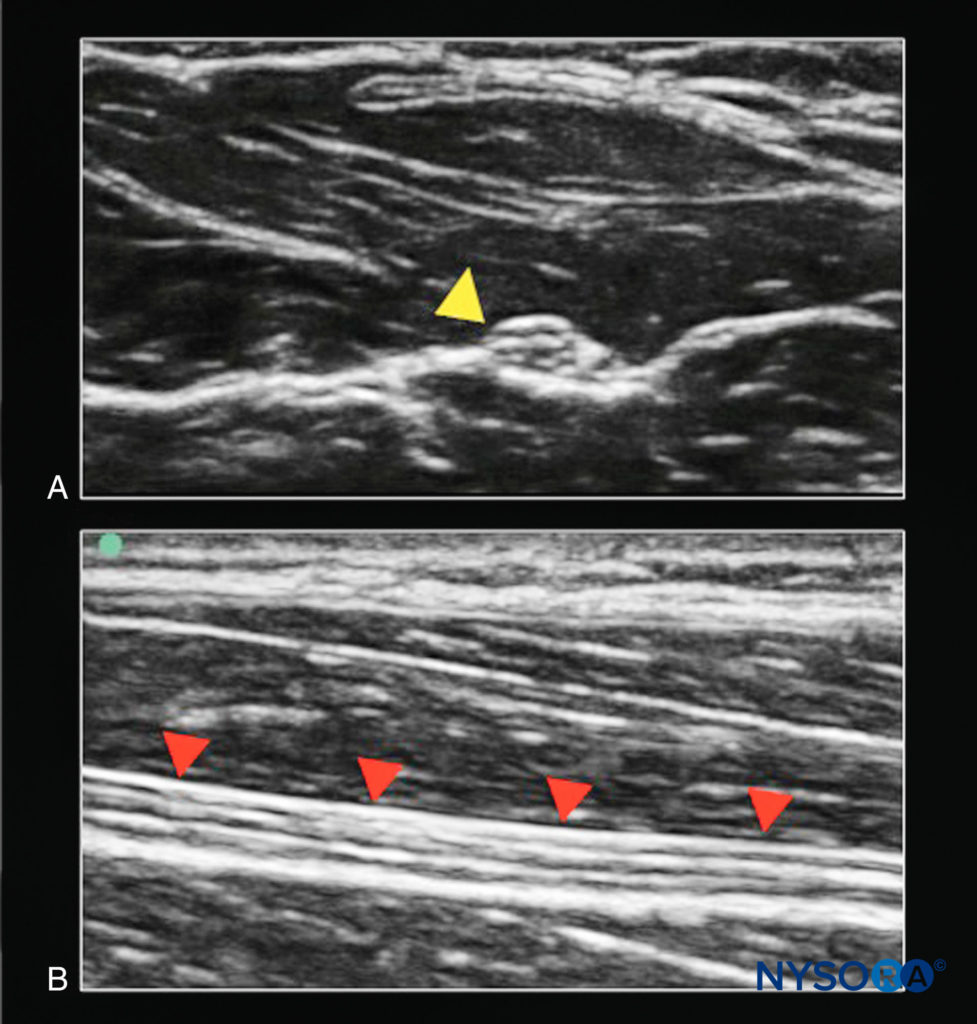
在通过平面内成像将针尖推向目标神经时,应该谨慎和慎重,试图始终保持针头在平面内。表3)。 平面内针尖的特点是从斜面产生的双回波返回。
表3。 超声引导神经阻滞期间的安全提示。
| 执行“预块扫描”以确定解剖结构 利用彩色多普勒设置来识别血管 如果尖端未定位,请勿推进针头 “Hydrodissection”可用于描绘解剖结构 当通过筋膜推向神经时,靠近 切线地 慢慢穿过筋膜,等待“砰”的一声或突然 释放 通过后重新优化针尖图像 招牌 当对针神经接口有疑问时,轻轻 移动针头以确定神经没有 随它移动(表明尖端嵌入在 神经外膜) |
超声从针的浅壁和深壁反射,导致可与针杆的单次返回区分开来的阶梯状外观。 当光束在针轴上下移动时,超声波探头的细微滑动有助于确认尖端的位置。
通常,会遇到阻碍进针的筋膜平面。 这些坚韧的结缔组织层可能被视为“帐篷”,因为尖端推动它们,突然让位并弹回原来的位置。 这种突然的变化可能会产生两个后果:首先,针头可能会在无意中快速推进,超出操作者的意图(除非这是预料到的); 其次,针可能会移出平面。 此时,应停止针的向前运动,直到再次优化平面内图像。 这种筋膜平面通常位于神经靶点的表面或附近,如肌间沟、腋神经血管束或股神经。 如果没有预料到筋膜平面的突然释放,这种运动实际上可能导致针头向前推进并遇到神经。 出于这个原因,建议切向接近神经,突出针头的推进,使其尖端靠近神经,但不瞄准其中心。
当以较浅的角度接近时,这些坚韧的面部平面所遇到的阻力也可能会无意中重定向针头。 暂时使针角变陡可以允许更容易和更受控的通过。 不幸的是,超声引导并不总是能产生清晰的图像,使人们能够将神经组织与周围组织区分开来。 在这种情况下,随着针头的推进,“水分离”(故意将液体注入组织平面)可用于分离结构,从而使成像更清晰,使用葡萄糖或局部麻醉剂溶液。
此外,随着针头的推进,可以观察组织的行为,以帮助定位针尖相对于神经组织的位置。
虽然曾经有人认为用针尖接触神经可能会导致感觉异常,事实上,这被认为是一种合适的神经定位技术,但我们现在知道,针状神经接触并不会始终引发感觉异常。 这强调需要通过超声成像准确定位针尖,并在 PNB 期间使用额外的监测来检测危险的针-神经关系,例如神经刺激和注射压力监测。
NYSORA 小贴士
- 应通过利用可以包含或引导药物围绕神经的筋膜平面或鞘来优化局部麻醉溶液的沉积
并沿其路线纵向。 - 对于没有这种局部筋膜封闭的神经,应以圆周方式注射溶液以加速阻滞的发生。
使用超声刺激周围神经
几十年来,周围神经刺激器 (PNS) 一直是 PNB 期间神经定位的标准工具,成功率高,并发症发生率低。然而,广泛采用 超声成像 对其在 PNB 中持续扮演的角色提出质疑。十多年前,Perlas 等人在针与神经接触的超声成像过程中评估了上肢周围神经对周围神经刺激的敏感性。作者报告说,尽管可以看到针尖压入神经表面,但刺激器设置为提供 0.5 mA 或更低的电流时,超过 25% 的时间没有发生运动刺激。
已经进行了几项具有各种不同模块的研究,以评估这种本地化工具与 UGRA 相关联的效用。 无论是锁骨上阻滞、腋窝阻滞还是股骨阻滞,作者都表明在超声引导下的 PNB 期间添加神经刺激器作为神经定位工具对成功没有帮助。
此外,Robards 等人发现,在腘窝阻滞期间对 PNS 0.2 和 0.5 mA 之间没有运动反应并不总是排除将针放置在神经内,并且这种刺激实际上可能导致不必要的针进入神经的操作。
然而,出于除确保阻滞功效之外的原因,刺激器可能可用作 UGRA 的辅助手段。 因为已经确定低于 0.2 mA 的神经刺激阈值表明针尖放置在神经内的可能性很高,所以在 UGRA 期间可以使用刺激器作为安全监测器。 在超声引导下深度神经阻滞或超声图像不如预期精确时,神经刺激器尤为必要。 在这种情况下,诱发的运动反应可以警告束内注射局部麻醉剂。
此外,在某些情况下,可能需要更精确地识别不同的神经,例如在腋窝阻滞期间,PNS 通过其对电刺激的特定运动反应来描绘神经。 在某些解剖位置,可能存在仅通过可视化难以识别的神经结构,无论它们是阻塞的目标还是只想用针头避开它们; 在这些情况下,PNS 对于提供这种识别可能是非常宝贵的。
最后,有些神经不适合超声可视化,主要是因为深度或骨对超声传输的干扰。 最常见的例子是腰丛后路,其中超声可用于识别局部骨结构以引导阻滞,但 PNS 仍然是引导针尖接近腰椎的有价值工具神经丛的神经。
总体而言,大量数据表明,在超声引导下的神经阻滞期间常规使用神经刺激器会产生临床相关的安全信息,这些信息可以影响临床决策并积极影响患者安全。
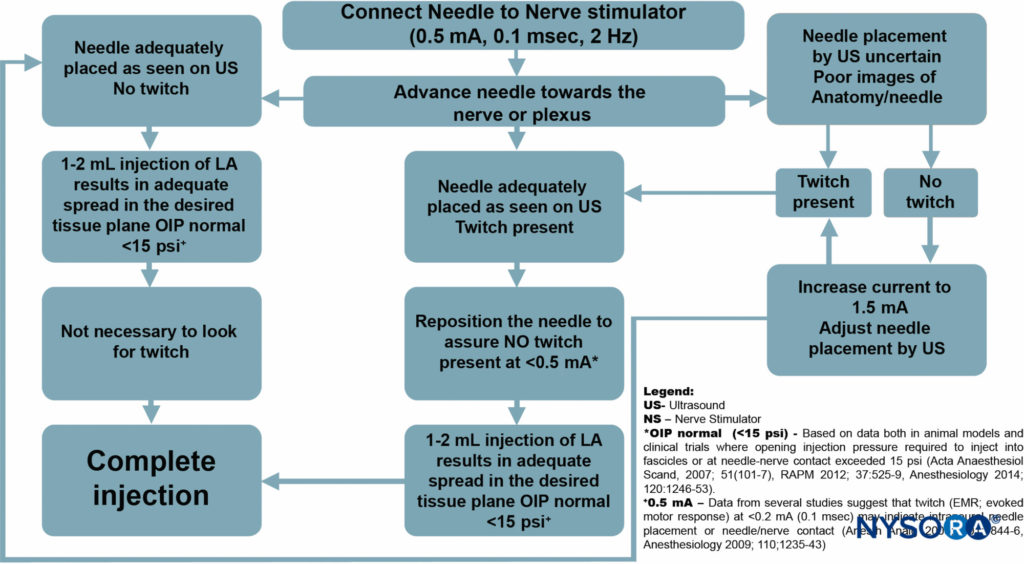
然而,建议的常规使用 UGRA 神经刺激的主要目的是为了安全监测,而不是神经定位。图8)。 在这种能力下,神经刺激器可以简单地设置为 0.5 mA (0.1 ms)、2 Hz,而无需在整个过程中改变电流强度。
虽然不寻求运动反应,但运动反应的发生应该需要停止进针并稍微撤回针,因为在当前输送设置下的运动反应几乎总是表明针-神经接触或神经内针放置。
优化局部麻醉剂在目标神经附近的输送
在目标神经附近准确放置针头后,在确定抽吸对血管内针头放置不利后,在包含要麻醉的神经的组织平面内注射局部麻醉剂。表4).
表4。 优化局麻药沉积。
| 以小等分注射局部麻醉剂溶液 观察注射过程中是否有疼痛或高压 确保在针尖观察到液体的扩散 注射过程中 在注射之间抽吸 注意可能隔离的筋膜平面 或引导解决方案 避免局麻药沉积到肌肉中 对于四肢的孤立神经,寻求创造一个“甜甜圈” 或神经周围的“光环” 对于筋膜内的神经,寻求“填充” 筋膜受限于溶液a |
Brull 等人评估了长期以来的观点,即局部麻醉剂溶液应该以圆周方式引导在可见神经周围,必要时改变针头位置,而不是简单地让溶液沿着神经的一个方面积聚一针位置。
他们发现,前者的区块建立速度比后者快 33%。 虽然一般建议在神经周围创建“甜甜圈”或“光环”,但某些神经由于其解剖状况,可能不需要这种刻意的圆周放置。 这通常由覆盖或周围筋膜平面的位置和配置决定,例如在肌间沟和股骨三角处。 在随后的特定 UGRA 部分中描述了每个神经周围的局部麻醉剂的最佳输送。
局部麻醉剂注射的实时成像允许评估流体的正确处置。 注射阶段应使用少量局部麻醉剂(3-5 mL)进行,每次之间留出一小段时间,以便在继续注射之前出现任何局部麻醉剂全身毒性(LAST)症状的证据按照美国区域麻醉和疼痛医学协会 (ASRA) 指南的建议给药。
此外,每个等分试样的输送应在抽吸之前进行,并应注意打开注射压力或抱怨目标神经分布的疼痛或感觉异常。
虽然超声已被证明可以降低血管内针头放置的可能性,但仍可能发生 LAST 血管内注射。 因此,必须了解血管的位置,血管的膨胀压力非常低,以至于在体表的普通压力与传感器一起完全消除了它们的管腔。 因此,在预块扫描期间使用彩色多普勒筛查血管的存在是有帮助的。 然而,小血管可能会被遗漏,并且多普勒功能在更深的地方会恶化。
因此,必须在整个注射过程中观察超声图像,以寻找针尖处的局部麻醉溶液扩散组织的证据。 未能看到这种扩散表明针尖不在平面内或在血管内腔中。
错误的针头放置在血管和神经中都有描述。 Moayeri 等人在一项基于尸体的研究中表明,超声成像对周围神经的注射很敏感,只有 0.5 mL 就会引起明显的神经扩张迹象。 与注射大量局部麻醉剂相比,这种可视化允许立即拔出针头,这可能会减少神经损伤的机会。
结论
超声检查彻底改变了区域麻醉领域。 该技术的有效应用需要了解二维解剖结构、神经和解剖结构的最佳成像、准确的实时针引导和精确的局部麻醉剂输送。 这些元素的组合确保了从这种强大的成像模式中获得最大的好处,确保神经阻滞的成功率和提高患者的安全性,特别是在 LAST 方面。
参考文献:
- Kapral S、Krafft P、Eibenberger K 等人:超声引导锁骨上入路用于臂丛神经区域麻醉。 Anesth Analg 1994;78:507–513。
- Marhofer P、Schrogendofer K、Koinig H 等:超声引导改善三合一阻滞的感觉阻滞和起效时间。 Anesth Analg 1997;85:854–857。
- Marhofer P、Schrogendofer K、Wallner T 等人:超声引导可减少 3 合 1 块的局部麻醉剂用量。 Reg Anesth Pain Med 1998;23:584–588。
- Perlas A、Chan VW、Simons M:使用超声和电刺激进行臂丛神经检查和定位。 麻醉学 2003;99:429–435。
- Gray AT:超声引导下的区域麻醉。 麻醉学 2006; 104:368–373。
- Manickam BP、Perlas A、Chan VW 等:术前系统调查在超声引导下的区域麻醉中的作用。 Reg Anesth Pain Med 2008;33:566–570。
- BD、Brull R 站点:周围区域麻醉中的超声引导:哲学、循证医学和技术。 Curr Opin Anesth 2006;19:630–639。
- Sites BD、Chan VW、Neal JM 等:美国局部麻醉和疼痛医学协会和欧洲局部麻醉和疼痛治疗协会联合委员会建议在超声引导下进行局部麻醉的教育和培训。 Reg Anesth Pain Med 2010;35(增刊 1):S74-80。
- Orebaugh SL、Bigeleisen PE、Kentor ML:区域麻醉轮换对麻醉科住院医师超声识别解剖结构的影响。 麻醉学报 2009;53:364–368。
- Orebaugh SL、Williams BA、Kentor ML 等人:使用超声引导的 Interscalene 阻滞:经验对居民表现的影响。 Acta Anaesth Scand 2009;53:1268–1274。
- Adhikary SD、Hadzic A、McQuillan PM:用于在超声引导下的区域麻醉期间教授手眼协调的模拟器。 Br J Anaesth 2013;111(5):844–845。
- Wegener JT、van Doorn T、Eshuis JH 等:超声引导区域麻醉中图像判读电子教程的价值。 Reg Anesth 疼痛医学 2013;38:44-49。
- Woodworth GE、Chen EM、Horn JL 等人:基于计算机的视频和模拟在超声引导下的区域麻醉培训中的功效。 临床麻醉杂志 2014;26:212–221。
- Sites BD、Spence BC、Gallagher JD 等人:表征与学习超声引导外周区域麻醉相关的新手行为。 Reg Anesth Pain Med 2007;32:107-115。
- BD、Spence BC、Gallagher J 等站点:区域麻醉与超声相遇:转型中的专业。 ACTA 麻醉扫描 2008;52:456–466。
- Speer M、McLennan N、Nixon C:平面超声成像新手。 Reg Anesth Pain Med 2013;38:350–352。
- Ball RD、Scouras NE、Orebaugh S 等人:比较住院医师针引导与徒手超声技术用于中心静脉导管通路的随机前瞻性观察模拟研究。 Br J Anaesth 2012;108:72–79。
- Schafhalter-Zoppoth I, Gray AT:肌皮神经:周围神经阻滞的超声表现。 Reg Anesth Pain Med 2005;30:385–390。
- Moayeri N、van Geffen GJ、Bruhn J 等:坐骨神经的超声、横断面解剖和组织学之间的相关性。 Reg Anesth Pain Med 2010;35:442–449。
- Bonnel F:成人臂丛神经的显微解剖:显微外科手术的解剖学和组织学基础。 显微外科 1984;5:107-118。
- van Geffen GJ、Moayeri N、Bruhn J 等:超声成像、横断面解剖和臂丛神经组织学之间的相关性。 Reg Anesth Pain Med 2009;34:490–497。
- Moayeri N,Bigeleisen PE,Groen GJ:臂丛神经和周围隔室的定量结构,以及它们对神经丛阻滞的可能意义。 麻醉学 2008;108:299–304。
- Sylvestri E、Martinoli C、Derchi LE 等:周围神经的回声纹理:US 与组织学发现和肌腱鉴别标准之间的相关性。 放射学 1995;197:291–296。
- McCartney CJ、Xu D、Constantinescu C 等:前臂周围神经的超声检查。 Reg Anesth Pain Med 2007;32:434–439。
- Sites BD、Brull R、Chan VW 等:与超声引导区域麻醉相关的伪影和陷阱错误。 Reg Anesth Pain Med 2007;32:419–433。
- Chin KJ、Perlas A、Chan VW 等:超声引导区域麻醉中的针头可视化:挑战和解决方案。 Reg Anesth Pain Med 2008;33:532–544。
- Hebard S, Hocking G:回声技术可以提高超声引导区域麻醉期间的针头可见度。 Reg Anesth Pain Med 2011;36:185–189。
- Rettig HC,Gielen MJ:徒手技术还是机械导针装置? [信] Reg Anesth Pain Med 2009;34:608–609。
- 不列颠哥伦比亚省的 Tsui:使用便携式激光装置促进针在平面内与超声波束对齐。 Reg Anesth Pain Med 2007;32:84-88。
- Wong SW、Niazi AU、Chin KJ 等:使用 SonixGPS 针跟踪系统的实时超声引导脊髓麻醉。 Can J Anaesth 2013;60:50-53。
- Wiesmann T、Borntrager A、Zoremba M 等人:复合成像技术和回声针设计。 Reg Anesth 疼痛医学 2013; 38:452–455。
- Soong J, Schafhalter-Zoppoth I, Gray AT:换能器角度对股神经超声可见度的重要性。 Reg Anesth 疼痛医学 2005;30:505。
- Alakkad H,Chin KJ:良好的针刺技术在超声引导下腋窝阻滞中的重要性。 Reg Anesth 2013;38(2):166。
- Bigeleisen PE1,Moayeri N,Groen GJ。 超声引导锁骨上阻滞期间的神经外与神经内刺激阈值。 麻醉学。 2009;110:1235–43。
- Hadzic A,Dilberovic F,Shah S,Kulenovic A,Kapur E,Zaciragic A,Cosovic E,Vuckovic I,Divanovic KA,Mornjakovic Z,Thys DM,Santos AC。 神经内注射和高注射压力的组合导致狗的肌束损伤和神经功能缺损。 Reg Anesth Pain Med 2004;29:417-23。
- Auroy Y、Benhamou D、Bargues L:法国局部麻醉的主要并发症。 麻醉学 2002;97:1274–1280。
- Perlas A、Niazi A、McCartney C 等人:运动反应对神经刺激的敏感性以及通过超声评估的神经定位感觉异常。 Reg Anesth Pain Med 2006;31:445–450。
- Beach ML, Sites BD, Gallagher JD:使用神经刺激器并不能提高超声引导锁骨上阻滞的疗效。 临床麻醉杂志 2006;18:580–584。
- Chan VW、Perlas A、McCartney CJ 等:超声引导提高腋窝臂丛神经阻滞的成功率。 Can J Anaesth 2007;54:176–182。
- Sites BD、Beach ML、Chinn CD 等:用超声与超声和神经刺激进行股神经阻滞后感觉和运动丧失的比较。 Reg Anesth Pain Med 2009;34:508–513。
- Robards C、Hadzic A、Somasundraram L 等人:腘坐骨神经阻滞期间低电流刺激的神经内注射。 麻醉剂
2009; 109:673-677。 - Sigenthaler A、Moriggl B、Mlekusch S 等人:超声引导的肩胛上神经阻滞:一种新型锁骨上入路的描述。 Reg Anesth Pain Med 2012;37:325–328。
- Hanson NA,Auyong DB:在肌间沟阻滞期间肩胛背侧和胸长神经的系统超声识别。 Reg Anesth Pain Med 2013;38:54-57。
- Karmakar MK、Ho AM、Li X 等:超声引导腰丛神经阻滞通过腰椎超声三叉戟的声窗。 Br J Anaesth 2008;100:533–537。
- Gadsden J、Latmore M、Levine DM、Robinson A:高开放注射压力与股神经阻滞期间的针神经和针筋膜接触有关。 Reg Anesth Pain Med 2016;41(1):50-55。
- Gadsden JC、Choi JJ、Lin E、Robinson A:在超声引导下肌间沟臂丛神经阻滞期间,打开注射压力始终检测针-神经接触。 麻醉学 2014;120(5):1246–1253。
- Brull R、MacFarlane AJ、Parrington SJ 等人:环向注射是否有利于超声引导下的腘窝坐骨神经阻滞? Reg Anesth Pain Med 2011;36:266–270。
- Spence BC、Beach ML、Gallagher JD 等:超声引导下肌间沟阻滞:了解局部麻醉剂的注射位置。 麻醉 2011;66(6):509–514。
- Neal JM、Bernards CM、Butterworth JF 等:ASRA 实践咨询
局麻药全身毒性。 Reg Anesth Pain Med 2010;35:350–352。 - Abrahams MS、Aziz MF、Fu RF 等:超声引导与电神经刺激对周围神经阻滞的比较:随机对照试验的系统评价和荟萃分析。 麻醉 2009;102:408-417。
- Zetlaoui PJ、Labbe JP、Benhamou D:腋丛神经阻滞的超声引导不会阻止血管内注射 [信]。 麻醉学 2008;109:761。
- VadeBancouer TR、Weinberg GL、Oswald S 等人:超声引导锁骨上肱动脉期间血管内注射的早期检测
丛阻滞。 Reg Anesth Pain Med 2008;33:278–279。 - Liu SS、YaDeau JT、Shaw PM 等:超声引导下肌间沟和锁骨上神经阻滞的意外神经内注射和术后神经系统并发症的发生率。 麻醉 2011;66:1365–2044。
- Hara K、Sakura S、Yokokawa N 等:超声引导下臀下坐骨神经阻滞期间无意神经内注射的发生率和影响。 Reg Anesth Pain Med 2012;37:289–293。
- Krediet AC、Moayer N、Bleys RL 等:神经内或神经外:定位低容量注射的诊断准确性或超声评估。 Reg Anesth 疼痛医学 2014;39:409–413。