Steve Roberts
INTRODUZIONE
L'anestesia regionale è una parte essenziale della moderna pratica anestesiologica pediatrica, poiché offre molti vantaggi significativi al paziente e all'ospedale (Tabella 1). Tuttavia, nonostante un forte corpus di prove che mettano in evidenza i vantaggi dell'anestesia regionale, è stato solo relativamente di recente che l'anestesia regionale ha iniziato a diventare un luogo più comune nella pratica anestetica. Ampi studi prospettici della Società di anestesiologi pediatrici di lingua francese (ADARPEF) non hanno dimostrato alcun aumento del rischio per i bambini di avere blocchi eseguiti in anestesia generale. Tuttavia, le complicanze erano quattro volte maggiori nei bambini di età inferiore a 6 mesi rispetto a quelli di età superiore a 6 mesi.
Storicamente, si pensava che i neonati richiedessero poca o nessuna analgesia. Tuttavia, un'analgesia inadeguata nel neonato può causare cambiamenti biocomportamentali che possono modulare le risposte future al dolore durante l'infanzia. Di conseguenza, le tecniche avanzate di anestesia regionale (p. es., l'analgesia epidurale) sono diventate sempre più utilizzate nei bambini di tutte le età. È interessante notare che gli studi ADARPEF hanno identificato che ora c'è una tendenza ad allontanarsi dai blocchi neuroassiali centrali verso le tecniche di catetere nervoso periferico. Questo cambiamento potrebbe essere stato influenzato dai progressi nella chirurgia mininvasiva e dalla somministrazione più prevedibile di tecniche di catetere periferico nella moderna pratica dell'anestesia regionale.
Tutte le tecniche di anestesia regionale possono essere eseguite in sicurezza nella popolazione pediatrica con una formazione adeguata e attrezzature moderne.
TABELLA 1. Vantaggi dell'anestesia regionale nei bambini.
| Benefici per il paziente | Analgesia superiore: si traduce in pazienti e genitori/caregiver più calmi. |
| MAC ridotto: rischio ridotto di GA più profondo, emergenza più regolare, ritorno dell'appetito più precoce. | |
| Neurotossicità: questo potenziale problema è dose-dipendente di GA; pertanto, una ridotta esposizione al MAC può essere vantaggiosa. | |
| Stabilità emodinamica: fino a 8 anni di età, i CNB raramente causano ipotensione significativa. | |
| Ridotto fabbisogno di supporto postoperatorio del ventilatore: in particolare nei neonati e nei lattanti sottoposti a chirurgia addominale superiore e toracica. | |
| Ottiene la risposta allo stress ormonale. | |
| Ridotta perdita di sangue intraoperatoria: dimostrata durante la riparazione dell'ipospadia, la riparazione della schisi e la tonsillectomia. | |
| Funzione gastrointestinale migliorata: peristalsi meglio mantenuta; miglioramento della perfusione splancnica nei casi di NEC e gastroschisi | |
| Evita la necessità di GA: i neonati prematuri sottoposti a GA sono a rischio di apnea postoperatoria. | |
| Benefici ospedalieri | Più facile da allattare: i bambini indolori richiedono meno manodopera da curare. |
| MAC ridotto: scarica rapida dal recupero di primo stadio. | |
| Ridotto fabbisogno di supporto ventilatorio postoperatorio: questo è di particolare beneficio quando il supporto PICU è limitato. | |
| Durata ridotta del soggiorno. |
DIFFERENZE ANATOMICHE TRA BAMBINI E ADULTI
Per quanto riguarda l'anatomia, la fisiologia e la farmacologia, gli adolescenti possono essere considerati "piccoli adulti"; tuttavia, neonati e bambini necessitano di un'attenzione speciale. Anatomicamente, la principale differenza sta nella colonna vertebrale e nel suo contenuto; questo argomento è descritto più dettagliatamente in Anestesia e analgesia epidurale e spinale pediatrica. Fisiologicamente, ci sono una serie di differenze riscontrate nel sistema nervoso pediatrico in via di sviluppo rispetto agli adulti. La mielinizzazione è incompleta alla nascita e il completamento del processo può richiedere 12 anni; di conseguenza, concentrazioni più basse di anestetico locale possono essere efficacemente utilizzate nella popolazione pediatrica, riducendo così anche il rischio di tossicità. Sebbene le vie nocicettive siano fondamentalmente le stesse nei bambini e negli adulti, ci sono differenze che possono causare un dolore maggiore nei bambini rispetto agli adulti. Nei bambini, il campo ricettivo di un neurone può essere maggiore, portando a una scarsa localizzazione del dolore. Le vie inibitorie discendenti sono immature e ciò può consentire input nocicettivi non modulati alle vie del dolore spinale ascendente. Le immaturità fisiologiche del fegato neonatale in associazione con una gittata cardiaca relativamente elevata producono differenze farmacologiche che si combinano per aumentare il rischio di tossicità da anestetico locale nei neonati.
FARMACOLOGIA DEGLI ANESTETICI LOCALI NEI PAZIENTI PEDIATRICI
Esistono due gruppi principali di farmaci anestetici locali utilizzati nell'anestesia regionale pediatrica: gli amino esteri e le amino ammidi. (Una discussione dettagliata di questi farmaci può essere trovata in Farmacologia clinica degli anestetici locali.) La farmacocinetica dell'anestetico locale nei bambini è relativamente scarsa, e specialmente nei neonati, è limitata; sfortunatamente, è questa fascia di età che è a maggior rischio di tossicità da farmaci anestetici locali.
Anestetici locali di tipo aminoammidico
Il gruppo di anestetici locali più comunemente usati nella pratica pediatrica sono le amino ammidi: lidocaina, bupivacaina, ropivacaina e levobupivacaina. Gli anestetici locali aminoammidici subiscono un metabolismo epatico. Tuttavia, il fegato neonatale è immaturo, con i sistemi citocromici che maturano a velocità variabili: il CYP3A4 entro i primi 9 mesi di vita rispetto al CYP1A2, che può richiedere fino a 8 anni di età per maturare. Il volume di distribuzione allo stato stazionario nei neonati è maggiore che negli adulti. I compartimenti fluidi cambiano drasticamente con l'età, l'80% del peso corporeo è costituito da acqua in un neonato prematuro, il 75% in un neonato a termine, il 65% in un neonato e il 60% nei bambini più grandi. Con l'aumentare dell'età, il fluido intracellulare aumenta dal 20% del peso corporeo nei neonati prematuri al 30% osservato negli adulti; entro questo lasso di tempo, i fluidi extracellulari sono dimezzati. Gli anestetici locali sono solubili in acqua; pertanto, i cambiamenti legati all'età nella composizione del compartimento dei fluidi sono significativi. I neonati hanno livelli più bassi di proteine che legano l'anestetico locale (p. es., alfa-1-glicoproteina acida e albumina), il che porta a un aumento della frazione di anestetico locale non legato e quindi a un rischio maggiore di tossicità. Tuttavia, nelle prime 48 ore dopo l'intervento, c'è un aumento della glicoproteina alfa-1-acida che può agire per proteggere il neonato. La clearance di questi farmaci è diminuita in quelli di età inferiore ai 3 mesi, raggiungendo gradualmente i livelli degli adulti entro gli 8 mesi di età. Di conseguenza, le emivite di eliminazione degli anestetici locali sono più lunghe nei neonati e nei lattanti rispetto agli adulti.
Bupivacaine
La bupivacaina è un isomero con l- e d-enantiomero, il d-enantiomero che causa la maggior parte degli effetti avversi che si osservano nell'uomo. Dato che la bupivacaina è il più tossico tra gli anestetici locali aminoammidici, si dovrebbe prendere in considerazione l'utilizzo di un'alternativa più sicura, in particolare per i neonati e quando vengono somministrate tecniche di infusione continua attraverso cateteri a permanenza. La farmacocinetica e la farmacodinamica della bupivacaina sono state ben documentate in letteratura. La concentrazione preferita per i bambini è dello 0.25% per i blocchi nervosi periferici e dello 0.1% per le infusioni continue. I bambini più grandi possono tollerare una dose maggiore di soluzione di anestetico locale (0.4 mg/kg/ora) rispetto a neonati e lattanti (0.2 mg/kg/ora). Il dosaggio di bupivacaina è limitato a 2–4 mg/kg per un'iniezione singola e 0.2–0.4 mg/kg per un'infusione continua.
Ropivacaine
La ropivacaina è un nuovo anestetico locale amidico che viene utilizzato più frequentemente in chirurgia pediatrica. È un l-enantiomero con meno effetti collaterali cardiovascolari e sul sistema nervoso centrale rispetto alla bupivacaina. La ropivacaina ha lievi proprietà vasocostrittive che possono spiegare il Tmax più lungo quando somministrata per via caudale rispetto alla bupivacaina. Sono disponibili dati di farmacocinetica nei bambini sull'uso di ropivacaina in infusioni continue e per iniezioni singole. Gli studi pediatrici hanno dimostrato una durata d'azione più lunga con la ropivacaina rispetto alla mepivacaina quando usata per il blocco dei nervi periferici. Si deve prestare attenzione anche durante l'uso di ropivacaina nei bambini, poiché sono stati segnalati casi di tossicità cardiovascolare.
Levobupivacaina
La levobupivacaina è un nuovo l-enantiomero con un rischio potenzialmente minore di grave tossicità cardiovascolare. Sono disponibili dati di farmacocinetica nei bambini e l'intervallo di dosaggio è simile a quello della bupivacaina. Gli esperimenti sugli animali hanno dimostrato che la levobupivacaina provoca una minore depressione miocardica e una minore incidenza di indurre aritmie fatali rispetto alla bupivacaina. Sebbene questo farmaco offra al medico la possibilità di un farmaco meno cardiotossico, è comunque necessario prestare attenzione.
Anestetici locali di tipo estere
A causa della loro breve durata d'azione e della propensione a provocare reazioni allergiche, gli amino esteri (p. es., procaina, 2-cloroprocaina, tetracaina) sono il gruppo di anestetici locali meno comunemente usato. A differenza degli anestetici locali aminoammidici, gli amino esteri sono metabolizzati dalle colinesterasi plasmatiche. Di conseguenza, il metabolismo degli anestetici locali a base di esteri dipende dai livelli di colinesterasi plasmatica. Pertanto, nelle popolazioni con livelli di colinesterasi plasmatica ridotti, come neonati e bambini, il livello plasmatico di questi farmaci può essere aumentato, portando potenzialmente a livelli di farmaci tossici. La presenza della colinesterasi plasmatica limita anche la durata d'azione di questi farmaci, portando ad un'attività ridotta. Gli anestetici locali esteri più comuni utilizzati nei neonati e nei bambini sono la cloroprocaina e la tetracaina. Questi farmaci sono usati occasionalmente nei bambini come coadiuvante dell'anestesia spinale in neonati precedentemente prematuri sottoposti ad anestesia spinale o come unica soluzione anestetica per l'analgesia caudale. La tetracaina è stata segnalata nell'anestesia spinale, specialmente nei neonati prematuri, come unico anestetico per la riparazione dell'ernia inguinale. La 2-cloroprocaina è stata ampiamente utilizzata nei bambini per l'analgesia nello spazio neuroassiale centrale.
DOSAGGIO DI ANESTETICI LOCALI NEI PAZIENTI PEDIATRICI
La maggior parte delle dosi di farmaco nei pazienti pediatrici si basa sul peso del paziente (Tabella 2), sebbene sia spesso dibattuto se il peso corporeo totale o la massa corporea magra siano più appropriati per i calcoli dei farmaci. Tuttavia, questo potrebbe non essere applicabile a considerazioni sull'anestesia locale; studi condotti su neonati sottoposti ad anestesia spinale hanno rilevato un fabbisogno maggiore di soluzione anestetica locale (in scala di peso) rispetto alle loro controparti adulte che utilizzano bupivacaina o tetracaina.
TABELLA 2. Dosi massime raccomandate e durata d'azione approssimativa degli agenti anestetici locali comunemente usati.
| Anestetico locale | Classe | Dose massima (mg/kg)a | Durata dell'azione (min) | Infusione (mg/kg/ora) |
|---|---|---|---|---|
| procaina | Estere | 10 | 60-90 | - |
| 2-cloroprocaina | Estere | 20 | 30-60 | - |
| tetracaina | Estere | 1.5 | 180-600 | - |
| Lidocaina | amidi | 5 | 90-200 | - |
| Bupivacaine | amidi | 2.5 | 180-600 | 0.2-0.4 |
| Ropivacaine | amidi | 2.5 | 180-600 | 0.2-0.5 |
| Levobupivacaina | amidi | 2.5 | 180-600 | 0.2-0.5 |
Anche la concentrazione di anestetico locale somministrato deve essere attentamente considerata. Viene spesso utilizzata una concentrazione più bassa di anestetico locale a lunga durata d'azione (p. es., 0.25% di levobupivacaina) poiché anche il bambino sta ricevendo un anestetico generale; pertanto, il blocco viene utilizzato solo per l'analgesia. Tuttavia, in alcuni scenari, devono essere somministrate concentrazioni inferiori o superiori di anestetico locale. Concentrazioni più basse (p. es., 0.125% di levobupivacaina) sono utili per ridurre il rischio di tossicità nei neonati e hanno meno probabilità di mascherare la sindrome compartimentale o ritardare la deambulazione. Concentrazioni più elevate di anestetico locale (p. es., levobupivacaina allo 0.5%) dovrebbero essere prese in considerazione quando è desiderabile un blocco motorio profondo (p. es., un intervento chirurgico di trasferimento del tendine degli arti inferiori nei bambini con paralisi cerebrale).
TOSSICITÀ DEI FARMACI ANESTETICI LOCALI
La tossicità degli anestetici locali nei bambini comprende la tossicità cardiovascolare e del sistema nervoso centrale (Tabella 3) e reazioni allergiche alle soluzioni di anestetico locale a base di esteri. Le differenze farmacocinetiche già discusse, insieme all'immaturità della barriera ematoencefalica, possono rendere più probabile la tossicità del sistema nervoso centrale nei neonati. Tuttavia, la co-somministrazione di anestesia generale può mascherare i primi segni e sintomi di tossicità sistemica. La dose di anestetico locale per i bambini è sempre calcolata su base milligrammo per chilogrammo, piuttosto che sui volumi previsti come nell'anestesia regionale per adulti. Sebbene sia riconosciuto che, tra i pazienti pediatrici, i neonati sono a più alto rischio di tossicità sistemica, la cautela dovrebbe essere la norma per i bambini di tutte le età, poiché negli adolescenti sono state registrate concentrazioni più elevate di alcuni anestetici locali rispetto agli adulti. Sono stati riportati anche livelli plasmatici tossici a seguito di dosi sicure di anestetico locale utilizzato per i blocchi caudali e ileo-inguinali, quindi si raccomanda la dose minima efficace.
TABELLA 3. Tossicità sistemica della soluzione di anestetico locale.
| Sistema nervoso centralea |
| Vertigini e vertigini |
| Disturbi visivi e uditivi |
| Contrazione muscolare e tremori |
| Convulsioni generalizzate |
| Cardiovascolare |
| Effetti cardiaci diretti |
| Fase rapida depressa di ripolarizzazione delle fibre di Purkinje |
| Sparo spontaneo depresso del nodo senoatriale |
| Effetto inotropo negativo sul muscolo cardiaco |
| L'afflusso di calcio è alterato, con conseguente diminuzione della contrattilità miocardica |
| Effetti sul tono vascolare |
| Basse concentrazioni: vasocostrizione |
| Alte concentrazioni: vasodilatazione |
| Aumento della resistenza vascolare polmonare |
È interessante notare che Weintraud et al. hanno scoperto che i blocchi ileoina-guinali guidati dagli Stati Uniti determinavano concentrazioni plasmatiche più elevate rispetto alle tecniche basate sui punti di riferimento. Ciò può essere dovuto a una maggiore superficie di assorbimento creata posizionando l'anestetico locale precisamente su un piano fasciale rispetto ai depositi multipli all'interno del muscolo che spesso si verificano con un metodo basato sul punto di riferimento.
Consigli NYSORA
Prevenire la tossicità sistemica nella popolazione pediatrica
- Scegli un farmaco meno tossico (p. es., levobupivacaina o ropivacaina).
- Non superare la dose massima (nei neonati può essere prudente dimezzare la dose massima).
- Iniettare piccole aliquote e aspirare ripetutamente.
- Gli Stati Uniti consentono l'uso di dosi più basse di farmaci e la visualizzazione dell'iniezione.
- Fare attenzione alle dosi ripetute e limitare le infusioni nei neonati a 48 ore.
- Una dose di prova contenente adrenalina può essere utilizzata per identificare l'iniezione intravascolare, ma è limitata dalla somministrazione di anestetico generale.
- Indipendentemente dalla tecnica utilizzata, tutti i bambini, a cui viene somministrata una qualsiasi soluzione di anestetico locale, in particolare se somministrati in infusione continua, devono essere monitorati continuamente per rilevare eventuali effetti avversi.
Consigli NYSORA
Gestione della tossicità da anestetico locale
Nella pratica pediatrica, i primi segni premonitori e sintomi di tossicità possono essere mascherati dalla somministrazione concomitante di anestesia generale. Ciò significa che il primo segno potrebbe essere un'aritmia o un collasso cardiovascolare. Considerare quanto segue quando si gestisce la tossicità dell'anestetico locale:
- Interrompere l'iniezione di anestetico locale.
- Istituire il supporto vitale di base e chiedere assistenza.
- Proteggere le vie aeree, ventilare con il 100% di ossigeno e ottenere l'accesso endovenoso.
- Le convulsioni possono essere gestite con una benzodiazepina o un agente anestetico di induzione.
- Se si è verificato un arresto cardiaco, iniziare il supporto vitale avanzato.
- Si noti che le aritmie sono spesso refrattarie e pertanto la rianimazione dovrebbe essere prolungata.
- Somministrazione lipidica. L'Associazione degli Anestesisti di Gran Bretagna e Irlanda ha pubblicato un semplice protocollo da seguire (Figure 1 ).
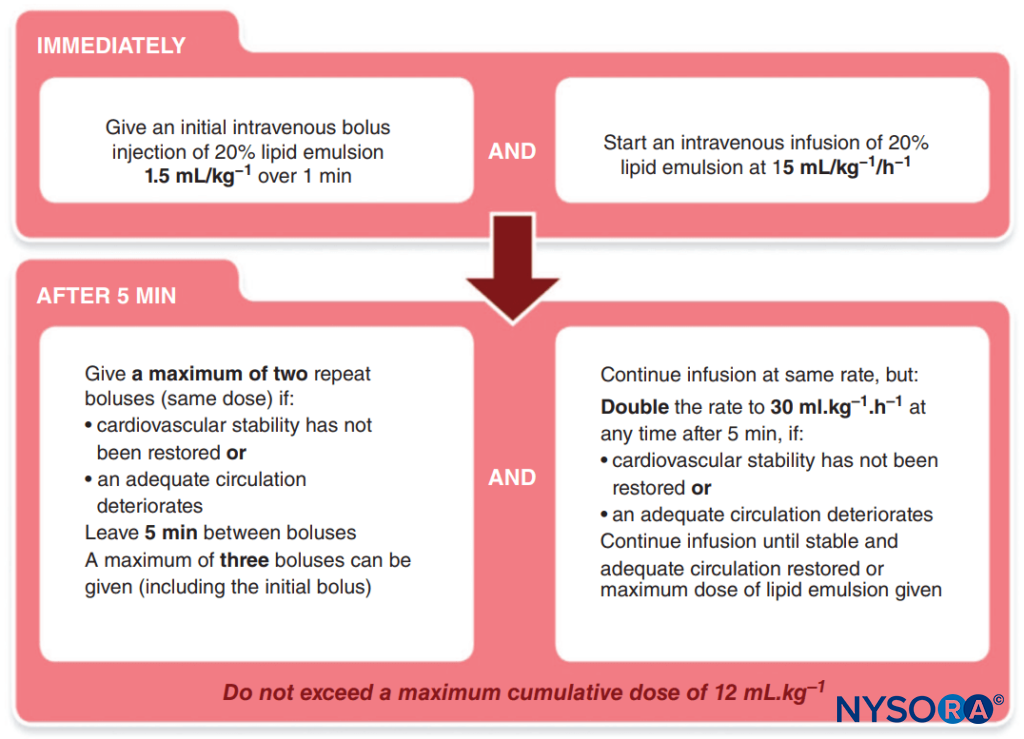
FIGURA 1. Protocollo dell'Associazione degli anestesisti di Gran Bretagna e Irlanda (AAGBI) per la tossicità da anestetico locale.
ANESTESIA TOPICA
È importante discutere l'uso dell'anestesia topica nei bambini perché è comunemente usata nella pratica clinica per fornire analgesia per il posizionamento del catetere endovenoso, la puntura lombare e altre procedure invasive (p. es., la circoncisione nei neonati). Le preparazioni più comuni includono lidocaina, tetracaina, benzocaina e prilocaina. La soluzione anestetica topica permea attraverso la pelle per fornire analgesia. Le tre preparazioni più comuni disponibili includono la miscela eutettica di anestetici locali e locali (EMLA), LMX-4 (soluzione liposomiale di lidocaina al 4%) e Ametop (gel di ametocaina al 4%). EMLA contiene lidocaina e prilocaina e deve essere applicato almeno un'ora prima dell'incannulamento. La sua durata d'azione è di soli 30–60 minuti, anche se può essere lasciata in posa per 4–5 ore. LMX-4 richiede solo 30 minuti per avere effetto e può anche essere lasciato acceso per 4-5 ore. Ametop richiede 45 minuti per avere effetto e deve essere rimosso entro un'ora dall'applicazione; la sua durata d'effetto è fino a 3 ore, poiché si lega alle proteine nello strato corneo. Ametop è vasodilatatore, che può aiutare l'incannulamento. Tuttavia, Ametop può causare eritema ed edema, che possono oscurare le vene.
Consigli NYSORA
Le seguenti sono considerazioni per i bambini sottoposti ad anestesia regionale:
- L'anestesia regionale è per lo più comunemente eseguita con il paziente in anestesia generale.
- La dose di anestetico locale utilizzata è molto inferiore a quella degli adulti ed è calcolata in milligrammi per chilogrammo).
- Utilizzare un anestetico locale alla concentrazione efficace più bassa.
- Se si prevede un dolore moderato o grave, è necessaria un'intensa fisioterapia dopo l'intervento o se è presente una storia di dolore cronico, prendere in considerazione l'utilizzo di una tecnica con catetere.
- Nei bambini sono riportate molte meno complicanze dell'anestesia regionale rispetto agli adulti.
- Ottenere sempre il consenso o il consenso del paziente se il bambino è più grande.
- Spiegare sempre la parestesia postoperatoria ai pazienti.
VALUTAZIONE PREOPERATORIA
La visita preoperatoria è un'opportunità per valutare e preparare il paziente e la famiglia all'intervento chirurgico e alla tecnica anestetica proposti. È importante che l'anestesista comprenda l'intervento chirurgico previsto in modo che possa essere presa la decisione di eseguire una tecnica di anestesia regionale a iniezione singola o continua. In generale, dovrebbe essere scelto il blocco più periferico, poiché questo in genere ha il rischio più basso e il minor numero di effetti collaterali e avrà quindi una maggiore accettabilità sia per il paziente che per i genitori o gli operatori sanitari. Una tecnica di catetere è raccomandata per interventi chirurgici da moderati a maggiori, procedure che richiedono una fisioterapia postoperatoria prolungata e per bambini con dolore cronico. È anche importante garantire che ci sia personale infermieristico formato per gestire le tecniche di anestesia regionale continua.
L'anestesista dovrebbe cercare potenziali controindicazioni (p. es., comorbidità) a una data tecnica di anestesia regionale. Dovrebbe essere presa un'anamnesi completa del dolore, cercando specificamente una storia di dolore cronico o spasticità muscolare. I bambini con bisogni speciali possono essere particolarmente difficili e l'anestesista deve sapere come il bambino affronta ed esprime il dolore. L'esame anestetico preoperatorio standard dovrebbe includere un esame del sito di inserimento del blocco proposto per identificare elementi quali difficoltà anatomiche (p. es., scoliosi) e infezione locale. Nei bambini con malattie neurologiche, deve essere documentato il loro deficit neurologico pre-operatorio. L'anestesista dovrebbe spiegare i vantaggi, gli effetti collaterali e le potenziali complicanze del piano anestetico proposto al bambino e ai genitori/caregiver; è prudente anche discutere un “piano B” in caso di fallimento della tecnica proposta. Dovrebbero essere discusse strategie analgesiche alternative in modo da poter fornire il consenso informato. In particolare, le parestesie postoperatorie della tecnica regionale dovrebbero essere spiegate ai bambini in termini comprensibili, poiché spesso si tratta di un'esperienza che trovano difficile affrontare. Se verrà utilizzata una tecnica di anestesia regionale continua, rassicurare il bambino che la rimozione del catetere non sarà dolorosa. I genitori o gli operatori sanitari in genere forniscono il consenso per una procedura per il loro bambino. Tuttavia, se il bambino ha la capacità cognitiva di discernere il bene dal male, si suggerisce di ottenere anche il consenso del bambino per una tecnica regionale. Si discute su quando o quale possa essere questa età. Se un bambino rifiuta di sottoporsi a una procedura regionale nonostante l'insistenza dei genitori o di chi si prende cura di loro, è importante che l'anestesista fornisca una modalità alternativa di sollievo dal dolore.
Deve essere presa in considerazione la premedicazione analgesica con paracetamolo (paracetamolo) e un farmaco antinfiammatorio non steroideo (FANS), soprattutto quando è noto che il blocco non fornirà un'analgesia totale (p. es., un blocco del piano trasverso dell'addome [TAP] per appendicectomia). Le istruzioni postoperatorie devono essere fornite prima dell'intervento e rafforzate dopo l'intervento al momento della dimissione.
ANESTESIA REGIONALE: SVEGLIO O SONNO?
Se sia meglio che il paziente sia sveglio o addormentato durante l'anestesia regionale è stata una questione controversa negli adulti e questo dibattito un tempo permeava il regno della pratica dell'anestesia regionale pediatrica. Posizionare un blocco regionale in un bambino sveglio è difficile a causa dell'incapacità del bambino di cooperare e dell'incapacità cognitiva del bambino di relazionarsi con sintomi come parestesie o dolore. Pertanto, è meglio fornire al bambino una tecnica regionale in sedazione profonda o dopo l'induzione dell'anestesia generale; questa pratica è da tempo il consenso degli anestesisti pediatrici negli Stati Uniti e all'estero.
Tuttavia, ci sono due scenari in cui le tecniche regionali sveglie vengono utilizzate nei bambini. In primo luogo, si pensava che, evitando l'anestesia generale nei neonati prematuri sottoposti a interventi chirurgici minori, si potesse ridurre l'incidenza dell'apnea postoperatoria. Questo è probabilmente un problema minore ora che i polmoni prematuri neonatali sono meglio protetti e con la disponibilità di nuovi agenti inalatori che forniscono un'emergenza più rapida.
In secondo luogo, il bambino più maturo può essere considerato idoneo per una tecnica regionale in stato di veglia quando viene sottoposto a un intervento chirurgico minore se preferisce o quando un'anestesia generale è considerata troppo rischiosa (p. es., biopsia linfonodale in un adolescente con una massa mediastinica). Per i pazienti più anziani è fondamentale preparare il bambino ei genitori o chi si prende cura di loro per tutta la visita in sala operatoria, non solo per l'inserimento del blocco. L'inserimento del blocco può essere reso più confortevole applicando una crema anestetica topica (EMLA ha la migliore penetrazione) sul sito di iniezione proposto. Durante la visita in sala operatoria, il bambino dovrebbe essere sostenuto e distratto da un'infermiera o da uno specialista del gioco. Il bambino può anche trovare un'utile distrazione nell'uso di un lettore DVD o MP3. Potrebbe essere necessario utilizzare protossido di azoto (Entonox) o dosi ansiolitiche di propofol o remifentanil per facilitare il procedimento. Marhofer et al. hanno dimostrato che nello scenario traumatologico pediatrico, i blocchi del plesso brachiale sono inseriti più comodamente con l'ecografia che con la stimolazione nervosa. Negli ospedali pediatrici, è necessario ricordare al personale di sala operatoria e al chirurgo che il paziente sarà sveglio e che i farmaci e le attrezzature necessarie per passare all'anestesia generale devono essere pronti.
GESTIONE PERIOPERATIVA DEL BLOCCO
Alcune semplici regole devono essere seguite quando si esegue qualsiasi tecnica di anestesia regionale nei bambini. Un assistente qualificato dovrebbe essere sempre presente e questa persona dovrebbe comprendere i principi di base dell'anestesia regionale, in particolare la necessità di aspirare regolarmente prima dell'iniezione, la necessità di avvertire l'anestesista della resistenza all'iniezione. Inoltre, l'assistente dovrebbe essere in grado di apportare modifiche di base allo stimolatore del nervo periferico (SNP) e alle macchine ecografiche.
Il bambino deve disporre di vie aeree sicure, accesso endovenoso e monitoraggio completo prima di iniziare il blocco. Nell'ambito della checklist per la sicurezza chirurgica dell'Organizzazione mondiale della sanità (OMS), il consenso e il lato dell'intervento chirurgico vengono controllati e, appena prima dell'inserimento del blocco, il sito deve essere nuovamente confermato con l'assistente dell'anestesista.
Il bambino, la macchina ecografica (se utilizzata), l'attrezzatura e l'anestesista devono essere posizionati in modo ergonomico.
C'è un certo dibattito sugli standard minimi per l'asepsi per l'anestesia regionale. Per le tecniche a iniezione singola è sufficiente strofinarsi le mani, indossare guanti sterili, applicare una soluzione alcolica sulla pelle del paziente e coprire la sonda ecografica. Per le tecniche con catetere, si consiglia una tecnica asettica più rigorosa. Quando si esegue qualsiasi tecnica di catetere, è utile quando si drappeggia il bambino per avere un'ampia area anatomica visibile; ciò consente all'anestesista spazio sufficiente per eseguire una mappatura/scansione esplorativa e anche una migliore visione, e quindi apprezzamento, dell'anatomia del paziente (particolarmente importante quando si posiziona l'epidurale nei bambini con scoliosi). Può essere utile eseguire il tunneling del catetere, poiché ciò facilita la fissazione e, in alcuni casi, può ridurre il rischio di infezione (p. es., con un catetere caudale, il catetere può essere incanalato lontano dall'area del pannolino.
Non esiste una dose di prova ideale; pertanto, si suggerisce un'aspirazione ripetuta e frequente durante l'iniezione. Quando non si prevede che il blocco copra tutti gli aspetti del dolore chirurgico (p. es., un blocco della guaina del retto per la piloromiotomia), si deve prendere in considerazione la somministrazione di paracetamolo per via endovenosa e/o di un FANS per retto per aiutare l'analgesia. Altri adiuvanti possono rivelarsi utili (p. es., il solfato di magnesio intraoperatorio 50 mg/kg può ridurre gli spasmi muscolari postoperatori nei pazienti con paralisi cerebrale infantile sottoposti a chirurgia degli arti inferiori).
È opinione dell'autore che, ove possibile, l'efficacia della tecnica di anestesia regionale non debba essere oscurata dalla somministrazione di oppioidi o di protossido di azoto. È importante nella valutazione intraoperatoria del blocco che eventuali variazioni della frequenza cardiaca e della pressione sanguigna siano annotate e correlate allo specifico intervento chirurgico in quel momento. Ciò consente la pianificazione dei blocchi di soccorso al termine della procedura. Anche con blocchi riusciti, possono verificarsi risposte cardiovascolari occasionali a stimoli chirurgici, poiché i blocchi vengono generalmente eseguiti utilizzando una concentrazione inferiore di anestetico locale (p. es., 0.25% levobupivacaina) e, se si utilizza un laccio emostatico, un aumento graduale della frequenza cardiaca e la pressione sanguigna si verificherà dopo i primi 30-40 minuti.
Il grado di stabilità cardiovascolare intraoperatoria aiuta l'anestesista a decidere se l'eventuale sofferenza del paziente durante la prima fase del recupero è dovuta al dolore o ad un'altra causa (p. es., delirio di emergenza). sconvolto, allora si dovrebbe presumere che il paziente stia soffrendo, e questo dovrebbe essere affrontato rapidamente somministrando un oppiaceo ad azione rapida (p. es., fentanil).
CURA POSTOPERATORIA
I consigli postoperatori relativi alla protezione dell'area anestetizzata devono essere forniti verbalmente prima dell'intervento e ripetuti dopo l'intervento e devono essere fornite anche istruzioni scritte alla famiglia. La famiglia e il bambino dovrebbero essere avvertiti della debolezza muscolare e della diminuzione della sensibilità. Le imbracature devono essere fornite ai pazienti pediatrici con blocchi degli arti superiori. I bambini ambulatoriali con blocchi degli arti inferiori dovrebbero avere i mezzi per mobilitarsi e tornare a casa organizzati. Ogni istituto deve disporre di linee guida per l'assistenza infermieristica ospedaliera e il monitoraggio delle tecniche di anestesia regionale e il personale deve ricevere una formazione regolare sulla gestione dei blocchi regionali nel postoperatorio e sulla cura dell'estremità anestetizzata. In genere è più economico e sicuro collocare i pazienti che ricevono anestesia regionale e analgesia in reparti specifici. (Per ulteriori informazioni su questo argomento, vedere Gestione del dolore acuto e cronico nei bambini.)
FORMAZIONE
La formazione degli anestesisti in anestesia e anatomia regionale pediatrica è essenziale per la sua attuazione sicura e di successo. Ove possibile, ogni dipartimento dovrebbe fornire un approccio strutturato all'insegnamento dei blocchi semplici comuni: guaina caudale, peniena, femorale, ascellare, ileo-inguinale e del retto. La formazione dovrebbe includere le tecniche di scansione e agugliatura degli Stati Uniti. Una volta che le abilità di base dell'agugliatura negli Stati Uniti sono state apprese sui fantasmi e le abilità di scansione sviluppate su volontari adulti, queste abilità possono quindi essere trasferite al contesto clinico. In genere, queste tecniche sono più facili e più sicure eseguite prima sui pazienti più anziani.
Consigli NYSORA
Ove possibile, ogni dipartimento dovrebbe fornire un approccio strutturato all'insegnamento dei blocchi comuni: guaina caudale, peniena, femorale, ascellare, ileo-inguinale e del retto.
SOMMARIO
L'anestesia regionale migliora l'esperienza postoperatoria sia dei bambini che dei genitori o degli operatori sanitari e facilita l'uso efficiente delle strutture ospedaliere e si prevede che l'uso dell'anestesia regionale nei bambini continuerà a crescere in popolarità. Le tecniche di anestesia regionale dovrebbero fornire il corretto equilibrio tra rischi e benefici per i bambini e la chirurgia di oggi. Gli Stati Uniti stanno consentendo a una gamma più ampia di blocchi periferici di essere utilizzati in modo più sicuro e affidabile nei bambini. La tecnologia è importante, ma non sostituisce una solida comprensione dell'anatomia e un elevato standard di pratica generale sicura.
BIBLIOGRAFIA
- Giaufre E, Dalens B, Gombert A: Epidemiologia e morbilità dell'anestesia regionale nei bambini: un'indagine prospettica di un anno della Società di anestesisti pediatrici di lingua francese. Anesth Analg 1996;83:904–912.
- Ecoffey C, Lacroix F, Giaufre E et al: Epidemiologia e morbilità dell'anestesia regionale nei bambini: un'indagine prospettica di follow-up di un anno della Società di anestesiologi pediatrici di lingua francese (ADARPEF). Pediatr Anesth 2010;20:1061–1069.
- Taddio A, Katz J, Ilersich AL, Koren G: Effetto della circoncisione neonatale sulla risposta al dolore durante la successiva vaccinazione di routine [vedi commenti]. Lancetta 1997;349:599–503.
- Peutrell JM, Mather SJ: Anestesia regionale nei neonati e nei bambini. Oxford: Oxford University Press, 1997.
- Suresh S, Wheeler M: Pratica anestesia regionale pediatrica. Anesthesiol Clin North Am 2002;20:83–113.
- Fitzgerald M, Walker SM: Gestione del dolore infantile: un approccio neurobiologico dello sviluppo. Nat Clin Pract Neurol 2009;5:35–50.
- Mazoit JX, Dalens BJ: farmacocinetica degli anestetici locali nei neonati e nei bambini. Clin Pharmacokinet 2004;43:17–32.
- Besunder JB, Reed MD, Blumer JL: Principi di biodisposizione dei farmaci nel neonato. Una valutazione critica dell'interfaccia farmacocinetica-farmacodinamica (Parte I). Clin Pharmacokinet 1988;14: 189–216.
- Besunder JB, Reed MD, Blumer JL: Principi di biodisposizione dei farmaci nel neonato. Una valutazione critica dell'interfaccia farmacocinetica-farmacodinamica (Parte II). Clin Pharmacokinet 1988;14: 261–286.
- Mazoit JX, Denson DD, Samii K: farmacocinetica della bupivacaina dopo l'anestesia caudale nei bambini. Anestesiologia 1988;68:387–391.
- Ecoffey C, Desparmet J, Maury M, et al: Bupivacaina nei bambini: farmacocinetica dopo anestesia caudale. Anestesiologia 1985;63: 447–448.
- Murat I, Montay G, Delleur MM, et al: farmacocinetica della bupivacaina durante l'anestesia epidurale nei bambini. Eur J Anaesthesiol 1988;5: 113–120.
- Berde CB: Tossicità degli anestetici locali nei neonati e nei bambini. [Revisione]. J Pediatr 1993;122(Pt 2):S14–S20.
- Petitjeans F, Mion G, Puidupin M, et al: Tachicardia e convulsioni indotte dall'iniezione accidentale di ropivacaina intravascolare durante il blocco sciatico. Acta Anaesthesiol Scand 2002;46:616–617.
- Ivani G, Mereto N, Lampugnani E, et al: Ropivacaina in chirurgia pediatrica: risultati preliminari. Paediatr Anaesth 1998;8:127–129.
- Ivani G, Mazzarello G, Lampugnani E, DeNegri P, Torre M, Lonnqvist PA: Ropivacaine per blocchi centrali nei bambini. Anestesia 1998;53 (Suppl 2): 74–76.
- Ala-Kokko TI, Partanen A, Karinen J, et al: farmacocinetica dello 0.2% di ropivacaina e dello 0.2% di bupivacaina dopo i blocchi caudali nei bambini. Acta Anaesthesiol Scand 2000;44:1099–1102.
- Dalens B, Ecoffey C, Joly A, et al: farmacocinetica ed effetto analgesico della ropivacaina dopo il blocco del nervo ileoinguinale/ileoipogastrico nei bambini. Paediatr Anaesth 2001;11:415–420.
- Fernandez-Guisasola J, Andueza A, Burgos E, et al: un confronto tra lo 0.5% di ropivacaina e l'1% di mepivacaina per il blocco del nervo sciatico nella fossa poplitea. Acta Anaesthesiol Scand 2001;45:967–970.
- Ivani G, DeNegri P, Lonnqvist PA, et al: un confronto di tre diverse concentrazioni di levobupivacaina per il blocco caudale nei bambini (tabella). Anesth Analg 2003;97:368–371.
- Lerman J, Nolan J, Eyres R, et al: Efficacia, sicurezza e farmacocinetica della levobupivacaina con e senza fentanil dopo infusione epidurale continua nei bambini: uno studio multicentrico. Anestesiologia 2003;99: 1166–1174.
- Ala-Kokko TI, Raiha E, Karinen J, et al: farmacocinetica dello 0.5% di levobupivacaina dopo il blocco del nervo ileo-inguinale-ileoipogastrico nei bambini. Acta Anaesthesiol Scand 2005;49:397–400.
- Foster RH, Markham A: Levobupivacaina: una revisione della sua farmacologia e uso come anestetico locale. Droghe 2000;59:551–579.
- Mather LE, Huang YF, Veering B, Pryor ME: farmacocinetica sistemica e regionale degli enantiomeri di levobupivacaina e bupivacaina negli ovini. Anesth Analg 1998;86:805–811.
- Tobias JD, O'Dell N: Cloroprocaina per l'anestesia epidurale nei neonati e nei bambini. AANA J 1995;63:131–135.
- Raj PP, Ohlweiler D, Hitt BA, Denson DD: Cinetica degli esteri anestetici locali e effetti dei farmaci adiuvanti sull'idrolisi della 2-cloroprocaina. Anestesiologia 1980;53:307–314.
- Tobias JD, Rasmussen GE, Holcomb GW III, et al: Anestesia caudale continua con cloroprocaina in aggiunta all'anestesia generale nei neonati. Can J Anaesth 1996;43:69–72.
- Crowhust JA: Deficit di colinesterasi. Terapia intensiva di Anaesth 1983; 11:7–9.
- Kuhnert BR, Philipson EH, Pimental R, Kuhnert PM: un blocco epidurale prolungato con cloroprocaina in un paziente postpartum con pseudocolinesterasi anormale. Anestesiologia 1982;56:477–478.
- Monedero P, Hess P: blocco epidurale elevato con cloroprocaina in una partoriente con bassa attività pseudocolinesterasica. Can J Anaesth 2001;48:318–319.
- Kuhnert BR, Kuhnert PM, Prochaska AL, Gross TL: Livelli plasmatici di 2-cloroprocaina nei pazienti ostetrici e nei loro neonati dopo anestesia epidurale. Anestesiologia 1980;53:21–25.
- Henderson K, Sethna NF, Berde CB: Anestesia caudale continua per la riparazione dell'ernia inguinale negli ex neonati pretermine. J Clin Anesth 1993;5: 129–133.
- Krane EJ, Haberkern CM, Jacobson LE: apnea postoperatoria, bradicardia e desaturazione di ossigeno in neonati prematuri: confronto prospettico di anestesia spinale e generale. Anesth Analg 1995;80: 7–13.
- Henderson K, Sethna NF, Berde CB: Anestesia caudale continua per la riparazione dell'ernia inguinale negli ex neonati pretermine. J Clin Anesth 1993;5:129–133.
- Suresh S, Cote CJ: anestetici locali per neonati e bambini. In Yaffe SJ, Aranda JV (a cura di): farmacologia neonatale e pediatrica, principi terapeutici in pratica, 3a ed. Filadelfia: Lippincott Williams & Wilkins, 2004.
- Frumiento C, Abajian JC, Vane DW: Anestesia spinale per neonati pretermine sottoposti a riparazione dell'ernia inguinale. Arch Surg 2000;135:445–451.
- Kasten GW, Martin ST: Tossicità cardiovascolare della bupivacaina: confronto del trattamento con bretilio e lidocaina. Anesth Analg 1985;64:911–916.
- Murat I, Esteve C, Montay G, et al: farmacocinetica ed effetti cardiovascolari della bupivacaina durante l'anestesia epidurale nei bambini con distrofia muscolare di Duchenne. Anestesiologia 1987;67:249–252.
- Graf BM: La cardiotossicità degli anestetici locali: il posto della ropivacaina. Curr Top Med Chem 2001;1:207–214.
- Bergman BD, Hebl JR, Kent J, Horlocker TT: complicazioni neurologiche di 405 cateteri ascellari continui consecutivi (tabella). Anesth Analg 2003;96:247–252.
- Berde CB: Convulsioni associate all'anestesia regionale pediatrica [commento editoriale] [vedi commenti]. Anesth Analg 1992;75:164–166.
- Weintraud M, Lundblad M, Kettner SC et al: Ultrasuoni rispetto alla tecnica basata sul punto di riferimento per il blocco del nervo ileoinguinale-ileoipogastrico nei bambini: le implicazioni sui livelli plasmatici della ropivacaina. Anesth Analg 2009;108:1488–1492.
- Ludot H, Tharin JY, Belouadah M, et al: Rianimazione riuscita dopo aritmia vebtricolare indotta da ropivacaina e lidocaina a seguito di blocco del plesso lombare posteriore in un bambino. Anesth Analg 2008;106: 1572–1574.
- Acharya AB, Bustani PC, Phillips JD, et al: studio controllato randomizzato di miscela eutettica di crema anestetica locale per prelievo venoso in neonati pretermine sani. Arch Dis Child fetale neonatale Ed 1998;78:F138–F142.
- Benini F, Johnston CC, Faucher D, Aranda JV: Anestesia topica durante la circoncisione nei neonati. JAMA 1993;270:850–853.
- Gourrier E, Karoubi P, el Hanache A, et al: Uso della crema EMLA in un reparto di neonatologia. Dolore 1996;68:431–434.
- Eichenfield LF, Funk A, Fallon-Friedlander S, Cunningham BB: uno studio clinico per valutare l'efficacia di ELA-Max (4% di lidocaina liposomiale) rispetto alla miscela eutettica di crema anestetica locale per la riduzione del dolore della venipuntura nei bambini. Pediatria 2002;109:1093–1099.
- Jain A, Rutter N: Gel topico di ametocaina nel neonato: quanto tempo funziona e quanto dura? Arch Dis Child Fetale Neonatale Ed 2000:83:F211–214.
- Tait AR, Voepel-Lewis T, Malviya S: Capiscono? (Parte II): consenso dei bambini che partecipano alla ricerca clinica in anestesia e chirurgia. Anestesiologia 2003;98:609–614.
- Krane EJ, Dalens BJ, Murat I, Murrell D: La sicurezza delle epidurali posizionate durante l'anestesia generale. Reg Anesth Antidolorifico 1998;23:433–438.
- Marhofer P, Sitzwohl C, GreherM, Kapral S: guida ecografica per l'anestesia del plesso brachiale infraclavicolare nei bambini. Anestesia 2004;59:642–646.

