INTRODUCTION
Les nerfs intercostaux (NIC) innervent les principales parties de la peau et de la musculature de la paroi thoracique et abdominale. Le bloc de ces nerfs a été décrit pour la première fois par Braun en 1907 dans le manuel Die Lokalanastesie. Dans les années 1940, les cliniciens ont remarqué que les blocs nerveux intercostaux (ICNB) pouvaient réduire les complications pulmonaires et les besoins en opioïdes après une chirurgie abdominale haute. En 1981, l'ICNB continu a été introduit pour surmonter les problèmes associés aux injections multiples répétées. Aujourd'hui, l'ICNB est utilisé dans une variété de conditions de douleur aiguë et chronique affectant le thorax et le haut de l'abdomen, y compris la chirurgie du sein et de la paroi thoracique. L'introduction du guidage échographique dans la pratique de l'anesthésie régionale facilite encore sa pratique. Les inconvénients du bloc intercostal incluent cependant la nécessité d'une expertise technique, les risques de pneumothorax et toxicité anesthésique locale avec plusieurs niveaux de bloc.
INDICATIONS
L'ICNB fournit une excellente analgésie chez les patients souffrant de fractures des côtes et pour les douleurs post-chirurgicales après une chirurgie thoracique et abdominale supérieure telle qu'une thoracotomie, une thoracostomie, une mastectomie, une gastrostomie et une cholécystectomie. Les paramètres respiratoires montrent généralement des améliorations impressionnantes sur le soulagement de la douleur. bloc des deux dermatomes au-dessus et des deux au-dessous du niveau de l'incision chirurgicale est nécessaire. ICNB ne bloque pas les douleurs abdominales viscérales, pour lesquelles un bloc du plexus coeliaque est nécessaire. L'ICNB neurolytique est utilisé pour gérer les douleurs chroniques telles que la douleur postmastectomie (T2) et la douleur postthoracotomie.
CONTRE-INDICATIONS
- Troubles de coagulation, bien que ce ne soit pas une contre-indication absolue
- Fournisseurs infection, manque d'expertise et de matériel de réanimation
ANATOMIE FONCTIONNELLE
Lorsque les nerfs thoraciques T1 à T12 émergent de leurs foramens intervertébraux respectifs, ils se divisent en rameaux suivants (Figure 1):
- Les rameaux communicants antérieurs gris et blancs appariés, qui passent en avant du ganglion et de la chaîne sympathiques.
- La branche cutanée postérieure, innervant la peau et les muscles de la région paravertébrale.
- La branche ventrale (ICN, l'objet principal de ce chapitre).
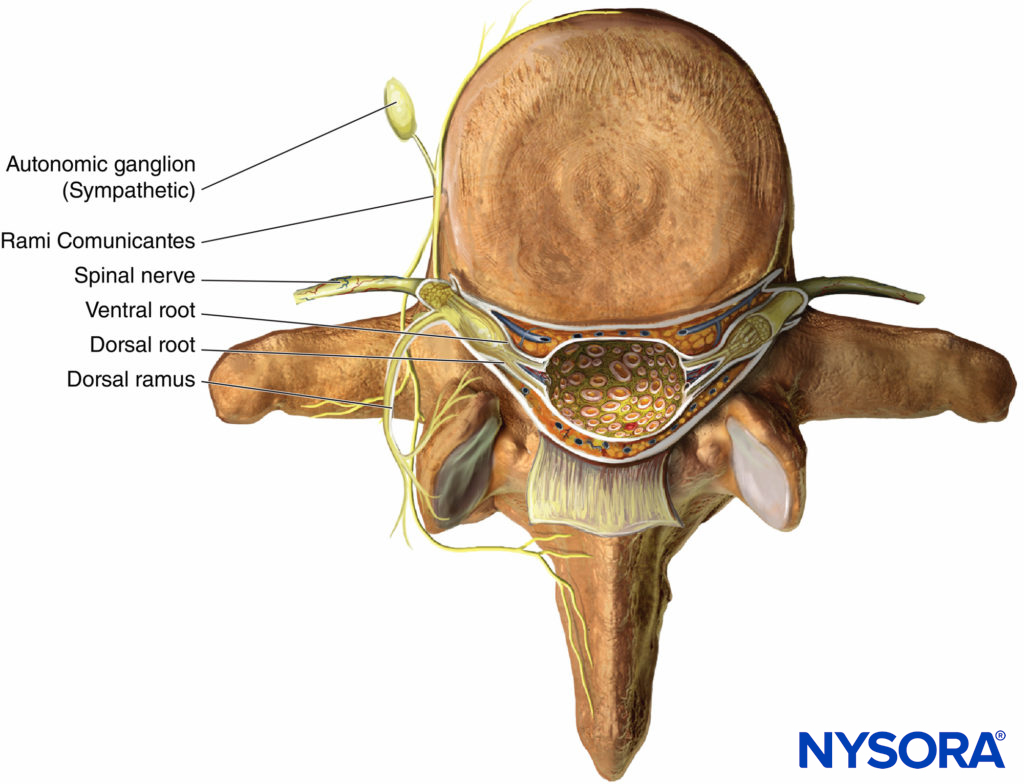
Figure 1. Anatomie du nerf spinal.
T1 et T2 envoient des fibres nerveuses aux membres supérieurs et au haut du thorax, T3 à T6 alimentent le thorax, T7 à T11 alimentent le bas du thorax et l'abdomen, et T12 innerve la paroi abdominale et la peau de la partie avant de la région fessière (Figure 2).
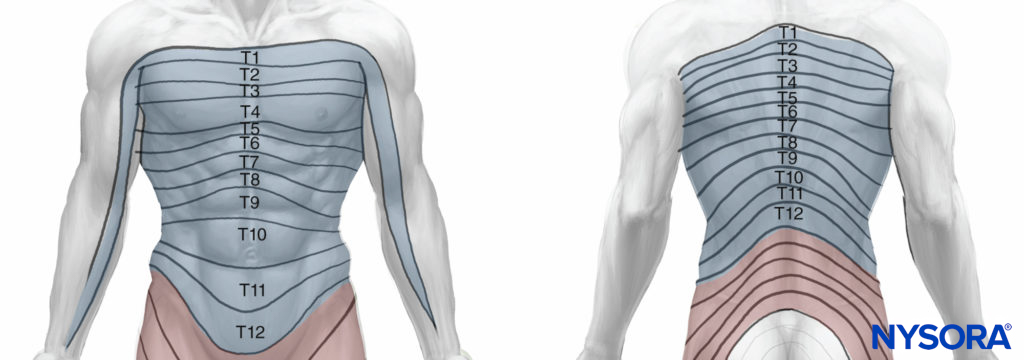
Figure 2. Distribution dermatomique des nerfs intercostaux.
Portant à la fois des fibres sensorielles et motrices, l'ICN perce la membrane intercostale postérieure à environ 3 cm (chez les adultes) en aval du foramen intervertébral pour pénétrer dans le bosquet sous-costal où il continue, pour la plupart, à courir parallèlement à la côte, bien que les branches puissent se trouvent souvent n'importe où entre les côtes adjacentes. Son parcours dans le thorax est pris en sandwich entre la plèvre pariétale et les muscles intercostaux les plus internes (intercostalis intimus) et les muscles intercostaux externes et internes (Chiffres 3 surélevées que pour les 4). Juste en avant de la ligne médio-axillaire, il donne la branche cutanée latérale. Lorsque l'ICN s'approche de la ligne médiane, il tourne vers l'avant et perce les muscles et la peau sus-jacents pour se terminer par la branche cutanée antérieure.
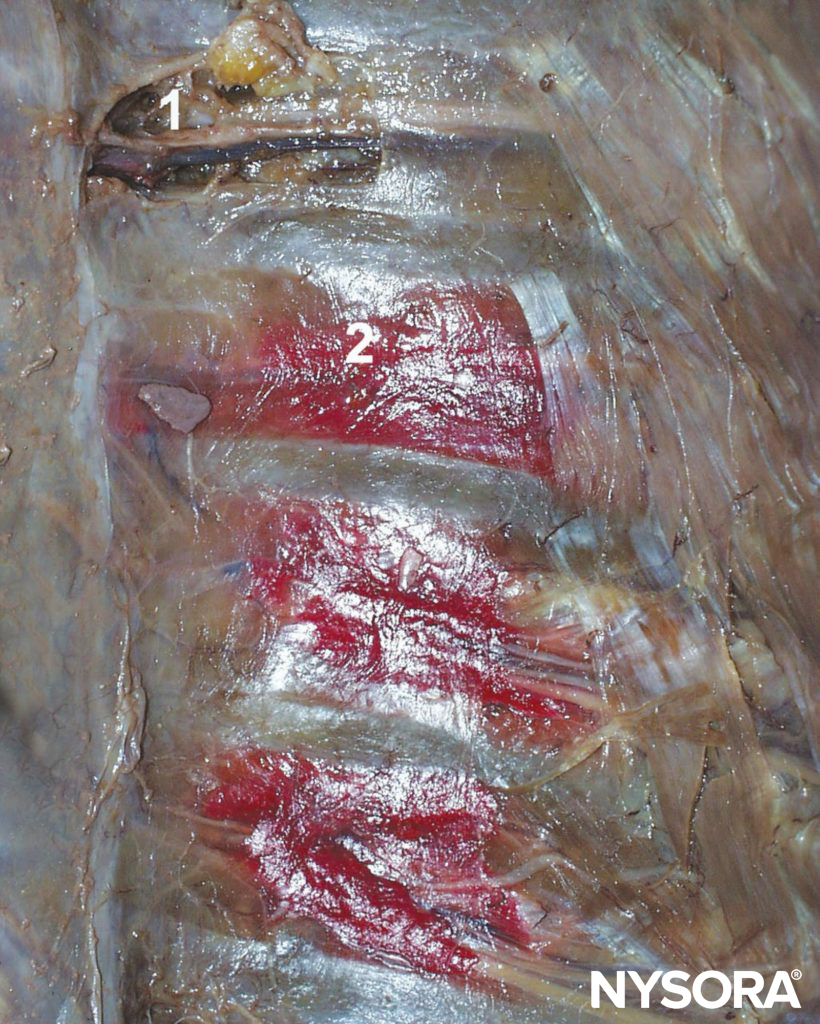
Figure 3 Nerfs intercostaux (accompagnés d'une artère et d'une veine intercostales) représentés dans le sillon intercostal vus de l'intérieur de la cavité thoracique ouverte d'un cadavre. Le colorant rouge illustre la propagation des solutions injectées dans le sillon intercostal pendant le bloc intercostal. 1. Nerf intercostal. 2. Distribution du colorant après injection dans le sillon intracostal.
Cependant, il existe de nombreuses variantes anatomiques. Le premier nerf thoracique (T1) n'a pas de branche cutanée antérieure, n'a généralement pas de branche cutanée latérale, et la plupart de ses fibres quittent l'espace intercostal en traversant le col de la première côte pour rejoindre celles de C8, tandis qu'un faisceau plus petit continue sur un véritable trajet intercostal pour alimenter les muscles de l'espace intercostal. Certaines fibres de T2 et T3 donnent naissance au nerf intercostobrachial, qui innerve l'aisselle et la peau de la face médiale de la partie supérieure du bras jusqu'au coude. De plus, la branche ventrale de T12 est similaire aux autres RIC mais est appelée nerf sous-costal car elle n'est pas positionnée entre deux côtes.
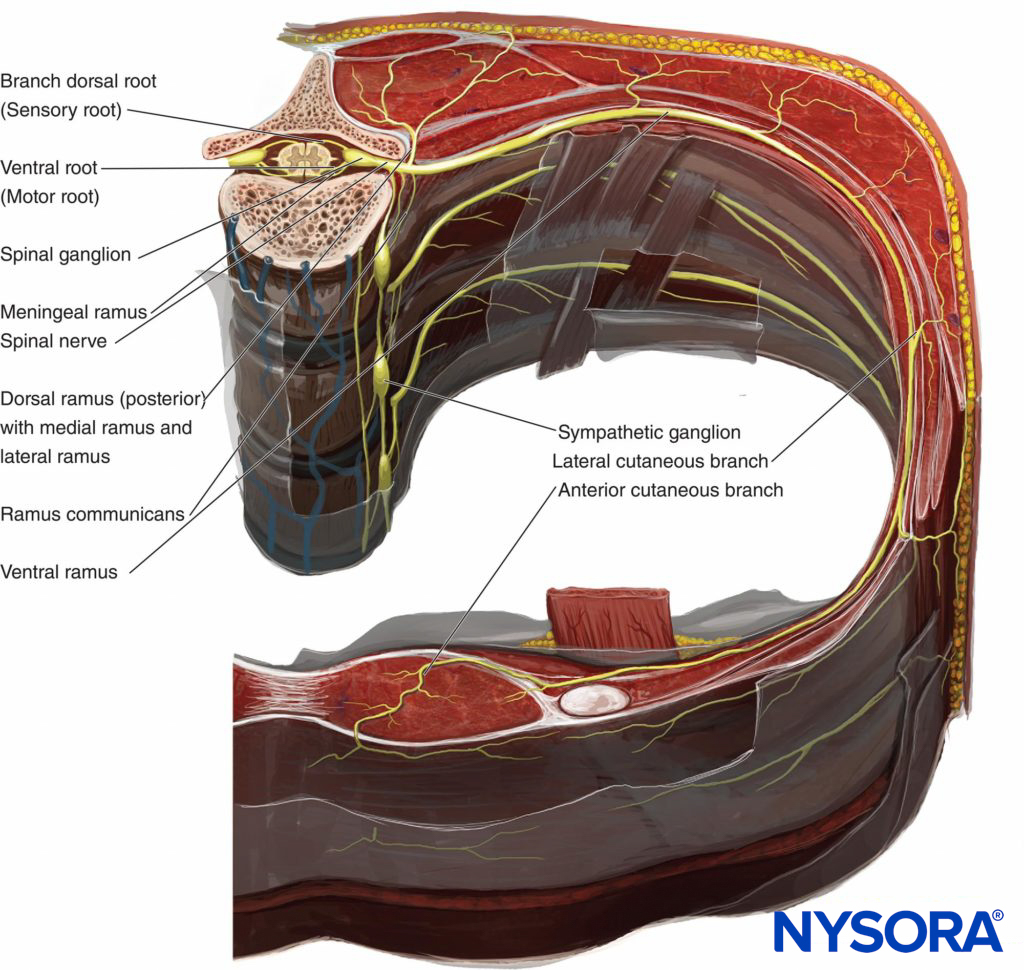
Figure 4. Anatomie du nerf intercostal.
Branche cutanée latérale
Les branches cutanées latérales de T2 à T11 traversent obliquement les muscles intercostaux internes et externes avant de se diviser en branches antérieure et postérieure (voir Figure 4). Ces branches alimentent les muscles et la peau du torse latéral. L'alimentation des branches antérieures de T7-T11 innerve la peau aussi loin en avant que le bord latéral du rectus abdominis. Les branches postérieures de T7-T11 alimentent la peau recouvrant le grand dorsal. La branche cutanée latérale de T12 ne se divise pas. La majeure partie de la branche ventrale de T12 rejoint celle de L1 pour former les nerfs iliohypogastrique, ilio-inguinal et génito-fémoral ; le reste perce le muscle abdominal transverse (TAM) pour se déplacer entre le TAM et le muscle oblique interne.
Branche cutanée antérieure
Les branches cutanées antérieures de T2 à T6 traversent les intercostaux externes et les muscles grands pectoraux pour pénétrer dans l'aponévrose superficielle près du bord latéral du sternum pour irriguer la peau de la partie antérieure du thorax près de la ligne médiane et légèrement au-delà (voir Figure 4). Des branches plus petites (T1 à T6) existent pour alimenter les muscles intercostaux et la plèvre pariétale, et ces branches peuvent traverser les espaces intercostaux adjacents. Les branches cutanées antérieures de T7 à T12 traversent la gaine du muscle droit postérieur pour fournir les nerfs moteurs au muscle droit et les fibres sensorielles à la peau de la paroi abdominale antérieure. Certaines branches finales de T7 à T12 continuent vers l'avant et, avec L1, innervent le péritoine pariétal de la paroi abdominale. Leur trajet antérieur se poursuit et devient superficiel près de la linea alba pour assurer l'innervation cutanée jusqu'à la ligne médiane de l'abdomen et quelques centimètres au-delà. Pour plus d'informations, voir Anatomie fonctionnelle de l'anesthésie régionale.
MÉCANISME DE BLOCAGE ET DISTRIBUTION DE L'ANESTHÉSIE
L'ICNB bloque les fibres sensorielles et motrices homolatérales des ICN. La solution anesthésique locale injectée dans le sillon sous-costal se répand à la fois distalement et proximalement ; une partie de l'injectat peut également pénétrer dans l'espace paravertébral. (voir Figure 3).
TECHNIQUE
Une ligne intraveineuse doit être installée et des médicaments de réanimation doivent être facilement disponibles. La sédation et l'analgésie sont toujours utilisées à bon escient. L'ICNB peut être réalisée chez un patient anesthésié, bien que anesthésie rachidienne a été rapporté chez des patients lorsque l'ICNB a été réalisée sous anesthésie générale, et il est à craindre que le risque de pneumothorax puisse être augmenté chez un patient sous ventilation à pression positive. Après le bloc, le patient doit être surveillé pour d'éventuelles complications, en particulier un pneumothorax retardé, toxicité anesthésique locale, ecchymose, et survenue d'une rachianesthésie (rare).
L'ICN peut être bloqué n'importe où en amont de la ligne médio-axillaire, là où la branche cutanée latérale prend son essor. Chez l'enfant, le bloc est couramment réalisé au niveau de la ligne axillaire postérieure ou, alternativement, juste latéralement aux muscles paraspinaux, à l'angle de la côte. Chez les adultes, le site le plus courant d'ICNB se situe à l'angle de la côte (à 6–8 cm des apophyses épineuses; Figure 5). A l'angle de la côte, la côte est relativement superficielle et facile à palper, et le sillon sous-costal est le plus large. Le nerf est inférieur à l'artère intercostale postérieure, qui est inférieure à la veine intercostale (Figure 6) (mnémonique : VAN [veine/artère/nerf]). Les VAN sont entourés de tissu adipeux et sont pris en sandwich entre les muscles intercostaux internes et intercostaux internes (intercostalis intimus). Le nerf fonctionne souvent sous la forme de trois ou quatre faisceaux séparés, sans gaine endoneurale enveloppante, ce qui le rend facilement accessible au blocage. Le blocage des nerfs intercostaux en dedans de l'angle de la côte n'est pas recommandé car les nerfs se trouvent profondément dans la membrane intercostale postérieure avec très peu de tissu entre celle-ci et la plèvre pariétale, et le muscle sacro-épineux sus-jacent rend la palpation des côtes difficile. En revanche, le bloc en aval de la ligne axillaire antérieure est plus difficile car le nerf a quitté le sillon sous-costal et est rentré dans l'espace intercostal et se situe dans la substance du muscle intercostal interne.
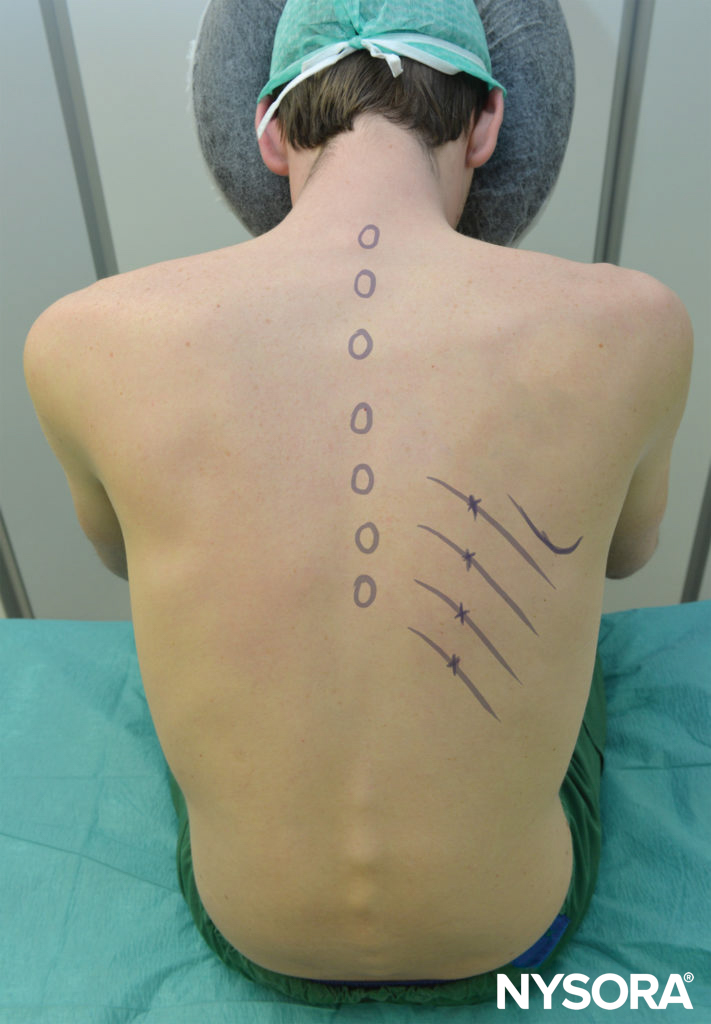
Figure 5. Le patient assis doit se pencher légèrement vers l'avant et être soutenu. Les bras doivent tirer les omoplates latéralement pour faciliter l'accès aux angles postérieurs des côtes au-dessus de T7. Les bords inférieurs des côtes à bloquer sont marqués juste latéralement au bord latéral du groupe musculaire sacrospinal (paraspineux), correspondant aux angles des côtes. Les points d'entrée de l'aiguille sont marqués à 6–8 cm de la ligne médiane chez la plupart des adultes.
L'ICNB peut être réalisée avec le patient en position ventrale, assise ou latérale (côté bloc vers le haut). En position couchée, un oreiller doit être placé sous le haut de l'abdomen du patient et les bras peuvent pendre sur les côtés. Le patient assis doit se pencher légèrement en avant en tenant un oreiller et être soutenu. Les bras doivent être en avant. La position du bras dans l'une ou l'autre position est de tirer les omoplates latéralement et de faciliter l'accès aux angles postérieurs des côtes au-dessus de T7 (voir Figure 5). Dans des conditions aseptiques, les sites de blocs sont identifiés.
Conseils NYSORA
- Les côtes peuvent être comptées à partir de la douzième côte, ou à partir de la septième côte (pointe inférieure de l'omoplate).
- Les bords inférieurs des côtes à bloquer sont marqués juste en dehors du bord latéral du groupe musculaire sacrospinal (paraspineux) (habituellement à 6–8 cm de la ligne médiane au niveau des côtes inférieures et à 4–7 cm de la ligne médiane au niveau du côtes supérieures), correspondant aux angles des côtes.
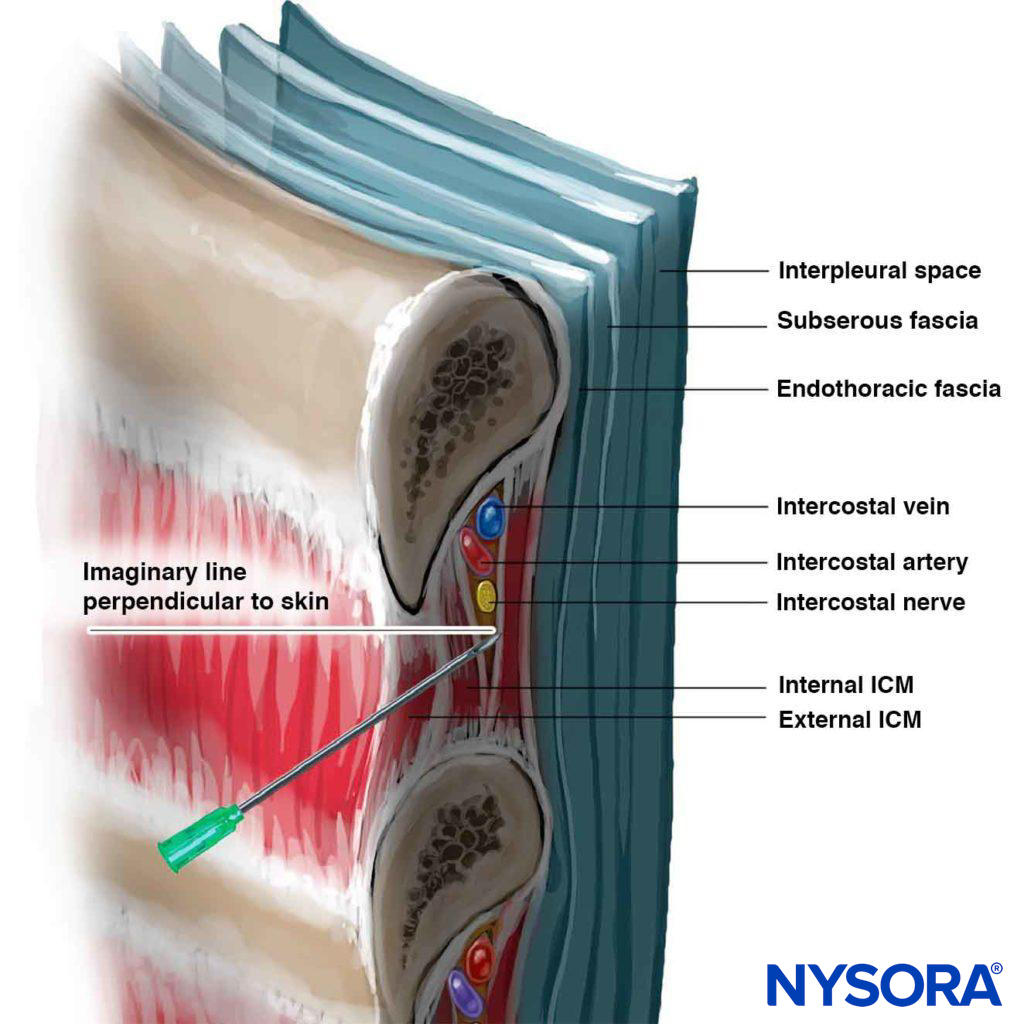
Figure 6. Angle d'aiguille requis pour entrer dans le sillon intercostal. Notez la relation entre les vaisseaux intercostaux et le nerf.
Les bords inférieurs des côtes à bloquer sont palpés et marqués (voir Figure 5). Les sites d'entrée de l'aiguille sont infiltrés avec de la lidocaïne 1 % à 2 %. Un site d'entrée est bien placé lorsqu'une aiguille y est introduite à 20 degrés céphalique (plan sagittal ; voir Figure 6) gratte sous le bord inférieur de la côte et atteint le sillon sous-costal. La peau est d'abord tirée vers le haut avec la main qui palpe d'environ 1 cm, et une aiguille de 4 à 5 cm, de calibre 22 à 24 (pour une injection unique) est introduite à travers le site d'entrée choisi à un angle de 20 degrés. angle céphalique avec le biseau face à la tête. L'aiguille est avancée jusqu'à ce qu'elle entre en contact avec la côte à une profondeur inférieure à 1 cm chez la plupart des patients. Une petite quantité d'anesthésique local peut être injectée pour anesthésier le périoste. Avec la main palpatrice tenant fermement l'aiguille et reposant solidement sur le dos du patient, la main d'injection "marche" doucement l'aiguille caudalement tandis que la peau est autorisée à se déplacer vers l'arrière sur la côte (Figure 7).
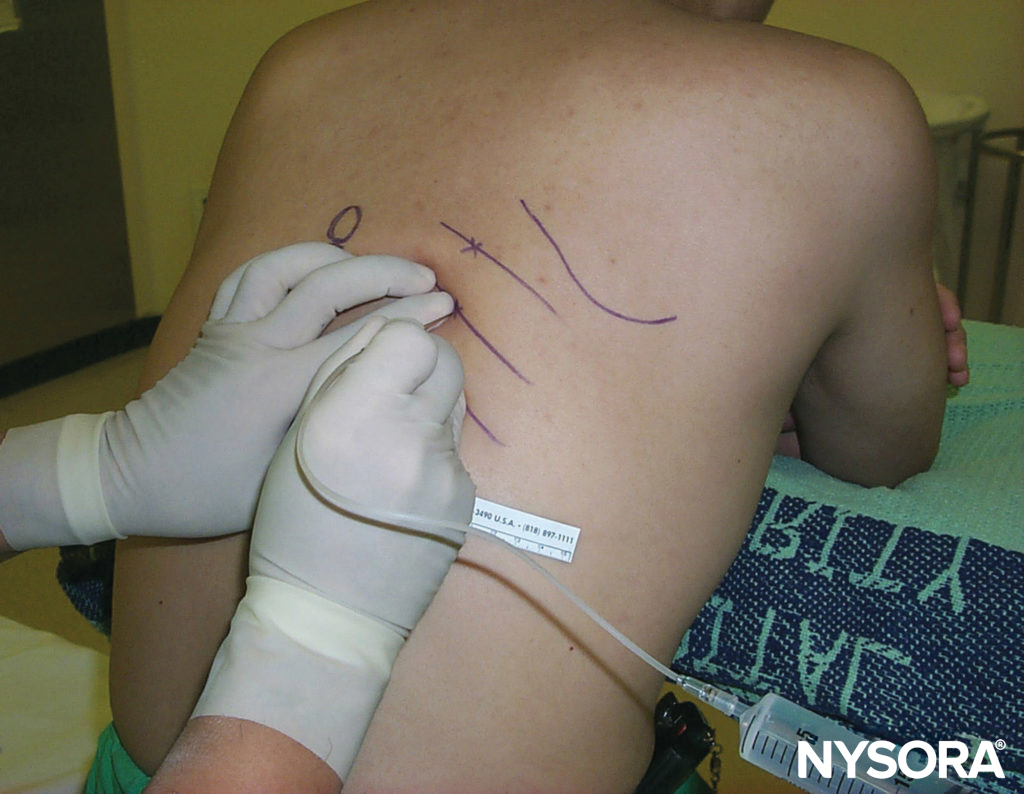
Figure 7. Avec la main palpatrice tenant fermement l'aiguille et reposant solidement sur le dos du patient pour contrôler l'avancement de l'aiguille, la main d'injection "marche" doucement l'aiguille caudalement tandis que la peau est autorisée à reculer sur la côte.
L'aiguille est maintenant avancée de quelques mm, tout en maintenant l'angle d'inclinaison céphalique de 20 degrés (même un léger angle de pointage caudé par l'aiguille réduit considérablement les chances de succès). Un subtil « donner » ou « éclater » du fascia du muscle intercostal interne peut être ressenti, surtout si une aiguille à biseau court est utilisée. Comme la distance moyenne entre la face postérieure de la côte et la plèvre est en moyenne de 8 mm, l'avancement de l'aiguille bien au-delà de quelques mm augmente le risque de pneumothorax. La paresthésie, bien qu'elle ne soit pas activement recherchée, se produit parfois comme une confirmation supplémentaire du placement correct de l'aiguille. Un guidage radiologique est conseillé pour les blocs neurolytiques. À ce stade, en cas d'aspiration de sang négative, 3 à 5 ml d'anesthésique local sont injectés. Pour un seul ICNB, il est souhaitable de bloquer au moins un ICN céphalique et un caudad parce qu'un certain degré d'innervation se chevauchant à partir d'ICN adjacents est courant. Pour s'assurer que la pointe de l'aiguille reste à l'emplacement optimal, non affectée par les mouvements de la main et de la poitrine, certains cliniciens préfèrent connecter un tube d'extension entre l'aiguille et la seringue et demander à un assistant d'effectuer l'aspiration et l'injection.
bloc de T1 à T7 est techniquement plus difficile en raison des omoplates et des muscles rhomboïdes. Pour cette raison, nous préférons effectuer une bloc paravertébral thoracique ou un bloc péridural lorsqu'un bloc thoracique haut est requis.
LES MEILLEURS ÉQUIPEMENTS
- Aiguille : Coup unique : aiguille de calibre 20 à 22 de 4 à 5 cm (adultes)
- Placement du cathéter : aiguille Tuohy de calibre 18 à 20 (adultes)
- Seringue et aiguille pour infiltration locale
- Seringue avec tubulure d'extension
- Matériel et médicaments de stérilisation et de réanimation, champs, marqueur, oreiller, fluoroscope portatif (pour les blocs neurolytiques)
En savoir plus sur le Équipement pour blocs nerveux périphériques.
CHOIX DE L'ANESTHÉSIQUE LOCAL
Le choix de anesthésie locale pour l'ICNB à injection unique comprend la bupivacaïne 0.25 % à 0.5 %, la lidocaïne 1 % à 2 % avec l'épinéphrine 1/200,000 1 à 400,000/0.5 5 et la ropivacaïne 12 %. Trois à 6 ml d'anesthésique local sont injectés à chaque niveau lors d'un ICNB à injections multiples. La durée d'action est habituellement de 30 ± 2 h. L'ajout d'épinéphrine à la bupivacaïne ou à la ropivacaïne ne prolonge pas significativement la durée du bloc, mais peut ralentir l'absorption systémique et augmenter la dose maximale autorisée en une seule injection de 3 %. La dose maximale de bupivacaïne est de 7 (pour une solution simple) à 7 (avec épinéphrine) mg/kg/injection (total en une fois)10 et 5–7 mg/kg/jour. La dose maximale de lidocaïne est de 7 à 20 (avec épinéphrine) mg/kg/injection30 et 2.5 mg/kg/jour. Les volontaires pourraient tolérer 4 % plus de ropivacaïne que de bupivacaïne avant que les symptômes neurologiques ne se développent. La dose maximale par injection unique de ropivacaïne est de 9 mg/kg et de 12 mg/kg avec l'épinéphrine, tandis que la dose quotidienne maximale est de 24 à 4 mg/kg/XNUMX h. L'injection unique maximale d'épinéphrine en tant qu'additif est de XNUMX mcg/kg. Les sites vasculaires favorisent une absorption plus rapide de l'anesthésique local et les taux sanguins d'anesthésique local après ICNB sont plus élevés que pour la plupart des autres procédures d'anesthésie régionale. A ce titre, il convient de laisser une marge de sécurité entre les doses administrées et les posologies maximales recommandées, notamment chez le jeune enfant ; les personnes âgées; patients affaiblis; et ceux qui ont une insuffisance cardiaque, hépatique ou rénale sous-jacente. Pour continu infusion, les patients peuvent généralement mieux tolérer une augmentation progressive du niveau d'anesthésique local plasmatique que des augmentations aiguës. Un régime recommandé est une dose de charge de 0.3 mL/kg suivie d'une perfusion de 0.1 mL/kg/h de bupivacaïne à 0.25 % ou de lidocaïne à 1 %.
Conseils NYSORA
- Le meilleur site d'insertion de l'aiguille pour l'ICNB est l'angle de la côte, à environ 7 cm latéralement à la ligne médiane chez l'adulte.
- L'angle d'entrée idéal dans le sillon sous-costal est d'environ 20 degrés céphalique.
- L'analgésie péridurale peut être une alternative mieux adaptée aux ICNB bilatéraux en raison du risque de pneumothorax bilatéral et du potentiel de toxicité de l'anesthésique local en raison de la forte dose d'anesthésique local nécessaire.
- ICNB au-dessus de T7 peut être difficile à cause des omoplates ; une technique alternative comme le bloc paravertébral ou épidural doit être envisagée.
COMPLICATIONS
La principale préoccupation est un pneumothorax, qui peut survenir dans environ 1 % des cas. Le pneumothorax compressif et la nécessité subséquente d'une thoracostomie tubaire sont toutefois rares. Si un pneumothorax asymptomatique est détecté, la meilleure prise en charge est l'observation, la réassurance et, si nécessaire, une supplémentation en oxygène. Le péritoine et les viscères abdominaux risquent de pénétrer lorsque les ICN inférieurs sont bloqués. L'absorption de l'anesthésique local de l'espace intercostal est rapide ; la concentration plasmatique artérielle culmine en 5 à 10 minutes et la concentration plasmatique veineuse culmine plusieurs minutes plus tard.
EN RÉSUMÉ
L'ICNB est une technique d'anesthésie régionale utile ; qui est très efficace pour contrôler la douleur impliquant le thorax et le haut de l'abdomen. Bien qu'il existe un risque de pneumothorax et toxicité anesthésique locale, ceux-ci peuvent être réduits avec une technique appropriée et en tenant compte de la dose de médicament maximale autorisée. L'utilisation appropriée de l'ICNB comprend l'équilibrage de ses avantages et inconvénients par rapport à ceux des techniques alternatives telles que épidurale surélevées que pour les bloc paravertébral. Avec une expertise et des indications appropriées, le bloc nerveux intercostal peut fournir une option anesthésique particulièrement appropriée chez les patients chez qui les choix d'anesthésie générale ou régionale peuvent être limités.
Mises à jour cliniques
Coppens et al. (Anesthésiologie, 2025Cette étude multicentrique, randomisée en double aveugle, menée auprès de 100 patients subissant une thoracoscopie vidéo-assistée uniportale, compare le bloc intercostal (ICNB) réalisé par le chirurgien au bloc du plan des muscles érecteurs du rachis (ESPB) réalisé par l'anesthésiste. L'ICNB a entraîné une consommation de morphine significativement plus faible à 12 et 24 heures, des scores de douleur postopératoire précoce plus bas et une réduction des besoins en analgésiques de secours par rapport à l'ESPB, sans différence en termes de complications ou de durée d'hospitalisation. Il est à noter que l'ESPB était associé à des concentrations systémiques de ropivacaïne plus élevées, remettant en question les hypothèses concernant l'absorption de l'anesthésique local liée à l'ICNB et confirmant l'efficacité supérieure de l'ICNB comme stratégie analgésique précoce en chirurgie thoracique uniportale.
- En savoir plus sur l'étude ICI. (en anglais seulement).
Li et al. (Journal coréen de la douleur, 2024Une étude rétrospective cas-témoins a été menée auprès de 128 patients atteints de zona thoracique aigu. Cette étude comparait un traitement antiviral seul à un traitement antiviral associé à un bloc paravertébral thoracique (BPT) ou à un bloc intercostal (BIC) sous contrôle échographique. Le BPT et le BIC ont tous deux significativement réduit le score de gravité du zona à 30 jours, diminué le recours aux analgésiques de secours, amélioré la qualité de vie et réduit l'incidence des névralgies post-zostériennes par rapport au traitement antiviral seul, sans différence d'efficacité entre le BPT et le BIC. Le BIC était associé à une durée d'intervention plus courte et à une gêne moindre liée à la ponction, ce qui en fait une alternative plus rapide et plus sûre au BPT pour la prise en charge de la douleur aiguë du zona et la prophylaxie potentielle des névralgies post-zostériennes.
- En savoir plus sur l'étude ICI. (en anglais seulement).