Steve Roberts
INTRODUCCIÓN
La anestesia regional es una parte esencial de la práctica anestésica pediátrica moderna y aporta muchas ventajas significativas al paciente y al hospital (Tabla 1). Sin embargo, a pesar de un fuerte cuerpo de evidencia que destaca las ventajas de la anestesia regional, ha sido relativamente recientemente que la anestesia regional ha comenzado a convertirse en un lugar más común en la práctica anestésica. Grandes estudios prospectivos realizados por la Sociedad de Anestesiólogos Pediátricos de Lengua Francesa (ADARPEF) no han demostrado un mayor riesgo para los niños a los que se les realizan bloqueos bajo anestesia general. Sin embargo, las complicaciones fueron cuatro veces mayores en los niños menores de 6 meses en comparación con los mayores de 6 meses.
Históricamente, se pensaba que los recién nacidos requerían poca o ninguna analgesia. Sin embargo, la analgesia inadecuada en el recién nacido puede causar cambios bioconductuales que pueden modular futuras respuestas al dolor en la infancia. Como consecuencia, las técnicas avanzadas de anestesia regional (p. ej., analgesia epidural) se utilizan cada vez más en niños de todas las edades. Curiosamente, los estudios ADARPEF identificaron que ahora hay una tendencia a alejarse de los bloqueos neuroaxiales centrales hacia técnicas de catéter de nervio periférico. Este cambio puede haber sido influenciado por los avances en la cirugía mínimamente invasiva y la administración más predecible de técnicas de catéter periférico en la práctica moderna de anestesia regional.
Todas las técnicas de anestesia regional se pueden realizar de manera segura en la población pediátrica con el entrenamiento adecuado y equipo moderno.
TABLA 1. Ventajas de la anestesia regional en niños.
| Beneficios para el paciente. | Analgesia superior: Resultados en pacientes y padres/cuidadores más tranquilos. |
| MAC reducido: riesgo reducido de GA más profundo, emergencia más suave, retorno más temprano del apetito. | |
| Neurotoxicidad: este problema potencial depende de la dosis de GA; por lo tanto, una exposición reducida a MAC puede ser beneficiosa. | |
| Estabilidad hemodinámica: hasta los 8 años de edad, los BGC rara vez causan hipotensión significativa. | |
| Necesidad reducida de asistencia respiratoria posoperatoria: en particular en recién nacidos y lactantes sometidos a cirugía torácica y abdominal superior. | |
| Obtunds la respuesta de estrés hormonal. | |
| Reducción de la pérdida de sangre intraoperatoria: demostrada durante la reparación de hipospadias, reparación de hendiduras y amigdalectomía. | |
| Función GI mejorada: mejor mantenimiento del peristaltismo; perfusión esplácnica mejorada en casos de NEC y gastrosquisis | |
| Evita la necesidad de AG: los bebés prematuros que se someten a AG tienen riesgo de apnea posoperatoria. | |
| beneficios hospitalarios | Más fácil de amamantar: los niños sin dolor requieren menos trabajo para cuidar. |
| MAC reducido: Descarga rápida desde la recuperación de la primera etapa. | |
| Requerimiento reducido de soporte ventilatorio postoperatorio: Esto es particularmente beneficioso cuando el soporte de la UCIP es limitado. | |
| Reducción de la duración de la estancia. |
DIFERENCIAS ANATÓMICAS ENTRE NIÑOS Y ADULTOS
Con respecto a la anatomía, fisiología y farmacología, los adolescentes pueden ser considerados “pequeños adultos”; sin embargo, los recién nacidos y los bebés necesitan una consideración especial. Anatómicamente, la principal diferencia radica en la columna vertebral y su contenido; este tema se describe con mayor detalle en Epidural Pediátrica y Anestesia y Analgesia Espinal. Fisiológicamente, se encuentran una serie de diferencias en el desarrollo del sistema nervioso pediátrico en comparación con los adultos. La mielinización es incompleta al nacer y el proceso puede tardar 12 años en completarse; en consecuencia, se pueden utilizar eficazmente concentraciones más bajas de anestésico local en la población pediátrica, lo que también reduce el riesgo de toxicidad. Aunque las vías nociceptivas son fundamentalmente las mismas en niños que en adultos, existen diferencias que pueden provocar que los niños experimenten más dolor que los adultos. En los niños, el campo receptivo de una neurona puede ser mayor, lo que conduce a una mala localización del dolor. Las vías inhibitorias descendentes son inmaduras y esto puede permitir entradas nociceptivas no moduladas a las vías ascendentes del dolor espinal. Las inmadureces fisiológicas del hígado neonatal en asociación con un gasto cardíaco relativamente alto producen diferencias farmacológicas que se combinan para aumentar el riesgo de toxicidad por anestésicos locales en los recién nacidos.
FARMACOLOGÍA DE LOS ANESTÉSICOS LOCALES EN PACIENTES PEDIÁTRICOS
Hay dos grupos principales de fármacos anestésicos locales utilizados en la anestesia regional pediátrica: los aminoésteres y las aminoamidas. (Se puede encontrar una discusión detallada de estos medicamentos en Farmacología Clínica de los Anestésicos Locales.) Hay relativamente poca farmacocinética de anestésicos locales en niños, y especialmente en neonatos, es limitada; desafortunadamente, es este grupo de edad el que tiene mayor riesgo de toxicidad por anestésicos locales.
Anestésicos locales de tipo aminoamida
El grupo de anestésicos locales más comúnmente utilizado en la práctica pediátrica son las aminoamidas: lidocaína, bupivacaína, ropivacaína y levobupivacaína. Los anestésicos locales de aminoamida experimentan metabolismo hepático. Sin embargo, el hígado neonatal es inmaduro, y los sistemas de citocromos maduran a ritmos variables: el CYP3A4 dentro de los primeros 9 meses de vida en comparación con el CYP1A2, que puede tardar hasta los 8 años en madurar. El volumen de distribución en estado estacionario en lactantes es mayor que en adultos. Los compartimentos de líquidos cambian drásticamente con la edad, el 80 % del peso corporal consiste en agua en un recién nacido prematuro, el 75 % en un recién nacido a término, el 65 % en un lactante y el 60 % en niños mayores. A medida que aumenta la edad, el líquido intracelular aumenta del 20% del peso corporal en los recién nacidos prematuros al 30% observado en los adultos; dentro de este marco de tiempo, los fluidos extracelulares se reducen a la mitad. Los anestésicos locales son solubles en agua; por lo tanto, los cambios relacionados con la edad en la composición del compartimiento de fluidos son significativos. Los lactantes tienen niveles más bajos de proteínas fijadoras de anestésicos locales (p. ej., glucoproteína ácida alfa-1 y albúmina), lo que conduce a una mayor fracción de anestésico local libre y, por tanto, a un mayor riesgo de toxicidad. Sin embargo, en las primeras 48 horas después de la operación, hay un aumento de la glicoproteína ácida alfa-1 que puede actuar para proteger al recién nacido. El aclaramiento de estos fármacos disminuye en los menores de 3 meses de edad, alcanzando gradualmente los niveles de los adultos a los 8 meses de edad. En consecuencia, las semividas de eliminación de los anestésicos locales son más prolongadas en los recién nacidos y los lactantes que en los adultos.
Bupivacaína
La bupivacaína es un isómero con enantiómero l y d, y el enantiómero d causa la mayoría de los efectos adversos que se observan en humanos. Dado que la bupivacaína es el más tóxico de los anestésicos locales de aminoamida, se debe considerar el uso de una alternativa más segura, particularmente para los recién nacidos y cuando se administran técnicas de infusión continua a través de catéteres permanentes. La farmacocinética y la farmacodinámica de la bupivacaína están bien documentadas en la literatura. La concentración preferida para niños es 0.25% para bloqueos de nervios periféricos y 0.1% para infusiones continuas. Los niños mayores pueden tolerar una dosis más alta de solución anestésica local (0.4 mg/kg/h) en comparación con los recién nacidos y los lactantes (0.2 mg/kg/h). La dosis de bupivacaína se limita a 2 a 4 mg/kg para una inyección de dosis única y de 0.2 a 0.4 mg/kg para una infusión continua.
Ropivacaína
La ropivacaína es un anestésico local de amida más nuevo que se usa con más frecuencia en cirugía pediátrica. Es un enantiómero L con menos efectos secundarios cardiovasculares y del sistema nervioso central en comparación con la bupivacaína. La ropivacaína tiene propiedades vasoconstrictoras leves que pueden explicar el Tmax más prolongado cuando se administra por vía caudal en comparación con la bupivacaína. Hay datos farmacocinéticos disponibles en niños sobre el uso de ropivacaína en infusiones continuas, así como para inyecciones de una sola inyección. Los ensayos pediátricos han demostrado una mayor duración de la acción con ropivacaína que con mepivacaína cuando se utiliza para el bloqueo de nervios periféricos. También se debe tener precaución al usar ropivacaína en niños, ya que se han notificado casos de toxicidad cardiovascular.
Levobupivacaína
La levobupivacaína es un enantiómero L más nuevo con un riesgo potencialmente menor de toxicidad cardiovascular grave. Los datos farmacocinéticos están disponibles en niños y el intervalo de dosificación es similar al de la bupivacaína. Los experimentos con animales han demostrado que la levobupivacaína causa menos depresión miocárdica y una menor incidencia de inducir arritmias fatales en comparación con la bupivacaína. Aunque este fármaco ofrece al profesional la opción de un fármaco que es menos cardiotóxico, aún se debe tener precaución.
Anestésicos locales tipo éster
Debido a su corta duración de acción y propensión a causar reacciones alérgicas, los aminoésteres (p. ej., procaína, 2-cloroprocaína, tetracaína) son el grupo de anestésicos locales que se usa con menos frecuencia. A diferencia de los anestésicos locales de aminoamida, los aminoésteres son metabolizados por las colinesterasas plasmáticas. Como resultado, el metabolismo de los anestésicos locales de éster depende de los niveles plasmáticos de colinesterasa. Por lo tanto, en poblaciones con niveles de colinesterasa plasmáticos reducidos, como los recién nacidos y los lactantes, el nivel plasmático de estos fármacos puede aumentar, lo que podría conducir a niveles tóxicos del fármaco. La presencia de colinesterasa plasmática también limita la duración de la acción de estos fármacos, lo que conduce a una actividad más corta. Los anestésicos locales de éster más comunes que se usan en bebés y niños son la cloroprocaína y la tetracaína. Estos fármacos se utilizan ocasionalmente en niños como adyuvante de la anestesia raquídea en recién nacidos prematuros sometidos a anestesia raquídea o como única solución anestésica para la analgesia caudal. Se ha informado tetracaína en anestesia espinal, especialmente en bebés prematuros, como el único anestésico para la reparación de hernias inguinales. La 2-cloroprocaína se ha utilizado ampliamente en niños para analgesia en el espacio neuroaxial central.
DOSIFICACIÓN DE ANESTÉSICOS LOCALES EN PACIENTES PEDIÁTRICOS
La mayoría de las dosis de fármacos en pacientes pediátricos se basan en el peso del paciente (Tabla 2), aunque a menudo se debate si el peso corporal total o la masa corporal magra son más apropiados para los cálculos de fármacos. Sin embargo, esto puede no ser aplicable a las consideraciones de anestesia local; los estudios realizados en bebés sometidos a anestesia espinal encontraron un mayor requerimiento de solución anestésica local (en escala de peso) en comparación con sus contrapartes adultas que usaban bupivacaína o tetracaína.
TABLA 2. Dosis máximas recomendadas y duración aproximada de la acción de los agentes anestésicos locales de uso común.
| Anestesia local | Clase | Dosis máxima (mg/kg)a | Duración de la acción (min) | Infusión (mg/kg/h) |
|---|---|---|---|---|
| Procaína | Ester | 10 | 60-90 | - |
| 2-cloroprocaína | Ester | 20 | 30-60 | - |
| Tetracaína | Ester | 1.5 | 180-600 | - |
| Lidocaína | amidas | 5 | 90-200 | - |
| Bupivacaína | amidas | 2.5 | 180-600 | 0.2-0.4 |
| Ropivacaína | amidas | 2.5 | 180-600 | 0.2-0.5 |
| Levobupivacaína | amidas | 2.5 | 180-600 | 0.2-0.5 |
La concentración de anestésico local administrado también debe considerarse cuidadosamente. A menudo se utiliza una concentración más baja de anestésico local de acción prolongada (p. ej., levobupivacaína al 0.25 %) porque el niño también recibe anestesia general; por lo tanto, el bloqueo se usa solo para analgesia. Sin embargo, en ciertos escenarios, se deben administrar concentraciones más bajas o más altas de anestésico local. Las concentraciones más bajas (p. ej., levobupivacaína al 0.125 %) son útiles para disminuir el riesgo de toxicidad en los recién nacidos y es menos probable que enmascaren el síndrome compartimental o retrasen la deambulación. Se deben considerar concentraciones más altas de anestésico local (p. ej., levobupivacaína al 0.5 %) cuando sea deseable un bloqueo motor profundo (p. ej., cirugía de transferencia de tendones de miembros inferiores en niños con parálisis cerebral).
TOXICIDAD DE LOS FÁRMACOS ANESTÉSICOS LOCALES
La toxicidad de los anestésicos locales en niños incluye toxicidad cardiovascular y del sistema nervioso central.Tabla 3) y reacciones alérgicas a las soluciones anestésicas locales de éster. Las diferencias farmacocinéticas ya discutidas, junto con la inmadurez de la barrera hematoencefálica, pueden hacer que la toxicidad del sistema nervioso central sea más probable en los recién nacidos. Sin embargo, la coadministración de anestesia general puede enmascarar signos y síntomas tempranos de toxicidad sistémica. La dosis de anestésico local para niños siempre se calcula en miligramos por kilogramo, en lugar de los volúmenes predichos como en la anestesia regional para adultos. Si bien se reconoce que, de los pacientes pediátricos, los bebés tienen un mayor riesgo de toxicidad sistémica, la precaución debe ser la norma para los niños de todas las edades, ya que se han registrado concentraciones más altas de algunos anestésicos locales en adolescentes en comparación con los adultos. También se han informado niveles plasmáticos tóxicos luego de dosis seguras de anestésico local utilizadas para bloqueos caudales e ilioinguinales, por lo que se recomienda la dosis mínima efectiva.
TABLA 3. Toxicidad sistémica de la solución anestésica local.
| Sistema nervioso centrala |
| Mareos y aturdimiento |
| Alteraciones visuales y auditivas |
| Espasmos musculares y temblores |
| Convulsiones generalizadas |
| Cardiovascular |
| Efectos cardíacos directos |
| Fase rápida deprimida de la repolarización de las fibras de Purkinje |
| Disparo espontáneo deprimido del nódulo sinoauricular |
| Efecto inotrópico negativo sobre el músculo cardíaco |
| Alteración del flujo de entrada de calcio, lo que conduce a una disminución de la contractilidad miocárdica |
| Efectos sobre el tono vascular |
| Bajas concentraciones: vasoconstricción |
| Altas concentraciones: vasodilatación |
| Aumento de la resistencia vascular pulmonar |
Curiosamente, Weintraud et al. encontraron que los bloqueos ilioinguinales guiados por ecografía dieron como resultado concentraciones plasmáticas más altas en comparación con las técnicas basadas en puntos de referencia. Esto puede deberse a una mayor superficie de absorción creada al colocar el anestésico local precisamente en un plano fascial en comparación con los múltiples depósitos dentro del músculo que a menudo ocurren con un método basado en puntos de referencia.
Consejos NYSORA
Prevención de la toxicidad sistémica en la población pediátrica
- Elija un fármaco menos tóxico (p. ej., levobupivacaína o ropivacaína).
- No exceda la dosis máxima (en neonatos, puede ser prudente reducir a la mitad la dosis máxima).
- Inyecte pequeñas alícuotas y aspire repetidamente.
- La ecografía permite el uso de dosis más bajas de fármacos y la visualización de inyecciones.
- Tenga cuidado con las dosis repetidas y limite las infusiones en recién nacidos a 48 horas.
- Se puede usar una dosis de prueba que contenga epinefrina para identificar la inyección intravascular, pero está limitada por el anestésico general que se administre.
- Independientemente de la técnica que se utilice, todos los niños que reciban cualquier solución anestésica local, especialmente cuando se administren en infusiones continuas, deben ser monitoreados continuamente para detectar efectos adversos.
Consejos NYSORA
Manejo de la toxicidad de los anestésicos locales
En la práctica pediátrica, los primeros signos y síntomas de toxicidad pueden quedar enmascarados por la administración concomitante de anestesia general. Esto significa que el primer signo puede ser arritmia o colapso cardiovascular. Tenga en cuenta lo siguiente cuando maneje la toxicidad del anestésico local:
- Detener la inyección de anestésico local.
- Instale soporte vital básico y solicite asistencia.
- Asegure las vías respiratorias, ventile con oxígeno al 100 % y obtenga acceso intravenoso.
- Las convulsiones se pueden controlar con una benzodiazepina o un agente de inducción anestésica.
- Si se ha producido un paro cardíaco, inicie soporte vital avanzado.
- Tenga en cuenta que las arritmias a menudo son refractarias y, por lo tanto, la reanimación debe prolongarse.
- administración de lípidos. La Asociación de Anestesistas de Gran Bretaña e Irlanda ha publicado un protocolo sencillo a seguir (Figura 1 y XNUMX).
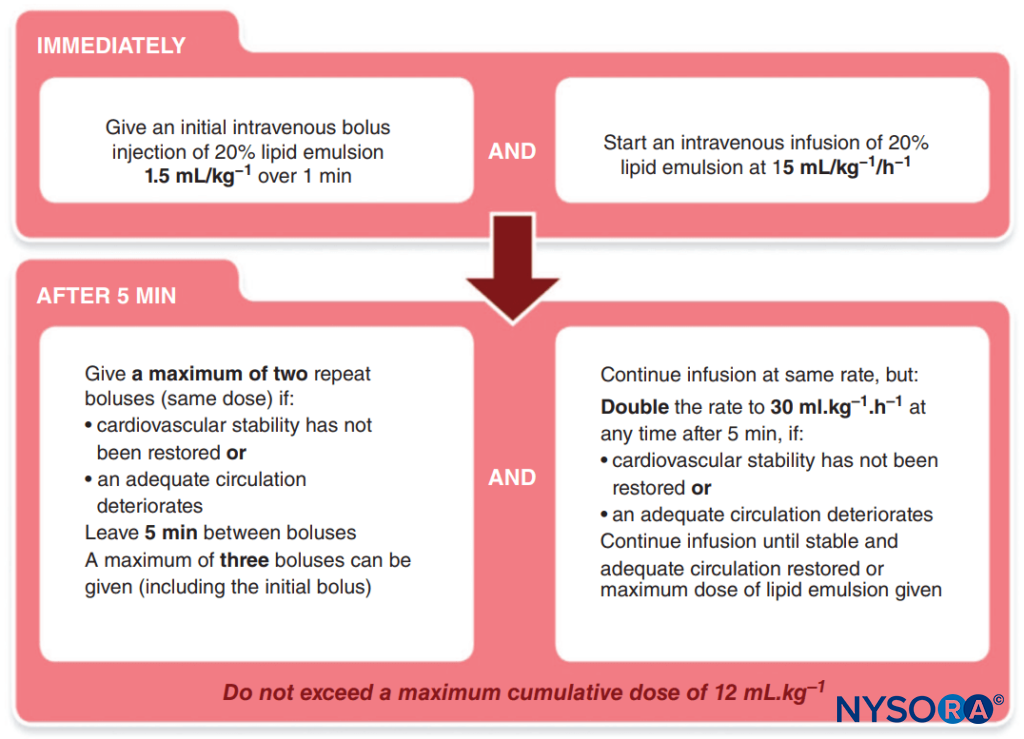
FIGURA 1. Protocolo de la Asociación de Anestesistas de Gran Bretaña e Irlanda (AAGBI) para la toxicidad de los anestésicos locales.
ANESTESIA TÓPICA
Es importante discutir el uso de anestesia tópica en niños porque se usa comúnmente en la práctica clínica para proporcionar analgesia para la colocación de catéteres intravenosos, punción lumbar y otros procedimientos invasivos (p. ej., circuncisión en recién nacidos). Las preparaciones más comunes incluyen lidocaína, tetracaína, benzocaína y prilocaína. La solución anestésica tópica penetra a través de la piel para proporcionar analgesia. Las tres preparaciones más comunes disponibles incluyen mezcla eutéctica de anestésicos locales (EMLA), LMX-4 (solución de lidocaína liposomal al 4 %) y Ametop (gel de ametocaína al 4 %). EMLA contiene lidocaína y prilocaína y debe aplicarse al menos una hora antes de la canulación. Su duración de acción es de solo 30 a 60 minutos, aunque se puede dejar actuar durante 4 a 5 horas. LMX-4 requiere solo 30 minutos para hacer efecto y también se puede dejar encendido durante 4 a 5 horas. Ametop requiere 45 minutos para hacer efecto y debe eliminarse dentro de la hora de la aplicación; su duración de efecto es de hasta 3 horas, ya que se une a las proteínas en el estrato córneo. Ametop es vasodilatador, lo que puede ayudar a la canulación. Sin embargo, Ametop puede causar eritema y edema, lo que puede oscurecer las venas.
Consejos NYSORA
Las siguientes son consideraciones para los niños que se someten a anestesia regional:
- La anestesia regional generalmente se realiza con el paciente bajo anestesia general.
- La dosis de anestésico local utilizada es mucho más baja que para los adultos y se calcula en miligramos por kilogramo).
- Use un anestésico local a la concentración efectiva más baja.
- Si se espera dolor moderado o severo, se requiere fisioterapia intensa después de la operación o hay antecedentes de dolor crónico, considere usar una técnica de catéter.
- Se informan muchas menos complicaciones de la anestesia regional en niños que en adultos.
- Obtenga siempre el asentimiento o consentimiento del paciente si el niño es mayor.
- Siempre explique la parestesia postoperatoria a los pacientes.
EVALUACIÓN PREOPERATORIA
La visita preoperatoria es una oportunidad para evaluar y preparar al paciente y la familia para la cirugía y la técnica anestésica propuestas. Es importante que el anestesiólogo comprenda la cirugía prevista para que pueda tomar la decisión de realizar una técnica de anestesia regional de inyección única o continua. En general, se debe elegir el bloqueo más periférico, ya que generalmente tiene el riesgo más bajo y la menor cantidad de efectos secundarios y, por lo tanto, tendrá una mayor aceptabilidad para el paciente y los padres o cuidadores por igual. Se recomienda una técnica de catéter para cirugía moderada a mayor, procedimientos que requerirán fisioterapia posoperatoria prolongada y para niños con dolor crónico. También es importante asegurarse de que habrá personal de enfermería capacitado para manejar técnicas de anestesia regional continua.
El anestesiólogo debe buscar posibles contraindicaciones (p. ej., comorbilidades) para una técnica anestésica regional determinada. Se debe realizar un historial completo del dolor, buscando específicamente un historial de dolor crónico o espasticidad muscular. Los niños con necesidades especiales pueden ser particularmente desafiantes y el anestesiólogo necesita saber cómo el niño enfrenta y expresa el dolor. El examen anestésico preoperatorio estándar debe incluir un examen del sitio de inserción del bloque propuesto para identificar cosas tales como dificultades anatómicas (p. ej., escoliosis) e infección local. En niños con enfermedad neurológica, se debe documentar su déficit neurológico preoperatorio. El anestesiólogo debe explicar las ventajas, los efectos secundarios y las posibles complicaciones del plan anestésico propuesto al niño y a los padres/cuidadores; es prudente también discutir un “plan B” en caso de que falle la técnica propuesta. Se deben discutir estrategias analgésicas alternativas para que se pueda dar el consentimiento informado. En particular, las parestesias postoperatorias de la técnica regional deben explicarse a los niños en términos que puedan entender, ya que a menudo es una experiencia difícil de sobrellevar. Si se utilizará una técnica de anestesia regional continua, asegúrele al niño que la extracción del catéter no será dolorosa. Los padres o cuidadores suelen dar su consentimiento para un procedimiento para su hijo. Sin embargo, si el niño tiene la capacidad cognitiva de distinguir el bien del mal, se sugiere que también se obtenga el consentimiento del niño para una técnica regional. Existe un debate sobre cuándo o cuál puede ser esta edad. Si un niño se niega a someterse a un procedimiento regional a pesar de la insistencia de los padres o cuidadores, es importante que el anestesiólogo proporcione una modalidad alternativa de alivio del dolor.
Se debe considerar la premedicación analgésica con paracetamol (acetaminofén) y un fármaco antiinflamatorio no esteroideo (AINE), especialmente cuando se sabe que el bloqueo no proporcionará una analgesia total (p. ej., un bloqueo del plano transverso del abdomen [TAP] para una apendicectomía). Las instrucciones postoperatorias deben darse antes de la operación y reforzarse después de la operación al alta.
ANESTESIA REGIONAL: ¿DESPIERTO O DORMIDO?
Si es mejor que el paciente esté despierto o dormido durante la anestesia regional ha sido un tema controvertido en adultos, y este debate alguna vez permeó el ámbito de la práctica de la anestesia regional pediátrica. Es difícil colocar un bloqueo regional en un niño despierto debido a la incapacidad del niño para cooperar, así como a la incapacidad cognitiva del niño para relacionarse con síntomas como parestesia o dolor. Por lo tanto, es mejor proporcionar al niño una técnica regional bajo sedación profunda o después de la inducción de anestesia general; esta práctica ha sido el consenso de los anestesiólogos pediátricos en los EE. UU. y en el extranjero durante algún tiempo.
Sin embargo, existen dos escenarios en los que se utilizan técnicas regionales despiertas en niños. Primero, se pensó que al evitar la anestesia general en bebés prematuros sometidos a cirugía menor, se podría reducir la incidencia de apnea posoperatoria. Este es probablemente un problema menor ahora que los pulmones de los recién nacidos prematuros están mejor protegidos y con la disponibilidad de agentes inhalatorios más nuevos que brindan una emergencia más rápida.
En segundo lugar, el niño más maduro puede ser considerado adecuado para una técnica regional despierto cuando se somete a una cirugía menor si lo prefiere o cuando la anestesia general se considera demasiado riesgosa (p. ej., biopsia de ganglio linfático en un adolescente con una masa mediastínica). Para pacientes mayores, es fundamental preparar al niño y a los padres o cuidadores para toda la visita al quirófano, no solo para la inserción del bloqueo. La inserción del bloque se puede hacer más cómoda aplicando una crema anestésica tópica (EMLA tiene la mejor penetración) sobre el sitio de inyección propuesto. Durante la visita al quirófano, el niño debe ser apoyado y distraído por una enfermera o un especialista en juegos. El niño también puede encontrar el uso de un reproductor de DVD o MP3 como una distracción útil. Puede ser necesario el uso de óxido nitroso (Entonox) o dosis ansiolíticas de propofol o remifentanilo para facilitar el proceso. Marhofer et al. han demostrado que en el escenario del trauma pediátrico, los bloqueos del plexo braquial se insertan más cómodamente con ecografía que con estimulación nerviosa. En los hospitales pediátricos, se debe recordar al personal de quirófano y al cirujano que el paciente estará despierto y que los medicamentos y el equipo necesarios para convertir a la anestesia general deben estar listos.
MANEJO DEL BLOQUEO PERIOPERATORIO
Se deben seguir algunas reglas simples al realizar cualquier técnica de anestesia regional en niños. Un asistente capacitado debe estar presente en todo momento, y este individuo debe comprender los principios básicos de la anestesia regional, en particular la necesidad de aspirar regularmente antes de la inyección, la necesidad de advertir al anestesiólogo acerca de la resistencia a la inyección. Además, el asistente debe poder realizar ajustes básicos en el estimulador de nervios periféricos (PNS) y en las máquinas de ultrasonido.
El niño debe tener una vía aérea segura, acceso intravenoso y monitoreo completo antes de comenzar el bloqueo. Como parte de la Lista de Verificación de Seguridad Quirúrgica de la Organización Mundial de la Salud (OMS), se verifica el consentimiento y el lado de la cirugía, y justo antes de la inserción del bloque, el sitio debe confirmarse nuevamente con el asistente del anestesiólogo.
El niño, la máquina de ultrasonido (cuando se usa), el equipo y el anestesiólogo deben colocarse ergonómicamente.
Existe cierto debate sobre los estándares mínimos de asepsia para la anestesia regional. Para las técnicas de inyección única, es suficiente lavarse las manos, usar guantes estériles, aplicar una solución alcohólica en la piel del paciente y cubrir la sonda de ultrasonido. Para las técnicas con catéter, se aconseja una técnica aséptica más rigurosa. Cuando se realiza cualquier técnica con catéter, es útil tener visible una gran área anatómica al cubrir al niño; esto le permite al anestesiólogo espacio suficiente para realizar un mapeo/escaneo de exploración y también una mejor vista y, por lo tanto, una apreciación de la anatomía del paciente (particularmente importante cuando se colocan epidurales en niños con escoliosis). Puede ser beneficioso tunelizar el catéter, ya que esto ayuda a la fijación y, en algunos casos, puede disminuir el riesgo de infección (p. ej., con un catéter caudal, el catéter se puede canalizar lejos del área del pañal).
No existe una dosis de prueba ideal; por lo tanto, se sugiere una aspiración repetida y frecuente durante la inyección. Cuando no se espera que el bloqueo cubra todos los aspectos del dolor quirúrgico (p. ej., un bloqueo de la vaina del recto para piloromiotomía), se debe considerar la administración de paracetamol por vía intravenosa y/o un AINE. por recto para ayudar a la analgesia. Otros adyuvantes pueden resultar beneficiosos (p. ej., 50 mg/kg de sulfato de magnesio intraoperatorio pueden disminuir los espasmos musculares posoperatorios en pacientes con parálisis cerebral que se someten a cirugía de las extremidades inferiores).
Es opinión del autor que, en la medida de lo posible, la eficacia de la técnica anestésica regional no debe verse oscurecida por la administración de opioides u óxido nitroso. Es importante en la evaluación intraoperatoria del bloqueo que cualquier cambio en la frecuencia cardíaca y la presión arterial se anote y se relacione con los procedimientos quirúrgicos específicos en ese momento. Esto permite la planificación de bloques de rescate al final del procedimiento. Incluso con bloqueos exitosos, pueden ocurrir respuestas cardiovasculares ocasionales a los estímulos quirúrgicos, ya que los bloqueos generalmente se realizan usando una concentración más baja de anestésico local (p. ej., levobupivacaína al 0.25 %) y, si se usa un torniquete, un aumento gradual de la frecuencia cardíaca y la presión arterial ocurrirá después de los primeros 30 a 40 minutos.
El grado de estabilidad cardiovascular intraoperatoria ayuda al anestesiólogo a decidir si el malestar del paciente durante la primera etapa de la recuperación se debe al dolor o a otra causa (p. ej., delirio de emergencia). malestar, entonces se debe suponer que el paciente tiene dolor, y esto se debe tratar rápidamente mediante la administración de un opiáceo de acción rápida (p. ej., fentanilo).
CUIDADO POSTOPERATORIO
Los consejos postoperatorios relacionados con la protección del área anestesiada deben darse verbalmente antes de la operación y repetirse después de la operación, y también se deben dar instrucciones escritas a la familia. Se debe advertir a la familia y al niño sobre la debilidad muscular y la disminución de la sensibilidad. Se deben proporcionar cabestrillos a los pacientes pediátricos con bloqueos en las extremidades superiores. Los niños ambulatorios con bloqueos en las extremidades inferiores deben disponer de los medios necesarios para movilizarse y viajar a casa. Toda institución debe contar con lineamientos para la atención de enfermería hospitalaria y el seguimiento de las técnicas de anestesia regional, y el personal debe recibir educación periódica sobre el manejo de los bloqueos regionales en el posoperatorio y el cuidado de la extremidad anestesiada. Por lo general, es más económico y seguro ubicar a los pacientes que reciben anestesia regional y analgesia en salas específicas. (Para más información sobre este tema, véase Manejo del dolor agudo y crónico en niños.)
CURSOS
La formación de los anestesiólogos en anestesia regional y anatomía pediátrica es fundamental para su implantación exitosa y segura. Siempre que sea posible, cada departamento debe proporcionar un enfoque estructurado para enseñar los bloqueos simples comunes: caudal, peneano, femoral, axilar, ilioinguinal y vaina del recto. La capacitación debe incluir técnicas de ecografía y punción. Una vez que se han aprendido las habilidades básicas de punción de EE. UU. en fantasmas y habilidades de exploración desarrolladas en voluntarios adultos, estas habilidades pueden transferirse al entorno clínico. En general, estas técnicas son más fáciles y seguras de realizar primero en pacientes mayores.
Consejos NYSORA
Siempre que sea posible, cada departamento debe proporcionar un enfoque estructurado para enseñar los bloques comunes: caudal, peneano, femoral, axilar, ilioinguinal y vaina del recto.
RESUMEN
La anestesia regional mejora la experiencia postoperatoria tanto de los niños como de los padres o cuidadores y facilita el uso eficiente de las instalaciones hospitalarias y se espera que el uso de la anestesia regional en niños siga creciendo en popularidad. Las técnicas de anestesia regional deben proporcionar el equilibrio correcto entre riesgos y beneficios para los niños y la cirugía de hoy. EE. UU. está permitiendo que una mayor variedad de bloques periféricos sean más seguros y fiables para su uso en niños. La tecnología es importante, pero no reemplaza una sólida comprensión de la anatomía y un alto nivel de práctica general segura.
Referencias
- Giaufre E, Dalens B, Gombert A: Epidemiología y morbilidad de la anestesia regional en niños: una encuesta prospectiva de un año de la Sociedad de Anestesiólogos Pediátricos de Lengua Francesa. Anesth Analg 1996;83:904–912.
- Ecoffey C, Lacroix F, Giaufre E et al: Epidemiología y morbilidad de la anestesia regional en niños: una encuesta prospectiva de seguimiento de un año de la Sociedad de Anestesiólogos Pediátricos de Lengua Francesa (ADARPEF). Pediatr Anesth 2010;20:1061–1069.
- Taddio A, Katz J, Ilersich AL, Koren G: Efecto de la circuncisión neonatal en la respuesta al dolor durante la vacunación de rutina posterior [ver comentarios]. Lancet 1997;349:599–503.
- Peutrell JM, Mather SJ: Anestesia regional en bebés y niños. Oxford: Oxford University Press, 1997.
- Suresh S, Wheeler M: Anestesia regional pediátrica práctica. Anesthesiol Clin North Am 2002;20:83–113.
- Fitzgerald M, Walker SM: Manejo del dolor infantil: un enfoque neurobiológico del desarrollo. Nat Clin Pract Neurol 2009;5:35–50.
- Mazoit JX, Dalens BJ: Farmacocinética de los anestésicos locales en bebés y niños. Clin Pharmacokinet 2004;43:17–32.
- Besunder JB, Reed MD, Blumer JL: Principios de biodisposición de fármacos en el recién nacido. Una evaluación crítica de la interfaz farmacocinética-farmacodinámica (Parte I). Clin Pharmacokinet 1988;14: 189–216.
- Besunder JB, Reed MD, Blumer JL: Principios de biodisposición de fármacos en el recién nacido. Una evaluación crítica de la interfaz farmacocinética-farmacodinámica (Parte II). Clin Pharmacokinet 1988;14: 261–286.
- Mazoit JX, Denson DD, Samii K: Farmacocinética de la bupivacaína después de la anestesia caudal en bebés. Anestesiología 1988;68:387–391.
- Ecoffey C, Desparmet J, Maury M, et al: Bupivacaína en niños: farmacocinética después de la anestesia caudal. Anestesiología 1985;63: 447–448.
- Murat I, Montay G, Delleur MM, et al: Farmacocinética de la bupivacaína durante la anestesia epidural en niños. Eur J Anaesthesiol 1988;5: 113–120.
- Berde CB: Toxicidad de los anestésicos locales en lactantes y niños. [Revisar]. J Pediatr 1993;122(Pt 2):S14–S20.
- Petitjeans F, Mion G, Puidupin M, et al: Taquicardia y convulsiones inducidas por inyección intravascular accidental de ropivacaína durante el bloqueo ciático. Acta Anaesthesiol Scand 2002;46:616–617.
- Ivani G, Mereto N, Lampugnani E, et al: Ropivacaína en cirugía pediátrica: resultados preliminares. Paediatr Anaesth 1998;8:127–129.
- Ivani G, Mazzarello G, Lampugnani E, DeNegri P, Torre M, Lonnqvist PA: ropivacaína para bloqueos centrales en niños. Anestesia 1998; 53 (Suplemento 2): 74–76.
- Ala-Kokko TI, Partanen A, Karinen J, et al: Farmacocinética de ropivacaína al 0.2 % y bupivacaína al 0.2 % después de bloqueos caudales en niños. Acta Anaesthesiol Scand 2000;44:1099–1102.
- Dalens B, Ecoffey C, Joly A, et al: Farmacocinética y efecto analgésico de la ropivacaína después del bloqueo del nervio ilioinguinal/iliohipogástrico en niños. Paediatr Anaesth 2001;11:415–420.
- Fernandez-Guisasola J, Andueza A, Burgos E, et al: Una comparación de ropivacaína al 0.5% y mepivacaína al 1% para el bloqueo del nervio ciático en la fosa poplítea. Acta Anaesthesiol Scand 2001;45:967–970.
- Ivani G, DeNegri P, Lonnqvist PA, et al: Una comparación de tres concentraciones diferentes de levobupivacaína para el bloqueo caudal en niños (tabla). Anesth Analg 2003;97:368–371.
- Lerman J, Nolan J, Eyres R, et al: Eficacia, seguridad y farmacocinética de la levobupivacaína con y sin fentanilo después de la infusión epidural continua en niños: un ensayo multicéntrico. Anestesiología 2003;99: 1166–1174.
- Ala-Kokko TI, Raiha E, Karinen J, et al: Farmacocinética de levobupivacaína al 0.5 % después del bloqueo del nervio ilioinguinal-iliohipogástrico en niños. Acta Anaesthesiol Scand 2005;49:397–400.
- Foster RH, Markham A: Levobupivacaína: una revisión de su farmacología y uso como anestésico local. Drogas 2000;59:551–579.
- Mather LE, Huang YF, Veering B, Pryor ME: Farmacocinética sistémica y regional de levobupivacaína y enantiómeros de bupivacaína en ovejas. Anesth Analg 1998;86:805–811.
- Tobias JD, O'Dell N: Cloroprocaína para anestesia epidural en bebés y niños. AANA J 1995;63:131–135.
- Raj PP, Ohlweiler D, Hitt BA, Denson DD: Cinética de los ésteres anestésicos locales y los efectos de los fármacos adyuvantes en la hidrólisis de 2-cloroprocaína. Anestesiología 1980;53:307–314.
- Tobias JD, Rasmussen GE, Holcomb GW III, et al: Anestesia caudal continua con cloroprocaína como complemento de la anestesia general en recién nacidos. Can J Anaesth 1996;43:69–72.
- Crowhust JA: deficiencia de colinesterasa. Anaesth Cuidados Intensivos 1983;11:7–9.
- Kuhnert BR, Philipson EH, Pimental R, Kuhnert PM: Un bloqueo epidural prolongado con cloroprocaína en una paciente posparto con pseudocolinesterasa anormal. Anestesiología 1982;56:477–478.
- Monedero P, Hess P: Bloqueo epidural alto con cloroprocaína en una parturienta con baja actividad de pseudocolinesterasa. Can J Anaesth 2001;48:318–319.
- Kuhnert BR, Kuhnert PM, Prochaska AL, Gross TL: niveles plasmáticos de 2-cloroprocaína en pacientes obstétricas y sus recién nacidos después de la anestesia epidural. Anestesiología 1980;53:21–25.
- Henderson K, Sethna NF, Berde CB: Anestesia caudal continua para la reparación de hernias inguinales en ex bebés prematuros. J Clin Anesth 1993;5: 129–133.
- Krane EJ, Haberkern CM, Jacobson LE: Apnea posoperatoria, bradicardia y desaturación de oxígeno en bebés anteriormente prematuros: comparación prospectiva de anestesia espinal y general. Anesth Analg 1995;80: 7–13.
- Henderson K, Sethna NF, Berde CB: Anestesia caudal continua para la reparación de hernias inguinales en ex bebés prematuros. J Clin Anesth 1993;5:129–133.
- Suresh S, Cote CJ: Anestésicos locales para bebés y niños. En Yaffe SJ, Aranda JV (eds): Farmacología neonatal y pediátrica, Principios terapéuticos en la práctica, 3ra ed. Filadelfia: Lippincott Williams & Wilkins, 2004.
- Frumiento C, Abajian JC, Vane DW: anestesia espinal para bebés prematuros sometidos a reparación de hernia inguinal. Arch Surg 2000; 135: 445–451.
- Kasten GW, Martin ST: Toxicidad cardiovascular de bupivacaína: comparación del tratamiento con bretilio y lidocaína. Anesth Analg 1985;64:911–916.
- Murat I, Esteve C, Montay G, et al: Farmacocinética y efectos cardiovasculares de la bupivacaína durante la anestesia epidural en niños con distrofia muscular de Duchenne. Anestesiología 1987;67:249–252.
- Graf BM: La cardiotoxicidad de los anestésicos locales: el lugar de la ropivacaína. Curr Top Med Chem 2001;1:207–214.
- Bergman BD, Hebl JR, Kent J, Horlocker TT: Complicaciones neurológicas de 405 catéteres axilares continuos consecutivos (tabla). Anesth Analg 2003;96:247–252.
- Berde CB: Convulsiones asociadas a la anestesia regional pediátrica [comentario editorial] [ver comentarios]. Anesth Analg 1992;75:164–166.
- Weintraud M, Lundblad M, Kettner SC et al: Ultrasonido versus técnica basada en puntos de referencia para el bloqueo del nervio ilioinguinal-iliohipogástrico en niños: las implicaciones en los niveles plasmáticos de ropivacaína. Anesth Analg 2009;108:1488–1492.
- Ludot H, Tharin JY, Belouadah M, et al: Reanimación exitosa después de la arritmia vebtricular inducida por ropivacaína y lidocaína después del bloqueo del plexo lumbar posterior en un niño. Anesth Analg 2008;106: 1572–1574.
- Acharya AB, Bustani PC, Phillips JD, et al: Ensayo controlado aleatorizado de mezcla eutéctica de crema anestésica local para punción venosa en bebés prematuros sanos. Arch Dis Child Fetal Neonatal Ed 1998;78:F138–F142.
- Benini F, Johnston CC, Faucher D, Aranda JV: Anestesia tópica durante la circuncisión en recién nacidos. JAMA 1993;270:850–853.
- Gourrier E, Karoubi P, el Hanache A, et al: Uso de crema EMLA en un departamento de neonatología. Dolor 1996;68:431–434.
- Eichenfield LF, Funk A, Fallon-Friedlander S, Cunningham BB: un estudio clínico para evaluar la eficacia de ELA-Max (lidocaína liposomal al 4 %) en comparación con una mezcla eutéctica de crema anestésica local para reducir el dolor de la venopunción en niños. Pediatría 2002;109:1093–1099.
- Jain A, Rutter N: Gel de ametocaína tópica en el recién nacido: ¿qué tan pronto funciona y cuánto dura? Arch Dis Child Fetal Neonatal Ed 2000:83:F211–214.
- Tait AR, Voepel-Lewis T, Malviya S: ¿Entienden? (Parte II): asentimiento de los niños que participan en investigaciones clínicas sobre anestesia y cirugía. Anestesiología 2003;98:609–614.
- Krane EJ, Dalens BJ, Murat I, Murrell D: La seguridad de las epidurales colocadas durante la anestesia general. Reg Anesth Pain Med 1998;23:433–438.
- Marhofer P, Sitzwohl C, GreherM, Kapral S: guía de ultrasonido para la anestesia del plexo braquial infraclavicular en niños. Anestesia 2004;59:642–646.

