Honorio T. Benzon, Rasha S. Jabri y Tom C. Van Zundert
INTRODUCCIÓN
El hematoma intraespinal es una condición relativamente rara que resulta de una variedad de causas. Las causas traumáticas incluyen la punción lumbar y la anestesia neuroaxial. Es más probable que ocurra en pacientes anticoagulados o trombocitopénicos, pacientes con enfermedad neoplásica o con enfermedad hepática o alcoholismo. Aproximadamente un cuarto a un tercio de todos los casos están asociados con la terapia de anticoagulación. El riesgo de formación de hematoma intraespinal después de la administración de anestesia neuroaxial y analgesia aumenta en pacientes que han recibido terapia anticoagulante o tienen un trastorno de la coagulación. Por esta razón, la anestesia neuroaxial a menudo está contraindicada en presencia de una coagulopatía. Otros factores de riesgo para el desarrollo de hematoma epidural o espinal incluyen la dificultad técnica (múltiples intentos) en la realización de los procedimientos neuroaxiales debido a anomalías anatómicas de la columna y punciones múltiples o sangrientas.
Originalmente se informó que la incidencia de hematoma espinal era de uno en 150,000 220,000 epidurales y uno en 2700 19,505 anestésicos espinales. Recientes estudios epidemiológicos han demostrado que la incidencia de hematoma espinal es más frecuente, variando de uno en 1 a uno en 21,643 epidurales. El estudio más reciente mostró un riesgo general de 3800 en 200,000 inyecciones epidurales. Los ancianos (uno de cada 315) tienen un mayor riesgo debido a anomalías degenerativas de la columna, osteoporosis y enfermedad vascular periférica. Las poblaciones obstétricas parecen tener una menor incidencia de hematoma espinal (uno en XNUMX XNUMX), probablemente secundario al estado de hipercoagulabilidad del embarazo, la mayor capacidad del espacio epidural en las parturientas más jóvenes y la presión intraepidural más alta. Con base en un amplio estudio retrospectivo reciente, la incidencia de hematoma epidural en pacientes con coagulación anormal puede ser tan baja como uno en XNUMX pacientes.
La introducción de la heparina de bajo peso molecular (HBPM) se asoció con un aumento en la incidencia de hematoma espinal, lo que resultó en una advertencia por parte de la Administración de Alimentos y Medicamentos (FDA) y la introducción de la primera declaración de consenso sobre anestesia regional en pacientes. sobre anticoagulantes por la Sociedad Americana de Anestesia Regional y Medicina del Dolor (ASRA) en 1998. Las guías se basaron en una extensa revisión de la literatura y de la farmacología de los diferentes anticoagulantes.
Se hicieron recomendaciones sobre el momento del bloqueo del nervio neuroaxial, la retirada del catéter epidural y la posterior administración de anticoagulantes. En particular, la ASRA recomendó el uso de bajas concentraciones de anestésicos locales para la infusión epidural (para preservar la fuerza motora y facilitar la monitorización) y la monitorización neurológica posterior. Las guías de consenso, publicadas en 1998 y actualizadas en 2003 y 2010, han ayudado mucho a los médicos en la toma de decisiones con respecto al uso de procedimientos neuroaxiales en el contexto de la terapia anticoagulante. Otros dos conjuntos de directrices, publicados por la Sociedad Europea de Anestesiología y la Sociedad Escandinava de Anestesiología y Medicina de Cuidados Intensivos, son influyentes en Europa.
En este capítulo, discutimos la importancia de los anticoagulantes comunes y esperamos ofrecer al lector una guía en la toma de decisiones sobre el uso de anestesia neuroaxial y bloqueos de nervios periféricos (BNP) en la práctica clínica. También hablaremos de los nuevos anticoagulantes, medicamentos que no estaban adecuadamente cubiertos en las últimas guías ASRA y solo parcialmente cubiertos por las guías europeas y escandinavas. Siga el enlace para obtener más información sobre Diagnóstico y manejo del hematoma espinal y del nervio periférico.
TERAPIA ANTIPLAQUETARIA
Los medicamentos antiplaquetarios inhiben la enzima ciclooxigenasa plaquetaria e impiden la síntesis de tromboxano A2. El tromboxano A2 es un potente vasoconstrictor que facilita las reacciones secundarias de agregación y liberación de plaquetas. El papel de las plaquetas en la coagulación y la hemostasia se muestra en Figuras 1 y 2. Las plaquetas de los pacientes que toman estos medicamentos tienen una adherencia plaquetaria normal al subendotelio y una formación normal del tapón hemostático primario. Se puede formar un coágulo adecuado, aunque potencialmente frágil. Aunque tales tapones pueden ser barreras hemostáticas satisfactorias para lesiones vasculares más pequeñas, es posible que no aseguren la formación adecuada de coágulos hemostáticos perioperatorios. Se debe suponer que la función plaquetaria en pacientes que reciben medicamentos antiplaquetarios está disminuida durante 1 semana con aspirina y de 1 a 6 días con medicamentos antiinflamatorios no esteroideos (AINE). Esta suposición no tiene en cuenta la formación continua de plaquetas nuevas y funcionales. La producción continua de plaquetas frescas que funcionan normalmente, combinada con la función residual de las plaquetas que ya circulan, puede explicar la relativa seguridad de realizar procedimientos neuroaxiales en estos pacientes.
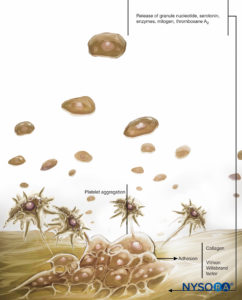
FIGURA 1. Papel de las plaquetas en la coagulación. Las plaquetas llevan a cabo su papel en la hemostasia a través de tres reacciones básicas: adhesión, activación (y secreción) y agregación. Cuando se daña el endotelio vascular, las plaquetas se unen rápidamente al subendotelio mediante un proceso denominado adhesión.
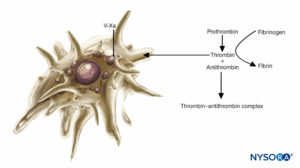
FIGURA 2. Papel de las plaquetas en la coagulación: Las plaquetas apoyan las reacciones de coagulación del plasma. Cuando se activan, las plaquetas se unen a varios complejos de proteínas plasmáticas y secretan una forma activada de factor V (factor Va), que se une a la superficie de las plaquetas y se une al factor Xa. A continuación, el factor Xa unido a plaquetas acelera la conversión de protrombina en trombina.
El riesgo de hematoma epidural y espinal en pacientes con terapia antiplaquetaria se ha elevado por un informe de caso de formación de hematoma epidural espontáneo en ausencia de anestesia espinal o epidural en un paciente con antecedentes de ingestión de aspirina. Vandermeulen y colegas implicaron la terapia antiplaquetaria en 3 de los 61 casos de hematoma espinal que ocurrieron después de la anestesia espinal o epidural. Otros estudios han mostrado un riesgo relativamente bajo de hematoma espinal en pacientes que toman aspirina o AINE que se someten a un procedimiento neuroaxial. El Grupo de Estudio Colaborativo de Aspirina en Dosis Baja durante el Embarazo (CLASP) incluyó a 1422 pacientes obstétricas de alto riesgo a las que se les administró 60 mg de aspirina al día y se sometieron a anestesia epidural sin secuelas neurológicas. En un estudio retrospectivo de 1013 anestésicos espinales y epidurales en los que el 39% de los pacientes tomaron medicamentos antiplaquetarios, incluido el 11% de los pacientes que tomaban múltiples medicamentos antiplaquetarios, ningún paciente desarrolló signos de hematoma espinal.
Los pacientes con medicamentos antiplaquetarios, sin embargo, mostraron una mayor incidencia de aspiración de sangre a través de la aguja espinal o epidural o del catéter. Un estudio prospectivo posterior en 1000 pacientes, el 39% de los cuales informaron tratamiento antiagregante plaquetario preoperatorio, observó la ausencia de complicaciones hemorrágicas. Por lo tanto, la terapia antiplaquetaria preoperatoria no fue un factor de riesgo para la colocación de agujas o catéteres con sangre. Se observaron como factores de riesgo significativos el sexo femenino, la edad avanzada, los antecedentes de hematomas o sangrado excesivos, la técnica de catéter continuo, el calibre de la aguja grande, los intentos múltiples y la colocación difícil de la aguja. Los estudios clínicos en pacientes de la clínica del dolor son similares a los que se someten a cirugía. Los pacientes que tomaban aspirina o AINE que se sometieron a inyecciones epidurales de esteroides no desarrollaron signos ni síntomas de hematoma intraespinal.
La falta de correlación entre la medicación antiplaquetaria y la colocación de agujas o catéteres con sangre proporciona alguna evidencia de que la terapia antiplaquetaria preoperatoria no representa un factor de riesgo significativo para el desarrollo de disfunción neurológica por hematoma espinal en pacientes que reciben terapia antiplaquetaria. Cabe señalar que ha habido informes de casos de hematoma intraespinal en pacientes que toman aspirina o AINE, aunque hubo factores que complicaron estos informes de casos. Estos incluyeron la administración concomitante de heparina, angioma venoso epidural coexistente y dificultad técnica para realizar el procedimiento. Más recientemente, se han publicado más informes de casos de hematoma espinal en relación con los procedimientos de intervención del dolor, específicamente las colocaciones de estimulación de la médula espinal.
Con base en la evidencia disponible, la ASRA ha hecho varias recomendaciones sobre los medicamentos antiplaquetarios. La terapia antiplaquetaria preoperatoria no representa un factor de riesgo significativo para el desarrollo de disfunción neurológica por hematoma espinal en pacientes que reciben terapia antiplaquetaria. Sin embargo, el riesgo de complicaciones hemorrágicas puede aumentar en pacientes que reciben varios medicamentos antiplaquetarios y el uso concomitante de otros medicamentos que afectan los mecanismos de coagulación, como anticoagulantes orales, heparina estándar y LMWH.
Consejos NYSORA
- Probablemente sea seguro realizar procedimientos de anestesia neuroaxial y regional en pacientes que toman aspirina y AINE.
- Los factores de riesgo para el aumento del sangrado y el hematoma espinal incluyen la ingesta de varios medicamentos antiplaquetarios por parte del paciente y los intentos múltiples.
Aspirina y procedimientos intervencionistas para el dolor
Ha habido varios informes de casos de hematoma espinal después de la inyección epidural de esteroides o la colocación o extracción de un estimulador de la médula espinal en pacientes que tomaban aspirina sola, AINE solo o cuando se siguieron las pautas de ASRA. Estos sucesos pueden estar relacionados con las frecuentes anomalías de la columna que se encuentran en estos pacientes, la presencia de fibrosis después de la cirugía de la columna, el uso de agujas más grandes en la colocación del estimulador de la médula espinal o las frecuentes manipulaciones (avances y retracciones) de los electrodos.
Los medicamentos utilizados en el manejo del dolor también provocan sangrado; estos incluyen oxcarbazepina y los inhibidores selectivos de la recaptación de serotonina. Por estas razones, la ASRA se puso en contacto con la Sociedad Europea de Anestesia Regional y Terapia del Dolor, la Academia Estadounidense de Medicina del Dolor, la Sociedad Internacional de Neuromodulación, la Sociedad Norteamericana de Neuromodulación y el Instituto Mundial del Dolor para formular pautas específicas para los procedimientos intervencionistas del dolor. . En contraste con las pautas de anestesia regional de ASRA, las pautas de múltiples sociedades recomendaron suspender la aspirina durante 4 a 6 días antes de los procedimientos intervencionistas para el dolor.
Consejos NYSORA
Las guías sobre procedimientos intervencionistas del dolor en pacientes con medicamentos antiplaquetarios y anticoagulantes son más restrictivas que las de anestesia regional.
Inhibidores COX-2 e inhibidores P2Y12
Los inhibidores de la ciclooxigenasa-2 (COX-2) ganaron popularidad debido a sus propiedades analgésicas y la falta de efectos plaquetarios y gastrointestinales, y los estudios han demostrado su propiedad analgésica en una variedad de entornos perioperatorios.
Los medicamentos tienen una toxicidad gastrointestinal (GI) mínima y son ideales para pacientes que tienen un mayor riesgo de eventos adversos graves en el GI superior. En comparación con la aspirina o los AINE, el efecto de los inhibidores de la COX-2 sobre la agregación plaquetaria y los tiempos de sangrado no fue diferente al del placebo. La pérdida de sangre no aumenta durante la cirugía de fusión espinal cuando se administran inhibidores de la COX-2 antes de la operación. Las propiedades plaquetarias de estos fármacos los hacen ideales para el uso perioperatorio cuando se planea la anestesia neuroaxial. Desafortunadamente, el rofecoxib y el valdecoxib han sido retirados del mercado debido a sus efectos secundarios cardiovasculares, dejando solo disponible el celecoxib, pero en dosis más bajas que las recomendadas anteriormente.
Los fármacos tienopiridínicos ticlopidina y clopidogrel no tienen efecto directo sobre el metabolismo del ácido araquidónico. Estos fármacos previenen la agregación plaquetaria al inhibir la activación plaquetaria mediada por el receptor de adenosina difosfato (ADP). También modulan el músculo liso vascular, reduciendo la contracción vascular. La ticlopidina rara vez se usa porque causa neutropenia, púrpura trombocitopénica e hipercolesterolemia.
Se prefiere el clopidogrel debido a su perfil de seguridad mejorado y eficacia comprobada. Se observó que era mejor que la aspirina en pacientes con enfermedad vascular periférica. La inhibición máxima de la agregación plaquetaria inducida por ADP con clopidogrel ocurre 3 a 5 días después del inicio de una dosis estándar (75 mg), pero dentro de las 4 a 6 horas posteriores a la administración de una dosis de carga alta de 300 a 600 mg. Por lo general, se administra una gran dosis de carga a los pacientes antes de someterse a una intervención coronaria percutánea (ICP). Ha habido un informe de caso de hematoma espinal en un paciente con ticlopidina. Aunque no ha habido ningún caso de hematoma intraespinal en un paciente que tomaba clopidogrel solo, se informó un caso de tetraplejía en un paciente que tomaba clopidogrel, diclofenaco y aspirina.
Para los fármacos de tienopiridina, se recomienda suspender la ticlopidina durante 10 a 14 días y el clopidogrel durante 7 días antes de la inyección neuroaxial. Ha habido informes de casos sobre la seguridad de la anestesia espinal 5 días después de suspender el clopidogrel. Un estudio mostró que la mayoría de los pacientes tenían una inhibición plaquetaria mínima 5 días después de suspender el clopidogrel. Si se debe realizar un procedimiento neuroaxial 5 a 6 días después de la interrupción del clopidogrel, entonces se debe realizar un ensayo de P2Y12 u otra prueba apropiada para garantizar una inhibición mínima o nula de la actividad plaquetaria.
Consejos NYSORA
- Las pautas de ASRA recomiendan un intervalo de 7 días entre la interrupción del clopidogrel y un procedimiento neuroaxial.
- Si se debe realizar una anestesia espinal o epidural, se recomienda una prueba de función plaquetaria para asegurarse de que la inhibición plaquetaria residual haya desaparecido o sea insignificante.
Para una prueba de estimulación de la médula espinal, se puede observar una interrupción de 5 días ya que el paciente no recibirá clopidogrel durante la prueba. Se debe realizar una prueba de la función plaquetaria (p. ej., el ensayo VerifyNow P2Y12 o la porción de mapeo de plaquetas del Thrombelastograph [TEG]) para garantizar una actividad plaquetaria adecuada.
Medicamentos antiplaquetarios más nuevos
El clopidogrel es el fármaco antiplaquetario de uso común en la terapia antiplaquetaria dual, en la que la aspirina se combina con un inhibidor del receptor P2Y12, en pacientes con síndromes coronarios agudos. El prasugrel es un profármaco similar al clopidogrel pero con características beneficiosas sobre el clopidogrel, y el ticagrelor es un inhibidor del receptor P2Y12 de acción directa. La mediana del tiempo hasta el efecto máximo es de 1 hora con prasugrel y de 4 horas con clopidogrel. El tiempo medio para alcanzar la concentración plasmática máxima con prasugrel es de 30 minutos y su vida media media es de 3.7 horas. Estos valores no reflejan la duración de la inhibición plaquetaria porque la inhibición del receptor P2Y12 es irreversible. La actividad plaquetaria tarda 7 días en normalizarse después de suspender el prasugrel.
El prasugrel y el ticagrelor causan una inhibición del 90% de la función plaquetaria en comparación con el 60%-70% del clopidogrel. Los pacientes con un índice de masa corporal (IMC) bajo, los mayores de 75 años y los que tienen antecedentes de accidente cerebrovascular tienen riesgo de hemorragia. A diferencia del clopidogrel, el prasugrel se convierte de forma fiable en su metabolito activo y no tiene interacciones farmacológicas. Además, no es susceptible a polimorfismos genéticos.
Ticagrelor se une reversiblemente al receptor P2Y12, bloqueando la activación del receptor mediada por ADP. A diferencia de las tienopiridinas, el metabolito activo y el fármaco original exhiben actividad antiplaquetaria siendo el fármaco original responsable de la mayor parte de la inhibición plaquetaria in vivo. El efecto antiplaquetario del ticagrelor es rápido; La inhibición plaquetaria máxima se produce de 2 a 4 horas después de la ingesta en comparación con las 24 horas con clopidogrel. La inhibición plaquetaria media del ticagrelor es del 93 % frente al 58 % del clopidogrel. La recuperación plaquetaria es rápida con ticagrelor; la actividad plaquetaria es normal a los 5 días después de la última dosis.
Tiempo entre la interrupción/reanudación de un fármaco antiplaquetario y la inyección neuroaxial
El intervalo entre la suspensión de un fármaco antiplaquetario y la inyección neuroaxial se basa en el porcentaje de inhibición plaquetaria y el porcentaje de recambio plaquetario. Prasugrel y ticagrelor causan una inhibición del 90%. Todos los días se forma del 15 al 50 por ciento de la reserva de plaquetas circulantes, lo que da como resultado plaquetas nuevas que comprenden del 75 al 5% de la reserva de plaquetas circulantes 7 a 5 días después de la interrupción del fármaco. Se ha recomendado un intervalo de 7 a 7 días para ticagrelor y de 10 a 7 días para prasugrel. Estas recomendaciones son adecuadas ya que la agregación plaquetaria se normaliza a los 5 días de suspender prasugrel ya los XNUMX días de ticagrelor.
Las guías escandinavas señalan que es aceptable reiniciar los fármacos antiplaquetarios en el momento de retirar el catéter, mientras que las guías de la Sociedad Europea de Anestesiología recomiendan un intervalo de 6 horas entre la retirada del catéter epidural y la reanudación de prasugrel o ticagrelor. Otras revisiones han recomendado precaución al reiniciar prasugrel y ticagrelor debido a su rápido efecto y potente inhibición antiplaquetaria. Un intervalo de 24 horas puede ser más apropiado para estos agentes.
Consejos NYSORA
- Prasugrel y ticagrelor deben suspenderse 7 y 5 días, respectivamente, antes de una raquídea o epidural.
- Los fármacos antiplaquetarios pueden reiniciarse 6 a 24 h después de un procedimiento neuroaxial o de la extracción del catéter.
Monitoreo de la función plaquetaria
Se consideró que el tiempo de sangrado de Ivy era un predictor confiable de sangrado anormal en pacientes que recibían medicamentos antiplaquetarios. Sin embargo, el tiempo de sangrado posterior a la aspirina no es un indicador confiable de la función plaquetaria. Existe una gran variabilidad intra e interpaciente en los resultados de la prueba, y no hay evidencia que sugiera que el tiempo de sangrado pueda predecir la función hemostática, ya que los estudios no han podido mostrar una correlación entre la prolongación del tiempo de sangrado inducida por aspirina y la pérdida de sangre quirúrgica. .
Ahora se encuentran disponibles ensayos especiales de función plaquetaria para monitorear la agregación y desgranulación de las plaquetas. El analizador de función plaquetaria (PFA) es una prueba de función plaquetaria in vitro. Es una buena prueba de detección de la enfermedad de von Willebrand y controla el efecto de la administración de desmopresina. La PFA se prolonga después de la terapia antiplaquetaria. Desafortunadamente, el PFA-100 no es una prueba sensible para monitorear la función antiplaquetaria de los inhibidores de P2Y12, clopidogrel, prasugrel y ticagrelor. Sin embargo, el PFA-200, una actualización reciente del PFA-100, parece ser sensible a los efectos de los inhibidores de P2Y12. Sin embargo, todavía faltan estudios en el punto de atención sobre esta nueva prueba de PFA.
Las pruebas más nuevas que monitorean la actividad del receptor P2Y12 incluyen el ensayo de fosfoproteína estimulada por vasodilatador (VASP), el ensayo VerifyNow, la prueba de agregometría de plaquetas múltiples (Multiplate) y el componente de mapeo de plaquetas del Thromboelastograph (TEG). El ensayo VerifyNow puede controlar los efectos antiplaquetarios de la aspirina y los inhibidores de P2Y12. El componente de mapeo de plaquetas del TEG se usa comúnmente en cirugía y anestesiología, mientras que VerifyNow es el ensayo predominante en cardiología clínica. Una revisión sobre el control de la función plaquetaria ha sido discutida por varias revisiones y está más allá del alcance de este capítulo.
ANTICOAGULANTES ORALES
La warfarina ejerce su efecto anticoagulante al interferir con la síntesis de los factores de coagulación dependientes de la vitamina K (VII, IX, X y trombina) (Figura 3 y XNUMX). También inhibe las proteínas anticoagulantes C y S. El factor VII tiene una vida media relativamente corta (6 a 8 h) y el tiempo de protrombina (TP) puede prolongarse hasta el rango terapéutico (1.5 a 2 veces lo normal) dentro de 24 a 36 horas. La proteína C anticoagulante también tiene una vida media corta (6 a 7 h). La prolongación inicial de la razón normalizada internacional (INR) es el resultado de los efectos competitivos de la reducción del factor VII y la proteína C y el lavado de los factores de coagulación existentes. Debido a esto, el INR es impredecible durante la etapa inicial del tratamiento con warfarina. El factor VII participa sólo en la vía extrínseca y no se logra una anticoagulación adecuada hasta que los niveles de los factores biológicamente activos II (vida media de 50 h) y X están lo suficientemente bajos. Esto requiere de 4 a 5 días. En ocasiones, se emplean altas dosis de carga de warfarina (15 mg) durante los primeros 2 a 3 días de tratamiento, y el efecto anticoagulante deseado se logra dentro de las 48 a 72 horas. El efecto anticoagulante de la warfarina persiste durante 4 a 6 días después de la terminación de la terapia mientras se sintetizan nuevos factores de vitamina K biológicamente activos. Los inconvenientes del tratamiento con warfarina incluyen la necesidad de monitorizar su efecto con monitorización seriada del INR, su interacción con otros fármacos y la necesidad de suspenderla unos días antes de la cirugía. El efecto de la warfarina puede revertirse mediante la transfusión de plasma fresco congelado e inyecciones de vitamina K. El concentrado de complejo de protrombina (PCC) de 3 o 4 factores puede usarse para antagonizar la warfarina en situaciones de emergencia.
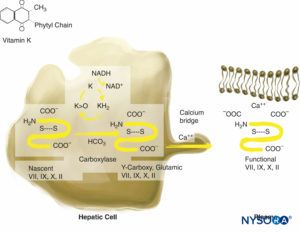
FIGURA 3. Síntesis del factor de coagulación dependiente de vitamina K. La vitamina K es necesaria para la modificación postraduccional de la protrombina; proteínas C y S; y los factores VII, IX y X. La vitamina K se almacena en los hepatocitos.
Existen pocos datos sobre el riesgo de hematoma espinal en pacientes con catéteres espinales o epidurales permanentes que posteriormente son anticoagulados con warfarina. Odoom y Sih realizaron 1000 anestésicos epidurales lumbares continuos en 950 pacientes que se sometieron a procedimientos vasculares y recibieron anticoagulantes orales preoperatorios. Se disminuyó el trombotest (una prueba de la actividad del factor IX) y se prolongó el tiempo de tromboplastina parcial activada (TTPa) en todos los pacientes antes de la colocación epidural. También se administró heparina en el intraoperatorio. Los catéteres epidurales permanecieron colocados durante 48 horas después de la operación y no hubo complicaciones neurológicas. Desafortunadamente, no se describió el estado de coagulación de los pacientes en el momento de retirar el catéter. Aunque los resultados de este estudio son tranquilizadores, la naturaleza anticuada del trombotest como medida de anticoagulación combinada con el estado de coagulación desconocido de los pacientes en el momento de la extracción del catéter limita la utilidad del estudio.
El uso de un catéter epidural o intratecal permanente y el momento de su extracción en un paciente anticoagulado son controvertidos. Aunque el trauma de la colocación de la aguja se produce con las técnicas de catéter continuo y de dosis única, la presencia de un catéter permanente puede provocar lesiones adicionales en los tejidos y las estructuras vasculares.
Dado que se han producido hematomas intraespinales después de la extracción del catéter, se recomienda que se apliquen los mismos valores de laboratorio para la colocación y extracción del catéter epidural. No se informaron hematomas espinales en 192 pacientes que recibieron analgesia epidural posoperatoria junto con dosis bajas de warfarina después de una artroplastia total de rodilla.
En este estudio, los pacientes recibieron warfarina para prolongar su PT de 15.0 a 17.3 segundos. Los catéteres epidurales se dejaron fijos durante 37 ± 15 horas (rango 13-96 h). El TP medio en el momento de la retirada del catéter epidural fue de 13.4 ± 2 segundos (rango 10.6-25.8 s). Este y varios estudios posteriores han documentado la seguridad relativa de la anticoagulación con warfarina en dosis bajas en pacientes con un catéter epidural permanente. Otro estudio mostró que los niveles de INR más altos (hasta 1.9) son aceptables para la extracción de catéteres epidurales siempre que se realice dentro de las 12 a 14 horas posteriores a la ingesta de warfarina. Un estudio mostró la ausencia de hematoma espinal cuando los catéteres epidurales se retiraron 2-3 días después de la ingesta de warfarina, incluso con INR marcadamente elevados. Debe estudiarse la práctica de retirar el catéter epidural 3 días después del inicio de la warfarina, cuando los niveles de los factores de coagulación VII, IX y X son bajos (los niveles del factor II aún pueden ser aceptables). Este es especialmente el caso, ya que los pacientes varían mucho en su respuesta a la warfarina, lo que llevó a algunos autores a recomendar una estrecha vigilancia del estado de la coagulación para evitar una prolongación excesiva del PT. Los factores responsables de un PT y PTT prolongados se ilustran en Figuras 4 y 5.
La ASRA recomendó un valor de INR de 1.4 o menos como aceptable para la realización de bloqueos nerviosos neuroaxiales. Este valor se basa en estudios que mostraron una hemostasia perioperatoria excelente cuando el valor de INR era ≤1.5. Los estudios sobre los niveles de factores de coagulación en diferentes valores de INR han demostrado que la disminución de estos factores puede no ser significativa en un INR de 1.5. Con valores de INR de 1.5 a 2.0, se observó que las concentraciones de factor II eran del 74 % al 82 % de los valores iniciales, mientras que los niveles de factor VII eran del 27 % al 54 % de los valores iniciales.
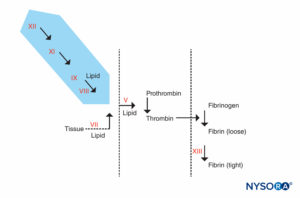
FIGURA 4. Reacción de coagulación. Los factores responsables de un PTT prolongado se encuentran en el área sombreada. Los pacientes que tienen un PTT anormal pero cuyo PT y otras pruebas son normales se pueden dividir en 2 grupos: los que son propensos a sangrar y los que no. Los pacientes que no sangran pueden tener un PTT extremadamente prolongado (90 segundos o más) pero no tienen antecedentes de sangrado. Tendrán una deficiencia de factor XII, precalicreína o cininógeno de alto peso molecular. A estos pacientes no se les debe negar la cirugía o la anestesia epidural. El otro grupo, los pacientes que sangran, tienen PTT prolongado y antecedentes de sangrado. Tendrán una deficiencia de factor VIII (hemofilia A), factor IX (hemofilia B o enfermedad de Christmas) o factor XI.
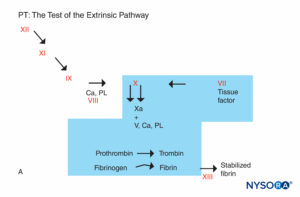
FIGURA 5A. Reacción de coagulación. Los factores involucrados en PT están en el área sombreada. El PT se realiza añadiendo una fuente de factor tisular al plasma del paciente junto con calcio o fosfolípidos. El factor tisular forma un complejo con el factor VII y lo activa. (Ca, calcio; PL, fosfolípido.)
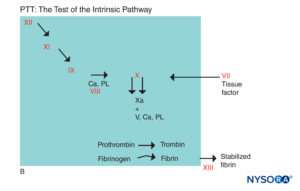
FIGURA 5B. Reacción de coagulación. Los factores involucrados en PTT están en el área sombreada. Al evaluar el PTT, la coagulación es iniciada por un agente que activa el complejo factor de Hageman, cininógeno y precalicreína. La mayoría de los factores de coagulación se detectan mediante PTT, excepto los factores VII y XIII, la proteína que estabiliza los coágulos de fibrina al entrecruzarlos y los componentes del sistema fibrinolítico. (Ca, calcio; PL, fosfolípido.)
A valores de INR de 2.1 ± 1 durante la fase inicial de la administración de warfarina, los factores II y VII fueron 65 ± 28 % y 25 ± 20 % de los valores de control. Actividades del 40% se consideran adecuadas para la hemostasia normal en el momento de la cirugía mayor. Otro estudio encontró que con INR de 1.3–2, bajo anticoagulación estable con warfarina, las concentraciones de los factores de coagulación VII, IX y X estaban dentro de los límites normales.
El médico debe conocer el efecto de la warfarina en la cascada de la coagulación y el papel del INR en el control de este efecto. Para minimizar el riesgo de complicaciones, la ASRA recomienda varias precauciones. El tratamiento crónico con warfarina oral debe interrumpirse y medirse el INR antes de realizar un bloqueo del nervio neuroaxial. El uso concomitante de otros medicamentos, como aspirina, AINE y heparinas, que afectan el mecanismo de coagulación, aumenta el riesgo de complicaciones hemorrágicas sin afectar el INR. Si se administra una dosis inicial de warfarina antes de la cirugía, se debe verificar el INR si la dosis se administró más de 24 horas antes. Si los pacientes están en tratamiento con dosis bajas de warfarina (dosis diaria media de aproximadamente 5 mg) durante la analgesia epidural, se debe controlar el INR diariamente y antes de retirar el catéter si la dosis inicial se administró hace más de 36 horas. Las dosis diarias más altas pueden necesitar un control más intensivo. La dosis de warfarina debe mantenerse o reducirse cuando el INR es >3 en pacientes con catéteres neuroaxiales permanentes para prevenir el hematoma epidural y el hemartroma. Durante la terapia con warfarina, el estado neurológico del paciente debe controlarse de forma rutinaria durante la infusión analgésica epidural, así como 24 horas después de que se haya retirado el catéter. Se deben utilizar concentraciones diluidas de anestésico local para minimizar el grado de bloqueo sensorial y motor. Se debe ejercer el juicio clínico al tomar decisiones acerca de retirar o mantener los catéteres neuroaxiales en pacientes con niveles terapéuticos de anticoagulación durante la infusión del catéter neuroaxial. La dosis de warfarina debe reducirse en pacientes que probablemente tengan una mejor respuesta al fármaco, especialmente en los ancianos. Para pacientes con anticoagulación oral crónica, se debe suspender la warfarina y medir el INR.
Consejos NYSORA
- Un INR de 1.4, en ausencia de hematomas fáciles y función hepática normal, es aceptable antes de la inyección neuroaxial en pacientes planificados para bloqueos nerviosos neuroaxiales.
- Se debe verificar el INR si el paciente tomó warfarina más de 24 horas antes.
- El INR debe ser normal 5 días después de suspender la warfarina antes de un procedimiento neuroaxial
HEPARINA
Heparina intravenosa
La heparina es un polisacárido complejo que ejerce su efecto anticoagulante al unirse a la antitrombina. El cambio conformacional en la antitrombina acelera su capacidad para inactivar los factores de trombina Xa y IXa.
La heparina no fraccionada libera inhibidores de la vía del factor tisular del endotelio, aumentando su actividad contra el factor Xa. El efecto anticoagulante de la heparina subcutánea tarda de 1 a 2 horas, pero el efecto de la heparina intravenosa es inmediato. De hecho, el tiempo de coagulación se prolonga de 2 a 4 veces el nivel basal 5 minutos después de la inyección intravenosa de 10,000 1.5 unidades de heparina. La heparina tiene una vida media de 2 a 4 horas. La dosis terapéutica de heparina cesa a las 6-1.5 horas de su administración. El aPTT se usa para controlar el efecto de la heparina; la anticoagulación terapéutica se logra con una prolongación del aPTT mayor de 0.2 veces el valor basal o un nivel de heparina de 0.4 a XNUMX U/mL. El aPTT generalmente no se prolonga con la administración subcutánea de dosis bajas de heparina y no se controla. La protamina neutraliza el efecto de la heparina administrada por vía intravenosa.
La heparina no es el anticoagulante ideal ya que es una mezcla de moléculas, de las cuales sólo una fracción tiene actividad anticoagulante. Se une al factor plaquetario 4 y al factor von Willebrand. El complejo heparina-antitrombina tampoco es muy eficaz para neutralizar la trombina unida al coágulo. Finalmente, la heparina se asocia con trombocitopenia inmunológica y trombosis inmunomediada. Para los pacientes que reciben terapia estándar con heparina, el riesgo de complicaciones hemorrágicas aumenta en presencia de otros medicamentos que afectan otros mecanismos de coagulación, como la aspirina, los AINE, las LMWH y los anticoagulantes orales. Varios estudios han demostrado la seguridad de la anestesia raquídea o epidural seguida de heparinización sistémica si se observan ciertas precauciones. Rao y El-Etr no informaron hematomas espinales en más de 4000 pacientes que se sometieron a cirugía vascular de las extremidades inferiores bajo anestesia espinal o epidural continua. En su estudio, se excluyeron los pacientes con trastornos de la coagulación preexistentes, la heparinización se produjo al menos 60 minutos después de la colocación del catéter, el nivel de anticoagulación se controló cuidadosamente y los catéteres permanentes se retiraron en un momento en que la actividad de la heparina era baja. La cirugía se canceló en pacientes cuando se notó sangre franca en la aguja y se realizó al día siguiente bajo anestesia general. Los mismos hallazgos se observaron en un informe posterior en la literatura neurológica. Ruff y Dougherty observaron hematomas espinales en 7 de 342 (2%) pacientes que se sometieron a punción lumbar y posterior heparinización para evaluar isquemia cerebral.
La presencia de sangre durante el procedimiento, la terapia concomitante con aspirina y la heparinización dentro de 1 hora fueron identificados como factores de riesgo en el desarrollo de hematoma espinal. La ASRA ha hecho varias recomendaciones para cuando se usa una técnica neuroaxial en presencia de anticoagulación intraoperatoria. La ASRA aconseja que se evite la técnica en pacientes con otras coagulopatías. Debe haber un retraso de al menos 1 hora entre la colocación de la aguja y la administración de heparina. El catéter debe retirarse 2 a 4 horas después de la última dosis de heparina y 1 hora antes de la siguiente administración de heparina. El TTPa o tiempo de coagulación activado (ACT) debe controlarse para evitar un efecto excesivo de la heparina. El paciente debe ser seguido postoperatoriamente para la detección temprana de la reaparición del bloqueo motor. Se recomiendan concentraciones diluidas de anestésicos locales para minimizar el bloqueo motor.
Aunque puede haber un mayor riesgo en el caso de una colocación traumática (con sangre) o difícil de la aguja, no hay datos que respalden la cancelación obligatoria de la cirugía. La decisión de proceder debe basarse en el juicio clínico apropiado y en una discusión completa con el cirujano y el paciente.
Consejos NYSORA
- Debe haber un retraso de al menos 1 hora entre un procedimiento neuroaxial y la readministración de heparina.
- El catéter se puede retirar de 2 a 4 horas después de la última dosis de heparina.
Ocasionalmente se realizan procedimientos neuroaxiales en pacientes que se someten a circulación extracorpórea. Se han recomendado las siguientes precauciones para prevenir el desarrollo de hematoma intraespinal en estos pacientes:
- Deben evitarse los procedimientos neuroaxiales en pacientes con coagulopatía conocida.
- La cirugía debe retrasarse 24 horas en pacientes con punción traumática.
- El tiempo desde el procedimiento neuroaxial hasta la heparinización sistémica debe ser superior a 1 hora.
- La heparinización y la reversión deben monitorearse y controlarse estrictamente.
- El catéter epidural debe retirarse cuando se restablezca la coagulación normal y el paciente debe ser monitoreado de cerca para detectar signos de hematoma espinal.
Heparina subcutánea
La base terapéutica de la heparina subcutánea en dosis bajas dos veces al día (5000 8 unidades cada 12 a 5000 h) es la inhibición del factor X activado mediada por heparina. Se requieren dosis más pequeñas de heparina cuando se administran como profilaxis en lugar de como tratamiento para la enfermedad tromboembólica. Después de la inyección intramuscular o subcutánea de 40 unidades de heparina, el efecto anticoagulante máximo se observa en 50 a 4 minutos y vuelve a la línea base en 6 a XNUMX horas. El aPTT puede permanecer en el rango normal y, a menudo, no se controla. Sin embargo, se han informado amplias variaciones en las respuestas de pacientes individuales a la heparina subcutánea. Las técnicas neuroaxiales no están contraindicadas durante la profilaxis subcutánea (minidosis), pero el riesgo de hemorragia puede reducirse retrasando la administración de heparina hasta después del bloqueo nervioso. El sangrado puede aumentar en pacientes debilitados o después de una terapia prolongada. La seguridad de la anestesia neuroaxial mayor en presencia de anticoagulación con dosis subcutáneas dos veces al día de heparina no fraccionada ha sido documentada por varios estudios. El régimen de heparina subcutánea dos veces al día ha sido reemplazado por un régimen de tres veces al día en la mayoría de los hospitales para disminuir la incidencia de tromboembolismo venoso posoperatorio. Sin embargo, esta práctica se ha asociado con hematomas espontáneos. Por esta razón, las últimas pautas de ASRA recomiendan no realizar procedimientos neuroaxiales en pacientes con un régimen de tres veces al día hasta que haya más datos disponibles.
Consejos NYSORA
- Los procedimientos neuroaxiales se pueden realizar en pacientes que reciben heparina subcutánea dos veces al día.
- Debido a la falta de datos adecuados, la ASRA recomienda que los procedimientos neuroaxiales no se realicen en pacientes que reciben heparina subcutánea tres veces al día.
Heparina de bajo peso molecular
La heparina no fraccionada es una mezcla heterogénea de cadenas de polisacáridos que se pueden separar en fragmentos de varios pesos moleculares. El efecto anticoagulante de la HBPM es similar al de la heparina no fraccionada; activa la antitrombina, acelerando la interacción de la antitrombina con la trombina y el factor Xa. La LMWH tiene una mayor actividad contra el factor Xa, mientras que la heparina no fraccionada tiene una actividad equivalente contra la trombina y el factor Xa. La semivida plasmática de las HBPM varía de 2 a 4 horas después de una inyección intravenosa y de 3 a 6 horas después de una inyección subcutánea; la vida media de una LMWH es 2 a 4 veces mayor que la de la heparina estándar. Tiene una baja afinidad por las proteínas plasmáticas, lo que se traduce en una mayor biodisponibilidad. Las ventajas de la HBPM sobre la heparina no fraccionada incluyen una biodisponibilidad más alta y más predecible después de la administración subcutánea y una vida media biológica más prolongada. Además, no se requiere monitoreo de laboratorio de la respuesta anticoagulante de HBPM, y no es necesario ajustar la dosis por peso (aunque puede ocurrir una sobredosis en pacientes con un IMC bajo). La LMWH muestra un efecto antitrombótico dependiente de la dosis que se evalúa con precisión midiendo el nivel de actividad anti-Xa. La recuperación de la actividad anti-factor Xa después de una inyección subcutánea de HBPM se aproxima al 100%, haciendo innecesaria la monitorización de laboratorio excepto en pacientes con insuficiencia renal o aquellos con peso corporal inferior a 50 kg o superior a 80 kg. El tiempo de reacción del trombolastograma parece correlacionarse con la concentración sérica de anti-Xa.
Las tres HBPM disponibles en el mercado en los Estados Unidos son enoxaparina (Lovenox), dalteparina (Fragmin) y tinzaparina (Innohep), aunque la última se suspendió debido a su bajo uso. La enoxaparina se administra una vez al día o cada 12 horas cuando se usa como profilaxis, y la dalteparina y la tinzaparina se administran una vez al día. Los tres fármacos parecen tener una eficacia comparable en el tratamiento y prevención del tromboembolismo venoso. La enoxaparina y la dalteparina tienen una eficacia comparable en la prevención de la muerte o el infarto de miocardio en pacientes con angina inestable.
La dosis tromboprofiláctica recomendada en Estados Unidos es de 30 mg de enoxaparina dos veces al día, aunque algunos médicos aumentan la dosis en pacientes obesos (1.5 mg/kg al día o 1 mg/kg cada 12 horas). El esquema de dosificación europeo es de 20 a 40 mg de enoxaparina una vez al día, y los pacientes reciben su dosis inicial 12 horas antes de la cirugía, una práctica que no se observa en los Estados Unidos.
Numerosos casos de hematoma neuroaxial ocurrieron en los Estados Unidos, lo que llevó a la FDA a emitir un aviso de salud en diciembre de 1997 y la convocatoria de la primera conferencia de consenso ASRA sobre anticoagulación y anestesia neuroaxial. Las pautas de ASRA recomiendan que se administre la dosis efectiva más pequeña de HBPM. La administración posoperatoria de la terapia con HBPM debe retrasarse tanto como sea posible, por un mínimo de 12 horas e idealmente 24 horas después de la operación. Una dosis única de anestesia espinal puede ser la técnica neuroaxial más segura en pacientes que reciben HBPM preoperatoria. Se recomienda esperar al menos 12 horas después de la dosis de HBPM profiláctica antes de realizar una técnica neuroaxial. Los pacientes que reciben dosis más altas de HBPM (p. ej., enoxaparina 1 mg/kg dos veces al día) requieren demoras más prolongadas (24 h). El catéter debe retirarse cuando la actividad anticoagulante sea baja, al menos 12 horas después de la administración profiláctica de HBPM y 4 horas antes de la siguiente dosis. Debe observarse una vigilancia extrema del estado neurológico del paciente si se implementa la tromboprofilaxis con HBPM mientras se está infundiendo un catéter permanente. Se recomienda una solución diluida de anestésico local para poder monitorear mejor la función neurológica. El uso de otros medicamentos que afectan la hemostasia, como los antiplaquetarios, la heparina estándar, el dextrano o los anticoagulantes orales, en combinación con la HBPM crea un riesgo adicional de complicaciones hemorrágicas.
Consejos NYSORA
- En pacientes que reciben una dosis profiláctica de HBPM, se recomienda un intervalo de 12 horas antes de una inyección neuroaxial.
- Para los pacientes que reciben una dosis terapéutica de HBPM, es apropiado un intervalo de 24 horas.
- La FDA ha recomendado un retraso de 4 horas después de la extracción del catéter epidural antes de que se reanude la HBPM.
TERAPIA TROMBOLÍTICA
Los agentes trombolíticos disuelven activamente los coágulos de fibrina que ya se han formado. Los activadores exógenos del plasminógeno, como la estreptocinasa y la urocinasa, no solo disuelven el trombo sino que también afectan al plasminógeno circulante, lo que conduce a una disminución de los niveles tanto de plasminógeno como de fibrina. El activador del plasminógeno de tipo tisular recombinante (r-TPA), un agente endógeno, es más selectivo para la fibrina y tiene menos efecto sobre los niveles de plasminógeno circulante. La lisis del coágulo conduce a una elevación de los productos de degradación de la fibrina, que tienen un efecto anticoagulante al inhibir la agregación plaquetaria.
Aunque la colocación de aguja y catéter epidural o espinal con heparinización posterior parece relativamente segura, el riesgo de hematoma espinal en pacientes que reciben terapia trombolítica no está bien definido. Se han informado en la literatura casos de hematoma espinal en pacientes que tenían catéteres epidurales o epidurales permanentes y que recibieron agentes trombolíticos.
Las pautas de ASRA hacen recomendaciones con respecto a los procedimientos neuroaxiales después de la terapia trombolítica o fibrinolítica. El uso concomitante de heparina con fármacos fibrinolíticos o trombolíticos coloca a los pacientes en alto riesgo de hemorragia neuroaxial adversa durante la anestesia raquídea o epidural. Excepto en circunstancias muy inusuales, se debe advertir a los pacientes que reciben terapia fibrinolítica o trombolítica que no reciban anestesia espinal o epidural. No hay datos disponibles para determinar claramente el período de tiempo adecuado después de la interrupción de estos fármacos y la realización segura de una técnica neuroaxial. Las guías europeas recomiendan dejar el catéter epidural colocado cuando a un paciente se le administra un fármaco trombolítico, y retirarlo solo cuando el efecto del fármaco haya desaparecido. Las guías escandinavas recomiendan un intervalo de 24 horas entre la interrupción del fármaco y el procedimiento neuroaxial. Se recomienda un control neurológico frecuente durante un período de tiempo adecuado en pacientes que han tenido bloqueos del nervio neuroaxial después de la terapia fibrinolítica o trombolítica. Si un paciente tiene una infusión epidural continua y ha recibido terapia fibrinolítica o trombolítica, se deben usar medicamentos que minimicen el bloqueo sensorial y motor. No ha habido una recomendación definitiva sobre el momento de retirar los catéteres neuroaxiales en pacientes que inesperadamente reciben terapia fibrinolítica o trombolítica. La medición de los niveles de fibrinógeno puede ser útil para guiar una decisión sobre el retiro o el mantenimiento del catéter.
Terapia de hierbas
Los medicamentos a base de hierbas más utilizados son el ajo, el ginkgo y el ginseng. El ajo inhibe la agregación plaquetaria y su efecto sobre la hemostasia parece durar 7 días. Ginkgo inhibe el factor activador de plaquetas y su efecto dura 36 horas. El ginseng tiene una variedad de efectos: inhibe la agregación plaquetaria in vitro y prolonga tanto el tiempo de trombina (TT) como el aPTT en animales de laboratorio; su efecto dura 24 horas. A pesar de su efecto sobre la función plaquetaria, los medicamentos a base de hierbas por sí mismos no parecen presentar un riesgo significativo adicional en el desarrollo de hematoma espinal en pacientes que reciben anestesia epidural o espinal. Los datos clínicos disponibles no respaldan la interrupción obligatoria de estos medicamentos o la cancelación de la cirugía en pacientes en los que se han continuado estos medicamentos. Sin embargo, el uso concomitante de otros medicamentos que afectan los mecanismos de coagulación, como anticoagulantes orales o heparina, puede aumentar el riesgo de complicaciones hemorrágicas en estos pacientes. No existe una prueba aceptada para evaluar la adecuación de la hemostasia en el paciente que ha tomado medicamentos a base de hierbas. En este momento, no parece haber preocupaciones específicas en cuanto al momento del bloqueo del nervio neuroaxial en relación con la dosificación de la terapia a base de hierbas, el control posoperatorio o el momento de la extracción del catéter neuroaxial.
Inhibidores de trombina
Los derivados de la hirudina recombinantes, incluida la desirudina y la bivalirudina, inhiben tanto la trombina libre como la unida al coágulo. Argatroban, un derivado de la l-arginina, tiene un mecanismo de acción similar. Estos fármacos se utilizan principalmente en el tratamiento de la trombocitopenia inducida por heparina. No hay reversión farmacológica del efecto de estos fármacos. No ha habido informes de casos de hematoma espinal relacionado con anestesia neuroaxial en pacientes que recibieron un inhibidor de trombina. Sin embargo, se han notificado hemorragias intracraneales espontáneas. De acuerdo con las pautas de ASRA, no se puede hacer ninguna declaración sobre la evaluación de riesgos y el manejo del paciente.
El fondaparinux
Fondaparinux es un anticoagulante sintético que produce su efecto antitrombótico a través de la inhibición selectiva del factor Xa. El fármaco exhibe consistencia en su efecto anticoagulante ya que se sintetiza químicamente. Es 100% biodisponible. De rápida absorción, alcanza su máxima concentración a las 1.7 horas de su administración. Su vida media es de 17 a 21 horas.
Fondaparinux se recomienda como agente antitrombótico después de una cirugía ortopédica mayor y como tratamiento inicial para la embolia pulmonar. La vida media extendida (aproximadamente 20 horas) permite la dosificación una vez al día. La FDA ha emitido una advertencia de recuadro negro para fondaparinux similar a la de las HBPM y la heparina.
Se desconoce el riesgo real de hematoma espinal con fondaparinux. Un estudio no mostró complicaciones en pacientes que recibieron inyecciones neuroaxiales. En este estudio, los catéteres se retiraron 36 horas después de la última dosis de fondaparinux y la dosificación se retrasó 12 horas después de retirar el catéter. Los pacientes fueron excluidos del estudio si presentaban dificultades para realizar el procedimiento neuroaxial (requirieron más de 3 intentos), el procedimiento se complicó con sangrado, requirieron antiagregantes plaquetarios o se planeó retirar el catéter epidural al día siguiente de la cirugía. Debido a los requisitos poco realistas en la práctica clínica, la ASRA no recomienda el uso de fondaparinux en presencia de un catéter epidural permanente. Sus recomendaciones se basan en el efecto antitrombótico sostenido e irreversible de fondaparinux, la dosificación postoperatoria temprana y el hematoma espinal informado durante los ensayos clínicos iniciales del fármaco. La vigilancia estrecha de la literatura sobre los factores de riesgo asociados con el sangrado quirúrgico puede ser útil en la evaluación del riesgo y el tratamiento del paciente. La realización de técnicas neuroaxiales debe realizarse en las condiciones utilizadas en los ensayos clínicos (paso único de la aguja, colocación atraumática de la aguja, evitación de catéteres neuroaxiales permanentes). Si esto no es factible, se debe considerar un método alternativo de profilaxis.
Resumen
El intervalo de tiempo entre la suspensión del anticoagulante y el procedimiento neuroaxial y entre la retirada del catéter epidural y la reanudación del fármaco se resumen en Tabla 1.
TABLA 1. Intervalos de tiempo recomendados antes o después del procedimiento neuroaxial y la extracción del catéter epidural.
| Droga | Tiempo antes del neuroaxial Procedimiento o retiro del catéter | Tiempo después del neuroaxial Procedimiento o retiro del catéter | Comentarios |
|---|---|---|---|
| Aspirina | Ninguna | Ninguna | |
| Los AINE | Ninguna | Ninguna | |
| El clopidogrel | 7 días* | Después de la extracción del catéter | Según las directrices europeas y escandinavas |
| Prasugrel | 7-10 días | 6h | Según las directrices europeas |
| Ticagrelor | 5 días | 6h | (Como anteriormente) |
| Warfarina | 5 días (INR normal) | Después de la extracción del cateter | |
| Heparina (IV) | 4-6 horas. | 1-2h | |
| La heparina | |||
| -(Esc, OFERTA) | Ninguna | Ninguna | |
| -(Esc, TID) | No es aplicable | Procedimiento neuroaxial | |
| HBPM | |||
| Profiláctico | 12 horas | 4 horas | recomendación de la FDA |
| Terapéutico | 24 horas | 4 horas | |
| El fondaparinux | 36-42 horas | 6-12 horas | Según las directrices europeas. ASRA recomienda no realizar procedimientos neuroaxiales en pacientes que toman el fármaco. *Si se debe realizar un procedimiento neuroaxial a los 5 días, se recomienda una prueba de función plaquetaria (ver texto |
NUEVOS ANTICOAGULANTES
Una discusión de los nuevos anticoagulantes dabigatrán, rivaroxabán y apixabán implica una revisión de cierta información de antecedentes.
El intervalo entre la interrupción del anticoagulante y la inyección neuroaxial y entre el procedimiento neuroaxial o retiro del catéter epidural y reanudación del anticoagulante
Se ha recomendado que dos vidas medias es un compromiso adecuado entre el riesgo de tromboembolismo venoso (TEV) y la prevención del hematoma espinal. Las guías europeas y escandinavas recomendaron un intervalo de 2 semividas entre la interrupción del anticoagulante y la inyección neuroaxial.
Se tomó esta decisión porque la TEV subclínica ocurre en un buen porcentaje de pacientes inmediatamente después de la cirugía y tener anticoagulación residual podría prevenir esta ocurrencia. La presencia de anticoagulación residual facilita la transición a la anticoagulación completa después de un procedimiento neuroaxial. Después de 1, 2, 3, 4, 5 y 6 vidas medias, los siguientes porcentajes de fármaco permanecen en circulación: 50 %, 25 %, 12.5 %, 6.25 %,
3.125% y 1.5625%, respectivamente (Tabla 2). Sin embargo, estos hallazgos se basan en estudios en voluntarios sanos jóvenes en estudios farmacocinéticos de dosis única en ausencia de otros anticoagulantes. Por el contrario, en la práctica clínica los pacientes suelen ser de mayor edad y con comorbilidades concomitantes.
TABLA 2. Intervalos de tiempo recomendados antes o después del procedimiento neuroaxial y catéter epidural para los nuevos anticoagulantes.
| Droga | Media vida | Directrices europeas | Directrices escandinavas | Cinco vidas medias |
|---|---|---|---|---|
| Dabigatrán | 12-17h 28 horas (enfermedad renal) | (Contraindicado por fabricante) | Informacion no disponible | 85h (4d) 6d (pacientes renales) |
| Rivaroxaban | 9-13h | 22-26h | 18 horas | 65h (3d) |
| Apixaban | 15.2 +/-8.5h | 26-30h | Informacion no disponible | 75h (3-4d) |
En pacientes con riesgo de TEV, como aquellos con antecedentes de accidente cerebrovascular, podría ser apropiado un intervalo de vida media de 2 o 3, reconociendo que no se asegura una hemostasia adecuada. Para pacientes sin factores de riesgo trombótico, un intervalo de 4 a 6 semividas entre la última dosis de anticoagulante y la inyección neuroaxial asegura una eliminación más completa del fármaco y un menor riesgo de sangrado. Un compromiso entre las recomendaciones conservadoras de 4 a 6 vidas medias y 2 a 3 vidas medias es un intervalo de 5 vidas medias con la terapia puente de HBPM.
En cuanto a la reanudación del anticoagulante tras inyección neuroaxial o retirada de catéter epidural, las guías escandinavas se basan en la recomendación de Rosencher et al. de 8 horas menos el tiempo que tarda el anticoagulante en alcanzar el efecto máximo.
Se supuso que ocho horas eran suficientes para que el coágulo se estabilizara, una suposición respaldada por la eficacia de los agentes trombolíticos para lisar un coágulo si se administran dentro de las 6 horas posteriores a la formación del coágulo. Tertri y sus colegas también notaron que administrar enoxaparina dentro de las 24 a 48 horas posteriores a la hemorragia intracerebral no aumentó el tamaño del hematoma, por lo que un intervalo de 24 horas probablemente sea más seguro. Otros autores recomiendan un abordaje más conservador porque la reinstitución de la terapia antitrombótica dentro de las 24 horas posteriores a un procedimiento mayor podría aumentar el riesgo de hemorragia periprocedimiento. Liew y Douketis recomiendan un mínimo de 24 horas en pacientes con bajo riesgo hemorrágico y 48 horas en aquellos con alto riesgo hemorrágico antes de reanudar dabigatrán, rivaroxabán o apixabán. Por lo tanto, las opciones son 8 horas o 24 horas menos el efecto máximo del fármaco.
Probablemente haya poca diferencia entre estas dos opciones ya que los riesgos de TEV, accidente cerebrovascular o síndrome coronario agudo probablemente sean los mismos. Además, el inicio y los tiempos de efecto máximo de los nuevos anticoagulantes son cortos.
Dabigatrán
El etexilato de dabigatrán es un profármaco que es hidrolizado por esterasas en el estómago al fármaco activo. El etexilato de dabigatrán tiene una biodisponibilidad del 7.2%. Dabigatrán es un inhibidor directo de la trombina que bloquea nerviosamente la interacción de la trombina con diversos sustratos. Las concentraciones plasmáticas máximas se alcanzan entre 1.5 y 3 horas después de la ingesta del profármaco. Tiene una vida media de 14 a 17 horas. El aclaramiento renal representa el 80% del aclaramiento total de dabigatrán. En casos de enfermedad renal terminal, la vida media de eliminación se duplica de 14 a 28 horas.
Dabigatrán es eficaz en el tratamiento de la TEV aguda y en la prevención de la TEV recurrente. En pacientes con fibrilación auricular, dabigatrán reduce las tasas de accidente cerebrovascular y embolia sistémica en un grado similar al de la warfarina. No se demostró que dabigatrán sea consistente en la prevención de TEV después de una cirugía articular total. Los estudios han demostrado que es más eficaz, no inferior o inferior a la enoxaparina. Un metanálisis de los ensayos no observó diferencias entre dabigatrán y enoxaparina en ninguno de los criterios de valoración analizados. El fabricante afirma que no se deben colocar catéteres epidurales en pacientes que reciben dabigatrán. Levy y sus colegas recomendaron un intervalo mínimo de 2 horas entre la extracción del catéter permanente y la administración de dabigatrán. Este intervalo parece ser más corto que 6 horas, es decir, la diferencia entre 8 horas menos el tiempo de 2 horas para alcanzar el efecto máximo del fármaco. Ha habido informes de aumento del sangrado después de tomar dabigatrán. La Sociedad de Hematología de Australia y Nueva Zelanda identificó 78 episodios hemorrágicos en aproximadamente 7000 pacientes durante un período de 2 meses. Sin embargo, una auditoría de la FDA concluyó que no hubo un aumento absoluto de sangrado con dabigatrán en comparación con warfarina.
El aPTT se prolonga después de dabigatrán, pero la relación es curvilínea. El tiempo de trombina (TT), también conocido como tiempo de coagulación de la trombina (TCT), es muy sensible a los efectos de dabigatrán y se usa más apropiadamente para detectar la presencia del efecto anticoagulante de dabigatrán que para cuantificar el efecto del fármaco. Un TT diluido tiene similitud en las concentraciones plasmáticas de dabigatrán farmacológicamente relevantes. El tiempo de coagulación de la ecarina (TEC), que mide directamente la generación de trombina, es dependiente de la dosis prolongado por dabigatrán. Es el ensayo más sensible para dabigatrán, pero pocas instituciones tienen la prueba disponible. El tiempo de protrombina (TP) es la prueba menos sensible. El TT diluido y el ECT son las pruebas de elección para dabigatrán.
Hasta la fecha, no existe un antídoto para revertir el efecto de dabigatrán o de los otros nuevos anticoagulantes orales. El carbón activado impide la absorción del fármaco, pero debe administrarse dentro de las 2 horas posteriores a la ingestión de dabigatrán. La diálisis podría acelerar la eliminación del fármaco. Se han sugerido concentrados de complejos plasmáticos (PCC) que contienen 3 (factores II, IX y X) o 4 (factores II, VII, IX y X) factores de coagulación, pero no se ha demostrado su eficacia. Idarucizumab, un fragmento de anticuerpo monoclonal que se une con dabigatrán libre y unido a trombina, fue aprobado recientemente por la FDA.
Consejos NYSORA
- Dabigatrán depende principalmente de los riñones para su eliminación, y su vida media se duplica en pacientes con enfermedad renal.
- En estos pacientes se recomienda un intervalo más largo entre la interrupción del fármaco y el procedimiento neuroaxial, probablemente de 6 días.
Rivaroxaban
Rivaroxabán es un inhibidor directo del factor Xa. Las concentraciones plasmáticas máximas se observan dentro de las 2.5 a 4 horas, y la inhibición máxima del factor Xa (hasta 68 %) ocurre 3 horas después de la dosificación y se mantiene durante al menos 12 horas, o 24 a 48 horas cuando se administran dosis más altas en ancianos. pacientes El rivaroxabán tiene una vida media terminal de 5.7 a 9.2 horas, pero puede durar hasta 11 a 13 horas en pacientes de edad avanzada debido a la disminución de la función renal relacionada con la edad. Un tercio del fármaco se elimina por los riñones, un tercio por la ruta fecal/biliar y un tercio se convierte en metabolitos inactivos. La concentración máxima no se ve afectada por la obesidad (pacientes que pesan ≥120 kg), pero aumenta en un 24 % en pacientes que pesan ≤50 kg. El aclaramiento renal de rivaroxabán disminuye con el aumento de la insuficiencia renal.
Rivaroxabán es eficaz en el tratamiento de la TEV sintomática y no inferior a la warfarina en la prevención del accidente cerebrovascular embólico durante la fibrilación auricular. La adición de rivaroxabán a la terapia antiplaquetaria estándar reduce el criterio de valoración compuesto de muerte por causas cardiovasculares, infarto de miocardio o accidente cerebrovascular en pacientes con un síndrome coronario agudo reciente. Se informó que el rivaroxabán es tan efectivo o superior a la enoxaparina en la prevención del TEV después de la cirugía total de la articulación. En los estudios RECORD 1, 2, 3 y 4, rivaroxabán fue un agente tromboprofiláctico más eficaz que la enoxaparina, con un perfil de seguridad similar. Rosencher et al. declaró que los catéteres epidurales no se retiraban hasta al menos 2 semividas después de la última dosis de rivaroxabán, y la siguiente dosis de rivaroxabán se administraba 4-6 horas después de retirar el catéter. Ninguno de los 1141 pacientes que recibieron rivaroxabán y anestesia neuroaxial desarrolló hematoma espinal. Sin embargo, este pequeño número de pacientes no es suficiente para llegar a una conclusión firme sobre la seguridad perioperatoria de este régimen.
Las guías europeas y escandinavas recomiendan un intervalo de 2 semividas entre la suspensión del rivaroxabán y la colocación o retirada del catéter epidural (18 horas en las guías escandinavas y 22 a 26 horas en las guías europeas). Estas guías también recomiendan un intervalo de 4 a 6 horas antes de reanudar la siguiente dosis, ya que el rivaroxabán tarda de 2.5 a 4 horas en alcanzar el efecto máximo.
Se observó una correlación lineal entre los efectos de rivaroxaban y PT. Sin embargo, existe una marcada variabilidad en la sensibilidad de los reactivos de PT a rivaroxabán, por lo que se recomienda que cada laboratorio calibre su PT específicamente para rivaroxabán. El aPTT carece de suficiente sensibilidad para determinar el efecto de rivaroxabán. La inhibición del factor Xa también puede ser un sustituto de las concentraciones plasmáticas de rivaroxabán. El PT y anti-Xa son las pruebas recomendadas para monitorizar los efectos de rivaroxabán.
Se ha recomendado el uso de carbón activado para eliminar rivaroxabán, pero debe administrarse dentro de las 8 horas posteriores a la toma de rivaroxabán. Se ha demostrado que un PCC de 4 factores revierte la actividad anticoagulante in vitro de rivaroxabán en voluntarios sanos. Debido a su alta unión a proteínas, es posible que el rivaroxabán y el apixabán no sean dializables.
Apixaban
Apixabán es un inhibidor del factor Xa altamente específico. Se absorbe rápidamente y alcanza concentraciones máximas en 1 a 2 horas. Los estudios han demostrado que la vida media terminal de apixabán es de 13.5 +/- 9.9 horas, o de 15.2 +/- 8.5 horas después de una dosis única de 5 mg y de 11.7 +/- 3.3 después de dosis múltiples de 5 mg. La concentración plasmática máxima se ve afectada por el peso corporal, con concentraciones más altas de apixabán en sujetos con bajo peso corporal. La actividad plasmática anti-factor Xa ha mostrado una relación lineal directa con la concentración plasmática de apixabán.
Apixaban tiene una biodisponibilidad oral de más del 45%. Después de la administración oral, se elimina por múltiples vías de eliminación, así como por excreción renal e intestinal directa. Veinticuatro a 29 por ciento de la dosis se excreta a través de los riñones y el 56% de la dosis se recupera en las heces. Más de la mitad de apixaban se excreta sin cambios, lo que reduce el riesgo de interacciones metabólicas entre fármacos. Apixaban es eficaz para reducir los accidentes cerebrovasculares o la embolia sistémica sin aumentar el riesgo de hemorragia. El apixabán es superior a la warfarina en la prevención de accidentes cerebrovasculares o embolias sistémicas en pacientes con fibrilación auricular. Apixabán proporciona una tromboprofilaxis eficaz en la artroplastia total de rodilla, comparable a la enoxaparina o la warfarina. El apixabán es igualmente eficaz con la enoxaparina para prevenir el TEV después de un reemplazo total de rodilla (TKR), mientras que tiene una tasa menor o similar de hemorragia mayor. El apixabán es más efectivo que la enoxaparina para prevenir el TEV después del reemplazo total de cadera (RTC) sin aumento del sangrado. En este ensayo, "los dispositivos relacionados con la anestesia intratecal o epidural se retiraron al menos 5 horas antes de la primera dosis" de apixabán. En todos los estudios de apixabán, el fármaco se inició 12 a 24 horas después de la cirugía.
En comparación con rivaroxaban, apixaban tiene poco efecto sobre el PT cuando se administra en dosis aprobadas. El ensayo de PT diluido ha mejorado la sensibilidad sobre el PT convencional. Parece haber una correlación lineal entre la actividad anti-Xa y las concentraciones plasmáticas de apixabán. Se observó que el ensayo anti-Xa es más sensible que el PT y tan sensible como el ensayo PT diluido y parece ser la mejor opción para el control clínico del efecto anticoagulante de apixabán. El carbón activado, administrado dentro de las 3 horas posteriores a la ingestión, reduce la absorción de apixabán.
Andexanet es una proteína señuelo recombinante modificada del factor Xa humano que se une y secuestra los inhibidores del factor Xa. Los estudios en voluntarios y en pacientes demostraron que andexanet reverencia la actividad anticoagulante de rivaroxabán y apixabán. A partir de 2016, andexanet aún no está clínicamente disponible en los Estados Unidos.
Resumen de recomendaciones para los nuevos anticoagulantes
Si bien un intervalo de vida media de 2 a 3 puede ser aceptable en pacientes con alto riesgo de TEV o accidente cerebrovascular, un intervalo de vida media de 4 a 6 entre la suspensión del fármaco y la inyección neuroaxial probablemente sea más seguro en la mayoría de los pacientes con dosis bajas. riesgo de trombosis. Un intervalo de vida media de 5 junto con una terapia puente de HBPM es una alternativa en la mayoría de los pacientes, como se muestra en Tabla 2. Después de un procedimiento neuroaxial o la extracción de un catéter epidural, el anticoagulante se puede reanudar 6 horas (8 horas menos el efecto de inicio/máximo del fármaco, que suele ser de 2 horas) más tarde. Los anticoagulantes generalmente se reanudan dentro de las 24 a 48 horas en la mayoría de los pacientes, pero se pueden reanudar antes en pacientes que tienen un mayor riesgo de TEV o accidente cerebrovascular; es decir, 24 horas menos el tiempo hasta el efecto máximo del fármaco. Otros recomendaron un intervalo de 24 horas (Tabla 3)
TABLA 3. Intervalos de tiempo recomendados para la reanudación del fármaco después del procedimiento neuroaxial o la extracción del catéter.
| Droga | Directrices europeas | Directrices escandinavas | Liew y Douketis (102); Connolly y Spyropoulos (98) |
|---|---|---|---|
| Dabigatrán | 6h | 6h | 24 horas |
| Rivaroxaban | 4-6h | 6h | 24 horas |
| Apixaban | 4-6h | 6h | 24 horas |
El control de laboratorio del efecto anticoagulante es apropiado en algunas situaciones, y se sugieren agentes de reversión cuando existe la necesidad de restaurar rápidamente la función hemostática.
Consejos NYSORA
- Para los nuevos anticoagulantes, se recomienda un intervalo de vida media de 5 entre la interrupción del fármaco y el procedimiento neuroaxial hasta que haya más experiencia con estos agentes.
- Se recomienda un intervalo de 8 o 24 horas hasta el efecto máximo del fármaco antes de reanudar el fármaco después de retirar el catéter; un intervalo de 24 horas es probablemente el más seguro.
CARACTERÍSTICAS CLÍNICAS, DIAGNÓSTICO Y MANEJO DEL HEMATOMA EPIDURAL
Los pacientes que desarrollan un hematoma espinal generalmente se presentan con dolor de espalda repentino, severo y constante con o sin un componente radicular. La percusión sobre la columna agrava el dolor al igual que las maniobras que aumentan la presión intraespinal, como toser, estornudar o hacer esfuerzos. Además, el regreso de la debilidad motora y/o el déficit sensorial después de la aparente resolución del bloqueo epidural o espinal es altamente sugestivo de formación de hematoma epidural o espinal. Los hallazgos motores y sensoriales dependen por completo del nivel y el tamaño del hematoma, pero pueden incluir debilidad, paresia, pérdida de la función intestinal o vesical y prácticamente cualquier déficit sensorial. La resonancia magnética nuclear (RMN) es el estudio diagnóstico de elección. El diagnóstico diferencial incluye absceso espinal, neoplasia epidural, hernia discal aguda y hemorragia subaracnoidea espinal. La recuperación sin cirugía es rara, y debe obtenerse una interconsulta neuroquirúrgica para considerar una laminectomía descompresiva de emergencia tan pronto como se sospeche un hematoma espinal. La recuperación funcional está relacionada principalmente con el tiempo que los síntomas están presentes antes de la cirugía. Las características clínicas, el diagnóstico, el diagnóstico diferencial y el tratamiento de un paciente con hematoma espinal se analizan con más detalle en Toxicidad Sistémica de Anestésicos Locales.
RESUMEN
Los médicos deben actualizar periódicamente su base de conocimientos sobre nuevos medicamentos anticoagulantes, protocolos de anticoagulación, recomendaciones de las guías actuales y alertas de la FDA. Dado que el hematoma espinal puede ocurrir incluso en ausencia de factores de riesgo identificables, la vigilancia en el control es fundamental para la evaluación temprana de la disfunción neurológica y la pronta intervención. La decisión de realizar un bloqueo neuroaxial y el momento de retirar el catéter en un paciente que recibe terapia anticoagulante debe tomarse de forma individual, sopesando los beneficios de la anestesia regional frente al riesgo pequeño, aunque definitivo, de hematoma espinal.
Anticoagulación y bloqueos de nervios periféricos
Si es apropiado, se pueden realizar bloqueos de nervios periféricos en pacientes que toman anticoagulantes. A diferencia de los procedimientos neuroaxiales en presencia de anticoagulantes, no se han realizado estudios prospectivos sobre bloqueos de nervios periféricos en presencia de anticoagulantes. La ASRA recomienda las mismas pautas para los bloqueos de nervios periféricos que para los procedimientos neuroaxiales. Se han informado casos de psoas y hematomas retroperitoneales después de bloqueos nerviosos del plexo lumbar y bloqueos nerviosos del compartimiento del psoas. Estos pacientes estaban tomando enoxaparina, ticlopidina o clopidogrel. En algunos casos, el hematoma se produjo a pesar del cumplimiento de las directrices de la ASRA.
Los síntomas de formación de hematomas después del bloqueo de nervios periféricos pueden incluir dolor (dolor en el flanco o paravertebral, o dolor en la ingle en caso de hemorragia del psoas), sensibilidad en el área, disminución constante de la hemoglobina/hematocrito, hipotensión debida a hipovolemia y déficit sensitivo-motor. El diagnóstico definitivo se realiza mediante tomografía computarizada (TC); la ecografía también se puede utilizar para detectar la presencia de hematoma subcapsular renal después del bloqueo del nervio del compartimiento del psoas. El tratamiento puede incluir interconsulta quirúrgica, reversión de la anticoagulación, transfusión de sangre según sea necesario y conducta expectante versus drenaje quirúrgico.
Probablemente sea demasiado restrictivo adaptar las directrices de la ASRA sobre bloqueos de nervios neuroaxiales a pacientes sometidos a bloqueos de nervios periféricos. La Sociedad Europea de Anestesiología ha señalado que las directrices para el bloqueo del nervio neuroaxial no se aplican de forma rutinaria a los bloqueos de los nervios periféricos. La Sociedad Austriaca de Anestesiología, Reanimación y Cuidados Intensivos, por otro lado, ha sugerido que los bloqueos nerviosos superficiales se pueden realizar con seguridad en presencia de anticoagulantes. Debido a la posibilidad de hematoma retroperitoneal, los bloqueos del plexo lumbar y de los nervios paravertebrales merecen las mismas recomendaciones que las inyecciones neuroaxiales. Las mismas pautas también deben aplicarse a los bloqueos nerviosos simpáticos viscerales. Por lo tanto, las pautas de ASRA pueden ser aplicables a bloqueos nerviosos en áreas vasculares y no comprimibles, como bloqueos nerviosos del plexo celíaco, bloqueos nerviosos del plexo hipogástrico superior y bloqueos nerviosos del plexo lumbar. Los médicos deben individualizar su decisión y discutir los riesgos y beneficios del bloqueo nervioso con el paciente y el cirujano. Lo que es más importante, el médico debe seguir de cerca al paciente después de la colocación del bloqueo nervioso.
Consejos NYSORA
- Las pautas sobre inyecciones neuroaxiales también deben aplicarse a los bloqueos nerviosos del plexo lumbar y los bloqueos nerviosos simpáticos viscerales.
- Para los bloqueos nerviosos superficiales, probablemente se pueden realizar bloqueos nerviosos regionales guiados por ecografía en presencia de anticoagulación residual.
Referencias
- Horlocker TT, Wedel DJ: Anticoagulación y bloqueo del nervio neuroaxial: perspectiva histórica, implicaciones anestésicas y gestión de riesgos. Reg Anesth Pain Med 1998;23:129–134.
- Tryba M: [Anestesia regional epidural y heparina de bajo peso molecular: Pro]. Anasthesiol Intensivmed Notfallmed Schmerzther 1993;28:179–181.
- Pöpping DM, Zahn PK, Van Aken HK, Dasch B, Boche R, Pogatzki-Zahn EM: Efectividad y seguridad del manejo del dolor posoperatorio: una encuesta de 18 925 pacientes consecutivos entre 1998 y 2006 (2.ª revisión): análisis de una base de datos de forma prospectiva datos levantados. Hermano J Anaesth 2008;101:832–840.
- Moen V, Dahlgren N, Irestedt L: Complicaciones neurológicas graves después de bloqueos neuroaxiales centrales en Suecia 1990–1999. Anestesiología 2004;101:950–959.
- Volk T, Wolf A, Van Aken H, Bürkle H, Wiebalck A, Steinfeldt T: Incidencia de hematoma espinal después de la punción epidural: análisis de la red alemana de seguridad en anestesia regional. Eur J Anaesthesiol 2012;29:170–176.
- Ehrenfeld JM, Agarwal AK, Henneman JP, Sandberg WS: Estimación de la incidencia de sospecha de hematoma epidural y el costo oculto de imágenes del cateterismo epidural: una revisión retrospectiva de 43,200 casos. Reg Anesth Pain Med 2013;38:409–414.
- Bateman BT, Mhyre JM, Ehrenfeld J, et al: El riesgo y los resultados de los hematomas epidurales después del cateterismo epidural obstétrico y perioperatorio: un informe del consorcio de investigación del grupo multicéntrico de resultados perioperatorios. Anesth Analg 2013:116:1380–1385.
- Horlocker T, Kopp S: Hematoma epidural después del bloqueo epidural en los Estados Unidos: ya no se trata solo de heparina de bajo peso molecular después de la cirugía ortopédica. Anesth Analg 2013;116:1195–1197.
- Horlocker T: Bloqueo neuroaxial en pacientes con estenosis espinal: entre la espada y la pared. Anesth Analg 2010;110:1305.
- Gulur P, Tsui B, Pathak R, Koury KM, Lee H: Análisis retrospectivo de la incidencia de hematoma epidural en pacientes con catéteres epidurales y parámetros de coagulación anormales. Hermano J Anaesth 2015;114:808–811.
- Heit JA, Horlocker TT (eds): Anestesia neuroaxial y anticoagulación. Reg Anesth Pain Med 1998;23:S129–S193.
- Horlocker TT, Wedel DJ, Benzon HT, et al: Anestesia regional en el paciente anticoagulado: Definición de los riesgos (La segunda conferencia de consenso de ASRA sobre anestesia neuroaxial y anticoagulación). Reg Anesth Pain Med 2003;28:171–197.
- Horlocker TT, Wedel DJ, Rowlingson JC, et al: Anestesia regional en el paciente que recibe terapia antitrombótica o terapia trombolítica: Directrices basadas en la evidencia de la Sociedad Estadounidense de Anestesia Regional y Medicina del Dolor (tercera edición). Reg Anesth Pain Med 2010;35:64–101.
- Gogarten W, Vandermeulen E, Van Aken H, Kozek S, Llau JV, Samama CM: Sociedad Europea de Anestesiología. Anestesia regional y agentes antitrombóticos: recomendaciones de la Sociedad Europea de Anestesiología. Eur J Anaesthesiol 2010;27:999–1015.
- Breivik H, Bang U, Jalonen J, Vigfusson G, Alahuhta S, Lagerkranser M: Directrices nórdicas para bloqueos neuroaxiales en hemostasia alterada de la Sociedad Escandinava de Anestesiología y Medicina de Cuidados Intensivos. Acta Anaesthesiol Scand 2010;54:16–41.
- Cronberg S, Wallmark E, Söderberg I: Efecto sobre la agregación plaquetaria de la administración oral de 10 analgésicos no esteroideos a humanos. Scand J Haematol 1984;33:155–159.
- Locke GE, Giorgio AJ, Biggers SL Jr, et al: Hematoma epidural espinal agudo secundario a sangrado prolongado inducido por aspirina. Surg Neurol 1976;5:293–296.
- Vandermeulen EP, Van Aken H, Vermylen J: anticoagulantes y anestesia espinal-epidural. Anesth Analg 1994;79:1165–1177.
- CLASP (Estudio Colaborativo de Aspirina en Dosis Baja en el Embarazo) Grupo Colaborativo. CLASP: un ensayo aleatorizado de aspirina en dosis bajas para la prevención y el tratamiento de la preeclampsia entre 9364 mujeres embarazadas. Lancet 1994;343:619–629.
- Horlocker TT, Wedel DJ, Offord KP: ¿La terapia antiplaquetaria preoperatoria aumenta el riesgo de complicaciones hemorrágicas asociadas con la anestesia regional? Anesth Analg 1990;70:631–634.
- Horlocker TT, Wedel DJ, Schroeder DR, et al: La terapia antiplaquetaria preoperatoria no aumenta el riesgo de hematoma espinal asociado con la anestesia regional. Anesth Analg 1995;80:303–309.
- Benzon HT, Brunner EA, Vaisrub N: Tiempo de sangrado y bloqueos nerviosos después de la aspirina. Reg Anesth 1984;9:86–90.
- Horlocker TT, Bajwa ZH, Ashraft Z, et al: Evaluación de riesgos de complicaciones hemorrágicas asociadas con medicamentos antiinflamatorios no esteroideos en pacientes ambulatorios de clínicas de dolor que se someten a inyección epidural de esteroides. Anesth Analg 2002;95: 1691–1697.
- Benzon HT, Wong HY, Siddiqui T, et al: Precaución al realizar inyecciones epidurales en pacientes con varios fármacos antiplaquetarios. Anestesiología 1999;91:1558–1559.
- Benzon HT, Huntoon M: ¿Necesitamos nuevas pautas para los procedimientos intervencionistas del dolor en pacientes con anticoagulantes? Reg Anesth Pain Med 2014;39:1–3.
- Giberson CE, Barbosa J, Brooks ES, et al: Hematomas epidurales después de la extracción de los cables de prueba del estimulador percutáneo de la médula espinal: informes de dos casos. Reg Anesth Pain Med 2014;39:73–77.
- Williams KN, Jackowski A, Evans PJD: Hematoma epidural que requiere descompresión quirúrgica después de repetidas inyecciones epidurales de esteroides cervicales para el dolor crónico. Dolor 1990;42:197–199.
- Ain RJ, Vance MB: Hematoma epidural después de la inyección epidural de esteroides en un paciente que retuvo la enoxaparina según las pautas. Anestesiología 2005;102:701–703.
- Buvanendran A, Young A: Hematoma epidural espinal después de la colocación del cable de prueba del estimulador de la médula espinal en un paciente que toma aspirina. Reg Anesth Pain Med 2014;39:70–72.
- Desai MJ, Dua S: Hematoma perineural después de la inyección de esteroides transforaminal lumbar que causa radiculopatía lumbar aguda sobre crónica: informe de un caso. Práctica del dolor 2014;14:271–277.
- Mahmoud J, Mathews M, Verna S, Basil B: Trombocitopenia inducida por oxcarbazepina. Psicosomática 2006;47:73–74.
- Meijer WEE, Heerdink ER, Nolen WA, Herings RMC, Leufkens HGM, Egberts ACG. Asociación del riesgo de sangrado anormal con el grado de inhibición de la recaptación de serotonina por parte de los antidepresivos. Arch Intern Med 2004;164:2367–2370.
- Narouze S, Benzon HT, Provenzano DA, et al: Procedimientos intervencionistas de columna vertebral y dolor en pacientes con medicamentos antiplaquetarios y anticoagulantes: pautas de la Sociedad Estadounidense de Anestesia Regional y Medicina del Dolor, la Sociedad Europea de Anestesia Regional y Terapia del Dolor, la Academia Estadounidense de Medicina del Dolor, la Sociedad Internacional de Neuromodulación, la Sociedad Norteamericana de Neuromodulación y el Instituto Mundial del Dolor. Reg Anesth Pain Med 2015;40: 182–212.
- Gajraj NM: Inhibidores de la ciclooxigenasa-2. Anesth Analg 2003; 96: 1720–1738.
- Buvanendran A, Kroin JS, Tuman KJ, et al: Efectos de la administración perioperatoria de un inhibidor selectivo de la ciclooxigenasa 2 en el manejo del dolor y la recuperación de la función después del reemplazo de rodilla: un ensayo controlado aleatorio. JAMA 2003;290:2411–2418.
- Gajraj NM, Joshi GP: Papel de los inhibidores de la ciclooxigenasa-2 en el manejo del dolor posoperatorio. Anesthesiol Clin Norteamérica 2005;23:49–72.
- Desjardins PJ, Shu VS, Recker DP, et al: Una dosis preoperatoria única de valdecoxib, un nuevo inhibidor específico de la ciclooxigenasa-2, alivia el dolor posquirúrgico oral o bunionectomía. Anestesiología 2002;97:565–573.
- Sinatra RS, Shen QJ, Halaszynski T, et al: Suspensión oral preoperatoria de rofecoxib como complemento analgésico después de una cirugía abdominal inferior: los efectos de un dolor dependiente del esfuerzo y la función pulmonar. Anesth Analg 2003;98:135–140.
- Lessee PT, Hubbard RC, Karim A, et al: Efectos de celecoxib, un nuevo inhibidor de la ciclooxigenasa-2, sobre la función plaquetaria en adultos sanos: un ensayo clínico aleatorizado. J Clin Pharmacol 2000;40:124–132.
- van Heeken H, Schwartz JI, Depre M, et al: Actividad inhibitoria comparativa de rofecoxib, meloxicam, diclofenaco, ibuprofeno y naproxeno en COX-2 versus COX-1 en voluntarios sanos. J Clin Pharmacol 2000;40:1109–1120.
- Greenberg H, Gottesdiener K, Huntington M, et al: Un nuevo inhibidor de la ciclooxigenasa-2, rofecoxib (VIOXX) no alteró los efectos antiplaquetarios de la aspirina en dosis bajas en voluntarios sanos. J Clin Pharmacol 2000;40:1509–1515.
- Psaty BM, Furberg CD: Inhibidores de la Cox-2: lecciones sobre la seguridad de los medicamentos. N Engl J Med 2005;352:1133–1135.
- Schror K: Fármacos antiplaquetarios: una revisión comparativa. Drogas 1995;50:7–28.
- Yang LH, Fareed J: Acción vasomoduladora de clopidogrel y ticlopidina. Thromb Res 1997;86:479–491.
- Comité Directivo de CAPRIE: un ensayo aleatorizado ciego de clopidogrel versus aspirina en pacientes con riesgo de accidente cerebrovascular isquémico (CAPRIE). Lancet 1996;348:1329–1339.
- Helft G, Osende JI, Worthley SG, et al: efecto antitrombótico agudo de un régimen de carga frontal de clopidogrel en pacientes con aterosclerosis en aspirina. Arterioscler Thromb Vasc Biol 2000;29:2316–2321.
- Mayumi T, Dohi S: Hematoma subaracnoideo espinal después de una punción lumbar en un paciente que recibe terapia antiplaquetaria. Anesth Analg 1983;62:777–779.
- Benzon HT, McCarthy R, Benzon HA, et al: Determinación de la actividad antiplaquetaria residual de clopidogrel. Hermano J Anaesth 2011;107: 966–971.
- Hall R, Mazer CD: Medicamentos antiplaquetarios: una revisión de su farmacología y manejo en el período perioperatorio. Anesth Analg 2011;112: 292–318.
- Wallentin L: Inhibidores de P2Y(12): diferencias en propiedades y mecanismos de acción y posibles consecuencias para el uso clínico. Eur Heart J 2009;30:1964–1977.
- Capodanno D, Ferreiro JL, Angiolillo DJ: Terapia antiplaquetaria: nuevos agentes farmacológicos y paradigmas cambiantes. J Thromb Haemost 2013;11(Suplemento 1):316–329.
- Brandt JT, Payne CD, Wiviott SD, et al: Una comparación de las dosis de carga de prasugrel y clopidogrel sobre la función plaquetaria: la magnitud de la inhibición plaquetaria está relacionada con la formación de metabolitos activos. Am Heart J 2007;153:66.e9–16.
- Dobesh PP: farmacocinética y farmacodinámica de prasugrel, un inhibidor de la tienopiridina P2Y12. Farmacoterapia 2009;29:1089–1102.
- Asai F, Jacubowski JA, Nagamura H, et al: Actividad inhibidora de plaquetas y farmacocinética de prasugrel (CS-747), un nuevo inhibidor de tienopiridina P2Y12: un estudio de dosis única ascendente en humanos sanos. Plaquetas 2006;17:209–217.
- Wiviott SD, Trenk D, Frelinger AL, et al: Prasugrel comparado con dosis altas de carga y mantenimiento de clopidogrel en pacientes con intervención coronaria percutánea planificada: el prasugrel en comparación con clopidogrel para la inhibición de la activación y agregación de plaquetas: trombólisis en el infarto de miocardio 44 prueba. Circulación 2007; 116: 2923–2932.
- Wiviott SD, Antman EM, Winters KJ, et al: Comparación aleatoria de prasugrel (CS-747, LY640315), un nuevo antagonista de tienopiridina P2Y12, con clopidogrel en la intervención coronaria percutánea: resultados de la Utilización conjunta de medicamentos para bloquear plaquetas de forma óptima (JUMBO )-ensayo TIMI 26. Circulación 2005;111:3366–3373.
- Brandt JT, Close SL, Iturria SJ, et al: Los polimorfismos comunes de CYP2C19 y CYP2C9 afectan la respuesta farmacocinética y farmacodinámica a clopidogrel pero no a prasugrel. J Thromb Haemost 2007;5:2429–2436.
- Mega JL, Close SL, Wiviott SD, et al: Polimorfismos genéticos del citocromo P450 y la respuesta a prasugrel: relación con los resultados farmacocinéticos, farmacodinámicos y clínicos. Circulación 2009;119:2553–2560.
- Teng R, Butler K: farmacocinética, farmacodinámica, tolerabilidad y seguridad de dosis únicas ascendentes de ticagrelor, un antagonista del receptor oral P2Y(12) de unión reversible, en sujetos sanos. Eur J Clin Pharmacol 2010;66:487–496.
- Teng R, Oliver S, Hayes MA, Butler K: Absorción, distribución, metabolismo y excreción de ticagrelor en sujetos sanos. Drug Metab Dispos 2010;38:1514–1521.
- Husted S, Emanuelsson H, Heptinstall S, Sandset PM, Wickens M, Peters G: farmacodinámica, farmacocinética y seguridad del antagonista oral reversible de P2Y12 AZD6140 con aspirina en pacientes con aterosclerosis: una comparación doble ciego con clopidogrel con aspirina. Eur Heart J 2006;27:1038–1047.
- Gurbel PA, Bliden KP, Butler K, et al: Evaluación aleatoria doble ciego del INICIO y DESCONEXIÓN de los efectos antiplaquetarios de ticagrelor versus clopidogrel en pacientes con enfermedad arterial coronaria estable: el estudio ONSET/OFFSET. Circulación 2009;120:2577–2585.
- George JN: Plaquetas. Lancet 2000;355:1531–1539.
- van Giezen J, Nilsson L, Berntsson P, et al: Ticagrelor se une a P2Y(12) humano independientemente del ADP, pero antagoniza la señalización del receptor inducida por ADP y la agregación plaquetaria. J Thromb Haemost 2009;7:1556–1565.
- Baron TH, Kamath PS, McBane RD: Manejo de la terapia antitrombótica en pacientes sometidos a procedimientos invasivos. N Engl J Med 2013;368:2113–2124.
- Rodgers RPC, Levin J: Una reevaluación crítica del tiempo de sangrado. Semin Thromb Hemost 1990;16:1–20.
- Ferraris VA, Swanson E: Uso de aspirina y pérdida de sangre perioperatoria en pacientes sometidos a operaciones inesperadas. Surg Gynecol Obstet 1983;156:439–442.
- Mammen EF, Comp PC, Gossselin R, et al: sistema PFA-100. Un nuevo método para la evaluación de la disfunción plaquetaria. Semin Thromb Hemost 1998;24:195–202.
- Edwards A, Jakubowski JA, Rechner AR, Sugidachi A, Harrison P: Evaluación del cartucho de prueba INNOVANCE PFA P2Y: sensibilidad al bloqueo P2Y(12) e influencia del anticoagulante. Plaquetas 2012;23: 106–115.
- Gorog DA, Fuster V: Pruebas de función plaquetaria en cardiología clínica. J Am Coll Cardiol 2013;61:2115–2129.
- Bouman HJ, Parlak E, van Werkum JW, et al: ¿Qué prueba de función plaquetaria es adecuada para monitorear la respuesta al clopidogrel? Un análisis farmacocinético sobre el metabolito activo de clopidogrel. J Thromb Haemost 2010;8:482–488.
- van Werkum JW, Harmsze AM, Elsenberg EH, Bouman HJ, ten Berg JM, Hackeng CM: El uso del sistema VerifyNow para monitorear la terapia antiplaquetaria: una revisión de la evidencia actual. Plaquetas 2008;19:479–488.
- Mueller T, Dieplinger B, Poelz W, Haltmayer M: Utilidad del instrumento PFA-100 y el novedoso analizador multiplaca para la evaluación de los efectos de la espirina y el clopidogrel en la función plaquetaria en pacientes con enfermedades cardiovasculares. Clin Appl Thromb Hemost 2009;15:652–659.
- Scharbert G, Auer A, Kozek-Langenecker S: Evaluación del ensayo de mapeo de plaquetas en tromboelastometría rotacional ROTEM. Plaquetas 2009;20:125–130.
- Malinin A, Pokov A, Swaim L, Kotob M, Serebruany V: Validación de un cartucho VerifyNow-P2Y12 para monitorear la inhibición plaquetaria con clopidogrel. Métodos Find Exp Clin Pharmacol 2006;28:315.
- Benzon HT, Avram J, Green D, Bonow RO: Nuevos anticoagulantes orales y anestesia regional. Br J Anaesth 2013;111(Suplemento 1):i96–i113.
- Kearon C, Hirsh J: Manejo de la anticoagulación antes y después de la cirugía electiva. N Engl J Med 1997;336:1506–1511.
- Harrison L, Johnston M, Massicote MP, et al: Comparación de dosis de 5 mg y 10 mg al inicio de la terapia con warfarina. Ann Intern Med 1997;126:133–136.
- Benzon HT, Benzon HA, Kirby-Nolan M, Avram MJ, Nader A: Niveles de factor VII y factores de riesgo para el aumento de la razón internacional normalizada en la fase temprana de la terapia con warfarina. Anestesiología 2010;112:298–304.
- Schulman S, Lockner D, Bergstrom K, Blomback M: anticoagulación oral inicial intensiva y tratamiento más breve con heparina en la trombosis venosa profunda. Thromb Haemost 10984;52:276–280.
- Enneking FK, Benzon HT: anticoagulantes orales y anestesia regional: una perspectiva. Reg Anesth Pain Med 1998;23:140–145.
- Odoom JA, Sih IL: Analgesia epidural y terapia anticoagulante. Anestesia 1983;38:254–259.
- Horlocker TT: Cuándo retirar un catéter espinal o epidural en un paciente anticoagulado. Reg Anesth 1993; 18:264–265.
- Horlocker TT, Wedel DJ, Schlichting JL: Analgesia epidural postoperatoria y terapia anticoagulante oral. Anesth Analg 1994;79:89–93.
- Wu CL, Perkins FM: Profilaxis con anticoagulantes orales y extracción del catéter epidural. Reg Anesth 1996;21:517–524.
- Liu SS, Buvanendran A, Viscusi ER, et al: Extracción sin complicaciones de catéteres epidurales en 4365 pacientes con índice normalizado internacional superior a 1.4 durante el inicio del tratamiento con warfarina. Reg Anesth Pain Med 2011;36:231–235.
- Weinstock DM, Chang P, Aronson DL, et al: Comparación de las concentraciones de protrombina plasmática y factor VII y protrombina F1 en orina en pacientes en tratamiento prolongado con warfarina y aquellos en fase inicial. Am J Hematol 1998;57:193–199.
- Jerkeman A, Astermark J, Hedner U, et al: Correlación entre diferentes intensidades de tratamiento antivitamina K y parámetros de coagulación. Thromb Res 2000;98:467–471.
- Abildgaard U, Lindahl AK, Sandset PM: La heparina requiere antitrombina e inhibidor de la vía extrínseca para su efecto anticoagulante en la sangre humana. Hemostasia 1991;21:254–257.
- Murray DJ, Brodsnahan WJ, Pennell B, et al: Detección de heparina por el tiempo de coagulación activado: una comparación de la sensibilidad de las pruebas de coagulación y los ensayos de heparina. J Cardiothorac Vasc Anesth 1997; 11:24–28.
- Shapiro SS. El tratamiento de la trombosis en el siglo XXI. N Engl J Med 21;2003:349–1762.
- Rao TL, El-Etr AA: Anticoagulación después de la colocación de catéteres epidurales y subaracnoideos: una evaluación de las secuelas neurológicas. Anestesiología 1981;55:618–620.
- Ruff DL, Dougherty JH: Complicaciones de la anticoagulación seguida de anticoagulación. Accidente cerebrovascular 1981; 12: 879–881.
- Liu SS, Mulroy MF: Anestesia y analgesia neuroaxial en presencia de heparina estándar. Reg Anesth Pain Med 1998;23:157–163.
- Chaney MA: Anestesia y analgesia intratecal y epidural para cirugía cardíaca. Anesth Analg 1997;84:1211–1221.
- Geerts WH, Bergqvist D, Pineo GF, et al: Prevención del tromboembolismo venoso. Directrices de práctica clínica basadas en la evidencia del American College of Chest Physicians (8ª edición). Cofre 2008;133: 381S–453S.
- King CS, Holley AB, Jackson JL, et al: Dosis de heparina dos veces versus tres veces al día para la profilaxis de la tromboembolia en la población general: un metanálisis. Cofre 2007;131:507–516.
- Weitz JI. Tratamiento farmacológico: heparinas de bajo peso molecular. N Engl J Med 1997;337:688–698.
- Horlocker TT, Heit JA: Heparina de bajo peso molecular: bioquímica, farmacología, regímenes de profilaxis perioperatoria y pautas para el manejo de la anestesia regional. Anesth Analg 1997;85:874–885.
- Bara L, Billaud E, Gramond G, et al: Farmacocinética comparativa de una heparina de bajo peso molecular (PK 10 169) y heparina no fraccionada después de la administración intravenosa y subcutánea. Thromb Res 1985;39:631–636.
- Klein S, Slaughter T, Vail PT, et al: Trombelastografía como medida perioperatoria de anticoagulación resultante de heparina de bajo peso molecular: una comparación con concentraciones de anti-Xa. Anesth Analg 2000;91:1091–1095.
- White RH: Heparinas de bajo peso molecular: ¿son todas iguales? Br J Haematol 2003;121:12–20.
- Horlocker TT, Wedel DJ: Bloqueo neuroaxial y heparina de bajo peso molecular: equilibrando la analgesia perioperatoria y la tromboprofilaxis. Reg Anesth Pain Med 1998;23:164–177.
- Administración de Drogas y Alimentos de los Estados Unidos. Comunicado de la FDA sobre la seguridad de los medicamentos: recomendaciones actualizadas para disminuir el riesgo de sangrado de la columna vertebral y parálisis en pacientes que toman heparinas de bajo peso molecular. http://www.fda.gov/drugs/drugsafety/ucm373595.htm. Actualizado el 19 de enero de 2016. Consultado el 9 de septiembre de 2015.
- Rosenquist RW, Brown DL: Hemorragia neuroaxial: fibrinolíticos/trombolíticos. Reg Anesth Pain Med 1998;23S:152–156.
- Bauer KA: Fondaparinux: propiedades básicas y eficacia y seguridad en la profilaxis del tromboembolismo venoso. Am J Orthop 2002;31:4–10.
- Turpie AG, Bauer KA, Eriksson BL, et al: Fondaparinux vs enoxaparina para la prevención del tromboembolismo venoso en cirugía ortopédica mayor: un metanálisis de 4 estudios aleatorizados doble ciego. Arch Intern Med 2002; 162: 1833–1840.
- Los investigadores de Matisse: fondaparinux subcutáneo versus heparina no fraccionada intravenosa en el tratamiento inicial de la embolia pulmonar. N Engl J Med 2003;349:1695–1702.
- Singelyn FJ, Verheyen CC, Piovella F, Van Aken HK, Rosenceher N, EXPERT Investigadores del estudio: La seguridad y eficacia de la tromboprofilaxis prolongada con fondaparinux después de una cirugía ortopédica mayor del miembro inferior con o sin un catéter neuroaxial o de nervio periférico profundo: el EXPERT Estudiar. Anesth Analg 2007;105:1540–1547.
- Rosencher N, Bonnet MP, Sessler DI: Nuevos agentes antitrombóticos seleccionados y anestesia neuroaxial para cirugía ortopédica mayor: estrategias de manejo. Anestesia 2007;62:1154–1160.
- Greenblatt DJ: Eliminación de la vida media de las drogas: valor y limitaciones. Ann Rev Med 985;36:421–427.
- Olesen JB, Lip GY, Hansen ML, et al: Validación de esquemas de estratificación de riesgo para predecir accidente cerebrovascular y tromboembolismo en pacientes con fibrilación auricular: estudio de cohorte a nivel nacional. BMJ 2011;342:d124.
- Connolly G, Spyropoulos AC: Cuestiones prácticas, limitaciones y gestión periprocedimiento de los NOAC. J Thromb Thrombolysis 2013;36:212–222.
- Garcia D, Barrett YC, Ramaciotti E, Weitz JI: Evaluación de laboratorio de los efectos anticoagulantes de la próxima generación de anticoagulantes orales. J Thromb Haemost 2013;11:245–252.
- IST-3 Collaborative Group: Los beneficios y daños de la trombólisis intravenosa con activador del plasminógeno tisular recombinante dentro de las 6 h del accidente cerebrovascular isquémico agudo (el tercer ensayo internacional de accidente cerebrovascular [IST-3]): un ensayo aleatorizado. Lancet 2012;379:2352–2363.
- Tertri S, Hakal J, Juvela S, et al: Seguridad de la enoxaparina subcutánea en dosis bajas para la prevención del tromboembolismo venoso después de una hemorragia intracerebral primaria. Thromb Res 2008;123:206–212.
- Liew A, Douketis J: Manejo perioperatorio de pacientes que reciben un nuevo anticoagulante oral. Intern Emerg Med 2013;8:477–484.
- Blech S, Ebner T, Ludwig-Schwellinger E, Stangier J, Roth W: El metabolismo y la disposición del inhibidor de trombina directo oral, dabigatrán, en humanos. Drug Metab Disposition 2008;36:386–399.
- Di Nisio M, Middeldorp S, Buller HR. Inhibidores directos de la trombina. N Engl J Med 2005;353:1028–1040.
- Levy JH, Faraoni D, Spring JL, Douketis JD, Samana CM: Manejo de nuevos anticoagulantes orales en el entorno perioperatorio y de la unidad de cuidados intensivos. Anestesiología 2013;118:1466–1474.
- Stangier J, Clemens A: Farmacología, farmacocinética y farmacodinámica del etexilato de dabigatrán, un inhibidor directo de la trombina oral. Clin Appl Thromb Hemost 2009;15(S1):9S–16S.
- Stangier J, Stahle H, Rathgen K, Fuhr R: farmacocinética y farmacodinámica del inhibidor de trombina oral directo dabigatrán en sujetos ancianos sanos. Clin Pharmacokinet 2008;47:47–59.
- Eisert WG, Hauel N, Stangier J, Wienen W, Clemens A, Van Ryn J: Dabigatrán: un inhibidor no peptídico reversible, novedoso y oral de la trombina. Arterioscler Thromb Vasc Biol 2010;30:1885–1889.
- Stangier J, Rathgen K, Stahle H, Mazur D: Influencia de la insuficiencia renal en la farmacocinética y farmacodinámica del etexilato de dabigatrán oral. Un estudio abierto, de grupos paralelos y de un solo centro. Clin Pharmacokinet 2010;49:259–268.
- Ezekowitz MD, Reilly PA, Nehmiz G, et al. Dabigatrán con o sin aspirina concomitante en comparación con warfarina sola en pacientes con fibrilación auricular no valvular (Estudio PETRO). Am J Cardiol 2007;100: 1419–1426.
- Ericksson BI, Dahl OE, Buller HR, et al; Grupo de estudio BISTRO II: un nuevo inhibidor de trombina directo oral, etexilato de dabigatrán, en comparación con enoxaparina para la prevención de eventos tromboembólicos después del reemplazo total de cadera o rodilla: el ensayo aleatorio BISTRO II. J Thromb Haemost 2005;3:103–111.
- Ericksson BI, Dahl OE, Rosencher N, et al; Grupo de estudio RE-MODEL: Etexilato de dabigatrán oral frente a enoxaparina subcutánea para la prevención del tromboembolismo venoso después del reemplazo total de rodilla: el ensayo aleatorizado RE-MODEL. J Thromb Haemost 2007;5:2178–2185.
- Ericksson BI, Dahl OE, Rosencher N, et al; Grupo de Estudio RENOVAR. Etexilato de dabigatrán versus enoxaparina para la prevención del tromboembolismo venoso después del reemplazo total de cadera: un ensayo aleatorizado, doble ciego, de no inferioridad. Lancet 2007;370:949–956.
- Comité de redacción de RE-MOBILIZE, Ginsberg JS, Davidson BL, Comp PC, et al: Inhibidor de trombina oral etexilato de dabigatrán frente al régimen de enoxaparina norteamericano para la prevención del tromboembolismo venoso después de la cirugía de artroplastia de rodilla. J Artroplastia 2009;24:1–9.
- Wolowacz SE, Roskell NS, Plumb JM, Caprini JA, Ericksson BI: Eficacia y seguridad del etaxilato de dabigatrán para la prevención del tromboembolismo venoso después de una artroplastia de cadera o rodilla. Un meta-análisis. Thromb Haemost 2009;101:77–85.
- Harper P, Young L, Merriman E: Riesgo de sangrado con dabigatrán en ancianos frágiles. N Engl J Med 2012;366:864–866.
- Tripodi A: El laboratorio y los anticoagulantes orales directos. Sangre 2013;121:4032–4035.
- Siegal DM, Cuker A: Reversión de nuevos anticoagulantes orales en pacientes con hemorragia mayor. J Thromb Thrombolysis 2013;35:391–398.
- Miyares MA, Davis K: Anticoagulantes orales más nuevos: una revisión de las opciones de monitoreo de laboratorio y agentes de reversión en el paciente hemorrágico. Am J Health Syst Pharm 2012;69:1473–1484.
- Baron TH, Kamath PS, McBane RD: Manejo de la terapia antitrombótica en pacientes sometidos a procedimientos invasivos. N Engl J Med 2013;368:2113–2124.
- Breuer G, Weiss DR, Ringwald J: "Nuevos" anticoagulantes orales directos en el entorno perioperatorio. Curr Opin Anaesthesiol 2014;27:409–419.
- Lévy S: Antitrombóticos clínicamente disponibles más nuevos y sus antídotos. J Interv Card Electrofisiol 2014;40:269–275.
- Laux V, Perzborn E, Kubitza D, Misselwitz F: Características preclínicas y clínicas de rivaroxabán: un nuevo inhibidor oral directo del factor Xa. Sem Thromb Hemost 2007;33:515–523.
- Kubitza D, Becka M, Wensing G, Voith B, Zuehlsdorf M: Seguridad, farmacodinámica y farmacocinética de BAY 59-7939, un inhibidor oral directo del factor Xa, después de dosis múltiples en sujetos masculinos sanos. Eur J Clin Pharmacol 2005;61:873–880.
- Jiang J, Hu Y, Zhang J, et al: Seguridad, farmacocinética y farmacodinámica de dosis únicas de rivaroxabán, un inhibidor oral directo del factor Xa, en sujetos chinos de edad avanzada. Thromb Haemost 2010;103:234–241.
- Kubitza D, Becka M, Roth A, Mueck W: Estudio de aumento de dosis de la farmacocinética y farmacodinámica de rivaroxabán en sujetos sanos de edad avanzada. Curr Med Res Opin 2008;24:2757–2765.
- Ericksson BI, Quinlan DJ, Weitz JI: farmacodinámica y farmacocinética comparativas de la trombina directa oral y los inhibidores del factor Xa en desarrollo. Clin Pharmacokinet 2009;48:1–22.
- Weitz JI, Eikelboom JW, Samama MM: Nuevos fármacos antitrombóticos. Cofre 2012;141S:e120S–e151S.
- Kubitza D, Becka M, Mueck W, et al: Efectos de la insuficiencia renal en la farmacocinética, la farmacodinámica y la seguridad de rivaroxabán, un inhibidor oral directo del factor Xa. Br J Clin Pharmacol 2010;70:703–712.
- Patel MR, Mahaffey KW, Garg J, et al; Investigadores de ROCKET AF: rivaroxabán versus warfarina en la fibrilación auricular no valvular. N Engl J Med 2011;365:883–891.
- Eriksson BI, Borris LC, Friedman RJ, et al; Grupo de estudio RECORD1: rivaroxabán versus enoxaparina para la tromboprofilaxis después de la artroplastia de cadera. N Engl J Med 2008;358:2765–2775.
- Kakkar AK, Brenner B, Dahl O, et al; Investigadores de RECORD2: rivaroxabán de duración extendida versus enoxaparina a corto plazo para la prevención del tromboembolismo venoso después de la artroplastia total de cadera: un ensayo controlado aleatorio doble ciego. Lancet 2008;372:31–39.
- Lassen MR, Ageno W, Borris LC, et al; Investigadores de RECORD3: rivaroxabán versus enoxaparina para la tromboprofilaxis después de la artroplastia total de rodilla. N Eng J Med 2008;358:2776–2786.
- Turpie AG, Lassen MR, Davidson BL, et al; Investigadores de RECORD4: Rivaroxaban versus enoxaparina para la tromboprofilaxis después de la artroplastia total de rodilla (RECORD4): un ensayo aleatorizado. Lancet 2009;373: 1673–1680.
- Ericksson BI, Kakkar AK, Turpie AG, et al: Rivaroxabán oral para la prevención del tromboembolismo venoso sintomático después del reemplazo electivo de cadera y rodilla. J Bone Joint Surg Br 2009;91:636–644.
- Rosencher N, Liau JV, Mueck W, Loewe A, Berkowitz SD, Homering M: Incidencia de hematoma neuroaxial después de una cirugía total de cadera o rodilla: programa RECORD (rivaroxabán frente a enoxaparina). Acta Anaesthesiol Scand 2013;57:565–572.
- Samama MM: Qué prueba usar para medir el efecto anticoagulante de rivaroxabán: el ensayo anti-factor Xa. J Thromb Haemost 2013;11:579–580.
- Raghavan N, Frost CE, Yu Z, et al: Metabolismo y farmacocinética de apixabán después de la administración oral a humanos. Drug Metab Dispos 2009;37:74–81.
- Frost C, Wang J, Nepal S, et al: Apixaban, un inhibidor oral directo del factor Xa: seguridad de dosis única, farmacocinética, farmacodinámica y efecto de los alimentos en sujetos sanos. BrJ Pharmacol 2013;75:476–487.
- Frost C, Nepal S, Wang J, et al: Seguridad, farmacocinética y farmacodinámica de múltiples dosis orales de apixabán, un inhibidor del factor Xa, en sujetos sanos. Br J Clin Pharmacol 2013;76:776–786.
- Zhang D, He K, Raghavan N, et al: Metabolismo comparativo de apixabán marcado con 14C en ratones, ratas, conejos, perros y humanos. Drug Metab Dispos 2009;37:1738–1748.
- Lassen MR, Davidson BL, Gallus A, Pineo G, Ansell J, Deitchman D: La eficacia y seguridad de apixabán, un inhibidor oral directo del factor Xa, como tromboprofilaxis en pacientes después de un reemplazo total de rodilla. J Thromb Haemost 2007;5:2368–2375.
- Lassen MR, Rasskob GE, Gallus A, Pineo G, Chen D, Portman RJ: Apixabán o enoxaparina para la tromboprofilaxis después del reemplazo de rodilla. N Engl J Med 2009;361:594–604.
- Lassen MR, Raskob GE, Gallus A, Pineo G, Chen D, Hornick P; Investigadores de ADVANCE-2: Apixabán versus enoxaparina para la tromboprofilaxis después del reemplazo de rodilla (ADVANCE-2): un ensayo aleatorizado doble ciego. Lancet 2010;375:807–815.
- Lassen MR, Gallus A, Raskob GE, Pineo G, Chen D, Ramirez LM; Investigadores de ADVANCE-3: Apixabán versus enoxaparina para la tromboprofilaxis después del reemplazo de cadera. N Engl J Med 2010;363: 2487–2498.
- Barrett YC, Wang Z, Frost C, Shenker A: Medición de laboratorio clínico de inhibidores directos del factor Xa: el ensayo anti Xa es preferible al ensayo del tiempo de protrombina. Thromb Haemost 2010;104:1263–1271.
- Kozek-Langenecker SA, Fries D, Gutl M, et al: Anestesia locorregional e inhibidores de la coagulación. Recomendaciones del grupo de trabajo sobre coagulación perioperatoria de la Sociedad Austriaca de Anestesiología y Medicina de Cuidados Intensivos. Anestesista 2005;54:476–484.
- Siegal DM, Curnutte JT, Connolly SJ, et al. Andexanet alfa para la reversión de la actividad inhibidora del factor Xa. N Engl J Med 2015;373: 2413–242

