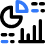Nota: Si está buscando información sobre Anestesia y Analgesia Epidural para pacientes, haga clic aquí.
Roulhac D. Toledano y Marc Van de Velde*
*Los autores desean agradecer a Michael A. Maloney, MB, BAO, ChB, por su ayuda con las tablas y figuras.
INTRODUCCIÓN
Las indicaciones clínicas para la anestesia y la analgesia epidurales se han ampliado significativamente en las últimas décadas. La analgesia epidural se usa a menudo para complementar la anestesia general (AG) para procedimientos quirúrgicos en pacientes de todas las edades con enfermedad comórbida de moderada a grave; proporcionar analgesia en el intraoperatorio, postoperatorio, periparto, y entornos al final de la vida; y se puede utilizar como anestésico primario para cirugías desde el mediastino hasta las extremidades inferiores. Además, las técnicas epidurales se utilizan cada vez más para procedimientos de diagnóstico, tratamiento del dolor agudo y tratamiento del dolor crónico. El bloqueo epidural también puede reducir la respuesta al estrés quirúrgico, el riesgo de recurrencia del cáncer, la incidencia de eventos tromboembólicos perioperatorios y, posiblemente, la morbilidad y mortalidad asociadas con la cirugía mayor.
Este capítulo cubre los aspectos esenciales de la anestesia y la analgesia epidurales. Después de una breve historia de la transformación de las técnicas de catéter epidural de inyección única a continua, revisa (1) las indicaciones y contraindicaciones del bloqueo epidural; (2) consideraciones anatómicas básicas para la colocación epidural; (3) efectos fisiológicos del bloqueo epidural; (4) farmacología de los fármacos utilizados para la anestesia y analgesia epidural; (5) técnicas para la colocación epidural exitosa; y (6) complicaciones mayores y menores asociadas con el bloqueo epidural. Este capítulo también aborda varias áreas de controversia relacionadas con las técnicas epidurales. Estos incluyen controversias sobre la anatomía del espacio epidural, la dosis de prueba de epinefrina tradicional, los métodos utilizados para identificar el espacio epidural y si los resultados clínicos particulares pueden mejorarse con técnicas epidurales en comparación con la AG. Información más detallada sobre los anestésicos locales (AL), el mecanismo de bloqueo neuroaxial, el combinado espinal-epidural (CSE) técnica, anestesia obstétricay complicaciones de bloqueo neuroaxial central se proporciona siguiendo los enlaces.
Del Compendio de anestesia regional: infografía de anestesia epidural.
BRIEF HISTORY
El neurólogo J. Leonard Corning propuso inyectar una solución anestésica en el espacio epidural en la década de 1880, pero dedicó su investigación principalmente a los bloqueos de los nervios subaracnoideos. A pesar de haber acuñado el término anestesia espinal, es posible que, sin saberlo, haya estado investigando el espacio epidural. A los médicos franceses Jean Sicard y Fernand Cathelin se les atribuye la primera administración intencional de anestesia epidural. A principios del siglo XX, introdujeron de forma independiente bloqueos nerviosos caudales de una sola inyección con cocaína para procedimientos neurológicos y genitourinarios, respectivamente.
Diecinueve años más tarde, el cirujano español Fidel Pagés Miravé describió un abordaje toracolumbar de un solo disparo para la anestesia “peridural”, identificando el espacio epidural a través de sutiles distinciones táctiles en los ligamentos. En una década y aparentemente sin el conocimiento del trabajo de Pagés, el cirujano italiano Achille Dogliotti popularizó una técnica reproducible de pérdida de resistencia (LOR) para identificar el espacio epidural. Contemporáneamente, el cirujano argentino Alberto Gutiérrez describió el “signo de la gota” para la identificación del espacio epidural.
Varias innovaciones de Eugene Aburel, Robert Hingson, Waldo Edwards y James Southworth, entre otros, intentaron prolongar la técnica epidural de un solo disparo. Sin embargo, al anestesiólogo cubano Manuel Martínez Curbelo se le atribuye la adaptación de la técnica subaracnoidea continua de Edward Tuohy para el espacio epidural en 1947. Sus esfuerzos se vieron facilitados por un amplio conocimiento de la anatomía, una experiencia de primera mano observando a Tuohy en la Clínica Mayo y la disponibilidad de Agujas Tuohy de calibre 16 y pequeños catéteres ureterales graduados de 3.5 French, que se curvaron al salir por la punta de la aguja. Desde entonces han surgido varias modificaciones de la aguja Tuohy, en sí misma una modificación de la aguja Huber.
El catéter epidural también ha evolucionado desde sus orígenes como un catéter ureteral modificado. Varios fabricantes utilizan actualmente mezclas de nailon para producir catéteres delgados, resistentes a las torceduras, con la rigidez y la resistencia a la tracción adecuadas. El catéter reforzado con alambre representa el avance tecnológico más reciente en el diseño de catéteres epidurales. La adición de una espiral circunferencial de acero inoxidable dentro de un catéter de nailon o poliuretano confiere una mayor flexibilidad en comparación con los catéteres de nailon estándar y puede disminuir la incidencia de canulación venosa, colocación intratecal, migración del catéter y parestesias.
INDICACIONES
Esta sección presenta indicaciones comunes y controvertidas para el uso del bloqueo epidural lumbar y torácico en cirugía de las extremidades inferiores, genitourinaria, vascular, ginecológica, colorrectal y cardiotorácica. También revisa indicaciones novedosas y menos comunes para la anestesia y analgesia epidural, incluso para el tratamiento de pacientes con sepsis y trastornos médicos poco comunes.Tabla 1).
TABLA 1. Ejemplos de aplicaciones para bloqueo epidural.
| Especialidad | Procedimiento quirúrgico |
|---|---|
| Cirugía Ortopédica | Cirugía mayor de cadera y rodilla, fracturas pélvicas |
| cirugía obstétrica | Parto por cesárea, analgesia de parto |
| Cirugía ginecológica | Histerectomía, procedimientos del suelo pélvico |
| Cirugía General | Cirugía mamaria, hepática, gástrica, colónica |
| Cirugía Pediátrica | Reparación de hernia inguinal, cirugía ortopédica |
| Cirugía ambulatoria | Cirugía de pie, rodilla, cadera, anorrectal |
| Cirugía cardiotorácica | Toracotomía, esofagectomía, timectomía, injerto de derivación de arteria coronaria (con y sin bomba) |
| Cirugía urológica | Prostatectomía, cistectomía, litotricia, nefrectomía |
| Cirugía vascular | Amputación de extremidades inferiores, procedimientos de revascularización |
| Condiciones médicas | Hiperreflexia autonómica, miastenia grave, feocromocitoma, hipertermia maligna conocida o sospechada |
Bloqueo epidural lumbar
La anestesia epidural se ha administrado con mayor frecuencia para procedimientos que involucran las extremidades inferiores, la pelvis, el perineo y la parte inferior del abdomen, pero se usa cada vez más como único anestésico o como complemento de la AG para una mayor diversidad de procedimientos. Esta sección examina varias indicaciones comunes para el bloqueo epidural lumbar, incluida la cirugía ortopédica de las extremidades inferiores, los procedimientos vasculares infrainguinales y las cirugías ginecológicas genitourinarias y vaginales. Cuando corresponde, revisa los beneficios y los inconvenientes del uso de técnicas neuroaxiales frente a la AG para procedimientos específicos.
Cirugía Ortopédica Mayor de las Extremidades Inferiores
Tanto la tromboprofilaxis perioperatoria con anticoagulantes como la creciente dependencia de los bloqueos de nervios periféricos han influido en el uso actual del bloqueo epidural lumbar continuo para la cirugía de las extremidades inferiores. No obstante, el bloqueo neuroaxial como único anestésico o como complemento de la AG o de las técnicas periféricas sigue siendo ampliamente utilizado para las cirugías ortopédicas mayores de las extremidades inferiores. El control efectivo del dolor posoperatorio proporcionado por bloqueos nerviosos periféricos o neuroaxiales, o una combinación de las dos técnicas, mejora la satisfacción del paciente, permite la deambulación temprana, acelera la recuperación funcional y puede acortar la estancia hospitalaria, particularmente después de una cirugía mayor de rodilla. Otros beneficios potenciales del uso del bloqueo neuroaxial en lugar de la AG incluyen la reducción de la incidencia de trombosis venosa profunda (TVP) en pacientes que se someten a una cirugía de reemplazo total de cadera y rodilla, la mejora de la función cognitiva posoperatoria y la disminución de la pérdida de sangre intraoperatoria y los requisitos de transfusión. Un metanálisis reciente también demostró una reducción estadísticamente significativa en el tiempo operatorio cuando se usó bloqueo neuroaxial en pacientes sometidos a reemplazo total de cadera electivo, aunque los autores no distinguieron entre técnicas espinales y epidurales.
Procedimientos ortopédicos mayores que se pueden realizar bajo epidural, CSEo epidural integrada y AG incluyen artroplastia primaria de cadera o rodilla, cirugía por fractura de cadera, artroplastia de revisión, artroplastia total de rodilla bilateral, injerto óseo acetabular e inserción de prótesis femorales de vástago largo (Tabla 2). Anestesia espinal puede ser la técnica preferida en algunos de estos casos, particularmente si el dolor postoperatorio anticipado es leve o insignificante (p. ej., artroplastia total de cadera) o si se planea un bloqueo de nervio periférico complementario.
TABLA 2. Cirugías ortopédicas adecuadas para anestesia epidural, combinada espinal-epidural o epidural-general integrada.
| Procedimiento | Nivel sensorial Requerido |
|---|---|
| Reducción cerrada y externa fijación de la pelvis | Técnica neuroaxial rara vez adecuado para cirugía; epidural útil para postoperatorio analgesia |
| Artroplastia de cadera, artrodesis, sinovectomía | T10 |
| Fijación interna de reducción abierta de fractura acetabular | T10 |
| Fijación interna de reducción abierta de fémur, tibia, tobillo o pie | T12 |
| Reducción cerrada y externa fijación de fémur y tibia | T12 |
| Por encima y por debajo de la rodilla amputación | T12 (T8 con torniquete) |
| artrotomía de rodilla | T12 (T8 con torniquete) |
| artroscopia de rodilla | T12 |
| Reparación/reconstrucción de rodilla ligamentos | T12 |
| Reemplazo total de rodilla | T12 (T8 con torniquete) |
| Tibia distal, tobillo y pie procedimientos | T12 |
| Artroscopia de tobillo, artrotomía, artrodesis | T12 |
| Amputación transmetatarsiana | T12 |
La anestesia a T10 con la colocación de la aguja en L3 a L4 es adecuada para la mayoría de estos procedimientos.
El uso de anestesia neuroaxial para cirugía ortopédica mayor no está exento de riesgos y desafíos. Los pacientes de edad avanzada, las víctimas de traumatismos y las personas con hemofilia que desarrollan complicaciones por sangrado recurrente en las articulaciones pueden no ser candidatos apropiados para el bloqueo regional. En general, los procedimientos epidurales son bien tolerados en pacientes con comorbilidades relacionadas con la edad, como enfermedad pulmonar restrictiva, depuración hepática prolongada de fármacos, hipertensión (HTN), arteriopatía coronaria (CAD) e insuficiencia renal. Los pacientes ancianos pueden beneficiarse de la disminución de la confusión y el delirio posoperatorios asociados con la anestesia regional, siempre que la hipotensión intraoperatoria se mantenga al mínimo. Sin embargo, la prevención de los cambios hemodinámicos inducidos por la simpatectomía excesiva puede ser un desafío, ya que estos pacientes son menos capaces de responder a la hipotensión y más propensos a la descompensación cardíaca y al edema pulmonar en respuesta a la administración rápida de líquidos. Una técnica epidural con un nivel sensorial por debajo de T10, apropiado para muchas cirugías ortopédicas, y la administración juiciosa de líquidos y vasopresores pueden minimizar estos riesgos.
Los pacientes de edad avanzada comúnmente se presentan para cirugía con medicamentos anticoagulantes o antiplaquetarios y pueden representar un riesgo de lesión neurológica relacionada con el bloqueo neuroaxial central. Si se selecciona una técnica epidural para estos u otros pacientes de alto riesgo, se debe tener en cuenta el momento adecuado tanto para el inicio del bloqueo como para la retirada del catéter en relación con el momento de la administración del fármaco anticoagulante. Para los pacientes traumatizados, lograr la posición adecuada para la administración de anestesia epidural puede presentar un desafío. El inicio del bloqueo neuroaxial en posición lateral puede mejorar las posibilidades de éxito. Intraoperatoriamente, el dolor del torniquete se puede anticipar con bloqueo espinal o epidural, pero ocurre con más frecuencia con este último. Si bien el mecanismo aún no se comprende bien, por lo general se presenta dentro de la hora posterior al inflado del torniquete, aumenta en intensidad con el tiempo y se acompaña de taquicardia y presión arterial elevada. La administración de morfina intratecal o epidural sin conservantes puede retrasar la aparición del dolor del torniquete.
Cirugía Vascular de Miembro Inferior
Hay varios beneficios potenciales del uso de anestesia y analgesia neuroaxial para procedimientos vasculares de las extremidades inferiores.
Los pacientes que se someten a cirugía vascular comúnmente tienen múltiples enfermedades sistémicas importantes, como CAD, enfermedad cerebrovascular (ECV), diabetes mellitus (DM), insuficiencia renal crónica, HTA crónica y enfermedad pulmonar obstructiva crónica (EPOC). Los pacientes que se presentan para una embolectomía arterial también pueden tener condiciones que los predisponen a la formación de trombos intracardíacos, como estenosis mitral o fibrilación auricular. Evitar la AG en esta población de pacientes de alto riesgo posiblemente mejore la permeabilidad del injerto, reduciendo la necesidad de reexploración y reduciendo el riesgo de complicaciones tromboembólicas; estas son algunas de las ventajas de usar anestesia regional. Sin embargo, el manejo de estos individuos a menudo se complica por la alta probabilidad de que estén tomando medicamentos antiplaquetarios o anticoagulantes prequirúrgicos y requerirán anticoagulación sistémica adicional durante y después de la operación. Por lo tanto, se considera que estos pacientes tienen un mayor riesgo de hematoma epidural; es necesario un análisis cuidadoso de riesgo-beneficio antes de iniciar el bloqueo epidural.
También se debe considerar el tipo de procedimiento vascular a realizar, la duración anticipada del procedimiento, la posible necesidad de monitoreo invasivo y la extracción oportuna del catéter epidural antes de la transición a la terapia de anticoagulación oral. Mantener la normotermia, garantizar que la fuerza motora pueda evaluarse rápidamente en el posoperatorio y proporcionar una sedación adecuada durante los procedimientos prolongados son desafíos adicionales.
Los procedimientos vasculares infrainguinales que son adecuados para el bloqueo epidural incluyen cirugías de derivación arterial, embolectomía arterial y trombectomía venosa o escisión de vena (Tabla 3).
TABLA 3. Ejemplos de procedimientos vasculares realizados con bloqueo epidural.
| Reparación de aneurisma aórtico abdominal (técnica neuroaxial rara vez adecuada como único anestésico) |
| Bypass aortofemoral |
| Bypass de la arteria renal |
| Bypass de la arteria mesentérica |
| Bypass arterial infrainguinal con vena safena o injerto sintético |
| embolectomía |
| Trombectomía |
| Procedimientos endovasculares (dilatación con balón intraluminal con colocación de stent; reparación de aneurismas) |
La titulación lenta de LA para alcanzar un nivel de T8-T10, mientras se mantiene la estabilidad hemodinámica, es óptima. La adición de epinefrina a los AL es controvertida debido a la preocupación de que su efecto vasoconstrictor pueda poner en peligro un suministro de sangre ya débil a la médula espinal. Los estudios hasta la fecha no han podido demostrar una diferencia en la morbilidad y mortalidad cardiovascular y pulmonar con el uso de anestesia epidural en comparación con la anestesia general para estos procedimientos, aunque las técnicas epidurales pueden ser superiores para promover la supervivencia del injerto.
Procedimientos Genitourinarios Inferiores
El bloqueo epidural lumbar como anestésico primario o como complemento de la AG es una opción adecuada para una variedad de procedimientos genitourinarios. La anestesia epidural con un nivel sensorial T9-T10 se puede usar para la resección transuretral de la próstata (TURP), aunque se puede preferir la anestesia espinal debido a su cobertura sacra mejorada, bloqueo sensorial más denso y duración más corta. Ambas técnicas se consideran superiores a la AG por varias razones, incluida la detección más temprana de cambios en el estado mental asociados con el síndrome de RTUP; la capacidad del paciente para comunicar el dolor irruptivo si se produce una complicación adversa, como la perforación de la cápsula prostática o la vejiga; el potencial de disminución del sangrado; y la disminución de los riesgos de eventos tromboembólicos perioperatorios y sobrecarga de líquidos (Tabla 4). Además, los pacientes que se presentan para esta y otras cirugías de próstata son generalmente ancianos, con múltiples comorbilidades y tienen un bajo riesgo de ciertas complicaciones del bloqueo neuroaxial, como la cefalea pospunción dural (CPPD).
TABLA 4. Beneficios del bloqueo neuroaxial central frente a la anestesia general para la resección transuretral de próstata.
| Detección temprana de cambios en el estado mental |
| Detección temprana de dolor irruptivo (indicativo de perforación capsular/vejiga) |
| Reducción de la pérdida de sangre |
| Disminución de la incidencia de trombosis venosa profunda |
| Disminución de la incidencia de sobrecarga circulatoria |
| Mejor control del dolor postoperatorio |
Otros procedimientos transuretrales, como la cistoscopia y la extracción de cálculos ureterales, se pueden realizar bajo anestesia general, anestesia tópica o bloqueo neuroaxial, según la extensión y la complejidad del procedimiento, las comorbilidades del paciente y la preferencia del paciente, el anestesiólogo y el cirujano. Cabe destacar que los pacientes parapléjicos y tetrapléjicos comprenden un subconjunto de pacientes que se presentan para cistoscopias repetidas y procedimientos de extracción de cálculos; A menudo se prefiere la anestesia neuroaxial en estos pacientes debido al riesgo de hiperreflexia autonómica (AH) (consulte la sección separada sobre este tema).
Debido a que estos procedimientos se realizan de forma ambulatoria, debe evitarse el bloqueo epidural residual prolongado. Aunque existe cierta variabilidad interindividual, se requiere un nivel sensorial tan alto como T8 para los procedimientos que involucran los uréteres, mientras que un nivel sensorial T9-T10 es apropiado para los procedimientos que involucran la vejiga.Tabla 5).
TABLA 5. Nivel sensorial requerido para procedimientos genitourinarios.
| Procedimiento | Nivel sensorial requerido |
|---|---|
| Nefrectomía | Considerar anestesia general-epidural combinada |
| Cistectomía | T4 |
| Choque litotricia extracorpórea por ondas | T6 |
| Prostatectomía abierta | T8 |
| Extracción de cálculos ureterales | T8 |
| La cistoscopia | T9 |
| Resección transuretral de próstata | T9 |
| Cirugía que involucra testículos | T10 |
| Cirugía que involucra el pene | L1 |
| Procedimientos uretrales | bloque sacro |
Cirugías Ginecológicas Vaginales
Se pueden realizar varias cirugías ginecológicas vaginales con bloqueo epidural, aunque puede ser más apropiado el bloqueo espinal o GA de una sola inyección y, en algunos casos, el bloqueo nervioso paracervical o la anestesia tópica (Tabla 6). Se puede realizar una dilatación y curetaje (D&C) bajo bloqueo nervioso paracervical, AG o bloqueo neuroaxial.
TABLA 6. Procedimientos ginecológicos vaginales adecuados para bloqueo epidural.
| Dilatación y legrado |
| Histeroscopia (con o sin medios de distensión) |
| Procedimientos de incontinencia urinaria |
| Histerectomía |
Si se selecciona anestesia neuroaxial, es apropiado un nivel sensorial T10. Si bien la histeroscopia diagnóstica ambulatoria se puede realizar bajo AL, la histeroscopia con medios de distensión generalmente requiere anestesia general o neuroaxial.
La anestesia epidural puede tener la desventaja de aumentar la absorción de glicina en comparación con la anestesia general. Sin embargo, los cambios en el estado mental relacionados con la absorción de la solución de irrigación hipotónica se detectan más fácilmente en pacientes despiertos. Para los procedimientos de incontinencia urinaria, la anestesia epidural ofrece la ventaja de permitir que el paciente participe en la prueba de tos intraoperatoria, lo que teóricamente disminuye el riesgo de disfunción miccional posoperatoria, aunque la incidencia de este resultado adverso no parece aumentar con la AG. Un nivel sensorial T10 proporciona suficiente anestesia para los procedimientos de la vejiga, pero el nivel debe extenderse a T4 si se abre el peritoneo. La histerectomía vaginal se puede realizar bajo anestesia general o neuroaxial (más comúnmente espinal). Un nivel sensorial T4-T6 es apropiado para los procedimientos uterinos.
Anestesia y analgesia epidural torácica
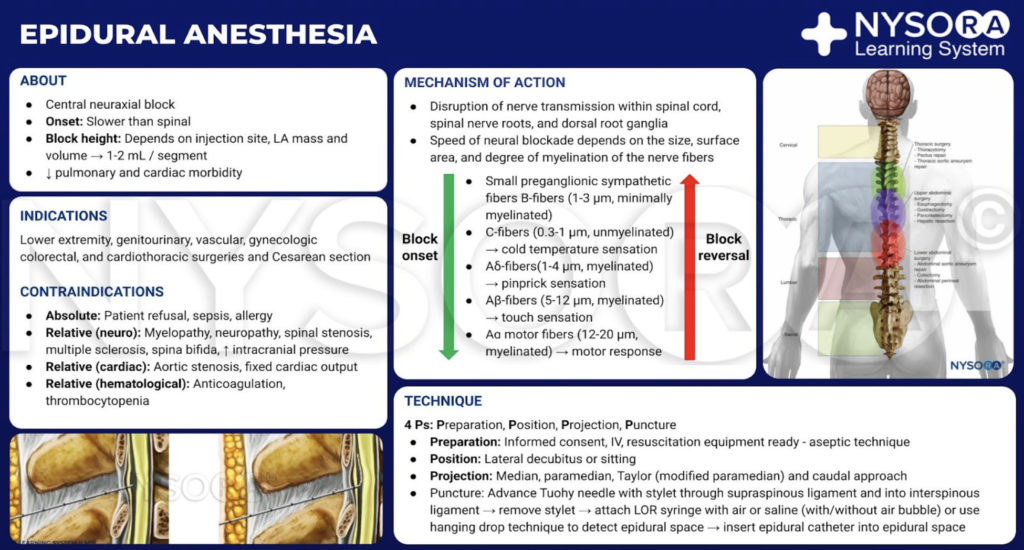
Los beneficios y las indicaciones de la anestesia epidural torácica (TEA) se están expandiendo (Tabla 7). TEA ofrece una analgesia perioperatoria superior en comparación con los opioides sistémicos, disminuye las complicaciones pulmonares posoperatorias, disminuye la duración del íleo posoperatorio y disminuye la mortalidad en pacientes con fracturas costales múltiples, entre otras cosas. Esta sección explora el papel de la TEA como anestésico primario o como adyuvante de la AG para cirugía cardíaca, torácica, abdominal, colorrectal, genitourinaria y ginecológica (Figura 1 y XNUMX). También revisa el papel cada vez mayor de TEA para la cirugía torácica asistida por video (VATS) y la cirugía laparoscópica.
TABLA 7. Beneficios de la anestesia y analgesia epidural torácica.
| Analgesia perioperatoria mejorada en comparación con otros modalidades |
| Disminución de las complicaciones pulmonares postoperatorias |
| Disminución de la duración del íleo postoperatorio |
| Disminución de la duración de la ventilación mecánica |
| Disminución de la mortalidad en pacientes con fracturas costales |
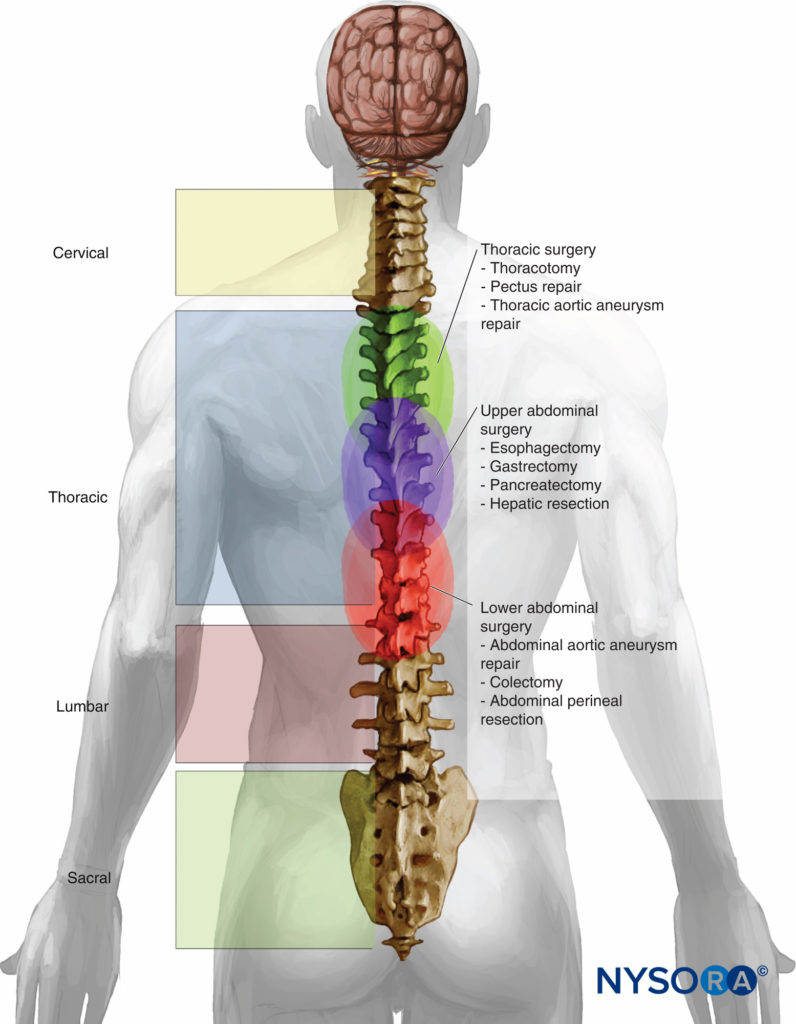
Figura 1 y XNUMX. Nivel de colocación en cirugías realizadas con anestesia y analgesia epidural torácica.
Cirugía Cardiaca
El TEA alto (bloqueo de los cinco segmentos torácicos superiores) como adyuvante de la AG en cirugía cardíaca con derivación cardiopulmonar (CEC) ha ganado interés en las últimas décadas. Los supuestos beneficios incluyen una mejor distribución del flujo sanguíneo coronario, una menor demanda de oxígeno, una mejor función regional del ventrículo izquierdo, una reducción en la incidencia de arritmias supraventriculares, atenuación de la respuesta al estrés quirúrgico, una mejor estabilidad hemodinámica intraoperatoria, una recuperación más rápida de la conciencia, una mejor analgesia posoperatoria, y una reducción de las complicaciones renales y pulmonares postoperatorias.
Varios de estos beneficios potenciales pueden atribuirse al bloqueo selectivo de la inervación simpática cardíaca (los segmentos espinales T1-T4). Sin embargo, la inserción de un catéter epidural en pacientes que requieren heparinización completa para CPB conlleva el riesgo de hematoma epidural.
La evidencia a favor de la TEA alta para la cirugía cardíaca no es concluyente. Un estudio realizado por Liu y colegas que comparó TEA con GA tradicional basado en opioides para injerto de derivación de arteria coronaria (CABG) con CEC no encontró diferencias en las tasas de mortalidad o infarto de miocardio, pero demostró una reducción estadísticamente significativa en el riesgo de arritmias cardíacas posoperatorias y complicaciones pulmonares, puntuaciones de dolor mejoradas y extubación traqueal más temprana en el grupo TEA. Por el contrario, un ensayo de control aleatorizado reciente que comparó los efectos clínicos de la AG de vía rápida con TEA versus la AG de vía rápida sola en más de 600 pacientes que se sometieron a cirugía cardíaca electiva (tanto con bomba como sin bomba) no encontró diferencias estadísticamente significativas en 30 días. supervivencia libre de infarto de miocardio, complicaciones pulmonares, insuficiencia renal o accidente cerebrovascular. La duración de la ventilación mecánica, la duración de la estancia en la unidad de cuidados intensivos (UCI), la duración de la estancia en el hospital y la calidad de vida a los 30 días de seguimiento también fueron similares para los dos grupos. En general, el papel de la TEA como adyuvante de la AG para la cirugía cardíaca con CEC sigue siendo controvertido.
El papel de la TEA alta en la cirugía de derivación de la arteria coronaria sin circulación extracorpórea (OPCAB, por sus siglas en inglés) también se debate en la literatura. TEA ofrece las ventajas de evitar la intubación de la tráquea en casos seleccionados de CABG, extubación más temprana en pacientes que reciben AG y reducción del dolor y la morbilidad posoperatoria. Sin embargo, persisten las preocupaciones sobre la ventilación comprometida con un bloqueo sensorial alto, hipotensión debido a simpaticolisis y hematoma epidural, a pesar de la dosis de heparina muy reducida en comparación con los casos de CEC. Un reciente ensayo prospectivo, aleatorizado y controlado de más de 200 pacientes sometidos a cirugía OPCAB encontró que la adición de TEA alta a la AG redujo significativamente la incidencia de arritmias posoperatorias, mejoró el control del dolor y mejoró la calidad de la recuperación. Hasta que se disponga de datos de resultados más definitivos, el papel de las técnicas neuroaxiales en la cirugía OPCAB sigue siendo incierto.
Procedimientos quirúrgicos torácicos y abdominales superiores
La anestesia y la analgesia epidurales se usan comúnmente para la cirugía torácica y del abdomen superior, incluidas la gastrectomía, la esofagectomía, la lobectomía y los procedimientos de la aorta torácica descendente.Tabla 8).
TABLA 8. Indicaciones de anestesia y analgesia epidural torácica.
| Región anatómica | Procedimiento |
|---|---|
| Tórax | Toracotomía |
| Reparación de pectus |
|
| Reparación de aneurisma torácico |
|
| Timctomía |
|
| Cirugía torácica asistida por video | |
| Abdomen superior | esofagectomía |
| gastrectomía |
|
| Pancreatectomía |
|
| colecistectomía |
|
| Resección hepática | |
| Abdomen bajo | Reparación de aneurisma de aorta abdominal |
| Colectomía |
|
| Resección intestinal |
|
| Resección abdominal perineal | |
| urogenital/ ginecológico | Cistectomía |
| Nefrectomía |
|
| Reparación ureteral |
|
| Prostatectomía radical abdominal |
|
| Reducción de tumores de ovario |
|
| Exenteración pélvica |
|
| Histerectomía abdominal total |
Se usa con menos frecuencia para VATS, a menos que se anticipe mucho la conversión a un procedimiento abierto o si el paciente tiene un alto riesgo de complicaciones por la AG. El bloqueo epidural para muchos de estos procedimientos suele servir como adyuvante de la AG y como componente esencial del tratamiento del dolor posoperatorio. Sin embargo, la administración concomitante de TEA alta con GA conlleva riesgos de bradicardia intraoperatoria, hipotensión y cambios en la resistencia de las vías respiratorias. Existe cierto debate sobre si se requiere la activación intraoperatoria del bloqueo epidural para apreciar los beneficios analgésicos de la TEA o si la activación posoperatoria produce beneficios equivalentes. Una revisión sistemática realizada por Møiniche y colegas encontró que el momento de varios tipos de analgesia, incluidos los analgésicos epidurales, los opioides intravenosos y los LA periféricos, no influyó en la calidad del control del dolor posoperatorio.
La anestesia epidural torácica iniciada en la región torácica media a superior también se puede utilizar para procedimientos de mama. Los beneficios pueden incluir analgesia posoperatoria superior, menor incidencia de náuseas y vómitos posoperatorios (NVPO), mayor satisfacción del paciente y evitar la intubación traqueal en pacientes con comorbilidades moderadas a graves. El nivel sensorial requerido depende del procedimiento: un nivel que se extienda desde T1 a T7 es adecuado para el aumento de senos; Se requiere C5-T7 para la mastectomía radical modificada; y C5-L1 se requiere para la mastectomía con reconstrucción con colgajo transverso del recto abdominal miocutáneo (TRAM) (Tabla 9). El catéter epidural se puede introducir en T2-T4 para lograr el bloqueo segmentario de los dermatomas torácicos para la mayoría de los procedimientos mamarios; la colocación en T8-T10 es adecuada para la reconstrucción con colgajo TRAM.
TABLA 9. Nivel sensorial requerido para los procedimientos mamarios.
| La cirugía | Segmentario bloquear |
|---|---|
| Mastectomía radical modificada | C5-T7 |
| Mastectomía con recto transverso colgajo abdominal | C5-L1 |
| mastectomía parcial; aumento de senos | T1 – T7 |
El bloqueo epidural proporciona un adyuvante útil a la AG para procedimientos dentro de la cavidad torácica, como cirugía pulmonar y esofágica. Los beneficios de la TEA para estos procedimientos incluyen analgesia postoperatoria mejorada; morbilidad pulmonar reducida (p. ej., atelectasia, neumonía e hipoxemia); resolución rápida del íleo postoperatorio; y disminución del catabolismo posoperatorio, que puede preservar la masa muscular. El bloqueo epidural segmentario de T1-T10 proporciona un bloqueo sensorial de la incisión de la toracotomía y el sitio de inserción del tubo torácico.
Las cirugías abdominales superiores que se pueden realizar con anestesia epidural y analgesia incluyen esofagectomía, gastrectomía, pancreatectomía, resección hepática y colecistectomía. También se han informado colecistectomía laparoscópica con bloqueo epidural30 y gastrectomía distal con anestesia general-epidural combinada. La colocación de un catéter epidural mediotorácico con bloqueo segmentario que se extiende desde T5 (T4 para cirugía laparoscópica) a T8 es apropiada para la mayoría de los procedimientos abdominales superiores y, debido a la preservación de la raíz nerviosa lumbar y sacra, tiene un riesgo mínimo de déficits motores en las extremidades inferiores, retención urinaria, hipotensión, y otras secuelas de la anestesia epidural lumbar.
Procedimientos Vasculares Suprainguinales
Una epidural mediotorácica superior se puede utilizar como adyuvante de la AG para cirugías de la aorta abdominal y sus principales ramas. El bloqueo epidural para la derivación aortofemoral, la derivación de la arteria renal y la reparación de aneurismas de la aorta abdominal puede proporcionar un mejor control del dolor posoperatorio, facilitar la extubación temprana de la tráquea, permitir la deambulación temprana y disminuir el riesgo de eventos tromboembólicos en pacientes que tienen un riesgo particularmente alto de esta complicada complicación. Sin embargo, el bloqueo epidural intraoperatorio puede complicar el manejo de los cambios hemodinámicos asociados con el pinzamiento y desbloqueo de la aorta, así como comprometer la evaluación temprana de la función motora en el período posoperatorio inmediato. Se necesita un nivel sensorial de T6 a T12 para una incisión abdominal extensa; se requiere un nivel que se extienda desde T4 a T12 para lograr la denervación de las vísceras.
Litotricia extracorpórea por ondas de choque, prostatectomía, cistectomía, nefrectomía
La litotricia extracorpórea por ondas de choque (ESWL) con o sin inmersión en agua se puede realizar bajo anestesia general o neuroaxial. Es necesario un nivel sensorial T6-T12 cuando se seleccionan técnicas neuroaxiales. El bloqueo epidural se asocia con menos hipotensión intraoperatoria que la raquídea de un solo disparo, aunque ambas técnicas sirven para evitar la AG en pacientes de alto riesgo potencial.
La cirugía abierta de próstata, la cistectomía radical y derivación urinaria, y la nefrectomía simple, parcial y radical se pueden realizar bajo bloqueo neuroaxial, ya sea solo o en combinación con AG, según el procedimiento. Algunas ventajas potenciales de la neuroaxial en comparación con la AG para la prostatectomía radical retropúbica incluyen la disminución de la pérdida de sangre y transfusiones intraoperatorias, la disminución de la incidencia de eventos tromboembólicos posoperatorios, la mejora de la analgesia y el nivel de actividad hasta 9 semanas después de la operación, el retorno más rápido de la función intestinal y varias otras ventajas. -ventajas controvertidas de la anestesia neuroaxial, como un tiempo más rápido para el alta hospitalaria y costos hospitalarios reducidos. Para el procedimiento abierto, los pacientes pueden requerir una sedación generosa en ausencia de una técnica neuroaxial general combinada. Se requiere nivel sensitivo T6, con colocación de catéter en región torácica media. La cistectomía radical se realiza en pacientes con cáncer de vejiga invasivo y puede tener mejores resultados con una combinación de anestesia general y epidural en comparación con la AG sola.
El bloqueo epidural puede proporcionar hipotensión controlada intraoperatoriamente, lo que contribuye a disminuir la pérdida de sangre y optimizar el alivio del dolor posoperatorio. Una epidural torácica media con un nivel sensorial T6 es apropiada. Aunque a menudo se requiere AG para la nefrectomía radical debido a la preocupación por la posición del paciente, la hipotensión intraoperatoria y la posibilidad de una pérdida significativa de sangre intraoperatoria, la analgesia epidural proporciona un alivio del dolor posoperatorio más eficaz que los opioides sistémicos y evita los efectos adversos de estos últimos.
Varias otras cirugías relacionadas con la urología se pueden realizar con bloqueo neuroaxial como único anestésico o como adyuvante de la AG. El uso de una técnica epidural-AG combinada en pacientes con tumores suprarrenales funcionales sometidos a adrenalectomía laparoscópica es seguro y eficaz y puede tener el beneficio adicional de minimizar las fluctuaciones en los niveles hormonales. Cabe señalar, sin embargo, que el bloqueo epidural puede no disminuir los efectos presores de la estimulación tumoral directa. También se ha informado el uso de anestesia epidural para biopsia laparoscópica retroperitoneal en pacientes que no son candidatos para biopsia percutánea.
Cirugías Abdominales Inferiores y Ginecológicas
La histerectomía abdominal total a menudo se realiza bajo AG, una anestesia epidural general combinada o anestesia neuroaxial con o sin sedación. Aunque todavía no es una rutina, la laparoscopia ginecológica se realiza cada vez más bajo anestesia neuroaxial, por lo general con inclinación de Trendelenburg disminuida, presiones de insuflación de CO2 reducidas (por debajo de 15 mm Hg) y opioides suplementarios o antiinflamatorios no esteroideos (NSAID, por sus siglas en inglés) para minimizar el dolor de hombro referido. El bloqueo epidural para procedimientos abiertos tiene las ventajas de proporcionar una analgesia postoperatoria prolongada, disminuir la incidencia de NVPO y eventos tromboembólicos perioperatorios, e influir potencialmente en la función inmunitaria perioperatoria y, de manera relacionada, la recurrencia del cáncer en pacientes sometidas a histerectomía por cáncer de ovario o relacionado. El efecto de analgesia preventiva propuesto proporcionado por el bloqueo neuroaxial durante la histerectomía abdominal requiere más investigación. Un nivel sensorial que se extiende a T4 o T6 proporciona suficiente anestesia para los procedimientos que involucran el útero. Es apropiada la inserción de un catéter epidural en la región lumbar con grandes volúmenes de AL para elevar el nivel sensorial o la colocación torácica baja o media. El dolor visceral relacionado con la manipulación intestinal y peritoneal disminuye a medida que aumenta el nivel del bloqueo; un nivel de T3–T4 puede ser óptimo.
La colectomía abierta y laparoscópica, la sigmoidectomía y la apendicectomía se encuentran entre otras cirugías abdominales inferiores que se pueden realizar bajo anestesia neuroaxial, con o sin AG. De particular interés en pacientes sometidos a cirugía intestinal, el bloqueo epidural torácico disminuye la duración del íleo posoperatorio, posiblemente sin afectar la cicatrización anastomótica y la fuga. La analgesia postoperatoria superior asociada con las infusiones epidurales continuas, con o sin opioides, muy probablemente mejore la función pulmonar postoperatoria en pacientes sometidos a cirugía gastrointestinal (GI), aunque no se han realizado ensayos controlados aleatorios específicos. En combinación con la alimentación temprana y la deambulación, la TEA desempeña un papel en el alta hospitalaria temprana después de ciertas cirugías gastrointestinales. Se ha demostrado un resultado similar después de la resección colónica laparoscópica, seguida de analgesia epidural durante 2 días y nutrición oral temprana y movilización (es decir, rehabilitación multimodal). La colocación de un catéter epidural entre T9 y T11 suele ser adecuada para los procedimientos abdominales inferiores; se requiere un bloqueo sensorial que se extienda a T7 o T9 para la mayoría de las cirugías colónicas (resección sigmoidea, ileotransversostomía, hemicolectomía).
Trastornos médicos poco comunes y escenarios clínicos
La anestesia y la analgesia epidurales también pueden estar indicadas en el manejo perioperatorio de pacientes con condiciones médicas específicas o enfermedades coexistentes, como miastenia grave (MG), AH, hipertermia maligna (HM), EPOC, feocromocitoma (consulte la discusión anterior) y septicemia. Varios otros subgrupos de pacientes pueden beneficiarse de las técnicas de catéter epidural continuo, incluidas las pacientes de cuidados paliativos, las parturientas con comorbilidades y las pacientes con riesgo de neoplasias malignas recurrentes.
Miastenia Gravis
Los pacientes con MG plantean desafíos particulares para los anestesiólogos, incluidas las respuestas anormales a los agentes bloqueadores neuromusculares despolarizantes y no despolarizantes; dificultad potencial para revertir el bloqueo neuromuscular residual en pacientes que toman inhibidores de la colinesterasa; requisitos prolongados de ventilación mecánica posoperatoria; riesgo de insuficiencia respiratoria posquirúrgica; y preocupaciones sobre el manejo del dolor posoperatorio. El bloqueo epidural elimina la necesidad de relajantes musculares intraoperatorios en pacientes miasténicos y proporciona un alivio del dolor posoperatorio superior en comparación con los opioides, al mismo tiempo que minimiza el riesgo de depresión respiratoria inducida por opioides y disfunción pulmonar. Debido a la posibilidad de que el metabolismo del éster LA se prolongue en pacientes que toman inhibidores de la colinesterasa, se puede preferir la amida LA para el tratamiento de pacientes miasténicos. También pueden ser apropiadas dosis reducidas de LA. Las preocupaciones por comprometer la función respiratoria de un paciente miasténico con una epidural alta parecen ser infundadas.
Hiperreflexia autonómica
Las técnicas epidurales son apropiadas para el manejo perioperatorio de pacientes con HA. La AH ocurre hasta en 85% de los pacientes con lesiones de la médula espinal en T4-T7 o más como resultado de la actividad simpática desinhibida. En respuesta a la estimulación visceral o cutánea por debajo del nivel de la lesión y en ausencia de inhibición central descendente, los pacientes pueden desarrollar una hiperactividad simpática extrema aguda. En general, se produce una vasoconstricción intensa por debajo del nivel de la lesión de la médula espinal, con vasodilatación por encima. Los pacientes pueden experimentar sudoración, náuseas, sofocos, palidez, escalofríos, obstrucción nasal, visión borrosa, dolor de cabeza, dificultad para respirar, convulsiones y arritmias cardíacas. La bradicardia refleja se observa en la mayoría de los casos. La hipertensión arterial grave que pone en peligro la vida puede provocar hemorragia intracraneal, isquemia miocárdica, edema pulmonar y muerte. El bloqueo epidural como único anestésico, como complemento de la AG o para la analgesia del trabajo de parto atenúa las perturbaciones fisiológicas asociadas con la AH, aunque el bloqueo nervioso incompleto de los segmentos sacros o los segmentos perdidos pueden contribuir a una alta tasa de fracaso. La anestesia espinal, cuyo nervio bloquea la rama aferente de este reflejo potencialmente letal, y la AG profunda previenen de manera más confiable la HA.
Hipertermia maligna
El manejo anestésico de la HM presenta un desafío para el anestesiólogo. La HM es un síndrome clínico de metabolismo marcadamente acelerado desencadenado principalmente por agentes volátiles y el agente despolarizante succinilcolina. Los pacientes susceptibles pueden desarrollar fiebre, taquicardia, hipercarbia, taquipnea, arritmias, hipoxemia, sudoración profusa, HTA, mioglobinuria, acidosis mixta y rigidez muscular en respuesta a la exposición a agentes volátiles o succinilcolina, aunque se han notificado casos en los que no hay evidencia agente desencadenante. Las complicaciones tardías pueden incluir coagulopatía de consumo, insuficiencia renal aguda, necrosis muscular, edema pulmonar y secuelas neurológicas. Evitar la exposición a los agentes desencadenantes es una piedra angular en el manejo de los pacientes susceptibles a la HM.
Siempre que sea adecuado, se recomiendan bloqueos nerviosos neuroaxiales locales, periféricos o centrales, ya que se informa que estas técnicas son más seguras que el uso de AG. Tanto los LA de éster como los de amida se consideran seguros en pacientes susceptibles a HM, al igual que la epinefrina, aunque persiste la controversia en la literatura.
Afección pulmonar obstructiva crónica
El bloqueo epidural es una opción anestésica razonable para pacientes con EPOC someterse a una cirugía mayor debido a la preocupación por la ventilación mecánica prolongada. Sin embargo, si las técnicas epidurales reducen las complicaciones pulmonares en pacientes con EPOC no es conocido. En un análisis controlado por propensión reciente de más de 500 pacientes con EPOC sometidos a cirugía abdominal, la analgesia epidural como adyuvante de la AG se asoció con una reducción estadísticamente significativa del riesgo de neumonía posoperatoria. Los pacientes con el tipo más grave de EPOC se beneficiaron de manera desproporcionada. El estudio también encontró un efecto beneficioso no significativo de la analgesia epidural sobre la mortalidad a los 30 días, una tendencia que se ha demostrado en otros estudios.
Cirugía Pediátrica
Existe una cantidad considerable de literatura dedicada al uso de la anestesia regional para la cirugía pediátrica tanto en el ámbito hospitalario como ambulatorio. Las ventajas del bloqueo neuroaxial para la población pediátrica incluyen analgesia postoperatoria óptima, que es particularmente importante en la reparación de escoliosis extensa, reparación de pectus excavatum y procedimientos abdominales y torácicos mayores; disminución de los requisitos de GA; despertar más temprano; y alta más temprana en el entorno ambulatorio. Ciertos subgrupos de pacientes pediátricos, como aquellos con fibrosis quística, antecedentes familiares de HM o antecedentes de prematuridad, también se benefician del uso de anestesia neuroaxial en lugar de AG. Sin embargo, la negativa de los padres, las preocupaciones sobre la realización de bloqueos nerviosos regionales en pacientes anestesiados y las preocupaciones sobre las vías respiratorias en pacientes con reservas de oxígeno limitadas plantean desafíos para el uso rutinario del bloqueo neuroaxial en esta población de pacientes.
El abordaje caudal de un solo disparo al espacio epidural, con o sin sedación, se usa comúnmente en pacientes pediátricos para una variedad de cirugías, que incluyen circuncisión, reparación de hipospadias, herniorrafia inguinal y orquidopexia.
Los catéteres caudales continuos pueden avanzar en dirección cefálica a niveles vertebrales más altos y usarse como único anestésico o como adyuvante de la AG. La anestesia lumbar y la TEA proporcionan un bloqueo sensorial más confiable a niveles segmentarios más altos en niños mayores. Ver "Anestesia regional en pacientes pediátricos: consideraciones generales” para una discusión más detallada de bloqueos nerviosos caudales y Anestesia Caudal.
Cirugía Ambulatoria
La anestesia raquídea o los bloqueos de nervios periféricos son preferibles a las técnicas epidurales para la mayoría de los escenarios clínicos en el entorno ambulatorio debido a la preocupación por el inicio relativamente lento del bloqueo epidural, la retención urinaria, la inmovilidad prolongada, la CPPD y el retraso en el alta. El uso de AL de acción corta, cuando corresponda, puede obviar estas preocupaciones. Las técnicas epidurales tienen las ventajas de permitir una titulación lenta de los AL, la capacidad de adaptar la altura y la duración del bloqueo nervioso al procedimiento quirúrgico y un menor riesgo de síntomas neurológicos transitorios (TNS) en comparación con la anestesia espinal. La artroplastia total de cadera, la artroscopia de rodilla, la cirugía del pie, la herniorrafia inguinal, la laparoscopia pélvica y los procedimientos anorrectales se encuentran entre las muchas cirugías ambulatorias que se pueden realizar con bloqueo neuroaxial como anestesia principal. Para obtener información sobre el bloqueo regional en el entorno ambulatorio, consulte: Bloqueos de nervios periféricos para cirugía ambulatoria.
Analgesia y Anestesia Laboral
Las parturientas comprenden el grupo más grande que recibe analgesia epidural. Para un adecuado alivio del dolor durante la primera etapa del trabajo de parto, es necesaria la cobertura de los dermatomas desde T10 hasta L1; la analgesia debe extenderse caudalmente a S2-S4 (para incluir el nervio pudendo) durante la segunda etapa del trabajo de parto. La colocación epidural en el espacio intermedio L3-L4 es más común en pacientes en trabajo de parto.
Sin embargo, los puntos de referencia anatómicos de la superficie pueden ser difíciles de apreciar en pacientes obstétricas y es posible que no identifiquen de manera confiable el espacio intermedio deseado en este subgrupo de pacientes debido tanto a la rotación anterior de la pelvis como a la lordosis lumbar exagerada. Varios otros factores pueden afectar la facilidad de la colocación epidural y la propagación de los LA administrados por vía epidural en parturientas, incluida la congestión de las venas epidurales, los niveles hormonales elevados y el aumento de peso excesivo. Referirse a "Anestesia Regional Obstétrica” para obtener información adicional sobre las técnicas epidurales en pacientes en trabajo de parto.
Observaciones
Han surgido varias aplicaciones no anestésicas para los procedimientos epidurales. Las técnicas de infusión de catéter epidural se utilizan cada vez más para controlar el dolor al final de la vida tanto en niños como en adultos, incluidos aquellos con dolor relacionado con el cáncer. También hay un interés en evolución sobre si la anestesia y la analgesia epidurales pueden tener un papel protector en la sepsis. De particular interés es si los pacientes en estado crítico pueden beneficiarse del aumento de la perfusión y oxigenación de los órganos esplácnicos, así como de la inmunomodulación, que se observa en pacientes sanos que han recibido anestesia epidural. Sin embargo, se necesitan estudios adicionales para evaluar el riesgo y los beneficios de las técnicas epidurales en la sepsis. Otra aplicación novedosa para los AL epidurales propone que las infusiones continuas pueden mejorar el flujo sanguíneo placentario en parturientas con perfusión uterina crónicamente comprometida y restricción del crecimiento intrauterino.
Hay un cuerpo creciente de literatura dedicada a los posibles efectos beneficiosos de la analgesia epidural en pacientes con cáncer, aunque los datos son preliminares y, en ocasiones, contradictorios. El estrés quirúrgico y ciertos agentes anestésicos suprimen la función inmunitaria del huésped, incluida su capacidad para eliminar las células tumorales circulantes, y pueden predisponer a los pacientes con cáncer a infecciones posoperatorias, crecimiento tumoral y metástasis. Estudios recientes han demostrado una función inmunitaria perioperatoria mejorada con el uso de TEA en pacientes sometidas a histerectomía radical laparoscópica electiva por cáncer de cuello uterino. También se ha demostrado que los complementos regionales de la anestesia tienen efectos beneficiosos contra la recurrencia del cáncer de mama y de próstata. Estos efectos protectores pueden reflejar tanto la disminución de los requerimientos de opioides como la respuesta de estrés neurohumoral reducida asociada con el bloqueo epidural.
CONTRAINDICACIONES
Las complicaciones graves de las técnicas epidurales son raras. Sin embargo, los hematomas epidurales, los abscesos epidurales, la lesión nerviosa permanente, la infección y el colapso cardiovascular, entre otros eventos adversos, se han atribuido al bloqueo neuroaxial. Como resultado, es esencial comprender las condiciones que pueden predisponer a ciertas poblaciones de pacientes a estas y otras complicaciones. Esta sección revisa las contraindicaciones absolutas, relativas y controvertidas para la colocación epidural (Tabla 10). En última instancia, se recomienda un análisis de riesgo-beneficio con especial énfasis en las comorbilidades del paciente, la anatomía de las vías respiratorias, las preferencias del paciente y el tipo y la duración de la cirugía antes de iniciar el bloqueo epidural.
TABLA 10. Contraindicaciones del bloqueo epidural.
| Absoluto | negativa del paciente |
| Anomalías graves de la coagulación (p. ej., coagulación intravascular diseminada franca) |
|
| Relativo y controvertido | Sepsis |
| Presión intracraneal elevada |
|
| Anticoagulantes |
|
| La trombocitopenia |
|
| Otras diátesis hemorrágicas |
|
| nervioso central preexistente trastornos del sistema (p. ej., esclerosis múltiple) |
|
| Fiebre/infección (p. ej., virus de la varicela zóster) |
|
| Estados dependientes de precarga (p. ej., estenosis aórtica) |
|
| Cirugía de espalda previa, lesión neurológica preexistente, dolor de espalda |
|
| Colocación en adultos anestesiados |
|
| Colocación de la aguja a través del tatuaje |
Contraindicaciones absolutas
Aunque históricamente las contraindicaciones del bloqueo epidural se han clasificado como absolutas, relativas y controvertidas, las opiniones sobre las contraindicaciones absolutas han evolucionado con los avances en el equipo, las técnicas y la experiencia del médico. Actualmente, la negativa del paciente puede considerarse la única contraindicación absoluta para el bloqueo epidural. Aunque la coagulopatía se considera una contraindicación relativa, está contraindicado iniciar el bloqueo neuroaxial en presencia de anomalías graves de la coagulación, como la coagulación intravascular diseminada (CID) franca. La mayoría de las otras condiciones patológicas comprenden contraindicaciones relativas o controvertidas y requieren un análisis cuidadoso de riesgo-beneficio antes de iniciar el bloqueo epidural.
Contraindicaciones relativas y controvertidas
Sepsis
Existe un interés creciente en el uso de anestesia y analgesia epidurales para modular las respuestas inflamatorias y para prevenir o tratar la isquemia miocárdica, la disfunción respiratoria y la isquemia esplácnica en pacientes sépticos. Sin embargo, no hay evidencia suficiente para determinar si el bloqueo epidural es dañino o protector en la sepsis. A pesar de los beneficios potenciales de las técnicas regionales en este contexto, muchos anestesiólogos pueden ser reacios a iniciar el bloqueo epidural en pacientes sépticos debido a la preocupación por la hipovolemia relativa, la hipotensión refractaria, la coagulopatía y la introducción de patógenos transmitidos por la sangre en el espacio epidural o subaracnoideo. Si se selecciona la anestesia regional, puede ser factible una técnica de dosificación de inicio lento después o con la administración simultánea de antibióticos, fluidos intravenosos y vasopresores.
Aumento de la presión intracraneal
La punción dural accidental (ADP) en el contexto de presión intracraneal elevada (ICP) con evidencia radiológica de flujo de líquido cefalorraquídeo (LCR) obstruido o efecto de masa con o sin desplazamiento de la línea media puede poner a los pacientes en riesgo de hernia cerebral y otro deterioro neurológico. Los pacientes con aumento de la PIC al inicio también pueden experimentar un aumento adicional de la presión en la inyección epidural del fármaco. Se recomienda encarecidamente la consulta con un experto neurológico, y se debe descartar la localización de signos y síntomas neurológicos mediante la anamnesis y el examen físico antes de iniciar el bloqueo neuroaxial en pacientes con nuevos síntomas neurológicos o lesiones intracraneales conocidas (Tabla 11). Un árbol de decisiones puede ayudar a evaluar si es seguro proceder con técnicas neuroaxiales en presencia de lesiones ocupantes de espacio intracraneales (Figura 2 y XNUMX).
TABLA 11. Signos y síntomas de presión intracraneal elevada.
| Dolor de cabeza |
| Somnolencia |
| Náuseas y vómitos |
| Convulsiones de nueva aparición |
| Disminución del nivel de conciencia |
| Papiledema |
| Cambios pupilares |
| Signos neurológicos focales |
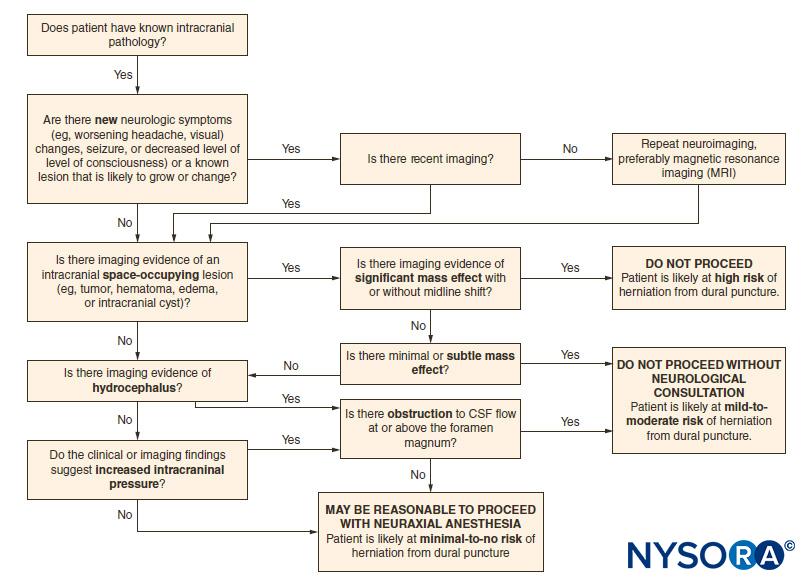
Figura 2 y XNUMX. Algoritmo de seguridad para el bloqueo neuroaxial en pacientes con lesiones ocupantes de espacio intracraneales. LCR = líquido cefalorraquídeo. (Reproducido con permiso de Leffert LR, Schwamm LH: Neuroaxial anestesia en parturientas con patología intracraneal: una revisión integral y reevaluación del riesgo. Anesthesiology. 2013 Sep;119(3):703-718.)
Coagulopatía
La coagulopatía es una contraindicación relativa para la colocación epidural, aunque se justifica una consideración minuciosa de la etiología y la gravedad de la coagulopatía caso por caso. Los anticoagulantes aumentan el riesgo de hematoma epidural y deben suspenderse de manera oportuna antes de iniciar el bloqueo epidural. También se deben tomar precauciones antes de retirar el catéter epidural, ya que la extracción del catéter puede ser tan traumática como la colocación del catéter.
Consejos NYSORA
• Tanto la colocación de la aguja epidural como del catéter conllevan un riesgo de hematoma epidural en pacientes que reciben anticoagulantes. Se deben observar precauciones similares durante la colocación y extracción de catéteres epidurales.
La Sociedad Estadounidense de Anestesia Regional y Medicina del Dolor actualiza periódicamente sus pautas para el inicio de la anestesia regional en pacientes que reciben terapia antitrombótica o trombolítica. En resumen, las técnicas neuroaxiales en pacientes que reciben heparina no fraccionada (HNF) subcutánea con pautas de dosificación de 5000 U cada 12 horas se consideran seguras.Tabla 12).
TABLA 12. Bloqueo epidural en pacientes que reciben terapia antitrombótica.
| AINE (aspirina) | Sin contraindicaciones |
| El clopidogrel | Espere 7 días antes de la colocación epidural |
| 5000 U subcutánea HNF cada 12 horas | Sin contraindicaciones |
| >10,000 XNUMX U subcutáneas de HNF al día | Seguridad no establecida |
| heparina intravenosa | Espere al menos 60 minutos después de la instrumentación antes de la administración de heparina; considerar aPTT y esperar de 2 a 4 horas antes de retirar el catéter |
| Dosis tromboprofiláctica de HBPM | Espere 12 horas antes de la colocación epidural |
| Dosis terapéutica de HBPM | Espere 24 horas antes de la colocación epidural |
| Warfarina | Espere a que el INR se normalice antes del bloqueo neuroaxial; retirar el catéter neuroaxial cuando INR < 1.5 |
Los riesgos y beneficios de la HNF tres veces al día o más de 10,000 4 U diarias deben evaluarse de forma individual; se debe mantener la vigilancia para detectar nuevos o empeoramiento de neurodeficiencias en este entorno. Para los pacientes que reciben heparina durante más de 2 días, se debe evaluar un recuento de plaquetas antes del bloqueo del nervio neuroaxial o la extracción del catéter debido a la preocupación por la trombocitopenia inducida por heparina (TIH). En pacientes que reciben heparinización sistémica, se recomienda evaluar el tiempo de tromboplastina plasmática activada (aPTT) y suspender la heparina durante 4 a 1 horas antes de la manipulación o extracción del catéter. La administración intraoperatoria de heparina intravenosa debe retrasarse al menos 24 hora después de la colocación epidural; no se requiere un retraso antes de la administración de heparina subcutánea. En los casos de heparinización completa para la CEC, las precauciones adicionales incluyen retrasar la cirugía durante XNUMX horas en caso de una punción traumática, controlar estrictamente el efecto y la reversión de la heparina y retirar los catéteres cuando se restablece la coagulación normal.
El bloqueo epidural en pacientes que toman aspirina y AINE sin aspirina se considera seguro, ya que el riesgo de hematoma epidural es bajo. La colocación de la aguja debe retrasarse 12 horas en pacientes que reciben tromboprofilaxis con heparina de bajo peso molecular (HBPM) y 24 horas en aquellos que reciben dosis terapéuticas. Se recomienda suspender la warfarina durante varios días antes de la cirugía y que el índice internacional normalizado (INR) vuelva a la línea base antes del inicio de las técnicas epidurales. Un INR por debajo de 1.5 se considera suficiente para la extracción del catéter, aunque muchos médicos pueden sentirse cómodos manipulando catéteres con valores de INR más altos. Consulte el Capítulo 52 para obtener información más detallada sobre estos y otros agentes más nuevos.
Las técnicas neuroaxiales están contraindicadas en el contexto de CID, que puede complicar sepsis, traumatismo, insuficiencia hepática, desprendimiento de placenta, embolia de líquido amniótico y transfusión masiva, entre otros procesos patológicos.Tabla 13). Si se desarrolla DIC después de la colocación epidural, el catéter debe retirarse una vez que se hayan restablecido los parámetros normales de coagulación.
TABLA 13. Condiciones asociadas con la coagulación intravascular diseminada.
| Sepsis |
| Trauma (lesión en la cabeza, lesión extensa de tejidos blandos, embolia grasa, hemorragia masiva) |
| transfusión masiva |
| Neoplasia maligna (carcinoma pancreático, enfermedad mieloproliferativa) |
| Periparto (embolia de líquido amniótico, desprendimiento de placenta, síndrome HELLP [hemólisis, enzimas hepáticas elevadas y recuento bajo de plaquetas], placentación anormal) |
| Trastornos vasculares (aneurisma aórtico, hemangioma gigante) |
| Trastornos inmunológicos (reacción transfusional hemolítica, rechazo de trasplantes, reacción alérgica grave) |
| Insuficiencia hepática |
Trombocitopenia y otros trastornos hemorrágicos comunes
La trombocitopenia, que puede ser causada por varias condiciones patológicas, es una contraindicación relativa para la anestesia neuroaxial.
Si bien actualmente no existe un recuento de plaquetas universalmente aceptado por debajo del cual se deba evitar la colocación epidural, muchos médicos se sienten cómodos con un recuento de plaquetas superior a 70,000 3 mmXNUMX en ausencia de hemorragia clínica. Sin embargo, el límite puede ser más alto o más bajo, según la etiología de la trombocitopenia, el historial de sangrado, la tendencia en el número de plaquetas, las características individuales del paciente (p. ej., una vía aérea difícil conocida o sospechada) y la experiencia del proveedor y el nivel de comodidad. En general, la función plaquetaria es normal en condiciones como la trombocitopenia gestacional y la púrpura trombocitopénica inmune (PTI).
Consejos NYSORA
• La etiología de la trombocitopenia, el historial de sangrado del paciente y la tendencia en el recuento de plaquetas deben tenerse en cuenta al determinar la seguridad del inicio del bloqueo epidural en pacientes trombocitopénicos. Ciertas condiciones, como la PTI y la trombocitopenia gestacional, se asocian con plaquetas funcionales a pesar de un recuento bajo de plaquetas.
Un recuento de plaquetas por debajo de 50,000 3 mm2 en el marco de la PTI puede responder a los corticosteroides o la inmunoglobulina intravenosa (IVIG), cuando sea necesario. Los defectos plaquetarios funcionales pueden estar presentes en varias afecciones menos comunes, como el síndrome HELLP (hemólisis, enzimas hepáticas elevadas y recuento bajo de plaquetas); púrpura trombocitopénica trombótica (PTT); y síndrome urémico hemolítico (SUH). Otras afecciones, como el lupus eritematoso sistémico (LES), el síndrome antifosfolípido, la enfermedad de von Willebrand tipo XNUMXB (vWD), la HIT y la DIC, se asocian con trombocitopenia de diversos grados.Tabla 14).
TABLA 14. Causas de la trombocitopenia.
| Autoinmune | trombocitopénica idiopática púrpura |
| trombocitopénica trombótica púrpura |
|
| Síndrome antifosfolípido |
|
| Lupus eritematoso sistémico | |
| periparto | Trombocitopenia gestacional |
| Preeclampsia (HELLP [hemólisis, enzimas hepáticas elevadas, y recuento bajo de plaquetas]) |
|
| enfermedad de von Willebrand | Tipo 2B |
| Relacionado con drogas | Inducida por heparina trombocitopenia |
| Metildopa |
|
| Sulfametoxazol | |
| linfoproliferativo trastornos | |
| urémico hemolítico síndrome |
No se ha establecido un recuento de plaquetas estándar para la extracción del catéter. Si bien algunas fuentes sugieren que 60,000 3 mmXNUMX es apropiado, se ha informado la extracción del catéter sin secuelas adversas en recuentos por debajo de ese límite. Si el número de plaquetas o la función se alteran después de colocar un catéter epidural, como en el caso de una CID intraoperatoria, el catéter debe permanecer in situ hasta que se resuelva la coagulopatía. Otras diátesis hemorrágicas comunes que comprenden contraindicaciones relativas para el inicio del bloqueo epidural incluyen la hemofilia, la vWD y los trastornos relacionados con los anticoagulantes lúpicos y los anticuerpos anticardiolipina. La hemofilia A y B son enfermedades ligadas al cromosoma X caracterizadas por deficiencias en los factores VIII y IX, respectivamente. Aunque faltan pautas específicas, los procedimientos neuroaxiales se consideran seguros en portadores de la enfermedad con niveles normales de factor y sin complicaciones hemorrágicas. Las técnicas neuroaxiales se han realizado sin secuelas adversas en pacientes homocigóticos después de la terapia de reemplazo de factor una vez que los niveles de factor y el TTPa se han normalizado. Los pacientes con anticoagulantes lúpicos y anticuerpos anticardiolipina están predispuestos a la agregación plaquetaria, trombocitopenia y, debido a las interacciones entre los anticuerpos y las membranas plaquetarias, a la trombosis. Como resultado, muchas de estas pacientes son anticoaguladas con heparina en el período periparto o perioperatorio. Los niveles de heparina deben controlarse con un ensayo de heparina en sangre, tiempo de trombina o prueba de coagulación activada antes de realizar un bloqueo neuroaxial. Cabe señalar que el aPTT está elevado al inicio del estudio en estos pacientes y es probable que permanezca elevado después de suspender la heparina debido a las interacciones entre los anticuerpos circulantes y las pruebas de coagulación.
La enfermedad de von Willebrand es el trastorno hemorrágico hereditario más común. Se caracteriza por una deficiencia cuantitativa (tipo 1 y tipo 3) o cualitativa (tipo 2) del factor von Willebrand (vWF), una glicoproteína plasmática que se une y estabiliza el factor VIII y media la adhesión plaquetaria en los sitios de lesión vascular. La presentación clínica de la vWD varía: los pacientes con tipo 1, el tipo más común, experimentan sangrado mucocutáneo, hematomas fáciles y menorragia; los pacientes con vWD tipo 2 pueden experimentar sangrado de moderado a severo y, en el caso del tipo 2B, trombocitopenia; el tipo 3, que es raro, se presenta con sangrado severo, incluyendo hemartrosis (Tabla 15).
TABLA 15. Clasificación de la enfermedad de von Willebrand.
| Tipo de Propiedad | Trastorno subyacente | Presentación Clínica/Características |
|---|---|---|
| 1 | Cantidad deficiente de vWF | Hemorragia mucocutánea, epistaxis, hematomas fáciles, menorragia |
| 2A | Defecto en la calidad del vWF | Sangrado moderado |
| 2B | FvW anormal | Sangrado moderado; trombocitopenia; riesgo de trombosis |
| 2M | Unión anormal de vWF | Extraño; sangrado significativo |
| 2N | Sitios de unión de vWF inactivos | Puede haber niveles bajos de factor VIII y niveles normales de vWF |
| 3 | Deficiencia severa de vWF | Sangrado severo, hemartrosis, hematomas musculares |
Tanto las opciones de tratamiento como la decisión de proceder con el bloqueo neuroaxial también varían con las diferentes presentaciones de la enfermedad. El tipo I responde a la desmopresina (DDAVP), que promueve la secreción de vWF almacenado en las células endoteliales y da como resultado un aumento rápido tanto del vWF como del factor VIII en plasma. Los concentrados de factor VIII y el crioprecipitado son opciones de tratamiento para la EvW tipo 2 y tipo 3. Las pruebas de laboratorio especializadas pueden ayudar a confirmar el diagnóstico y el tipo de vWD, pero no están ampliamente disponibles; las pruebas estándar de coagulación pueden servir para descartar otros trastornos hemorrágicos. Además de una historia clínica y un examen físico completos, la colaboración con un hematólogo y otros miembros del equipo, y una revisión de los resultados de laboratorio pertinentes, se debe realizar un análisis de riesgo-beneficio antes de iniciar los procedimientos epidurales en pacientes con vWD.
Trastornos preexistentes del sistema nervioso central
Históricamente, la administración de bloqueo neuroaxial ha estado contraindicada en pacientes con enfermedad preexistente del sistema nervioso central (SNC), incluida la esclerosis múltiple (EM), el síndrome pospolio (PPS) y el síndrome de Guillain-Barré (GBS). En el caso de la EM, se pensaba que los nervios desmielinizados eran más vulnerables a la neurotoxicidad inducida por LA. Un estudio inicial de Bader y colegas sugirió una asociación entre la recaída de la EM y concentraciones más altas de LA epidural entre las parturientas, aunque un estudio posterior en la misma población de pacientes no pudo demostrar un efecto adverso de la anestesia epidural en la tasa de recaída o la progresión de la enfermedad. enfermedad. Un estudio retrospectivo más reciente realizado por Hebl y colegas no encontró evidencia de recaída de la EM después de la anestesia espinal o epidural en 35 pacientes, 18 de los cuales recibieron bloqueo epidural. Si bien es poco probable que la anestesia y la analgesia epidurales provoquen exacerbaciones de la EM, faltan estudios definitivos sobre las propiedades farmacológicas de los LA en la EM, los regímenes de dosificación óptimos y si los LA interactúan directamente con las lesiones de la EM. Hasta que haya más datos disponibles, es razonable usar AL de baja concentración y realizar una evaluación y documentación exhaustivas de la gravedad de la enfermedad y el estado neurológico antes de iniciar el bloqueo neuroaxial central en pacientes con EM. Estos pacientes también deben ser informados del posible agravamiento de los síntomas, independientemente de la técnica anestésica.
La decisión de realizar anestesia epidural en pacientes con SPP, la enfermedad de la neurona motora más prevalente en América del Norte, requiere un análisis cuidadoso de los posibles riesgos y beneficios caso por caso. El SPP es una manifestación de inicio tardío de la infección por poliomielitis aguda que se presenta con fatiga, dolor articular y atrofia muscular en los grupos musculares previamente afectados. Las técnicas epidurales en esta población de pacientes pueden complicarse por la dificultad de la punción relacionada con la anatomía anormal de la columna, el posible empeoramiento de los síntomas y la debilidad respiratoria transitoria. Alternativamente, GA presenta desafíos relacionados con la sensibilidad a los relajantes musculares y sedantes y riesgos de compromiso respiratorio y aspiración. Aunque los datos son limitados, no hay evidencia de que las técnicas epidurales contribuyan al empeoramiento de los síntomas neurológicos en pacientes con SPP.
También falta evidencia que vincule las técnicas epidurales con la activación o la recurrencia del SGB. El GBS se presenta con debilidad motora progresiva, parálisis ascendente y arreflexia, muy probablemente atribuible a una respuesta inflamatoria posterior a la infección. La edad avanzada al inicio y la enfermedad inicial grave se encuentran entre los factores de riesgo de disfunción neurológica prolongada. La anestesia epidural se ha utilizado con éxito en pacientes con GBS, más comúnmente en pacientes obstétricas, aunque se han informado respuestas hemodinámicas exageradas (hipotensión y bradicardia), diseminación de LA mayor de lo normal y empeoramiento de los síntomas neurológicos. Como siempre, se justifica un análisis de riesgo-beneficio antes de realizar el bloqueo epidural en pacientes con GBS, al igual que la evaluación y documentación del examen neurológico del paciente y una discusión detallada de los riesgos de la anestesia. Es razonable evitar las técnicas regionales durante los períodos de inflamación neuronal aguda.
Los pacientes con espina bífida también pueden presentar un desafío único para los anestesiólogos. La espina bífida oculta ocurre cuando el arco neural no se cierra sin herniar las meninges o los tejidos neurales. Por lo general, se limita a una vértebra, aunque un pequeño porcentaje de personas afectadas tienen afectación de dos o más vértebras con anomalías neurológicas asociadas, anomalías subyacentes de la médula y escoliosis. En general, el uso de técnicas epidurales no está contraindicado en pacientes con espina bífida oculta, aunque la colocación al nivel de la lesión oculta, más comúnmente en L5 a S1, puede tener un mayor riesgo de punción dural y parches o más altos que respuesta normal a los LA. Por el contrario, la colocación epidural en pacientes con espina bífida quística tiene varios riesgos potenciales, incluido el riesgo de lesión directa de la médula debido a un cono medular bajo, propagación impredecible o mayor de lo esperado de las LA y mayor riesgo de punción dural. .
Fiebre o Infección
Existe controversia con respecto a la administración de anestesia neuroaxial en pacientes febriles y en individuos infectados con el virus de la inmunodeficiencia humana (VIH), el virus del herpes simple tipo 2 (HSV-2) y el virus de la varicela zoster (VZV). El uso de anestesia regional en presencia de febrícula de origen infeccioso es controvertido debido a la preocupación de propagar el agente infeccioso al espacio epidural o subaracnoideo, con la subsiguiente meningitis o formación de abscesos epidurales. Afortunadamente, las complicaciones infecciosas de la anestesia regional son raras y los estudios hasta la fecha no han podido demostrar una relación causal entre los procedimientos neuroaxiales, con o sin punción dural, y las complicaciones neurológicas subsiguientes. Si bien no existen pautas universales, los datos disponibles sugieren que la fiebre no impide la administración segura de anestesia y analgesia epidural. El manejo anestésico de los pacientes febriles debe basarse en un análisis riesgo-beneficio individual. Ya sea que se elija anestesia general o regional, la terapia con antibióticos debe completarse antes o durante el inicio de la anestesia. La adherencia a técnicas asépticas estrictas y el seguimiento posterior al procedimiento para detectar y tratar cualquier complicación son esenciales.
Históricamente, ha habido preocupaciones sobre la seguridad de los procedimientos neuroaxiales en personas infectadas por el VIH debido tanto al riesgo teórico de inoculación del virus en el SNC como a la posibilidad de que las manifestaciones neurológicas del VIH puedan atribuirse a la técnica anestésica. Sin embargo, el SNC se infecta temprano en el curso de la infección por VIH y no hay evidencia de que la instrumentación neuroaxial, incluido un parche sanguíneo epidural (EBP) para el tratamiento de la CPPD, confiera un riesgo adicional de propagación viral al SNC. Tampoco hay evidencia de que la introducción de sangre infectada con VIH en el LCR pueda exacerbar una infección preexistente del SNC, como la meningitis. Las preocupaciones de que las secuelas neurológicas del VIH puedan atribuirse a la técnica neuroaxial tampoco parecen tener fundamento, ya que es poco probable que exista una relación temporal entre la colocación de la epidural y la aparición de los déficits neurológicos. No obstante, se recomienda la documentación completa de cualquier déficit neurológico preexistente, dado que las complicaciones neurológicas del VIH no son infrecuentes y que las personas VIH positivas tienen un alto riesgo de otras enfermedades de transmisión sexual que afectan el SNC. Los riesgos potenciales deben discutirse con anticipación y, como siempre, se debe mantener una técnica aséptica estricta para proteger tanto al paciente como al proveedor de anestesiología.
Las áreas de preocupación con respecto al uso de anestesia regional en pacientes con HSV-2 incluyen el riesgo de introducir el virus en el SNC durante la administración de anestesia neuroaxial; la posibilidad de que una infección diseminada que se desarrolla después de un anestésico regional pueda atribuirse al propio anestésico, a pesar de la falta de una relación causal; y la seguridad de las técnicas neuroaxiales en los brotes primarios de HSV-2, que pueden ser silenciosos y difíciles de distinguir de los brotes secundarios, pero que se presentan más comúnmente con viremia, síntomas constitucionales, lesiones genitales y, en un pequeño porcentaje de pacientes, meningitis aséptica. No hay casos documentados de complicaciones sépticas o neurológicas después de procedimientos neuroaxiales en pacientes con infección por HSV secundaria (es decir, recurrente); sin embargo, no se ha establecido la seguridad de la anestesia regional en pacientes con infección primaria. Crosby y sus colegas realizaron un análisis retrospectivo de 6 años de 89 pacientes con infección secundaria por HSV que recibieron anestesia epidural para parto por cesárea e informaron que ningún paciente sufrió complicaciones sépticas o neurológicas.
De manera similar, en su encuesta retrospectiva de 164 parturientas con infección secundaria por HSV que recibieron anestesia espinal, epidural o AG para parto por cesárea, Bader et al no informaron resultados adversos relacionados con la anestesia. Con base en los hallazgos de estas y otras series informadas, parece seguro usar anestesia raquídea o epidural en pacientes con infección secundaria por HSV. Sin embargo, a la espera de datos más concluyentes, parece prudente evitar el bloqueo neuroaxial en pacientes con viremia por HSV-2. También existen preocupaciones con respecto al uso de anestesia regional en adultos con infecciones por VZV primarias o recurrentes, como herpes zoster (es decir, herpes zoster) y neuralgia posherpética (PHN). Sin embargo, los procedimientos neuroaxiales, incluidas las inyecciones epidurales de esteroides, se usan con frecuencia para tratar el herpes zoster agudo, prevenir la PHN y tratar el dolor asociado con la PHN, a menudo junto con la terapia antiviral. La presencia de lesiones activas en el lugar de la inyección se considera una contraindicación para estas y otras técnicas neuroaxiales. Para el pequeño subgrupo de pacientes que están infectados con VZV primario en la edad adulta, pueden producirse complicaciones graves como meningitis aséptica, encefalitis y neumonía por varicela. La realización de la anestesia regional en este contexto es más controvertida, pero puede ser preferible a la AG en algunos casos, principalmente debido a la preocupación por la neumonía. En última instancia, se recomienda un análisis cuidadoso de riesgo-beneficio, además de la evaluación y documentación de cualquier déficit neurológico preexistente, antes de iniciar el bloqueo neuroaxial en estos pacientes.
La infección cutánea localizada en el sitio de la punción prevista con la aguja es otra contraindicación relativa para el bloqueo neuroaxial, principalmente debido a la preocupación de que pueda producirse un absceso epidural espinal (SEA, por sus siglas en inglés) o meningitis. La diseminación hematógena de una infección localizada se ha implicado en SEA, aunque no se ha establecido claramente una relación causal en los casos notificados. El mantenimiento de estrictas precauciones estériles y un bajo índice de sospecha en presencia de signos neurológicos pueden minimizar el riesgo. Se debe intentar la inserción de la aguja después de la administración adecuada de antibióticos y se recomienda un sitio alejado de la infección localizada.
Cirugía de espalda previa, lesión neurológica preexistente y dolor de espalda
Tradicionalmente, un antecedente de cirugía de espalda anterior se consideraba una contraindicación relativa para el bloqueo neuroaxial debido a la preocupación por la infección, la exacerbación de los déficits neurológicos preexistentes y una mayor probabilidad de bloqueo nervioso difícil o fallido. Las dificultades técnicas pueden estar relacionadas con cambios degenerativos por encima o por debajo del nivel de fusión, adherencias en el espacio epidural, obliteración del espacio epidural, tejido cicatricial denso en el punto de entrada previsto de la aguja en la superficie de la piel, la presencia de material de injerto y la presencia de varillas extensas que impiden la identificación o el acceso a la línea media. A pesar de estas preocupaciones, un gran estudio retrospectivo de pacientes con antecedentes de estenosis espinal, neuropatía periférica o radiculopatía lumbar encontró que la cirugía espinal previa no afectó la tasa de éxito o la frecuencia de complicaciones técnicas. En pacientes con varillas de metal (p. ej., varillas de Harrington), las radiografías anteroposterior y lateral o una copia del informe operatorio pueden ayudar a identificar la extensión de la instrumentación, así como la presencia de anomalías anatómicas adicionales. El ultrasonido puede ayudar en la identificación de la línea media en casos epidurales difíciles. Las posibles complicaciones, como la diseminación craneal irregular, limitada o excesiva de las AL y un mayor riesgo de CPPD si se requieren múltiples intentos de colocación, deben discutirse con el paciente durante el proceso de consentimiento informado. Es de destacar que se pueden esperar dificultades técnicas similares encontradas durante la técnica original durante un procedimiento de EBP. Debido a estas y otras preocupaciones, se puede preferir la anestesia espinal, cuando sea apropiado, al bloqueo epidural.
El dolor de espalda es un problema omnipresente que no debe considerarse una contraindicación para el bloqueo neuroaxial y, más bien, es una indicación relativamente común para las inyecciones epidurales de esteroides y AL. Un estudio reciente encontró una tasa más alta que la reportada previamente de nuevos déficits neurológicos y empeoramiento de los síntomas preexistentes en pacientes con radiculopatía compresiva o múltiples trastornos neurológicos (estenosis espinal o enfermedad del disco lumbar) que recibieron anestesia neuroaxial. Sin embargo, no se estableció claramente una relación causal. Muchas de las inquietudes relacionadas con los procedimientos neuroaxiales en pacientes con dolor de espalda pueden abordarse antes de iniciar la anestesia neuroaxial con una historia clínica y un examen físico exhaustivos; no es raro que la causa del dolor de espalda no sea de origen neurológico. En estos casos, las técnicas regionales no se asocian con dolor de espalda de nueva aparición y es poco probable que exacerben la afección preexistente. Debido a que los pacientes con afecciones neurológicas preexistentes pueden tener un mayor riesgo de complicaciones neurológicas posoperatorias después de las técnicas neuroaxiales, se justifica un análisis cuidadoso de riesgo-beneficio caso por caso. Deben documentarse los déficits o síntomas neurológicos preexistentes y su gravedad.
Estados dependientes de precarga
Tradicionalmente, el bloqueo neuroaxial se ha considerado contraindicado en pacientes con estenosis aórtica (EA) severa y otras condiciones dependientes de la precarga, como la miocardiopatía hipertrófica obstructiva (hipertrofia septal asimétrica, ASH), debido al riesgo de descompensación aguda en respuesta a la disminución vascular sistémica. resistencia (RVS). Las últimas etapas de AS se asocian con disminución de la distensibilidad diastólica, alteración de la relajación, aumento de la demanda miocárdica de oxígeno y disminución de la perfusión del endocardio. La RVS disminuida en el contexto de GA o bloqueo neuroaxial conduce a una disminución de la perfusión y la contractilidad coronarias, con una mayor reducción del gasto cardíaco (GC) y empeoramiento de la hipotensión. La bradicardia, la taquicardia y otras arritmias también se toleran mal. La evidencia actual con respecto a la anestesia regional en pacientes con EA se basa en informes de casos y carece de la validez científica proporcionada por ensayos controlados aleatorios. Sin embargo, parece que la CSE cuidadosamente valorada y las técnicas epidurales y espinales continuas, más comúnmente con monitoreo invasivo, pueden ser opciones aceptables para pacientes con AS. Los anestésicos espinales de inyección única generalmente están contraindicados, ya que es esencial el inicio gradual del bloqueo simpático.
Los objetivos anestésicos para pacientes con ASH son similares, con énfasis en mantener la precarga, la poscarga, la euvolemia y la resistencia vascular, mientras se evita la taquicardia y la contractilidad aumentada. La monitorización invasiva y, si es necesario, la ecocardiografía transtorácica intermitente pueden ayudar a orientar los requisitos de líquidos y vasopresores, así como a orientar el tratamiento en caso de descompensación aguda.
Colocación epidural en pacientes anestesiados
El inicio del bloqueo epidural en adultos bajo AG es controvertido debido a la preocupación de que estos pacientes no puedan responder al dolor y, por lo tanto, puedan tener un mayor riesgo de complicaciones neurológicas. De hecho, las parestesias durante la realización del bloqueo nervioso y el dolor en la inyección de AL se han identificado como factores de riesgo de déficit neurológicos graves después de las técnicas regionales. En consecuencia, algunos expertos consideran que la comunicación cercana con el paciente es un componente esencial de la aplicación epidural segura. Los datos actuales respaldan la práctica de la inserción epidural en pacientes despiertos o mínimamente sedados, pero la colocación de agujas y catéteres en adultos anestesiados puede ser una alternativa aceptable en casos seleccionados. Los estudios de inserción epidural lumbar mientras los pacientes se someten a AG han demostrado que el riesgo de complicaciones neurológicas es pequeño. En general, se desconoce el riesgo relativo de la administración del bloqueo epidural en pacientes anestesiados, en comparación con la colocación de la epidural en pacientes despiertos, debido a la baja incidencia general de complicaciones neurológicas graves asociadas con la anestesia regional.
Inserción de aguja a través de un tatuaje
Las preocupaciones de que la punción de un tatuaje durante la colocación de la epidural pueda tener secuelas adversas aparecen sin fundamento en la literatura. Los riesgos teóricos están relacionados principalmente con la introducción de un pigmento potencialmente tóxico o cancerígeno en el espacio epidural, subdural o subaracnoideo. Sin embargo, hasta la fecha no se han informado en la literatura complicaciones significativas relacionadas con la inserción de una aguja a través de un tatuaje, aunque no se pueden descartar las posibles consecuencias a largo plazo.
ANATOMÍA
La comprensión de la anatomía de la columna vertebral, el canal espinal, el espacio epidural y su contenido, y las variaciones anatómicas comúnmente encontradas entre los individuos, es esencial para el inicio seguro y eficaz del bloqueo epidural. Una imagen mental tridimensional de la anatomía de la columna vertebral también ayuda en la resolución de problemas cuando la identificación del espacio epidural es equívoca o cuando ocurren complicaciones del cateterismo epidural, como bloqueo unilateral, canulación intravascular o migración del catéter. Esta sección presenta las consideraciones anatómicas básicas para una anestesia y analgesia epidurales exitosas y revisa varias controversias en el campo de la anatomía aplicada, incluida la precisión de los puntos de referencia anatómicos para estimar el nivel de la apófisis espinosa, la existencia (o falta de ella) de un compartimento subdural y el contenido del espacio epidural.
La columna vertebral
Apariencia general
Siete vértebras cervicales, 12 torácicas, 5 lumbares, 5 sacras fusionadas y 3 a 5 (más comúnmente 4) vértebras coccígeas fusionadas comprenden la columna vertebral. La columna vertebral es recta cuando se ve dorsal o ventralmente. Cuando se ve de lado, las regiones cervical y lumbar son cóncavas en la parte posterior (lordosis), y las regiones torácica y sacra son cóncavas en la parte anterior (cifosis) (Figura 3 y XNUMX).
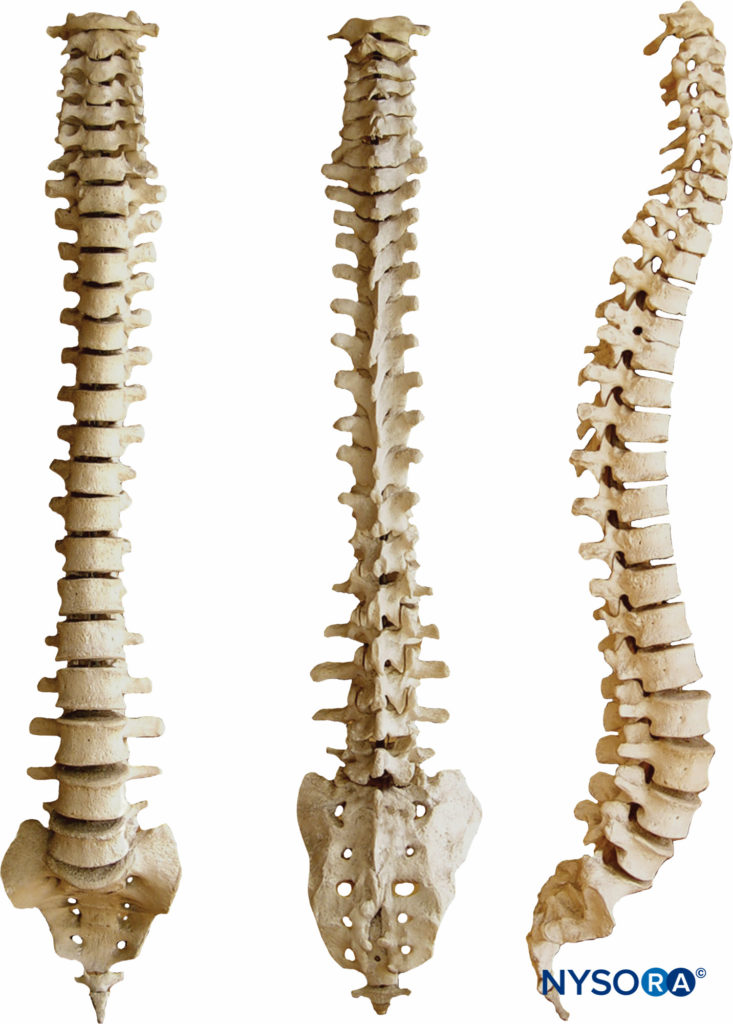
Figura 3 y XNUMX. Curvas espinales fisiológicas: vistas anterior, posterior y lateral (de izquierda a derecha).
Las cuatro curvas espinales fisiológicas están completamente desarrolladas a los 10 años de edad y se vuelven más pronunciadas durante el embarazo y con el envejecimiento. En decúbito supino, C5 y L3 se sitúan en los puntos más altos de la lordosis; los picos de cifosis ocurren en T5 a T7 y en S2.
Consejos NYSORA
C5 y L3 comprenden los puntos más altos de lordosis en posición supina; los puntos más altos de cifosis son T5 a T7 y S2.
Estructura de las vértebras
Con las excepciones de C1 y C2 y las regiones sacra y coxígea fusionadas, la estructura general de cada vértebra consta de un cuerpo vertebral anterior (corpus, centrum) y un arco óseo posterior. El arco está formado por las láminas; los pedículos, que se extienden desde los márgenes posterolaterales del cuerpo vertebral; y la superficie posterior del propio cuerpo vertebral. Además de las apófisis espinosas, que se forman por la fusión de las láminas en la línea media, el arco vertebral sostiene tres pares de apófisis que emergen del punto donde se unen las láminas y los pedículos: dos apófisis transversas, dos apófisis articulares superiores y dos procesos articulares inferiores. Los arcos vertebrales adyacentes encierran el canal vertebral y rodean porciones de la médula espinal longitudinal. El canal espinal se comunica con el espacio paravertebral a través de espacios entre los pedículos de vértebras sucesivas. Estos agujeros intervertebrales sirven como pasajes para los nervios, arterias y venas segmentarias.
Existe una variación sustancial en el tamaño y la forma de los cuerpos vertebrales, las apófisis espinosas y el canal espinal en diferentes niveles de la columna vertebral.Figura 4 y XNUMX). C3 a C7 tienen los cuerpos vertebrales más pequeños, mientras que el canal espinal a este nivel es ancho, mide 25 mm. Estas vértebras cervicales, con la excepción de C7, tienen apófisis espinosas cortas y bifurcadas. C7, la vértebra prominente, tiene una apófisis espinosa horizontal larga, delgada y fácilmente palpable que sobresale en la base del cuello y que a menudo sirve como punto de referencia superficial durante los procedimientos epidurales. Sin embargo, la primera apófisis espinosa torácica puede ser igual o más prominente que C7 en hasta un tercio de los hombres, así como en pacientes delgados y en pacientes con escoliosis y enfermedades degenerativas. La vértebra prominente también puede ser difícil de distinguir de C6 en hasta la mitad de los individuos, más comúnmente mujeres.
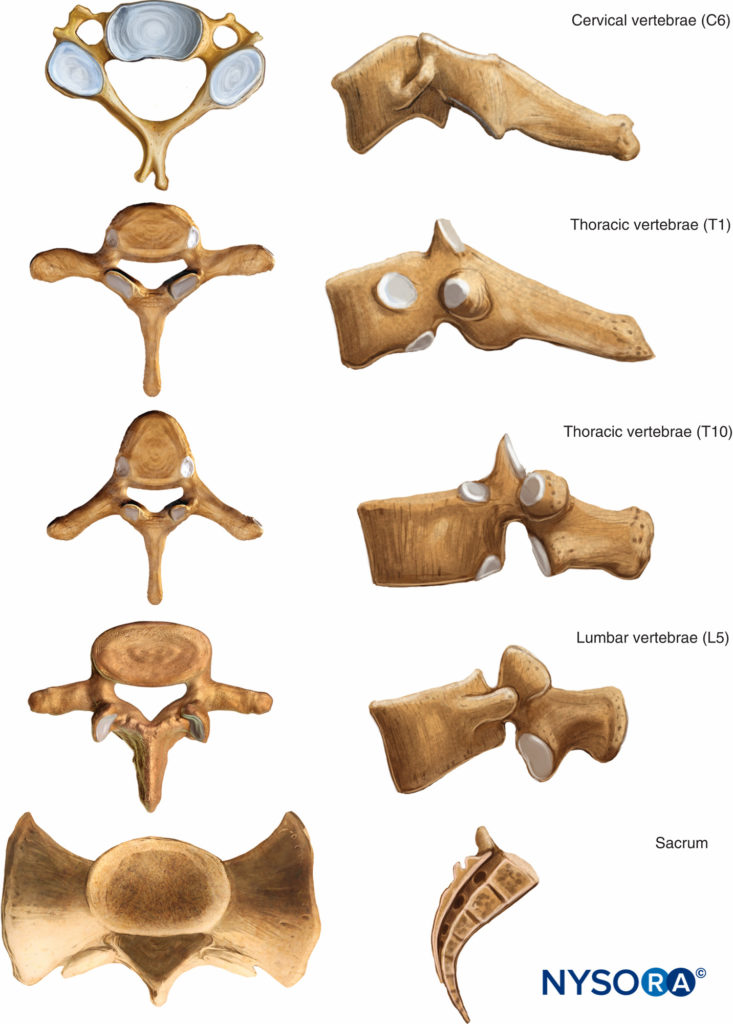
Figura 4 y XNUMX. Tamaño y forma de los cuerpos vertebrales a diferentes niveles de la columna.
Los cuerpos vertebrales torácicos son más grandes que los cuerpos vertebrales cervicales y son más anchos en la dimensión posterior que en la anterior, lo que contribuye a la característica curvatura torácica. Las apófisis espinosas torácicas largas y delgadas, con puntas que apuntan caudalmente, tienen un ángulo más pronunciado entre T4 y T9, lo que dificulta la inserción de la aguja epidural en la línea media en la región torácica media. Más allá de T10, se parecen cada vez más a los de la región lumbar. Cada vértebra torácica se articula con costillas a lo largo del borde dorsolateral de su cuerpo, una característica que puede ayudar a distinguir las regiones torácica inferior y lumbar superior. El ángulo inferior de la escápula y la costilla 12 son ampliamente utilizados en la práctica clínica para estimar el nivel de la cruz del proceso espinoso L1 (Tabla 16).
TABLA 16. Puntos de referencia anatómicos para identificar apófisis espinosas de T7 y T12, respectivamente. A menudo se supone que la línea imaginaria que conecta el margen más caudal de las 12 costillas
niveles vertebrales.
| Vértebra prominente | C7 |
| Raíz de la espina de la escápula | T3 |
| Ángulo inferior de la escápula | T7 |
| margen de la costilla | L1 |
| Cara superior de la ilíaca cresta | L3, L4 |
| Iliaca posterior superior espina | S2 |
Las vértebras lumbares son los segmentos móviles más grandes, con dimensiones anteriores más gruesas que posteriores que contribuyen a la curvatura lumbar característica. Las apófisis espinosas de esta región son romas y grandes, con puntas que apuntan hacia atrás.
Las variaciones anatómicas en la región lumbosacra que pueden tener implicaciones clínicas no son infrecuentes. La sacralización de la última vértebra lumbar, marcada por la fusión de L5 con el hueso sacro, y la lumbarización de S1 y S2, en las que la fusión es incompleta, pueden dificultar la numeración y la identificación del nivel lumbar correcto. Aunque probablemente no tenga importancia clínica, también se ha encontrado que los pacientes con sacralización tienen una posición más alta del cono medular, que delimita el extremo en forma de cono de la médula espinal, que aquellos con lumbarización o sin vértebras de transición lumbosacras. En ausencia de estas vértebras de transición, el espacio intermedio más grande y fácilmente palpable corresponde a L5 a S1.
Puntos de referencia anatómicos superficiales para identificar el nivel de la columna
Los puntos de referencia de la superficie se utilizan a menudo para identificar el nivel espinal deseado durante el inicio de la anestesia epidural (Figura 5 y XNUMX).
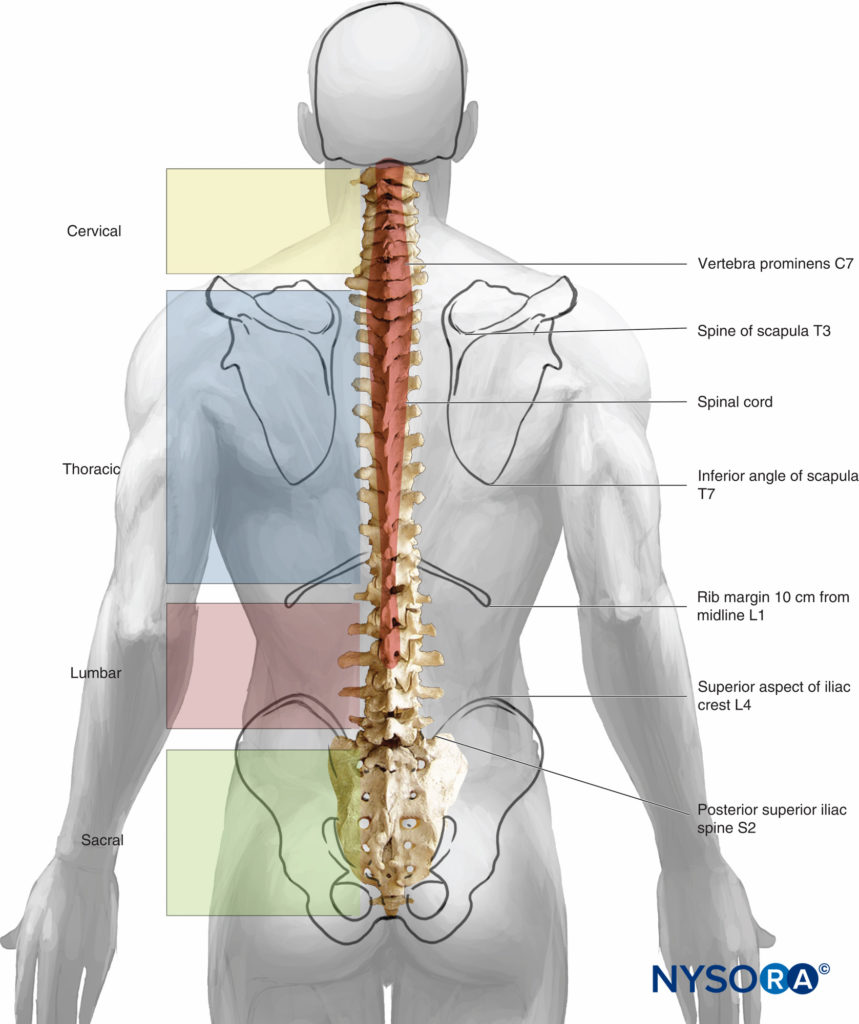
Figura 5 y XNUMX. Puntos de referencia esqueléticos utilizados para determinar el nivel de colocación epidural.
Sin embargo, la palpación y la inspección de los puntos de referencia anatómicos superficiales pueden no ayudar a localizar el espacio intervertebral correcto, particularmente cuando se consideran variaciones individuales en el nivel vertebral de estos puntos de referencia, la terminación variable del cono medular entre el tercio medio de T12 y el tercio superior de L3, y el pobre historial de los anestesiólogos para identificar el espacio intermedio correcto.
Los errores comunes al usar puntos de referencia esqueléticos para identificar el nivel de punción incluyen los siguientes: la vértebra prominente se confunde comúnmente con C6 y T1; la escápula puede ser difícil de identificar durante la colocación de TEA en pacientes obesos; rastrear la vértebra unida a la costilla 12 puede ser engañoso, particularmente en pacientes obesos; y la línea que conecta las espinas ilíacas posterosuperiores, a menudo utilizada para identificar S2, comúnmente cruza la línea media en niveles variables entre L5 y S1. Varios estudios han demostrado que la línea de Tuffier (también conocida como línea de Jacoby o línea intercristalina), que se une a la cara superior de las crestas ilíacas, puede cruzar la línea media al menos uno, y quizás dos, niveles más altos que el interespacio L4-L5 predicho. particularmente en pacientes embarazadas, ancianos y obesos. Los anestesiólogos tienen un historial deficiente en la estimación del espacio intermedio correcto en función de puntos de referencia externos. Van Gessel y sus colegas encontraron que el nivel de punción lumbar se identifica erróneamente hasta en un 59 % de las veces. En un estudio más reciente, Broadbent y colaboradores encontraron que los médicos identifican el nivel lumbar correcto en solo el 29% de los casos; el espacio se identifica erróneamente por dos niveles espinales, con el nivel real más alto que el previsto, en el 14% de los casos. Lirk et al confirmaron la tendencia de los anestesistas capacitados a colocar la aguja epidural más cranealmente de lo previsto, con mayor frecuencia dentro de un espacio intermedio del nivel previsto, también en la columna cervical y torácica. En general, dada la importancia de seleccionar el sitio correcto de punción, se recomienda precaución al utilizar puntos de referencia anatómicos superficiales para identificar los espacios intervertebrales. La creciente confianza en la determinación por ultrasonido del nivel espinal puede disminuir la incidencia de complicaciones relacionadas con la identificación errónea del espacio intermedio previsto.
Articulaciones y Ligamentos de la Columna Vertebral
General
Las vértebras adyacentes de las regiones cervical, torácica y lumbar, excepto C1 y C2, están separadas y amortiguadas por discos intervertebrales fibrocartilaginosos. El núcleo blando y elástico de cada disco, el núcleo pulposo, se compone principalmente de agua, así como de fibras elásticas y reticulares dispersas. El anillo fibrocartilaginoso fibroso rodea el núcleo pulposo y une los discos a los cuerpos de las vértebras adyacentes. Los discos, que representan hasta un cuarto de la longitud de la columna vertebral de un adulto, pierden su contenido de agua a medida que envejecemos, lo que contribuye al acortamiento de la columna vertebral, reduce su eficacia como amortiguadores y la hace más propensa a sufrir lesiones. , particularmente en la región lumbar.
Los procesos articulares surgen en la unión entre los pedículos y las láminas. Los procesos articulares superior e inferior se proyectan craneal y caudalmente, respectivamente, a ambos lados de cada vértebra. Los arcos vertebrales están conectados por articulaciones facetarias, que unen las apófisis articulares inferiores de una vértebra con las apófisis articulares superiores de la vértebra más caudal. Las articulaciones facetarias están fuertemente inervadas por la rama medial de la rama dorsal de los nervios espinales. Esta inervación sirve para dirigir la contracción del músculo que mueve la columna vertebral.
Los ligamentos longitudinales
Los ligamentos longitudinales anterior y posterior sostienen la columna vertebral, uniendo los cuerpos vertebrales y los discos intervertebrales.Figura 6 y XNUMX). El ligamento longitudinal posterior, que forma la pared anterior del canal vertebral, es menos ancho que su contraparte anterior y se debilita con la edad y otros procesos degenerativos. Clínicamente, la hernia de disco ocurre principalmente en la porción paramediana del disco posterior, en los puntos débiles del ligamento longitudinal posterior. Esta área comprende el espacio epidural anterior, a diferencia del espacio epidural posterior más relevante clínicamente, y no debe interferir con la colocación de la aguja epidural.
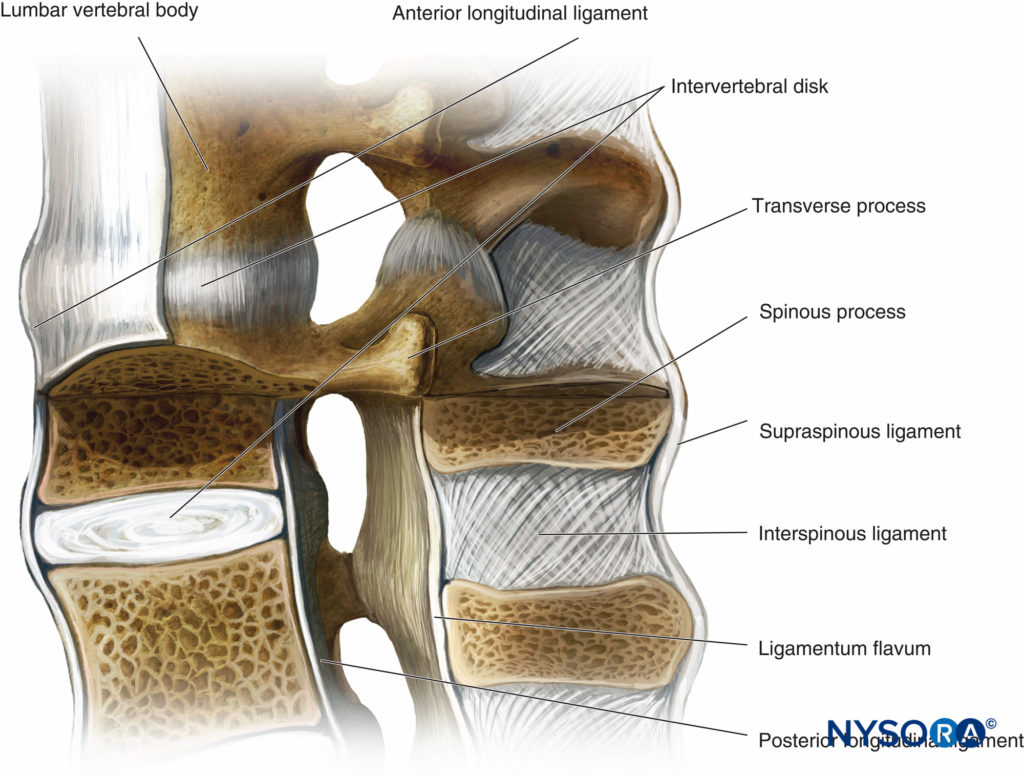
Figura 6 y XNUMX Ligamentos del canal vertebral.
Consejos NYSORA
• La hernia de disco ocurre principalmente en los puntos débiles del ligamento longitudinal posterior en un área que comprende el espacio epidural anterior, a diferencia del espacio epidural posterior más relevante clínicamente.
No obstante, se recomienda la documentación completa del dolor preexistente y los déficits neurológicos en pacientes con hernia de disco conocida antes de iniciar la anestesia epidural. También de relevancia clínica, una extensión lateral membranosa del ligamento longitudinal posterior puede servir como una barrera para la propagación de soluciones epidurales y parece acordonar las venas anteriores a la duramadre lejos del resto del espacio epidural.
Consejos NYSORA
• Una extensión lateral membranosa del ligamento longitudinal posterior parece acordonar las venas en el espacio epidural anterolateral, donde es más probable que ocurra la punción de la vena epidural y la canulación del catéter.
Los ligamentos supraespinoso e interespinoso
Varios otros ligamentos que sostienen la columna vertebral sirven como puntos de referencia anatómicos clave durante la colocación de la aguja epidural. El ligamento supraespinoso conecta las puntas de las apófisis espinosas de C7 a L5; por encima de C7 y extendiéndose hasta la base del cráneo, se denomina ligamento nucal. Este ligamento relativamente superficial e inextensible es más prominente en la región torácica superior y se vuelve más delgado y menos visible hacia la región lumbar inferior. El ligamento interespinoso, directamente anterior al ligamento supraespinoso, atraviesa el espacio entre las apófisis espinosas adyacentes en dirección posterocraneal. Está menos desarrollado en la región cervical, lo que puede contribuir a un LOR falso durante los procedimientos epidurales cervicales.
En el examen histológico, el ligamento interespinoso parece tener cavidades intermitentes en la línea media llenas de grasa. Tanto los ligamentos supraespinosos como los interespinosos están compuestos de fibras colágenas que producen un sonido de "crujido" característico o una sensación táctil distintiva a medida que avanza la aguja epidural. Durante el inicio de la colocación epidural a través del abordaje de la línea media, estos ligamentos sirven como sitios apropiados para acoplar la aguja, aunque algunos médicos pueden acoplar la aguja más cerca del espacio epidural, en el ligamento amarillo. Una aguja epidural “floja” que se inclina lateralmente antes de conectar la jeringa LOR puede indicar un abordaje fuera de la línea media, lejos de los ligamentos supraespinosos o interespinosos.
El ligamento amarillo
El ligamento amarillo conecta la lámina de las vértebras adyacentes desde el borde inferior de C2 hasta el borde superior de S1. Lateralmente, se extiende hacia los agujeros intervertebrales, donde se une a la cápsula del proceso articular.
Anteriormente, limita el canal vertebral y forma el borde posterior del espacio epidural. En cada nivel de la columna, los ligamentos amarillos derecho e izquierdo se unen discontinuamente en un ángulo agudo con la abertura orientada en dirección ventral, formando ocasionalmente espacios en la línea media llenos de grasa epidural. En contraste con los ligamentos colágenos interespinosos y supraespinosos, el ligamento amarillo comprende principalmente fibras elásticas gruesas dispuestas longitudinalmente en una red apretada.
Las áreas de osificación del ligamento amarillo ocurren en diferentes niveles del canal vertebral y parecen ser una variante normal. Estos espolones óseos, que pueden contribuir a los síntomas neurológicos preexistentes y podrían impedir el avance de la aguja epidural, se encuentran con mayor frecuencia en la región torácica inferior, entre T9 y T11, y disminuyen tanto en frecuencia como en tamaño en las direcciones caudal y craneal.
El ligamento amarillo tiene características variables, muchas de las cuales son discutidas en la literatura, en diferentes niveles vertebrales. Primero, su grosor varía en diferentes niveles y, posiblemente, en diferentes estados fisiológicos, con un rango de 1.5 a 3.0 mm en el segmento cervical, 3.0 a 5.0 mm en el segmento torácico, 5.0 a 6.0 mm en el segmento lumbar y 2.0 mm. –6.0 mm en la región caudal (Tabla 17). En pacientes embarazadas aisladas, se ha informado que el ligamento amarillo tiene un grosor de hasta 10 mm, presumiblemente debido a edema. También cabe destacar que el grosor del flavum varía dentro del propio espacio intermedio, siendo la región caudal significativamente más gruesa que la rostral.
TABLA 17. Grosor del ligamento amarillo a diferentes niveles vertebrales.
| Nivel Vertebral | Espesor (mm) |
|---|---|
| Cervical | 1.5-3.0 |
| torácica | 3.0-5.0 |
| Lumbar | 5.0-6.0 |
| Caudal | 2.0-6.0 |
Consejos NYSORA
• El ligamento amarillo varía en grosor en diferentes niveles de la columna y es más grueso en la región lumbar. Su grosor también varía dentro de cada interespacio.
Clínicamente, estos diversos grados de grosor pueden influir en el riesgo de punción dural involuntaria o determinar si es posible inyectar una solución anestésica en el espacio epidural con la aguja de infiltración cutánea.
Otra controversia se refiere a la incidencia y ubicación de los espacios formados por la fusión incompleta del ligamento amarillo derecho e izquierdo. En su estudio de 52 cadáveres humanos, Lirk y sus colegas encontraron que hasta el 74 % de los flava en la región cervical son discontinuos en la línea media. Estos espacios varían en ubicación, algunos ocupan toda la altura del ligamento amarillo entre arcos vertebrales sucesivos y otros ocupan solo la tercera porción caudal.Figura 7 y XNUMX).
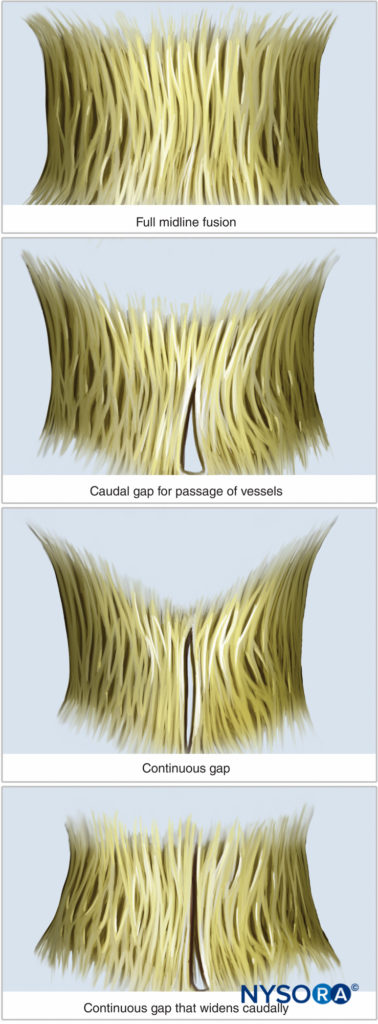
Figura 7 y XNUMX. Ligamentum flavum con diferentes tipos de espacios en la línea media.
Las venas que conectan los plexos venosos vertebrales posterior externo e interno no es raro que atraviesen la porción caudal de los espacios. En otro estudio cadavérico, Lirk et al. determinaron que las brechas en la línea media torácica eran menos frecuentes que las cervicales, pero más frecuentes que las de la región lumbar, con una incidencia de hasta el 35.2 % en T10 a T11. En estudios cadavéricos del ligamento amarillo lumbar, los espacios se encontraron con mayor frecuencia en L1 y L2 (22.2 %) y disminuyeron caudalmente (11.4 % en L2 a L4; 9.3 % en L4 a L5; 0 % en L5 a S1). Clínicamente, estos espacios pueden contribuir a que no se identifique el espacio epidural mediante la técnica LOR en la línea media. El sonido característico de “pop” y la sensación táctil conferidos por la penetración de las fibras elásticas del ligamento amarillo pueden estar ausentes en el contexto de un arco ligamentoso discontinuo. La profundidad del espacio epidural en la línea media también puede verse afectada.
Consejos NYSORA
• Los espacios en la línea media del ligamento amarillo representan una fusión incompleta del ligamento amarillo derecho e izquierdo. Son comunes en la columna cervical y disminuyen en frecuencia en las regiones torácica y lumbar. El grosor variable del ligamento amarillo y la presencia de espacios en la línea media pueden contribuir a que no se identifique el espacio epidural.
El Canal Espinal General
Las vértebras sirven principalmente para soportar el peso de la cabeza, el cuello y el tronco; trasladar ese peso a los miembros inferiores; y proteger el contenido del canal espinal, incluida la médula espinal. Una extensión del bulbo raquídeo, la médula espinal sirve como conducto entre el SNC y los nervios periféricos a través de 31 pares de nervios espinales (8 cervicales, 12 torácicos, 5 lumbares, 5 sacros y 1 coccígeo) (Figura 8 y XNUMX). El cordón adulto mide aproximadamente 45 cm o 18 pulgadas y tiene dos regiones de mayor diámetro en C2-T2 y en T9-L2, áreas que se corresponden con el origen de la inervación de las extremidades superiores e inferiores. Sin embargo, su nivel de terminación varía con la edad, así como entre individuos de grupos de edad similares. Como resultado de una discrepancia en el ritmo de crecimiento de la médula espinal y la columna vertebral durante el desarrollo, la médula espinal al nacer termina aproximadamente en L3. A los 6-12 meses de edad, el nivel de terminación es paralelo al de los adultos, más comúnmente en L1. Debajo del cono medular, las largas raíces dorsal y ventral de todos los nervios espinales debajo de L1 forman un haz conocido como cauda equina o cola de caballo. Una colección de hebras de tejido fibroso libre de neuronas envuelto en piamadre comprende el filum terminale y se extiende desde la punta inferior del cono medular hasta la segunda o tercera vértebra sacra.
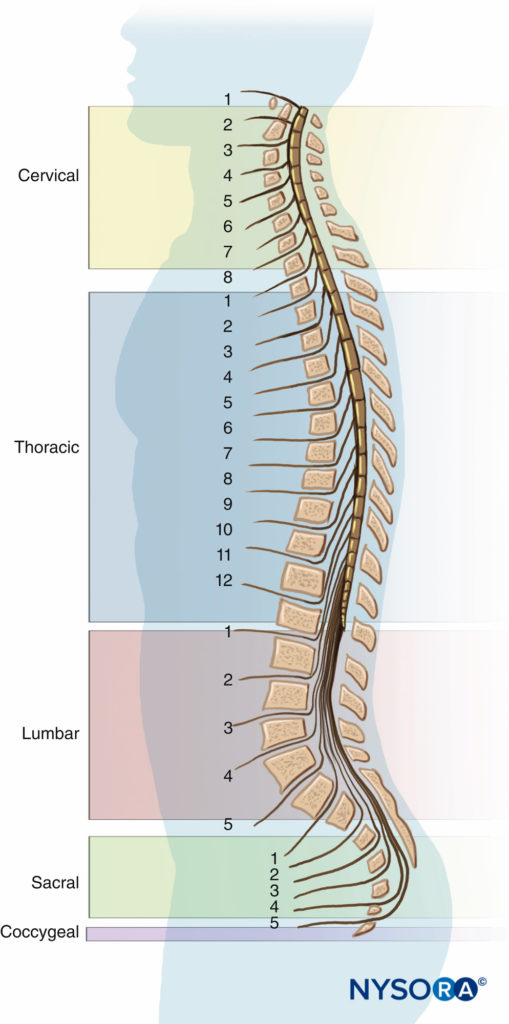
Figura 8 y XNUMX. Columna vertebral con nervios espinales.
Nervios espinales
Los nervios espinales se clasifican como nervios mixtos porque contienen un componente tanto sensorial como motor y, en muchos casos, fibras autonómicas. Cada nervio se forma a partir de la fusión de raíces nerviosas dorsales (sensoriales) y ventrales (somáticas y motoras viscerales) cuando salen del canal vertebral distal a los ganglios de la raíz dorsal, que contienen los cuerpos celulares de las neuronas sensoriales a cada lado de la médula espinal y se encuentran entre los pedículos de las vértebras adyacentes.
En general, las raíces dorsales son más grandes y se bloquean con mayor facilidad que las raíces ventrales, un fenómeno que puede explicarse en parte por la mayor superficie de exposición a los LA proporcionada por las raíces dorsales agrupadas.
A nivel cervical, el primer par de nervios espinales sale entre el cráneo y C1. Los nervios cervicales subsiguientes continúan saliendo por encima de la vértebra correspondiente, asumiendo el nombre de la vértebra que les sigue inmediatamente. Sin embargo, se produce una transición entre la séptima vértebra cervical y la primera torácica, donde sale un octavo par de nervios cervicales; a partir de entonces, los nervios espinales salen por debajo de la vértebra correspondiente y toman el nombre de la vértebra inmediatamente superior.
Los nervios espinales se dividen en ramas primarias anterior y posterior poco después de salir de los agujeros intervertebrales. Los ramos anteriores (ventrales) irrigan el lado ventrolateral del tronco, las estructuras de la pared del cuerpo y las extremidades. Los ramos primarios posteriores (dorsales) inervan regiones específicas de la piel que se asemejan a bandas horizontales que se extienden desde el origen de cada par de nervios espinales, llamados dermatomas, y los músculos de la espalda. Clínicamente, el conocimiento de los dermatomas es fundamental a la hora de planificar la anestesia en regiones cutáneas específicas (Figura 9 y XNUMX), aunque es posible que la anestesia no se confiera de manera confiable a las vísceras subyacentes debido a una inervación separada, y existe una superposición significativa en la inervación del nervio espinal de los dermatomas adyacentes (Tabla 18).
TABLA 18. Correlación del punto de referencia de la superficie con el nivel del dermatoma.
| Nivel de bloque | Hito anatómico |
|---|---|
| C6 | Pulgar |
| C8 | quinto dedo |
| T1 | Cara interna del brazo |
| T4 | Cabecillas radios |
| T6 | Proceso de xifoides |
| T10 | Ombligo |
| T12 | Ligamento inguinal |
| S1 | Cara lateral del pie |
| S2-S4 | Perineo |
Existe una intrincada relación entre los nervios espinales y el sistema nervioso autónomo (Figura 10 y XNUMX). Las fibras nerviosas simpáticas preganglionares se originan en la médula espinal desde T1 a L2 y se bloquean en diversos grados durante la anestesia epidural.
Salen de la médula espinal con los nervios espinales y forman la cadena simpática, que se extiende por toda la longitud de la columna vertebral en las caras anterolaterales de los cuerpos vertebrales. La cadena da lugar al ganglio estrellado, los nervios esplácnicos y el plexo celíaco, entre otras cosas. Hay beneficios potenciales y desventajas marcadas para el bloqueo epidural del sistema nervioso simpático. TEA parece aumentar la movilidad GI al bloquear el suministro simpático a los ganglios mesentéricos inferiores, lo que reduce la incidencia de íleo posoperatorio. La anestesia epidural también puede bloquear los nervios de la respuesta de estrés sistémico a la cirugía, en parte mediante el bloqueo del sistema nervioso simpático. Sin embargo, el bloqueo simpático torácico medio a bajo puede estar asociado con la dilatación de los lechos vasculares esplácnicos, un marcado aumento en la capacitancia venosa, una disminución en la precarga del corazón derecho y muchos de los otros efectos indeseables (ver Efectos fisiológicos de la epidural). bloquear).
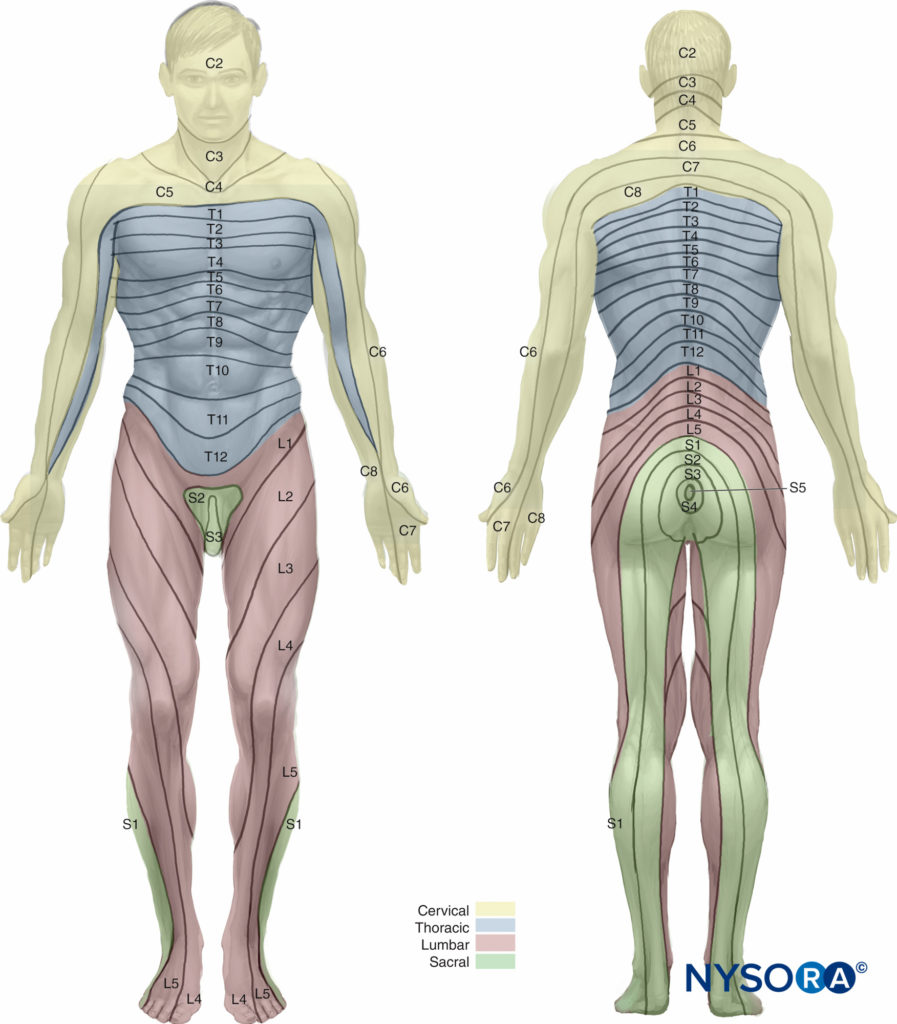
Figura 9 y XNUMX. Distribución de los dermatomas.
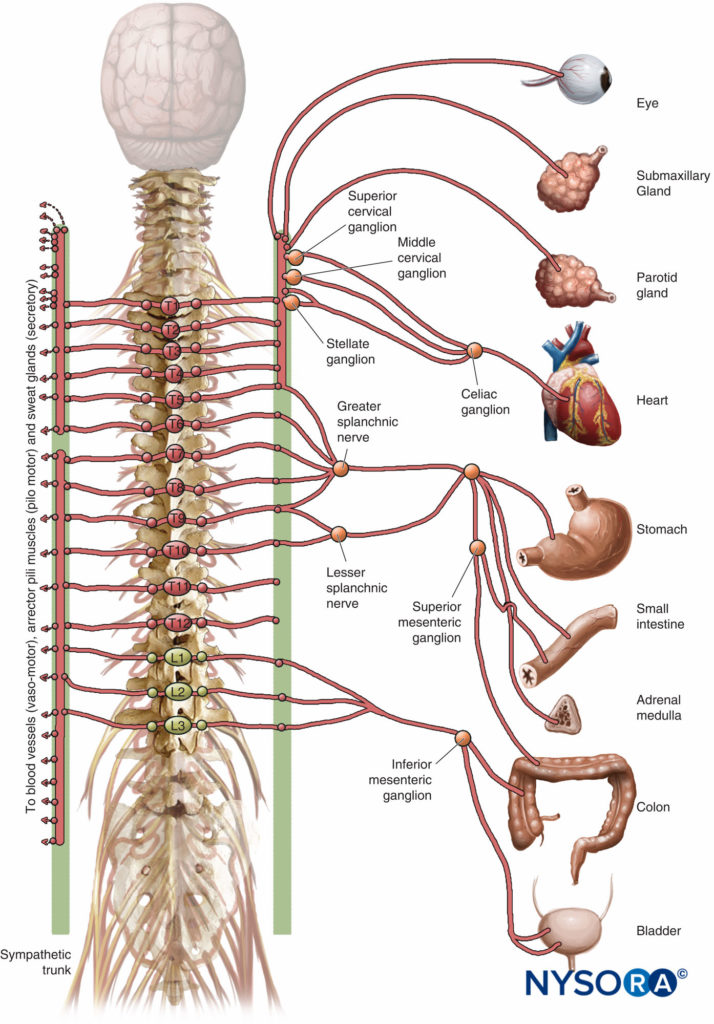
Figura 10 y XNUMX. Sistema nervioso simpático.
Los componentes craneales y sacros comprenden el sistema nervioso parasimpático. El nervio vago, en particular, proporciona inervación parasimpática a un área amplia, que incluye la cabeza, el cuello, los órganos torácicos y partes del tracto digestivo. La inervación parasimpática de la vejiga, el intestino grueso descendente y el recto se originan en los niveles S2 a S4 de la médula espinal.
Meninges espinales
Las meninges espinales cubren la médula y las raíces nerviosas y se continúan con las meninges craneales que rodean y protegen el cerebro.Figura 11 y XNUMX). La duramadre, la capa más externa, resistente y predominantemente colágena, encierra el SNC y proporciona puntos localizados de unión al cráneo, el sacro y las vértebras para anclar la médula espinal dentro del canal vertebral. Cranealmente, la duramadre espinal se fusiona con el periostio al nivel del foramen magnum; caudalmente, se fusiona con elementos del filum terminale y contribuye a la formación del ligamento coccígeo; lateralmente, la duramadre rodea las raíces nerviosas cuando salen de los agujeros intervertebrales. La duramadre toca el canal espinal en áreas, pero no se adhiere a él excepto en condiciones patológicas. También confiere permeabilidad y resistencia mecánica al saco dural, que termina en S1 a S2 en adultos y S3 a S4 en bebés. Los manguitos de la raíz del nervio espinal, que se ha postulado que desempeñan un papel en la captación de los LA administrados por vía epidural, son proyecciones laterales tanto de la duramadre como de la lámina aracnoidea subyacente.
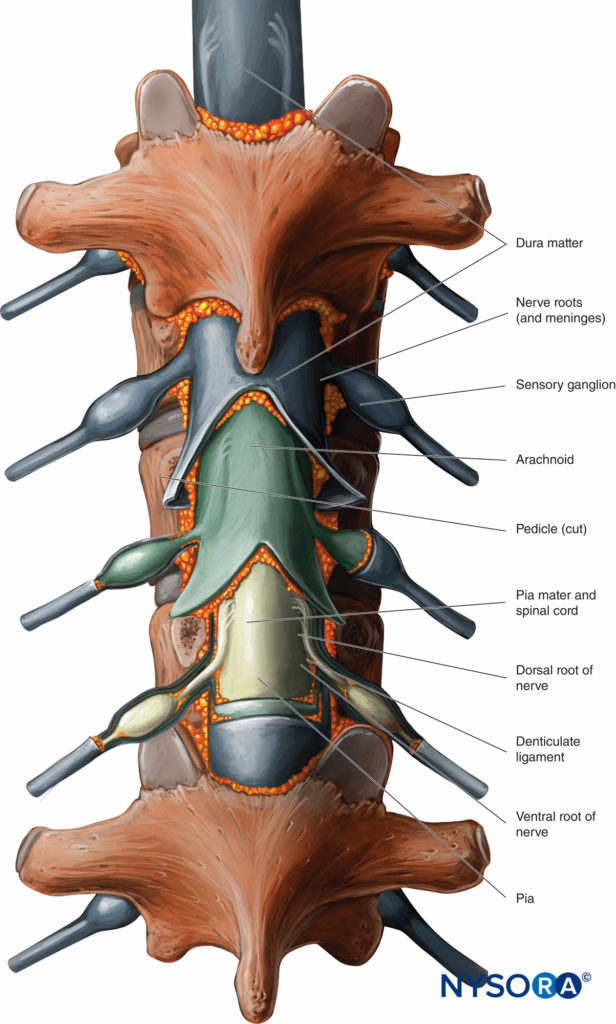
Figura 11 y XNUMX. Meninges espinales.
La aracnoides mater flexible, la capa meníngea media, está unida laxamente a la cara interna de la duramadre y encierra la médula espinal y el LCR circundante dentro del espacio subaracnoideo. Se compone de capas de células de tipo epitelial conectadas por uniones estrechas y oclusivas, que le confieren una baja permeabilidad.
Las capas de células de la aracnoides están orientadas paralelas al eje longitudinal de la médula espinal (cefalocaudal), un hallazgo que ha llevado a algunos investigadores a afirmar que la arquitectura de la aracnoides, más que la duramadre, explica la diferencia en tasas de dolor de cabeza entre inserciones perpendiculares y paralelas de agujas espinales biseladas. En virtud de su flexibilidad, la aracnoides puede resistir la punción de una aguja que avanza durante el inicio de la anestesia raquídea o CSE. Un tabique subaracnoideo discontinuo (septum posticum) que se extiende desde la parte posterior de la médula espinal hasta la aracnoides puede contribuir a la diseminación irregular de las AL en el espacio subaracnoideo.
La capa meníngea más interna, la piamadre, envuelve de cerca la médula espinal subyacente y sus vasos sanguíneos, así como las raíces nerviosas y los vasos sanguíneos en el espacio subaracnoideo, y parece tener áreas fenestradas que pueden influir en la transferencia de AL durante los bloqueos de los nervios subaracnoideos. . Caudalmente, la piamadre continúa
desde la punta inferior del cono medular como el filum terminale y se fusiona con el ligamento sacrococcígeo.
Es posible que se pueda crear una cavidad en la interfaz aracnoides-dura que puede explicar los bloqueos nerviosos epidurales irregulares o fallidos con una extensión cefálica mayor a la esperada (los llamados bloqueos nerviosos subdurales). Las primeras investigaciones sugirieron que el espacio extraaracnoideo subdural comprendía un verdadero espacio potencial, con líquido seroso
que permitió el movimiento de las capas de la duramadre y la aracnoides una al lado de la otra. Blomberg usó la espinoscopia en estudios de cadáveres para demostrar su existencia en hasta el 66% de los humanos.
Sin embargo, la evidencia reciente sugiere que, a diferencia de un espacio potencial, esta interfaz aracnoides-dura es un área propensa a la tensión mecánica que se abre solo después de un traumatismo directo, como la inyección de aire o líquido. También es posible que estas hendiduras en realidad puedan ocurrir entre capas de aracnoides en lugar de entre las células del borde dural en la interfaz aracnoides-dura. Más información sobre las meninges espinales y las estructuras relacionadas se detallan en “Anatomía ultraestructural de las meninges espinales y estructuras relacionadas".
Consejos NYSORA
Pueden formarse hendiduras en la interfase aracnoides-duramadre como resultado de tensión mecánica y traumatismo directo. La inyección de un gran volumen de AL destinado al espacio epidural en esta área puede resultar en un bloqueo del nervio subdural.
Suministro de sangre
Las arterias vertebrales y segmentarias irrigan la médula espinal. Una sola arteria espinal anterior y dos arterias espinales posteriores, y sus ramificaciones, surgen de las arterias vertebrales e irrigan los dos tercios anteriores de la médula espinal y el resto de la médula, respectivamente.Figura 12 y XNUMX). La arteria anterior es delgada en el nivel torácico medio de la médula espinal, un área que también tiene un suministro de sangre colateral limitado. Las arterias segmentarias, que emergen de ramas de las arterias cervical e ilíaca, entre otras, se extienden a lo largo de toda la médula espinal y se anastomosan con las arterias anterior y posterior. La arteria de Adamkiewicz se encuentra entre las arterias segmentarias más grandes y es más comúnmente unilateral, y surge del lado izquierdo de la aorta entre T8 y L1. En cuanto al sistema venoso, las venas espinales anterior y posterior, que se anastomosan con el plexo vertebral interno en el espacio epidural, drenan en las venas ácigos, hemiácigos e ilíacas internas, entre otras venas segmentarias, a través de las venas intervertebrales. El plexo venoso vertebral interno consta de dos vasos longitudinales anteriores y dos posteriores con una distribución variable y se postula que está involucrado en la colocación de catéteres y agujas epidurales sangrientas o traumáticas.
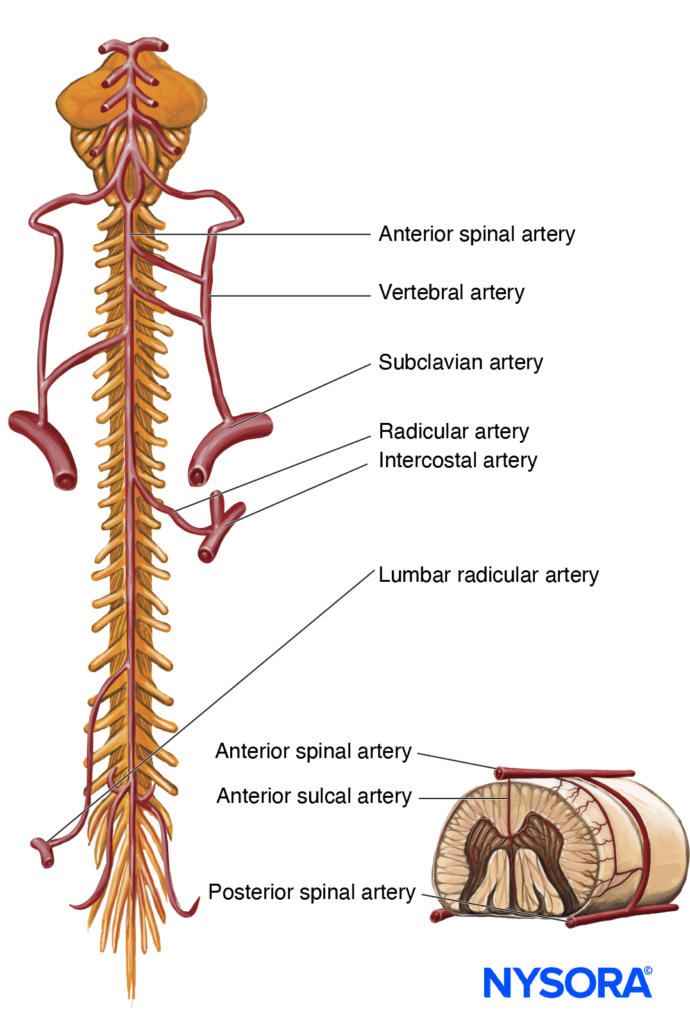
Figura 12 y XNUMX. Suministro de sangre de la médula espinal.
espacio epidural
El espacio epidural rodea circunferencialmente la duramadre y se extiende desde el agujero magno hasta el ligamento sacrococcígeo. El espacio está delimitado posteriormente por el ligamento amarillo, lateralmente por los pedículos y los agujeros intervertebrales, y anteriormente por el ligamento longitudinal posterior. De los tres compartimentos del espacio epidural (posterior, lateral y anterior), el espacio epidural posterior es el más relevante clínicamente. El espacio epidural en general contiene tejido adiposo, vasos sanguíneos, raíces nerviosas y tejido conectivo laxo en una distribución no uniforme. Las venas en el espacio se continúan con los vasos ilíacos en la pelvis y el sistema ácigos en las paredes corporales abdominal y torácica. Debido a que el plexo no tiene válvulas, la sangre de cualquiera de los sistemas conectados puede fluir hacia los vasos epidurales.
A diferencia del dogma tradicional, estos vasos se ubican principalmente en el espacio epidural anterior, donde están confinados en gran medida por la extensión membranosa del ligamento longitudinal posterior106 (Figura 13 y XNUMX). Esta área es probablemente un sitio común de punción de vasos sanguíneos con catéter epidural. También de importancia clínica, la presión subatmosférica del espacio epidural disminuye significativamente en la región lumbar, lo que puede afectar tanto a las técnicas de identificación del espacio epidural como a la caída colgante y a la forma de onda de la presión epidural.
Los contenidos del espacio epidural y sus implicaciones clínicas han sido ampliamente debatidos en la literatura. La cantidad de tejido adiposo en el espacio epidural parece afectar la diseminación de LA, pero no está claro si la grasa epidural prolonga la duración del bloqueo nervioso sirviendo como reservorio o disminuye la cantidad de fármaco disponible, lo que ralentiza el inicio, o ambas cosas. Se especula que la reducción del tejido adiposo con la edad explica en parte los niveles más altos y el inicio más rápido de la anestesia epidural en los ancianos.
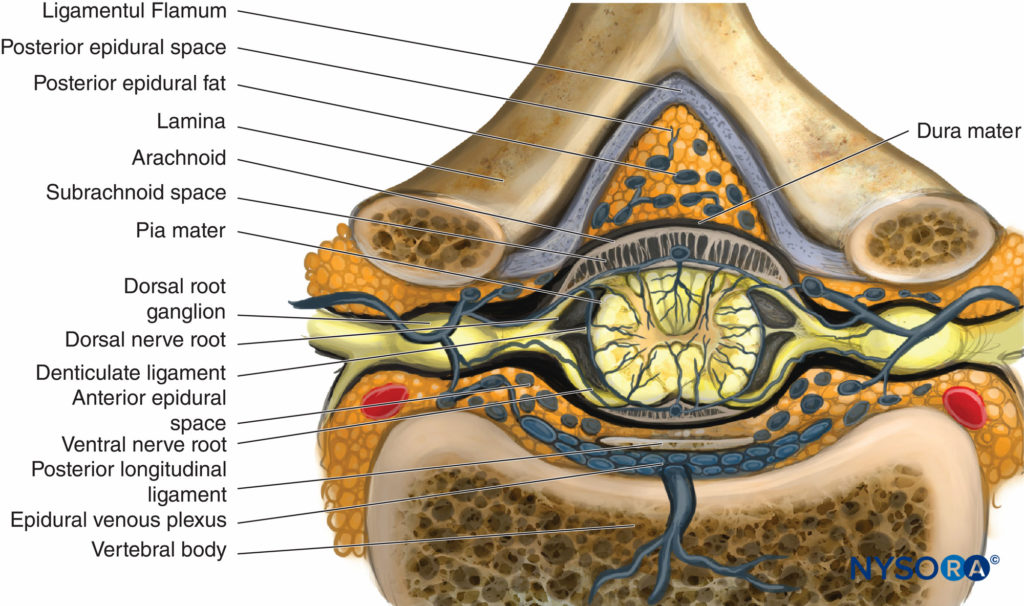
Figura 13 y XNUMX. Distribución de la vena epidural en la región lumbar.
De manera similar, el aumento de tejido adiposo en el área lumbar inferior donde el saco dural se estrecha puede contribuir a los efectos variables de las inyecciones de AL por debajo de L4-L5. Finalmente, el tejido adiposo en el espacio de la línea media, donde se fusionan los ligamentos amarillos, puede alterar la sensación táctil que normalmente se aprecia durante la técnica LOR.
Otra controversia anatómica del espacio epidural se refiere a si los tabiques, alternativamente descritos como hebras escasas y como una membrana continua que une la duramadre al ligamento amarillo, obstruyen el avance del catéter, afectan la propagación y el inicio de las AL y contribuyen a los bloqueos nerviosos unilaterales y al bloqueo no intencional. punciones durales. Sin embargo, estos tabiques se han identificado más recientemente como un artefacto de la almohadilla de grasa epidural posterior de la línea media. Estas inserciones grasas en la línea media no parecen tener un efecto clínicamente significativo sobre la propagación de las AL. Más bien, Hogan ha postulado que la distribución de la solución no es uniforme y se dirige entre las estructuras del espacio epidural de acuerdo con las presiones diferenciales.
Distancia de la piel al espacio epidural
La distancia de la piel al espacio epidural varía en los diferentes niveles de la columna vertebral. En la región cervical, Han y sus colegas encontraron que la profundidad promedio de la piel al espacio epidural (a través del abordaje de la línea media) era más superficial en C5 y C6 y aumentaba en la dirección caudal. Fujinaka et al señalaron que es difícil predecir la profundidad real del espacio epidural cervical en función de las características clínicas. Por el contrario, Aldrete y colaboradores, utilizando imágenes por resonancia magnética (IRM) para medir la profundidad desde la piel hasta el ligamento amarillo interno, observaron la mayor profundidad en los niveles de C6 a T1, con una media de 5.7 cm, posiblemente debido a la presencia de tejido graso (la llamada joroba) en la zona. La profundidad al espacio en la región torácica media desde la línea media está influenciada principalmente por el ángulo caudal agudo de las apófisis espinosas. Como resultado del ángulo pronunciado y los impedimentos óseos en esta región, a menudo se prefiere el abordaje paramediano para la colocación epidural torácica media. Varios estudios han buscado medir la profundidad del espacio epidural a nivel lumbar. Los estudios de parturientas muestran un rango de profundidad de la piel al espacio de 2 a 9 cm, con un 89% en el rango de 3.5 a 7.5 cm. En su búsqueda de un modelo multivariante para predecir la distancia en una población obstétrica, Segal y sus colegas confirmaron asociaciones previamente reportadas entre aumento de peso y mayor profundidad, así como entre raza oriental y espacios menos profundos, sin asociación independiente entre raza y profundidad después de controlar por peso En un estudio anterior, Sutton y Linter registraron que la piel del espacio extradural en 3011 parturientas era de 4 a 6 cm en el 76 % de las participantes del estudio. Se encontró que los pacientes con una profundidad superficial de 2 a 4 cm, que comprenden el 16% de la población del estudio, tenían un riesgo tres veces mayor de punción dural no intencional. Es de destacar que la poca profundidad cae dentro del rango de longitud de la aguja de infiltración LA. En general, las estimaciones de la profundidad del espacio epidural no se pueden aplicar a la población en general, ya que las variables independientes, como el grado de flexión, la posición del paciente, la formación de hoyuelos y edema en la piel y el tejido subcutáneo, y el ángulo de inserción de la aguja, entre otras cosas, son difíciles de cuantificar y controlar. En un futuro próximo, la determinación ecográfica de rutina de la profundidad del espacio de forma individual antes o durante la colocación de la aguja epidural podría proporcionar los medios más fiables para disminuir el riesgo de punción dural inadvertida y otras complicaciones de la anestesia epidural. La fluoroscopia es más apropiada en la región cervical, donde la lesión de la médula espinal, la anestesia espinal total y la inyección intraarterial se encuentran entre las posibles complicaciones.
La profundidad variable del espacio epidural posterior es otra medida clínicamente relevante que puede influir en la incidencia de punción dural inadvertida. El espacio epidural posterior visto en el plano sagital de la línea media se ha descrito como en dientes de sierra, lo que caracteriza su forma segmentada. Si bien los estudios son contradictorios, en cada nivel segmentario, la profundidad del espacio epidural posterior parece menor en el extremo caudal. A pesar de estas variaciones, la distancia entre el ligamento amarillo y la dura suele estimarse en 7 mm, con un amplio rango de 2 mm a 2.5 cm. Esta distancia anterior-posterior es mayor en la región lumbar, en L3-L4, disminuye en la región torácica y está ausente en la región cervical.
EFECTOS FISIOLÓGICOS DEL BLOQUEO EPIDURAL
El bloqueo epidural proporciona anestesia quirúrgica, relajación muscular intraoperatoria y alivio del dolor intraparto y posoperatorio con efectos directos e indirectos generalizados en varios sistemas fisiológicos. La extensión de estos efectos fisiológicos depende del nivel de colocación y del número de segmentos espinales bloqueados. En general, los bloqueos nerviosos epidurales torácicos altos (es decir, por encima de T5) y los bloqueos nerviosos epidurales extensos se asocian con cambios fisiológicos más profundos que los bloqueos nerviosos con niveles sensoriales bajos (es decir, por debajo de T10). En esta sección se revisan las alteraciones fisiológicas relacionadas con la anestesia y analgesia epidural.
Bloque diferencial
El bloqueo diferencial ocurre cuando las funciones nerviosas sensoriales, motoras y simpáticas se obstruyen a diferentes velocidades y en diferentes grados. Puede observarse tanto en el inicio como en la regresión del bloqueo nervioso. En general, el bloqueo simpático, que suele ser incompleto, se extiende de dos a seis dermatomas más arriba que el bloqueo sensitivo, que a su vez es más alto que el bloqueo motor. El bloqueo sensorial también ocurre con una concentración más baja o dosis total de LA y se desarrolla más rápido que el bloqueo motor. Entre las funciones sensoriales, primero se bloquea la temperatura, luego el pinchazo y, finalmente, el tacto.
Aunque el mecanismo del bloqueo diferencial no se ha dilucidado por completo, puede atribuirse a las características anatómicas de los nervios bloqueados (p. ej., diámetro y presencia o ausencia de mielina), la longitud del tejido nervioso bloqueado (se requiere una longitud mínima de nervio bloqueado para bloqueo neuronal efectivo), diferencias en la composición de la membrana lipídica nerviosa y del canal iónico, actividad axonal concurrente durante el inicio del bloqueo nervioso y tipo y concentración de LA. Estos y varios otros mecanismos pueden contribuir colectivamente al bloqueo diferencial.
Efectos del sistema nervioso central
El flujo sanguíneo cerebral (FSC) está autorregulado y no se ve afectado por el bloqueo epidural a menos que el paciente experimente una hipotensión pronunciada. Sin embargo, la anestesia neuroaxial parece tener un efecto sedante y reducir los requisitos anestésicos de varios agentes, incluidos midazolam, propofol, tiopental, fentanilo y agentes volátiles. El grado de sedación y el efecto de ahorro de la concentración alveolar mínima (MAC) parecen estar correlacionados con la altura y el nivel del bloqueo del nervio sensorial; el bloqueo de los dermatomas torácicos medios se asocia con mayores efectos sedantes que el bloqueo de los segmentos lumbares inferiores. Aunque los datos son contradictorios, los LA de mayor concentración pueden contribuir a un mayor efecto de ahorro de MAC. La adición de adyuvantes opioides, como la morfina, a la solución epidural de AL no parece reducir más los requerimientos de agentes volátiles, aunque sí contribuye a mejorar las puntuaciones de dolor posoperatorio. En general, la disminución de los requisitos anestésicos se ha atribuido más comúnmente a la disminución de la entrada aferente inducida por el bloqueo del nervio neuroaxial más que a los efectos sistémicos de los LA, la farmacocinética alterada o la acción directa de los LA en el cerebro.
Varios estudios han demostrado una reducción de los requisitos hipnóticos y anestésicos después del bloqueo neuroaxial central. En un estudio inicial de 53 hombres adultos con estado físico I y II de la Sociedad Estadounidense de Anestesiólogos (ASA), Tverskoy y sus colegas determinaron que el bloqueo subaracnoideo con bupivacaína disminuyó los requisitos hipnóticos tanto para midazolam como para tiopental. Un estudio posterior, también en pacientes con estado físico ASA I y II, determinó que la bupivacaína epidural disminuía profundamente los requerimientos hipnóticos de midazolam. De manera similar, en un pequeño ensayo prospectivo, aleatorizado, doble ciego, controlado con placebo, Hodgson y colegas encontraron que la anestesia epidural con lidocaína redujo la CAM de sevoflurano hasta en un 50 %. Más recientemente, se ha demostrado que la bupivacaína epidural administrada por vía caudal tiene un efecto moderador sobre los requisitos de fentanilo y sevoflurano intravenosos durante la cirugía ortopédica en niños.
Efectos cardiovasculares y hemodinámicos
Los cambios cardiovasculares asociados con la anestesia y la analgesia epidurales se deben principalmente al bloqueo de la conducción de las fibras nerviosas simpáticas. Estos cambios incluyen vasodilatación venosa y arterial, RVS reducida, cambios en la cronotropía y la inotropía, y alteraciones asociadas en la presión arterial y el GC. El tipo y la intensidad de estos cambios están relacionados con el nivel de bloqueo nervioso, el número total de dermatomas bloqueados y , en relación con el tipo y la dosis de LA administrados. En general, los bloqueos nerviosos torácicos bajos o epidurales lumbares no se asocian con cambios hemodinámicos significativos, mientras que los bloqueos nerviosos torácicos superiores (particularmente los que involucran las fibras simpáticas T1-T4) pueden causar cambios más marcados, no todos los cuales son perjudiciales. Sin embargo, factores como el embarazo, la edad, las comorbilidades, la posición del paciente y la hipovolemia pueden complicar el cuadro clínico y los efectos cardiovasculares previstos.
La hipotensión
La hipotensión asociada con el bloqueo neuroaxial se debe principalmente a la vasodilatación y al aumento de la capacitancia del lecho vascular. Tanto la inhibición directa del flujo simpático hacia los nervios que inervan los vasos sanguíneos como la disminución de la liberación de catecolaminas endógenas de las glándulas suprarrenales contribuyen a la vasodilatación arterial y venosa. En general, el músculo liso arteriolar mantiene un tono autónomo, incluso en el marco de una simpatectomía completa, mientras que las venas y las vénulas se dilatan al máximo. Sin embargo, se produce cierto grado de vasodilatación arteriolar. El efecto venodilatorio también predomina debido a la gran cantidad de sangre en el sistema venoso en comparación con el sistema arterial.
El grado de hipotensión asociado con el bloqueo epidural se correlaciona con el nivel sensorial. Por ejemplo, se produce un aumento más marcado de la capacitancia venosa con el bloqueo del flujo de salida simpático a las venas esplácnicas (T6 a L1) debido a la dilatación del extenso lecho esplácnico. Con bloqueos nerviosos epidurales bajos, la vasoconstricción de áreas no bloqueadas y la liberación de catecolaminas del sistema medular suprarrenal compensan parcialmente la acumulación venosa y arteriolar y las reducciones en la presión arterial media. En general, los pacientes sanos normovolémicos experimentan una disminución nominal de la resistencia periférica y la presión arterial durante el inicio y el mantenimiento del bloqueo epidural. Los factores de riesgo de hipotensión apreciable durante la anestesia neuroaxial incluyen un nivel sensorial por encima de T5, presión inicial baja, edad avanzada y anestesia neuroaxial general combinada.
Los pacientes severamente hipovolémicos y los pacientes con problemas cardíacos también tienen más probabilidades de experimentar una hipotensión significativa que requiera soporte vasopresor e inotrópico. La hipotensión ocurre con más frecuencia con las espinales que con las epidurales, a pesar de grados equivalentes de bloqueo simpático.
Ritmo cardíaco y función cardíaca
En general, los cambios en la frecuencia cardíaca y la función ventricular varían con el nivel de bloqueo, con cambios más pronunciados a medida que aumenta el nivel. Cuando se bloquean las fibras simpáticas cardíacas de T1 a T4, se produce una disminución de la contractilidad cardíaca y bradicardia, lo que da como resultado una disminución del GC. La bradicardia también resulta de la disminución de la actividad del receptor de estiramiento auricular atribuida a la disminución de la presión auricular derecha. La acumulación venosa también contribuye a la reducción del GC, particularmente con bloqueos nerviosos más altos. Missant et al estudiaron los efectos de la anestesia epidural sobre la función ventricular izquierda y derecha en un modelo de cerdo y encontraron que la anestesia epidural lumbar redujo la RVS sin afectar la función ventricular izquierda o derecha. Sin embargo, TEA redujo la contractilidad del ventrículo izquierdo y redujo mínimamente la RVS, preservando la función del ventrículo derecho.
El bloqueo neuroaxial parece tener ciertos efectos beneficiosos sobre el sistema cardiovascular, como la mejora del flujo sanguíneo miocárdico y el equilibrio de oxígeno miocárdico. Se ha observado que la oxigenación de los tejidos mejora con TEA alta en ciertas circunstancias, particularmente con la administración de líquidos por vía intravenosa.
La TEA también parece tener efectos antianginosos, mejora la perfusión coronaria y mejora la recuperación de la isquemia miocárdica reversible. Sin embargo, si esto resulta en un mejor resultado cardíaco perioperatorio después de una cirugía torácica o cardíaca mayor, es un tema de debate en curso. Varios autores han planteado la hipótesis de que la TEA también puede proteger contra las arritmias posoperatorias y la fibrilación auricular después de cirugías cardíacas y torácicas mayores. Sin embargo, los datos son contradictorios. Svircevic et al realizaron un metanálisis que comparó GA y TEA para cirugía cardíaca y notaron menos arritmias supraventriculares posoperatorias. Sin embargo, Gu et al, en otro metanálisis reciente, no pudieron respaldar tal efecto.
Efectos pulmonares
Los cambios motores y simpáticos asociados con la anestesia epidural pueden afectar la función pulmonar, según el nivel de bloqueo. En general, el volumen corriente permanece invariable incluso durante bloqueos nerviosos neuroaxiales altos, mientras que la capacidad vital puede reducirse debido a la disminución del volumen de reserva espiratorio que se produce cuando se bloquean los músculos accesorios implicados en la espiración.
La capacidad para toser y eliminar las secreciones respiratorias también puede verse afectada, particularmente en pacientes con una función respiratoria gravemente comprometida al inicio. Sin embargo, la función de los músculos inspiratorios no se ve afectada y debe seguir siendo suficiente para proporcionar una función ventilatoria adecuada.
Los niveles sensoriales más altos pueden resultar en cambios más marcados en la función pulmonar. En un estudio centinela, Freund et al. insertaron un catéter epidural lumbar y administraron un volumen medio de 20 ml de lidocaína al 2%. Se logró un bloqueo nervioso extenso a T4, pero la disminución de la capacidad vital fue mínima. Sin embargo, la inserción del catéter a niveles más altos, con una mayor diseminación concomitante de LA, da como resultado un trastorno pulmonar más pronunciado.
Por el contrario, cuando se usa TEA en el posoperatorio, se puede observar un efecto positivo neto sobre la función pulmonar, muy probablemente porque el mayor alivio del dolor evita la colocación de férulas. En un artículo de revisión reciente, Lirk y Hollmann determinaron el papel de la TEA y confirmaron los beneficios en la cirugía mayor abdominal y torácica.
La rara aparición de paro respiratorio después de un bloqueo epidural o espinal alto puede atribuirse a la hipoperfusión del centro respiratorio en el tronco encefálico más que a los efectos directos de LA sobre el nervio frénico o el SNC.
Efectos gastrointestinales
El flujo de salida simpático al tracto GI surge de T5 a T12, mientras que la inervación parasimpática es suministrada por el nervio vago. La simpatectomía asociada con el bloqueo epidural en los niveles torácicos medios a bajos da como resultado un tono vagal sin oposición, que se manifiesta clínicamente con un aumento del peristaltismo, esfínteres relajados, un aumento de las secreciones GI y, probablemente, una restauración más rápida de la motilidad GI en la fase posoperatoria . Las náuseas y los vómitos suelen acompañar a la hiperperistalsis y pueden tratarse de manera eficaz con atropina intravenosa. En teoría, el aumento de la motilidad intestinal podría contribuir a la ruptura de las anastomosis quirúrgicas, pero esto no se ha demostrado en la literatura. Más bien, la TEA puede disminuir el riesgo de fuga anastomótica y mejorar la perfusión intestinal perioperatoria, aunque los datos son algo contradictorios. Numerosos estudios experimentales y clínicos han demostrado que la TEA protege contra la hipoperfusión esplácnica y reduce el íleo posoperatorio. Sin embargo, no se observan beneficios similares con la anestesia epidural lumbar.
Efectos renales/genitourinarios
Debido a que el flujo sanguíneo renal (FBR) se mantiene a través de la autorregulación, la anestesia epidural tiene poco efecto sobre la función renal en individuos sanos. Los mecanismos compensatorios y de retroalimentación (dilatación arteriolar aferente y vasoconstricción arteriolar eferente) aseguran RBF constante en un amplio rango de presiones (50 a 150 mHg). Durante períodos transitorios de hipotensión por debajo de 50 mm Hg, se mantiene adecuadamente el suministro de oxígeno a los riñones.
Se ha postulado que el bloqueo neuroaxial a nivel lumbar afecta el control de la función de la vejiga como consecuencia del bloqueo de las raíces nerviosas S2-S4, que transportan los nervios simpáticos y parasimpáticos que inervan la vejiga. La retención urinaria puede ocurrir hasta que desaparezca el efecto del bloqueo nervioso. El médico debe evitar administrar un volumen excesivo de líquidos por vía intravenosa si no se ha colocado un catéter urinario.
Efectos neuroendocrinos
El estrés quirúrgico produce una variedad de cambios en la respuesta inmune y humoral del huésped. Son frecuentes el aumento del catabolismo proteico y el consumo de oxígeno. Se han documentado concentraciones plasmáticas aumentadas de catecolaminas, vasopresina, hormona del crecimiento, renina, angiotensina, cortisol, glucosa, hormona antidiurética y hormona estimulante de la tiroides después de la estimulación simpática asociada con cirugía abierta mayor y mínimamente invasiva. Las manifestaciones perioperatorias de la respuesta al estrés quirúrgico pueden incluir HTA, taquicardia, hiperglucemia, función inmunitaria suprimida y función renal alterada. Los niveles elevados de catecolaminas también pueden causar un aumento de la poscarga del ventrículo izquierdo y, en combinación con otras respuestas patológicas al estrés (p. ej., respuestas proinflamatorias que pueden conducir a la inestabilidad de la placa a través de la activación de la metaloproteinasa de la matriz; niveles elevados de la hormona liberadora de corticotropina que reducen la liberación cardíaca de óxido nítrico, aumentar la producción de endotelina y agravar la disfunción endotelial coronaria), desencadenar síndromes coronarios agudos e infartos de miocardio en pacientes con cardiopatía coexistente. Se cree que la información sensorial aferente del sitio quirúrgico juega un papel fundamental en esta respuesta.
La respuesta al estrés quirúrgico puede verse influida por el bloqueo simpático durante la anestesia y la analgesia epidurales. Los mecanismos involucrados no están resueltos, pero lo más probable es que incluyan tanto el bloqueo directo de las señales aferentes y eferentes durante el estrés quirúrgico como los efectos directos de los agentes LA. Brodner et al demostraron que TEA combinado con GA dio como resultado una respuesta de estrés quirúrgico reducida en comparación con GA solo.
El efecto más crítico de la activación neuroendocrina en el período perioperatorio es el aumento de la noradrenalina plasmática, que alcanza su punto máximo aproximadamente 18 horas después de que se inicia el estímulo quirúrgico. El aumento de noradrenalina plasmática se asocia con la activación del óxido nítrico en el endotelio de pacientes con enfermedad aterosclerótica, produciendo vasoespasmo paradójico. Así, en pacientes con enfermedad aterosclerótica significativa, la combinación de vasoespasmo y un estado de hipercoagulabilidad pueden ser los factores modulados por los efectos cardioprotectores de la TEA. De hecho, los estudios indicaron que el flujo sanguíneo de las arterias coronarias mejora con TEA.
Termorregulación
La hipotermia tiene efectos secundarios significativos, como mayor morbilidad cardíaca, deterioro de la coagulación, mayor pérdida de sangre y mayor riesgo de infección. La tasa y severidad de la hipotermia asociada con la anestesia epidural es similar a la observada durante los casos bajo AG. La hipotermia asociada con la anestesia neuroaxial se debe principalmente a la vasodilatación periférica que produce la redistribución del calor desde el centro hacia la periferia. Además, la producción de calor reducida (debido a la actividad metabólica reducida) da como resultado un balance de calor negativo debido a la pérdida de calor sin cambios. Finalmente, se altera el control de la termorregulación. Es de destacar que el recalentamiento con dispositivos de calentamiento por aire forzado ocurre más rápidamente con la anestesia neuroaxial en comparación con la AG debido a la vasodilatación periférica.
Sistema de coagulación
El postoperatorio es un estado de marcada hipercoagulabilidad. El bloqueo neuroaxial se asocia con un menor riesgo de TVP y embolia pulmonar, así como con un menor riesgo de trombosis arterial y venosa.
FARMACOLOGIA DEL bloque EPIDURAL
La comprensión de la fisiología de la conducción nerviosa y la farmacología de los AL es esencial para el éxito del bloqueo epidural. La potencia y la duración de los AL, el bloqueo preferencial de las fibras sensoriales y motoras y la duración anticipada de la cirugía o la necesidad de analgesia posoperatoria son factores que deben considerarse antes de iniciar el bloqueo epidural. Esta sección cubre varios aspectos prácticos para lograr una anestesia y analgesia epidural eficaces.
Las soluciones epidurales pueden contener un LA con o sin un fármaco adyuvante. La dosis, el volumen y la concentración, así como el sitio de inyección, de la solución de LA varían, lo que da como resultado diferentes efectos farmacodinámicos. Las fibras nerviosas A, B y C varían en tamaño y en presencia de una vaina de mielina. Las fibras A-delta y C son responsables de la transmisión de la temperatura y el dolor. Las fibras B son fibras autonómicas. Las fibras A más grandes (especialmente las fibras A-alfa) son fibras motoras. Las fibras C son amielínicas y de menor tamaño. Debido a que carecen de una vaina protectora de mielina y una barrera de difusión, se bloquean rápidamente. Las fibras A y B están mielinizadas y son de mayor tamaño que las fibras C. Las fibras B son responsables de la transmisión del sistema nervioso autónomo. Son de menor tamaño que las fibras A-delta, pero más grandes que las fibras C. Está ampliamente aceptado que las fibras autonómicas son más susceptibles al bloqueo del nervio LA que las fibras sensoriales. El AL administrado por vía epidural bloquea preferentemente la función neural simpática; esto explica el bloqueo dermatomal simpático más extenso en comparación con los bloqueos nerviosos sensitivos y motores. Sin embargo, Ginosar et al sugirieron recientemente que la función sensorial era más susceptible al bloqueo que la función simpática. Varios otros estudios coincidieron. La dosis y la concentración de LA utilizada pueden explicar los diferentes hallazgos en estos estudios. Debido a su gruesa vaina de mielina, las fibras motoras requieren mucho más LA y mucho más tiempo antes de que se logre un bloqueo nervioso adecuado.
Los anestésicos locales producen un bloqueo nervioso reversible al bloquear el paso de sodio a través de la membrana nerviosa. Cuando se inyecta LA en el espacio epidural, ocurren varias cosas. La mayor parte del AL inyectado se absorbe en la sangre venosa y una gran parte se retiene en el tejido graso epidural. Los principales sitios de acción de un AL administrado por vía epidural son las raíces nerviosas ventrales y dorsales que pasan a través del espacio epidural. Sin embargo, según los estudios que utilizan LA marcados, los LA pueden cruzar la duramadre y penetrar la médula espinal, pero en menor medida que su penetración en las raíces nerviosas espinales. Las raíces nerviosas segmentarias son fibras nerviosas sensoriales, motoras y simpáticas mixtas. Por lo tanto, los tres tipos de fibras se verán afectados (en diversos grados).
Elección de anestésicos locales
Los fármacos utilizados para el bloqueo epidural se pueden clasificar en AL de acción corta, intermedia y prolongada. El inicio del bloqueo epidural en los dermatomas que rodean inmediatamente el sitio de la inyección generalmente se puede detectar dentro de los 5 o 10 minutos, si no antes. El tiempo hasta el efecto máximo varía según el tipo de AL y la dosis/volumen administrado (Tabla 19).
TABLA 19. Anestésicos locales de uso común para la anestesia y analgesia epidural.
| Droga | Concentracion (%) | Tiempo de inicio (min) | Duración (minutos) |
|---|---|---|---|
| 2-cloroprocaína | 3 | 5-15 | 30-90 |
| Lidocaína | 2 | 10-20 | 60-120 |
| Bupivacaína | 0.0625-0.5 | 15-20 | 160-220 |
| Ropivacaína | 0.1-0.75 | 15-20 | 140-220 |
| Levobupivacaína | 0.0625-0.5 | 15-20 | 150-225 |
El LA de acción más corta para el bloqueo neuroaxial es la cloroprocaína, un éster. En el pasado, la cloroprocaína se asociaba con aracnoiditis adhesiva cuando se administraban accidentalmente grandes volúmenes en el espacio subaracnoideo. Además, no es infrecuente que se notifique dolor de espalda intenso cuando se administran grandes volúmenes en el espacio epidural, muy probablemente debido a los conservantes de ácido etilendiaminotetraacético (EDTA) y bisulfito en la solución. Desde 1996, la cloroprocaína sin conservantes ha estado disponible y no se ha asociado con efectos neurotóxicos ni dolor de espalda. En entornos ambulatorios y para partos por cesárea de emergencia con epidurales in situ, la cloroprocaína puede proporcionar una excelente anestesia quirúrgica rápidamente, sin demorar el alta de la sala de recuperación.
Administrada por vía epidural, la lidocaína al 2% es un LA de acción intermedia que se usa comúnmente para la anestesia quirúrgica. Cuando se agrega epinefrina a la solución (1:200,000), prolonga la duración de la acción hasta en un 60%.
Los AL de acción prolongada utilizados para el bloqueo epidural son bupivacaína, levobupivacaína (ya no está disponible en los Estados Unidos) y ropivacaína. Las concentraciones diluidas (p. ej., 0.1 % a 0.25 %) se pueden usar para la analgesia, mientras que las concentraciones más altas (p. ej., 0.5 %) pueden ser más apropiadas para la anestesia quirúrgica. La adición de epinefrina a estas soluciones puede prolongar la duración de la acción, aunque este efecto es menos fiable con los agentes de acción prolongada que con los de acción intermedia. La inyección intravascular accidental de bupivacaína puede dar lugar a reacciones cardiotóxicas graves (hipotensión, bloqueo del nervio auriculoventricular, fibrilación ventricular y torsades de pointes) refractarias a los métodos habituales de reanimación. La justificación de la resistencia a las medidas de reanimación radica en su alto grado de unión a proteínas y su efecto más pronunciado sobre el bloqueo de los canales de sodio cardiacos. La levobupivacaína, el enantiómero S de la bupivacaína, tiene un perfil similar al de la bupivacaína pero con efectos cardiotóxicos menos pronunciados. La ropivacaína, un análogo de la mepivacaína, tiene un perfil de acción similar al de la bupivacaína. En la mayoría de los estudios, la ropivacaína ha demostrado una duración de acción ligeramente más corta que la bupivacaína, potencialmente con un bloqueo nervioso motor menos denso en dosis equipotentes. Un impedimento para el uso más amplio de la ropivacaína en la práctica clínica es su mayor costo.
Inicio y duración de los anestésicos locales
La alcalinización de los LA, que se comercializan en un estado ionizado soluble en agua, acelera el inicio. Al aumentar la concentración de la forma no ionizada, hay más LA soluble en lípidos disponible para penetrar la vaina neural y la membrana nerviosa. La adición de bicarbonato de sodio inmediatamente antes de la inyección de lidocaína, mepivacaína o cloroprocaína produce un inicio de la anestesia clínicamente significativo más rápido y también puede contribuir a un bloqueo nervioso más denso. Sin embargo, la ropivacaína y la bupivacaína precipitarán con la adición de bicarbonato a menos que se utilice una concentración muy baja. No se ha demostrado que la combinación de fármacos de acción corta y prolongada para un inicio rápido y un bloqueo prolongado de los nervios sensoriales sea eficaz. Por ejemplo, mezclar 2-cloroprocaína con bupivacaína para el inicio rápido de la primera y la duración prolongada de la última da como resultado una reducción de la duración y la eficacia de la bupivacaína.160 La administración continua de fármacos y el uso de aditivos evitan la necesidad de mezclar los AL.
Consejos NYSORA
No se ha demostrado que sea eficaz la combinación de AL de acción corta, intermedia o prolongada para un inicio rápido con una duración prolongada de la acción. Droga continua
la administración y el uso de aditivos evitan la necesidad de mezclar los LA.
Agregar epinefrina a ciertos LA puede aumentar la duración de la acción, muy probablemente al disminuir la absorción vascular. El efecto es mayor con 2-cloroprocaína, lidocaína y mepivacaína y es menos efectivo con los agentes de acción prolongada. No se ha demostrado que otros vasoconstrictores, como la fenilefrina, sean tan efectivos para reducir los niveles máximos de LA en sangre como la epinefrina.
Adyuvantes a los Anestésicos Locales en el Espacio Epidural
Recientemente se ha estudiado una variedad de otras clases de fármacos para tratar de mejorar la calidad del bloqueo neuroaxial. Además de varios opioides (p. ej., fentanilo, sufentanilo y preparaciones de morfina); agonistas α-adrenérgicos; inhibidores de la colinesterasa; agonistas-antagonistas opioides semisintéticos; ketamina; y midazolam han sido estudiados, con resultados mixtos. La administración de clonidina en el espacio epidural ha sido ampliamente estudiada. Un agonista adrenérgico α2, la clonidina parece prolongar la duración de la acción de los AL, aunque el mecanismo aún no está claro. Los estudios en animales han demostrado que la clonidina reduce el flujo sanguíneo regional de la médula espinal y, por lo tanto, reduce la velocidad de eliminación del fármaco. Kroin y colegas demostraron que el mecanismo por el cual la clonidina prolonga la duración de un bloqueo nervioso cuando se mezcla con LA no está mediado por adrenorreceptores α; más bien, es más probable que esté relacionado con la corriente catiónica activada por hiperpolarización Ih.
Algunos de los beneficios potenciales de la administración de clonidina en el espacio epidural pueden incluir los siguientes:
1. Prolongación y potenciación de los efectos de las AL epidurales sin riesgo adicional de hipotensión
2. Reducción de los requerimientos de dosis de AL para la analgesia epidural del trabajo de parto
3. Analgesia eficaz sin deterioro motor
4. Efecto sinérgico con opioides y agonistas-antagonistas opioides
5. Modulación de la respuesta de estrés a la cirugía torácica
6. Preservación de la función pulmonar después de la toracotomía
7. Posible reducción en la respuesta de citoquinas, reduciendo aún más la sensibilidad al dolor
Los efectos secundarios comúnmente asociados con la clonidina epidural incluyen hipotensión independiente de la dosis, bradicardia, sedación y sequedad de boca. La combinación de clonidina con otros agentes, como opiáceos, anticolinérgicos, agonistas-antagonistas de opiáceos y ketamina, puede potenciar los efectos beneficiosos de estos fármacos y minimizar los efectos secundarios adversos.
La neostigmina, un inhibidor de la colinesterasa, es una adición más reciente a la lista de aditivos epidurales para la analgesia selectiva. El mecanismo de acción de su efecto analgésico parece ser la inhibición de la descomposición de la acetilcolina y la estimulación indirecta de los receptores muscarínicos y nicotínicos en la médula espinal. Aunque la experiencia con neostigmina epidural es limitada, se ha informado que brinda alivio del dolor posoperatorio sin inducir depresión respiratoria, deterioro motor o hipotensión. Cuando se combina con otros opioides, clonidina y LA, puede brindar beneficios similares a la clonidina sin el perfil de efectos secundarios de cualquiera de estos medicamentos administrados solos. Las observaciones en pacientes con dolor por cáncer mostraron que su uso podría estar asociado con menos náuseas y vómitos que la aplicación intratecal. En una investigación que aleatorizó a 48 pacientes para recibir 0, 1, 2 o 4 μg/kg de neostigmina epidural además de un anestésico espinal de bupivacaína para una cirugía menor de rodilla, no se observó ningún caso de náuseas o vómitos intraoperatorios, y las puntuaciones de náuseas posoperatorias no aumentaron. difieren entre grupos. Estos resultados deben ser corroborados por estudios adicionales antes de que se pueda recomendar la neostigmina epidural para la práctica diaria.
Se han considerado otros agentes, como ketamina, tramadol, droperidol y midazolam, para la administración epidural, con resultados mixtos. Existe una gran controversia en torno al uso de midazolam por vía intratecal. A pesar de múltiples publicaciones que recomiendan su uso, estudios recientes han demostrado que incluso una sola dosis de midazolam intratecal puede tener efectos neurotóxicos. Hasta que se pueda garantizar su perfil de seguridad en sujetos humanos, no se recomienda su uso neuroaxial en este momento.
Un agente que se muestra prometedor es la formulación de liberación prolongada de uno de los opioides más antiguos, la morfina. DepoDur, el nombre comercial de la morfina epidural de liberación prolongada, utiliza un sistema de liberación de fármacos llamado DepoFoam. DepoFoam está compuesto por partículas microscópicas a base de lípidos con vesículas internas que contienen el fármaco activo y lo liberan lentamente. Estudios recientes han demostrado un alivio eficaz del dolor con efectos secundarios relativamente menores durante hasta 48 horas cuando se dosifica adecuadamente. Sin embargo, las preocupaciones sobre la depresión respiratoria tardía han limitado su uso clínico en esta etapa temprana de su uso clínico.
Otros factores que afectan el sitio de inyección del bloqueo epidural
El bloqueo epidural es más efectivo cuando el bloqueo del nervio o el catéter se inserta en un lugar que corresponde a los dermatomas cubiertos por la incisión quirúrgica. El inicio más rápido y el bloqueo nervioso más denso ocurren en el sitio de la inyección. Al insertar el catéter más cerca de la distribución dermatomal del sitio quirúrgico, se puede administrar una dosis más baja de fármaco, lo que reduce los efectos secundarios. Este concepto es especialmente importante cuando se utiliza la analgesia epidural torácica para la analgesia posoperatoria.
Después de la inyección epidural lumbar, los efectos analgésicos y anestésicos se extienden en mayor grado craneal que caudalmente. Cabe señalar que hay un retraso en el inicio de la anestesia en los segmentos L5-S1 secundario al tamaño más grande de estas raíces nerviosas. Con la inyección torácica, el LA se extiende uniformemente desde el sitio de la inyección, pero encuentra resistencia para bloquearse en la región lumbar debido a las raíces nerviosas más grandes. Controlando la dosis en la región torácica se puede establecer un verdadero bloqueo segmentario que afecte únicamente a la región torácica. Se preservarán las regiones lumbar y sacra, evitando así un bloqueo simpático más extenso y la subsiguiente hipotensión y disfunción vesical asociadas, así como el bloqueo motor de las extremidades inferiores.
Dosis, volumen y concentración
La dosis de AL necesaria para la anestesia o analgesia epidural es función de la concentración de la solución y del volumen inyectado. La concentración de la droga afecta la densidad del bloqueo nervioso; cuanto mayor sea la concentración, más profundo será el bloqueo de los nervios motores y sensoriales. Concentraciones más bajas pueden producir selectivamente un bloqueo nervioso sensorial.
El volumen y la dosis total de LA son las variables que afectan el grado de extensión del bloqueo nervioso. Un mayor volumen de la misma concentración de LA bloqueará los nervios de un mayor número de segmentos. Sin embargo, si la dosis total de LA no cambia pero la concentración se duplica, el volumen puede reducirse a la mitad para lograr una distribución similar de LA. Una pauta generalmente aceptada para la dosificación de la anestesia epidural en adultos es de 1 a 2 ml por segmento a bloquear. Esta pauta debe ajustarse para pacientes más bajos y para pacientes muy altos. Por ejemplo, para lograr un nivel sensorial T10 con una inyección L3-L4, se deben administrar aproximadamente 8 ml de LA. Por debajo de las concentraciones del equivalente de lidocaína al 1%, el bloqueo de los nervios motores es mínimo, independientemente del volumen de AL inyectado, a menos que las dosis se administren a intervalos repetidos.
El tiempo para repetir una dosis de LA depende de la duración del fármaco. Las dosis deben administrarse antes de que el bloqueo nervioso retroceda hasta el punto en que el paciente experimente dolor, lo que comúnmente se conoce como “tiempo hasta la regresión de dos segmentos”. Esto se define como el tiempo que tarda el bloqueo del nervio sensorial en retroceder dos niveles de dermatoma. Cuando se ha producido una regresión de dos segmentos, se puede administrar con seguridad entre un tercio y la mitad de la dosis de carga inicial para mantener el bloqueo nervioso. Por ejemplo, el tiempo de regresión de dos segmentos de la lidocaína es de 60 a 140 minutos (Tabla 20).
TABLA 20. Redosificación de anestésicos locales.
| Droga | Concentracion (%) | Tiempo para dos segmentos Regresión (min) | Tiempo recomendado para "Recargar" Dosis desde la dosis inicial (min) |
|---|---|---|---|
| 2-cloroprocaína | 3 | 45-75 | 45 |
| Lidocaína | 2 | 60-140 | 60 |
| Bupivacaína | 0.10 | 180-260 | 120 |
| Ropivacaína | 0.10 | 180-260 | 120 |
Posicionamiento del paciente
La posición del paciente durante el inicio del bloqueo epidural no parece afectar la difusión resultante de la analgesia o la anestesia. El paciente puede colocarse en posición lateral o sentada. La línea media de la columna es más fácil de palpar cuando el paciente está sentado, especialmente en el paciente obeso, lo que facilita técnicamente el bloqueo del nervio. Ya sea que el paciente esté sentado o en posición lateral, no hay una diferencia significativa en la altura del bloqueo nervioso. En un estudio de Seow et al., se sugirió que el tiempo de inicio, la duración y la densidad del bloqueo del nervio motor son ligeramente más rápidos en el lado dependiente cuando la epidural se coloca con el paciente en posición lateral.
Características de los pacientes: edad, peso, altura y embarazo
Con el avance de la edad, se reduce la dosis de LA requerida para lograr un bloqueo nervioso específico. Algunos estudios han observado una diferencia no clínicamente significativa en la altura del bloqueo nervioso (entre uno y cuatro segmentos más alto) con un volumen y una concentración fijos de LA en pacientes mayores de 50 años. La mayor propagación en los ancianos puede estar relacionada con el tamaño reducido de la intervertebral foramen, que teóricamente limita la salida de los LA del espacio epidural. También se ha propuesto una disminución de la grasa epidural, que permite que una mayor cantidad del fármaco inunde los nervios, y cambios en la distensibilidad del espacio epidural, que pueden conducir a una mayor extensión cefálica.
Hay poca correlación entre la extensión de la analgesia y el peso del paciente. Sin embargo, en pacientes con obesidad mórbida, puede haber compresión del espacio epidural relacionada con el aumento de la presión intraabdominal; se puede lograr un mayor bloqueo nervioso con una dosis dada de LA.
La altura parece jugar un papel pequeño en los requisitos de LA. Para pacientes bajos (≤5 pies 2 pulgadas), la práctica común ha sido reducir la dosis a 1 ml por segmento a bloquear (en lugar de 2 ml por segmento). Bromage sugirió un régimen de dosificación más preciso consistente en aumentar la dosis de LA en 0.1 ml por segmento por cada 2 pulgadas por encima de los 5 pies de altura. La práctica más segura es usar dosis incrementales y monitorear el efecto para evitar niveles anestésicos excesivamente altos.
El embarazo provoca una mayor sensibilidad tanto a los AL como a los anestésicos generales, aunque los estudios sobre las causas son contradictorios. Los niveles elevados de progesterona y endorfinas endógenas pueden contribuir. Se ha publicado evidencia contradictoria con respecto a la propagación de LA en mujeres embarazadas versus no embarazadas.
Bloqueo nervioso epidural intermitente versus continuo
La decisión de utilizar una dosificación intermitente después de la dosis de carga inicial, una infusión continua o una dosificación en bolo intermitente programada o controlada por el paciente puede estar influenciada por la naturaleza de la cirugía o el procedimiento, el personal y el equipo.
Todas estas opciones pueden proporcionar analgesia o anestesia epidural segura y eficaz. Las ventajas de la infusión continua incluyen una mayor estabilidad cardiovascular, menos requisitos de mano de obra, menor incidencia de taquifilaxia, menor frecuencia y gravedad de los efectos secundarios relacionados con las inyecciones en bolo, menor propagación rostral, menor riesgo de contaminación potencial y la capacidad de lograr un estado estacionario. de anestesia La dosificación de bolo manual intermitente, por otro lado, es simple y no requiere equipo adicional (p. ej., dispositivos de infusión).
TÉCNICA EPIDURAL
Varios factores influyen en el éxito del bloqueo epidural, incluida la experiencia y el conocimiento de la anatomía del médico, la preparación y el posicionamiento del paciente, el nivel de inserción del catéter epidural y la técnica utilizada para iniciar el procedimiento.
Esta sección revisa los factores que contribuyen a la colocación epidural exitosa, comenzando con la selección y preparación del paciente, los requisitos del equipo y las recomendaciones actuales para la prevención de complicaciones infecciosas asociadas con las técnicas neuroaxiales. Luego presenta aspectos técnicos de la colocación epidural cervical, torácica y lumbar y aborda diversas controversias relacionadas con la técnica de bloqueo neuroaxial, como el método óptimo para identificar el espacio epidural y la eficacia de la dosis de prueba epidural.
Evaluación del paciente
Como en el caso de cualquier anestesia, los riesgos y beneficios de la colocación epidural deben discutirse con el paciente de manera consistente con el consentimiento informado. Todas las inquietudes y preguntas deben abordarse antes de la administración de la premedicación. Cuando exista una barrera del idioma, se deben utilizar intérpretes capacitados o servicios de traducción telefónica. El historial médico del paciente y la lista de medicamentos activos deben revisarse antes de iniciar el bloqueo epidural, con especial énfasis en la presencia de condiciones que puedan predisponer al paciente a complicaciones graves. Debe tenerse en cuenta el tratamiento farmacológico que influya en la función de coagulación del paciente o en la respuesta fisiológica al bloqueo de las fibras preganglionares simpáticas, incluso cuando se administró la última dosis. También se debe documentar la última ingesta oral del paciente. Para aquellos pacientes que reciben bloqueo epidural como único anestésico o como adyuvante de la AG para procedimientos quirúrgicos electivos, se deben hacer cumplir las pautas de la ASA sobre nada por vía oral. Los pacientes con condiciones médicas que empeoran con la poscarga o la precarga reducidas (p. ej., EA grave, estenosis mitral, miocardiopatía hipertrófica) y los pacientes que pueden experimentar un empeoramiento de la dificultad para respirar, como aquellos con enfermedad pulmonar restrictiva o EPOC grave, pueden requerir pruebas adicionales. Las condiciones clínicas que predisponen a los pacientes a infecciones neuroaxiales, como inmunosupresión, DM, pancreatitis y abuso de alcohol o drogas, pueden requerir una evaluación adicional o estudios de laboratorio. Se deben evaluar y documentar los déficits neurológicos o trastornos del SNC preexistentes. Los antecedentes de sensibilidad o reacción adversa a los opioides o los LA y las complicaciones relacionadas con procedimientos epidurales previos requieren más investigación.
El examen físico debe incluir una evaluación de la columna vertebral en busca de evidencia de escoliosis o cirugía de espalda previa, infección focal, rango de movimiento severamente limitado u otros hallazgos que pueden hacer que la colocación epidural sea más difícil o imposible. La obesidad, especialmente la obesidad central, puede oscurecer los puntos de referencia de la superficie.
No se requieren estudios de laboratorio de rutina para la colocación epidural en pacientes sanos para procedimientos de rutina. Muchos médicos pueden optar por obtener un conteo completo de células sanguíneas (CBC), particularmente cuando se espera una pérdida de sangre apreciable o cuando se sabe que el paciente está anémico. Se debe obtener una evaluación inicial del estado de coagulación del paciente o el recuento de plaquetas en pacientes con trastornos de la coagulación conocidos o sospechados, diátesis hemorrágica y trombocitopenia, así como en pacientes que reciben terapia antitrombótica o trombolítica o cualquier medicamento que se sabe que afecta la calidad o función de las plaquetas (además de AINE de rutina).
Consejos NYSORA
• No se requieren estudios de laboratorio de rutina para iniciar el bloqueo epidural en pacientes sanos para procedimientos de rutina.
• Los pacientes con trastornos hemorrágicos conocidos o sospechados y aquellos que reciben terapia antitrombótica o trombolítica requieren una evaluación del estado de coagulación inicial o el recuento de plaquetas (y posiblemente la función plaquetaria).
• Los pacientes que se someten a cirugías con pérdida de sangre anticipada o cambios hemodinámicos pueden requerir estudios adicionales, incluido un hemograma completo.
PREPARACIÓN
Se debe asegurar un catéter intravenoso de gran calibre para la administración de líquidos o medicamentos de emergencia antes de iniciar el bloqueo epidural. La precarga de líquidos no es necesaria y puede ser perjudicial en ciertos subgrupos de pacientes con presión oncótica coloidal sérica disminuida (p. ej., aquellas con quemaduras, pacientes con preeclampsia).
Sin embargo, las condiciones reversibles, como la hipovolemia grave, deben controlarse antes de la colocación y dosificación del bloqueo nervioso.
El control adecuado durante la realización del bloqueo epidural depende del propósito del bloqueo nervioso epidural y de cuándo y dónde se administrará la epidural. Los bloqueos nerviosos epidurales para la analgesia, como la analgesia del trabajo de parto, requieren una monitorización intermitente de la presión arterial durante la colocación y durante la infusión epidural, así como una oximetría de pulso continua con monitorización de la frecuencia cardíaca durante la colocación y el inicio del bloqueo nervioso. Debe estar disponible el monitoreo de electrocardiograma (ECG). En pacientes en trabajo de parto, se recomienda la monitorización de la frecuencia cardíaca fetal antes y después de la colocación si la monitorización continua no es factible.
Los sedantes o analgésicos se administran con frecuencia para aliviar el estrés y la incomodidad del paciente durante la colocación de la epidural y pueden requerir monitores y equipos adicionales, como una cánula nasal. Si se administran premedicaciones, debe estar presente personal médico que pueda proporcionar un seguimiento continuo. Cabe destacar que se debe evitar la sedación excesiva para garantizar la cooperación del paciente durante la colocación, para detectar la presencia de parestesias durante la colocación y para evaluar el nivel de bloqueo sensorial y el efecto de la dosis de prueba (si se administra). Se requieren monitores ASA estándar para el inicio y el manejo intraoperatorio de la anestesia epidural. Los medicamentos y equipos de emergencia deben estar fácilmente disponibles durante el inicio de todos los procedimientos neuroaxiales centrales (Tabla 21).
TABLA 21. Equipo de emergencia y medicamentos para el inicio del bloqueo neuroaxial.
| equipo de vía aérea | Bolso Ambu con mascarilla |
| Fuente de oxígeno |
|
| Vías respiratorias orales y nasales |
|
| Mangos y hojas de laringoscopio |
|
| tubos endotraqueales |
|
| Estilete/bougie de Eschmann |
|
| Jeringas y agujas | |
| Medicamentos de emergencia | La efedrina |
| Fenilefrina |
|
| La epinefrina |
|
| La atropina |
|
| Sedante hipnótico |
|
| emulsión de lípidos al 20% |
|
| Succinilcolina |
Comunicación con el personal quirúrgico
Una conversación con el personal quirúrgico sobre el abordaje quirúrgico, la posición deseada del paciente, la duración estimada del procedimiento quirúrgico, los objetivos anestésicos o analgésicos del bloqueo y los requisitos analgésicos posoperatorios pueden ayudar a determinar si una epidural continua, una sola Es preferible una inyección epidural o una CSE. El personal quirúrgico también puede compartir información sobre el paciente que no está fácilmente disponible en el historial o que no es evidente de inmediato durante la entrevista preoperatoria.
Cuando sea factible, para minimizar los retrasos innecesarios, el bloqueo nervioso puede iniciarse en el área preoperatoria o en el quirófano mientras el personal de enfermería prepara el equipo quirúrgico.
Donde sea que se realice el bloqueo nervioso, es esencial contar con espacio suficiente para el anestesiólogo y, de manera óptima, un asistente, así como equipo adecuado de iluminación, monitoreo y reanimación.
Equipos
Las bandejas epidurales desechables, estériles y preparadas comercialmente están disponibles de varios fabricantes. Un kit estándar normalmente incluye lo siguiente: un paño estéril; hisopos de preparación; esponjas de gasa 4 × 4; una toalla de papel; solución de povidona yodada; una ampolla de cloruro de sodio al 0.9% sin conservantes; una ampolla de 5 mL de lidocaína al 1.5% con epinefrina 1:200,000; una ampolla de 5 mL de lidocaína al 1% para infiltración cutánea; un dispositivo de filtrado (aguja o pajilla); un filtro bacteriano; agujas y jeringas de varios tamaños; una aguja epidural estilizada con marcas de cm; una jeringa LOR de vidrio o plástico de 5 o 10 ml (ya sea Luer lock o Luer slip); un dispositivo de seguridad del conector del catéter; un catéter epidural con graduaciones centimétricas y un conector/adaptador; un dispositivo de asistencia de hilo (TAD); un protector de agujas para desechar objetos punzocortantes; y etiquetas
En un kit epidural para adultos, la aguja epidural suele ser de calibre 17 o 18 y 9 cm (aproximadamente 3.5 pulgadas) de largo, con marcas en la superficie a intervalos de 1 cm. Hay disponibles agujas más largas de hasta 15 cm (6 pulgadas) de largo para pacientes obesos. La aguja Tuohy, que suele suministrarse en kits no personalizados, tiene una punta curva con un bisel romo diseñado para permitir una identificación más fácil del tejido a medida que avanza la aguja y facilitar el paso del catéter epidural. Las alas en la unión del eje y el centro de la aguja pueden permitir un mejor control a medida que la aguja pasa a través del tejido, particularmente cuando se usa la técnica de "gota colgante" para la identificación del espacio epidural, aunque algunos médicos pueden preferir agujas epidurales sin alas o con alas acoplables. (Figura 14 y XNUMX).

Figura 14 y XNUMX. Agujas epidurales: configuración de bisel y ala.
También están disponibles agujas epidurales con una abertura posterior para la salida de una aguja espinal (para CSE) y agujas de doble luz con aberturas separadas para la aguja espinal y el catéter.
Los catéteres epidurales varían en diámetro, materiales y diseño de la punta. En los kits preparados comercialmente, los catéteres de calibre 19 suelen combinarse con agujas epidurales de calibre 17; Los catéteres de calibre 20 se emparejan con agujas de calibre 18. Muchos catéteres epidurales actualmente disponibles son mezclas de nailon con diversos grados de rigidez para facilitar el enhebrado. Algunos catéteres rígidos de nailon tienen puntas flexibles especialmente diseñadas para desviarse de las venas, los nervios y otros obstáculos que se encuentran en el espacio epidural. Los catéteres reforzados con alambre incrustados en un catéter de mezcla de nailon o poliuretano representan un avance tecnológico más reciente y se están volviendo cada vez más populares (Figura 15 y XNUMX). Las versiones para adultos tienen un diámetro de calibre 19 y están diseñadas para usarse con una aguja epidural de calibre 17; versiones pediátricas están disponibles de algunos fabricantes.

Figura 15 y XNUMX. Catéter reforzado con alambre de un solo orificio en el extremo. (Usado con permiso de Epimed International.)
Muchos catéteres de nailon y reforzados con alambre disponibles en el mercado se fabrican en versiones de orificio único y multiorificio (Figura 16 y XNUMX). La falta de datos sólidos impide una evaluación completa de si los resultados clínicos, como la incidencia de parestesias, la canulación de la vena epidural, la migración intratecal y la analgesia adecuada, mejoran con el diseño de puerto único o multipuerto. Sin embargo, un ensayo prospectivo, simple ciego, aleatorizado y controlado realizado en 2009 por Spiegel et al investigó el éxito de la analgesia del trabajo de parto, la cantidad de episodios de dolor irruptivo que requerían medicamentos complementarios y la aparición de complicaciones, como parestesias y colocación de catéteres intravasculares e intratecales. , en 493 parturientas que recibieron un catéter de poliuretano reforzado con alambre de un solo orificio terminal o un catéter de nailon reforzado con alambre de múltiples orificios. Los autores no encontraron diferencias estadísticamente significativas en los resultados entre los dos grupos y postularon que la flexibilidad que brinda la bobina de alambre puede eliminar cualquiera de las posibles ventajas del diseño de puertos múltiples.

Figura 16 y XNUMX. Catéter multiorificio reforzado con alambre. (Usado con permiso de Epimed International.)
Consejos NYSORA
• El uso de catéteres epidurales reforzados con alambre parece reducir la incidencia de complicaciones asociadas con las técnicas epidurales, incluida la canalización de la vena epidural, parestesias y analgesia inadecuada.
• Los datos actuales sugieren que los resultados clínicos son similares con el uso de catéteres con resorte unipuerto y multipuerto; la flexibilidad que ofrece el serpentín de acero inoxidable parece anular cualquier beneficio potencial de un diseño multipuerto.
El equipo adicional que puede ser necesario para el inicio de los procedimientos epidurales incluye clorhexidina al 0.5 % con etanol (Hydrex®) o clorhexidina al 2 % con alcohol isopropílico al 70 % (ChloraPrep®), que no se suministra en bandejas epidurales; un vendaje oclusivo estéril transparente para el sitio de punción; y cinta adhesiva para asegurar el catéter. Para minimizar el riesgo remoto de aracnoiditis química, la solución de desinfección de la piel no debe entrar en contacto con los medicamentos o equipos epidurales y debe dejarse secar por un tiempo adecuado. Por lo general, un gran apósito transparente (p. ej., Tegaderm) y cinta adhesiva son suficientes para evitar que el catéter se desprenda y para mantener el sitio de inserción epidural visible y limpio. Se puede colocar una pluma estéril para etiquetar medicamentos y una aguja espinal de calibre 25 o 27 (para CSE) en el campo estéril.
Consejos NYSORA
• Se recomienda un vendaje oclusivo transparente y estéril para evitar que el catéter se desprenda.
• El catéter y sus marcas en centímetros deben ser visibles para el anestesista para asegurarse de que el catéter permanezca en el sitio de inserción original y que el líquido cefalorraquídeo y el hemo no regresen antes de la dosificación.
Analgesia y sedación durante el inicio del bloqueo nervioso
Se puede proporcionar analgesia o sedación para mejorar la comodidad del paciente durante el bloqueo neuroaxial. Sin embargo, hay evidencia emergente de que los sedantes intravenosos pueden aumentar la percepción del dolor de una manera específica para el tipo de agente y el tipo de dolor. Suele ser suficiente una sedación ligera con una benzodiazepina (más comúnmente midazolam) o un opioide de acción corta antes de la colocación epidural. Esto también puede ser apropiado para pacientes obstétricas. En un pequeño estudio aleatorio doble ciego, Frölich y sus colegas encontraron que la analgesia y la sedación maternas con fentanilo y midazolam antes de la colocación de la columna vertebral no se asociaron con efectos neonatales adversos. Es importante destacar que las madres tanto del grupo que recibió premedicación como del grupo de control no mostraron diferencias en su capacidad para recordar los nacimientos de sus bebés.
Para aquellos que prefieren estar "dormidos" durante la colocación de la epidural, se puede titular una infusión de propofol para mantener la sedación sin deterioro respiratorio en entornos clínicos seleccionados.
Sin embargo, es preferible tener pacientes adultos despiertos y lo suficientemente cooperativos para alertar al anestesista sobre la presencia de parestesias durante el inicio del bloqueo neuroaxial y para participar en la evaluación del nivel sensorial. En escenarios clínicos en los que la administración de premedicación antes de la colocación de la epidural puede no ser adecuada, parece haber un efecto placebo por el uso de palabras más suaves y tranquilizadoras durante la administración de lidocaína en la roncha cutánea, que a menudo se considera la parte más dolorosa del tratamiento. procedimiento. Los estudios sugieren que los siguientes consejos también pueden servir para reducir el dolor en la inyección de AL: La cloroprocaína (con o sin bicarbonato de sodio) puede ser menos dolorosa que la lidocaína para la infiltración de la piel; ajustar el pH de la lidocaína para aproximarse al pH fisiológico reduce el dolor de la inyección; y la crioanalgesia (refrigeración de la piel) puede ser tan efectiva como amortiguar la solución de LA con bicarbonato de sodio.
Consejos NYSORA
Los siguientes consejos pueden servir para reducir el dolor en la inyección de AL para la infiltración de la piel:
• Comunicación con el paciente durante el procedimiento y tranquilidad verbal
• Ajuste del pH de la lidocaína con la adición de bicarbonato de sodio para aproximarse más al pH fisiológico
• Enfriamiento de la piel (crioanalgesia) o anestesia tópica antes de la punción de la piel
Posicionamiento del paciente
El posicionamiento óptimo del paciente es esencial para una colocación epidural exitosa. Según el estado médico del paciente (p. ej., constitución corporal y capacidad para cooperar), el procedimiento planificado, la experiencia del anestesista, la baricidad de la solución intratecal (para la colocación de CSE) y varios otros factores, la posición sentada, decúbito lateral, navaja , o se puede utilizar la posición prona.
Cada posición tiene ventajas y desventajas. Independientemente de la posición que se seleccione para el inicio de los procedimientos neuroaxiales, es útil contar con un asistente que ayude a mantener la posición hasta que finalice el procedimiento. En general, mientras que el bloqueo del nervio epidural se puede iniciar con el paciente en cualquier posición que permita el acceso a la espalda, la colocación incorrecta puede convertir una colocación epidural que de otro modo sería fácil en un desafío innecesario. Varios dispositivos de posicionamiento están disponibles comercialmente para facilitar el posicionamiento del paciente sin la ayuda del personal de enfermería.
Posición para sentarse
En general, es técnicamente más fácil identificar la línea media en la posición sentada, particularmente en pacientes obesos y escolióticos. Los anestesistas también pueden tener más experiencia y sentirse más cómodos realizando procedimientos neuroaxiales en posición sentada. También se ha observado que la posición sentada proporciona la ruta más directa al espacio epidural, con una distancia más corta de la piel al espacio y, en el caso de CSE con AL sin dextrosa y opioides intratecales hipobáricos, una mayor extensión cefálica del bloqueo del nervio sensorial. . Sin embargo, las pacientes de edad avanzada, las parturientas en etapas avanzadas del trabajo de parto, las pacientes con fracturas de cadera, las pacientes muy sedadas y las pacientes que no cooperan pueden no ser capaces de asumir o mantener la posición sentada.Tabla 22).
TABLA 22. Ventajas de la posición sentada para
inicio del bloqueo neuroaxial.
| Más fácil de identificar la línea media, particularmente en obesos y pacientes escolióticos |
| Profesionales más experimentados en posición sentada |
| Menor tiempo de procedimiento |
| Distancia más corta de la piel al espacio epidural |
| Mayor difusión cefálica de las soluciones hipobáricas |
Si se elige la posición sentada, se debe ayudar al paciente a sentarse en la mesa de operaciones o en la cama con la parte posterior de las rodillas tocando el borde de la cama y los pies descansando sobre un taburete o colgando sobre la cama. El paciente debe relajar los hombros y curvar la espalda hacia el médico, asumiendo una posición "encorvada" o "gato loco". Es útil tener un asistente parado frente al paciente y ayudarlo a lograr la máxima flexión de la columna (Figura 17 y XNUMX). Flexionar el cuello debería ayudar a flexionar la parte inferior de la columna y abrir los espacios vertebrales (Figura 18 y XNUMX). Pedirle al paciente que abrace una almohada también puede ayudar con el posicionamiento.
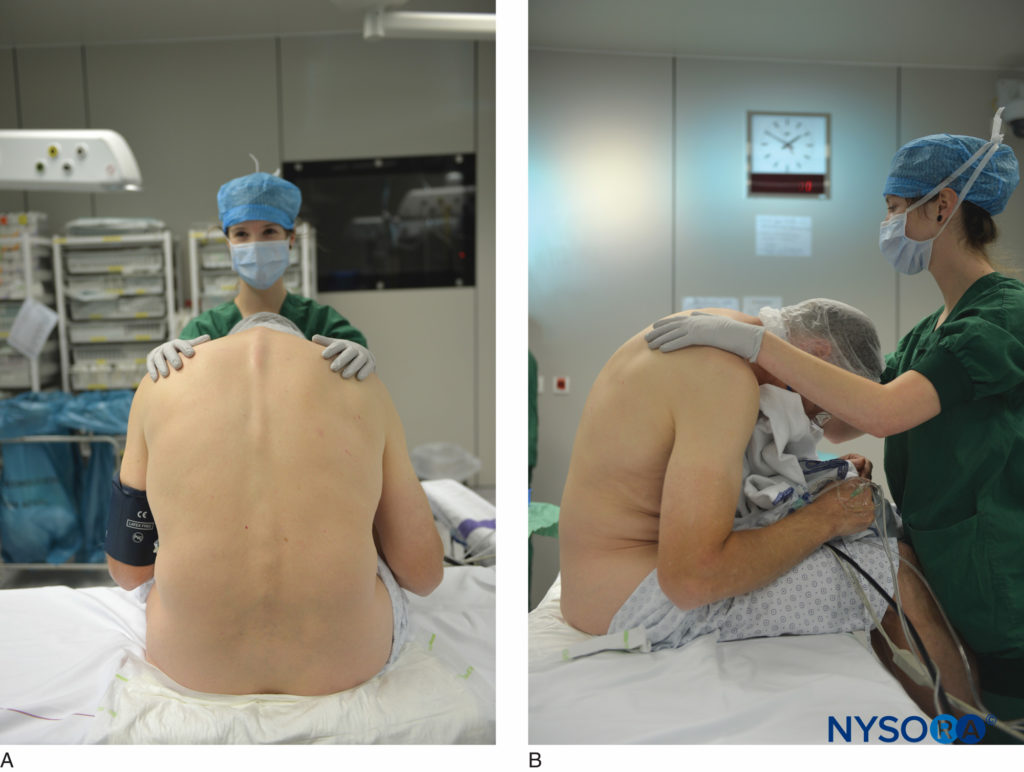
Figura 17 y XNUMX. A, B: Colocación epidural en posición sentada con un asistente que ayuda a colocar al paciente.
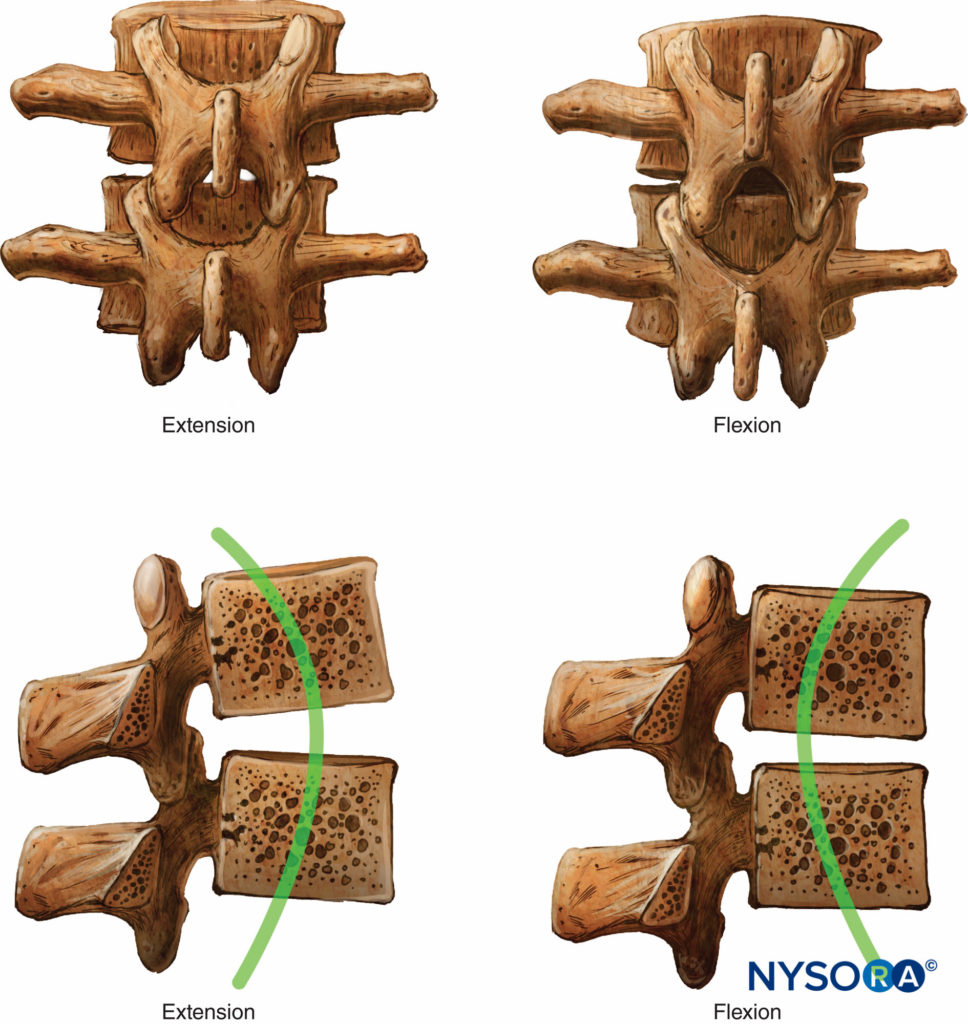
Figura 18 y XNUMX. Flexión versus extensión durante la colocación epidural.
Posición de decúbito lateral
La posición de decúbito lateral puede ser más apropiada para pacientes que no pueden sentarse cómodamente. Los beneficios adicionales incluyen lo siguiente: la sedación se puede usar de manera más liberal; los reflejos vagales se pueden minimizar; los cambios hemodinámicos pueden tolerarse mejor; puede haber menos necesidad de un asistente bien capacitado para ayudar a mantener la posición; y parece haber una incidencia reducida de canulación no intencional de la vena epidural y punción dural (Tabla 23). Finalmente, en el caso de CSE con AL hiperbáricas, los bloqueos nerviosos unilaterales para ciertos procedimientos ortopédicos pueden lograrse más fácilmente en la posición lateral.
TABLA 23.
| La sedación se puede usar más liberalmente. |
| Reducción del movimiento del paciente |
| Mayor comodidad para el paciente |
| Mejora de la cooperación del paciente |
| Mejora de la satisfacción del paciente. |
| Reducción del desplazamiento del catéter |
| Disminución de la incidencia de canulación de la vena epidural |
| Atenuación de los reflejos vagales |
| Cambios hemodinámicos mejor tolerados |
| Es posible que no se requiera asistencia de cabecera |
| Bloqueo unilateral intencional para procedimientos quirúrgicos factible |
En decúbito lateral, la espalda del paciente debe estar completamente alineada con el borde de la mesa o cama (Figura 19 y XNUMX).
Figura 19 y XNUMX. Colocación epidural en posición lateral.
La posición en decúbito lateral izquierdo puede ser preferible para los médicos diestros y puede proporcionar una estabilidad hemodinámica mejorada para las parturientas. El plano coronal del paciente debe ser perpendicular al suelo, con las puntas de las apófisis espinosas apuntando hacia la pared. Los muslos deben estar flexionados hacia el abdomen y las rodillas contra el pecho; el cuello debe estar en una posición neutra o flexionado para que la barbilla descanse sobre el pecho. Pedirle al paciente que "asuma la posición fetal" puede ayudar a flexionar la columna al máximo. Las caderas deben estar alineadas una encima de la otra, y el brazo no dependiente debe extenderse hacia la cadera no dependiente y descansar sobre ella. Es posible que sea necesario elevar la cabeza del paciente con una almohada para evitar la rotación de la columna. Los pacientes obesos o aquellos con caderas más grandes pueden necesitar almohadas adicionales para mantener la alineación adecuada. Dirigir la aguja hacia una línea imaginaria que se extiende cefálica y caudal desde el ombligo puede optimizar las posibilidades de inserción en la línea media, lo cual es particularmente importante durante el inicio de CSE (Tabla 24). El bisel de la aguja epidural se dirige hacia la cabeza del paciente.
TABLA 24. Consejos para lograr una posición lateral óptima.
| Alinee la espalda del paciente con el borde de la mesa o la cama |
| Alinee el plano coronal perpendicular al piso |
| Flexiona los muslos hacia el abdomen |
| El cuello debe estar neutral o flexionado. |
| Alinear las caderas una encima de la otra |
| Apoyar el brazo no dependiente sobre la cadera no dependiente |
| Eleve la cabeza con una almohada para evitar la rotación de la columna |
Control de infección
La adherencia a técnicas asépticas estrictas es esencial durante el inicio y mantenimiento del bloqueo neuroaxial. El grupo de trabajo de la ASA sobre complicaciones infecciosas asociadas con técnicas neuroaxiales recomienda las siguientes medidas: quitarse las joyas de los dedos y las muñecas; lavarse las manos cuidadosamente antes de ponerse los guantes; use gorros, máscaras (cambiadas con cada encuentro con un nuevo paciente) y guantes estériles; use clorhexidina con alcohol para la preparación de la piel; cubra al paciente en condiciones estériles; y cubra el sitio de inserción del catéter con un vendaje oclusivo estéril. Una sola aplicación de clorhexidina con alcohol parece tan eficaz como dos aplicaciones para la desinfección de la piel. Cuando no se dispone de clorhexidina, que no se suministra en los kits epidurales, es preferible el uso de povidona yodada con alcohol a la povidona yodada sola. Todas las soluciones antisépticas se consideran neurotóxicas si entran en contacto directo con las meninges; se debe tener cuidado de mantener las agujas y los medicamentos en la bandeja epidural separados de los desinfectantes para la piel. Los filtros bacterianos pueden ser útiles para pacientes con infusiones epidurales continuas crónicas o prolongadas, pero no hay datos que respalden que disminuyan la incidencia de infecciones relacionadas con el catéter. El catéter debe
permanecer en su lugar no más tiempo del necesario, y las desconexiones del catéter y los cambios de filtro deben reducirse al mínimo. Los datos son insuficientes para respaldar el uso de una bata quirúrgica durante el inicio de los procedimientos epidurales (Tabla 25).
TABLA 25. Técnica aséptica durante el inicio y mantenimiento del bloqueo epidural.
| Quítese las joyas de los dedos y las muñecas |
| Realice un cuidadoso lavado de manos antes de ponerse los guantes. |
| Utilizar gorro, mascarilla y guantes estériles |
| Use clorhexidina con alcohol para la preparación de la piel. |
| Cubra al paciente en condiciones estériles |
| Cubrir el sitio de inserción del catéter con vendaje oclusivo estéril |
| Mantenga el catéter en su lugar no más de lo necesario |
| Mantenga la desconexión del catéter y los cambios de filtro al mínimo |
Técnicas para identificar el espacio epidural
Se pueden utilizar tres técnicas para identificar el espacio epidural: LOR, gota colgante y ecografía. A pesar del creciente interés en los procedimientos neuroaxiales asistidos por ultrasonido, la técnica LOR, que se basa en las diferentes densidades de tejido a medida que la aguja pasa a través de los ligamentos hacia el espacio epidural, es la técnica más utilizada. Tanto la LOR como el líquido, con o sin burbujas de aire, y el aire se reconocen como medios aceptables para identificar el espacio epidural. Los ensayos aleatorios que compararon la solución salina con el aire para la LOR sugirieron que la solución salina es superior. Sin embargo, estos ensayos pueden exagerar la diferencia entre los dos medios al obligar al anestesista a utilizar una técnica menos preferida. Independientemente de la técnica que se utilice durante la colocación epidural de rutina, es importante tener en cuenta que no se recomienda la LOR al aire para los procedimientos de EBP.
Falta evidencia en la literatura sobre el mejor método para identificar el espacio epidural en niños, que comúnmente son anestesiados durante la colocación. Recientemente, se ha recomendado el uso de ultrasonido. Sin embargo, la técnica puede ser engorrosa y requiere experiencia con imágenes de ultrasonido. Con los refinamientos en la tecnología y la expansión de la experiencia de los médicos, la guía por ultrasonido puede facilitar la colocación de catéteres epidurales en esta población de pacientes.
Pérdida de resistencia al aire
La técnica LOR a aire se asocia con varias complicaciones (Tabla 26). El aire es comprimible y puede dar como resultado un LOR falso y, en consecuencia, una mayor incidencia de ADP. El ADP en el contexto de LOR al aire puede provocar neumoencéfalo, un dolor de cabeza intenso que se desarrolla inmediatamente después de la inyección de aire en el espacio subaracnoideo. El neumoencéfalo, a su vez, puede provocar una lesión neurológica grave, como hemiparesia y convulsiones generalizadas, así como náuseas y vómitos y retraso en la recuperación de la AG.
TABLA 26. Complicaciones asociadas con la pérdida de resistencia al aire.
| Neumoencéfalo |
| Mayor riesgo de punción dural accidental |
| Inicio más rápido de los signos y síntomas de la CPPD |
| Mayor incidencia de CPPD |
| Bloqueo incompleto/irregular |
| Compresión de la médula espinal o de la raíz nerviosa por aire |
| Embolia aérea venosa |
| Enfisema subcutáneo |
| Mayor incidencia de canulación de la vena epidural |
| Inserción difícil del catéter |
La incidencia de CPPD y la aparición de síntomas también pueden ser mayores cuando se utiliza la técnica LOR to air para identificar el espacio epidural. Además, la técnica LOR a aire se ha asociado con una mayor incidencia de segmentos desbloqueados o alivio del dolor en parches y déficits neurológicos relacionados con la compresión de las raíces nerviosas o la médula espinal por burbujas de aire. Se ha informado embolismo aéreo venoso (EAV) en presencia de desgarros en el plexo venoso epidural o si la presión de la fuente de aire es mayor que la presión venosa. Finalmente, tanto una mayor incidencia de canulación venosa epidural como una inserción difícil del catéter se han asociado con LOR al aire, particularmente en ausencia de predistensión del líquido del espacio epidural, aunque los datos son contradictorios.
Los defensores de LOR al aire sienten que es más fácil detectar ADP si se usa solo aire, ya que cualquier retorno de líquido es innegablemente LCR en ausencia de inyección de solución salina. En el caso de un ADP equívoco, el LCR se puede distinguir de la solución salina con el uso de una tira reactiva de orina para verificar la glucosa y la proteína; si es positivo, se puede hacer el diagnóstico de LCR. El CSF también se puede distinguir de la solución salina o LA por el diferencial de temperatura; Se espera que el LCR sea la temperatura corporal. Los defensores del enfoque LOR al aire también señalan el bloqueo nervioso sensorial inadecuado y el retraso en el inicio del bloqueo nervioso que puede ocurrir si se inyectan grandes volúmenes de solución salina en el espacio epidural, presumiblemente debido a un efecto de dilución. Sin embargo, esto se puede evitar limitando la cantidad de solución salina inyectada. Para los profesionales que realizan CSE de forma rutinaria, también se podría argumentar que la inyección de solución salina complica la identificación del LCR antes de la administración de medicamentos intratecales.
Para identificar el espacio epidural con la técnica de LOR a aire, avance la aguja lentamente, ejerciendo una presión continua o intermitente sobre la jeringa de LOR. A medida que la aguja entra en el ligamento amarillo, suele haber una clara sensación de mayor resistencia seguida de un sutil "ceder" cuando se ejerce una ligera presión sobre el émbolo. Evite inyectar aire al identificar el espacio epidural debido a la posibilidad de neumoencéfalo (en caso de ADP) y analgesia irregular e inadecuada.
Pérdida de resistencia a la solución salina con o sin burbuja de aire
La jeringa se llena con 2–3 ml de solución salina o solución salina con una burbuja de aire claramente visible. La burbuja proporciona un indicador de la presión adecuada que se debe aplicar en la jeringa LOR; se comprimirá y proporcionará algo de resistencia si la punta de la aguja epidural se engancha en el ligamento, pero se disipará sin esfuerzo con solo una ligera presión una vez que la aguja entre en el espacio epidural. La solución salina se puede inyectar directamente para la predistensión de líquidos. La pequeña burbuja de aire no debería dar lugar a complicaciones asociadas con la LOR al aire si también se inyecta. Omita la burbuja de aire cuando realice una PBE debido a la remota posibilidad de que el aire pueda introducirse en el espacio subaracnoideo a través de la brecha meníngea.
Con LOR a solución salina con o sin aire, la aguja se avanza de la misma manera que con aire. Se puede ejercer presión continua o intermitente sobre el émbolo de la aguja.
La técnica de la gota colgante
La técnica de la gota colgante se basa en la presión subatmosférica del espacio epidural, que es más pronunciada y fiable en las regiones cervical y torácica que en los segmentos lumbares. La carpa dural del avance de la aguja epidural también contribuye a la presión que parece “succionar” la gota de líquido. Para identificar el espacio epidural con este abordaje, se requiere una aguja epidural con alas. Se coloca una gota de solución salina en el centro de la aguja una vez que la aguja se engancha en el ligamento. La aguja se avanza continuamente con los dedos pulgar e índice sujetando firmemente las alas y los dedos tercero a quinto de ambas manos colocados contra la espalda del paciente. La entrada en el espacio epidural se señala mediante la entrada de la gota en el centro de la aguja.
La técnica de la gota colgante es más efectiva en la región torácica, donde la presión subatmosférica es más notable. Sin embargo, esta técnica conlleva un mayor riesgo de desgarro meníngeo, en parte debido a la proximidad de la aguja epidural a la duramadre. Además, los pacientes con enfermedad pulmonar obstructiva grave pueden tener una presión subatmosférica atenuada, incluso en la región torácica; la técnica de la gota colgante puede no ser apropiada en este entorno.
Ecografia
La tecnología de ultrasonido se utiliza cada vez más para ayudar en la identificación del espacio epidural. Los estudios sugieren que el uso de ultrasonografía para identificar la profundidad anticipada del espacio, particularmente en parturientas obesas, y para identificar la línea media antes de la colocación reduce el número de intentos, minimiza el riesgo de complicaciones y facilita el procedimiento sin prolongarlo significativamente. La guía por ultrasonido también sirve para ayudar a identificar el espacio intermedio correcto, lo que puede ser difícil basándose únicamente en los puntos de referencia anatómicos. Consulte el Capítulo 40 para obtener información más detallada sobre las técnicas neuroaxiales guiadas por ecografía.
Técnica de Bloqueo Epidural
Hay cuatro accesos comunes al espacio epidural: línea media, paramediano, Taylor (paramediano modificado) y caudal. La experiencia clínica en cada una de estas técnicas le da al anestesiólogo más flexibilidad al realizar el bloqueo epidural. Para todos los enfoques, se deben colocar monitores y se debe preparar la piel y cubrirla de manera estéril antes de iniciar el procedimiento. El equipo de emergencia y la medicación deben estar disponibles de inmediato. Se puede usar sedación, según corresponda. En general, el bisel de la aguja epidural debe mirar en dirección cefálica, independientemente del abordaje utilizado para acceder al espacio epidural, a menos que se desee un bloqueo nervioso unilateral intencional (p. ej., para procedimientos ortopédicos de las extremidades inferiores realizados bajo CSE).
Enfoque de línea media
Este enfoque se usa más comúnmente para la colocación epidural en posición sentada y para procedimientos epidurales en la región lumbar, torácica baja y de la columna cervical.
1. Se puede colocar una bandeja epidural a la derecha del anestesiólogo para los médicos diestros ya la izquierda para los médicos zurdos.
2. Identifique el espacio intermedio deseado mediante puntos de referencia anatómicos superficiales y palpación o ecografía. La aguja que se usa para anestesiar la piel también se puede usar como una "aguja detectora" para ayudar a identificar puntos de referencia óseos, particularmente en pacientes obesos.
3. Infiltre la piel y el tejido subcutáneo con LA (por lo general, lidocaína al 1 %) a lo largo del recorrido previsto de la aguja epidural entre las apófisis espinosas adyacentes. Una roncha de piel grande con un volumen menor de LA en el tejido subcutáneo servirá para anestesiar la piel adecuadamente sin
oscureciendo los puntos de referencia.
4. Inserte la aguja epidural con estilete a lo largo de la misma vía con el bisel orientado en dirección cefálica. Durante la inserción de la aguja, el dorso de la mano del anestesiólogo que no aplica la inyección puede descansar sobre la espalda del paciente con el pulgar y el índice sosteniendo el centro de la aguja epidural. Un enfoque modificado consiste en avanzar con la mano dominante envuelta firmemente alrededor del centro de la aguja epidural mientras el dedo índice y el pulgar de la mano no dominante agarran y guían el cuerpo de la aguja. Colocar las puntas de los dedos medios en la espalda del paciente y sujetar las alas de la aguja con los dedos pulgar e índice es un método alternativo para enganchar la aguja.
Para acoplar correctamente la aguja epidural, avance a través de la piel, el tejido subcutáneo, el tejido adiposo, el ligamento supraespinoso, el ligamento interespinoso y, posiblemente, hasta el ligamento amarillo; en ese punto, la aguja debe asentarse firmemente en la línea media (Figura 20 y XNUMX). Si el eje de la aguja se tambalea o se desvía hacia un lado, no está correctamente anclado en el ligamento. La aguja epidural puede engancharse en el ligamento interespinoso o en el ligamento amarillo.
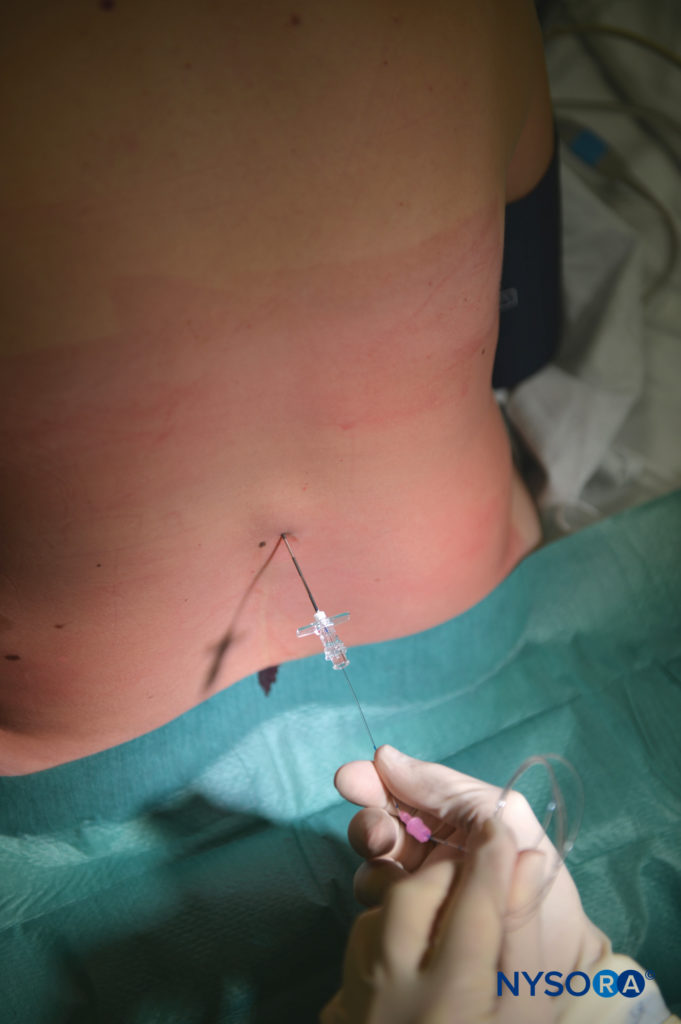
Figura 20 y XNUMX. Aguja epidural encajada en el ligamento de la línea media.
Consejos NYSORA
• La aguja epidural avanza a través de la piel, el tejido subcutáneo, el ligamento supraespinoso, el ligamento interespinoso y el ligamento amarillo antes de llegar al espacio epidural.
• La aguja puede engancharse en el ligamento interespinoso o en el ligamento amarillo durante el inicio del bloqueo epidural.
• La desviación lateral o una aguja “tambaleante” indica que la aguja no está bien enganchada en el ligamento, lo que requiere retirarla y redirigirla hacia la línea media.
Determinar qué ligamentos se atraviesan es una habilidad adquirida. El ligamento interespinoso puede sentirse "arenoso" contra la aguja que avanza, mientras que el ligamento amarillo ofrece más resistencia. Sin embargo, las brechas en la línea media del ligamento amarillo no son infrecuentes y las pacientes obstétricas pueden tener ligamentos más blandos. La profundidad desde la piel hasta el ligamento amarillo generalmente varía de 4 a 6 cm en adultos de tamaño normal, aunque existe una gran variabilidad. Después de penetrar los ligamentos, ya no es recomendable cambiar la dirección de la punta de la aguja sin retirar la aguja varios centímetros o al nivel de la piel. El estilete debe colocarse en la aguja epidural mientras se redirige para evitar la acumulación de restos óseos o tapones de tejido blando que puedan dificultar el flujo de LCR en caso de una ADP.
5. Retire el estilete de la aguja epidural y conecte la jeringa LOR con aire o solución salina (con o sin burbujas de aire) firmemente al centro de la aguja. Las jeringas LOR de vidrio o de plástico de baja resistencia son apropiadas. Se debe tener cuidado para asegurarse de que las jeringas de vidrio no estén "pegajosas".
Son apropiadas varias posiciones de la mano para hacer avanzar la aguja epidural hacia el espacio epidural: el dorso de la mano no dominante puede descansar firmemente sobre la espalda del paciente, con el pulgar y el índice sujetando el eje de la aguja, mientras se ejerce presión sobre el émbolo LOR de forma continua o continua. intermitentemente con el pulgar de la mano dominante. La mano no dominante puede descansar sobre la espalda del paciente con el pulgar y el índice extendiéndose hacia el centro de la aguja y estabilizándolo, mientras que el pulgar de la mano dominante aplica presión (Figura 21 y XNUMX). O bien, los dedos medio a cuarto o quinto de la mano no dominante pueden descansar sobre el dorso, con ambos dedos pulgar e índice sujetando las alas de la aguja epidural y la mano dominante liberando intermitentemente su posición y ejerciendo presión sobre el émbolo de la jeringa LOR (Figura 22 y XNUMX).
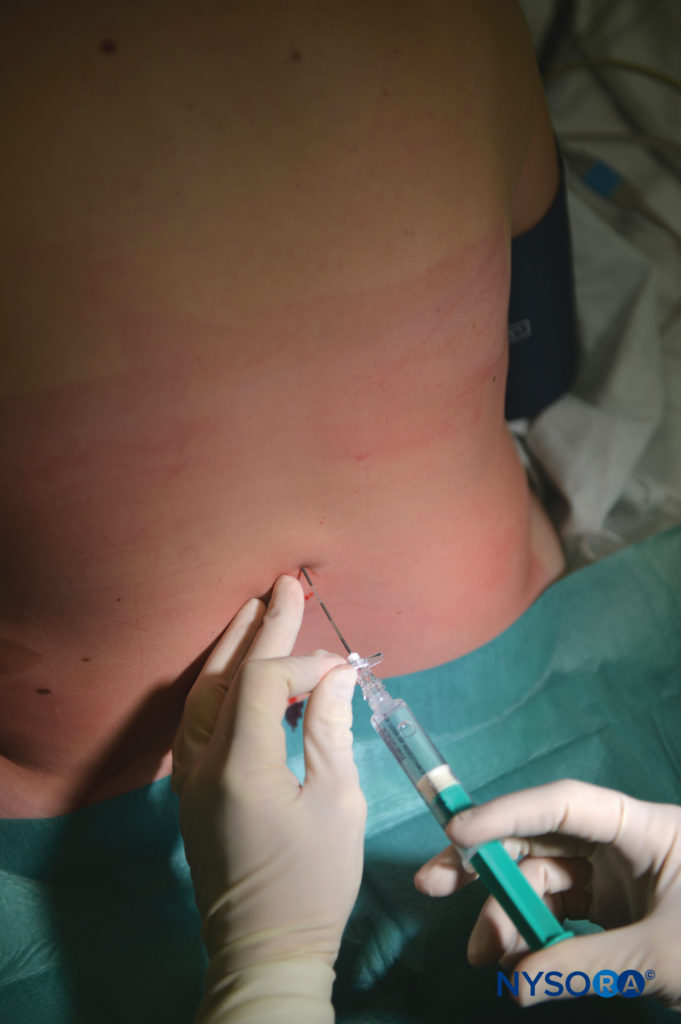
Figura 21 y XNUMX. Avance de la aguja epidural: mano no dominante en la espalda del paciente con el pulgar y el índice en el centro de la aguja.
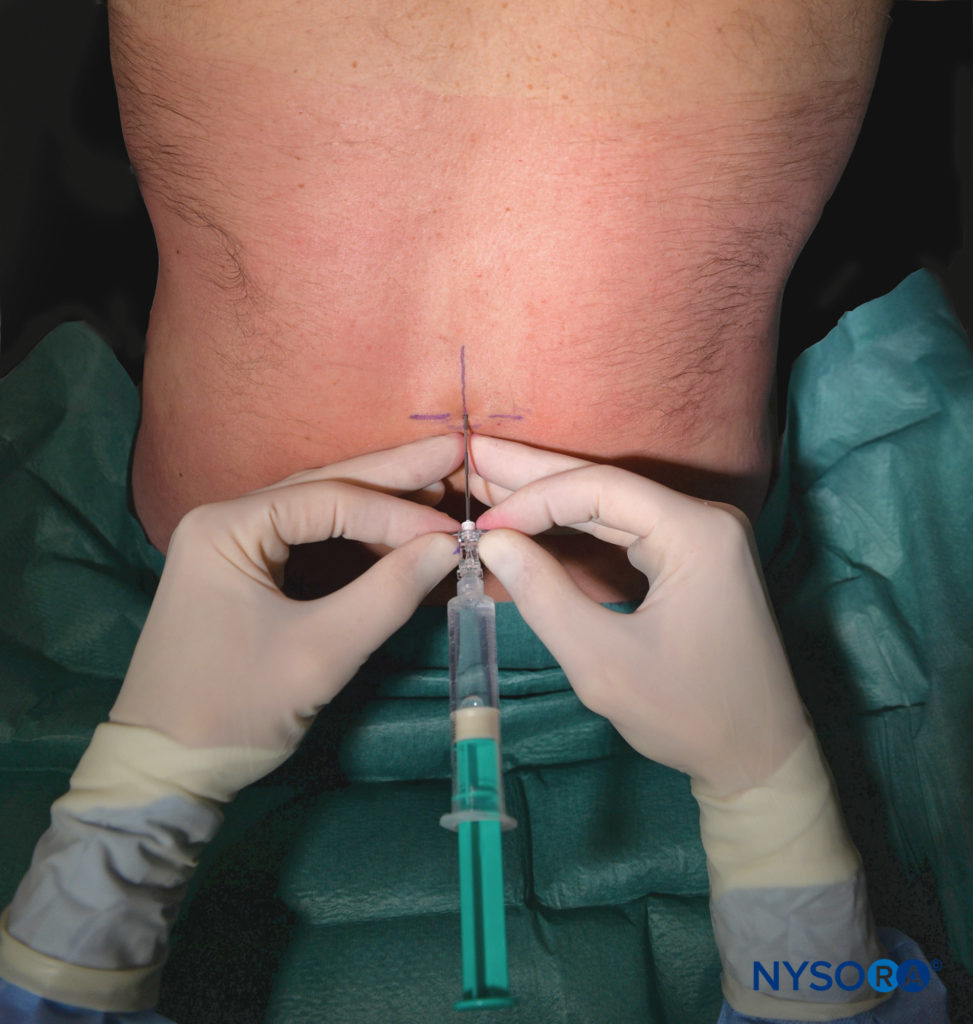
Figura 22 y XNUMX. Avance de la aguja epidural: pulgares e índices sujetando las alas.
A medida que la aguja entra en el espacio epidural, el émbolo de la jeringa LOR de repente "cede". Evite inyectar todo el contenido de la jeringa, particularmente con LOR al aire, si es posible. Para las epidurales continuas, se puede inyectar un pequeño volumen de solución salina en el espacio epidural para dilatar el espacio, lo que reduce el riesgo de canulación de la vena epidural y facilita la inserción del catéter. Tenga en cuenta la profundidad de la aguja en la piel. La marca de la aguja en la piel representa la profundidad desde la piel hasta el espacio epidural. Debido a que las marcas de centímetros no están numeradas, puede ser útil contar el número de marcas de centímetros entre la piel y el centro de la aguja epidural y restar ese número de la longitud de la aguja. Por ejemplo, si quedan 4 marcas visibles entre la piel y el centro de la aguja, reste 4 de 9 (la longitud común de una aguja epidural) para determinar que la profundidad del espacio epidural es de 5 cm.
Inserte el catéter con la ayuda del dispositivo de inserción que encaja en el cubo de la aguja epidural hasta que se visualice la marca de 15 cm entrando en el cubo de la aguja; luego, retire la aguja sin desalojar el catéter (Figura 23 y XNUMX). El catéter no debe introducirse más de 5 a 6 cm en el espacio epidural; 2–3 cm es apropiado para procedimientos quirúrgicos cortos. Para determinar dónde debe fijarse el catéter en la piel, agregue 2 a 6 cm, dependiendo de la distancia a la que se vaya a enhebrar el catéter, a la profundidad calculada previamente hasta el espacio epidural. Por ejemplo, si la aguja entró en el espacio epidural a los 7 cm, el catéter debe fijarse en la marca de 12 cm en la piel para asegurarse de que 5 cm del catéter descansen en el espacio epidural.
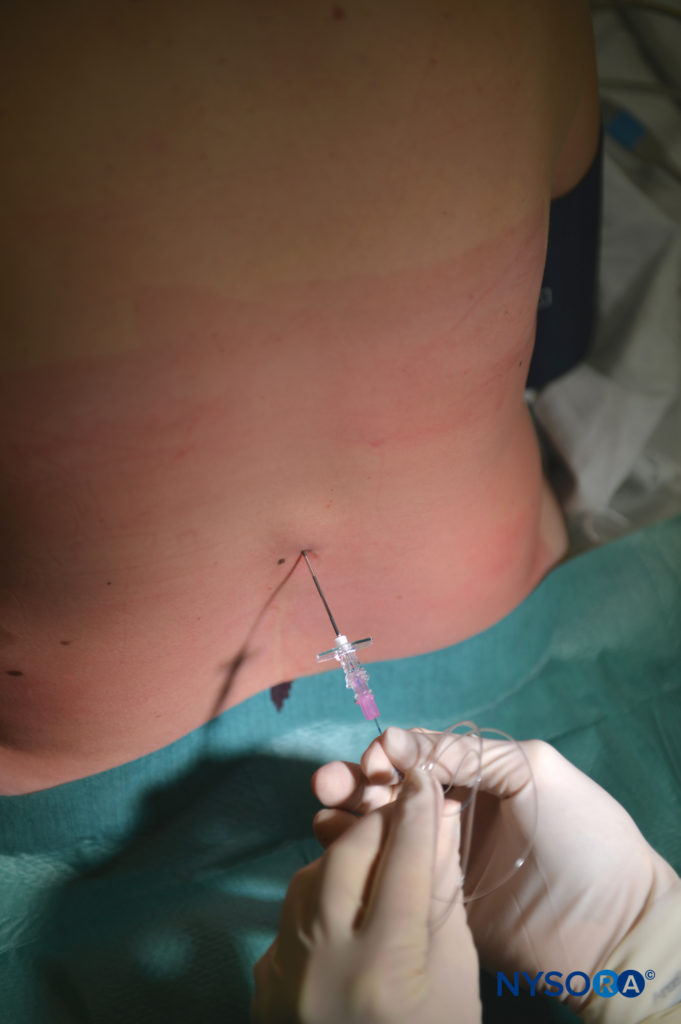
Figura 23 y XNUMX. Inserción del catéter epidural.
Consejos NYSORA
• Una manera fácil de medir la profundidad del espacio epidural cuando se usa la técnica LOR es contar el número de marcas de centímetros que son visibles entre la piel y el centro de la aguja. Resta ese número de la longitud de la aguja. Por ejemplo, la mayoría de las agujas epidurales tienen una longitud de 9 cm. Si las marcas de 4 centímetros son visibles después de la identificación del espacio epidural, reste 4 de 9 para concluir que la profundidad del espacio es de 5 cm. El catéter epidural debe insertarse no más de 5 o 6 cm más allá de esa distancia (es decir, pegado con cinta a 10–11 cm en la piel).
Para la técnica epidural de inyección única menos común, el LA se puede administrar directamente a través de la aguja en dosis divididas durante varios minutos. Esta técnica, sin embargo, requiere que el paciente permanezca inmóvil durante la dosificación y puede resultar en una presión dolorosa con grandes volúmenes Para la técnica de catéter continuo, no se recomienda administrar LA a través de la aguja, ya que no se puede verificar la colocación correcta del catéter.
Se debe aplicar un vendaje oclusivo transparente sobre el sitio de inserción para permitir la inspección del catéter. El catéter debe asegurarse a la espalda del paciente con el conector en el hombro del paciente. El uso de cinta transparente tiene la ventaja de permitir que el médico visualice las ventanas de "retroceso" proximal y distal del catéter antes de administrar bolos de LA.
Abordaje paramediano
El abordaje paramediano ofrece una abertura mayor en el espacio epidural que el abordaje de la línea media y es particularmente útil para pacientes que no pueden colocarse fácilmente o que no pueden flexionar la columna durante la colocación de la epidural; para pacientes con ligamentos calcificados o deformidades de la columna (p. ej., cifoescoliosis, cirugía lumbar previa); y para técnicas epidurales en el área torácica baja a media. Las apófisis espinosas de T4 a T9 tienen un ángulo agudo y puntas que apuntan caudalmente, lo que dificulta la inserción de la aguja epidural en la línea media.
La “sensación” del abordaje paramediano es diferente a la del abordaje de la línea media porque se penetran diferentes tejidos. Los ligamentos supraespinoso e interespinoso son estructuras de la línea media que no se atraviesan en el abordaje paramediano.
En cambio, la aguja epidural penetra el tejido paraespinoso con poca resistencia antes de entrar en el ligamento amarillo. Se han descrito varios enfoques de la técnica paramediana. Esencialmente, la entrada de la aguja se dirige caudal y lateralmente a la cara inferior de la apófisis espinosa superior del espacio intermedio deseado y sale de la lámina en dirección cefálica.Figura 24 y XNUMX).
1. Identifique el espacio intermedio deseado con puntos de referencia en la superficie, palpación o guía por ultrasonido. Levante una roncha de piel aproximadamente 1 cm lateral y 1 cm caudal a la cara inferior de la apófisis espinosa superior del nivel espinal deseado.
2. La aguja epidural se inserta a 15° del plano sagital, en ángulo hacia la línea media con una inclinación cefálica.
3. Si se encuentra hueso (muy probablemente lámina, si la profundidad y el ángulo de abordaje son apropiados), la aguja se redirige en dirección cefálica y medial (consulte la Parte VI, Anestesia pediátrica). Si se encuentra la cara lateral de la apófisis espinosa, la aguja debe redirigirse lateralmente y cefálicamente.
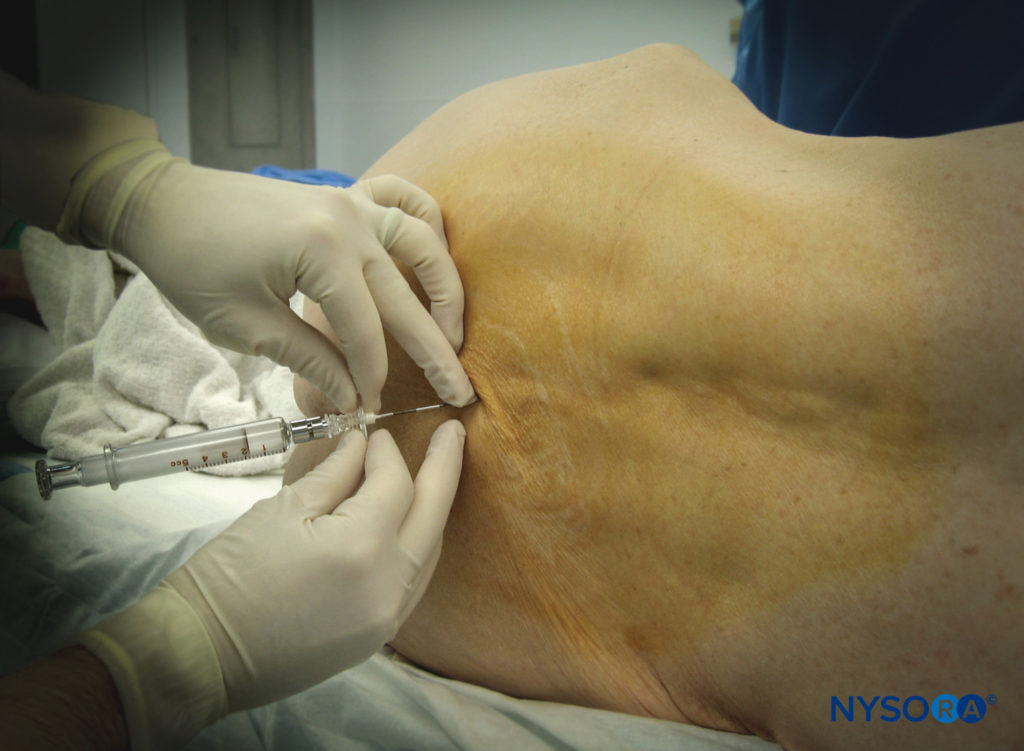
Figura 24 y XNUMX. Técnica epidural paramediana.
Enfoque de Taylor
El abordaje de Taylor es un abordaje paramediano modificado que utiliza el gran espacio intermedio L5-S1. Es un abordaje excelente para la cirugía de cadera o para cualquier cirugía de las extremidades inferiores en pacientes traumatizados que no pueden tolerar la posición sentada. Este enfoque puede proporcionar el único acceso disponible al espacio epidural en pacientes con ligamentos osificados.
1. Con el paciente sentado o en posición lateral, se coloca una roncha cutánea 1 cm medial y 1 cm caudal a la espina ilíaca posterosuperior.
2. La aguja epidural se inserta en este sitio en dirección medial y cefálica en un ángulo de 45° a 55°.
3. Al igual que en el abordaje paramediano clásico, la primera resistencia que se siente antes de entrar al espacio epidural es al entrar en el ligamento amarillo.
4. Si la aguja entra en contacto con el hueso (generalmente el sacro), la aguja debe alejarse del hueso hacia el ligamento y luego hacia el espacio epidural en direcciones progresivamente más mediales y cefálicas.
Abordaje Caudal
El abordaje caudal se usa comúnmente en pediatría para la colocación de un catéter epidural de inyección única o continua para la analgesia intraoperatoria y posoperatoria. En adultos, por lo general se reserva para procedimientos que requieren el bloqueo de los nervios sacros y lumbares (p. ej., cirugías anales y vaginales, herniorrafia inguinal, cistoscopia); epidurografía; y lisis de adherencias en pacientes con dolor lumbar con radiculopatía después de cirugía de columna.
El sacro es un hueso de forma triangular formado por la fusión de las vértebras sacras. La falta de fusión del quinto arco vertebral sacro crea la estructura conocida como hiato sacro, que está cubierto por el ligamento sacrococcígeo (una extensión del ligamento amarillo) y bordeado por prominencias óseas conocidas como cuernos sacros. El hiato sacro es el punto de acceso al espacio epidural sacro. Por lo general, se identifica como un surco sobre el cóccix (Figura 25 y XNUMX).
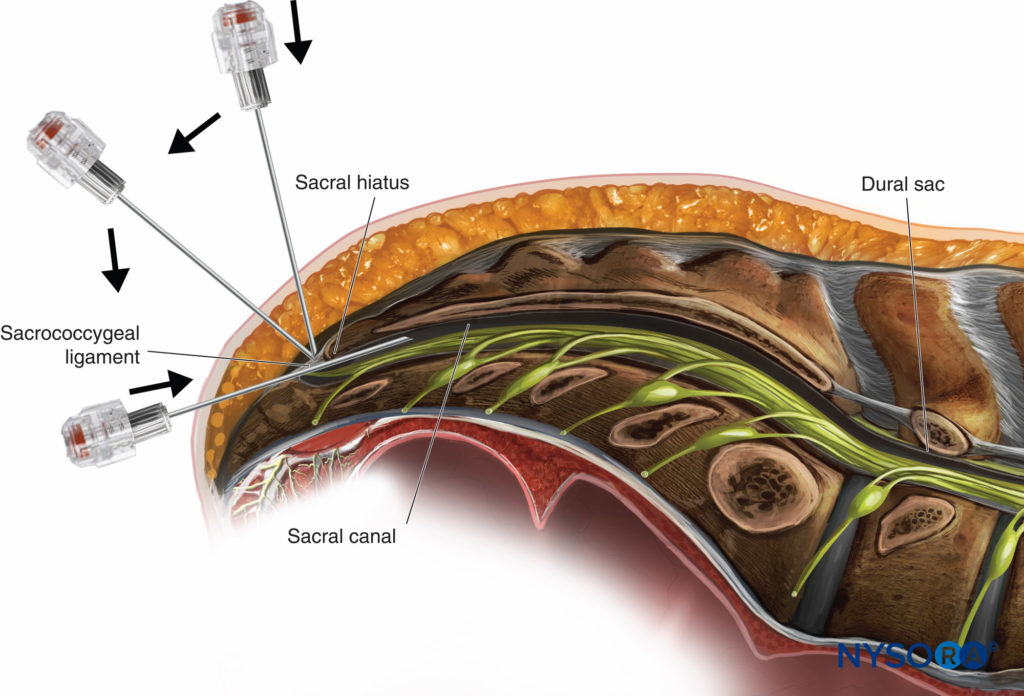
Figura 25 y XNUMX. Abordaje caudal para colocación de catéter epidural.
Si no se utiliza la fluoroscopia, existen dos métodos para identificar el hiato: (1) El hiato sacro se encuentra en el vértice de un triángulo equilátero que conecta las espinas ilíacas posterosuperiores y apunta caudalmente. (2) Las protuberancias óseas (los cuernos sacros) que rodean el hiato sacro pueden palparse aplicando una presión firme con el dedo índice a medida que se mueve cefálicamente desde el cóccix.
1. Coloque al paciente en posición lateral o prono (con una almohada debajo de la pelvis y las caderas en rotación interna, si es prono). En la posición lateral, la pierna dependiente se flexiona ligeramente, mientras que la pierna no dependiente se flexiona en mayor grado (hasta que la rodilla contacta con la cama).
2. Haga avanzar la aguja con una inclinación de 45° (en relación con la superficie de la piel).
3. Se siente un claro "chasquido" o "chasquido" cuando la aguja perfora la membrana sacrococcígea.
4. Si se encuentra el aspecto dorsal de la placa ventral del sacro, retire la aguja ligeramente, disminuya la ángulo de inserción y avance de nuevo. El ángulo de la aguja se reduce hasta que queda casi plano contra la piel (es decir, paralelo al plano coronal) para pacientes masculinos. Las pacientes femeninas pueden requerir una inclinación de 15°.
5. Después de encontrar LOR, avance la aguja ligeramente hacia el canal caudal. Avanzar demasiado puede provocar ADP o una inyección intravascular no intencionada o la canulación de la vena epidural durante la colocación del catéter. Si la LOR es equívoca, se pueden inyectar varios mililitros de solución salina a través de la aguja caudal mientras se palpa la piel que recubre el sacro. Es probable que la aguja esté colocada correctamente si no se desarrolla un bulto en la piel.
6. Aspire sangre o LCR antes de inyectar LA.
7. Se puede insertar un catéter epidural a través de la aguja y avanzar hasta el nivel deseado.
Bloqueo epidural cervical
Las técnicas epidurales cervicales continuas o de una sola inyección se utilizan para una variedad de procedimientos quirúrgicos y de dolor, que incluyen la endarterectomía carotídea, la tiroidectomía y las condiciones de dolor de cuello crónico. Tanto el abordaje de la línea media como el paramediano se utilizan para realizar procedimientos cervicales, aunque la guía fluoroscópica se está volviendo cada vez más común. El bloqueo epidural cervical puede iniciarse en decúbito prono, lateral o sentado. La posición prona se usa más comúnmente para procedimientos asistidos por fluoroscopia, aunque se puede usar la posición sentada. Cualquiera que sea la posición que se utilice, la flexión del cuello sirve para aumentar la distancia desde el ligamento amarillo hasta la duramadre, aumentando el margen de seguridad para estos procedimientos y para expandir el espacio interlaminar.
Como en el caso de los procedimientos epidurales lumbares y torácicos, tanto la técnica de LOR como la de gota colgante son métodos adecuados para identificar el espacio epidural. Para la LOR se puede utilizar aire (preferiblemente un volumen pequeño) o solución salina (con o sin burbujas de aire). Sin embargo, el ligamento amarillo es discontinuo en la línea media de la región cervical en un gran porcentaje de pacientes, lo que contribuye a un LOR falso. Además, es importante tener en cuenta que el ligamento amarillo es más delgado a este nivel (1.5-3 mm) que a nivel lumbar y torácico.
En la región cervical, el espacio intermedio C7-T1 es más ancho y de más fácil acceso. Además, la profundidad desde la piel hasta el espacio epidural es mayor en este espacio intermedio, y la distancia desde el espacio epidural hasta el saco dural es mayor que en otros niveles cervicales. Sin embargo, el uso de puntos de referencia de palpación y superficie para identificar el nivel de C7-T1 no siempre es confiable; la vértebra prominente (que se supone que es C7) se confunde con frecuencia con C6 y T1 en ciertas poblaciones de pacientes. Las inyecciones de una sola inyección a este nivel deben administrarse lentamente. Para las técnicas de catéter continuo, el catéter generalmente se enrosca no más de 2 a 3 cm.
Inicio y Manejo del Bloqueo Epidural
Dosis de prueba
Antes de administrar medicamentos a través del catéter epidural, se debe descartar la colocación subaracnoidea, intravascular y subdural. Aunque es raro, la migración del catéter puede ocurrir después de la confirmación inicial de que el catéter está en el espacio epidural; cada bolo debe estar precedido por la confirmación de la ubicación adecuada del catéter.
Aunque se ha cuestionado la eficacia de LA con epinefrina en la detección de catéteres mal colocados, muchos médicos siguen confiando rutinariamente en la dosis de prueba farmacológica. La dosis clásica combina 3 mL de lidocaína al 1.5% con 15 μg de epinefrina.
La inyección intratecal de 45 mg de lidocaína debería producir un bloqueo nervioso motor significativo si el catéter está en el espacio subaracnoideo, aunque la evidencia reciente sugiere que esto no siempre es confiable. Un cambio en la frecuencia cardíaca del 20 % o más (o, alternativamente, un aumento en la frecuencia cardíaca de 10 a 25 latidos por minuto) dentro de 1 minuto sugiere que el catéter se ha colocado (o ha migrado hacia) un vaso y debe ser sustituido. Si la frecuencia cardíaca no aumenta en un 20 % o más, o si no se desarrolla un bloqueo nervioso motor significativo en 5 minutos, la dosis de prueba se considera negativa. Se han observado excepciones a esta regla en pacientes en trabajo de parto, pacientes anestesiados y pacientes que reciben agentes bloqueantes β-adrenérgicos.
Confiar en los cambios del ECG después de la dosis de prueba y el uso de estimuladores nerviosos se han recomendado como métodos alternativos para confirmar la colocación epidural, aunque estos métodos también tienen deficiencias.
La seguridad y eficacia de la dosis de prueba tradicional se debate en la literatura. En pacientes en trabajo de parto, un cambio en la frecuencia cardíaca atribuido a la epinefrina puede deberse de hecho a una contracción dolorosa, lo que contribuye a una interpretación falsa positiva. Alternativamente, un resultado de prueba positivo verdadero en esta población de pacientes puede resultar en una disminución del flujo sanguíneo uterino inducida por epinefrina. Los pacientes con HTA, incluidas las mujeres con preeclampsia, pueden experimentar un aumento grave de la presión arterial que puede no tolerarse bien después de una dosis intravenosa de 15 μg de epinefrina. Los anestésicos generales volátiles pueden interferir con la respuesta a la epinefrina y contribuir a un alto porcentaje de resultados falsos negativos en los niños, que suelen ser anestesiados durante la colocación epidural. En pacientes que toman agentes bloqueantes β-adrenérgicos, los cambios en la frecuencia cardíaca pueden no ser confiables. Un aumento de la presión arterial sistólica superior a 20 mm Hg se ha utilizado como indicador de inyección intravascular en esta población de pacientes.
Se necesitan estudios adicionales para determinar la estrategia óptima para detectar la colocación de catéteres intratecales e intravasculares. Afortunadamente, con el uso generalizado de infusiones de LA de baja concentración para la analgesia epidural, el riesgo de toxicidad sistémica de LA se reduce considerablemente; la utilidad de una dosis de prueba tradicional para evaluar la canulación intravascular en este entorno es limitada. Además, las innovaciones en el diseño de catéteres epidurales en las últimas décadas, particularmente la introducción de catéteres flexibles, han contribuido a una marcada disminución en la incidencia tanto de migración del catéter intratecal como de canulación o migración venosa epidural. No obstante, se requiere una dosificación incremental de LA (es decir, alícuotas de 3 a 5 ml), con aspiración simultánea de sangre y LCR y observación cuidadosa cuando se administra una epidural. En el futuro, los nuevos métodos para detectar catéteres mal colocados, como la guía de señales acústicas, la estimulación nerviosa y la inserción guiada por ultrasonido, pueden reemplazar la dosis de prueba clásica.
Régimen de dosificación
Después de aspirar el catéter epidural para comprobar si hay sangre o LCR o después de una dosis de prueba negativa, se puede dosificar el catéter para proporcionar analgesia o anestesia. Como se mencionó, la concentración de LA determina la densidad del bloqueo nervioso, mientras que el volumen y la dosis total de LA determinan la propagación. Como pauta general, la dosis de carga inicial se puede determinar de la siguiente manera: 1 a 2 ml de AL por segmento para bloquear en una epidural lumbar, 0.7 ml por segmento para una epidural torácica y 3 ml por segmento para una epidural caudal. La dosis de carga debe administrarse a través del catéter en alícuotas de 3 a 5 ml a intervalos de 3 a 5 minutos, lo que permite evaluar la respuesta del paciente a la dosis y evitar la toxicidad sistémica. Las dosis de carga apropiadas para la analgesia posoperatoria incluyen 10 ml de bupivacaína, levobupivacaína o ropivacaína al 0.2%–0.25% con o sin adyuvantes; sin embargo, los pacientes pueden experimentar diversos grados de bloqueo de los nervios motores. La evidencia reciente sugiere que los volúmenes más altos de LA de baja concentración pueden proporcionar una mejor distribución y una mejor analgesia. Se pueden administrar hasta 20 ml de bupivacaína al 0.0625 %–0.125 % o la dosis equipotente de ropivacaína de forma incremental como dosis de carga. Se requieren AL de mayor concentración para la anestesia quirúrgica. Se pueden utilizar hasta 20 ml de lidocaína al 2 %, con o sin epinefrina 1:200,000 15 y bicarbonato de sodio, o 0.5 ml de bupivacaína o ropivacaína al XNUMX % para iniciar la anestesia epidural en la región lumbar.
El mantenimiento del nivel deseado de anestesia se puede lograr a través de una dosificación intermitente o continua después de la dosis de carga inicial. Con bolos manuales, se puede administrar de un cuarto a un tercio de la cantidad inicial a intervalos de tiempo, dependiendo de la duración de la acción del LA inicial (es decir, acción corta, intermedia o prolongada), aunque son apropiados varios regímenes de mantenimiento. Los bolos manuales generalmente se administran durante una cirugía prolongada; sin embargo, se puede iniciar una infusión continua después del bolo inicial para mantener la anestesia quirúrgica. Las infusiones continuas requieren la misma atención diligente al paciente que cualquier otro anestésico. La velocidad de infusión habitual es de 4 a 15 ml/h. El amplio rango generalmente depende de la edad, el peso, el grado de bloqueo sensorial o motor deseado en un paciente en particular; sitio de inserción del catéter; y el tipo y dosis de LA. Por lo tanto, la individualización es necesaria y no se puede aplicar una regla fija para este propósito.
La analgesia epidural controlada por el paciente (PCEA, por sus siglas en inglés), más comúnmente con infusiones de LA de baja concentración y complementos opioides, se usa cada vez más para la analgesia posoperatoria y para pacientes en trabajo de parto. Se puede programar un bolo a demanda a intervalos de tiempo, con o sin una dosis de carga y una infusión de fondo, para optimizar la comodidad del paciente con un menor consumo de LA. Se han desarrollado bombas que administran bolos obligatorios automatizados a intervalos de tiempo, con o sin infusión basal, aunque todavía no están ampliamente disponibles.
Para el bloqueo epidural torácico, se pueden usar varios regímenes de dosificación para minimizar los cambios hemodinámicos y el deterioro respiratorio (en pacientes despiertos). Una dosis inicial de 3 a 6 ml de bupivacaína diluida al 0.125 %–0.25 % o 0.1 %–0.2 % de ropivacaína con o sin fentanilo, hidromorfona o morfina sin conservantes puede seguirse de 3 ml de bupivacaína al 0.25 %–0.5 % cada 30 mín. Un régimen alternativo es el siguiente: Administrar una dosis de carga con 3-6 mL de bupivacaína al 0.125% o ropivacaína al 0.1%-0.2% con un opioide (fentanilo 2 μg/mL o hidromorfona 20 μg/mL) al menos 30 minutos antes del final del caso, según lo tolerado. Iniciar una infusión de bupivacaína al 0.0625% o ropivacaína al 0.1% con fentanilo o hidromorfona a 3-5 ml/h antes de que el paciente abandone el quirófano.
El nivel y la duración de la anestesia epidural dependen principalmente del lugar de la inyección y del volumen y la concentración del fármaco. Otros factores como la edad, el embarazo y el sexo son factores menos importantes pero deben tenerse en cuenta. La adición de epinefrina fresca y bicarbonato de sodio al 8.4 % a la lidocaína, la mepivacaína y la cloroprocaína disminuirá la latencia, mejorará la calidad y prolongará la duración del bloqueo nervioso. La epinefrina es menos eficaz con los LA de acción prolongada. Agregar bicarbonato a ropivacaína y bupivacaína puede causar precipitación. Se ha demostrado que la adición de opioides (p. ej., fentanilo) mejora la calidad del bloqueo nervioso sin ningún efecto sobre la duración.
Dosificación de recarga
Las dosis repetidas, comúnmente denominadas "recargas", deben administrarse antes de que el nivel del bloqueo nervioso haya retrocedido más de dos dermatomas. Se puede administrar de un cuarto a un tercio o más de la dosis de carga original de LA para cada dosis repetida, aunque se pueden requerir diferentes dosis adicionales para diferentes escenarios clínicos. Por ejemplo, si el paciente se siente cómodo pero el nivel sensorial no es el adecuado, puede ser apropiado un complemento de AL de alto volumen y baja concentración. Este también puede ser el caso si el bloqueo es unilateral o irregular, pero el paciente desea mantener la fuerza motora. Sin embargo, si la paciente requiere un bloqueo nervioso más denso para la anestesia quirúrgica o para la segunda etapa del trabajo de parto, por ejemplo, una mejor opción puede ser un volumen menor de un LA de mayor concentración. En general, el anestesiólogo debe tener un conocimiento práctico de las características del LA utilizado para implementar correctamente un protocolo de redosificación.
Resolución de problemas
La colocación epidural presenta desafíos únicos que están directamente relacionados con la experiencia del médico, el escenario clínico y las características del paciente, entre otras cosas. La mayoría de estos problemas se pueden superar si el médico reconoce el problema, está familiarizado con la anatomía de la columna vertebral y sabe cómo hacer ajustes en la técnica (Tabla 27).
TABLA 27. Resolución de problemas durante el inicio del bloqueo epidural.
| Problema | Explicación posible | la columna Acción |
|---|---|---|
| disquete de aguja; aguja ángulos lateralmente | Entrada fuera de la línea media; supraespinoso perdido ligamento | Vuelva a evaluar la línea media; redirigir la aguja |
| Contacto óseo a < 2 cm | apófisis espinosa contactada; flexión de la columna inadecuado | Reidentificar el espacio intermedio; coloque la aguja en caudal región del interespacio |
| Contacto óseo a ≥ 4 cm | Entrada de la aguja demasiado lateral; lámina contactada | Redirigir la aguja hacia la línea media |
| resistencia ósea a lo largo de | ligamentos osificados; columna vertebral artrítica | Considere el abordaje paramediano |
| Incapacidad para avanzar catéter | Falsa pérdida de resistencia; epidural estrecho espacio; aguja demasiado cerca de la duramadre; orificio de aguja obstruido | predistensión de líquidos; girar el bisel de la aguja; usar más rígido catéter; avance ligeramente la aguja epidural; intentar una nueva ubicación en un espacio intermedio diferente; retirar la aguja hasta el ligamento amarillo y adelantar |
| hemo en catéter | canulación de la vena epidural; entrada de aguja también lateral; venas epidurales hinchadas | Retire el catéter 1–2 cm y enjuague con solución salina; realizar una nueva colocación si el hemo persiste; considerar iniciar procedimiento epidural en lateral posición |
| Retorno de líquido tibio y transparente en aguja o catéter | Punción dural accidental; intratecal colocación | Distinguir el líquido cefalorraquídeo de solución salina o anestesia local; si hay líquido cefalorraquídeo, considerar columna continua o nueva colocación en interespacio diferente |
| Dolor/parestesia en inserción del catéter | Catéter avanzado > 6 cm en epidural espacio; catéter cerca de la raíz nerviosa | Retirar el catéter a < 6 cm en el espacio epidural (2-3 cm para procedimientos quirúrgicos cortos); llevar a cabo nueva colocación si el dolor persiste |
| Incapacidad para palpar procesos espinosos | Obesidad; artritis severa; paciente con cirugía de espalda anterior | Optimizar la posición del paciente; considerar la línea media abordaje para pacientes obesos; usar buscador largo aguja para ayudar a identificar puntos de referencia óseos; considerar la colocación en posición lateral si el paciente incapaz de flexionar la columna; usar ultrasonografía |
| Incapacidad para flexionar la columna | Anciano; artritis; paciente con antecedentes instrumentación espinal | Considere el abordaje paramediano; considerar colocación en posición lateral |
| Curvatura de la columna | Escoliosis | Utilice ultrasonografía; si es posible, realice procedimiento por debajo del nivel de la curvatura (de lo contrario aguja directa en la curva) |
Dificultad para identificar el espacio epidural
Varias medidas de solución de problemas pueden ayudar si se produce una LOR equívoca al tratar de identificar el espacio epidural. Primero, asegúrese de que la jeringa LOR esté bien conectada a la aguja epidural. Si usa la técnica de LOR a aire, luego ponga 2–3 ml de solución salina en la jeringa de LOR y presione suavemente (es decir, con el dedo meñique). Si usa LOR para solución salina, omita la burbuja para este paso. La solución salina fluirá fácilmente si la punta de la aguja epidural está en el espacio epidural, pero encontrará resistencia si la punta de la aguja está en tejido blando.
Si encuentra resistencia, continúe inyectando la solución salina en el tejido blando y luego reanude la técnica LOR original. A menudo, la retroalimentación familiar de la jeringa LOR regresa después de que la solución salina se haya disipado en los planos de los tejidos blandos.
Otro método para distinguir entre el tejido blando y el espacio epidural durante la técnica de LOR a solución salina es colocar una pequeña burbuja en la jeringa de LOR. La burbuja debe comprimirse en diversos grados cuando la aguja epidural está en un tejido blando o en un ligamento, pero inyectará sin esfuerzo si la aguja está en el espacio epidural.
Si el LOR sigue siendo equívoco, inserte una aguja espinal de calibre 25 o 27 a través de la aguja epidural para perforar la duramadre. Si se ve LCR en la aguja espinal, la aguja epidural está colocada correctamente. La ausencia de LCR indica que aún no se ha encontrado el espacio epidural o que la aguja epidural está fuera de la línea media, en el espacio epidural lateral. Si el LOR sigue siendo equívoco, intente enhebrar el catéter.
Muchos catéteres, particularmente las versiones flexibles o reforzadas con alambre, no avanzarán si la aguja epidural no está completamente en el espacio epidural.
Parestesias durante la colocación de la aguja o el catéter epidural
No es infrecuente que los pacientes informen parestesias durante los procedimientos epidurales, en particular al interrogatorio directo del médico. Debido a que una parestesia indica que la aguja o el catéter está cerca de un nervio, la aguja debe retirarse y redirigirse si la sensación persiste. Alternativamente, el procedimiento epidural se puede iniciar en otro espacio intermedio. Sin embargo, la mayoría de las veces, la aguja simplemente se puede redirigir lejos del lado donde se detectó la parestesia. Durante la colocación del catéter, la predistensión de líquidos puede ayudar a reducir la incidencia de parestesias, aunque los datos son contradictorios. Enhebrar el catéter no más de 5 a 6 cm parece reducir el riesgo de parestesias. El uso de catéteres flexibles y, en particular, catéteres reforzados con alambre también parece reducir la incidencia de parestesias. Si una parestesia es transitoria, es aceptable continuar avanzando la aguja o enhebrando el catéter.
Punción dural accidental
La punción dural accidental complica aproximadamente el 1% de los procedimientos epidurales, aunque la incidencia reportada varía sustancialmente en la literatura. Las opciones de manejo incluyen colocar un catéter espinal continuo o retirar la aguja epidural y repetir el procedimiento epidural en un espacio intermedio diferente. Ya sea que se coloque un catéter espinal o se realice una nueva colocación epidural, la elección debe hacerse rápidamente para evitar la salida excesiva de LCR a través de la aguja epidural de gran calibre. Una técnica espinal continua puede tener la ligera ventaja de reducir la incidencia de CPPD y la necesidad de una EBP (ver la discusión a continuación), aunque los datos son limitados y contradictorios. En los casos en que la identificación del espacio epidural fue difícil o con pacientes de alto riesgo (p. ej., parturientas obesas con alta probabilidad de conversión a cesárea y pacientes quirúrgicas con vía aérea difícil anticipada), la colocación de un catéter espinal continuo también puede ser ventajoso. Esta opción evita el riesgo de una segunda punción dural y se ha informado que brinda analgesia y anestesia confiables, aunque los datos son contradictorios. Las desventajas de enhebrar un catéter espinal continuo incluyen el riesgo de una inyección accidental de grandes dosis de AL destinadas al espacio epidural y, posiblemente, un mayor riesgo de infección. Deben existir protocolos para alertar a todos los proveedores cuando se coloca un catéter espinal.
Si el médico elige colocar la epidural en otro espacio intermedio, corre el riesgo de una segunda ADP. Además, existe una preocupación por el paso de LA desde el espacio epidural al subaracnoideo a través de la brecha dural, lo que resulta en un bloqueo nervioso mayor al anticipado. Aunque puede no ser necesario, es razonable reducir la tasa basal para bombas continuas o PCEA; como siempre, tenga cuidado al inyectar bolos de AL o morfina epidural. La evidencia no apoya el uso del catéter epidural para una PBE profiláctica, aunque estudios más recientes pueden demostrar algún beneficio. Consideraciones más detalladas sobre la anatomía, la fisiopatología y el tratamiento de la CPPD se analizan en Dolor de cabeza por punción dural.
Dificultad para enhebrar el catéter
No es infrecuente la dificultad para enhebrar el catéter, incluso si la aguja está bien encajada en el espacio epidural. Este problema es más común con los catéteres flexibles de punta blanda. Las medidas de solución de problemas incluyen confirmar que la aguja epidural esté colocada correctamente en el espacio epidural (consulte la discusión anterior); inyectando varios mililitros de solución salina para “abrir” el espacio epidural; avanzando ligeramente la aguja epidural para que todo el bisel encaje en el espacio epidural (la jeringa LOR con solución salina sin burbujas de aire debe colocarse durante este paso); rotar el bisel de la aguja epidural; insertar un catéter diferente, menos flexible; retraer la aguja hasta el ligamento e identificar nuevamente el espacio epidural; y repetir el procedimiento epidural a un nivel espinal diferente. Ocasionalmente, la aguja epidural se tapa con restos de tejido que bloquean el paso del catéter. Reemplazar y luego retirar el estilete puede servir para eliminar los desechos que obstruyen. La presión subatmosférica es variable en la región lumbar; Es poco probable que pedirle al paciente que respire profundamente facilite el enhebrado del catéter, particularmente cuando se trata de catéteres flexibles reforzados con alambre. En general, realizar una nueva colocación en otro espacio intercostal parece conferir menos riesgo de ADP que rotar la aguja o avanzar con cautela la aguja epidural. Si elige comenzar de nuevo en otro espacio intermedio, retire la aguja y el catéter simultáneamente para evitar que se rompa el catéter.
Bloqueo nervioso unilateral
Después de que una epidural ha sido dosificada adecuadamente, el paciente puede quejarse de que un lado está densamente bloqueado, mientras que el lado opuesto tiene dolor y función motora intactos. La explicación más común para un bloqueo nervioso unilateral es que el catéter ha avanzado demasiado en el espacio epidural, lo que permite que la punta del catéter entre en el agujero intervertebral o esté muy cerca de un nervio. Los datos actuales sugieren que no hay ninguna indicación para hacer avanzar un catéter (ya sea con un solo orificio en el extremo o con múltiples orificios) más de 6 cm en el espacio epidural. Si persiste un bloqueo nervioso unilateral a pesar de la profundidad de inserción adecuada, considere retirar el catéter 1 a 2 cm, dejando 3 a 4 cm (2 a 3 cm para procedimientos cortos) en el espacio epidural. Si el paciente continúa incómodo a pesar de la manipulación del catéter, colóquelo en posición lateral con el lado desbloqueado hacia abajo y administre varios mililitros de AL diluido. Si estas maniobras no surten efecto, reemplace el catéter.
Sangre en la aguja o catéter epidural
La canulación de la vena epidural no es infrecuente, aunque la incidencia ha disminuido sustancialmente con el uso generalizado de catéteres flexibles. Las venas epidurales se encuentran principalmente en el espacio epidural anterior, delimitadas por el ligamento longitudinal posterior y su fascia. Una punción con sangre puede ser una indicación de que la inserción de la aguja o el catéter es demasiado lateral y debe redirigirse hacia la línea media. Otras medidas para minimizar el riesgo de canulación de la vena epidural durante la inserción del catéter incluyen el uso de catéteres reforzados con alambre, la administración de líquido para abrir el espacio epidural antes de enhebrar el catéter y evitar la inserción del catéter más allá de 5 a 6 cm, entre otras ( ver Toxicidad sistémica de los anestésicos locales). Si la sangre regresa a través del catéter a pesar de estas medidas, el catéter puede retirarse ligeramente y enjuagarse con solución salina. Esto se puede repetir hasta que la sangre deje de regresar o el catéter no tenga suficiente longitud en el espacio epidural, momento en el cual se debe reemplazar el catéter.
Dolor a pesar de la altura y la densidad adecuadas del bloqueo nervioso
El dolor persistente a pesar de la altura y densidad adecuadas del bloqueo nervioso puede ser el resultado de un bloqueo incompleto ("ventana" de dolor), bloqueo "parcheado" o mala extensión sacra. Una ventana de dolor en la que un área pequeña y distinta permanece desbloqueada a pesar de un bloqueo nervioso denso puede ser difícil de solucionar. Es razonable administrar complementos y girar al paciente con el lado de la ventana del catéter hacia abajo. La inyección de opioides en el espacio epidural también puede ayudar. Sin embargo, realizar una técnica de CSE que aporta densidad desde la porción espinal o reemplazar la epidural
en otro espacio intermedio puede ser necesario. Se debe tener mucho cuidado al decidir realizar anestesia CSE en caso de anestesia epidural fallida, ya que puede haber un mayor riesgo de anestesia espinal alta. Siempre que sea posible, se debe considerar un catéter espinal continuo con dosificación gradual del anestésico espinal.
Un bloqueo nervioso "manchado" o "en parches" puede resultar de la inyección de aire cuando se utiliza la técnica de LOR a aire, de variaciones anatómicas individuales que contribuyen a los dermatomas "perdidos" o de la migración del catéter. Administrar LA adicional, con o sin un opioide, después de que haya transcurrido una cantidad de tiempo suficiente desde que la dosis inicial es adecuada. También puede ayudar retirar el catéter 1-2 cm y colocar al paciente con el lado menos bloqueado en posición dependiente. Sin embargo, también es razonable reemplazar el catéter, particularmente si se han administrado múltiples recargas y si existe una alta probabilidad de conversión a anestesia quirúrgica.
En el caso de mala extensión sacra, las siguientes medidas pueden ayudar: Levantar la cabecera de la cama y volver a colocar el catéter con un AL más concentrado; administrar 100 μg de fentanilo epidural para mejorar la calidad del bloqueo nervioso; o inyecte neostigmina sin conservantes, 500 a 750 μg o clonidina, 75 μg por vía epidural.
Reemplazar una epidural independiente con una CSE también mejora la analgesia sacra, ya que el nervio sacro es grande y, en ocasiones, es difícil bloquearlo con AL administrados en el espacio epidural.
Analgesia inadecuada a pesar del catéter epidural completamente dosificado
Muy a menudo, la mejor estrategia es reemplazar el catéter epidural. Para evaluar si una epidural está funcionando correctamente, sienta si ambas piernas están calientes al tacto (la vasodilatación inducida por LA debe hacer que las extremidades inferiores se calienten si la epidural está correctamente colocada y en pleno funcionamiento). Evalúe también si el paciente tiene disminución de la percepción de la temperatura y disminución de la respuesta al pinchazo en los dermatomas que corresponden al bloqueo sensorial esperado. Considere administrar una dosis definitiva de AL (p. ej., 5 a 10 ml de lidocaína al 2% con o sin epinefrina en dosis incrementales) para determinar si el catéter está funcionando, siempre que el bloqueo motor resultante no esté contraindicado. Evaluar la fuerza motora y la temperatura del paciente y la percepción del dolor después de cada dosis. Controle los signos vitales para detectar cualquier indicación de hipotensión inducida por simpatectomía. Es recomendable no administrar más de 10 mL de AL si el catéter permanece dudoso; retirar el catéter y realizar una anestesia espinal conlleva el riesgo de una espinal alta o total si ya se ha administrado una cantidad excesiva de AL por vía epidural. La evidencia reciente sugiere que el número de recargas es un indicador confiable de si una epidural utilizada para la analgesia puede usarse con éxito para la anestesia quirúrgica. Si se han administrado varios complementos y el grado de analgesia sigue siendo equívoco, se debe retirar y reemplazar el catéter.
Disipación del bloqueo nervioso que requiere dosis más grandes
Este problema se produce por varias razones posibles. Los pacientes que recibieron CSE con fentanilo espinal o una combinación de opioide y LA pueden experimentar una transición abrupta del alivio a un bloqueo nervioso epidural inadecuado, particularmente si la anestesia espinal se resolvió antes de que se acumulara un volumen suficiente de la infusión epidural. Es posible que se requieran dosis cada vez mayores de LA por epidural para compensar la dosis de carga epidural inadecuada y cumplir con las altas expectativas del paciente después de experimentar la comodidad de la porción espinal. Alternativamente, si el catéter epidural se ha utilizado para la analgesia y se ha dosificado con frecuencia, puede ocurrir taquifilaxia en la LA. Otra posibilidad es que el catéter haya migrado a un vaso (consulte la discusión anterior) o se haya desprendido por completo del espacio epidural. Si el catéter permanece en su sitio de inserción inicial, administre un bolo de AL de mayor concentración y aumente la velocidad de infusión (si es continua). Considere agregar un opioide o clonidina para mejorar la calidad del bloqueo nervioso.
Analgesia epidural fallida
El problema de la analgesia epidural fallida se ve a menudo en obstetricia. Se coloca un catéter epidural y se dosifica, pero el paciente permanece incómodo. Se administra más AL, con mejoría subjetiva. Posteriormente, la paciente es llevada al quirófano para cesárea, que requiere un nivel sensitivo T4 denso, y el bloqueo nervioso es inadecuado. Existen varias opciones si una epidural falla a pesar de las medidas de solución de problemas. En situaciones electivas, el catéter epidural se puede reemplazar, preferiblemente en un espacio intermedio diferente, y volver a colocar la dosis con precaución para disminuir el riesgo de bloqueo epidural alto. Para procedimientos más urgentes, se puede realizar un CSE. Es necesaria una dosis reducida de medicación espinal si se administró un gran volumen de LA epidural durante la resolución de problemas o si el paciente tiene un bloqueo nervioso parcial. Con una CSE, el nivel sensorial se puede elevar según sea necesario con dosificación epidural suplementaria. Una inyección espinal de dosis única reducida también puede ser apropiada si la velocidad de inicio es una preocupación.
Sin embargo, reemplazar una epidural fallida con una técnica espinal conlleva el riesgo de anestesia espinal alta o total. Infiltrar la piel y el tejido subcutáneo con AL o realizar un bloqueo de nervio periférico, dependiendo del tiempo restante de la cirugía y el tipo de cirugía, pueden brindar alternativas. La conversión a AG es apropiada si no hay tiempo suficiente para repetir la técnica neuroaxial o para colocar un bloqueo de nervio periférico o si realizar otro procedimiento neuroaxial presenta un riesgo indebido.
De manera óptima, una epidural que no funciona se reconocerá y reemplazará antes de que se hayan administrado grandes dosis de LA y antes de que se requieran técnicas anestésicas alternativas. El número de bolos requeridos para mantener una analgesia adecuada es un indicador confiable de que una epidural utilizada para analgesia puede fallar en la conversión a anestesia quirúrgica. Como regla general, si la función del catéter sigue siendo equívoca durante la dosificación, deje de inyectar después de un volumen predeterminado (p. ej., 10 ml) para asegurarse de que realizar otra técnica regional no conduzca a una anestesia espinal alta o total o a una toxicidad sistémica LA (LAST).
Dificultad para retirar el catéter epidural
Ocasionalmente, se encuentra resistencia al intentar retirar el catéter epidural. El uso de fuerza excesiva puede provocar la rotura del catéter y la retención de fragmentos de catéter. En caso de atrapamiento del catéter, colocar al paciente en decúbito lateral o en la posición de inserción original y aplicar una tracción suave y continua puede facilitar la extracción. En ocasiones, puede ser necesario colocar al paciente en la misma posición en la que se insertó el catéter. También se ha observado que sujetar el catéter a la piel bajo tracción y volver a intentar retirarlo más tarde, enhebrar un estilete e inyectar solución salina en un catéter reforzado con alambre ayuda en la extracción. Los informes de secuelas neurológicas de fragmentos retenidos son raros, lo que sugiere que la extracción quirúrgica no está justificada en el paciente asintomático.
COMPLICACIONES Y EFECTOS SECUNDARIOS COMUNES
Las complicaciones del bloqueo epidural pueden clasificarse en términos generales como relacionadas con el fármaco o el procedimiento. Las posibles complicaciones relacionadas con el fármaco incluyen LAST, alergia a los LA, lesión directa del tejido nervioso inducida por LA y errores del fármaco o del modo de administración. Las complicaciones relacionadas con el procedimiento pueden ser de leves a moderadas o transitorias, como dolor de espalda, neumoencéfalo y CPPD. Las complicaciones potencialmente mortales incluyen inyección subdural de AL, meningitis aséptica o infecciosa total o espinal alta, paro cardíaco, SEA, formación de hematoma epidural y lesiones neurológicas permanentes. En contraste con las complicaciones, varios efectos secundarios conocidos o esperados acompañan el inicio y mantenimiento del bloqueo epidural sin afectar negativamente los resultados del paciente a largo plazo. Esta sección revisa tanto las complicaciones como los efectos secundarios comunes asociados con el bloqueo epidural, con énfasis en los factores de riesgo, las medidas preventivas y el tratamiento. Varias de las complicaciones se tratan con mayor detalle en otras partes de este libro de texto.
Toxicidad Sistémica de Anestésicos Locales
La toxicidad sistémica del anestésico local resulta de una concentración plasmática excesiva en la sangre debido a una inyección intravascular no intencional o, con menos frecuencia, a la absorción sistémica en el sitio de la inyección. La inyección intravascular directa puede ocurrir con la canulación no intencional de la vena epidural durante la colocación del catéter o la posterior migración del catéter a un vaso. Los factores de riesgo para la canulación intravascular incluyen el traumatismo de los vasos epidurales durante el inicio del bloqueo nervioso, el uso de catéteres rígidos, el embarazo y la posición del paciente durante la colocación de la epidural, entre otros.Tabla 28).
TABLA 28. Factores de riesgo para la canulación de la vena epidural.
| Trauma a los vasos epidurales durante el inicio del bloqueo |
| Múltiples intentos de colocación |
| Catéter rígido y no flexible |
| Venas epidurales congestionadas (p. ej., embarazo) |
| Posición para sentarse |
El riesgo de canulación de la vena epidural en pacientes obstétricas puede reducirse con el inicio del bloqueo epidural en posición lateral, el uso de catéteres reforzados con alambre, el uso de catéteres de un solo orificio (en lugar de multiorificio), predistensión de líquidos con solución salina normal antes para enhebrar el catéter y limitar la profundidad del catéter a 6 cm o menos (Tabla 29). Limitar el número de intentos de colocación epidural; evitando el espacio epidural lateral, donde es más probable la punción del vaso; y evitar la administración directa de AL a través de la aguja epidural también puede reducir el riesgo de inyección intravascular directa.
TABLA 29. Estrategias para evitar la canulación de la vena epidural.
| Colocación en posición lateral |
| Uso de catéter flexible reforzado con alambre |
| Uso de catéter de orificio único versus multiorificio |
| Predistensión de líquidos antes de enhebrar el catéter |
| Limite la profundidad de inserción del catéter a < 6 cminserción |
Aunque los datos no son concluyentes con respecto al papel del material del catéter y la configuración de la punta, el uso de catéteres flexibles puede reducir el riesgo de migración posterior del catéter hacia un vaso. Debido a la salida preferencial del puerto proximal de los catéteres multipuerto durante las técnicas de infusión continua, existe una remota posibilidad de que un puerto distal pueda migrar a un vaso sin que se note hasta que se administre un bolo manual. Esto se puede evitar con el uso de un catéter de un solo orificio.
Se recomienda dosificar el catéter epidural en incrementos de 3 a 5 ml con aspiración negativa frecuente de sangre y LCR para detectar catéteres mal colocados. La mayoría de los catéteres epidurales disponibles comercialmente tienen ventanas de "retroceso" distal y proximal para facilitar la visualización de sangre o LCR en la aspiración. El uso de un vendaje transparente y cinta adhesiva mejora la visualización de estas ventanas. Aunque el uso de la dosis de prueba tradicional de epinefrina es controvertido, se puede usar una dosis de prueba para evaluar si la punta del catéter está en un vaso sanguíneo.
El grado de absorción sistémica está determinado en parte por el sitio de inyección, la dosis y concentración de LA inyectada, las propiedades del LA administrado, la vascularización del sitio de inyección y la presencia o ausencia de epinefrina en la solución. Ciertas condiciones y comorbilidades, como edad avanzada, insuficiencia hepática, baja concentración de proteínas plasmáticas, disfunción cardíaca grave, cardiopatía isquémica, anomalías de la conducción cardíaca y acidosis metabólica y respiratoria, también pueden predisponer a los pacientes a la toxicidad sistémica. En general, es menos probable que la absorción sistémica desde el espacio epidural
ocurrir que de las áreas de mayor vascularidad. Las áreas de mayor concentración plasmática por absorción en orden descendente son las siguientes: intercostal, caudal, paracervical, epidural, plexo braquial y ciático/femoral.Tabla 30).
TABLA 30. Orden relativo de la concentración plasmática máxima del anestésico local asociado con la anestesia regional (orden descendente).
| Intercostal |
| Caudal |
| paracervical |
| Epidural |
| Plexo braquial |
| ciático/femoral |
Sin embargo, el traumatismo de los vasos durante el inicio del procedimiento epidural puede dar lugar a una absorción intravascular desde el espacio epidural más rápida de lo previsto. La adición de epinefrina a la solución de LA disminuye la absorción sistémica, pero puede no ser adecuada en áreas altamente vascularizadas, donde la absorción sistémica es probable, o para todas las poblaciones de pacientes. La epinefrina también puede prolongar innecesariamente la duración de la acción de los AL. La toxicidad asociada con la absorción sistémica de los LA se puede reducir mediante una selección cuidadosa de los pacientes, manteniéndose atento a los signos y síntomas de toxicidad, limitando la dosis total de LA administrada, usando concentraciones apropiadas de LA y, posiblemente, usando los LA de amida más nuevos, como como ropivacaína y levobupivacaína.
La bupivacaína racémica se ha asociado con una mayor cardiotoxicidad debido a una unión mejorada y una disociación más lenta de los canales iónicos en el miocardio.
Los signos y síntomas tempranos del SNC de toxicidad por LA incluyen aturdimiento, mareos, tinnitus, entumecimiento y hormigueo perioral, dificultad para hablar, diplopía o visión borrosa, inquietud y confusión. Las contracciones musculares, los temblores de los músculos faciales y las extremidades, los escalofríos y las convulsiones generalizadas ocurren a concentraciones plasmáticas más altas, seguidas de una depresión global del SNC, que se manifiesta por somnolencia, pérdida del conocimiento y paro respiratorio. La acidosis, la hipercarbia y la hipoxia predisponen y exacerban la toxicidad del SNC. Las manifestaciones cardiovasculares a altas concentraciones plasmáticas incluyen hipotensión, bradicardia y otras arritmias, y paro cardíaco.Tabla 31).
Cuando se reconozca o se sospeche de LAST, absténgase de administrar LA adicional y solicite asistencia. El tratamiento requiere atención inmediata al apoyo de las vías respiratorias, supresión de la actividad convulsiva y preparación para la reanimación cardiopulmonar y, posiblemente, CPB. Las pautas actuales recomiendan limitar las dosis individuales de epinefrina a menos de 1 μg/kg durante los esfuerzos de reanimación. La terapia con emulsión de lípidos (20 %) debe comenzar con una dosis de carga inicial de 1.5 ml/kg, seguida de una infusión continua de 0.25 ml/kg/min durante un mínimo de 10 minutos después de que se haya restablecido la estabilidad circulatoria. Referirse a Toxicidad sistémica del anestésico local para una discusión más detallada de LAST.
TABLA 31. Signos y síntomas de la anestesia local
toxicidad sistémica.
| Sistema nervioso central Toxicidad | Toxicidad cardiovascular |
|---|---|
| hormigueo peribucal y entumecimiento | La hipotensión |
| Aturdimiento/mareos | Vasodilatación periférica |
| Tinnitus | bradicardia, conducción retrasos |
| Alteraciones visuales | Arritmias ventriculares |
| Inquietud, agitación | Paro cardíaco |
| trastornos del habla | |
| Temblando | |
| Convulsiones generalizadas | |
| Depresion respiratoria/ detener |
Alergia a los anestésicos locales
Pueden ocurrir verdaderas reacciones alérgicas a los LA, pero afortunadamente son raras. La mayoría de las reacciones documentadas no están mediadas por inmunoglobulina E (IgE) y se pueden atribuir a reacciones a otros agentes administrados concomitantemente (p. ej., aditivos, epinefrina, conservantes, antibióticos) o a una reacción de hipersensibilidad retardada de tipo IV (es decir, dermatitis de contacto leve). Alternativamente, las reacciones informadas pueden deberse a ansiedad, un episodio vasovagal, estimulación simpática endógena o una respuesta adversa del paciente al procedimiento quirúrgico, dental, oftálmico u obstétrico en sí.
Con base en una extensa revisión de la literatura, Bhole y sus colegas estimaron que la prevalencia de la verdadera alergia mediada por IgE era inferior al 1%. Una reacción mediada por inmunocomplejos asociada con niveles de complemento sérico reducidos o agotados es aún más rara.
Cuando un paciente informa antecedentes de alergia a los LA, es importante obtener una historia detallada, que incluya qué LA estuvo implicado, la dosis y la vía de administración, la reacción que ocurrió y el entorno clínico. Las reacciones alérgicas verdaderas pueden presentarse con una variedad de signos y síntomas dermatológicos, cardíacos o respiratorios, como urticaria, prurito, angioedema, hipotensión, shock y broncoespasmo. Aunque la literatura actual sugiere que las reacciones alérgicas a los LA de amida son más comunes que las reacciones a los LA de tipo enlace éster, esto puede reflejar el uso preferencial actual del primero. Históricamente, las reacciones adversas, especialmente la dermatitis de contacto, se han informado con mayor frecuencia con agentes de éster, como la procaína, la benzocaína, la tetracaína y la cloroprocaína. Esto puede atribuirse en parte al hecho de que los compuestos de éster son derivados del ácido para-aminobenzoico (PABA), un aditivo que se encuentra en muchos artículos para el hogar (p. ej., loción, protector solar, cosméticos); Se ha planteado la hipótesis de que la exposición previa a PABA sensibiliza a las personas a los ésteres LA. Alternativamente, el metilparabeno, un conservante en los LA de amida y éster que se metaboliza a PABA, puede ser responsable de muchas de las reacciones alérgicas notificadas. Se ha informado de reactividad cruzada entre los grupos amida y éster, pero es extremadamente rara y probablemente atribuible a un conservante común. Puede ocurrir reactividad cruzada entre los LA de éster y, con menor frecuencia, entre los LA de amida.
Actualmente se carece de pruebas confiables para identificar la sensibilidad a los LA. La presencia de triptasa de mastocitos en suero puede confirmar una reacción anafiláctica inmediatamente después, mientras que las pruebas de punción cutánea, las pruebas intradérmicas y las pruebas de provocación subcutánea pueden ayudar a identificar el agente causal. El manejo de una reacción alérgica a los LA incluye eliminar el agente agresor; administración temprana de epinefrina intravenosa para tratar la hipotensión y el colapso cardiovascular; apoyo de las vías respiratorias, si es necesario; y, posiblemente, la administración intravenosa de bloqueadores de los receptores de histamina-1 y -2, broncodilatadores y corticosteroides.
Aracnoiditis
La aracnoiditis es un trastorno raro caracterizado por cambios inflamatorios en la aracnoides. Aunque el mecanismo preciso sigue sin estar claro, se desarrolla fibrosis y se forman adherencias entre las raíces nerviosas y las membranas que rodean el cerebro, la médula espinal y la cauda equina. En casos adhesivos crónicos, los depósitos de colágeno finalmente encapsulan las raíces nerviosas, creando atrofia de las raíces nerviosas como resultado de una interrupción del suministro de sangre. Los traumatismos, la cirugía, las infecciones, los contaminantes, los desinfectantes, los medios de contraste, los tumores, la hemorragia subaracnoidea y la administración subaracnoidea de irritantes (p. ej., esteroides) pueden precipitar estos cambios inflamatorios. La administración intratecal accidental de grandes volúmenes de cloroprocaína que contiene el conservante bisulfito de sodio también se ha relacionado con la aracnoiditis, aunque el papel del conservante se ha cuestionado en estudios recientes.
No se ha establecido claramente en la literatura un vínculo entre el bloqueo del nervio epidural o la colocación de un catéter y la aracnoiditis. No existen datos sobre el riesgo de aracnoiditis con el uso de la solución antiséptica clorhexidina en humanos; no obstante, es prudente mantener la solución alejada de todos los fármacos y equipos de los kits espinales y epidurales y permitir que se seque antes de iniciar los procedimientos neuroaxiales. La clorhexidina en alcohol sigue siendo la solución de elección para la desinfección de la piel antes de iniciar el bloqueo neuroaxial central.
La presentación clínica de la aracnoiditis es compleja, con sintomatología variada y puede retrasarse varios meses. Las características clínicas más comunes son dolor de espalda que se irradia a las extremidades inferiores y aumenta con el esfuerzo; dolor de glúteos; espasmos musculares; disminución del rango de movimiento del tronco; anomalías sensoriales; debilidad motora o parálisis por debajo del nivel de la lesión que normalmente no progresa; y disfunción del esfínter urinario (Tabla 32).
Desafortunadamente, la presentación clínica mixta puede conducir a un diagnóstico erróneo y la aracnoiditis puede atribuirse incorrectamente a estenosis espinal, enfermedad del disco lumbar, tumores espinales u otras lesiones compresivas de la columna. El diagnóstico se puede confirmar mediante mielografía, tomografía computarizada (TC) o resonancia magnética. Los hallazgos característicos de la resonancia magnética muestran conglomerados de raíces que residen centralmente en el saco dural, adherencias que atan las raíces nerviosas en la periferia y tejido blando que reemplaza el espacio subaracnoideo.
TABLA 32. Presentación clínica de la aracnoiditis.
| Dolor de espalda que se irradia a las extremidades inferiores, empeora con la actividad |
| dolor de glúteos |
| Espasmos musculares |
| Debilidad/parálisis motora |
| Disminución del rango de movimiento del tronco. |
| Disfunción del esfínter urinario |
Desafortunadamente, es poco probable una mejoría neurológica significativa con las terapias actuales, incluidos los corticosteroides intravenosos, los AINE y la terapia con antibióticos. Los déficits pueden progresar a una discapacidad grave y permanente.
Dolor de espalda
El dolor de espalda es un síntoma posoperatorio común, con una incidencia que oscila entre el 3% y el 31% después de una cirugía no obstétrica, independientemente de la técnica anestésica. Aunque la etiología es multifactorial, tanto la lumbalgia posoperatoria como la periparto suelen atribuirse a técnicas neuroaxiales cuando existe una asociación temporal.
El dolor de espalda después del bloqueo epidural es más común, más severo y más duradero que después de los procedimientos espinales. El traumatismo local, la inflamación de los ligamentos, la punción con aguja de un disco intervertebral, el estiramiento de las cápsulas articulares y los ligamentos más allá de su rango fisiológico y el espasmo muscular pueden explicar parte del dolor de espalda postepidural informado. El uso de agujas más grandes, la inserción de catéteres y el aumento de volumen de las AL, en comparación con las técnicas espinales, también pueden jugar un papel. Grandes dosis epidurales de 2-cloroprocaína que contiene el conservante EDTA también se han asociado con dolor de espalda; no se han observado complicaciones similares con 2-cloroprocaína sin conservantes. En un estudio reciente, Hakim y sus colegas identificaron los siguientes factores de riesgo independientes para el dolor lumbar persistente (es decir, ≥3 meses) después de una cirugía no obstétrica con anestesia epidural: intentos múltiples de colocación epidural, índice de masa corporal (IMC) más alto, cirugía en la posición de litotomía, y tiempo quirúrgico superior a 2.5 horas.
El dolor de espalda después del bloqueo epidural suele ser autolimitado y debe resolverse en 7 a 10 días. Se debe alentar a los pacientes a que se abstengan de hacer reposo en cama. Los AINE, el paracetamol o el calor pueden proporcionar alivio sintomático. Si el dolor persiste, progresa o es desproporcionado de lo esperado, se deben considerar otras etiologías, como TNS, hernia de disco, estenosis espinal, aracnoiditis, sacroilitis, lesión musculoesquelética, lesión nerviosa, absceso epidural y hematoma epidural. . Las intervenciones profilácticas que pueden ayudar a prevenir el dolor de espalda asociado con los procedimientos epidurales incluyen realizar un bloqueo nervioso de campo para anestesiar los nervios espinales recurrentes que inervan los ligamentos y músculos interespinosos antes de iniciar el bloqueo epidural; agregar NSAID al LA utilizado para la infiltración de la piel; y la administración de dexametasona epidural.
A pesar de la asociación generalizada entre el dolor de espalda musculoesquelético y los procedimientos neuroaxiales, los estudios de mujeres embarazadas que recibieron analgesia epidural para el dolor de parto proporcionan evidencia convincente de que el dolor de espalda no está relacionado con las técnicas neuroaxiales. Varios ensayos controlados aleatorizados y estudios prospectivos de cohortes han demostrado que la analgesia epidural intraparto no provoca dolor de espalda posparto nuevo y a largo plazo.
Dolor de cabeza por punción dural
La cefalea posterior a la punción dural es una complicación común de la anestesia espinal, las punciones lumbares ("punciones espinales") y los procedimientos epidurales complicados por ADP o desgarro dural no reconocido. En general, se acepta que la incidencia de ADP es igual o inferior al 1%; hasta el 80% de los pacientes pueden experimentar CPPD después de ADP. Aunque el mecanismo preciso aún no se comprende bien, los signos y síntomas de la CPPD parecen ser el resultado de la fuga de LCR a través del orificio dural. En posición erguida, el tejido cerebral se hunde en la bóveda craneal, creando una tracción dolorosa en la duramadre, la hoz del cerebro, los vasos sanguíneos cerebrales, la tienda del cerebelo, los nervios craneales y las raíces nerviosas. Esta tracción también contribuye a las parálisis de los nervios craneales que se observan con frecuencia en pacientes con CPPD. La vasodilatación cerebral compensatoria en respuesta a la disminución del LCR también parece jugar un papel en la génesis y gravedad de la CPPD.
Falta una definición universalmente aceptada de CPPD en la literatura. Según la Sociedad Internacional de Dolor de Cabeza, una CPPD se desarrolla dentro de los 5 días posteriores a una punción lumbar, generalmente se acompaña de rigidez en el cuello o síntomas auditivos subjetivos,
y se resuelve espontáneamente dentro de las 2 semanas o después de un tratamiento efectivo con un EBP. Clínicamente, los pacientes comúnmente se quejan de un dolor de cabeza fronto-occipital que es leve o está ausente en la posición supina y se intensifica cuando se eleva la cabeza. El dolor puede extenderse al cuello, los hombros y las extremidades superiores y puede acompañarse de náuseas y vómitos, mareos, diplopía, tinnitus, visión borrosa, nistagmo y pérdida de la audición. La afectación de los nervios craneales debe impulsar una evaluación y un tratamiento expeditos. El dolor de cabeza se desarrolla dentro de las 48 horas en la gran mayoría de los casos (más comúnmente en las primeras 24 horas) (Tabla 33). Los dolores de cabeza que ocurren durante o inmediatamente después de los procedimientos epidurales son más probables debido a la inyección accidental de aire durante la identificación del espacio epidural con la técnica LOR to air (neumoencéfalo).
TABLA 33. Signos y síntomas de la cefalea pospunción dural.
| Cefalea fronto-occipital; se intensifica cuando la cabeza está elevado |
| Rigidez en el cuello |
| Dolor de cuello, hombro y/o brazo |
| Pérdida auditiva de tinnitus |
| Náuseas, vómitos, mareos |
| Diplopía, visión borrosa, nistagmo |
Por lo general, la CPPD se resuelve espontáneamente en 1 a 2 semanas, pero puede durar meses o incluso años; un porcentaje sustancial de pacientes puede desarrollar dolores de cabeza crónicos después de ADP con una aguja Tuohy de gran calibre.
Los factores de riesgo para la CPPD incluyen edad más joven, sexo femenino, IMC más bajo, embarazo, pujar durante la segunda etapa del trabajo de parto, el uso de agujas espinales cortantes versus atraumáticas y el uso de agujas de mayor calibre (Tabla 34). Existe evidencia menos convincente con respecto al papel de la orientación del bisel de la aguja, el número de punciones durales, el abordaje utilizado para ingresar al espacio epidural (paramediano versus línea media), la posición del paciente durante el inicio del procedimiento epidural y la técnica utilizada para identificar la epidural. espacio (LOR al aire versus solución salina con o sin una burbuja de aire).
TABLA 34. Factores de riesgo de la cefalea pospunción dural.
| Edad más joven |
| Genero femenino |
| Bajo índice de masa corporal |
| Pérdida de resistencia al aire. |
| Pujar durante la segunda etapa del trabajo de parto |
| Uso de aguja de corte. |
| Uso de aguja de mayor calibre |
Se han propuesto varias intervenciones para la prevención o el tratamiento de la CPPD. Parece haber poco beneficio de las medidas conservadoras, como el reposo en cama y la administración intensiva de líquidos. Sin embargo, se puede obtener alivio sintomático con analgésicos, agentes farmacológicos con propiedades vasoconstrictoras (cafeína, teofilina, sumatriptán) y, posiblemente, corticotropina (ACTH). En una revisión sistemática cuantitativa de la evidencia disponible sobre las medidas para prevenir la CPPD, Apfel et al. encontraron que la administración de morfina epidural antes de retirar el catéter puede otorgar alguna ventaja, pero esta conclusión se basó en un pequeño ensayo controlado aleatorio. En un metaanálisis reciente, Heesen et al. sugirió que la inserción de un catéter intratecal después de la ADP puede proteger contra la CPPD y puede reducir la necesidad de una PBE, pero se justifican estudios adicionales. La evidencia hasta la fecha sobre el uso rutinario de PBE profiláctica no es concluyente. Hay datos limitados para respaldar el parche epidural con solución salina normal, dextrano 40 y gelatina y pegamento de fibrina.
El parche de sangre epidural, preferiblemente al principio del curso del dolor de cabeza, sigue siendo el estándar de oro para el tratamiento. Los estudios observacionales informaron una recuperación rápida en más del 90 % de los pacientes después de la PBE, aunque el alivio puede ser transitorio en un pequeño porcentaje de estos pacientes. Un ensayo controlado aleatorio bien diseñado en pacientes neurológicos demostró que la EBP ofrece una resolución completa de los síntomas en un gran porcentaje de pacientes y reduce la gravedad de los síntomas en aquellos que no experimentan una resolución completa. Además, el tratamiento temprano con un EBP reduce la duración de la estadía en el hospital y las visitas a la sala de emergencias y permite que los pacientes reanuden sus actividades de la vida diaria antes de lo que sería posible con un manejo expectante.
Antes de realizar una PBE, se deben descartar otras causas de cefalea, como preeclampsia/eclampsia y meningitis. En determinados escenarios clínicos, también puede ser necesario descartar una PIC elevada. Usando técnicas estériles, el espacio epidural en o por debajo del nivel de ADP anterior se identifica usando LOR a solución salina normal. La burbuja de aire se omite debido a la preocupación de que el aire pueda entrar en la brecha dural y provocar neumoencéfalo. Se inyectan lentamente en el espacio hasta 20 ml de la sangre del paciente (extraído asépticamente); el médico debe dejar de inyectar sangre si el paciente experimenta dolor o presión de moderado a intenso en la región lumbar o del cuello. Aunque queda por determinar el volumen óptimo de sangre, la inyección de más de 20 ml parece no otorgar ningún beneficio adicional. El paciente normalmente permanece en decúbito supino durante al menos 1 hora después de la EBP. El dolor de espalda y, con menos frecuencia, el dolor de cuello se experimentan comúnmente durante el procedimiento y, cuando son intensos, pueden alertar al médico para que deje de inyectar sangre. Para minimizar el riesgo de infecciones y secuelas relacionadas, tanto la obtención de sangre autóloga como la identificación del espacio epidural deben realizarse mediante estrictas técnicas asépticas. Para una discusión más profunda de PDPH, consulte Dolor de cabeza por punción postdurale.
Inyección subdural
El espacio subdural ha sido descrito históricamente como un espacio potencial entre la aracnoides normalmente muy adherida y la duramadre suprayacente, aunque puede representar una hendidura a lo largo de la capa de células del borde dural que resulta solo del daño tisular directo. La inyección de una pequeña dosis de LA en el área puede tener profundos efectos hemodinámicos y simpaticolíticos.
La inyección subdural es una ocurrencia relativamente rara, con una incidencia estimada de 0.1% a 0.82% de las inyecciones epidurales. Las características clínicas que pueden ayudar a distinguir la anestesia subdural de la epidural o raquídea incluyen un bloqueo sensitivo más alto de lo esperado con escasa extensión caudal y preservación del sacro; un nivel superior al previsto de bloqueo motor de densidad variable; y una velocidad de inicio que se parece más a la anestesia epidural (10 a 20 minutos). Las inyecciones subdurales comúnmente dan como resultado un bloqueo bilateral, aunque pueden ocurrir bloqueos nerviosos unilaterales o parcheados, con cambios sensoriales y motores más notables en las extremidades superiores y analgesia y anestesia inadecuadas en las extremidades inferiores. Los pacientes pueden desarrollar síndrome de Horner (ptosis, miosis y anhidrosis), anestesia facial y corneal y disnea. Además, se puede desarrollar hipotensión de leve a moderada (Tabla 35). El tratamiento puede requerir soporte cardiovascular y respiratorio, incluida la administración de líquidos intravenosos y vasopresores y, posiblemente, intubación endotraqueal con ventilación mecánica. Sin embargo, reportes de casos han descrito el uso de catéteres subdurales para lograr anestesia quirúrgica.
TABLA 35. Presentación clínica de un bloqueo nervioso subdural.
| Bloqueo sensorial más alto de lo esperado |
| Pobre extensión caudal, preservación del sacro |
| Bloqueo motor de densidad variable superior a lo esperado |
| bloqueo generalmente bilateral, pero puede ser unilateral o asimétrico |
| Síndrome de Horner (ptosis, miosis, anhidrosis) |
| Anestesia facial y corneal |
| Disnea |
| La hipotensión |
Anestesia Espinal Total
El bloqueo espinal total, que complica aproximadamente 1 de cada 1400 intentos de procedimientos epidurales, puede resultar de ADP no reconocido con inyección no intencional de una dosis epidural de LA, la administración de una dosis grande de LA en el compartimento subdural y la migración no detectada de la punta del catéter epidural. hacia el espacio subaracnoideo. También se ha observado cuando un orificio de un catéter multiorificio se aloja en el espacio subaracnoideo; con translocación de LA a través de una ruptura dural accidental o intencional; después de las técnicas de CSE; y después de un bloqueo epidural fallido se reemplaza con una técnica espinal.
La anestesia espinal total por lo general se desarrolla a los pocos minutos de la administración de LA, aunque puede ocurrir inesperadamente más tarde con cambios en la posición del paciente o después de que un catéter epidural que funcionaba anteriormente haya migrado al espacio subaracnoideo. Durante el bloqueo espinal total, la AL se propaga lo suficientemente alto como para bloquear los nervios de toda la médula espinal y, ocasionalmente, del tronco encefálico. Los cambios sensoriales y motores ascendentes se desarrollan rápidamente, seguidos de hipotensión profunda, bradicardia, disnea y dificultad para fonar y tragar. La inconsciencia y la apnea pueden resultar de la acción directa del LA sobre el tronco del encéfalo, parálisis de los músculos respiratorios e hipoperfusión cerebral. El tratamiento incluye soporte de las vías respiratorias y, si es necesario, intubación endotraqueal; la administración de oxígeno al 100%; y soporte hemodinámico con fluidos intravenosos y vasopresores. La epinefrina debe usarse temprano y en dosis crecientes para estabilizar la frecuencia cardíaca y la presión arterial en pacientes inestables. A medida que el bloqueo nervioso retrocede, el paciente recuperará la conciencia y el control de la respiración, seguido de la recuperación de la función motora y sensorial. La administración de sedación hasta la remisión del bloqueo nervioso puede ser apropiada una vez que el paciente esté estable.
Por lo general, la anestesia espinal total puede evitarse durante las técnicas de catéter epidural continuo mediante la administración cuidadosa de LA en dosis pequeñas y divididas, con aspiración frecuente y, posiblemente, el uso de una dosis de prueba epidural. Los pacientes deben ser monitoreados durante las recargas, durante la dosificación incremental para lograr la anestesia quirúrgica y mientras estén en PCEA. Las quejas inusuales del paciente y los cambios hemodinámicos inesperados pueden justificar la extracción y el reemplazo inmediatos del catéter. Si se reconoce una punción dural no intencional durante la colocación de la aguja, se puede retirar la aguja y colocarla en otro espacio intermedio o se puede insertar un catéter espinal. Si se reconoce ADP después de la inserción del catéter, es apropiado continuar con una técnica espinal continua o repetir el procedimiento epidural en otro espacio intermedio. Es posible que se requiera una dosis reducida de AL si se coloca con éxito un catéter en un nivel espinal diferente después de una punción dural anterior. Si se coloca un catéter espinal, el catéter debe estar claramente etiquetado, la bomba de infusión debe estar etiquetada y configurada a una dosis reducida, y todos los médicos involucrados deben estar informados. De manera óptima, se deben implementar procedimientos y políticas con respecto al manejo de los catéteres espinales.
Absceso epidural espinal
El absceso epidural espinal es un trastorno raro que afecta de manera desproporcionada a pacientes ancianos e inmunocomprometidos. Las personas con estadías prolongadas en la unidad de cuidados intensivos, los usuarios de drogas intravenosas y los pacientes con bacteriemia, DM, dependencia del alcohol, cáncer, VIH y enfermedad renal en etapa terminal tienen un mayor riesgo en comparación con la población general.Tabla 36). En las últimas décadas, la incidencia de SEA ha aumentado, en parte debido al aumento de la instrumentación espinal, el aumento del uso de drogas ilícitas y el envejecimiento de la población.
TABLA 36. Condiciones predisponentes para el absceso epidural espinal.
| Mayor | Inyección de esteroides |
| La diabetes mellitus | Alcoholismo |
| VIH / SIDA | Enfermedad del higado |
| Uso crónico de esteroides | Fallo renal |
| Insuficiencia suprarrenal | Artritis reumatoide |
| Catéter epidural crónico | Celulitis |
| Urinario prolongado cateterismo | absceso del psoas |
| Dispositivo vascular permanente | Uso de drogas intravenosas |
| espinal reciente instrumentación | Osteomielitis |
Se estima que el 5% de los SEA están asociados con procedimientos epidurales. Los factores de riesgo para esta rara complicación incluyen infusiones de catéter epidural extendidas e infección localizada o sistémica al momento de iniciar el bloqueo nervioso. El sitio de colocación de la epidural también parece colocar a algunos pacientes en mayor riesgo de formación de SEA, con catéteres torácicos y lumbares implicados con más frecuencia que los catéteres cervicales. La mala adherencia a la técnica estéril y, posiblemente, los múltiples intentos de colocación epidural pueden poner a los pacientes en un riesgo adicional.
Las bacterias acceden al espacio epidural a través de diseminación hematógena (más comúnmente) o diseminación contigua; la fuente de acceso no se identifica en el resto de los casos. Staphylococcus aureus y, cada vez más, S. aureus resistente a la meticilina (MRSA) representan la gran mayoría de los casos de SEA. Los patógenos menos comúnmente involucrados incluyen Escherichia coli, Pseudomonas aeruginosa y Staphylococcus epidermidis, el último más comúnmente asociado con procedimientos neuroaxiales, incluido el bloqueo epidural y las inyecciones epidurales de esteroides. La infección parece lesionar la médula espinal por compresión mecánica directa o trombosis (oclusión vascular por tromboflebitis séptica) o una combinación de ambas, aunque no se ha dilucidado el mecanismo preciso.
El diagnóstico temprano, el tratamiento oportuno y el seguimiento constante son esenciales para evitar daños neurológicos irreversibles por SEA. Los síntomas clínicos más comunes son dolor de espalda, fiebre y cambios neurológicos, como debilidad en las piernas o deficiencias sensoriales, pero la mayoría de los pacientes no presentan esta tríada. En cambio, los pacientes pueden presentar disfunción de la vejiga, sepsis, meningitis, paraplejía o cuadriplejía, infección del tracto urinario (ITU), cambios en el estado mental, inflamación en el sitio del catéter, dolor de cabeza, rigidez en el cuello o náuseas y vómitos. Los síntomas se presentan con mayor frecuencia dentro de los 7 días, pero pueden demorarse 60 días o más. También pueden estar presentes un recuento elevado de glóbulos blancos (WBC) y una velocidad de sedimentación globular (VSG) o proteína C reactiva elevadas, pero estos hallazgos de laboratorio son inespecíficos. Si se sospecha SEA, la resonancia magnética realzada con gadolinio es la herramienta diagnóstica de elección. Algunos investigadores han propuesto que se considere la resonancia magnética en pacientes que han recibido catéteres epidurales si se desarrollan signos sistémicos y locales de infección (p. ej., pus o eritema en el sitio de inserción epidural), incluso en ausencia de déficits neurológicos.
La administración de antibióticos intravenosos de amplio espectro, en última instancia adaptados a cultivos de sangre o tejidos, sin drenaje quirúrgico, puede ser un tratamiento adecuado para la EAS en ausencia de síntomas neurológicos. Sin embargo, puede ser necesaria una intervención quirúrgica inmediata (laminectomía descompresiva, desbridamiento del tejido infectado y drenaje del absceso), según la presentación clínica. Lo más probable es que se deba a un retraso en el diagnóstico oa un diagnóstico erróneo inicial, la morbilidad asociada con la EAE sigue siendo alta, del 33 % al 47 %, mientras que se estima que la mortalidad es del 5 %. El estado neurológico antes de la intervención es el predictor más fuerte del resultado final. También existe una fuerte asociación entre mala evolución y edad mayor de 70 años, infección por cepa MRSA y presencia de DM o insuficiencia suprarrenal.
El riesgo y las secuelas a largo plazo de la EAS pueden reducirse con una selección cuidadosa de los pacientes, el mantenimiento de técnicas estériles estrictas durante el inicio de los procedimientos epidurales, la administración de antibióticos antes del inicio del bloqueo neuroaxial en pacientes con fiebre o infección localizada, la extracción de catéteres permanentes ante el signo más temprano de infección en el sitio de punción, y el mantenimiento de un alto índice de sospecha en pacientes con factores de riesgo que presentan síntomas neurológicos inespecíficos o signos de infección locales y sistémicos, posiblemente varias semanas después de un procedimiento epidural.
Meningitis
La meningitis bacteriana después de la anestesia epidural es un evento raro. Los microorganismos pueden transmitirse a través de jeringas, catéteres, agujas, tubos de infusión y medicamentos inyectados en el espacio epidural, así como del médico o del paciente. Pueden ocurrir complicaciones infecciosas similares con procedimientos no anestésicos, como EBP, mielografía, inyección epidural de esteroides y punción lumbar diagnóstica. La mayoría de los casos parecen ser causados por la contaminación del sitio de punción por organismos de la naso u orofaringe del proveedor de atención médica. Con menos frecuencia, están implicados los contaminantes de la piel esterilizada de manera incompleta y la diseminación directa o hematógena desde un sitio infeccioso endógeno. Se cree que una punción dural, como en el contexto de una CSE, espinal o ADP, coloca a los pacientes en mayor riesgo al permitir la transferencia de patógenos transmitidos por la sangre a través de la barrera hematoencefálica. Sin embargo, la incidencia de meningitis bacteriana sigue siendo baja a pesar del uso creciente de CSE y técnicas espinales. Además, la punción lumbar diagnóstica en el contexto de la bacteriemia rara vez se asocia con meningitis. Los factores de riesgo adicionales incluyen fallas en la técnica aséptica, reinserción del estilete que ha estado expuesto al aire ambiente, dificultad para realizar el procedimiento neuroaxial y, relacionados, múltiples intentos de colocación espinal o epidural.
Los signos y síntomas de la meningitis incluyen fiebre, dolor de cabeza, letargo, confusión, rigidez de nuca, náuseas/vómitos, fotofobia y signo de Kernig.Tabla 37).
TABLA 37. Signos y síntomas de la meningitis bacteriana.
| Fiebre |
| Cambios en el estado mental (letargo, confusión) |
| Dolor de cabeza |
| Rigidez de nuca |
| Náuseas, vómitos |
| Dolor de espalda |
| Fotofobia |
| Convulsiones |
| Déficits neurológicos focales |
| Signo de Kernig |
| Signo de Brudzinski |
Los síntomas generalmente se presentan dentro de las 6 a 36 horas posteriores al procedimiento anestésico. Debido a que la presentación clínica inicial es similar a la de una CPPD, el diagnóstico de meningitis puede retrasarse. La meningitis se puede distinguir de la CPPD por la presencia de fiebre, cambios en el estado mental (es decir, letargo y confusión) y un dolor de cabeza que no es de naturaleza posicional. El diagnóstico se confirma con análisis y cultivo del LCR con o sin TC de cráneo previa. El LCR suele estar turbio, con leucocitosis (predominantemente neutrófilos), contenido elevado de proteínas y concentración baja de glucosa. El diagnóstico precoz es fundamental. Los patógenos comunes incluyen Streptococcus salivarius y otras cepas de estreptococos viridans, S. aureus, P. aeruginosa, Neisseria meningitidis y Enterococcus faecalis. En muchos casos, no se aísla ningún organismo. El tratamiento de la meningitis bacteriana incluye terapia empírica inmediata con antibióticos de amplio espectro, como vancomicina con una cefalosporina de tercera generación, en última instancia adaptada a los resultados del cultivo de sangre o LCR. Las secuelas neurológicas pueden incluir parálisis de nervios craneales, hemiparesia, cuadriparesia y afasia. Si el diagnóstico y el tratamiento se retrasan, puede producirse la muerte. El cumplimiento de todas las precauciones asépticas, incluida la eliminación de las joyas, el lavado de manos, la preparación adecuada de la piel con paquetes individuales de solución antiséptica (preferiblemente clorhexidina con alcohol), el uso de paños y apósitos estériles y, como mínimo, el uso de gorros. guantes estériles y máscaras faciales (cambiadas entre cada contacto con el paciente), es fundamental para minimizar el riesgo de meningitis bacteriana asociada con la instrumentación neuroaxial. Deben ofrecerse alternativas a las técnicas neuroaxiales a los pacientes con alto riesgo de complicaciones infecciosas, y los pacientes con bacteriemia conocida o sospechada deben comenzar una terapia con antibióticos antes de la instrumentación neuroaxial.
Lesión de la médula espinal y la raíz nerviosa
Los déficits neurológicos pueden ser causados por un traumatismo directo en la médula espinal o los nervios espinales, por isquemia de la médula espinal, por inyección accidental de fármacos o sustancias químicas neurotóxicas, o por hematomas o abscesos. Afortunadamente, la lesión neurológica grave es una complicación extremadamente rara de la anestesia neuroaxial, con una incidencia estimada de 0.03 a 0.1%. Horlocker y sus colegas evaluaron los registros de más de 4000 pacientes que habían recibido epidurales lumbares para cirugía torácica mientras estaban bajo AG y no encontraron casos de complicaciones neurológicas. En otra revisión extensa de 45,000 40 pacientes sometidos a colocación epidural, se informaron 22 casos de lesiones neurológicas. Cabe destacar que XNUMX de estos pacientes experimentaron parestesias durante el procedimiento epidural. Ha habido algunos informes de casos de mielopatía y paraplejía que ocurren con epidurales torácicos colocados en pacientes anestesiados, pero estas complicaciones son extremadamente raras. La mayoría de las neuropatías periféricas asociadas con las técnicas neuroaxiales se resuelven espontáneamente. Las que se vuelven permanentes suelen limitarse a parestesias persistentes y debilidad motora limitada.
Síndrome de cauda equina
El síndrome de cauda equina (CES), un estado raro de compromiso neurológico debido a la compresión de la raíz lumbosacra, se caracteriza por disfunción intestinal y de la vejiga, dolor lumbar, pérdida sensorial perineal y otros déficits sensoriales en parches, ciática unilateral o bilateral y trastornos motores de las extremidades inferiores. debilidad. Se ha asociado con trauma, infección, posición de litotomía y compresión isquémica por hematoma, absceso, tumor, prolapso de disco intervertebral o espondilolistesis. CES también se ha relacionado con la neurotoxicidad directa de grandes volúmenes o altas concentraciones de AL hiperbárico en el LCR sacro. Las raíces nerviosas de la cauda equina tienen un epineuro poco desarrollado y un flujo sanguíneo limitado y parecen ser particularmente susceptibles a la acumulación de LA que puede acompañar a las infusiones espinales continuas con catéteres de microcalibre, inyección intratecal accidental de grandes dosis de LA destinados a la anestesia epidural, y repetir las inyecciones intratecales después de un bloqueo nervioso espinal fallido. También se han informado casos de CES después de espinales de un solo disparo.
Si la neurotoxicidad intrínseca de los LA, los factores microambientales, las dosis excesivamente grandes de los LA, el catéter de microcalibre utilizado para la anestesia espinal continua, el posicionamiento del paciente, el procedimiento quirúrgico o una combinación de estos factores son los principales responsables del CES, no se ha dilucidado completamente en la literatura. . La Administración de Drogas y Alimentos de EE. UU. (FDA) retiró del mercado los catéteres espinales continuos de pequeño calibre a principios de la década de 1990 después de una serie de informes de CES en relación con su uso. Sin embargo, la anestesia espinal continua sigue siendo una técnica útil. El uso de concentraciones más bajas de LA, la limitación de la dosis total de LA, la limitación de la profundidad de inserción del catéter espinal y el uso de maniobras para aumentar la propagación de LA si se sospecha una mala distribución pueden minimizar el riesgo de CES. Algunos investigadores también han abogado por el uso de alternativas a la lidocaína hiperbárica al 5% dado que existen alternativas seguras. Desafortunadamente, CES es una discapacidad permanente.
Los síntomas consistentes con este síndrome deben impulsar una consulta temprana de neurología y estudios de imagen. corticosteroides en dosis altas; descompresión quirúrgica (p. ej., en el caso de un quiste sinovial lumbar, hemangioma o tumores metastásicos); y el tratamiento del trastorno subyacente con agentes quimioterapéuticos o antibióticos (p. ej., en el caso de malignidad o formación de abscesos), pero hay datos limitados disponibles sobre las terapias óptimas y el curso de la recuperación.
Hematoma epidural
El hematoma epidural es una ocurrencia rara que puede conducir a la compresión del cordón umbilical, isquemia del cordón umbilical o mielopatía similar a la causada por un tumor que ocupa espacio. La incidencia de hematoma asociado con el bloqueo epidural se estima en 1:150,000, algo mayor que la de los anestésicos espinales (1:220,000). Sin embargo, la incidencia varía drásticamente con la población de pacientes y puede ser significativamente mayor en un subconjunto de pacientes con un espacio epidural menos compatible y una mayor probabilidad de trastornos de la coagulación. De hecho, las anomalías hemostáticas durante el inicio del bloqueo epidural o la extracción del catéter epidural están presentes en la mayoría de los casos informados, aunque una gran proporción de los casos documentados también ocurren espontáneamente, sin factores predisponentes.
La colocación complicada de la aguja epidural o del catéter también parece poner al paciente en riesgo de formación de hematoma epidural. Los trastornos de la coagulación que predisponen a los pacientes al desarrollo de hematoma epidural pueden ser iatrogénicos o secundarios a una enfermedad subyacente. Los trastornos iatrogénicos que pueden predisponer a los pacientes a la formación de hematomas epidurales a menudo se asocian con la terapia antitrombótica o trombolítica. Las pautas más recientes de la Sociedad Estadounidense de Anestesia Regional y Medicina del Dolor se pueden usar para ayudar al anestesiólogo a determinar el período más apropiado y seguro para iniciar el bloqueo epidural en pacientes anticoagulados (ver Anestesia neuroaxial y bloqueos de nervios periféricos en pacientes con anticoagulantes).
La trombocitopenia es una causa relativamente común de coagulopatía y puede estar relacionada con el embarazo (trombocitopenia gestacional, síndrome HELLP o preeclampsia/eclampsia), trastornos inmunitarios (p. ej., ITP) o disfunción hepática, entre otras cosas. Desafortunadamente, no existe un recuento de plaquetas universalmente aceptado que pueda considerarse seguro para realizar el bloqueo neuroaxial, y no existe una prueba de cabecera ampliamente disponible para evaluar la función plaquetaria. Debe tenerse en cuenta la naturaleza del trastorno subyacente (p. ej., ¿el proceso es dinámico, con una caída rápida de las plaquetas? ¿La función plaquetaria está intacta a pesar de un número bajo? ¿El paciente recibe tratamiento antiplaquetario concomitante?
¿Tiene él o ella otro trastorno que afecte la coagulación? y así sucesivamente), y los pacientes con trombocitopenia deben abordarse con precaución antes de iniciar el bloqueo neuroaxial.
Los signos y síntomas del hematoma epidural pueden progresar rápidamente desde déficits sensoriales o motores leves hasta paraplejia e incontinencia devastadoras. Los primeros signos incluyen dolor de espalda y presión, con déficits motores y sensoriales. El dolor de espalda asociado con el hematoma epidural puede ser severo y persistente.
Se produce incontinencia intestinal y vesical, dolor radicular y empeoramiento de los déficits neurológicos de las extremidades inferiores. El inicio de los síntomas suele ocurrir entre 12 horas y 2 días después del inicio del bloqueo neuroaxial o la extracción de un catéter epidural. Desafortunadamente, los déficits motores y sensoriales dentro de este período de tiempo pueden confundirse con un bloqueo epidural residual. La recurrencia del bloqueo motor y sensitivo después de la resolución parcial o total o, alternativamente, el bloqueo nervioso prolongado debe plantear la preocupación de un hematoma epidural y la consulta inmediata con un neurólogo o neurocirujano, así como una resonancia magnética inmediata. Una resonancia magnética negativa no puede descartar un hematoma en desarrollo, que puede no ser reconocido por un radiólogo sin experiencia. Se recomienda la descompresión quirúrgica dentro de las 8 horas para minimizar el riesgo de lesión neurológica permanente.
Síndrome de la arteria espinal anterior
El síndrome de la arteria espinal anterior (ASAS) ocurre más comúnmente en pacientes con enfermedad vascular y disminución concomitante del flujo sanguíneo espinal debido a obstrucción, compresión o hipotensión. Sin embargo, también se ha descrito en el contexto de hernia discal torácica aguda, espondilosis, malformación arteriovenosa y condiciones patológicas similares que pueden interrumpir el tenue flujo sanguíneo en la distribución de la arteria espinal anterior. ASAS es la complicación neurológica más común después de la cirugía aórtica abdominal, pero también se ha informado después de la cirugía en la columna torácica. La pérdida masiva de sangre y la hipotensión persistente inducida por la anestesia neuroaxial se han implicado en el desarrollo intraoperatorio de este síndrome potencialmente mortal. ASAS se presenta con paraplejía indolora inmediata y pérdida de la función sensorial de las extremidades inferiores. Se respetan la propiocepción y el sentido de la vibración. El pronóstico es malo, con déficits neurológicos permanentes e incapacitantes. La corrección de la hipotensión intraoperatoria es esencial en pacientes con alto riesgo de ASAS.
Paro cardíaco
El paro cardíaco que resulta en muerte o daño cerebral es una complicación rara del bloqueo epidural. Las causas incluyen anestesia espinal total no intencional, LAST, isquemia miocárdica, compromiso respiratorio o cualquiera de varios eventos circulatorios que no caen dentro de estas categorías, como bloqueo completo de las fibras aceleradoras cardíacas preganglionares o predominio vagal en el contexto de bloqueo simpático. Aunque el mecanismo del aumento del tono vagal no se ha esclarecido por completo, el bloqueo de las vías eferentes simpáticas produce vasodilatación y disminución del retorno venoso. La precarga disminuida, a su vez, puede aumentar el tono vagal cardíaco. Pueden producirse bradicardia, CO reducido y paro cardiaco, y pueden atribuirse en parte a la actividad refleja. El reflejo paradójico de Bezold-Jarisch, por ejemplo, desencadena la desaceleración de la frecuencia cardíaca en respuesta a la disminución del volumen ventricular para permitir más tiempo para el llenado completo del corazón.
Para minimizar el riesgo de paro cardíaco asociado con el predominio vagal después de los procedimientos neuroaxiales, Pollard y colegas propusieron el mantenimiento de una precarga adecuada, el uso de fármacos vagolíticos y agentes presores, si es necesario, la selección adecuada del paciente y la precaución al cambiar la posición del paciente. Se recomienda la administración temprana de epinefrina si la bradicardia es marcada. La vasopresina puede ser más eficaz que la epinefrina para la reanimación cardiopulmonar durante la anestesia epidural debido a su efecto más duradero y al mejor perfil ácido-base después de múltiples dosis, aunque se recomienda el cumplimiento del protocolo de soporte vital cardiovascular avanzado (ACLS, por sus siglas en inglés) más actual. Los factores de riesgo de paro cardíaco relacionados con el paciente después de la anestesia neuroaxial incluyen el sexo masculino, el estado físico ASA I, una frecuencia cardíaca basal baja (por debajo de 60), un nivel sensorial superior a T6, una edad inferior a 50, el uso de bloqueadores β-adrenérgicos y intervalo PR prolongado. El inicio rápido de la acción de los AL, el uso de AL que causan un bloqueo nervioso simpático más profundo y una extensión más amplia del bloqueo nervioso también se han asociado con hipotensión y bradicardia después del bloqueo epidural. Ligouri y sus colegas identificaron los siguientes factores secundarios que pueden precipitar o contribuir a la gravedad del aumento del tono vagal asociado con bradicardia y asistolia durante la anestesia epidural: administración de opioides, hipoxemia, sedación, hipercarbia, uso crónico de medicamentos y enfermedad médica coexistente.
Efectos secundarios
Varios efectos secundarios comunes acompañan a los procedimientos epidurales, que incluyen fiebre transitoria en pacientes obstétricas, náuseas y vómitos, prurito asociado con opioides neuroaxiales, escalofríos y retención urinaria. Numerosos estudios han encontrado una asociación entre la analgesia epidural durante el trabajo de parto y la fiebre intraparto materna de nueva aparición, aunque la relación puede no ser causal. El aumento de la temperatura materna suele ser subclínico y autolimitado y no parece tener un efecto adverso sobre el feto.
Las náuseas y los vómitos son comunes después de la AG y el bloqueo neuroaxial. En el contexto de la anestesia y la analgesia epidurales, las náuseas y los vómitos pueden atribuirse a la hipotensión o a los adyuvantes epidurales, como los opioides. Los opioides lipofílicos, como el fentanilo y el sufentanilo, administrados por vía epidural parecen reducir el riesgo de náuseas y vómitos en comparación con la morfina epidural. Se recomienda la administración de ondansetrón intravenoso (posiblemente en combinación con otros agentes antieméticos), oxígeno suplementario y ansiolíticos, así como la pronta corrección de la hipotensión y la hipovolemia, en el enfoque multimodal de la terapia. La dexametasona intravenosa también parece ser eficaz para reducir las náuseas y los vómitos asociados con la morfina epidural. La efedrina, que se cree que tiene efectos antieméticos no relacionados con sus efectos hemodinámicos, los antihistamínicos y los anticolinérgicos también son prometedores.
El prurito, un efecto secundario común de los opioides neuroaxiales, se observa con más frecuencia durante las espinales que en las epidurales. Por lo general, es transitorio y afecta más comúnmente a la nariz y otras áreas de la cara. El antagonista opioide puro naloxona revierte eficazmente el prurito inducido por opioides, pero a costa de revertir la analgesia. El agonista-antagonista parcial nalbufina parece ser el tratamiento más eficaz del prurito inducido por opioides. Una sola dosis de 5 mg suele ser suficiente; en ocasiones es necesaria una segunda dosis de 5 mg. Los antihistamínicos son ineficaces; el prurito inducido por opioides no es una reacción mediada por histamina.
Los escalofríos son otro efecto secundario común de la analgesia y la anestesia neuroaxiales, que ocurren más rápidamente y con mayor intensidad en la anestesia raquídea que en la epidural. El mecanismo sigue sin estar claro, pero puede estar relacionado en parte con el deterioro del control termorregulador central y la redistribución del calor corporal.
La hipotensión, definida por una reducción de más del 20% en la presión arterial sistólica, diastólica o media, es común después del bloqueo epidural. Los bloqueos nerviosos torácicos altos, la obesidad, la anestesia general y neuroaxial concurrentes, la hipovolemia y la pérdida excesiva de sangre intraoperatoria se encuentran entre los factores de riesgo. Los pacientes pueden presentar náuseas, vómitos, mareos, cambios en el estado mental, dificultad para respirar, dificultad para respirar y arritmias cardíacas. El colapso cardiovascular puede acompañar a los casos graves. Óptimamente, la presión arterial debe mantenerse dentro del 20% de la línea de base en reposo del paciente. Los métodos propuestos para reducir la incidencia de hipotensión después del bloqueo neuroaxial incluyen la administración juiciosa de vasopresores (más comúnmente, efedrina o fenilefrina); expansión de volumen con una solución cristaloide o coloide en el momento de iniciar el bloqueo nervioso (es decir, una cocarga); mantenimiento del desplazamiento uterino izquierdo después de las 18 a 20 semanas de gestación en pacientes obstétricas; cambiar la posición del paciente (p. ej., de supino a sentado) gradualmente; colocar el bloqueo nervioso en un segmento espinal inferior, cuando sea posible; titulación lenta de LA epidurales; y reduciendo la dosis de LA intratecal o epidural. En casos de hipotensión severa, la elevación de las extremidades inferiores o la colocación de un pantalón militar antichoque reducirá la acumulación venosa. También se deben considerar agentes presores adrenérgicos α y β alternativos, como la norepinefrina y la epinefrina. Se debe evitar colocar al paciente en Trendelenburg inverso en un intento de limitar la propagación de la AI; Trendelenburg servirá para aliviar la acumulación venosa en las extremidades inferiores y mejorar el flujo sanguíneo al corazón y al cerebro (Tabla 38). Muchas de estas medidas para reducir la incidencia y la gravedad de la hipotensión después del bloqueo neuroaxial siguen siendo objeto de debate en la literatura y están fuera del alcance de este capítulo.
TABLA 38. Tratamiento de la hipotensión después del bloqueo neuroaxial.
| Suspender la infusión epidural, si procede. |
| Expansión de volumen con administración de líquidos por vía intravenosa |
| Administración de vasopresores intravenosos (fenilefrina y/o efedrina) |
| Colocar al paciente en posición de Trendelenburg |
| Asegurar el desplazamiento uterino después de 18 a 20 semanas de gestación |
| Elevar las extremidades inferiores |
| Administrar atropina 0.4–0.5 mg IV con concurrente bradicardia |
| Envolver las piernas con medias disuasorias tromboembólicas/ manguera de compresión neumática; lugar militar antishock pantalones |
| Administración de norepinefrina o epinefrina según sea necesario |
RESUMEN
Tanto las indicaciones de las técnicas neuroaxiales como la población de pacientes que se considera adecuada para estos procedimientos se han ampliado en las últimas décadas. Actualmente se recomienda el bloqueo epidural como adyuvante de la AG para cirugías cardiotorácicas, vasculares mayores y otras cirugías de alto riesgo; como único anestésico en cirugías que antes se realizaban exclusivamente bajo AG; y para el manejo del dolor agudo y crónico. Las técnicas neuroaxiales también se utilizan cada vez más en el entorno ambulatorio, donde la disminución de las NVPO y el mejor alivio del dolor permiten un alta más temprana; para una variedad de procedimientos de diagnóstico; y para aliviar el dolor en adultos y niños al final de la vida.
Los beneficios del bloqueo epidural están bien establecidos. Las técnicas epidurales brindan un alivio óptimo del dolor después de cirugías mayores y se han asociado con menos complicaciones cardiovasculares, respiratorias, gastrointestinales y hematológicas en comparación con la AG. La incidencia de eventos tromboembólicos perioperatorios, el tiempo de recuperación de la función gastrointestinal y la duración de la estancia en cuidados intensivos, entre otras cosas, parecen reducirse con el bloqueo epidural. Además, la anestesia epidural se ha asociado con una supervivencia prolongada y una disminución de las tasas de recurrencia del cáncer en pacientes con cáncer de mama, colon localizado, próstata y ovario. Sin embargo, el papel potencial del bloqueo epidural en la reducción de la mortalidad después de una cirugía mayor aún se debate en la literatura.
A pesar de las muchas ventajas potenciales del bloqueo epidural, las técnicas neuroaxiales no están exentas de riesgos, aunque las complicaciones importantes son raras. Se justifica un análisis de riesgo-beneficio caso por caso y el consentimiento informado del paciente antes de iniciar el bloqueo epidural.
Este texto es una muestra del contenido de la Compendio de Anestesia Regional en NYSORA LMS.
de NYSORA Compendio de Anestesia Regional es simplemente el plan de estudios más completo y práctico sobre anestesia regional de la A a la Z, que presenta el contenido Premium de NYSORA. A diferencia de los libros de texto y los libros electrónicos, el Compendio se actualiza continuamente y presenta los videos, animaciones y contenido visual más nuevos de NYSORA.
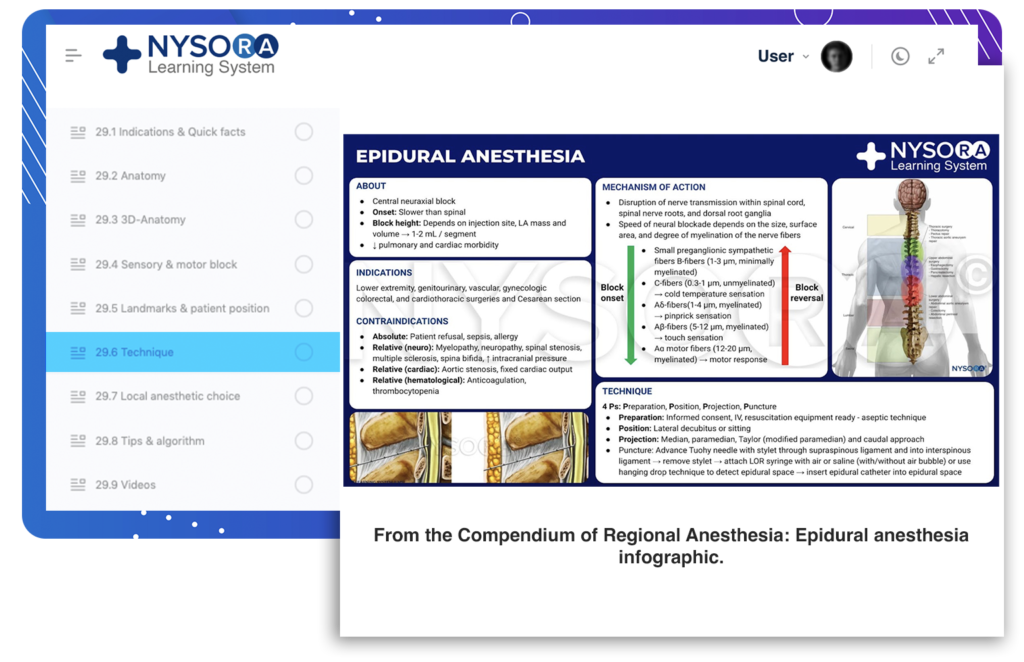
El Compendio es uno de varios cursos educativos estándar de oro sobre el Sistema de aprendizaje de NYSORA (NYSORA LMS), y la inscripción para NYSORALMS.com está libre. Sin embargo, el acceso COMPLETO al Compendio se basa en una suscripción anual, ya que requiere un ejército de ilustradores, editores de video y un equipo educativo para continuar convirtiéndolo en la MEJOR herramienta para la educación en todo lo relacionado con la anestesia regional. Si bien puede pensar en el compendio como un libro electrónico sobre esteroides, una prueba rápida le dará una idea en tiempo real de lo increíble que es realmente el Compendio. Su suscripción transformará la forma en que lee sobre la anestesia regional:
- Aprenda visualmente: todo lo regional, incluidos los procedimientos de bloqueo espinal, epidural y nervioso y los protocolos de manejo
- Revise las instrucciones de técnicas paso a paso para más de 60 bloqueos nerviosos
- Acceda a las ilustraciones, animaciones y videos legendarios de NYSORA (como Reverse Ultrasound Anatomy)
- Acceda a la información de RA en cualquier dispositivo a través de la plataforma de escritorio y la aplicación móvil
- Obtenga actualizaciones en tiempo real
- Revise las infografías para la preparación del examen (por ejemplo, EDRA)
- Use el feed de la comunidad con discusiones de casos reales, imágenes y videos publicados y discutidos por suscriptores y los mejores expertos del mundo por igual.
Incluso si no desea suscribirse al Compendio, regístrese en el LMS NYSORA, sea el primero en saber qué hay de nuevo en anestesia regional y participe en discusiones de casos.
Esto es de lo que se alimenta la actividad LMS NYSORA parece:
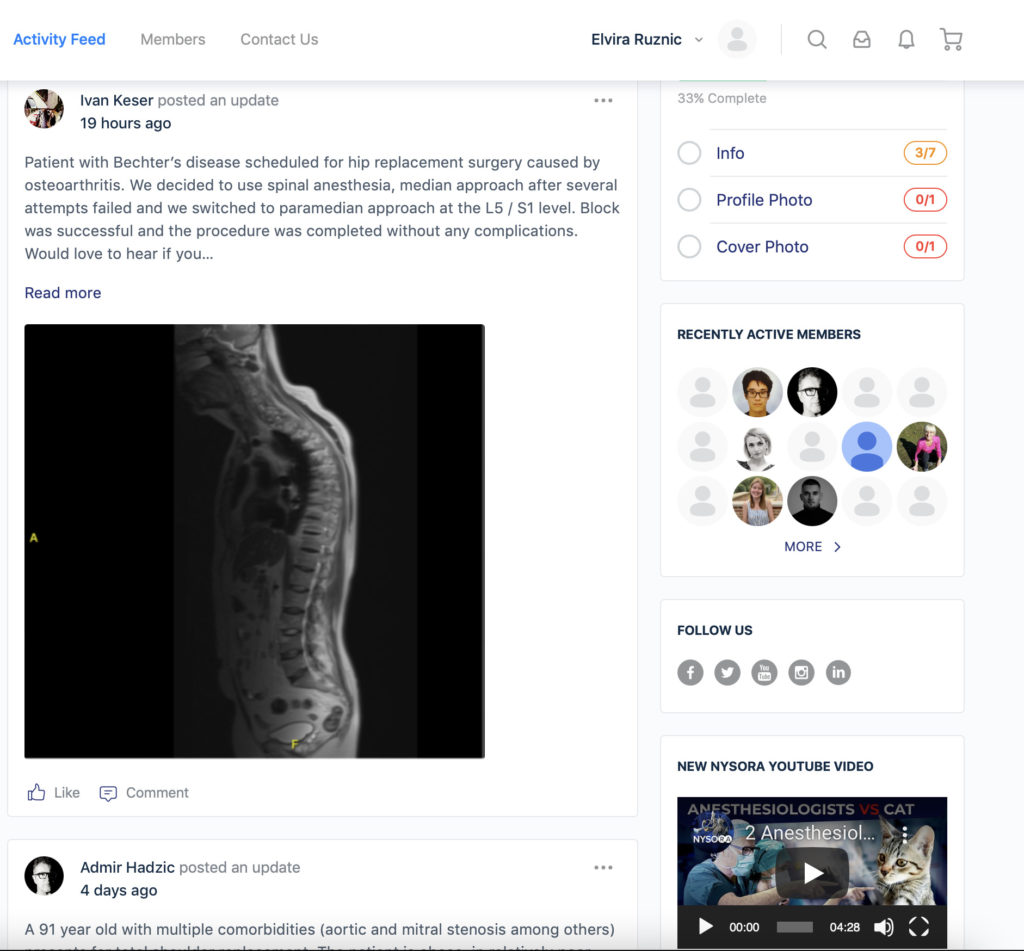
Estamos convencidos que una vez que experimentas la Compendio en LMS NYSORA, y nunca volverá a sus libros antiguos, y su suscripción ayudará a mantener NYSORA.com gratis para el resto del mundo.
Lectura adicional
- Frölich MA, Caton D: Pioneros en el diseño de agujas epidurales. Anesth Analg 2001;93:215–220.
- Cortés RC: Anestesia epidural lumbar, 1931-1936: un segundo debut. Rev Esp Anestesiol Reanim 2005;52:159–168.
- Dogliotti AM: Anestesia espinal peridural segmentaria: un nuevo método de bloqueo nervioso. Am J Surg 1933; 20:107–118.
- Curbelo MM: Anestesia segmentaria peridural continua mediante catéter ureteral. Curr Res Anesth Analg 1949; 28: 13–23.
- Modig J, Borg T, Karlström G, et al: tromboembolismo después del reemplazo total de cadera: papel de la anestesia epidural y general. Anesth Analg 1983;62:174–180.
- Jørgensen LN, Rasmussen LS, Nielsen P, et al: eficacia antitrombótica de la analgesia extradural continua después del reemplazo de rodilla. Hermano J Anaesth 1991;66:8–12.
- Rodgers A, Walker N, Schug S, et al: Reducción de la mortalidad y morbilidad postoperatorias con anestesia epidural o espinal: resultados de la descripción general de ensayos aleatorios. BMJ 2000;321:1–12.
- Mauermann WJ, Shilling AM, Zuo Z: Una comparación del bloqueo del nervio neuroaxial versus la anestesia general para el reemplazo total de cadera electivo: un metanálisis. Anesth Analg 2006;103:1018–1025.
- Schindler I: Anestesia regional en el anciano: Indicaciones y contraindicaciones. Acta Anaesthesiol Scand Suppl 1997;111:209–211.
- Cherng CH, Wong CS, Chang FL, et al: La morfina epidural retrasa la aparición del dolor del torniquete durante la anestesia epidural con lidocaína. Anesth Analg 2002;94:1614–1616.
- Christopherson R, Beattie C, Frank SM, et al: Morbilidad perioperatoria en pacientes asignados al azar a anestesia epidural o general para cirugía vascular de las extremidades inferiores. Anestesiología 1993;79:422–434.
- Sproviero M: Anestesia neuroaxial para procedimientos genitourinarios en adultos. En Wong CA (ed): Anestesia espinal y epidural. McGraw-Hill, 2007, págs. 229–236.
- Soriano D, Ajaj S, Chuong T, et al: aerosol de lidocaína e histeroscopia ambulatoria: ensayo aleatorizado controlado con placebo. Obstet Gynecol 2000;96:661–664.
- Goldenberg M, Cohen SB, Etchin A, et al: Un estudio comparativo prospectivo aleatorizado de anestesia general versus epidural para la resección endometrial histeroscópica transcervical. Am J Obstet Gynecol 2001;184: 273–276.
- Murphy M, Heit MH, Fouts L, et al. Efecto de la anestesia sobre la función miccional después del procedimiento de cinta vaginal sin tensión. Obstet Gynecol 2003; 101:666–670.
- Nerve Block BM, Liu SS, Rowlingson AJ, et al: Eficacia de la analgesia epidural posoperatoria: un metanálisis. JAMA 2003;290:2455–2463.
- Ballantyne JC, Carr DB, deFerranti S, et al: Los efectos comparativos de
terapias analgésicas posoperatorias sobre el resultado pulmonar: metanálisis acumulativos de ensayos controlados aleatorios. Anesth Analg 1998;86: 598–612. - Liu SS, Wu CL: Efecto de la analgesia posoperatoria en los principales
complicaciones: Una actualización sistémica de la evidencia. Anesth Analg 2007;104:689–702. - Manion SC, Brennan TJ: Analgesia epidural torácica y manejo del dolor agudo. Anestesiología 2011;115:181–188.
- Nygård E, Kofoed KF, Freiburg J, et al: Efectos de la analgesia epidural torácica alta sobre el flujo sanguíneo miocárdico en pacientes con cardiopatía isquémica. Circulación 2005; 111: 2165–2170.
- Scott NB, Turfrey DJ, Ray DA, et al: Un estudio prospectivo aleatorizado de los posibles beneficios de la anestesia epidural torácica y la analgesia en pacientes
sometidos a un injerto de derivación de la arteria coronaria. Anesth Analg 2001;93:
528-535. - Loick HM, Schmidt C, Van Aken, et al: La anestesia epidural torácica alta, pero no la clonidina, atenúa la respuesta de estrés perioperatorio a través de la simpatolisis y reduce la liberación de troponina T en pacientes que se someten a un injerto de derivación de la arteria coronaria. Anesth Analg 1999;88:701–709.
- Liu SS, Nerve Block BM, Wu CL: Efectos de la analgesia neuroaxial central perioperatoria en el resultado después de una cirugía de derivación de la arteria coronaria: un metanálisis. Anestesiología 2004;101:153–161.
- Svircevic V, Nierich AP, Moons KG, et al: anestesia epidural torácica para cirugía cardíaca: un ensayo aleatorizado. Anestesiología 2011;114:
262-270. - Caputo M, Alwair H, Rogers CA, et al: La anestesia epidural torácica mejora los resultados tempranos en pacientes que se someten a una cirugía de derivación de la arteria coronaria sin circulación extracorpórea: un ensayo prospectivo, aleatorizado y controlado. Anestesiología 2011;114:380–390.
- Møiniche S, Kehlet H, Dahl JB: Una revisión sistemática cualitativa y cuantitativa de la analgesia preventiva para el alivio del dolor posoperatorio: El papel del momento de la analgesia. Anestesiología 2002;96:725–741.
- Groeben H, Schäfer B, Pavlakovic G, et al: Función pulmonar bajo anestesia epidural segmentaria torácica alta con ropivacaína o bupivacaína en pacientes con enfermedad pulmonar obstructiva grave que se someten a cirugía mamaria. Anestesiología 2002;96:536–541.
- Diaz N, Wong CA: Anestesia neuroaxial para cirugía general. En Wong CA (ed): Anestesia espinal y epidural. McGraw-Hill, 2007, págs. 221–227.
- Matot I, Scheinin O, Eid A, et al: anestesia epidural y analgesia en la resección hepática. Anesth Analg 2002;95:1179–1181.
- Zhang HW, Chen YJ, Cao MH, et al: colecistectomía laparoscópica bajo anestesia epidural: una comparación retrospectiva de 100 pacientes. Am Surg 2012;78:107–110.
- Asakura K, Nakazawa K, Tanaka N, et al. Caso de paro cardíaco debido a
espasmo coronario durante la gastrectomía distal laparoscópica. Masui 2011; 60:75–79. - Shir Y, Raja SN, Frank SM, et al: Pérdida de sangre intraoperatoria durante la prostatectomía radical retropúbica. Anestesia epidural versus anestesia general. Urología 1995;45:993–999.
- Gottschalk A, Smith DS, Jobes DR, et al: analgesia epidural preventiva y recuperación de la prostatectomía radical: un ensayo controlado aleatorio. JAMA 1998;279:1076–1082.
- Stevens RA, Mikat-Stevens M, Flanigan R, et al: ¿La elección de la técnica anestésica afecta la recuperación de la función intestinal después de la prostatectomía radical? Urología 1998;52:213–218.
- Ozyuvaci E, Altan A, Karadeniz T, et al: Anestesia general versus anestesia epidural y general en la cistectomía radical. Urol Int 2005;74: 62–67.
- Micali S, Jarrett TW, Pappa P, et al: Eficacia de la anestesia epidural para biopsia renal retroperitoneoscópica. Urología 2000;55:590.
- Richards JT, Read JR, Chambers WA. La anestesia epidural como método de analgesia preventiva para la histerectomía abdominal. Anestesia 1998;53:296–298.
- Mihic DN, Abram SE: Anestesia regional óptima para la histerectomía abdominal: Bloqueo combinado de los nervios subaracnoideo y epidural en comparación con otras técnicas regionales. Eur J Anesthesiol 1993;10:
297-301. - Holte K, Kehlet H: Analgesia epidural y riesgo de fuga anastomótica. Reg Anesth Pain Med 2001;26:111.
- Kehlet H, Mogensen T: Estancia hospitalaria de 2 días después de una sigmoidectomía abierta con un programa de rehabilitación multimodal. Br J Surg 1999;86: 227–230.
- Bardram L, Funch-Jensen P, Kehlet H: Rehabilitación rápida en pacientes de edad avanzada después de una resección colónica laparoscópica. Br J Surg 2000;87: 1540–1545.
- Blichfeldt-Lauridsen L, Hansen BD: Anestesia y miastenia gravis. Acta Anaesthesiol Scand 2012;56:17–22.
- Kirsh JR, Diringer MN, Borel CO, et al: La morfina epidural lumbar preoperatoria mejora la analgesia posoperatoria y la función ventilatoria después de la timectomía transesternal en pacientes con miastenia grave. Crit Care Med 1991;19:1474–1479.
- Bagshaw O: una combinación de anestesia intravenosa total y epidural torácica para la timectomía en la miastenia gravis juvenil. Pediatr Anaesth 2007;17:370–374.
- Hambly PR, Martin B: Anestesia para lesiones crónicas de la médula espinal. Anestesia 1998;53:273–289.
- Lambert DH, Deane RS, Mazuzan JE: Anestesia y control de la presión arterial en pacientes con lesión de la médula espinal. Anesth Analg 1982;61: 344–348.
- Ording H: Incidencia de hipertermia maligna en Dinamarca. Anesth Analg 1985;64:700–704.
- van Lier F, van der Geest PJ, Hoeks SE, et al: La analgesia epidural se asocia con mejores resultados de salud de pacientes quirúrgicos con enfermedad pulmonar obstructiva crónica. Anestesiología 2011;115:315–321.
- Mulroy MF, Salinas FV: Técnicas neuroaxiales para anestesia ambulatoria. Int Anesthesiol Clin 2005;43:129–141.
- Anghelescu DL, Faughnan LG, Baker JN, et al: Uso de bloqueos nerviosos epidurales y periféricos al final de la vida en niños y adultos jóvenes con cáncer: la colaboración entre un servicio de dolor y un servicio de cuidados paliativos. Pediatr Anaesth 2010;20:1070–1077.
- Sielenkämper AW, Van Aken H: Analgesia epidural en sepsis: Demasiado pronto para juzgar un nuevo concepto. Cuidados Intensivos Med 2004;30:1987–1989.
- Strümper D, Louwen F, Durieux ME, et al: Anestésicos locales epidurales: ¿un nuevo tratamiento para el retraso del crecimiento fetal? Diagnóstico Fetal Ther 2005; 20:208–213.
- Hong JY, Lim KT: Efecto de la analgesia epidural preventiva sobre la respuesta de las citocinas y el dolor posoperatorio en la histerectomía radical laparoscópica por cáncer de cuello uterino. Reg Anesth Pain Med 2008;33:44–51.
- Exadaktylos AK, Buggy DJ, Moriarty DC, et al: ¿Puede la técnica anestésica para la cirugía de cáncer de mama primario afectar la recurrencia o la metástasis? Anestesiología 2006;105:660–664.
- Biki B, Mascha E, Moriarty DC, et al. La técnica anestésica para la cirugía de prostatectomía radical afecta la recurrencia del cáncer: un análisis retrospectivo. Anestesiología 2008;109:180–187.
- Freise H, Van Aken H: Riesgos y beneficios de la anestesia epidural torácica. Hermano J Anaesth 2011;107:859–868.
- Mutz C, Vagts DA: Anestesia epidural torácica en sepsis: ¿es dañina o protectora? Cuidado crítico 2009;13:182.
- Su TM, Lan CM, Yang LC, et al: Tumor cerebral que se presenta con hernia fatal después del parto bajo anestesia epidural. Anestesiología 2002;96:508–509.
- Grocott HP, Mutch WA: Anestesia epidural y aumento agudo de la presión intracraneal: Hidrodinámica del espacio epidural lumbar en un modelo porcino. Anestesiología 1996;85:1086–1091.
- Leffert LR, Schwamm LH: Anestesia neuroaxial en parturientas con patología intracraneal: revisión integral y reevaluación del riesgo. Anestesiología 2013;119:703–718.
- Vandermeulen EP, Van Aken H, Vermylen J: anticoagulantes y anestesia espinal-epidural. Anesth Analg 1994;79:1165–1177.
- Horlocker TT, Wedel DJ, Rowlingson JC, et al: Anestesia regional en el paciente que recibe terapia antitrombótica o trombolítica: Directrices basadas en la evidencia de la Sociedad Estadounidense de Anestesia Regional y Medicina del Dolor (tercera edición). Reg Anesth Pain Med 2010;35:64–101.
- O'Rourke, N, Khan K, Hepner DL: Contraindicaciones para la anestesia neuroaxial. En Wong CA (ed): Anestesia espinal y epidural. McGraw-Hill, 2007, págs. 127–149.
- Choi S, Brull R: Técnicas neuroaxiales en pacientes obstétricas y no obstétricas con diátesis hemorrágica común. Anesth Analg 2009;109: 648–660.
- Bader AM, Hunt CO, Datta S, et al: Anestesia para la paciente obstétrica con esclerosis múltiple. J Clin Anesth 1988;1:21–24.
- Confavreux C, Hutchinson M, Hours MM, et al: Tasa de recaída relacionada con el embarazo en la esclerosis múltiple. Embarazo en el Grupo de Esclerosis Múltiple. N Engl J Med 1998;339:285–291.
- Hebl JR, Horlocker TT, Schroeder DR: Anestesia y analgesia neuroaxial en pacientes con trastornos preexistentes del sistema nervioso central. Anesth Analg 2006;103:223–228.
- Lirk P, Birmingham B, Hogan Q: Anestesia regional en pacientes con neuropatía preexistente. Int Anesthesiol Clin 2011;49:144–165.
- Wiertlewski S, Magot A, Drapier S, et al: Empeoramiento de los síntomas neurológicos después de la anestesia epidural para el trabajo de parto en una paciente de Guillain-Barré. Anesth Analg 2004;98:825–827.
- Toledano RD, Pian-Smith MC: Virus de la inmunodeficiencia humana: consideraciones y manejo maternos y fetales. En Suresh MS, Segal BS, Preston RL, et al (eds): Shnider and Levinson's Anesthesia for Obstetrics, 5th ed. Lippincott Williams & Wilkins, 2013, págs. 595–605.
- Crosby ET, Halpern SH, Rolbin SH: Anestesia epidural para la cesárea en pacientes con infecciones genitales recurrentes activas por herpes simple: una revisión retrospectiva. Can J Anaesth 1989;36:701–704.
- Bader AM, Camann WR, Datta S: Anestesia para parto por cesárea en pacientes con infecciones por el virus del herpes simple tipo 2. Reg Anesth 1990; 15:261–263.
- Brown NW, Parsons APR, Kam PCA: Consideraciones anestésicas en una parturienta con varicela que se presenta para cesárea. Anestesia 2003;58:1092–1095.
- Hebl JR, Horlocker TT, Kopp SL, et al: bloqueo neuroaxial en pacientes con estenosis espinal preexistente, enfermedad del disco lumbar o cirugía de columna previa: eficacia y complicaciones neurológicas. Anesth Analg 2010;111: 1511–1519.
- McDonald SB: ¿Está contraindicado el bloqueo neuroaxial en el paciente con estenosis aórtica? Reg Anesth Pain Med 2004;29:496–502.
- Ferguson EA, Paech MJ, Veltman MG: Miocardiopatía hipertrófica y cesárea: uso intraoperatorio de la ecocardiografía transtorácica. Int J Obstet Anesth 2006;15:311–316.
- Rosenquist RW, Birnbach DJ: Inserción epidural en adultos anestesiados: ¿Se lo agradecerán sus pacientes? Anesth Analg 2003;96:1545–1546.
- Horlocker TT, Abel MD, Messick JM, et al: Pequeño riesgo de complicaciones neurológicas graves relacionadas con la colocación del catéter epidural lumbar en pacientes anestesiados. Anesth Analg 2003;96:1547–1552.
- Han KR, Kim C, Park SK, et al: Distancia al espacio epidural cervical adulto. Reg Anesth Pain Med 2003;28:95–97.
- Stonelake PS, Burwell RG, Webb JK: Variación en los niveles vertebrales de la vértebra prominente y hoyuelos sacros en sujetos con escoliosis. J Anat 1988; 159: 165–172.
- Hughes RJ, Saifuddin A: Imágenes de vértebras de transición lumbosacras. Clin Radiol 2004;59:984–991.
- Kim JT, Bahk JH, Sung J: Influencia de la edad y el sexo en la posición del cono medular y la línea de Tuffier en adultos. Anestesiología 2003;99: 1359–1363.
- Saifuddin A, Burnett SJ, White J: La variación de la posición del cono medular en una población adulta. Un estudio de resonancia magnética. Columna vertebral 1998; 23: 1452–1456.
- Vandermeersch E, Kick O, Mollmann M, et al: CSE: la combinación de anestesia espinal y epidural. Reg Anaesth 1991; 14:108–112.
- Lirk P, Hogan Q: Anatomía espinal y epidural. En Wong CA (ed): Anestesia espinal y epidural. McGraw-Hill, 2007, 1–25.
- Lee AJ, Ranasinghe JS, Chehade JM, et al: Evaluación por ultrasonido del nivel vertebral de la línea intercristalina en el embarazo. Anesth Analg 2011;113:559–564.
- Van Gessel EF, Forster A, Gamulin Z: Anestesia espinal continua: ¿Adónde van los catéteres espinales? Anesth Analg 1993;76:1004–1007.
- Broadbent CR, Maxwell WB, Ferrie R, et al: Habilidad de los anestesistas para identificar un espacio intermedio lumbar marcado. Anestesia 2000;55: 1122–1126.
- Lirk P, Messner H, Deibl M, et al: Precisión en la estimación del nivel correcto del espacio intervertebral durante la anestesia lumbar, torácica y cervical. Acta Anaesthesiol Scand 2004;48:347–349.
- Hogan QH: Anatomía epidural lumbar. Una nueva mirada por sección criomicrótomo. Anestesiología 1991;75:767–775.
- Heylings DJ: ligamentos supraespinosos e interespinosos de la columna lumbar humana. J Anat 1978; 125: 127-131.
- Han KR, Kim C, Park SK, et al: Distancia al espacio epidural cervical adulto. Reg Anesth Pain Med 2003;28:95–97.
- Zarzur E: Estudios anatómicos del ligamento amarillo humano. Anesth Analg 1984;63:499–502.
- Williams DM, Gabrielsen TO, Latack JT, et al: Osificación en la unión cefálica del ligamento amarillo. Estudio anatómico y tomográfico. Radiología 1984; 150: 423–426.
- Brown DL: Anestesia espinal, epidural y caudal. En Miller RD, Fleisher LE, Johns RA, et al (eds): Miller's Anesthesia, 6th ed. Elsevier, 2005, págs. 1653–1683.
- Westbrook JL, Renowden SA, Carrie LE: Estudio de la anatomía de la región extradural mediante resonancia magnética. Br. J. Anaesth 1993; 71:495–498.
- Lirk P, Kolbitsch C, Putz G, et al: Ligamento torácico alto y cervical
flavum con frecuencia no se fusiona en la línea media. Anestesiología 2003;99: 1387–1390. - Lirk P, Colvin J, Steger B, et al: Incidencia del ligamento torácico inferior
lagunas de la línea media flavum. Hermano J Anaesth 2005;94:852–855. - Lirk P, Moriggl B, Colvin J, et al: La incidencia de brechas en la línea media del ligamento amarillo lumbar. Anesth Analg 2004;98:1178–1180.
- Reina MA, Villanueva MC, Machés F, et al: La ultraestructura del manguito de la raíz del nervio espinal humano en la columna lumbar. Anesth Analg 2008; 106:339–344.
- Bernards CM: Sofistería en medicina: Lecciones del espacio epidural.
Reg Anesth Pain Med 2005;30:56–66. - Reina MA, De León Casasola O, Villanueva MC, et al: Hallazgos ultraestructurales en la piamadre espinal humana en relación con la anestesia subaracnoidea. Anesth Analg 2004;98:1479–1485.
- Blomberg RG: El espacio extraarnoideo subdural lumbar de los humanos: un estudio anatómico utilizando espinacoscopia en casos de autopsia. Anesth Analg 1987;66:177–180.
- Haines DE: Sobre la cuestión de un espacio subdural. Rec. Anat 1991;230: 3–21.
- Boon JM, Abrahams PH, Meiring JH, et al: Punción lumbar: revisión anatómica de una habilidad clínica. Clin Anat 2004; 17:544–553.
- Hogan QH: Anatomía epidural: Nuevas observaciones. Can J Anaesth 1998;45:R40–48.
- Bernards CM: Anestesia epidural. En Mulroy MF, Bernards CM, McDonald SB, et al (eds): A Practical Approach to Regional Anesthesia, 4th ed. Lippincott Williams & Wilkins, 2009, pág. 104.
- Igarashi T, Hirabayashi Y, Shimizu R, et al: La estructura extradural lumbar cambia con el aumento de la edad. Hermano J Anaesth 1997;78:149–152.
- Blomberg R: La banda de tejido conectivo dorsomedial en el espacio epidural lumbar de los humanos: un estudio anatómico mediante epiduroscopia en casos de autopsia. Anesth Analg 1986;65;747–752.
- Hogan QH, Toth J: Anatomía de los tejidos blandos del canal espinal. Reg Anesth Pain Med 1999;24;303–310.
- Hogan QH: Distribución de la solución en el espacio epidural: Examen por sección criomicrótomo. Reg Anesth Pain Med 2002;27:150–156.
- Fujinaka MK, Lawson EF, Schukteis G, Wallace MS: profundidad epidural cervical: correlación entre el ángulo de la aguja, la anatomía cervical y el área de superficie corporal. Pain Med 2012;13:665–669.
- Aldrete JA, Mushin AU, Zapata JC, et al: Distancias de la piel al espacio epidural cervical según la lectura de películas de resonancia magnética: Consideración de la "almohadilla jorobada". J Clin Anesth 1998;10:309–313.
- Segal S, Beach M, Eappen S: Un modelo multivariante para predecir la distancia desde la piel hasta el espacio epidural en una población obstétrica. Reg Anesth 1996; 21: 451–455.
- Sutton DN, Linter SP: Profundidad del espacio extradural y punción dural.
Anestesia 1991;46:97–98. - Reynolds AF, Roberts PA, Pollay M, et al: Anatomía cuantitativa de la
espacio epidural toracolumbar. Neurocirugía 1986;17:905–907. - Hogan QH: Anatomía epidural examinada por sección de criomicrotomo. Influencia de la edad, el nivel vertebral y la enfermedad. Reg Anesth 1996;21: 395–406.
- Toprak HI, Ozpolat Z, Ozturk E, et al: La bupivacaína hiperbárica afecta las dosis de midazolam requeridas para la sedación después de la anestesia espinal. Eur J Anaesthesiol 2005;22:904–906.
- Shono A, Sakura S, Saito Y, et al: Comparación de anestesia epidural con lidocaína al 1% y al 2% combinada con anestesia general con sevoflurano utilizando un índice biespectral constante. Hermano J Anaesth 2003;91:825–829.
- Koo M, Sabaté A, Dalmau A, et al: Requisitos de sevoflurano durante la cirugía coloproctológica: diferencia entre dos regímenes epidurales diferentes. J Clin Anesth 2003;15:97–102.
- Eappen S, Kissin I: Efecto del bloqueo del nervio subaracnoideo con bupivacaína sobre los requisitos anestésicos para tiopental en ratas. Anestesiología 1998;88: 1036–1042.
- Tverskoy M, Shagal M, Finger J, et al: El bloqueo subaracnoideo de bupivacaína disminuye los requisitos hipnóticos de midazolam y tiopental. J Clin Anesth 1994;6:487–490.
- Tverskoy M, Shifrin V, Finger J, et al: Efecto del bloqueo nervioso epidural de bupivacaína en los requisitos hipnóticos de midazolam. Reg Anesth 1996;21: 209–213.
- Hodgson PS, Liu SS, Gras TW: ¿La anestesia epidural tiene efectos anestésicos generales? Un ensayo prospectivo, aleatorizado, doble ciego, controlado con placebo. Anestesiología 1999;91:1687–1692.
- Reinoso-Barbero F, Martínez-García E, Hernández-Gancedo MC, et al: Efecto de la bupivacaína epidural sobre los requerimientos de mantenimiento de sevoflurano evaluados por índice biespectral en niños. Eur J Anaesthesiol 2006;23:460–464.
- Holte K, Foss NB, Svensén C, et al: Anestesia epidural, hipotensión y
Cambios en el volumen intravascular. Anestesiología 2004;100:281–286. - Meisner A, Rolf A, Van Aken H: Anestesia epidural torácica y el paciente con enfermedad cardíaca: beneficios, riesgos y controversias. Anesth Analg 1997;85, 517–528.
- Missant C, Claus P, Rex S, Wouters PF: Efectos diferenciales de la anestesia epidural lumbar y torácica sobre la respuesta hemodinámica al dolor agudo
sobrecarga de presión ventricular. Hermano J Anaesth 2010;104:143–149. - Buggy DJ, Doherty WL, Hart EM, Pallet EJ: Tensión de oxígeno en la herida posoperatoria con analgesia epidural o intravenosa: un ensayo clínico prospectivo, aleatorizado, simple ciego. Anestesiología 2002;97:952–958.
- Kabon B, Fleischmann E, Treschan T, et al: Anestesia epidural torácica
aumenta la oxigenación de los tejidos durante la cirugía abdominal mayor. Anesth Analg 2003;97:1812–1817. - Olausson K, Magnusdottir H, Lurje L, et al: Antiisquémico y antianginoso
efectos de la anestesia epidural torácica versus los de la terapia médica convencional en el tratamiento de la angina de pecho inestable refractaria grave. Circulación 1997;96:2178–2182. - Richter A, Cederholm I, Fredrikson M, et al: Efecto de la analgesia epidural torácica a largo plazo sobre la angina de pecho refractaria: una experiencia de 10 años. J Cardiothorac Vasc Anesth 2012;26:822–828.
- Rolf N, Van de Velde M, Wouters PF, et al: La anestesia epidural torácica mejora la recuperación funcional del aturdimiento miocárdico en perros conscientes. Anesth Analg 1996;83:935–940.
- Rolf N, Meissner A, Van Aken H, et al: Los efectos de la epidural torácica
anestesia en la recuperación funcional del aturdimiento miocárdico en perros anestesiados con propofol. Anesth Analg 1997;84:723–729. - Freise H, Van Aken HK: Riesgos y beneficios de la anestesia epidural torácica. Hermano J Anaesth 2011;107:859–868.
- Svircevic V, van Dijk D, Nierich AP, et al: Metanálisis de anestesia epidural torácica versus anestesia general para cirugía cardíaca. Anestesiología 2011;114:271–282.
- Gu WJ, Wei CY, Huang DQ, et al: Metanálisis de ensayos controlados aleatorios sobre la eficacia de la anestesia epidural torácica para prevenir la fibrilación auricular después de un injerto de derivación de arteria coronaria. BMC Cardiovasc Disord 2012;12:1–7.
- Freund FG, Bonica JJ, Ward RJ, et al: Reserva ventilatoria y nivel de bloqueo del nervio motor durante la anestesia espinal y epidural alta. Anestesiología 1967;28:834–837.
- Groeben H: Anestesia epidural y función pulmonar. J. Anesth 2006; 20:290–299.
- Lirk P, Hollmann MW: Resultado después de la anestesia regional: ponderación de riesgos y beneficios. Minerva Anestesiol 2014;80:610–618.
- Sielenkämper AW, Van Aken H: Anestesia epidural torácica: más que solo anestesia/analgesia. Anestesiología 2003;99:523–525.
- Brodner G, Van Aken H, Hertle L, et al: El manejo perioperatorio multimodal, que combina analgesia epidural torácica, movilización forzada y nutrición oral, reduce el estrés hormonal y metabólico y mejora la convalecencia después de una cirugía urológica mayor. Anesth Analg 2001;92:1594–1600.
- Frank SM, Beattie C, Christopherson R, et al: Anestesia epidural versus anestesia general, temperatura ambiente del quirófano y edad del paciente como predictores de hipotermia inadvertida. Anestesiología 1992;77: 252–257.
- Matsukawa T, Sessler DI, Christensen R, et al: flujo y distribución de calor
durante la anestesia epidural. Anestesiología 1995;83: 961–967. - Szmuk P, Ezri T, Sessler D, et al: La anestesia espinal acelera el recalentamiento posoperatorio activo. Anestesiología 1997;87:1050–1054.
- Backman SB: Anestesia regional: vasodilatación mediada por simpatectomía. Can J Anaesth 2009;56:702–703.
- Greene NM: Área de bloqueo nervioso diferencial en anestesia espinal con tetracaína hiperbárica. Anestesiología 1958; 19:45–50.
- Brull SJ, Greene NM: Zonas de bloqueo nervioso sensorial diferencial durante la anestesia extradural. Hermano J Anaesth 1991;66:651–655.
- Valley MA, Bourke DL, Hamil MP, et al: Evolución temporal del bloqueo simpático durante la anestesia epidural: estudios de flujometría con láser Doppler o perfusión regional de la piel. Anesth Analg 1993;76:289–294.
- Ginosar Y, Weiniger CF, Kurz V, et al: Vasodilatación mediada por simpatectomía: un estudio aleatorio de concentración de bupivacaína epidural. Can J Anaesth 2009;56:213–221.
- Bengsston M: Cambios en el flujo sanguíneo y la temperatura de la piel durante la analgesia espinal evaluados por flujometría láser Doppler y termografía infrarroja. Acta Anaesthesiol Scand 1984;28:625–630.
- Kimura T, Goda Y, Kemmotsu O, et al: diferencias regionales en el flujo sanguíneo y la temperatura de la piel durante la anestesia espinal total. Can J Anaesth 1992;39:123–127.
- Bromage PR, Joyal AC, Binney JC: Fármacos anestésicos locales: penetración desde el espacio extradural espinal hacia el neuroeje. Ciencia 1963; 140: 392–394.
- Moore D, Spierdijk J, VanKleef J, et al: Neurotoxicidad de cloroprocaína: cuatro casos adicionales. Anesth Analg 1982;61:155–159.
- Lynch C 3rd: Depresión de la contractilidad miocárdica in vitro por bupivacaína, etidocaína y lidocaína. Anesth Analg 1986;65: 551–559.
- Graf B, Martin E, Bosnjak Z: efecto estereoespecífico de los isómeros de bupivacaína en la conducción auriculoventricular en el corazón de conejillo de Indias perfundido aislado. Anestesiología 1997;86:410–419.
- McClure JH: Ropivacaína. Hermano J Anaesth 1996;76:300–307.
- Bader AM, Datta A, Flanagan H, et al: Comparación del bloqueo de conducción inducido por bupivacaína y ropivacaína en el nervio vago de conejo aislado. Anesth Analg 1989;68:724–727.
- Curatolo M, Petersen-Felix S, Arendt-Nielsen L, et al: Agregar bicarbonato de sodio a la lidocaína mejora la profundidad del bloqueo epidural. Anesth Analg 1998;86:341–347.
- Corke BC, Carlson CG, Dettbarn WD: La influencia de la 2-cloroprocaína en la potencia analgésica posterior de la bupivacaína. Anestesiología 1984;60:25–27.
- Stanton-Hicks M, Berges PU, Bonica JJ: Efectos circulatorios del bloqueo nervioso peridural. IV. Comparación de los efectos de la epinefrina y la fenilefrina. Anestesiología 1973;39:308–314.
- Bouguet D: La clonidina caudal agregada a los anestésicos locales mejora la analgesia posoperatoria después de la cirugía anal en adultos. Anestesiología 1994; 81:A942.
- Kroin JS, Buvanendran A, Beck DR, et al: La prolongación de la clonidina de la analgesia con lidocaína después del bloqueo del nervio ciático en ratas está mediada por la corriente catiónica activada por hiperpolarización, no por los alfa-adrenorreceptores. Anestesiología 2004;101:488–494.
- Landau R, Schiffer E, Morales M, et al: El efecto ahorrador de dosis de la clonidina añadida a la ropivacaína para la analgesia epidural del trabajo de parto. Anesth Analg 2002;95:728–734.
- Kayacan N, Arici G, Karsli B, et al: Analgesia epidural controlada por el paciente durante el trabajo de parto: la adición de fentanilo o clonidina a la bupivacaína. Agri 2004;16:59–66.
- Novak-Jankovic V, Paver-Eržen V, Bovill JG, et al: Efecto de la clonidina epidural e intravenosa en la respuesta al estrés neuroendocrino e inmunológico en pacientes sometidos a cirugía pulmonar. Eur J Anaesthesiol 2000; 17:50–56.
- Matot I, Drenger B, Weissman C, et al: Clonidina epidural, bupivacaína y metadona como único agente analgésico después de la toracotomía para la resección pulmonar. Anestesia 2004;59:861–866.
- Wu CT, Jao SW, Borel CO: El efecto de la clonidina epidural sobre la respuesta perioperatoria de citocinas, el dolor posoperatorio y la función intestinal en pacientes sometidos a cirugía colorrectal. Anesth Analg 2004;99: 502–509.
- Roelants F, Lavand'homme PM, Mercier-Fuzier V: Administración epidural de neostigmina y clonidina para inducir la analgesia del trabajo de parto: evaluación de la eficacia y el efecto ahorrador de anestésico local. Anestesiología 2005;102:1205–1210.
- Boogmans T, Vertommen J, Valkenborgh T, et al: La neostigmina epidural y la clonidina mejoran la calidad de la analgesia epidural espinal combinada en el trabajo de parto: un ensayo controlado aleatorizado y doble ciego. Eur J Anaesthesiol 2014;31:190–196.
- Roelants F, Lavand'homme PM: La neostigmina epidural combinada con sufentanil proporciona una analgesia equilibrada y selectiva en las primeras etapas del trabajo de parto. Anestesiología 2004;101:439–444.
- Omais M, Lauretti G, Paccola CA: Morfina epidural y neostigmina para la analgesia posoperatoria después de una cirugía ortopédica. Anesth Analg 2002;95:1698–1701.
- Habib AS, Gan TJ. Uso de neostigmina en el tratamiento del dolor posoperatorio agudo y el dolor de parto: una revisión. CNS Drugs 2006;20: 821–839.
- Lauretti GR, Gomes JM, Reis MP, Pereira NL:. Dosis bajas de ketamina o neostigmina por vía epidural, pero no de midazolam, mejoran la analgesia con morfina en el tratamiento del dolor por cáncer terminal por vía epidural. J Clin Anesth 1999; 11(8):663–668.
- Lauretti GR, de Oliveira R, Perez MV, et al: Analgesia postoperatoria por neostigmina intraarticular y epidural después de una cirugía de rodilla. J Clin Anesth 2000;12:444–448.
- Johansen MJ, Gradert TL, Sattefield WC, et al: Seguridad de la infusión intratecal continua de midazolam en el modelo de oveja. Anesth Analg 2004;98:1528–1535.
- Bharti N, Madan R, Mohanty PR, et al: El midazolam intratecal agregado a la bupivacaína mejora la duración y la calidad de la anestesia espinal. Acta Anaesthesiol Scand 2003;47:1101–1105.
- Tucker AP, Mezzatesta J, Nadeson R, et al: Midazolam intratecal II: combinación con fentanilo intratecal para el dolor de parto. Anesth Analg 2004;98:1521–1527.
- Ugur B, Basaloglu K, Yurtseven T, et al: neurotoxicidad con la administración intratecal de dosis única de midazolam. Eur J Anaesthesiol 2005;22: 907–912.
- Yaksh TL, Allen JW: Perspectivas preclínicas sobre la implementación de midazolam intratecal: una advertencia. Anesth Analg 2004;98: 1509–1511.
- Gambling D, Hughes T, Martin G, et al: Una comparación de Depodur, una nueva morfina epidural de liberación prolongada de dosis única, con morfina epidural estándar para el alivio del dolor después de una cirugía abdominal inferior. Anesth Analg 2005;100:1065–1074.
- Viscusi ER, Martin G, Hartrick CT, et al: Cuarenta y ocho horas de alivio del dolor posoperatorio después de una artroplastia total de cadera con una nueva formulación epidural de morfina de liberación prolongada. Anestesiología 2005;102:1014–1022.
- Carvalho B, Riley E, Cohen SE, et al: Morfina epidural de liberación sostenida de dosis única en el tratamiento del dolor posoperatorio después de una cesárea electiva: resultados de un estudio controlado aleatorizado multicéntrico. Anesth Analg 2005;100:1150–1158.
- Magnusdottir H, Kimo K, Ricksten S: La analgesia epidural torácica alta no inhibe la actividad nerviosa simpática en las extremidades inferiores. Anestesiología 1999;91:1299–1304.
- Basse L, Werner M, Kehlet H: ¿Es necesario el drenaje urinario durante la anestesia epidural continua después de la resección colónica? Reg Anesth Pain Med 2000;25:498–501.
- Galindo A, Hernandez J, Benavides O, et al: Calidad de la anestesia extradural espinal: La influencia del diámetro de la raíz del nervio espinal. Hermano J Anaesth 1975;47:41–47.
- Duggan J, Bowler GM, McClure JH, et al: bloqueo nervioso extradural con bupivacaína: influencia de la dosis, el volumen, la concentración y las características del paciente. Hermano J Anaesth 1998;61:324–331.
- Sakura S, Sumi M, Kushizaki H, et al: La concentración de lidocaína afecta la intensidad del bloqueo del nervio sensorial durante la anestesia epidural lumbar. Anesth Analg 1999;88:123–127.
- Hodgkinson R, Husain FJ: Obesidad, gravedad y propagación de la anestesia epidural. Anesth Analg 1981;60:421–424.
- Seow LT, Lips FJ, Cousins MJ: Efecto de la posición lateral en el bloqueo epidural para cirugía. Anaesth Cuidados Intensivos 1983;11:97–102.
- Park WY, Hagins FM, Rivat EL, et al: Edad y respuesta a la dosis epidural en hombres adultos. Anestesiología 1982;56:318–320.
- Park WY, Massengale M, Kim SI, et al: Edad y difusión de las soluciones anestésicas locales en el espacio epidural. Anesth Analg 1980;59:768–771.
- Veering BT, Burm AG, van Kleef JW, et al: Anestesia epidural con bupivacaína: Efectos de la edad sobre el bloqueo neural y la farmacocinética. Anesth Analg 1987;66:589–593.
- Hirabayashi Y, Shimizu R, Matsuda I, et al: Efecto de la distensibilidad extradural y resistencia a la propagación de la analgesia extradural. Hermano J Anaesth 1990;65:508–513.
- Bromage PR, Bufoot MF, Crowell DE, et al: Calidad del bloqueo epidural. I. Influencia de los factores físicos. Hermano J Anaesth 1964;36: 342–352.
- Grundy EM, Zamora AM, Winnie AP: Comparación de la difusión de la anestesia epidural en mujeres embarazadas y no embarazadas. Anesth Analg 1978;57:544–546.
- Arakawa M: ¿El embarazo aumenta la eficacia de la anestesia epidural lumbar? Int J Obstet Anesth 2004;13:86–90.
- Henke VG, Bateman BT, Leffert LR: anestesia espinal en la preeclampsia severa. Anaesth Analg 2013;117:686–693.
- Spiegel JE, Vasudevan A, Li Y, et al: Un estudio prospectivo aleatorizado que compara dos catéteres epidurales flexibles para la analgesia del trabajo de parto. Hermano J Anaesth 2009;103:400–405.
- Frölich MA, Zhang K, Ness TJ: Efecto de la sedación en la percepción del dolor. Anestesiología 2013;118:611–621.
- Frölich MA, Burchfield DJ, Euliano TY, et al: Una dosis única de fentanilo y midazolam antes de la cesárea no tiene efectos adversos neonatales. Can J Anaesth 2006;53:79–85.
- Varelmann D, Pancaro C, Cappiello EC, et al: Hiperalgesia inducida por Nocebo durante la inyección de anestésico local. Anesth Analg 2010;110: 868–870.
- Marica LS, O'Day T, Janosky J, et al: La cloroprocaína es menos dolorosa que la lidocaína para la anestesia por infiltración cutánea. Anesth Analg 2002;94: 351–354.
- Cepeda MS, Tzortzopoulou A, Thackrey M, et al: Ajuste del pH de la lidocaína para reducir el dolor en la inyección. Base de datos Cochrane Syst Rev 2010;12:CD006581.
- Al Shahwan MA: Comparación prospectiva entre la lidocaína-epinefrina al 1% tamponada y el enfriamiento de la piel para reducir el dolor de la infiltración del anestésico local. Dermatol Surg 2012;38:1654–1659.
- Hamilton CL, Riley ET, Cohen SE: Cambios en la posición de los catéteres epidurales asociados con el movimiento del paciente. Anestesiología 1997;86: 778–784.
- Richardson MG, Thakur R, Abramowicz JS, et al: La postura materna influye en el grado de bloqueo de los nervios sensoriales producido por la bupivacaína sin dextrosa intratecal con fentanilo para la analgesia del parto. Anesth Analg 1996;83:1229–1233.
- Tsen LC: Las técnicas neuroaxiales para la analgesia del parto deben colocarse en posición lateral. Int J Obstet Anesth 2008;17:146–149.
- Grupo de Trabajo de la Sociedad Estadounidense de Anestesiólogos sobre Complicaciones Infecciosas Asociadas con Técnicas Neuroaxiales: Asesoramiento práctico para la prevención, diagnóstico y manejo de complicaciones infecciosas asociadas con técnicas neuroaxiales. Anestesiología 2010;112:530–545.
- Malhotra S, Dharmadasa A, Yentis SM: Una vs dos aplicaciones de clorhexidina/etanol para desinfectar la piel: Implicaciones para la anestesia regional. Anestesia 2011;66:574–578.
- Bogod DS: El aguijón en la cola: Antisepsia y el neuroeje revisitado.
Anestesia 2012;67:1305–1309. - Segal S, Arendt KW: Un estudio de efectividad retrospectivo de la pérdida de resistencia al aire o solución salina para la identificación del espacio epidural. Anesth Analg 2010;110:558–563.
- Laviola S, Kirvelä M, Spoto M: Neumoencéfalo con cefalea intensa y dilatación pupilar unilateral tras punción dural accidental durante anestesia epidural para cesárea. Anesth Analg 1999;88: 582–583.
- Van de Velde M: Identificación del espacio epidural: ¡Dejar de usar la técnica de pérdida de resistencia al aire! Acta Anaesthiol Belg 2006;57: 51–54.
- Dalens B, Bazin JE, Haberer JP: Burbujas epidurales como causa de analgesia incompleta durante la anestesia epidural. Anesth Analg 1987;66: 679–683.
- Naulty JS, Ostheimer GW, Datta S, et al: Incidencia de embolia gaseosa venosa durante la inserción del catéter epidural. Anestesiología 1982;57: 410–412.
- Evron S, Sessler D, Sadan O, et al: Identificación del espacio epidural: pérdida de resistencia con aire, lidocaína o la combinación de aire y lidocaína. Anesth Analg 2004;99:245–250.
- Balki M, Lee Y, Halpern S, et al: Imágenes por ultrasonido de la columna lumbar en el plano transversal: la correlación entre la profundidad estimada y real del espacio epidural en parturientas obesas. Anesth Analg 2009;108: 1876–1881.
- Mhyre JM: ¿Por qué las dosis de prueba farmacológicas no logran identificar el catéter intratecal no deseado en obstetricia? Anesth Analg 2013; 116:4–7.
- Tsui B, Gupta S, Finucane B: Confirmación de la colocación del catéter epidural mediante estimulación nerviosa. Can J Anaesth 1998;45: 640–644,1998.
- Lyons GR, Kocarev MG, Wilson RC, et al: Una comparación de los volúmenes mínimos de anestésico local y las dosis de bupivacaína epidural (0.125 % p/v y 0.25 % p/v) para la analgesia en el trabajo de parto. Anesth Analg 2007;104: 412–415.
- Wong CA, Ratliff JT, Sullivan JT, et al: Una comparación aleatoria de bolo epidural intermitente programado con infusión epidural continua para la analgesia del trabajo de parto. Anesth Analg 2006;102:904–909.
- Heesen M, Klohr S, Rossaint R, et al: ¿Se puede reducir la incidencia de punción dural accidental en mujeres en trabajo de parto? Una revisión sistemática y metanálisis. Minerva Anestesiol 2013;79:1187–1197.
- Van de Velde M, Schepers R, Berends N, et al: Diez años de experiencia con punción dural accidental y dolor de cabeza posterior a la punción dural en un departamento de anestesia obstétrica terciaria. Int J Obstet Anesth 2008;17: 329–335.
- Agerson AN, Scavone BM: Parche hemático epidural profiláctico después de una punción dural no intencional para la prevención de la cefalea pospunción dural en parturientas. Anesth Analg 2012;115:133–136.
- Bauer ME, Kountanis JA, Tsen LC, et al: Factores de riesgo para la conversión fallida de la analgesia epidural del trabajo de parto a la anestesia del parto por cesárea: una revisión sistemática y metanálisis de ensayos observacionales. Int J Obstet Anesth 2012;21:294–309.
- Toledano RD, Kodali BS, Camann WR: Fármacos anestésicos en la práctica obstétrica y ginecológica. Rev Obstet Gynecol 2009;2: 93–100.
- Mhyre JM, Greenfield ML, Tsen LC, et al: Una revisión sistemática de ensayos controlados aleatorios que evalúan estrategias para evitar la canulación de la vena epidural durante la colocación del catéter epidural obstétrico. Anesth Analg 2009;108:1232–1242.
- Neal JM, Mulroy MF, Weinberg GL: Lista de verificación de la Sociedad Estadounidense de Anestesia Regional y Medicina del Dolor para el manejo de la toxicidad sistémica de los anestésicos locales: versión 2012. Reg Anesth Pain Med 2012;37:16–18.
- Bhole MV, Manson AL, Seneviratne SL, et al: Alergia mediada por IgE a los anestésicos locales: separando el hecho de la percepción: una perspectiva del Reino Unido. Hermano J Anaesth 2012;108:903–911.
- Rice I, Wee MY, Thomson K: epidurales obstétricas y aracnoiditis adhesiva crónica. Hermano J Anaesth 2004;92:109–120.
- Taniguchi M, Bollen AW, Drasner K: bisulfito de sodio: ¿chivo expiatorio de la neurotoxicidad de la cloroprocaína? Anestesiología 2004;100:85–91.
- Checketts MR: Wash & go, pero ¿con qué? Soluciones antisépticas cutáneas para el bloqueo del nervio neuroaxial central. Anestesia 2012;67:819–822.
- Na EH, Han SJ, Kim MH: aparición tardía de aracnoiditis espinal después de un bloqueo del nervio caudal. J Spinal Cord Med 2011;34:616–619.
- Ross JS, Masaryk T, Modic M, et al: RM de aracnoiditis lumbar. Am J Roentgenol 1987;149:1025–1032.
- Wang YL, Hsieh JR, Chung HS, et al: La adición local de tenoxicam reduce la incidencia de dolor lumbar después de la anestesia epidural lumbar. Anestesiología 1998;89:1414–1417.
- Stevens RA, Urmey WF, Urquhart, et al: Dolor de espalda después de la anestesia epidural con cloroprocaína. Anestesiología 1993;78:492–497.
- Hakim SH, Narouze S, Shaker NN, et al: Factores de riesgo para el dolor lumbar persistente de nueva aparición después de una cirugía no obstétrica realizada con anestesia epidural. Reg Anesth Pain Med 2012;37:175–182.
- Wilkinson HA: Anestesia de bloqueo nervioso de campo para punción lumbar. JAMA 1983;249:2177.
- Wang YL, Tan PP, Yang CH, et al: La dexametasona epidural reduce la incidencia de dolor de espalda después de la anestesia epidural lumbar. Anesth Analg 1997;84:376–378.
- Breen TW: analgesia epidural y dolor de espalda. En Halpern Sh, Douglas MJ (eds): Anestesia obstétrica basada en la evidencia. Libros BMJ, 2005, págs. 208–216.
- Arendt K, Demaerschalk BM, Wingerchuck DM, et al: Agujas de punción lumbar atraumáticas: después de todos estos años, ¿todavía nos estamos perdiendo el punto? Neurólogo 2009;15:17–20.
- Brownridge P: El manejo del dolor de cabeza después de una punción dural accidental en pacientes obstétricas. Anaesth Cuidados Intensivos 1983;11:4–15.
- Comité de Clasificación de Dolor de Cabeza de la Sociedad Internacional de Dolor de Cabeza: La clasificación internacional de trastornos de dolor de cabeza, tercera edición. Cefalalgia 2013;33:629–808.
- Webb CA, Weyker PD, Zhang L, et al: La punción dural no intencional con una aguja Tuohy aumenta el riesgo de dolor de cabeza crónico. Anesth Analg 2012;115:124–132.
- Apfel CC, Saxena A, Cakmakkaya OS, et al: Prevención de la cefalea posterior a la punción dural después de una punción dural accidental: una revisión sistemática cuantitativa. Hermano J Anaesth 2010;105:255–263.
- Oedit R, van Kooten F, Bakker SL, et al: Eficacia del parche hemático epidural para el tratamiento de la cefalea posterior a la punción lumbar BLOPP: Un ensayo clínico controlado, aleatorizado, observador ciego. BMC Neurol 2005;
5: 12. - van Kooten F, Oedit R, Bakker SL, et al: parche de sangre epidural en el dolor de cabeza posterior a la punción dural: un ensayo clínico controlado, aleatorizado, ciego observado. J Neurol Neurosurg Psiquiatría 2008;79:553–559.
- Angle P, Tang SL, Thompson D, et al: El tratamiento expectante de la cefalea pospunción dural aumenta la duración de la estancia hospitalaria y las visitas a la sala de urgencias. Can J Anaesth 2005;52:397–402.
- Paech MJ, Doherty DA, Christmas T, et al: El volumen de sangre para el parche de sangre epidural en obstetricia: un ensayo clínico aleatorizado y ciego. Anesth Analg 2011;113:126–133.
- Haines DE: Sobre la cuestión de un espacio subdural. Rec. Anat 1991; 230:3–21.
- Lubenow T, Keh-Wong E, Kristof K, et al: Inyección subdural inadvertida: una complicación del bloqueo del nervio epidural. Anesth Analg 1988;67: 175–179.
- Paech MJ, Godkin R, Webster S: Complicaciones de la analgesia y anestesia epidural obstétrica: un análisis prospectivo de 10,995 1998 casos. Int J Obstet Anesth 7;5:11–XNUMX.
- Cappiello E, Tsen LC: Complicaciones y efectos secundarios de las técnicas neuroaxiales centrales. En Wong CA (ed): Anestesia espinal y epidural. McGraw-Hill, 2007, págs. 152–182.
- Grewal S, Hocking G, Wildsmith JA: Abscesos epidurales. Hermano J Anaesth 2006;96:292–302.
- Darouiche R, Absceso epidural espinal: N Engl J Med 2006;355: 2012–2020.
- Connor DE, Chittiboina P, Caldito G, et al: Comparación del manejo quirúrgico y no quirúrgico del absceso epidural espinal: una revisión retrospectiva de los predictores clínicos y de laboratorio del resultado neurológico. J Neurosurg Spine 2013;19:119–127.
- Curry WT, Hoh BL, Amin-Hanjani S, et al: absceso epidural espinal: presentación clínica, manejo y resultado. Surg Neurol 2005;63:364–371.
- Okano K, Kondo H, Tsuchiya R, et al: Absceso epidural espinal asociado con cateterismo epidural: Informe de un caso y revisión de la literatura. Jpn J Clin Oncol 1999;29:49–52.
- Danner RL, Hartman BJ: Actualización sobre el absceso epidural espinal: 35 casos y revisión de la literatura. Rev Infect Dis 1987;9:265–274.
- Huang PY, Chen SF, Chang WN, et al: absceso epidural espinal en adultos causado por Staphylococcus aureus: características clínicas y factores pronósticos. Clin Neurol Neurocirugía 2012;114:572–576.
- Baer ET: Meningitis bacteriana post-punción dural. Anestesiología 2006; 105:381–393.
- Reynolds F: Infecciones neurológicas después de la anestesia neuroaxial. Anesthesiol Clin 2008;26:23–52.
- Usubiaga JE: Complicaciones neurológicas posteriores a la anestesia epidural. Int Anaesthesiol 1975;13:1–153.
- Kane RE: Déficits neurológicos después de la anestesia epidural o espinal. Anesth Analg 1981;60:150–161.
- Kao M, Tsai S, Tsou M, et al: Paraplejía después de la detección tardía de una lesión involuntaria de la médula espinal durante el cateterismo epidural torácico en un paciente anciano anestesiado. Anesth Analg 2004;99:580–583.
- Loo CC, Irestedt L: Síndrome de cauda equina después de anestesia espinal con lignocaína hiperbárica al 5%: una revisión de seis casos de síndrome de cauda equina informados al Seguro Farmacéutico Sueco 1993–1997. Acta Anaesthesiol Scand 1999;43:371–379.
- Lambert DH, Hurley RJ: Síndrome de cauda equina y anestesia espinal continua. Anesth Analg 1991;72:817–819.
- Gerancher JC: Síndrome de cauda equina después de una única administración espinal de lidocaína hiperbárica al 5% a través de una aguja Whitacre de calibre 25. Anestesiología 1997;87:687–689.
- Benson JS: Alerta de seguridad de la Administración de Drogas y Alimentos de EE. UU.: síndrome de cauda equina asociado con el uso de catéteres de pequeño calibre en anestesia espinal continua. AANA J 1992;60:223.
- Rigler ML, Drasner K, Krejcie, TC, et al: Síndrome de cauda equina después de anestesia espinal continua. Anesth Analg 1991;72:275–281.
- Gaiser RR: ¿Debería usarse la lidocaína intratecal en el siglo XXI? J Clin Anesth 21;2000:12–476.
- Walters MA, Van de Velde M, Wilms G: Hematoma intratecal agudo después de la anestesia neuroaxial: Retraso en el diagnóstico después de imágenes radiológicas aparentemente normales. Int J Obstet Anesth 2012;21:181–185.
- Auroy Y, Narchi P, Messiah A, et al: Complicaciones graves relacionadas con la anestesia regional: resultados de una encuesta prospectiva en Francia. Anestesiología 1997;87:479–486.
- Pollard JB: mecanismos y estrategias comunes para la prevención y el tratamiento del paro cardíaco durante la anestesia epidural. J Clin Anesth 2002;14:52–56.
- Pollard JB: Paro cardíaco durante la anestesia espinal: mecanismos y estrategias comunes para la prevención. Anesth Analg 2001;92:252–256.
- Krismer AC, Hogan QH, Wenzel V, et al: La eficacia de la epinefrina o la vasopresina para la reanimación durante la anestesia epidural. Anesth Analg 2001;93:734–742.
- Curatolo M, Scaramozzino P, Venuti FS, et al: Factores asociados con hipotensión y bradicardia después del bloqueo epidural. Anesth Analg 1996;83:1033–1040.
- Liguori GA, Sharrock NE: Asistolia y bradicardia severa durante la anestesia epidural en pacientes ortopédicos. Anestesiología 1997;86: 250–257.
- Camann WR, Hortvet LA, Hughes N, et al: Regulación de la temperatura materna durante la analgesia extradural para el trabajo de parto. Br. J. Anaesth 1991;67: 565–568.
- Borgeat A, Ekatodramis G, Schenker CA: Náuseas y vómitos postoperatorios en anestesia regional: una revisión. Anestesiología 2003;98: 530–547.
- Allen TK, Jones CA, Habib AS: Dexametasona para la profilaxis de náuseas y vómitos posoperatorios asociados con la administración de morfina neuroaxial: una revisión sistemática y metanálisis. Anesth Analg 2012;114:813–822.
- Turnbull J, Moonesinghe R: epidurales perioperatorios: la controversia continúa. Br J Hosp Med 2011;72:538.
- Dong H, Zhang Y, Xi H: Los efectos de la anestesia y la analgesia epidurales sobre la citotoxicidad de las células asesinas naturales y la respuesta de citoquinas en pacientes con cáncer de ovario epitelial sometidos a resección radical, J Int Med Research 2012;40:1822–1829.