Objetivos de aprendizaje
- Describir los factores que contribuyen a la anestesia espinal alta
- Aplicar medidas preventivas para la raquianestesia alta
- Describir los síntomas de la anestesia espinal alta
- Manejar casos de raquianestesia alta
Definición y mecanismos
- La anestesia espinal alta es una complicación de las técnicas neuroaxiales centrales que incluyen espinal y anestesia epidural
- Se define como una propagación del anestésico local que afecta a los nervios espinales por encima de T4
- Los efectos son de gravedad variable dependiendo del nivel máximo que esté involucrado, pero pueden incluir compromiso cardiovascular y/o respiratorio.
- En la anestesia espinal total, hay una propagación intracraneal del anestésico local que resulta en la pérdida del conocimiento.
Factores contribuyentes
- Dosis de anestésico local
- Posicionamiento del paciente
- Bloqueo epidural preexistente
- Punción dural no reconocida e inyección intratecal
- Bloqueo subdural accidental
- Espacio intradural accidental
Prevención
- Analgesia/anestesia epidural:
-
- Usar bajas concentraciones de anestésico local para la analgesia del trabajo de parto
- Antes de la recarga:
- Evaluar bloque (para guiar la dosificación de recarga)
- Aspirar el catéter epidural con una jeringa de 2 ml para descartar colocación intratecal o intravenosa
- Considere administrar grandes volúmenes de anestésico local en dosis divididas (la urgencia clínica puede impedirlo)
- Anestesia espinal:
-
- Considere el nivel (y por lo tanto la dosis de anestésico local) requerido para la cirugía
- Posición del paciente: la altura del bloqueo se puede manipular durante un máximo de 30 minutos cuando se usan anestésicos hiperbáricos ("fuertes"). Si usa la posición con la cabeza hacia abajo para establecer el bloqueo, recuerde retirarlo lo antes posible.
- Características del paciente: considerar reducción de dosis en casos cortos o mórbidos obeso los pacientes
- Técnica:
- Considere los efectos de la velocidad de inyección.
- Evite el barbotaje excesivo
- Si se realiza una anestesia raquídea después de una epidural, puede ser necesaria una reducción de la dosis según el nivel de bloqueo existente (se han sugerido reducciones a 1-1.5 ml de anestésico local después de una recarga epidural fallida); no hay un consenso claro al respecto
- Anestesia epidural y espinal:
-
- No inyecte durante una contracción/tos/maniobra de Valsalva ya que esto puede aumentar la propagación cefálica del anestésico local.
- Se recomienda el uso de la cuña Oxford para evitar la propagación cefálica del anestésico local (y para optimizar el posicionamiento de la vía aérea en caso de requerir anestesia general)
Síntomas
| Nivel espinal | Área(s) afectada(s) | Síntomas |
|---|---|---|
| T1-T4 | Fibras simpáticas cardíacas bloqueadas | La hipotensión La bradicardia |
| C6-C8 | manos y brazos | Parestesia o entumecimiento en manos/brazos Debilidad de manos/brazos Dificultad para respirar (músculos respiratorios accesorios afectados) |
| C3-5 | Diafragma y hombros | Debilidad del hombro: compromiso respiratorio inminente Hipoventilación y/o desaturación Paro respiratorio |
| Propagación intracraneal | Tronco cerebral | trastornos del habla Sedación Pérdida de consciencia |
Administración
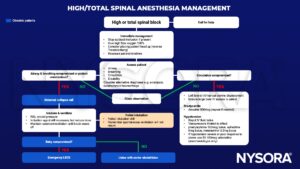
Lectura sugerida
- Sivanandan S., Surendran A. (2019) Manejo del bloqueo espinal total en obstetricia. Actualización en Anestesia, 34: 22-25.
- Reeve J. (2017) Guía clínica de confianza de la Fundación NHS: bloqueo regional alto (incluida la anestesia espinal total).
Nos encantaría saber de usted. Si detecta algún error, envíenos un correo electrónico a customerservice@nysora.com

