杰夫·加兹登
引言
近几十年来,全身麻醉并发症的发生率已大大降低,这主要是由于在麻醉期间监测呼吸和心血管功能的进步。 使用客观监测器,如脉搏血氧仪、二氧化碳图、心电图等,使从业者能够及时识别不断变化的生理参数,快速适当地进行干预,并指导他们的治疗决策。
传统上,区域麻醉的实践缺乏客观的监测器,这些监测器可以帮助从业者更客观地监测针-神经关系并预防神经损伤。 传统上,周围神经阻滞的实践依赖于主观终点来衡量对患者的潜在风险。 然而,随着标准化方法的引入和采用,这种情况正在发生变化,通过这些方法可以安全地执行周围神经阻滞,并将患者的风险降至最低。 例如,从业者现在可以使用超声检查来监测针-筋膜层的相互作用,而不是依靠感觉“咔哒”、“砰”和“划痕”来识别针尖位置。 同样,量化最小电流强度和注射阻力可用于收集对临床决策有用的额外数据,以最大程度地减少将针放置到不需要的组织平面、血管内或神经内易损解剖结构的风险。 因此,监测方面的最新进展可能会减少周围神经阻滞的三个最可怕的并发症: 神经损伤, 局麻药毒性,以及对相邻结构的意外损坏(“针刺事故”)。
本节的第一部分讨论了客观监测及其使用的基本原理。 后一部分侧重于记录神经阻滞程序,这是对监视器获得的客观信息的逻辑记录。 关于如何进行神经阻滞的客观而有力的文件具有明显的法医学意义,并提供了一个有用的数据库来指导安全性和有效性的进步。
监测
监测针神经关系的可用方法
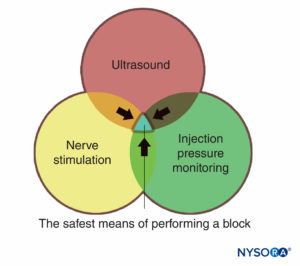
在医疗实践中使用的监视器是评估特定生理状态并警告临床医生即将发生的伤害的设备。 本章讨论的监测器包括用于神经刺激、超声检查和监测注射压力的监测器。 它们中的每一个都有其独特的优点和局限性,并且每个都最好以相加、互补的方式使用(图1) 以尽量减少对患者造成伤害的可能性,而不是仅仅依靠一台显示器提供的信息。 有足够的基于证据的信息表明,所有三个监视器的组合可能会在周围神经阻滞的实践中产生最安全的过程。
许多临床医生经常使用的另一种药理学监测器是在局部麻醉中使用肾上腺素。 有一些证据支持这种做法作为提高大多数患者在周围神经阻滞期间安全性的一种手段。 首先,它作为血管内吸收的标志物。 静脉注射 10 至 15 μg 肾上腺素可使收缩压可靠地增加 15 mmHg 以上,即使在镇静患者或接受 β 受体阻滞剂治疗的患者中也是如此。 认识到这种增加可能允许早期检测血管内注射,并允许临床医生迅速停止注射并提高对全身毒性迹象的警惕。 其次,肾上腺素降低了局部麻醉剂的血浆峰值水平,从而降低了全身毒性的风险。 关于肾上腺素的血管效应、血管收缩和神经缺血的担忧尚未得到证实,事实上 2.5 μg/mL (1:400,000) 的浓度与神经血流量增加有关,可能是由于 β -药物的作用。 因此,肾上腺素可以提高大剂量局麻药的安全性,而不会出现肢体缺血和神经系统死亡的风险。
值得注意的是,由于多种原因,在周围神经阻滞期间使用超声引导显着降低了局部麻醉剂严重全身毒性的风险。 这很可能是因为超声引导允许减少局部麻醉剂的体积和剂量,以通过监测其扩散来完成大多数神经阻滞程序。 此外,在超声上观察针路、避免血管内放置以及确认局麻药在组织中的扩散都增加了超声引导区域麻醉的安全性。
神经刺激
在 1980 年代,神经刺激在很大程度上取代了感觉异常作为神经定位的主要手段。 然而,它作为一种精确定位神经的方法的实用性最近受到了几项研究数据的挑战,这些研究表明,尽管经超声检查证实有密切的针神经接触,但诱发运动反应 (EMR) 可能不存在。 实际上,在许多针-神经接触甚至神经内针放置中,可能需要出乎意料的高电流强度来引发 EMR。 例如,在某些情况下,即使在超声上看到的神经内针放置,也只能在相对电流强度超过 1 mA 的情况下获得 EMR。
可能有多种因素有助于解释这种现象。 最重要的因素很可能是沿着最小电阻(阻抗)路径的电流分流。 换言之,即使当针紧邻神经时,电流也可能不必选择朝向神经行进,而是沿着阻力最小的路径行进以通过皮肤电极退出。 另一个因素可能包括复合神经中运动和感觉纤维的分布不均匀。
然而,这并不意味着周围神经的电刺激在超声引导的时代已经过时。 例如,来自几项动物和人类研究的数据表明,在非常低的电流(即 < 0.2 mA)下存在运动反应与这种情况下注射后的神经内针尖放置和神经内炎症有关。表1)。 Voelckel 等人。 据报道,当局部麻醉剂以 0.3 和 0.5 mA 之间的电流注射时,产生的神经组织没有显示出炎症过程的迹象,而小于 0.2 mA 的注射导致 50% 的神经出现淋巴细胞和粒细胞浸润。 蔡等人。 进行了一项类似的研究,调查到神经的距离对所需电流的影响; 虽然记录了各种距离的一系列电流,但只有在将针尖放置在神经内时才能在小于 0.2 mA 时获得电机响应。
表1。 最近对神经刺激电流和针尖位置的研究总结。
| 学习 | 联系原因 | 付款方式 | 发现 |
|---|---|---|---|
| Voelckel 等人 (2005)11 | 猪 (n = 10) | • 双侧进行后坐骨神经阻滞 • 两组 - 在 EMR 后以 0.3–0.5 mA 注射 - 在 EMR 后以 < 0.2 mA 注射 • 注射后 6 小时,采集坐骨神经进行组织学分析 | • 高电流组的正常、健康的神经外观 • 低电流组50% 的神经显示出淋巴细胞和多形性粒细胞亚、周的迹象。 并且在神经内 • 低电流组中的一个样本显示神经束膜和多根神经纤维的严重破坏 |
| 蔡等人(2008)12 | 猪 (n = 20) | • 全身麻醉 • 双侧暴露的坐骨神经 • 用针在从 2 厘米到神经内的不同距离施加电流 • 两名盲人观察者同意获得蹄抽动所需的最小电流 • 每个距离尝试 40 次 | • 坐骨神经抽搐只能达到 0.1 厘米或更近 • 引发电机响应所需的宽泛电流范围 • 只有当电流小于 0.2 mA 时,神经内才会产生运动反应 |
| 比格莱森等人 (2009)13 | 手/手腕手术患者(n = 55) | • 锁骨上阻滞 • 记录的最小电流 (mA) - 针在神经干外(但接触神经)- 在干内 • “神经内”位置通过 5 mL 局部麻醉剂注射进行超声检查确认 | • 神经外最小电流阈值中值 0.60 mA ± 0.37 mA • 神经外最小电流阈值中位数为 0.30 ± 0.19 mA • 当针头放置在神经外时,任何时候都没有观察到EMR,电流小于0.2 mA |
| 威斯曼等人 (2014)14 | 猪 (n = 6) | • 开放式臂丛神经模型 • 三个位置的刺激:神经内、针神经接触和距离神经 1 毫米 • 3 个脉冲持续时间测试(0.1、0.3 和 1 毫秒) | • 电流强度无法区分神经内接触和针神经接触 • 运动响应 < 0.2 mA(与脉冲持续时间无关)表明有神经内或针-神经接触 |
比格莱森等人。 研究了 55 名接受超声引导锁骨上臂丛神经阻滞的上肢手术患者。 作者着手确定遇到的第一个躯干内外的运动响应的最小电流阈值。 他们报告说,神经外的最小刺激阈值中位数为 0.60 mA,神经内为 0.3 mA。 然而,在神经外刺激电流为 0.2 mA 或更低时未观察到 EMR,而在神经内针放置时,36% 的患者在电流小于 0.2 mA 时出现 EMR 抽搐。 为了进一步完善这种关系,Wiesmann 及其同事在三个不同位置(神经内,针接触神经外膜,距离神经 1 毫米)向猪的臂丛施加电流,同时改变脉冲持续时间(0.1、0.3和 1.0 毫秒)。 引起运动反应的最小阈值电流在神经内和针神经接触位置之间是相同的,并且两者都显着低于 1 mm 外的位置。 脉冲持续时间对最小阈值电流没有影响。 这些作者得出结论,小于 0.2 mA(与脉冲持续时间无关)的运动反应表明神经内或针神经接触。 这一点很重要,因为已经确定,即使在没有刺穿神经外膜的情况下,即使是用力的针-神经(神经外膜)接触也会导致炎症和神经损伤的可能性。
总之,现有数据表明,在潜在危险的针神经关系(神经内/神经外膜放置)中,“低电流”引发 EMR 的敏感性约为 75%。 然而,当电流小于 0.5 mA 时,EMR 的特异性接近 100%。 换句话说,运动反应是由低强度刺激电流(例如,根据 Voelckel 等人,<0.2 mA)引起的,尖端总是在神经内或与神经外膜密切相关。 因此,神经刺激器的实用性是显而易见的:在 0.5 mA 时意外出现 EMR 表明存在危险的针-神经关系(例如,针-神经接触),并且可能允许操作员在针进入神经之前停止进针.
人们普遍认为,向神经内注射局部麻醉剂会带来神经损伤的危险因素。 因此,局部麻醉剂的神经外沉积构成了更安全的做法。 虽然毫无疑问是有用的,但超声检查远非对针神经关系的可靠监测。 由于注射到束中具有很高的受伤风险,因此增加对针尖位置的电监测对于安全性很有用,特别是在成像困难或图像质量差时具有挑战性的超声解剖结构的患者。 如果在低于 0.5 mA 的电流下引发 EMR,这表明针神经关系密切,应促使针头轻微退出并小心注射,同时避免打开注射压力大于 15 psi。 总体而言,神经刺激在时间或成本方面几乎不会增加神经阻滞手术的成本,并且还可以作为超声屏幕上显示的解剖图像的有用功能确认(例如,“是正中神经还是尺神经? ?”)。 由于这些原因,神经刺激应与超声一起常规使用,作为针尖位置的有价值的附加监测器。 学习更多关于 电神经刺激器和周围神经的定位。
超声
超声彻底改变了区域麻醉的实践,并允许该亚专业从少数人实践的艺术大幅演变为更具可重复性的科学。 优点是超声波可以实时看到针头,因此可以快速、更准确地将针头引导向目标。 当第一次尝试不充分时,超声还允许进行额外的注射,并将注射液准确地沉积到组织空间中以进行可重复的神经阻滞。 此外,即使在瘫痪的患者、没有用于 EMR 的肢体的截肢者等中,超声也可以进行神经阻滞。
出于多种原因,超声具有提高周围神经阻滞安全性的潜力。 可以看到并避免相邻的重要结构。 锁骨上阻滞的流行再次证明了这一点。 在超声之前,这种高效的阻滞作为臂丛神经的麻醉手段相对不受欢迎,因为害怕引起气胸,因为臂丛靠近胸膜和胸腔。 然而,由于臂丛神经,更重要的是肋骨、胸膜和锁骨下动脉可以在超声上识别,锁骨上阻滞在临床实践中已变得司空见惯。 无论如何,超声不应被认为是万无一失的,因为包括气胸在内的并发症在超声引导下仍然会发生。 同样,有报道称(尽管使用了)超声见证了血管内和神经内针的放置。
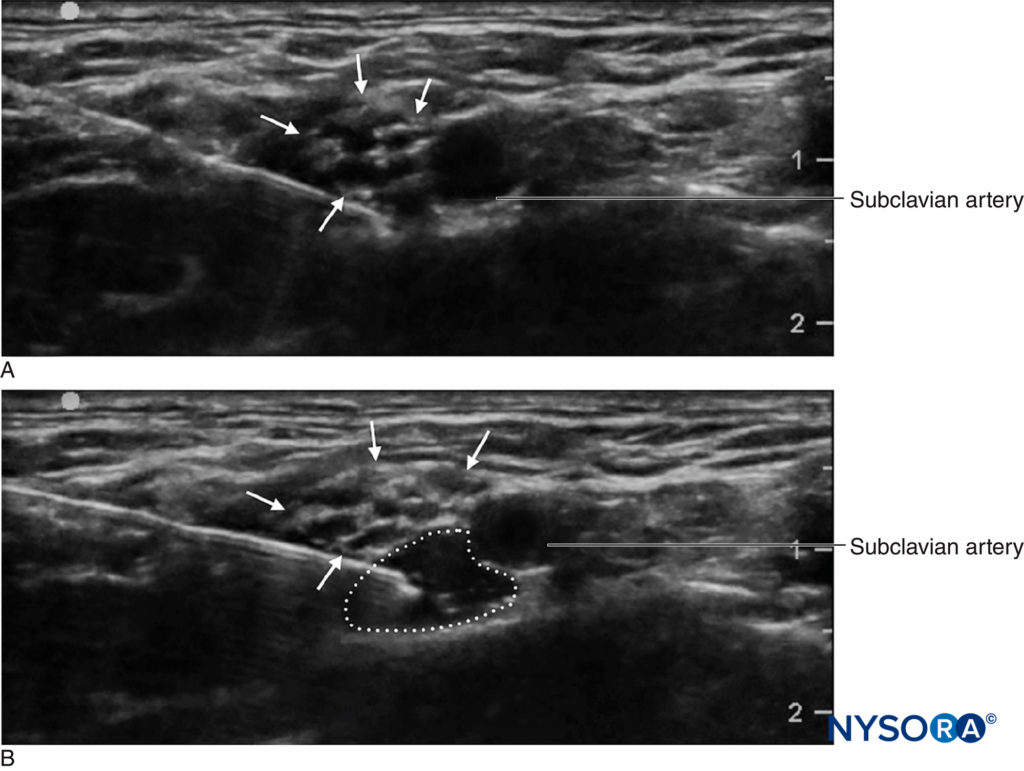
超声波筛查的一个重要优点是能够确定从皮肤到目标的距离。 这与在侧面蚀刻有深度标记的针头相结合,通过警告临床医生“停止距离”或临床医生应停止将针头推进到更深的组织并重新评估的深度来提供额外的安全余量。 超声波的另一个重要优势是能够实时查看局部麻醉剂分布。 (图2)。 如果在注射开始时没有看到相应的组织扩张,那么针尖可能不在预期的位置,临床医生可以停止注射并重新评估针尖的位置。 这在血管区域尤其重要,因为缺乏局部麻醉剂扩散可以指示血管内针的放置。 另一方面,当动脉管腔内出现回声“红晕”时,超声监测可用于诊断动脉内针尖放置,从而降低全身毒性的风险。
超声检查似乎可以降低局部麻醉剂全身毒性 (LAST) 的风险。 在一项对周围神经阻滞(>25,000 个周围神经阻滞)的大型多中心登记的分析中,使用超声引导将 LAST 的风险降低了 65% 以上。 作者提出的机制是能够显着减少完成区域阻滞所需的局部麻醉剂的体积和剂量。 事实上,减少局部麻醉成功所需的局部麻醉剂的剂量和体积是过去十年的一致趋势。 与超声前引导的区域麻醉技术相比,许多报告记录了实现等效阻滞所需的体积显着减少。 例如,只需不到 10 mL 的局部麻醉剂即可进行臂丛神经阻滞,而不会牺牲麻醉或镇痛效果。 即使整个体积的注射液是意外静脉内给药,也不太可能在平均体型的成年人中因 7 mL 体积为 0.5% 的罗哌卡因而导致严重的 LAST。相反,在周围神经期间使用超声引导阻滞并没有降低神经损伤的风险或发生率。
这种令人失望的观察记录在几份报告中,并且可能是多因素的。 辨别针神经关系的能力取决于用户和解剖结构。 事实上,研究表明,从业者可能会错过大约六分之一的神经内注射。 其次,超声机器的当前分辨率可能不足以区分肌内束外针尖位置。 这种差异至关重要,因为神经内(但束外)注射可能与损伤无关,而束内注射本身会产生临床和组织学损伤。 重要的是,不能将神经肿胀作为神经内注射的警告,因为一旦在超声上注意到这一点,就可能为时已晚,无法防止受伤。 这是因为即使是微量的局部麻醉剂,如果注入束中也会产生损伤,而如此少量的局部麻醉剂(例如,0.1-0.5 mL)可能无法通过超声检测到。 因此,依赖于组织扩张的视觉确认可能会在屏幕上检测到扩张之前导致损坏。
注射压力监测
当针尖位于犬坐骨神经束内位置时注射利多卡因与高开放压力(>20 psi)相关,随后在束状破裂后注射压力恢复正常(即<5 psi)。 相比之下,神经周围和神经内束外注射产生低开口和注射压力。 坐骨神经注射与高开放注射压力相关的肢体经历了神经病变的临床症状(肌肉萎缩、虚弱)以及神经损伤的组织学证据(炎症、神经结构的破坏)。 这意味着注射到低顺应性隔室中,例如在神经束膜束内,在开始注射之前需要高的打开注射压力。
神经内针尖位置也与人体尸体的高开放注射压力有关。 Orebaugh 等人使用超声波将针头插入尸体颈根,并在 5 秒内注射 15 mL 罗哌卡因和墨水的过程中量化压力。 与置于根部外的对照针相比(峰值压力 < 20 psi),神经内注射导致平均峰值压力为 49 psi(范围 37-66 psi)。 同样,Krol 等人在新鲜人体尸体(正中神经、尺神经和桡神经)的更远端神经中进行了超声引导下的神经内和神经周围注射,并且还报道了神经内的开放注射压力超过 15 psi,而神经外的开放注射压力小于 10 psi。
在一项对 16 名接受肩部手术的患者进行的临床研究中,肌间沟臂丛神经阻滞期间的针神经接触与大于 15 psi 的开口注射有关。 事实上,在针-神经接触处和针进入臂丛根之前,注射液的流动无法在低于 15 psi 的压力下开始。 当开始注射所需的开启注射压力达到 15 psi 时停止注射,97% 的受试者可以避免在该危险位置进行注射。 相比之下,距离神经 1 mm 的针头位置与在小于 15 psi 的开口压力下开始流动有关。 因此,作为针神经接触的监测器,大于 15 psi 的打开注射压力远比 0.5 或 0.2 mA 的最小阈值电流或感觉异常的发生更敏感。
这些数据表明,当系统中的压力接近 15 psi 而无法开始注射液时,这种高打开注射压力可能表明存在危险的针-神经关系或针头放置在错误的组织平面中。 因此,应停止注射并重新评估针头位置。
如何监测注射压力? 不幸的是,使用“手感”来避免高注射压力是不可靠的。 对有经验的从业者对注射压力视而不见并要求使用标准设备进行模拟注射的研究表明,所施加的压力存在很大差异,有些严重超过了既定的安全阈值。 同样,当被要求在动物模型中区分神经内注射和注射到其他组织(如肌肉或肌腱)时,麻醉师表现不佳。 因此,唯一有意义和可重复的监测是通过使用客观和可量化的方法来监测开启喷射压力。
虽然在周围神经阻滞期间监测注射压力的做法相对较新,但有几种监测选项。 Tsui 等人描述了一种“压缩空气注射技术”,将 10 mL 空气与局部麻醉剂一起吸入注射器。 保持注射器直立,通过只允许注射器内容物的气体部分压缩到其原始体积的一半或 1 mL,可以避免最大阈值 14.7 atm(或 5 psi)(图3)。 这是基于波义耳定律,该定律指出压力 × 体积必须是恒定的。 20 psi 或更低的压力被认为是在周围神经阻滞期间开始注射的安全阈值。 波义耳定律也被用于另一个简单的装置,该装置使用一个四通旋塞和一个充满空气的 1 毫升注射器。 如果在注射开始期间,液体弯月面达到 1 mL 注射器的中点(即 0.5 mL),这表明系统中的压力加倍(即,另一个大气压或 14.7 psi)。 这些都是廉价且普遍可用的方法来限制周围神经阻滞期间的注射压力。 实际限制包括需要将注射器保持直立或在吸气时定期将旋塞阀关闭 1-mL 注射器,这样空气就不会进入注射管。
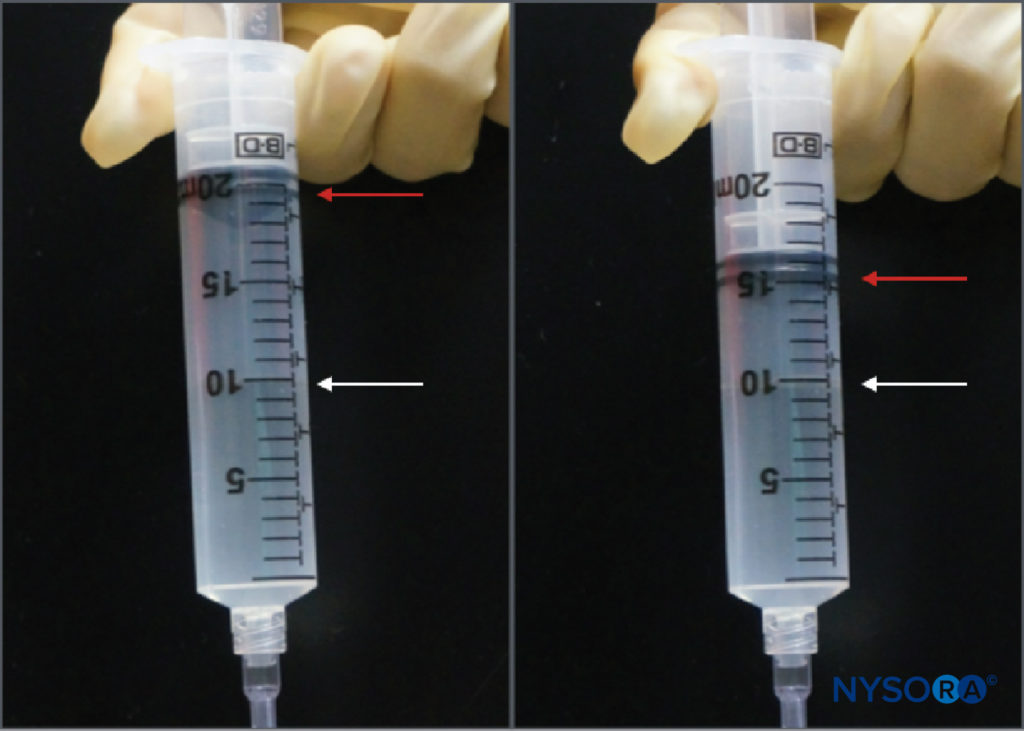
图3。 压缩空气喷射技术。 将 10 mL 的气泡放入局部麻醉剂注射器中,然后将其倒置。 将封闭系统中的气泡压缩到其原始体积的一半(即 5 mL)将使系统中的压力增加 1 个大气压(14.7 psi)。
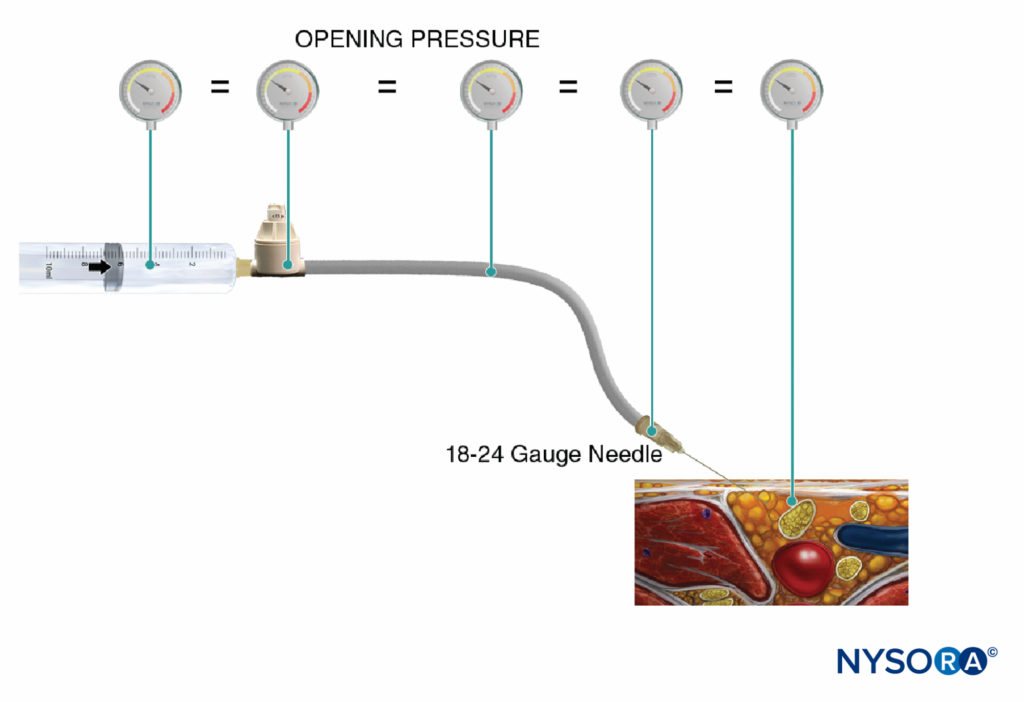
监测注射压力的另一种选择是使用专门为此目的制造的在线一次性压力计。 这些装置将注射器和针管连接起来,并通过弹簧加载活塞,使临床医生能够连续监测注射器-管-针系统中的压力。 活塞轴上的标记描绘了三种不同的压力阈值:小于 15 psi、15–20 psi 和大于 20 psi (图4)。 这种方法的一个优点是执行注射的助手可以轻松读取和传达获得的压力。 该方法还允许在周围神经阻滞过程中客观记录注射压力。 重要的是,开启压力(流动开始时的压力)与注射器、管道、针头或注射速度的大小无关(帕斯卡定律)(图5)。 虽然较小的注射器可以产生更大的压力,并且通过快速注射可以获得更高的注射压力,但开始流动的开启压力是相同的,并且与普通注射器管针尺寸的这些变量无关(即 18- 25 号)。 然而,当注射开始时,这些因素将影响达到的注射压力。 因此,建议在所有神经阻滞程序中使用缓慢、稳定的注射速度(10-15 mL/min)。 开启注射压力与每次针头重新定位和随后的注射有关。 在周围神经阻滞的其他几个方面,压力监测可能是一种有用的安全监测。 Gadsden 等人在一项对接受腰丛神经阻滞的患者进行的研究中,将其随机分配到低(<15 psi)和高(>20 psi)压力组,结果表明,高压组中 60% 的患者经历了双侧硬膜外阻滞。
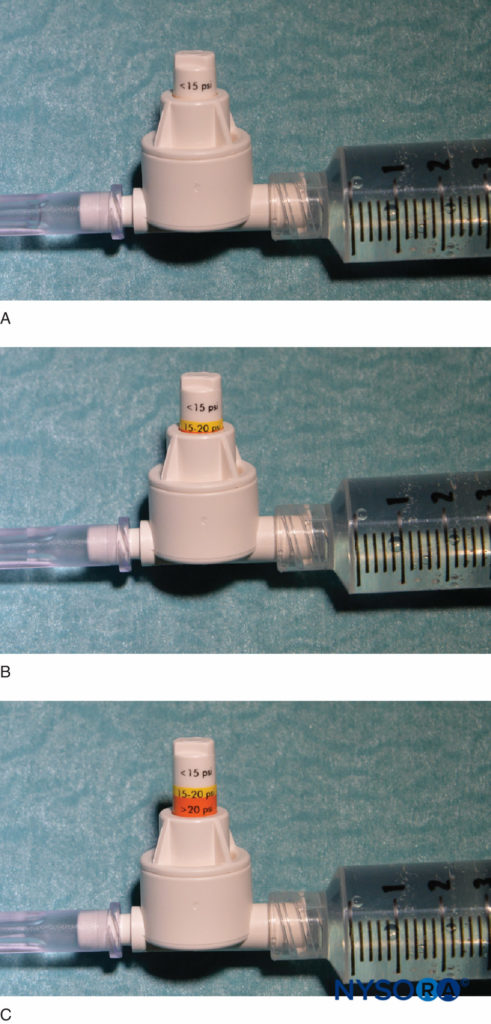
图4。 市售在线压力计的示例(B-Smart,B. Braun Medical,Bethlehem,PA)。 如分别在 A–C 中所见,监视器以颜色显示可移动活塞上的压力范围:0–15 psi(白色)、15–20 psi(黄色)和超过 20 psi(橙色)。 在临床应用中,准确的开放注射压力 (OIP) 不如防止超过与肌束损伤相关的 OIP 范围 (>15 psi) 重要。 实际上,这可以通过在整个注射周期 (>15 psi) 中以任何颜色出现在活塞上而中止注射来避免。 重要的是,开启压力(流动开始时的压力)与注射器、管道和针头或注射速度的大小无关(帕斯卡定律)。
此外,同一组中 50% 的患者在胸部分布出现硬膜外阻滞,而低压组中没有患者出现双侧或硬膜外阻滞。 同样,Gautier 等人证明,当志愿者在肌间沟臂丛神经阻滞期间被随机分配到低压(<15 psi)和高压(>20 psi)时,11% 的高压注射发生了颈椎硬膜外扩散(vs 0% 在低压组)。 此外,所有受试者都要求在高压条件下因不适而停止注射,但在低压注射期间不要求。 这些数据表明,在实施周围神经阻滞期间,监测开放注射压力对于安全性和患者舒适度的几个方面都很重要。
总结
随着更严格和更精确的神经定位方法的发展,区域麻醉已经从艺术过渡到科学。 监控外设块也应该采用相同的过程。 一起使用神经刺激、超声检查和注射压力监测提供了一个互补的客观数据包,可以指导临床医生执行最安全的阻滞。
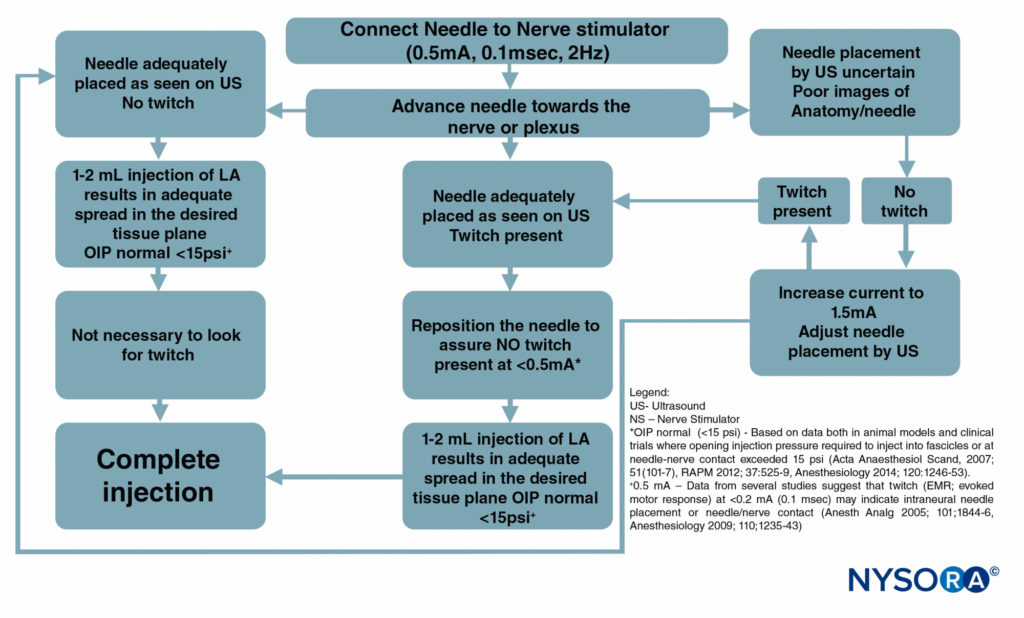
图6 是一个流程图,概述了这些监视器在我们的实践中是如何使用的。
文档
块过程注释
神经阻滞程序的文件已经落后于全身麻醉的文件,并且通常被归为麻醉记录角落的几行潦草的线条。 来自法律、计费和监管来源的压力越来越大,促使人们努力改进周围神经阻滞的文件。 包含本章前面提到的所有监测元素的周围神经阻滞文档表格的样本显示在 数字7 和 8. 这些可以被采用和修改以适应个人实践。 这些表格有许多特征,试图制定自己的程序说明的机构应该考虑这些特征。 其中包括:
纸质记录越来越多地被电子病历保存系统所取代。 使用诸如此类的计算机化系统,块文档很简单,因为可以通过指示相关文档项目从列表中快速选择块变量,而任何叙述元素都可以使用键盘快速键入(图8)。 易读性和更正错误的能力是电子版便笺的优势。
周围神经阻滞文档的另一个有用方面是记录超声图像或视频剪辑,以硬拷贝形式存储在患者病历中,或作为数字拷贝存储在电子健康记录 (EHR) 或单独的安全硬盘驱动器中。 从法医学的角度来看,这不仅是一种良好的做法,而且如果临床医生希望为使用超声引导开具账单,这也是必须采取的必要步骤。 任何硬拷贝都应附有患者识别标签、记录日期以及任何相关发现,并用标记突出显示,例如局部麻醉剂在神经周围扩散。 基本神经阻滞和脊髓麻醉程序的高度实用文档的其他示例显示在 数字9 和 10。
| 外周神经阻滞程序注释的有用特征 | 例如: |
|---|---|
| 指导从业者达到特定护理标准的要素 | 指示在局部麻醉溶液中使用肾上腺素的空格,或者如果没有使用,为什么不使用 |
| 效率和个性化能力之间的折衷 | 使用勾选框和空白行空格记录的信息 |
| 防止常见法医学挑战的文件 | 从业者必须表明患者的意识水平 |
| 符合监管机构的文件(例如,联合委员会) | 勾选框表示偏侧 |
| 促进成功计费的要素 | 许多保险公司要求的语言表明外科医生特别要求的块 |
| 所涉及的临床医生的文件以及以何种身份 | 主治人是执行街区的人,还是他或她在医疗上指导居民? |
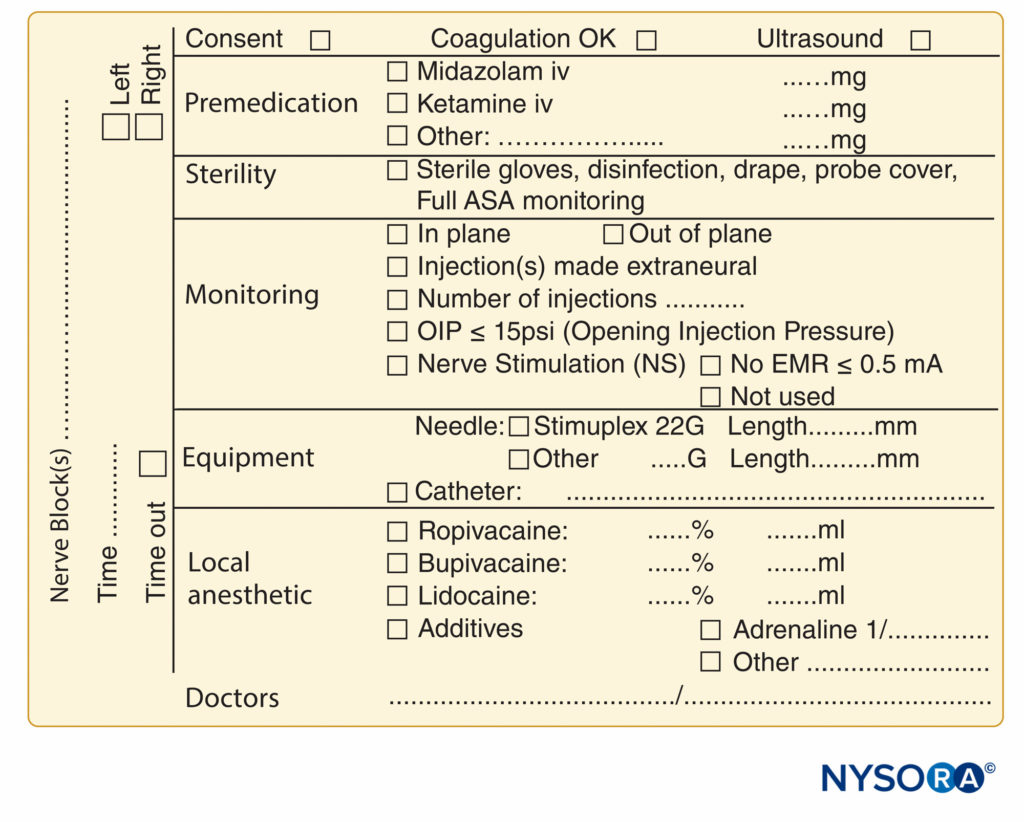
图9。 位于比利时亨克的 ZOL (Ziekenhuis Oost-Limburg) 的 NYSORA-Europe CREER(骨科手术研究、教育和加速康复中心)使用的周围神经阻滞程序文档的基本要素。
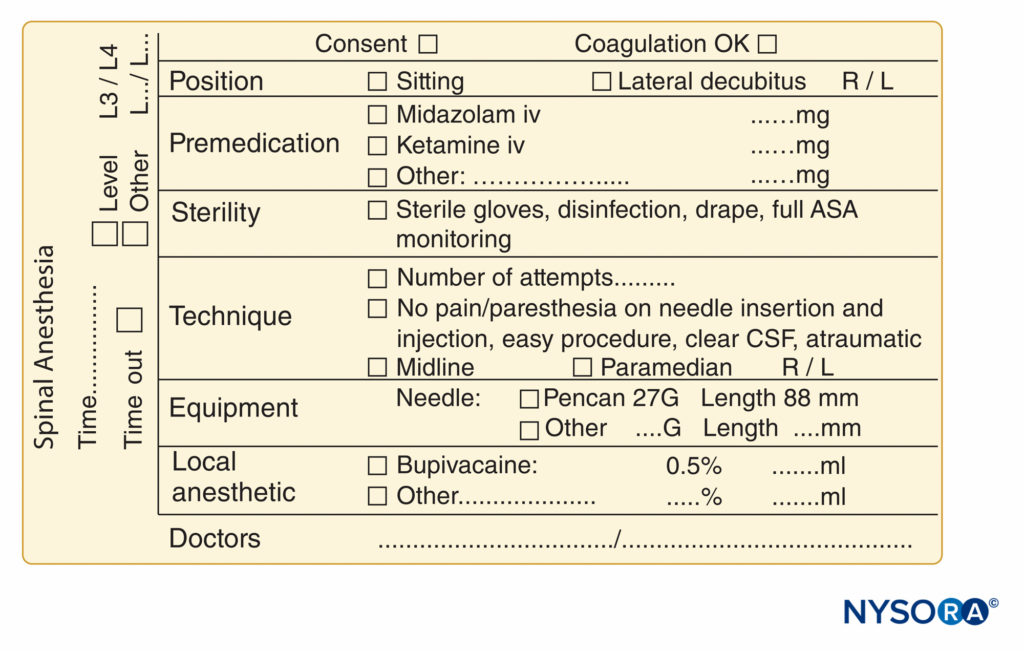
图10。 位于比利时亨克的 ZOL (Ziekenhuis Oost-Limburg) 的 NYSORA-Europe CREER(骨科手术研究、教育和加速康复中心)使用的脊柱麻醉程序文件的基本要素。
知情同意
知情同意文件是区域麻醉实践的一个重要方面。 在这个问题上的实践模式差异很大,并且通常无法获得神经阻滞程序的具体书面同意。 但是,出于多种原因,此过程的书面文档可能很重要:
- 患者在手术当天(当获得许多同意时)经常分心和焦虑,并且可能不记得与麻醉师讨论的细节。 研究表明,知情同意过程的书面记录可以提高患者对风险和收益的回忆。
- 书面同意书确定患者和医生之间就风险和益处进行了讨论。
- 可以定制一份区域麻醉的特定文件,以包括所有常见和严重的风险; 这使医生可以将它们作为例行事项向患者解释,并减少忽略重要风险的机会。
以下提示可用于最大化同意过程:
| 改进同意程序的建议。 |
|---|
| 简洁的。 一个简单、简短的解释比冗长的段落更有助于回忆风险和收益。 |
| 不仅包括严重和主要风险,还包括拟议区域麻醉程序的益处和预期结果。 如果只讨论风险,患者很难做出明智的选择。 |
| 使用同意过程作为同时教育患者的一种手段。 |
| 将表格副本提供给患者。 这已被证明有助于回忆与同意相关的信息。 |
参考文献:
- Buhre W,Rossaint R:麻醉中的围手术期管理和监测。 柳叶刀 2003;362:1839–1846。
- Guinard JP、Mulroy MF、Carpenter RL、Knopes KD:测试剂量:有和没有急性 β-肾上腺素能阻滞的最佳肾上腺素含量。 麻醉学 1990;73:386–392。
- Tanaka M,Sato M,Kimura T,Nishikawa T:模拟血管内试验剂量对镇静患者的疗效。 Anesth Analg 2001;93:1612–1617,目录。
- Karmakar MK,Ho AM-H,Law BK,Wong ASY,Shafer SL,Gin T:罗哌卡因在胸椎旁阻滞后加和不加肾上腺素的动脉和静脉药代动力学。 麻醉学 2005;103:704–711。
- Van Obbergh LJ、Roelants FA、Veyckemans F、Verbeeck RK:在儿童中,添加肾上腺素可改变尾部注射罗哌卡因的药代动力学。 Can J Anaesth 2003;50:593–598。
- Neal JM:局部麻醉剂中肾上腺素对中枢和周围神经系统的影响:神经毒性和神经血流。 Reg Anesth Pain Med 2003;28:124-134。
- Sites BD、Taenzer AH、Herrick MD 等:与 12,668 例超声引导神经阻滞相关的局部麻醉全身毒性和术后神经系统症状的发生率:来自前瞻性临床登记的分析。 Reg Anesth Pain Med 2012;37(5):478–482。
- Perlas A、Niazi A、McCartney C、Chan V、Xu D、Abbas S:通过超声评估的运动反应对神经刺激和神经定位感觉异常的敏感性。 Reg Anesth Pain Med 2006;31:445–450。
- Chan VWS、Brull R、McCartney CJL、Xu D、Abbas S、Shannon P:猪神经内注射和电刺激的超声和组织学研究。 Anesth Analg 2007;104:1281–1284,目录。
- Robards C、Hadzic A、Somasundaram L 等:腘坐骨神经阻滞期间低电流刺激的神经内注射。 Anesth Analg 2009;109:673–677。
- Voelckel WG、Klima G、Krismer AC 等:猪坐骨神经阻滞后的炎症迹象。 Anesth Analg 2005;101:1844–1846。
- Tsai TP、Vuckovic I、Dilberovic F 等:刺激电流的强度可能不是神经内针放置的可靠指标。 Reg Anesth Pain Med 2008;33:207–210。
- Bigeleisen PE,Moayeri N,Groen GJ:超声引导锁骨上阻滞期间的神经外刺激阈值与神经内刺激阈值。 麻醉学 2009;110:1235–1243。
- Wiesmann T、Bornträger A、Vassiliou T 等:引发诱发运动反应的最小电流强度无法区分针-神经接触和神经内针插入。 Anesth Analg 2014;118:681–686。
- Steinfeldt T、Graf J、Schneider J 等:猪模型中神经刺激后针-神经接触的组织学后果。 麻醉剂研究实践 2011;2011:591851。
- Steinfeldt T、Poeschl S、Nimphius W 等人:猪模型中针-神经接触期间的强制进针:组织学结果。 Anesth Analg 2011;113:417–420。
- Gadsden J、Latmore M、Levine DM、Robinson A:高开放注射压力与股神经阻滞期间的针神经和针筋膜接触有关。 Reg Anesth Pain Med 2016;41(1):50-55。
- Hogan QH:区域麻醉期间周围神经损伤的病理生理学。 Reg Anesth Pain Med 2008;33:435–441。
- Whitlock EL,Brenner MJ,Fox IK,Moradzadeh A,Hunter DA,Mackinnon SE:啮齿动物模型中罗哌卡因诱导的周围神经注射损伤。 Anesth Analg 2010;111(1):214–220。
- Sala-Blanch X、Ribalta T、Rivas E 等:神经内针插入后对人体坐骨神经的结构性损伤。 Reg Anesth Pain Med 2009;34:201-205。
- Hadzic A、Dilberovic F、Shah S 等:神经内注射和高注射压力的组合会导致狗的肌束损伤和神经功能缺损。 Reg Anesth Pain Med 2004;29:417–423。
- Gauss A、Tugtekin I、Georgieff M、Dinse-Lambracht A、Keipke D、Gorsewski G:超声引导下锁骨下和锁骨上臂丛神经阻滞中临床症状性气胸的发生率。 麻醉 2014;69:327–336。
- Russon K,Blanco R:用超声观察到的肌皮神经意外神经内注射。 Anesth Analg 2007;105:1504–1505,目录。
- Schafhalter-Zoppoth I,Zeitz ID,Gray AT:超声观察到的无意股神经穿刺和神经内注射。 Anesth Analg 2004;99:627–628。
- Loubert C、Williams SR、Hélie F、Arcand G:超声引导区域阻滞期间的并发症:意外血管内注射局部麻醉剂。 麻醉学 2008;108:759–760。
- Vadeboncouer T, Weinberg G, Oswald S, Angelov F:超声引导锁骨上臂丛神经阻滞过程中血管内注射的早期检测。 Reg Anesth Pain Med 2008;33:278–279。
- Martínez Navas A,DE LA Tabla González RO:超声引导技术允许在锁骨下臂丛神经阻滞期间早期检测血管内注射。 Acta Anaesthesiol Scand 2009;53:968–970。
- Barrington MJ, Kluger R:超声引导可降低周围神经阻滞后局部麻醉剂全身毒性的风险。 Reg Anesth Pain Med 2013;38:289–297。
- Orebaugh SL、Kentor ML、Williams BA:受监督学员与神经刺激器引导和超声引导的周围神经阻滞相关的不良后果:更新单站点数据库。 Reg Anesth Pain Med 2012;37:577–582。
- Casati A、Baciarello M、Di Cianni S 等:超声引导对阻断股神经所需的最小有效麻醉量的影响。 Br J Anaesth 2007;98:823–827。
- Sandhu NS、Bahniwal CS、Capan LM:在超声引导下减少利多卡因体积的锁骨下阻滞的可行性。 超声医学杂志 2006;25:51-56。
- Vandepitte C、Gautier P、Xu D、Salviz EA、Hadzic A:0.75% 的罗哌卡因有效体积,通过肌间沟臂丛阻滞所需的导管。 麻醉学 2013;118:863–867。
- Riazi S、Carmichael N、Awad I、Holtby RM、McCartney CJL:局麻药量(20 对 5 毫升)对超声引导下肌间沟臂丛阻滞的疗效和呼吸后果的影响。 Br J Anaesth 2008;101:549–556。
- O'Donnell B、Riordan J、Ahmad I、Iohom G:简要报告:在超声引导下腋下臂丛神经阻滞中使用 2 毫升 2010% 利多卡因对阻滞特性的临床评估。 Anesth Analg 111;808:810–XNUMX。
- Krediet AC,Moayeri N,Bleys RLAW,Groen GJ:神经内或神经外:用于定位低容量注射的超声评估的诊断准确性。 Reg Anesth Pain Med 2014;39:409–413。
- Liu SS,YaDeau JT,Shaw PM,Wilfred S,Shetty T,Gordon M:超声引导下肌间沟和锁骨上神经阻滞的意外神经内注射和术后神经系统并发症的发生率。 麻醉 2011;66:168–174。
- Hara K,Sakura S,Yokokawa N,Tadenuma S:超声引导下臀下坐骨神经阻滞期间无意神经内注射的发生率和影响。 Reg Anesth Pain Med 2012;37:289–293。
- Bigeleisen PE:超声引导腋窝阻滞期间的神经穿刺和明显的神经内注射并不总是导致神经损伤。 麻醉学 2006;105:779–783。
- Selander D、Dhunér KG、Lundborg G:用于区域麻醉的注射针导致的周围神经损伤。 针尖外伤急性影响的实验研究。 Acta Anaesthesiol Scand 1977;21:182–188。
- Orebaugh SL、Mukalel JJ、Krediet AC 等人:人体尸体模型中的臂丛神经根注射:注射液分布和对神经轴的影响。 Reg Anesth Pain Med 2012;37:525–529。
- Krol A、Szarko M、Vala A、De Andres J:对正中神经、桡神经和尺神经进行神经内和神经周围注射的压力监测:尸体研究的教训。 麻醉疼痛医学 2015;5:e22723。
- Gadsden JC、Choi JJ、Lin E、Robinson A:在超声引导下肌间沟臂丛神经阻滞期间,打开注射压力始终检测针-神经接触。 麻醉学 2014;120:1246–1253。
- Claudio R、Hadzic A、Shih H 等人:麻醉师在模拟周围神经阻滞过程中的注射压力。 Reg Anesth Pain Med 2004;29:201-205。
- Theron PS、Mackay Z、Gonzalez JG、Donaldson N、Blanco R:外周神经阻滞期间“注射器感觉”的动物模型。 Reg Anesth Pain Med 2009;34:330–332。
- Tsui BCH、Knezevich MP、Pillay JJ:使用压缩空气注射技术 (CAIT) 降低注射压力:一项体外研究。 Reg Anesth 疼痛医学 2008;33:168–173。
- Patil J、Ankireddy H、Wilkes A、Williams D、Lim M:一种用于局部神经阻滞/麻醉注射的简易压力计:一项初步研究。 J Clin Monit Comput 2015.doi:10.1007/s10877-015-9701-z。
- Gadsden JC、Lindenmuth DM、Hadzic A、Xu D、Somasundarum L、Flisinski KA:使用高压注射的腰丛神经阻滞导致对侧和硬膜外扩散。 麻醉学 2008;109:683–688。
- Gautier P, Vandepitte C, Schaub I, et al: 放射对比剂在健康志愿者肌间间隙的分布。 Anesth Analg 2015;120:1138–1141。
- Gerancher JC、Grice SC、Dewan DM、Eisenach J:对分娩和分娩硬膜外镇痛前知情同意的评估。 Int J Obstet Anesth 2000;9:168–173。