Ariana Nelson、Honorio T. Benzon、およびRasha S. Jabri
はじめに
脊髄硬膜外血腫(SEH)は、脊柱管の椎骨と硬膜の間の緩い輪状組織に血液が蓄積することです。 通常、血腫は無症候性ですが、まれに脊髄を圧迫し、神経学的に壊滅的な結果をもたらす可能性があります。 これらの症状には、感覚障害、腸および膀胱の失禁、運動衰弱、または重症の場合は患肢の完全な麻痺が含まれます。 この臨床実体は、1682年に医学文献で、Histoire de l'Academie Royale des Science(Volume 2; GJ Duverney)で脊髄硬膜外血腫として最初に記述されました。 ほぼ200年後の1869年に、SEHの最初の臨床診断のレポートがランセットで発表されました。
SEHは、本質的に自発的である場合もあれば、腰椎穿刺などの侵襲的処置の設定で発生する場合もあります。 脊髄幹麻酔、または脊椎手術。 血腫は、腰椎および特に馬尾領域の体積補償に利用できるより広いスペースと比較して、この領域の脊柱管が収縮していることを考えると、頸部および胸部領域で症候性である可能性が高くなります。
脊髄硬膜外血腫
入射
症候性SEHは、脊髄腔を占めるすべての病変の1%未満を占め4、毎年1万人に1人しか影響を及ぼしません。 SEHは無数の病因から生じますが、ほとんどの場合、硬膜外腔内またはその近くで行われる手技から生じます。 たとえば、SEHの存在は、脊椎手術後の患者の33%から100%の術後画像で確認できますが、患者が神経学的欠損を示すことはめったにありません。 2010年の系統的レビューでは、脊椎手術後の症候性SEHの全体的な計算された発生率は0.2%であり、個々の研究の計算は0%から1.0%の範囲でした。 したがって、SEHの発生率は、症候性SEHの発生率として日常的に引用されています。 以降、この章では、症候性という修飾用語が暗示されます。
脊髄幹麻酔後のSEHの発生率は、歴史的に、硬膜外麻酔の1分の150,000未満、脊髄くも膜下麻酔の1分の220,000未満であると概算されてきました。 しかし、最近の疫学研究によれば、発生率は増加している可能性があります。 この推定は、1:18,000の硬膜外ブロック後のSEHの発生率を発見した大規模なスウェーデンの研究によって確認されました。これは、1:200,000の産科発生率と1:3600の非常に高い発生率の平均から得られた数値です。膝関節形成術を受けている高齢の女性患者の集団で。 別の研究では、評価された母集団が下肢手術を受けている年配の女性のみを含むように狭められた場合、1:4741の全体的なSEH発生率が1:1000に増加したことが示されました。
この大きな格差は、これらの不一致の患者集団における危険因子の有無に起因する可能性があります。 妊娠は比較的凝固亢進状態を誘発し、産科患者はまた、高齢患者よりも大きく、より順応性のある硬膜外腔で若くなります。 産科患者におけるSEHの発生率の低下は、周産期に評価された709,837人の患者にSEHの認識された症例がなかった最近の研究で確認されました。 この研究では、周術期硬膜外留置を受けた患者で1:9000(95%信頼区間[CI]:1:20,189–1:4330)の発生率が認められました。
危険因子
年齢が上がると、SEHのリスクも高まります。 年齢に伴う硬膜外腔のサイズの縮小は、局所麻酔薬の広がりの研究で1967年に最初に報告されました。
これは、同量の血液が若い患者と比較して高齢患者のより小さな硬膜外腔の圧力を増加させるため、高齢者におけるSEHの発生率が高いことを説明するために推定することができます。 人種的な好みは報告されていませんが、SEHは女性でより頻繁に見られます。 これは、女性患者の骨粗鬆症の有病率が高いことによって説明される可能性があります。これは、椎骨の変形または骨折、および脊柱管の狭窄をもたらす椎体の拡大を引き起こします。 したがって、硬膜外腔の骨粗鬆症による狭窄は、SEHの性別と年齢の偏見の両方を説明する可能性があり、硬膜外分娩鎮痛と比較して、膝関節形成術の硬膜外麻酔後のSEHの可能性が50倍以上増加する可能性があります。 ただし、整形外科の集団では血栓予防が必要であり、深部静脈血栓症に対する定期的な予防を必要としない産科患者と比較して、SEHの発生率が比較的高いことに寄与する可能性があります。
確かに、SEHの最も重要な危険因子は、肝疾患、アルコール依存症、血小板減少症、または薬理学的抗凝固などの凝固系の生理学的またはiatrogenic障害の存在です。 最近の後ろ向き研究でも、Rh +血液型、1 Lを超える術中失血、10 g / dL未満のヘモグロビンレベル、および最初の2.0で48を超える国際感度比の患者における脊椎手術後のSEHの有意な増加が確認されました。時間。 脊髄幹麻酔に関連する抗凝固療法、ならびに抗凝固の長さと強度は、硬膜外血腫の最も重要な危険因子として特定されています。 すべてのSEH症例の約87分のXNUMXからXNUMX分のXNUMXは、抗凝固療法に関連しています。 脊髄幹麻酔に関連するSEHのすべての症例の広範なレビューでは、XNUMX%の患者が血液学的異常または技術的困難を伴う手技のいずれかを患っていました。 自然発生的な血腫の症例はまれですが、それらが発生した場合、抗凝固、血栓溶解、血液の悪液質、凝固障害、血小板減少症、新生物、血管奇形、または脊椎血管腫に関連することがよくあります。
抗凝固反応を誇張する可能性のある患者の体重の減少は、出血傾向の理論的懸念を表しており、女性および高齢者のリスク増加の説明として示唆されています。 しかし、スウェーデンでは、深部静脈血栓症の予防のための低分子量ヘパリンの性別ごとの減量が、女性におけるSEHの発生率の増加を改善することは示されていません。 血栓溶解療法は出血性合併症のリスクが最も高く、最近血栓溶解を受けた患者では脊髄幹麻酔を熱心に避ける必要があります。 詳細については 抗凝固薬を服用している患者の脊髄幹麻酔と末梢神経ブロック。
クリニカルパール
- 明白な危険因子のない患者における脊髄血腫のリスクの発生率に関する最近の研究は、硬膜外投与後に1:18,000に増加し、下肢手術を受けている高齢患者では1:3600、さらには1:1000に増加することを示しました。
血腫の病因と位置
SEHを引き起こす提案された要因には、外傷、抗凝固、血栓溶解、腰椎穿刺、硬膜外または脊椎麻酔、介入的脊椎手術または手術、凝固障害または出血性素因、門脈高血圧を伴う肝疾患、血管奇形、椎間板ヘルニア、脊椎骨のパジェット病が含まれます、Valsalvaの操作、および高血圧。 自然発生的なSEHの最も重要な原因は凝固障害であり、これは後天性(例、抗凝固療法、悪性腫瘍)または先天性(例、血友病)の可能性があります。 血管奇形が自発性硬膜外血腫の原因となることはめったにありません。 一連の4例でわずか158%、一連の6.5例で199%が血管奇形が原因であると報告されました。 あまり一般的ではない素因には、全身性エリテマトーデス、強直性脊椎炎、関節リウマチ、パジェット病、椎間板ヘルニア、高血圧などがあります。
背側静脈叢は、この神経叢に弁がなく、身体活動による血管内圧の上昇中に血流が逆転する可能性があるため、最も一般的に関係する出血の原因です。 これらの静脈は疎性結合組織にのみ囲まれているため保護が不足しているため、腹腔内または胸腔内の圧力が急激に上昇し、破裂や出血を引き起こしやすくなります。 硬膜外静脈叢は胸椎で最も顕著であり、自発的なSEHは胸椎および頸胸腔領域で最も頻繁に発生し、胸腰部がそれに続きます。 SEHは通常、髄腔の後方または後方にあります(図1)脊柱管の腹側の側面で後縦靭帯に硬膜嚢がしっかりと付着しているため、血腫の蓄積が防止されます。 胸部または腰部の背側の側面は一般的に関与しており、拡張は通常、わずかな椎骨レベルに制限されています。
妊娠中の女性では、妊娠の血行力学的変化に関連して、子宮の肥大による静脈圧の上昇が、既存の病的な硬膜外静脈叢壁の破裂の素因となる可能性があることが提案されています。 静脈源が最も広く受け入れられていますが、SEHの潜在的な動脈源に関して議論が続いており、この理論の支持者は、静脈圧が髄腔内圧よりも低いと述べています。 したがって、低圧硬膜外腔への順方向の流れは可能ですが、静脈血は脊髄の圧迫を引き起こすことはできませんでした。
NYSORAのヒント
- 脊柱管への出血は、顕著な硬膜外静脈叢のために、最も一般的に硬膜外腔で発生します。
- SEHは自発的である場合もあれば、腰椎穿刺や脊髄幹麻酔などの軽度の外傷に続く場合もあります。
- SEHは、主に抗凝固療法または血小板減少症の患者に発生します。
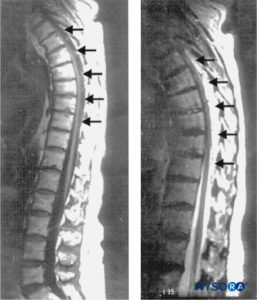
図1 胸腰椎の矢状磁気共鳴画像。 T3からT10、T11まで伸びる大きく複雑な硬膜外血腫は、T1強調画像(左;矢印)では低信号および等密度信号特性、T2強調画像(右;矢印)では高信号信号特性で見られます。 血腫の中心では、脊髄が胸椎の後面に接しています。
体(左)。 コード自体の信号異常は見られません。 (Schwarz SK、Wong CLの許可を得て複製、
マクドナルドWN:脊髄硬膜外血腫からの自然回復と非高齢者の非定型症状。 Jアナエスができます。 2004年51月〜6月; 557(561):XNUMX–XNUMX。)
歴史と身体検査
古典的に、SEHの症状は急性の軸性腰痛であり、対応する皮膚炎に放射状に広がり、神経根または脊髄圧迫の兆候を伴う限局性の神経学的欠損に発展します。 痛みは一般に、特に腰椎の椎間板ヘルニアを模倣する可能性のある神経根成分の有無にかかわらず、重度の局所的な一定の腰痛として説明されます。
腰痛は、脊椎への打診や、咳、くしゃみ、緊張などの脊椎内圧を上昇させる操作によって増幅されます。 ただし、2010年の分析では、腰痛は依然として一般的な初期症状であるにもかかわらず、下肢の脱力が最も一般的な兆候であることが示されました。 関連する症状には、しびれ、脱力感、尿失禁または便失禁などがあります。 痛みの発症は、持ち上げる、咳をする、くしゃみをする、バルサルバ法などの軽度の緊張に関連する場合がありますが、ほとんどの場合、痛みの発症は自然発生的です。
血腫のレベルとサイズに応じて、身体的所見には、片側または両側の脱力感、片側または両側の神経根性知覚異常を伴う感覚障害、深部腱反射のさまざまな変化、膀胱または肛門括約筋の緊張の変化が含まれる場合があります。 脊髄および神経根の機能障害の兆候は急速に現れ、対麻痺、または胸部または頸部の高い場所では対麻痺に進行する可能性があります。 脊髄幹麻酔または腰椎穿刺に関連するSEHの場合、新しいまたは進行性の術後神経症状の存在は、硬膜外血腫の可能性について医師に警告する必要があります。
NYSORAのヒント
- 患者は、椎間板ヘルニアを模倣する可能性のある神経根成分の有無にかかわらず、重度の局所的な一定の腰痛を呈する場合があります。
- 関連する症状には、脱力感、しびれ、尿失禁または便失禁などがあります。
- 脊髄または硬膜外ブロックが摩耗してから数時間後の感覚または運動障害の再発(腰痛の有無にかかわらず)は非常に病的であり、そうでないことが証明されるまで、脊髄または硬膜外血腫と見なして治療する必要があります。
- 保守的な管理後の神経学的回復は、麻痺のない腰痛と脚の衰弱のある患者で報告されています。
- 完全な運動障害から36時間以内、および部分的な障害から48時間以内に手術と減圧を行うと、神経学的回復が起こる可能性があります。
診断
前述のように、SEHの臨床所見には通常、対麻痺、四肢麻痺、または自律神経機能障害に急速に進行する可能性のある腰痛および運動/感覚障害が含まれます。
硬膜外血腫は通常、手術後最初の24〜48時間以内に現れます。 新規または進行性の神経学的症状は、硬膜外血腫を含む空間を占める病変を除外するための即時の臨床評価および診断的精密検査を保証します。 硬膜外鎮痛の存在下で発生する神経学的欠損は、局所麻酔薬からの寄与を除外するために、カテーテルを所定の位置に残したまま、注入を直ちに中止することを義務付けています。
硬膜外注入が神経学的症状の原因である場合、感覚および運動機能の回復が認められます。 それ以外の場合は、即時の精密検査とX線画像検査を取得し、脊椎外科医との協議により、進展する硬膜外病変を除外する必要があります。
神経学的欠損の進行を伴う急性軸性腰痛を呈する患者では、SEHをシミュレートするその他の病変を区別するために、神経根および脊髄圧迫に関連する病理学的実体の存在の即時評価が必要です。 硬膜外血腫が疑われる患者の臨床症状は、硬膜外膿瘍、脊髄疾患、新生物、または急性椎間板ヘルニアの症状に似ている可能性があります。 新規または進行性の術後神経症状の鑑別診断には、外科的神経弛緩、長期または誇張された神経軸ブロック、前脊髄動脈症候群、既存の神経障害の悪化、および以前に診断されていない神経状態の提示が含まれる。
出血の程度を評価し、感染の存在を判断するために、血小板を含む全血球計算を注文する必要があります。 プロトロンビン時間と活性化部分トロンボプラスチン時間は、出血素因の存在を決定します。
SEHの治療の遅れを最小限に抑えるには、迅速な放射線学的評価が不可欠です。 現在、磁気共鳴画像法(MRI)は、すべての面で脊柱と脊髄の迅速で非侵襲的な評価を可能にするため、脊椎の緊急事態に最適な画像診断法です。 脊椎MRIは、硬膜外血腫の位置を描写し、関連する血管奇形を特定する場合があります。 また、血腫の程度や脊髄圧迫の程度に関する情報も提供します。 MRIは、血腫の年齢の評価にも役立ちます(図1).
SEHのMRIの時間的特徴は、頭蓋内出血で見られるものと類似しています。 超急性期(最初の6時間)では、細胞内オキシヘモグロビンの存在の結果として、SEHはT1強調画像では脊髄と比較して等強度に見え、T2強調画像では軽度に高信号で不均一に見えます。 急性期(7〜72時間)では、血腫はT1強調画像では依然として等強度であり、T2強調画像では低強度になります。 これは、T2短縮を引き起こす細胞内デオキシヘモグロビンの存在によるものです。 メトヘモグロビンの濃度が増加すると、血腫はT1およびT2強調画像で高信号で均一になります。 ガドリニウム造影磁気共鳴血管造影(MRA)は、動静脈奇形の範囲をさらに明確にする可能性があります。
従来のコンピューター断層撮影(CT)は硬膜外血腫を診断する可能性がありますが、血腫が髄腔または脊髄に等密度であり、画質が胸部上部によく見られるアーチファクトの影響を受ける場合、偽陰性の結果をもたらす可能性があります。 脊椎CTスキャンは、肺実質と脊椎骨のコントラストが高いため、腰椎や頸椎よりも解像度が低い胸椎では診断できない場合があります。 血管形成の存在を明確に示すために、従来の血管造影法が必要となる場合があります。
脊髄造影、およびその後のCT脊髄造影は、以前は硬膜外血腫の診断の主なモダリティでした。 脊髄CTスキャンと組み合わせると、脊髄造影はSEHを脊髄内両凸および血液と同等の密度の超高密度病変として表示します。 これは、部分的または完全な脊髄ブロックを伴う硬膜外病変を示している可能性がありますが、所見は特定されていません。 さらに、脊髄造影は侵襲的であり、患者の臨床状態を悪化させる可能性があります。 さらに、非特異的造影ブロックまたは硬膜外凸状圧迫の視覚化により圧迫の兆候を示すことはできますが、脊髄造影では病変の性質と真の範囲を特定することはできません。 MRIがゴールドスタンダードの診断手段になっているため、これらの技術は現在、米国ではめったに使用されていません。
予防、治療、および予後
抗凝固療法を受けている、血栓溶解療法を受けている、または出血素因が疑われる個人では、腰椎穿刺または硬膜外麻酔を避ける必要があります。 麻酔科医は、抗凝固プロトコル、新しい抗凝固薬、および現在のガイドラインの推奨事項に関する知識を最新のものにすることが求められます。 抗血栓療法を受けている患者に脊髄幹麻酔を実施するかどうかの決定とカテーテル除去のタイミングは、特定の患者に対する局所麻酔の利点と脊髄硬膜外血腫のリスクを比較検討して、個別に行う必要があります。 American Society ofRegionalAnesthesiaとEuropeanandScandinavian Society of Anaesthesiologistsは、脊髄幹麻酔と抗凝固療法に関するコンセンサスステートメントを発表しました。これは、リスクのある患者に脊髄幹麻酔を行う際の意思決定プロセスのガイドラインに関する最新の情報源を提供します。要因(抗凝固薬を服用している患者の脊髄幹麻酔と末梢神経ブロックを参照)。
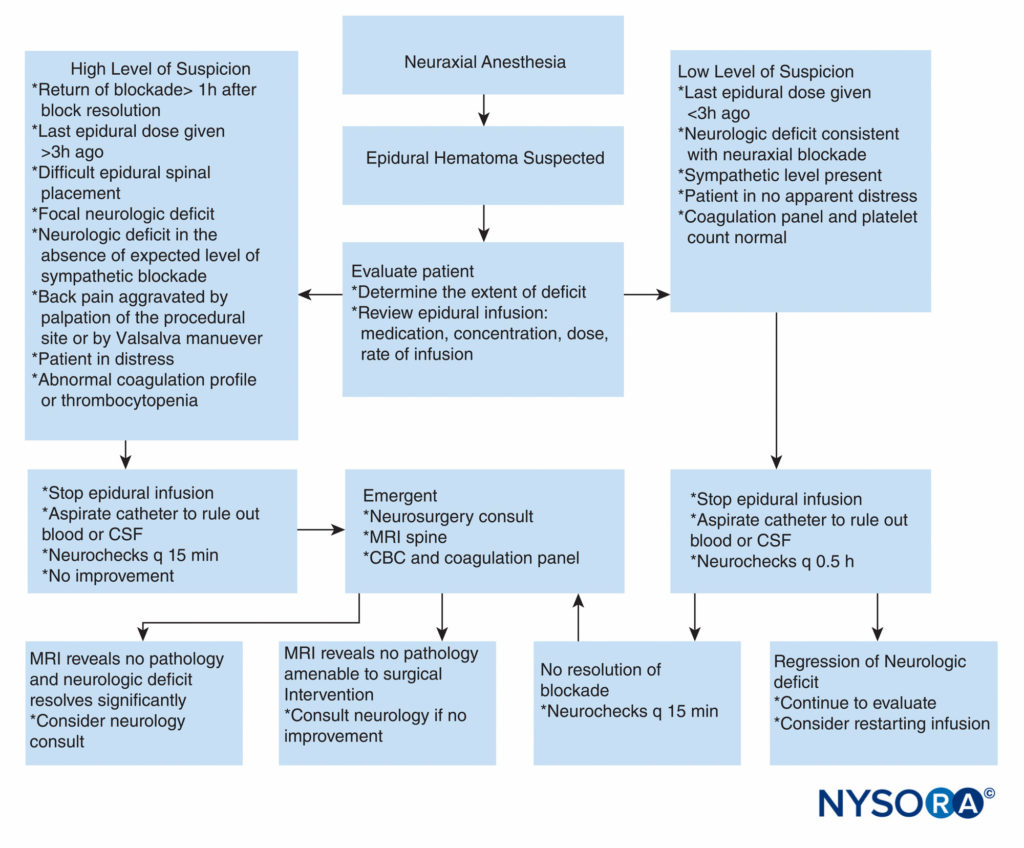
対照的に、外科患者の抗凝固に関するガイドラインはありません。 脊椎手術後の術後血腫の発生率に関する最近の後ろ向き研究では、SEH形成の可能性に影響を与えないように思われるため、おそらく患者は深部静脈血栓症の予防を受けるべきであると結論付けました。 ただし、SEHの壊滅的な結果を考えると、脊椎手術後の血栓予防の広範な施設の前に、さらなる前向き研究が必要です。 症例報告は、硬膜外血腫の保存的管理の成功を説明しています。 良好な転帰を伴う非手術的治療は、主に馬尾レベルに限局した血腫および軽度の神経学的欠損を伴う血腫で報告された。 患者が腰痛および下肢の脱力またはしびれを報告したが、下肢の麻痺を示さない場合、保守的な管理で完全な回復が起こり得るように思われる。 凝固異常の逆転、神経学的欠損の綿密な観察、そしてまれに、ステロイド投与は、手術なしで良い結果を達成するかもしれません。 疑わしい硬膜外血腫の管理への実際的なアプローチは、 図2.
緊急の外科的減圧は、臍帯機能の急性の妥協を引き起こすSEHのための選択の治療法です。 椎弓切除術に続いて、血腫の排出、出血部位の凝固、および硬膜の検査が行われます。 その後、硬膜が骨に固定され、硬膜外ドレナージが24時間使用されることがあります。 歴史的にドレーンの有効性については議論の余地がありますが、最近のデータは、顔面下ドレーンがSEH形成を大幅に減少させることを示唆しています。 手術なしでの長期の麻痺後の回復はまれであり、緊急の減圧椎弓切除術を検討するための外科的診察はできるだけ早く受けなければなりません。 全体の死亡率は8%です。 最終的に、手術チームはケースバイケースで観察または手術を決定する必要があります。 SEH後の回復の重要な要因は、術前の神経学的欠損のレベルと手術間隔です。 神経学的回復の予後は、主に患者の術前の神経学的状態および神経学的機能不全の期間に依存します。 怪我と外科的介入の間に遅延があると、予後は悪化します。
以前は、麻痺の発症と外科的介入の間に8時間以上経過した場合、完全な神経学的回復はありそうにないと考えられていました。 しかし、他の著者は、麻痺から12時間以内に手術を行うと回復することを指摘しています。
介入のためのこの推奨される時間枠は、不完全な運動障害から48時間以内、および完全な運動障害から36時間以内に手術を行うと、回復が達成できるという最近の発見によってさらに詳しく説明されています(テーブル1)。 72時間の症状の後の機能回復が報告されていることに注目するのは興味深いことです。 そのような間隔の後に機能回復が起こるかもしれないことは安心ですが、患者の症状の評価と緊急MRIには時間がかかります。 したがって、血腫の潜在的な緊急避難について脊椎外科医と相談する必要があります。
表1 手術のタイミングに関連した神経学的回復。
| 著者 | 麻痺と回復の間隔 |
|---|---|
| ウルフ68 | 完了の8時間36時間 運動障害 |
| ロートン他48 | 不完全な12時間48時間 運動障害 |
| GroenとVanAlphen69 |
脊髄硬膜外血腫:まとめ
脊髄硬膜外血腫は神経学的悪化のまれな原因であり、出血の場所と大きさに応じてさまざまな程度の自律神経、感覚、および運動障害を引き起こす可能性があります。 SEHは、急性または慢性、自発的、心的外傷後、または医原性である可能性があります。 既知の危険因子には、技術的に困難な脊髄幹麻酔、内因性または後天性凝固障害の存在、女性の性別、および高齢が含まれます。 文献の一貫性のないデータによって証明される潜在的な危険因子には、低ヘモグロビンレベル、Rh +抗体の存在、および脊髄の解剖学的異常が含まれます。 SEHはまれですが、脊髄圧迫の潜在的に可逆的な原因であることを考えると、完全な回復を可能にするために診断を遅滞なく行うことが不可欠です。 脊髄血腫は、特定可能な危険因子がない場合でも発生する可能性があります。 したがって、医療提供者は、新しい神経学的症状を監視する際に、疑惑と警戒の高い指標を維持する必要があります。
MRIはCTスキャンの速さで実施することはできませんが、感度が高く特異的であるため、診断モダリティとして選択されます。 神経学的悪化の迅速な検出は、早期の画像診断と迅速な介入にとって重要です。 麻痺がない場合、手術なしで回復が起こる可能性があることに注意することは心強いことです。 麻痺が発生した場合、脊髄と神経根の外科的減圧は、適度に速い間隔で達成された場合、完全な機能回復をもたらす可能性があります。 介入が遅れた場合、SEHの永続的な後遺症には、感覚障害、対麻痺、痙縮、神経因性疼痛、および尿道または肛門括約筋の機能障害が含まれる可能性があります。
神経ブロック後の末梢血腫
硬膜外腔の血腫は確かに、脊髄くも膜下麻酔または末梢局所麻酔の最も破壊的な出血性後遺症ですが、血腫は、単発または連続的な神経ブロックの後に末梢でも発生する可能性があります。 最も一般的な危険因子は、手順の難しさとそれに伴う抗凝固療法または抗血小板療法であるように思われます。 この合併症は非常にまれであり、これまでの文献で報告されている末梢神経ブロック(PNB)後の血腫は30例未満であり、出血が圧縮可能な末梢空間で発生することを考えると、SEHと比較してその結果はそれほど悲惨ではありません。
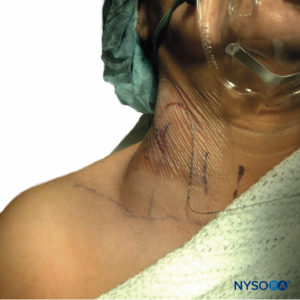
SEHとは対照的に、PNB後の血腫の症状は、神経学的機能障害はめったにありませんが、より一般的には目に見えるあざです(図3)、局所的な圧痛、ヘモグロビン/ヘマトクリット値の低下、または失血による相対的な低血圧。 これは、抗血小板療法の設定で腰椎交感神経ブロック後の後腹膜出血に続発する患者の死亡例が3つ報告されているため、末梢空間の順応性が重大な罹患率と死亡率を排除するということではありません。 患者は剖検で後腹膜腔でXNUMXLの血液を失ったことが判明しました。これは、従順な末梢によってもたらされる潜在的な脅威を物語っています。 実際、入院期間の延長、輸血の必要性、急性腎不全など、PNB血腫が原因で患者が重大な病的状態に陥った他のいくつかの症例が報告されています。
文献で報告されているすべての症例で、神経学的欠損が存在する場合、1年までに解消したことを考えると、罹患率のより懸念される原因は血腫への失血であるように思われます。 ただし、この合併症のまれな性質のため、抗凝固療法の設定でこの手順に関する推奨を専門家が行うことは困難です。 この困難は、米国地域麻酔疼痛医学会(ASRA)のガイドラインに従っている開業医にもかかわらず、血腫が発生した症例報告の存在によって悪化します。 さらに、エノキサパリンまたはXNUMX日XNUMX回のヘパリンを服用している患者に発生した自然発生血腫の症例が報告されています。 まとめると、これらの事実は、さまざまな国でいくぶん対照的なガイドラインにつながっています。 たとえば、ドイツ麻酔科集中治療学会は、PNBの前に抗凝固療法を中止することに関する推奨事項を発表しましたが、オーストリア学会は、坐骨神経痛や腋窩ブロックなどの遠位PNBが抗凝固療法を受けている患者に実施される可能性があると述べています。
ASRAガイドラインでは、脊髄幹麻酔に関する推奨事項を深部神経叢ブロックおよびPNBに適用する必要があると述べています。 したがって、抗凝固療法を受けている患者はこれらの麻酔技術の候補ではありませんが、一部の研究者は、超音波ガイダンスの出現により、これらの抗凝固療法を受けている患者は末梢神経の遮断を安全に受けることができると示唆しました。 さらに、研究では、超音波の使用による血管穿刺の発生率の低下だけでなく、局所麻酔薬の毒性率の低下も示されました。 このオプションは、抗凝固療法を受けている患者が全身麻酔のリスク要因を持っていることが多く、血行動態と体液状態の結果として生じる変動を回避することで恩恵を受けることを考えると、患者の安全性を向上させる可能性があります。
CTスキャンは現在、末梢組織、特に後腹膜腔の血液を診断するための最も一般的な画像技術です。 ただし、超音波は腎被膜下血腫の存在を示すために使用されています93 そして、この視覚化の方法に適した身体の領域では、CTよりも簡単にアクセスできる診断技術になる可能性があります。 PNBの初期配置での超音波の使用の増加は、超音波装置がすぐに利用できるようになるため、ブロック後血腫の疑いのある症例の診断を容易にする可能性があります。
タイムリーな診断が理想的ですが、PNB後の血腫のその後の治療は通常、待機療法です。 通常、外科チームに相談し、必要に応じて輸血を命じ、重症または急速に悪化している患者にのみ外科的ドレナージを検討します。 腰筋血腫の特定の症例報告は、血腫の外科的排出なしに解決し、患者は診断後数日から4ヶ月で感覚と運動の状態を取り戻しました。 末梢神経カテーテルに付随する血腫に関しては、これらもしばしば自己制限的ですが、外科的ドレナージが行われたという報告があります。
PNBまたは継続的な神経ブロック後の出血に関して利用可能なデータが不足していることを考えると、特定の患者に対する特定の麻酔技術の優位性を正確に判断することは難しい場合があります。 麻酔科医は、抗凝固薬を服用している患者のPNBの適合性に基づいて決定を個別化し、いつものように、ブロックのリスクと利点について患者と外科医と詳細に話し合う必要があります。 ブロックが行われる場合、患者は周術期に末梢血腫の徴候と症状を注意深く観察する必要があります。
参考文献
- Plagne R:L'hematoma硬膜外ラキジエン非外傷性(血腫硬膜外自発的)[論文]。 クレルモンフェラン、フランス:クレルモンフェラン大学、1961年。
- ジャクソンR:脊椎脳卒中の症例。 Lancet 1869; 2:538–539。
- Holtas S、Heiling M、Lonntoft M:自発性脊髄硬膜外血腫:MR画像と臨床相関での所見。 Radiology 1996; 199:409–413。
- Alexiadou-Rudolf C、Ernestus R、Nanassis K、et al:急性非外傷性脊髄硬膜外血腫。 Spine 1998; 23:1810–1813。
- Tekkok IH、Cataltepe O、Tata K、et al:継続的な硬膜外麻酔後の硬膜外血腫。 Br J Anaesth 1991; 67:112–115。
- Hejazi N、Thaper PY、Hassler W:非外傷性脊髄硬膜外血腫の1998例。 Neurol Med Chir 38; 718:723–XNUMX。
- Sokolowski MJ、Garvey TA、Perl Jら:術後腰部硬膜外血腫の前向き研究。 Spine 2008; 33:108–113。
- Glotzbecker MP、Bono CM、Wood KB、Harris M:術後脊髄硬膜外血腫:系統的レビュー。 Spine 2010; 35:E413–E420。
- トリバM:硬膜外局所麻酔と低分子ヘパリン:プロ[ドイツ語]。 Anasthesiol Intensivmed Notfallmed Schmerzther 1993; 28:179–181。
- Horlocker T:局所麻酔と急性疼痛管理の合併症。 Anesthesiol Clin 2011; 29:257–278。
- Moen V、Dahlgren N、Irestedt L:1990〜1999年のスウェーデンにおける中央脊髄幹麻酔後の重度の神経学的合併症。 Anesthesiology 2004; 101:950–959。
- Popping DM、Zahn PK、Van Aken HK、Dasch B、Boche R、Pogatzki-Zahn EM:術後疼痛管理の有効性と安全性:18,925年から1998年までの2006人の連続患者の調査(第2改訂):前向きに提起されたデータベース分析データ。 Br J Anaesth 2008; 101:832–840。
- Horlocker T、Kopp S:米国での硬膜外ブロック後の硬膜外血腫:整形外科手術後の低分子量ヘパリンだけではありません。 Anesth Analg 2013; 116:1195–1197。
- Bateman BT、Mhyre JM、Ehrenfeld J、et al:周術期および産科硬膜外カテーテル挿入後の硬膜外血腫のリスクと転帰:多施設周術期転帰グループ研究コンソーシアムからの報告。 Anesth Analg 2013; 116:1380–1385。
- Usubiaga JE、WJ、Usabiaga LE:硬膜外圧と硬膜外腔における麻酔液の拡散との関係。 Anesth Analg 1967; 46:440–446。
- Cummings SR、Nevitt MC、Browner WS、et al:骨粗鬆症性骨折研究グループの研究:白人女性の股関節骨折の危険因子。 N Engl J Med 1995; 332:767–773。
- Hasserius R、Johnell O、Nilsson BE、et al:股関節骨折患者は、人口ベースの研究の被験者よりも脊椎の変形が多い。 ボーン2003; 32:180–184。
- Awad JK、Kebaish KM、Donigan J、Cohen DB、Kostuik JP:術後脊髄硬膜外血腫の発症の危険因子の分析。 J Bone Joint Surg Br 2005; 87:1248–1252。
- Horlocker TT、Wedel DJ:脊髄幹麻酔と低分子量ヘパリン:周術期鎮痛と血栓予防のバランスを取ります。 Reg Anesth 1998; 23:164–177。
- Johnston RA:急性脊髄圧迫の管理。 J Neurol Neurosurg Psychiatr 1993; 56:1046–1054。
- Wysowski DK、Talarico L、Bacsanyi J、et al:脊髄および硬膜外血腫および低分子量ヘパリン。 N Engl J Med 1998; 338:1774–1775。
- Vandermeulen E、Van Aken H、Vermylen J:抗凝固剤と脊髄硬膜麻酔。 Anesth Analg 1994; 79:1165–1177。
- Dickman CA、Shedd SA、Spetzler RF:硬膜外麻酔に関連する脊髄硬膜外血腫:末梢血管血栓溶解療法を受けている患者における全身ヘパリン化の合併症。 麻酔学1990;72:947–950。
- Mattle H、Sieb JP、Rohner M、et al:非外傷性脊髄硬膜外および硬膜下血腫。 Neurology 1987; 37:1351–1356。
- Levine MN、Goldhaber SZ、Gore JM、et al:心筋梗塞および静脈血栓塞栓症の治療における血栓溶解療法の出血性合併症。 胸部1995;108(Suppl 4):291S–301S。
- Graziani N、Bouillot P、Figarella-Bragner D、et al:海綿状血管腫および脊髄硬膜外腔の動静脈奇形:11症例の報告。 Neurosurgery 1994; 35:856–864。
- Harik S、Raichle M、Reis D:抗凝固薬を服用している患者の脊髄硬膜外血腫を自発的に寛解させます。 N Engl J Med 1971; 284:1355–1357。
- Zuccarello M、Scanarini M、D'Avella、et al:抗凝固療法中の自発性脊髄硬膜外血腫。 Surg Neurol 1980; 14:411–413。
- Chen C、Fang W、Chen C、et al:寛解と再発を繰り返す自発性脊髄硬膜外血腫。 Neuroradiology 1997; 39:737–740。
- Groen R、Ponssen H:自発性脊髄硬膜外血腫:病因の研究。 J Neurolog Sci 1990; 98:121–138。
- パッカーN、カミンズB:自発的な硬膜外出血:外科的緊急事態。 Lancet 1978; 1:356–358。
- Hebl JR、Horlocker TT、Kopp SL、Schroeder DR:脊柱管狭窄症、腰椎椎間板疾患、または以前の脊椎手術を受けた患者の脊髄幹麻酔:有効性と神経学的合併症。 Anesth Analg 2010; 111:1511–1519。
- ジョセフA、ビネンJ:急性脊髄硬膜外血腫。 J Emerg Med 1993; 11:437–441。
- Beatty RM、Winston KR:自発的な頸部硬膜外血腫。 病因の考察。 J Neurosurg 1984; 61:143–148。
- Pan G、Kulkarni M、MacDougall DJ、et al:頸椎の外傷性硬膜外血腫:磁気共鳴画像法による診断。 J Neurosurg 1988; 68:798–801。
- Foo D、Rossier A:脊髄硬膜外血腫の外科的転帰を予測する際の術前の神経学的状態。 Surg Neurol 1981; 15:389–340。
- David S、Salluzzo RF、Bartfield JM、et al:トランペット演奏に続発するバルサルバ法の延長後の自発性頸胸部硬膜外過誤腫。 Am J Emerg Med 1997; 15:73–75。
- 福井M、スワンカーA、ウィリアムズR:急性自発性脊髄硬膜外血腫。 Am J Neuroradiol 1999; 20:1365–1372。
- ジョセフA、ビネンJ:急性脊髄硬膜外血腫。 J Emerg Med 1993; 11:437–441。
- Bidzinski J:妊娠中の自発性脊髄硬膜外血腫。 J Neurosurg 1966; 24:1017-1018。
- キャロルS、マルホトラR、ユースタスDら:妊娠中の自発性脊髄硬膜外血腫。 J Matern Fetal Med 1997; 6:218–219。
- Stoll AS、Sanchez M:硬膜外ブロック後の硬膜外血腫:疼痛管理におけるその使用への影響。 Surg Neurol 2002; 57:235–240。
- Bruyn GW、ニュージャージー州ボスマ:脊髄硬膜外血腫。 Vinken PJ、Bruyn GW(eds):Handbook ofClinicalNeurology。 北ホラント、1976年、1〜30ページ。
- Horlocker T、Wedel DJ、Rowlingson JCら:抗血栓療法または血栓溶解療法を受けている患者の局所麻酔:米国局所麻酔および疼痛医学のエビデンスに基づくガイドライン(第2010版)。 Reg Anesth Pain Med 35; 64:101–XNUMX。
- 松目M、下田M、渋谷N:自発性頸部硬膜外血腫。 Surg Neurol 1987; 28:381–384。
- Lonjon M、Paquis P、Chanalet S、et al:非外傷性脊髄硬膜外血腫:1997症例の報告と文献のレビュー。 Neurosurgery 41; 483:487–XNUMX。
- Cwik J:脊髄幹麻酔の術後の考察。 Anesthesiol Clin 2012; 30:433–443。
- Lawton M、Porter R、Heiserman J、et al:脊髄硬膜外血腫の外科的管理:外科的タイミングと神経学的転帰との関係。 J Neurosurg 1995; 83:1–7。
- Avrahami E、Tadmor R、Ram Z、et al:胸椎の自発性急性硬膜外血腫のMRデモンストレーション。 Neuroradiology 1989; 31:89–92。
- Mattle H、Sieb J、Rohner M、et al:非外傷性脊髄硬膜外および硬膜下血腫。 Neurology 1987; 37:1351–1356。
- Beatty RM、Winston KR:自発的な頸部硬膜外血腫。 病因の考察。 J Neurosurg 1984; 61:143–148。
- クーパーDW:自発的な脊髄硬膜外血腫。 症例報告。 J Neurosurg 1967; 26:343–345。
- Uribe JM、Moza K、Jimenez O、Green B、Levi AD:術後の脊髄硬膜外血腫の遅延。 Spine J 2003; 3:125–129。
- Gogarten W、Vandermeulen E、Van Aken H、Kozek S、Llau JV、Samama CM; 欧州麻酔学会:局所麻酔および抗血栓剤:欧州麻酔学会の推奨事項。 Eur J Anaesthesiol 2010; 27:999-1015。
- Breivik H、Bang U、Jalonen J、Vigfusson G、Alahuhta S、Lagerkranser M:スカンジナビア麻酔学会および集中治療医学による止血障害における脊髄幹麻酔の北欧ガイドライン。 Acta Anaesthesiol Scand 2010; 54:16–41。
- Jacobs LJ、Woods BI、Chen AF、Lunardini DJ、Holh JB、Lee JY:外科的安定化を必要とする脊髄外傷患者における血栓塞栓性化学予防の安全性。 Spine 2013; 38:E1041–7。
- Pahapill PA、Lownie SP:急性自発性脊髄硬膜外血腫の保存的治療。 Can J Anaesth 1998; 25:159–163。
- Schwarz SK、Wong CL、McDonald WN:非高齢者における非定型症状を伴う脊髄硬膜外血腫からの自然回復。 Can J Anesth 2004; 51:557–561。
- Benzon HT、Snitzer J、Hoxie S、Pollina R、Nelson A:脊髄硬膜外血腫の症例報告のレビュー。 16年2012月XNUMX日、ワシントンDCで開催された米国麻酔科学会の年次総会で発表されました。
- テーラーJ、ダンIF、スミスE:小児の経口抗凝固療法に関連する自発性脊髄硬膜外血腫の保守的な管理。 Childs Nerv Syst 2006; 22:1643–1645。
- Connoly SE、Winfree CJ、McCormick PC:組織プラスミノーゲン活性化因子後の脊髄硬膜外血腫の管理。 症例報告。 Spine 1996; 21:1694–1698。
- Lopez AG、Lara JMP、Hidalgo RH、Gonzalo PE; 急性心筋梗塞に対する血栓溶解療法後の脊髄硬膜外血腫。 Orthopedics 1999; 22:987–988。
- Marzai H、Eminoglu M、Orguc S:ドレーンは腰椎椎間板手術に役立ちますか? 前向き無作為化臨床試験。 J Spinal Disord Tech 2006; 19:171–177。
- Hejazi N、Thaper PY、Hassler W:非外傷性脊髄硬膜外血腫の1998例。 Neurol Med Chir 38; 718:723–XNUMX。
- Wolfgang P、Klaus M:以前の手術とは無関係の脊髄硬膜外血腫:15年以内に10つの施設で治療された2004の連続した症例の分析。 Spine 24; 555:561–XNUMX。
- Rohde V、KükerW、Reinges MHT、et al:自発的および非自発的脊髄硬膜外血腫の顕微手術治療:病因に関連した神経学的転帰。 Acta Neurochir 2000; 142:787–793。
- ウルフH:硬膜外麻酔と脊髄血腫。 Can J Anaesth 1996; 43:1260–1271。
- Mukerji N、ToddN.脊髄硬膜外血腫; 結果に影響を与える要因。 Br J Neurosurg 2013; 27:712–717。
- Groen RT、Van Alphen HA:自発性脊髄硬膜外血腫の手術治療:術後転帰を決定する要因の研究。 Neurosurgery 1996; 39:494–508。
- Enomato T、Maki Y、Nakagawa K、et al:自発性脊髄硬膜外血腫:症例報告。 Neurol Surg 1980; 8:875–880。
- Klein SM、D'Ercole F、Greengrass RA、et al:腰神経叢ブロック後の大腰筋血腫および腰神経叢障害に関連するエノキサパリン。 麻酔学1997;87:1576–1579。
- Weller RS、Gerancher JC、Crews JC、et al:腰神経叢ブロックを受け、後に抗凝固療法を受けた2003人の患者における神経学的欠損のない広範な後腹膜血腫。 Anesthesiology 98; 581:583–XNUMX。
- Maier C、Gleim M、Weiss T、Stachetzki U、Nicolas V、Zenz M:不可逆的な血小板凝集阻害剤の投薬を受けている2002人の患者の腰部交感神経遮断後の重度の出血。 Anesthesiology 97; 740:743–XNUMX。
- Poivert C、Malinovsky JM:坐骨神経ブロックおよびフォンダパリヌクス後の大腿血腫。 Ann Fr Anesth Reanim 2012; 31:484–485。
- Ferraro LH、Tardelli MA、Yamashita AM、Cardone JD、Kishi JM:抗凝固療法を受けた患者の超音波ガイド下大腿神経および坐骨神経ブロック。 症例報告。 Rev Bras Anestesiol 2010; 60:422–428。
- Clendenen SR、Robards CB、Wang RD、Greengrass RA:頸部血腫および術後敗血症に関連する継続的な斜角筋間ブロック。 Anesth Analg 2010; 110:1236–1238。
- Johr M:大腿神経の継続的な遮断の合併症。 Reg Anaesth(ドイツ語)1987; 10:37–38。
- Neuberger M、Breithbarth J、Reisig F、Lang D、Buttner J:継続的な末梢局所麻酔における合併症と有害事象。 3,491本のカテーテルに関する調査結果[ドイツ語]。 Anaesthesist 2006; 55:33–40。
- Wiegel M、Gottschaldt U、Hennebach R、Hirschberg T、Reske A:整形外科患者の継続的な末梢神経ブロックに関連する合併症と副作用。 Anesth Analg 2007; 104:1578–1582。
- Enneking FK、Chan V、Greger J、Hadzic A、Lang SA、Horlocker TT:下肢末梢神経ブロック:現在の理解の要点。 Reg Anesth Pain Med 2005; 30:4–35。
- Antonelli D、Fares L、Anene C:巨大な腹壁血腫に関連するエノキサパリン:2000症例の報告。 Am Surgeon 66; 797:800–XNUMX。
- Dickinson LD、Miller L、Patel CP、et al:エノキサパリンは、脳腫瘍を伴う深部静脈血栓症の予防のために術前に開始された場合、術後の頭蓋内出血の発生率を増加させます。 Neurosurgery 1998; 43:1074–1081。
- Ho KJ、Gawley SD、Young MR:エノキサパリン療法に関連する腰筋血腫および大腿神経障害。 Int J Clin Pract 2003; 57:553–554。
- Houde JP、Steinberg G:人工股関節全置換術に低分子量ヘパリンを使用した後の肝内出血。 J関節形成術1999;14:372–374。
- King CS、Holley AB、Jackson JL、et al:一般集団における血栓塞栓症予防のための2007日131回対507回のヘパリン投与:メタアナリシス。 胸部516;XNUMX:XNUMX–XNUMX。
- Kozek-Langenecker SA、Fries D、Gutl M、et al:阻害剤における局所麻酔と凝固。 オーストリア麻酔学会および集中治療医学の周術期凝固に関するタスクフォースの勧告[ドイツ語]。 Anaesthesist 2005; 54:476–484。
- Abrahams MS、Aziz MF、Fu RF、Horn JL:末梢神経ブロックの電気的神経刺激と比較した超音波ガイダンス:ランダム化比較試験の系統的レビューとメタアナリシス。 Br J Anaesth 2009; 102:408–417。
- Barrington MJ、Watts SA、Gledhill RA、et al:オーストラレーシア地域麻酔コラボレーションの予備結果:神経学的およびその他の合併症に対する7000を超える末梢神経および神経叢ブロックの前向き監査。 Reg Anesth Pain Med 2009; 34:534–541。
- サイトBD、Taenzer AH、Herrick MDら:12,668の超音波ガイド下神経ブロックに関連する局所全身毒性および術後神経症状の発生率。 将来の臨床レジストリからの分析。 Reg Anesth Pain Med 2012; 37:478–482。
- Orebaugh SL、Mentor ML、Williams BA:監視された訓練生による神経刺激装置誘導および超音波誘導末梢神経ブロックに関連する有害な結果:単一部位データベースの更新。 Reg Anesth Pain Med 2012; 37:577–582。
- Barrington MJ、Kluger R:超音波ガイダンスは、末梢神経ブロック後の局所麻酔薬毒性のリスクを軽減します。 Reg Anesth Pain Med 2013; 38:289–299。
- Monib S、Ritchie A、Thabet E:特発性後腹膜血腫。 J Surg Tech Case Rep 2011; 3:49–51。
- 相田S、高橋H、下司K:腰神経叢ブロック後の腎被膜下血腫。 麻酔学1996;84:452–455。