Kenneth D. Candido, Anthony R. Tharian e Alon P. Winnie
INTRODUZIONE
L'anestesia caudale è stata descritta all'inizio del secolo scorso da due medici francesi, Fernand Cathelin e Jean-Anthanase Sicard. La tecnica precedeva l'approccio lombare blocco del nervo epidurale da diversi anni. L'anestesia caudale, tuttavia, non ha guadagnato popolarità subito dopo il suo inizio. Uno dei motivi principali per cui l'anestesia caudale non è stata adottata sono le ampie variazioni anatomiche delle ossa sacrali e il conseguente tasso di fallimento associato ai tentativi di localizzare lo iato sacrale. Il tasso di fallimento dal 5% al 10% ha reso impopolare l'anestesia epidurale caudale fino a una rinascita di interesse negli anni '1940, guidata da Hingson e colleghi, che la usarono in anestesia ostetrica. L'anestesia epidurale caudale ha molte applicazioni, inclusa l'anestesia chirurgica nei bambini e negli adulti, nonché la gestione di condizioni di dolore acuto e cronico. Percentuali di successo del 98%-100% possono essere raggiunte nei neonati e nei bambini piccoli prima della pubertà, così come negli adulti magri. La tecnica del blocco del nervo epidurale caudale nella gestione del dolore è stata notevolmente migliorata dall'uso della guida fluoroscopica e dell'epidurografia, in cui è possibile ottenere alti tassi di successo.
Sfortunatamente, le indicazioni cliniche e soprattutto gli interventi terapeutici per il sollievo del dolore cronico nei soggetti con sindrome da chirurgia fallita alla schiena sono spesso più prevalenti nei pazienti con punti di repere caudali difficili. È stato suggerito che il tradizionale blocco del nervo peridurale lombare non dovrebbe essere tentato impiegando un approccio che richieda il posizionamento dell'ago attraverso una cicatrice chirurgica spinale a causa della probabilità di lacerazione della dura e della possibilità di indurre la formazione di ematomi sulla cauda equina quando il sangue dalla procedura diventa intrappolato tra gli strati di cicatrice e tessuti connettivi. In queste circostanze, si raccomanda di eseguire il blocco del nervo epidurale caudale guidato fluoroscopicamente al posto del tradizionale approccio di palpazione. In alternativa, l'uso degli ultrasuoni può essere appropriato per identificare lo iato sacrale e questa tecnica è stata recentemente descritta. La seconda rinascita della popolarità dell'anestesia caudale è andata di pari passo con la crescente necessità di trovare alternative sicure al blocco del nervo epidurale lombare convenzionale in popolazioni di pazienti selezionate, come gli individui con sindrome da intervento chirurgico alla schiena fallito.
CONSIDERAZIONI ANATOMICHE
L'osso sacro è un grande osso di forma triangolare formato dalla fusione delle cinque vertebre sacrali. Ha un apice smussato e caudale che si articola con il coccige. La sua ampia base superiore si articola con la quinta vertebra lombare all'angolo lombosacrale (vedi Figura 1A). La sua superficie dorsale è convessa e presenta una cresta mediana interrotta rialzata con quattro (a volte tre) tubercoli spinosi che rappresentano spine sacrali fuse. Affiancando la cresta mediana, la superficie posteriore è formata da lamine fuse. Lateralmente alla cresta mediana, quattro paia di forami dorsali conducono nel canale sacrale attraverso i forami intervertebrali, ciascuno dei quali trasmette il ramo dorsale di un nervo spinale sacrale (vedi Figura 1A). Al di sotto del quarto (o terzo) tubercolo spinoso, viene identificato uno iato sacrale arcuato nella parete posteriore del canale sacrale dovuto al mancato incontro della quinta coppia di lamine, esponendo la superficie dorsale del quinto corpo vertebrale sacrale. L'apertura caudale del canale è lo iato sacrale (v Figure 1B ed 1C) coperto dalla solida membrana elastica, il legamento sacrococcigeo, che è un'estensione del legamento flavum. Il quinto processo articolare inferiore sporgono caudalmente e fiancheggiano lo iato sacrale come cornua sacrale, collegata alla cornua coccigea da legamenti intercornuali.
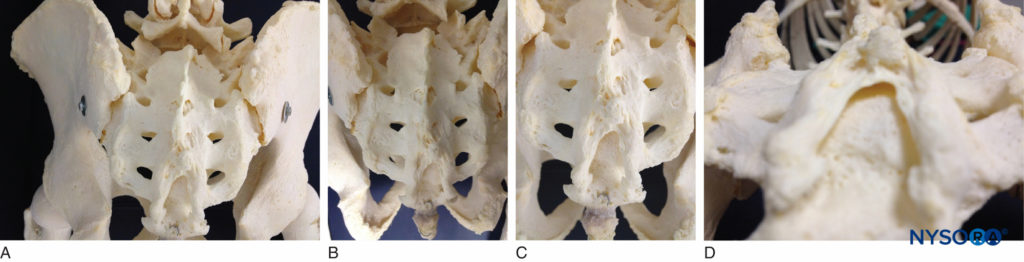
FIGURA 1. A: Esemplare scheletrico dell'osso sacro visto dal cranio alla caudale che mostra le quattro paia di forami dorsali, situati bilateralmente. B: Modello scheletrico che mostra lo iato sacrale e la sua relazione con il coccige e l'osso sacro. Il quinto processo articolare inferiore sporgono caudalmente e fiancheggiano lo iato sacrale come cornua sacrale. C: Modello scheletrico che mostra lo iato sacrale con la superficie dorsale esposta del quinto corpo vertebrale sacrale. D: Esemplare scheletrico visto da sotto lo iato sacrale
Il canale sacrale è di forma triangolare. È una continuazione del canale spinale lombare. Ciascuna parete laterale presenta quattro forami intervertebrali, attraverso i quali il canale è in contiguità con i forami sacrali pelvici e dorsali. I forami sacrali posteriori sono più piccoli delle loro controparti anteriori. Il canale sacrale contiene la cauda equina (compreso il filum terminale) e le meningi spinali. Vicino al suo livello medio (tipicamente il terzo medio di S2, ma variando dal punto medio di S1 al punto medio di S3), gli spazi subaracnoidei e subdurali cessano di esistere e le radici spinali sacrali inferiori e il filum terminale perforano l'aracnoide e la dura mater. Tuttavia, variazioni nella terminazione del sacco durale così come condizioni patologiche come il meningocele sacrale o le cisti sacrali perineurali possono aumentare le possibilità di puntura durale involontaria quando si esegue il blocco del nervo caudale in tali pazienti con anatomia anormale.
Il margine più basso del filum terminale emerge allo iato sacrale e attraversa la superficie dorsale della quinta vertebra sacrale e dell'articolazione sacrococcigea per raggiungere il coccige. Le radici del quinto nervo sacrale emergono anche attraverso lo iato mediale a ciascuno dei corni sacrali. Il canale sacrale contiene il plesso venoso epidurale, che generalmente termina in S4 ma che può continuare più caudalmente. La maggior parte di questi vasi è concentrata nella porzione anterolaterale del canale. Il resto del canale sacrale è riempito di tessuto adiposo, che è soggetto a una diminuzione della sua densità legata all'età. Questo cambiamento può essere responsabile del passaggio dalla diffusione prevedibile degli anestetici locali somministrati per l'anestesia caudale nei bambini alla diffusione segmentale limitata e imprevedibile osservata negli adulti.
Una notevole variabilità si verifica nell'anatomia dello iato sacrale tra individui di origini, razza e statura apparentemente simili. Quando gli individui invecchiano, i legamenti sovrastanti e la corna si ispessiscono in modo significativo. I margini iatali spesso sfidano il riconoscimento anche dalla punta delle dita abili. I problemi pratici legati all'anestesia caudale sono principalmente attribuibili ad ampie variazioni anatomiche di dimensioni, forma e orientamento dell'osso sacro. Trotter ha riassunto le principali variazioni anatomiche dell'osso sacro. Lo iato sacrale può essere quasi chiuso, aperto asimmetricamente o ampiamente aperto a causa di anomalie nel modello di fusione delle lamine degli archi sacrali. La spina bifida sacrale è stata osservata in circa il 2% dei maschi e nello 0.3% delle femmine. La profondità anteroposteriore del canale sacrale può variare da meno di 2 mm a più di 1 cm. Gli individui con canali sacrali aventi diametri antero-posteriori (AP) inferiori a circa 3 mm potrebbero non essere in grado di ospitare qualcosa di più grande di un ago calibro 21 (5% della popolazione).
Inoltre, la larghezza laterale del canale sacrale varia in modo significativo. Poiché la profondità e la larghezza possono variare, anche il volume del canale stesso può variare. Trotter ha scoperto che i volumi sacrali variavano tra 12 e 65 ml, con un volume medio di 33 ml. Uno studio di risonanza magnetica (MRI) su 37 pazienti adulti ha rilevato che il volume (esclusi i forami e il sacco durale) era di 14.4 ml, con un intervallo da 9.5 a 26.6 ml. I pazienti con capacità inferiori potrebbero non essere in grado di accogliere i volumi tipici di anestetici locali somministrati per l'anestesia epidurale per via caudale. In uno studio su cadavere su 53 campioni, la distanza media tra la punta del sacco durale e il bordo superiore dello iato sacrale, come indicato dalla membrana sacrococcigea, era di 45 mm, con un intervallo di 16-75 mm. Nello studio MRI menzionato, la distanza media è risultata essere 60.5 mm, con un intervallo di 34-80 mm.
La membrana sacrococcigea non è stata identificata nel 10.8% dei soggetti che utilizzano la risonanza magnetica. Una valutazione anatomica di 92 sacrali isolati ha rilevato che il 42% dei casi presentava sia uno iato che una cornua; Il 4% dei casi ha mostrato una pausa assente. L'apice dello iato sacrale, in quello studio, è stato notato nel 64% dei casi uscire a livello S4. La pausa è stata chiusa nel 3% dei casi.
I forami sacrali offrono passaggi anatomici che consentono la diffusione di soluzioni iniettate, come anestetici locali e adiuvanti (vedi Figura 1A). I forami sacrali posteriori sono essenzialmente sigillati dai muscoli multifido e sacrospinale, ma i forami anteriori non sono ostruiti da muscoli e legamenti, consentendo una pronta fuoriuscita delle soluzioni attraverso di essi. La curvatura sacrale varia sostanzialmente. In uno studio su cadavere, osservando l'anatomia dello spazio epidurale caudale, i corni sacrali non erano palpabili bilateralmente nel 14.3% e palpabili unilateralmente nel 24.5% dei campioni. Il livello di curvatura massima dell'osso sacro era a S3 nel 69.4% dei casi. Questa variabilità tende ad essere più grave nei maschi che nelle femmine.
Il significato clinico di questa scoperta è che un ago epidurale non ricurvo passerà più facilmente nel canale delle femmine rispetto ai maschi. L'angolo tra l'asse del canale lombare e quello sacrale varia tra 7° e 70° nei soggetti con marcata lordosi. L'implicazione clinica di questo risultato è che il flusso cefalico delle soluzioni iniettate caudalmente può essere più limitato nei pazienti lordotici con angoli lombosacrale esagerati rispetto a quelli con angoli lombosacrale più piatti, in cui gli assi dei canali lombare e sacrale sono più strettamente allineati.
Consigli NYSORA
- Una notevole variabilità si verifica nell'anatomia dello iato sacrale.
- Con l'avanzare dell'età i legamenti sovrastanti e la cornua si ispessiscono; di conseguenza, l'identificazione dei margini iatali sacrali diventa più difficile.
- Il tasso di successo dell'anestesia caudale dipende in gran parte dalle variazioni anatomiche di dimensioni, forma e orientamento dell'osso sacro.
Scopri Anatomia neuroassiale.
INDICAZIONI PER IL BLOCCO DEL NERVO EPIDURALE CAUDALE
Le indicazioni per il blocco del nervo epidurale caudale sono essenzialmente le stesse di blocco del nervo epidurale lombare, ma il suo uso può essere preferito quando si preferisce la diffusione del nervo sacrale di anestetici e adiuvanti rispetto alla diffusione del nervo lombare. L'imprevedibile diffusione cefalica degli anestetici somministrati nel canale caudale limita l'uso di questa tecnica in situazioni in cui è essenziale fornire un blocco neuroassiale del torace inferiore e dell'addome superiore. Sebbene questa modalità sia descritta per l'uso perioperatorio (ruolo decrescente) e per la gestione di scenari di dolore cronico negli adulti (ruolo crescente), il blocco del nervo caudale ha un'ampia gamma di indicazioni (Tabella 1). Trattamento riuscito di cefalea post-puntura eseguendo un cerotto epidurale attraverso un ago posizionato caudalmente è stato riportato.
TABELLA 1. Indicazioni per il blocco del nervo epidurale caudale.
| Chirurgici, Ostetrici, Diagnostici e Prognostici | |
|---|---|
| 1. | Anestesia chirurgica |
| 2. | Anestesia ostetrica |
| 3. | Blocco neurale differenziale per valutare il dolore pelvico, vescicale, perineale, genitale, rettale, anale e degli arti inferiori |
| 4. | Indicatore prognostico prima della distruzione dei nervi sacrali |
| Dolore acuto | |
|---|---|
| 1. | Lombalgia acuta |
| 2. | Radicolopatia lombare acuta |
| 3. | Palliazione nelle emergenze del dolore acuto |
| 4. | Il dolore postoperatorio |
| 5. | Dolore pelvico e agli arti inferiori secondario a trauma |
| 6. | Dolore da herpes zoster acuto |
| 7. | Insufficienza vascolare acuta degli arti inferiori |
| 8. | Idradenite suppurativa |
| Dolore benigno cronico | |
|---|---|
| 1. | Radicolopatia lombare |
| 2. | Stenosi spinale |
| 3. | Sindrome lombare |
| 4. | Fratture vertebrali da compressione |
| 5. | Polineuropatia diabetica |
| 6. | Nevralgia posterpetica |
| 7. | Distrofia simpatica riflessa |
| 8. | Orchialgia |
| 9. | Proctalgia |
| 10 | Sindromi dolorose pelviche |
| Dolore al cancro | |
|---|---|
| 1. | Dolore secondario a neoplasie pelviche, perineali, genitali o rettali |
| 2. | Metastasi ossee al bacino |
| 3. | Neuropatia periferica correlata alla chemioterapia |
| Situazioni speciali | |
|---|---|
| 1. | Pazienti con precedente intervento chirurgico alla colonna lombare |
| 2. | Pazienti “anticoagulati” o affetti da coagulopatia |
Consigli NYSORA
- Le indicazioni per il blocco del nervo epidurale caudale sono essenzialmente le stesse di quelle per il blocco del nervo epidurale lombare.
- Il blocco del nervo caudale può essere preferito al blocco del nervo epidurale lombare quando la diffusione del nervo sacrale di anestetici e adiuvanti è preferita rispetto alla diffusione del nervo lombare.
- L'imprevedibilità di accertare una consistente diffusione cefalica degli anestetici somministrati attraverso il canale caudale limita l'utilità di questa tecnica quando è essenziale fornire un blocco neuroassiale del torace inferiore e dell'addome superiore.
Altre indicazioni più recenti negli adulti meritano di essere citate e sono ulteriormente descritte in questo capitolo, inclusa l'esecuzione della neuroplastica epidurale percutanea; l'uso dell'analgesia caudale dopo un intervento chirurgico alla colonna lombare; analgesia caudale dopo chirurgia ortopedica degli arti inferiori; coadiuvanti anestetici locali per l'analgesia postoperatoria; e blocco del nervo caudale per eseguire la neurolisi per il trattamento del dolore da cancro intrattabile.
LA TECNICA DEL BLOCCO NERVOSO EPIDURALE CAUDALE
La tecnica classica del blocco del nervo epidurale caudale prevede la palpazione, l'identificazione e la puntura. I pazienti vengono valutati come per un qualsiasi blocco nervoso epidurale e le indicazioni e le controindicazioni relative e assolute alla sua performance sono identiche. Viene applicato un complemento completo di monitor non invasivi e vengono valutati i segni vitali di base. Si deve decidere se a continuo or tecnica a colpo singolo sarà impiegato. Per le tecniche continue, è preferibile un ago di tipo Tuohy con un orifizio rivolto lateralmente.
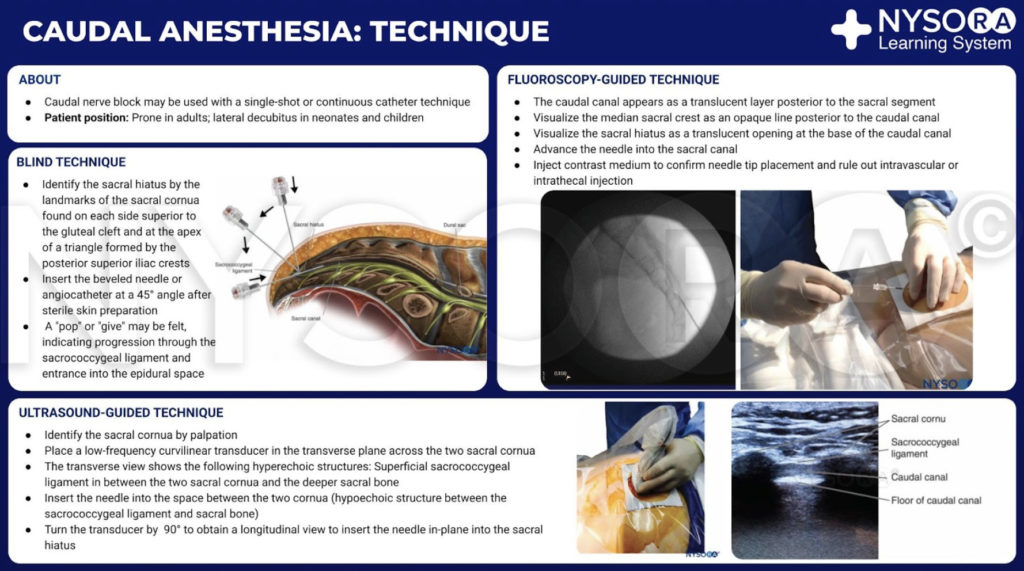
Dal Compendio dell'anestesia regionale: Tecniche per l'infografica dell'anestesia caudale.
Posizionamento del paziente
Diverse posizioni possono essere utilizzate negli adulti, rispetto alla posizione di decubito laterale nei neonati e nei bambini. La posizione laterale è spesso preferita in pediatria perché consente un facile accesso alle vie aeree quando è stata somministrata un'anestesia generale o una sedazione pesante prima di eseguire il blocco nervoso. Nei pazienti pediatrici, i blocchi nervosi possono essere eseguiti con il paziente completamente anestetizzato; questo non è raccomandato per i bambini più grandi e gli adulti. Negli adulti, la posizione prona è la più utilizzata, ma possono essere impiegate la posizione di decubito laterale o la posizione ginocchio-petto (nota anche come "ginocchio-gomito"). In posizione prona, il tavolo operatorio o il tavolo della sala operatoria deve essere flesso, oppure può essere posizionato un cuscino sotto la sinfisi pubica e le creste iliache per produrre una leggera flessione delle anche. Questa manovra facilita la palpazione del canale caudale. Le gambe sono separate con i talloni ruotati verso l'esterno per appianare la parte superiore della fessura anale, rilassando contemporaneamente i muscoli glutei. Per il posizionamento del blocco del nervo epidurale caudale nella partoriente, sono più comunemente utilizzate la posizione laterale (posizione di Sim) e la posizione ginocchio-gomito.
Punti di riferimento anatomici
Un tampone di garza asciutta viene posizionato nella fessura intergluteale per proteggere la zona anale e i genitali dallo iodio povidone o da altri disinfettanti (soprattutto alcol) usati per disinfettare la pelle. Successivamente vengono valutati i punti di riferimento anatomici. Le pieghe cutanee dei glutei sono utili guide per localizzare lo iato sacrale sottostante. In alternativa, un triangolo può essere segnato sulla pelle sopra l'osso sacro, utilizzando le spine iliache posteriori superiori (PSIS) come base, con l'apice rivolto inferiormente (caudalmente). Normalmente, questo apice si trova sopra o immediatamente adiacente allo iato sacrale. Tuttavia, uno studio recente ha indicato che l'identificazione dello iato sacrale utilizzando questo metodo potrebbe essere imprecisa perché il triangolo effettivo formato dallo iato sacrale e dai PSIS non è equiangolare. Una volta segnato lo iato, la punta dell'indice viene posizionata sulla punta del coccige nella fessura intergluteale mentre il pollice della stessa mano palpa i due corni sacrali situati 3–4 cm più rostralmente all'estremità superiore dell'intergluteo fenditura. La cornua sacrale può essere identificata muovendo delicatamente il dito indice palpante da un lato all'altro (Figure 2 ). Il pollice palpante dovrebbe affondare nell'incavo tra i due corni, come tra due nocche di un pugno. La preparazione della pelle sterile e il drappeggio dell'intera regione vengono eseguiti come di consueto.
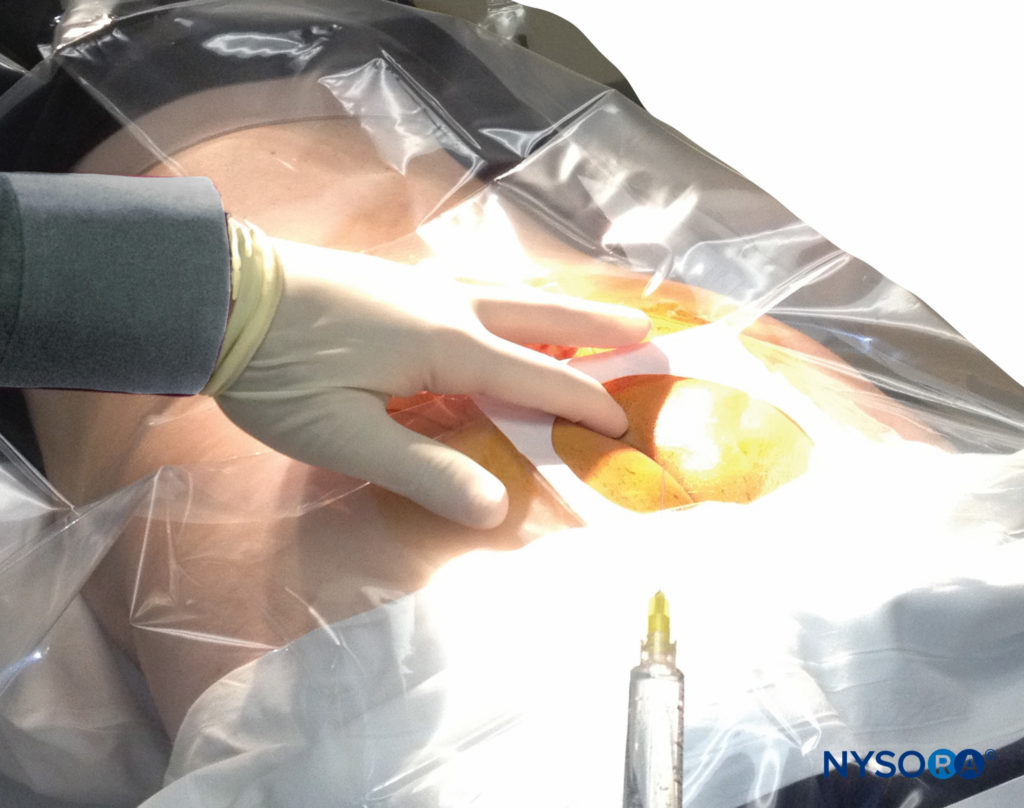
FIGURA 2. Tecnica di palpazione della linea mediana sopra lo iato sacrale. L'indice e il medio della palpazione sono sparsi sul quinto corpo vertebrale sacrale. Il legamento sacrococcigeo si trova direttamente sotto il dito palpante.
Tecnica mediante fluoroscopia
Un ago di piccolo calibro da 1.5 pollici viene quindi utilizzato per infiltrare la pelle sopra lo iato sacrale utilizzando 3-5 ml di 1%-1.5% di lidocaina HCl semplice (Figure 3 ). Se si utilizza la fluoroscopia, si ottiene una vista laterale per dimostrare i confini anatomici del canale sacrale. Di routine lasciamo l'ago per infiltrazione di anestetico locale in situ per questa vista perché dimostra se l'approccio è al livello appropriato per il successivo avanzamento dell'ago epidurale. Con la fluoroscopia, il canale caudale appare come uno strato traslucido posteriormente ai segmenti sacrali. La cresta sacrale mediana viene visualizzata come una linea opaca posteriore al canale caudale. Lo iato sacrale è solitamente visualizzato come un'apertura traslucida alla base del canale caudale. Il coccige può essere visto articolarsi con la superficie inferiore dell'osso sacro (Figure 4 ).
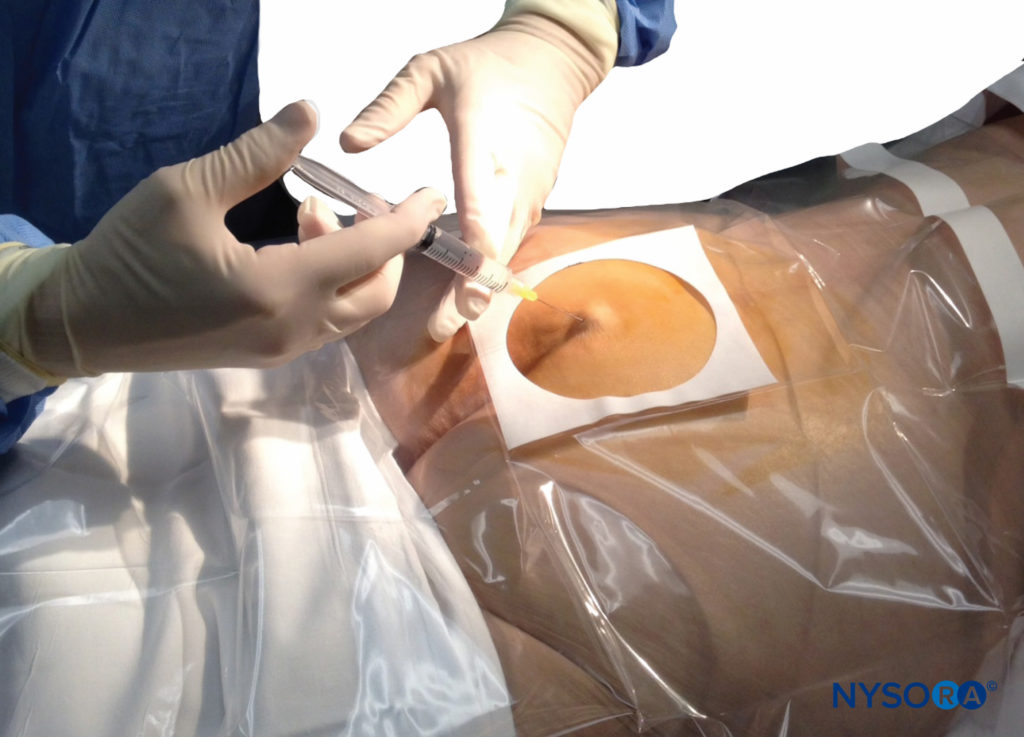
FIGURA 3. Tecnica di infiltrazione cutanea con anestetico locale. L'ago viene inserito prima sopra e poi nella sostanza del legamento sacrococcigeo.
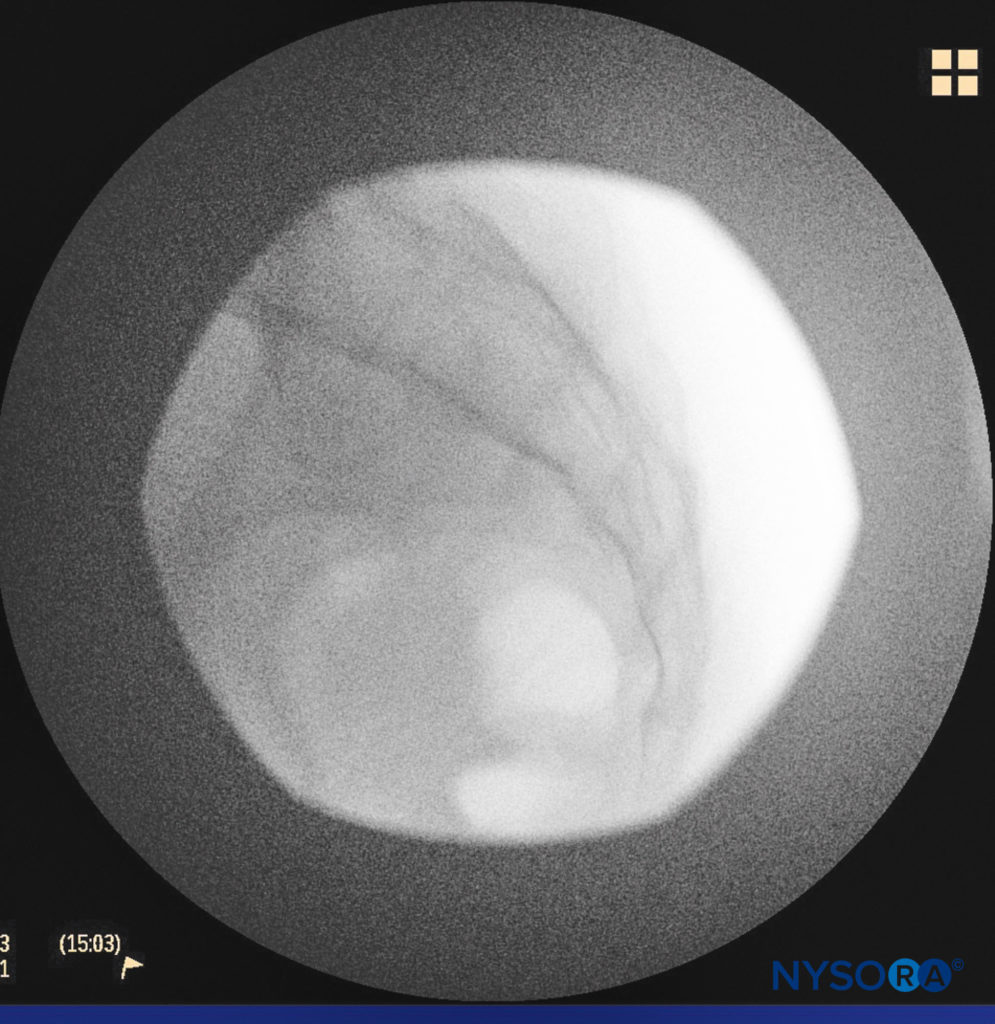
FIGURA 4. Immagine fluoroscopica laterale che mostra i confini del canale caudale.
Una volta che i tessuti sovrastanti lo iato sono stati anestetizzati, si inserisce un ago di tipo Tuohy calibro 17 o 18 nella linea mediana o, utilizzando un approccio laterale, nel canale caudale (Figure 5 , Figure 6 ). Una sensazione di un leggero "scatto" può essere apprezzata quando l'ago che avanza trafigge il legamento sacrococcigeo. Una volta che l'ago raggiunge la parete ventrale del canale sacrale, viene lentamente ritirato e riorientato, dirigendolo più cranialmente (deprimendo il mozzo e avanzando) per un ulteriore inserimento nel canale.
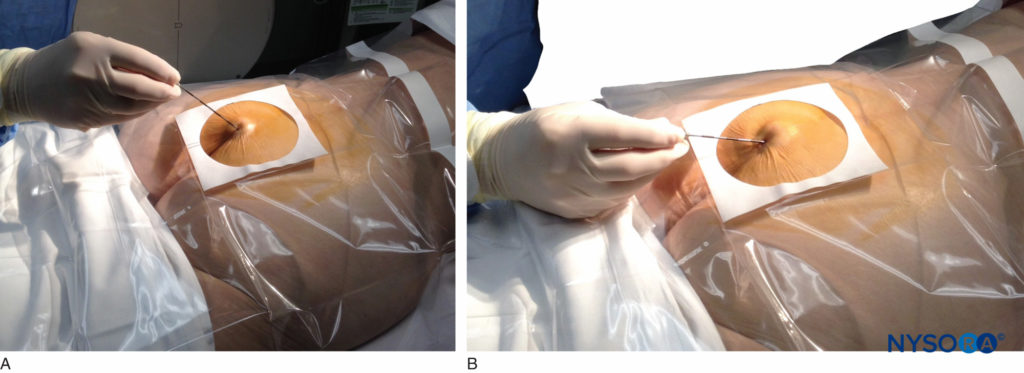
FIGURA 5. Un ago di tipo Tuohy calibro 18 viene fatto avanzare dalla pelle nello iato sacrale attraverso il legamento sacrococcigeo. Di solito, quando la fluoroscopia non è disponibile per verificare il corretto posizionamento dell'ago, una siringa caricata con aria o soluzione fisiologica viene attaccata all'ago e viene utilizzata la tecnica della perdita di resistenza per identificare lo spazio epidurale.
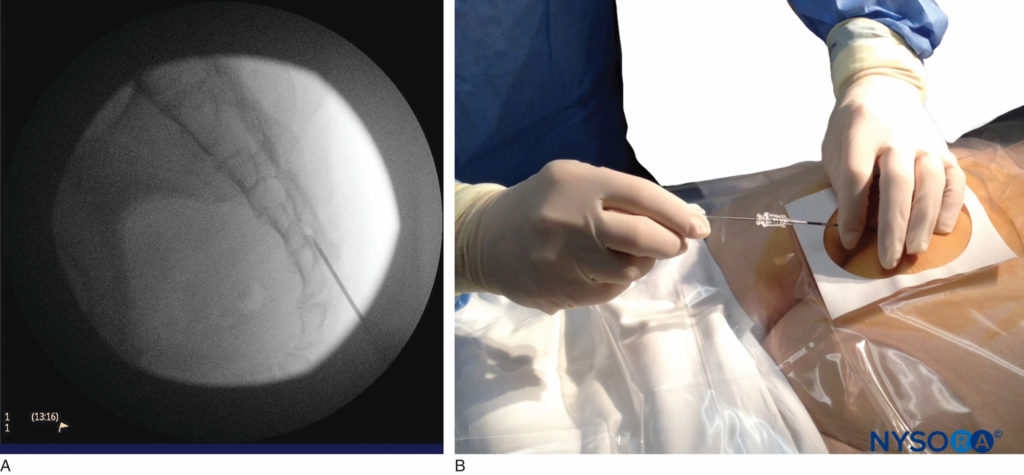
FIGURA 6. Immagine fluoroscopica laterale raffigurante l'ago Tuohy calibro 18 correttamente posizionato nello spazio epidurale caudale.
Utilizziamo la vista antero-posteriore una volta che l'ago epidurale è posizionato in modo sicuro all'interno del canale e il catetere epidurale è cefalico avanzato (Figure 7 , Figure 8 ). In questa proiezione, le creste sacrali intermedie appaiono come linee verticali opache su entrambi i lati della linea mediana. I forami sacrali sono visualizzati come aree traslucide e quasi circolari laterali alle creste sacrali intermedie. La presenza di gas intestinali può oscurare il riconoscimento di queste strutture. Una siringa caricata con aria o soluzione fisiologica contenente una piccola bolla d'aria viene quindi attaccata all'ago e viene utilizzata la tecnica della perdita di resistenza per stabilire l'ingresso nello spazio epidurale.

FIGURA 7. Un catetere continuo con uno stiletto in posizione viene fatto avanzare attraverso l'ago Tuohy calibro 18 posizionato nel canale.
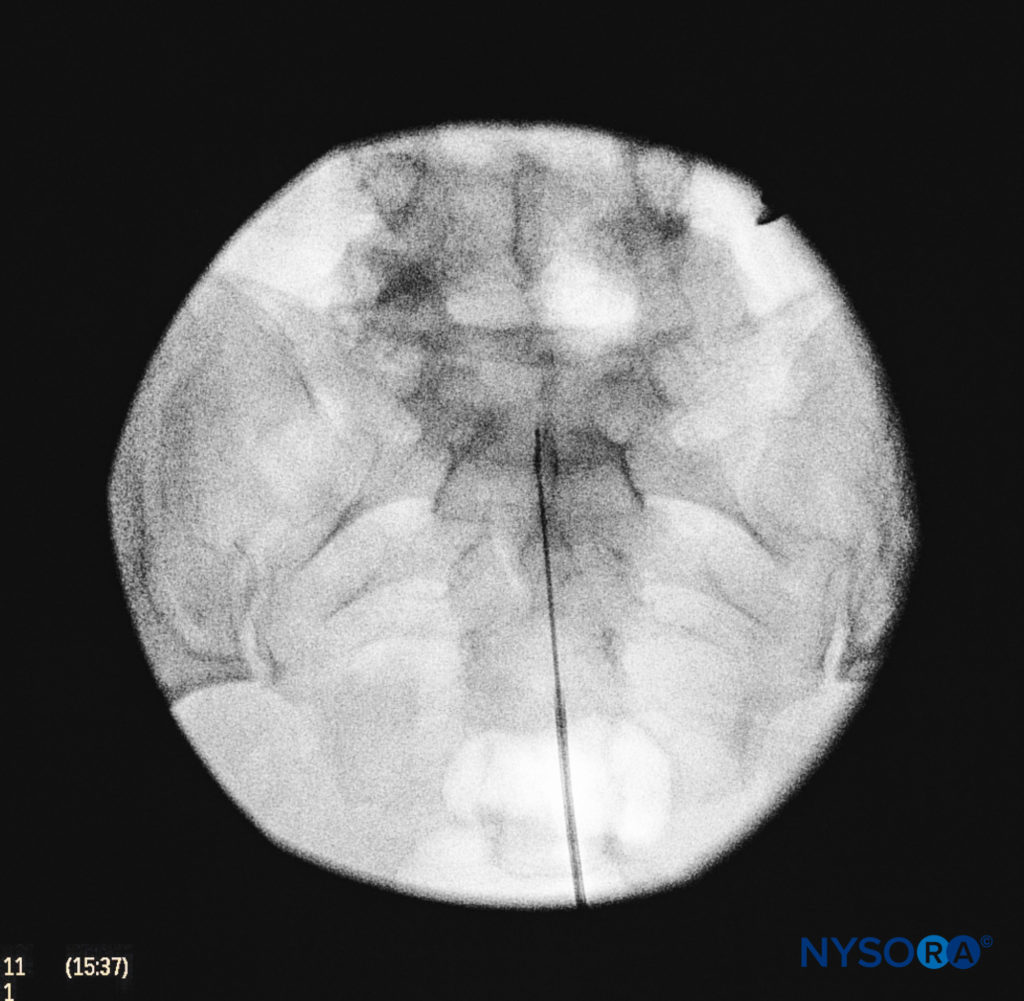
FIGURA 8. Imaging fluoroscopico anteroposteriore che illustra il corretto posizionamento dell'ago.
Consigli NYSORA
- La punta dell'ago dovrebbe rimanere al di sotto del livello S2 per evitare di strappare la dura.
- L'ago non dovrebbe mai essere fatto avanzare nello spazio troppo profondo.
- La cute corrispondente a circa 1 cm al di sotto del PSISs indica il livello S2 (estensione più caudale della dura madre).
- Il sacco durale si estende più in basso nei bambini rispetto agli adulti e gli aghi epidurali devono essere fatti avanzare con attenzione non più in profondità del livello S3 o S4.
È stato descritto un test acustico, chiamato anche test "whoosh", per identificare il corretto posizionamento dell'ago nel canale caudale. Questo suono caratteristico è stato notato durante l'auscultazione della regione toracolombare durante l'iniezione di 2-3 ml di aria nello spazio epidurale caudale. Il "test swoosh", descritto da Orme e Berg, sostituisce l'anestetico salino o locale invece dell'aria come iniettato.
Dei 108 pazienti con un blocco nervoso riuscito in uno studio, 98 hanno avuto un test positivo, senza risultati falsi positivi. Una volta confermato il corretto posizionamento dell'ago, viene inserito un catetere nella posizione desiderata (profondità) e la sua posizione confermata fluoroscopicamente quando lo si desidera (Figure 9 ). Ecografia color-doppler è stato anche descritto per guidare l'inserimento dell'ago nello spazio epidurale e per confermare qualsiasi iniezione intravascolare.
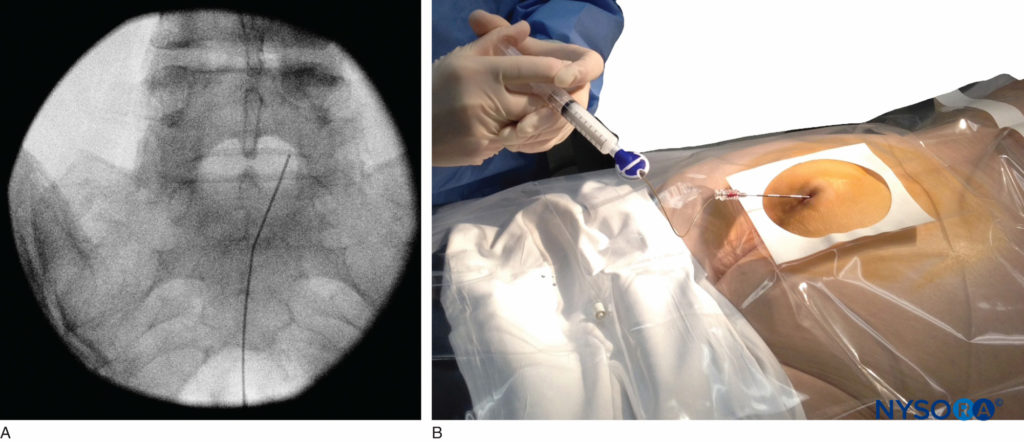
FIGURA 9. Immagine fluoroscopica anteroposteriore raffigurante il catetere avanzato nell'interspazio L5–S1.
BLOCCO NERVO CAUDALE GUIDATO DA ULTRASUONI
Gli ultrasuoni hanno svolto un ruolo crescente nell'anestesia regionale e nella gestione del dolore, la guida ecografica può essere utilizzata per identificare lo iato sacrale, facilitando così l'ingresso dell'ago nello iato, nonché per visualizzare l'avanzamento dell'ago nel canale caudale. Poiché i blocchi del nervo caudale sono relativamente facili da eseguire nella popolazione pediatrica, gli ultrasuoni potrebbero non essere significativamente vantaggiosi rispetto alle tecniche basate sui punti di riferimento. Tuttavia, nei pazienti adulti, per i quali l'anatomia dello iato sacrale, del canale caudale e del sacco durale sono variabili, la guida ecografica può rivelarsi utile nel ridurre il rischio di complicanze come traumi tissutali, puntura durale, tossicità da anestetico localee compromissione vascolare.
Tecnica
Con il paziente in posizione prona, i corni sacrali vengono identificati mediante palpazione utilizzando la tecnica descritta nella sezione sui reperi anatomici. Viene eseguita la preparazione della pelle sterile e il drappeggio dell'intera regione. Una sonda curvilinea a bassa frequenza è posta sul piano trasversale attraverso i due corni sacrali (Figure 10 ). Il cornua sacrale può essere visualizzato come due archi iperecogeni simmetrici, con una sfumatura ipoecogena sotto entrambe le linee, che collegano queste due strutture. Attraversando questa area ipoecogena ci sono due linee iperecogene, quella superficiale è il legamento sacrococcigeo e quella più profonda è la superficie ossea dorsale del sacro (Figure 11 ). Nello spazio tra i due corni viene inserito un ago calibro 22. Si avverte un "pop" distinto quando la punta dell'ago penetra nel legamento sacrococcigeo.
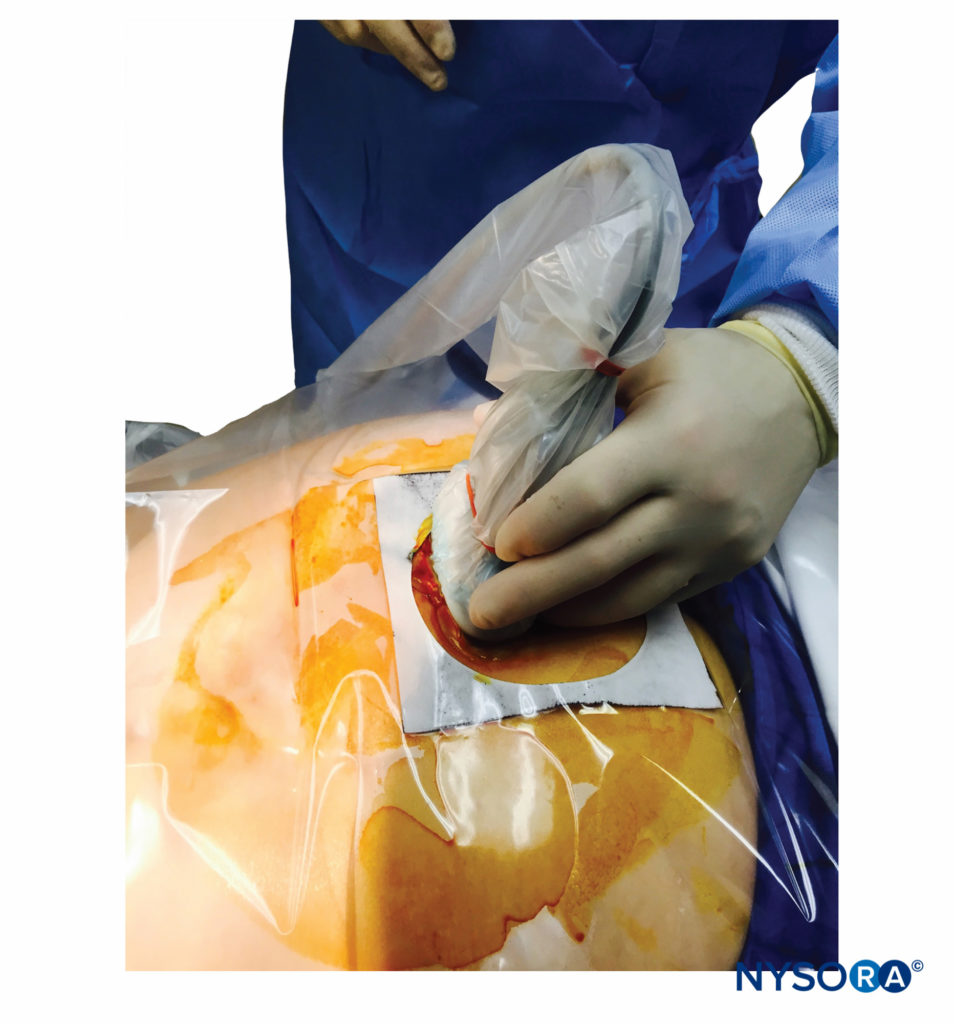
FIGURA 10. Una sonda ecografica curvilinea a bassa frequenza avvolta in un coprisonda sterile contenente gel posizionato sul piano trasversale attraverso i due corni sacrali.
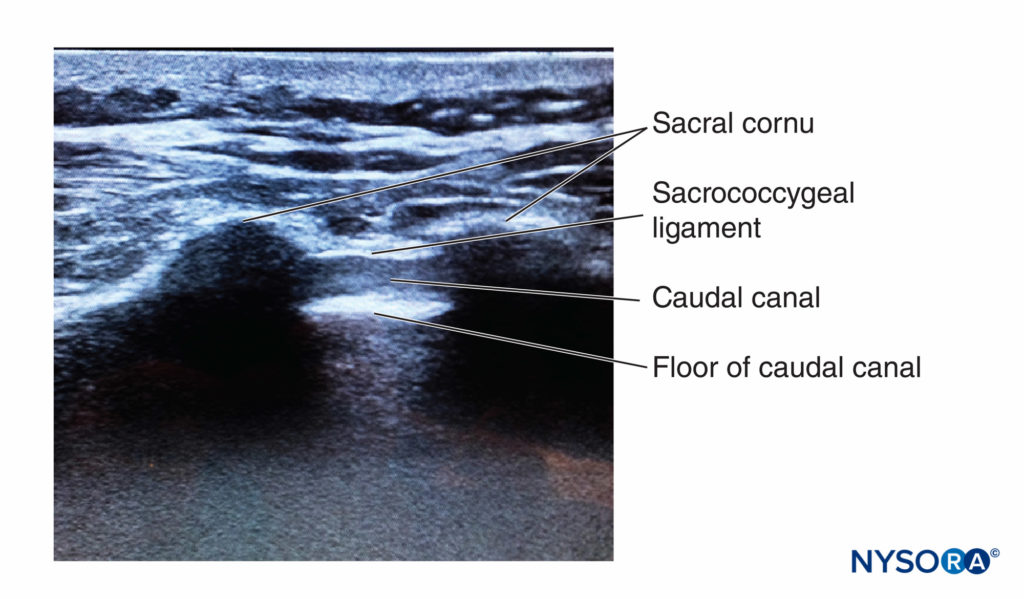
FIGURA 11. Immagine ecografica lungo l'asse corto del canale caudale, raffigurante il cornua sacrale, il legamento sacrococcigeo e il canale caudale.
A questo punto, l'orientamento della sonda viene cambiato nel piano sagittale (Figure 12 ), e il canale caudale è identificato come un canale ipoecogeno che si assottiglia caudalmente e delimitato da bande iperecogene dorsali e ventrali. La fascia dorsale è formata dall'aspetto osseo dorsale del canale caudale cranialmente e dal legamento sacrococcigeo caudalmente. La fascia ventrale è formata dalla superficie ossea ventrale del canale caudale (Figure 13 ).
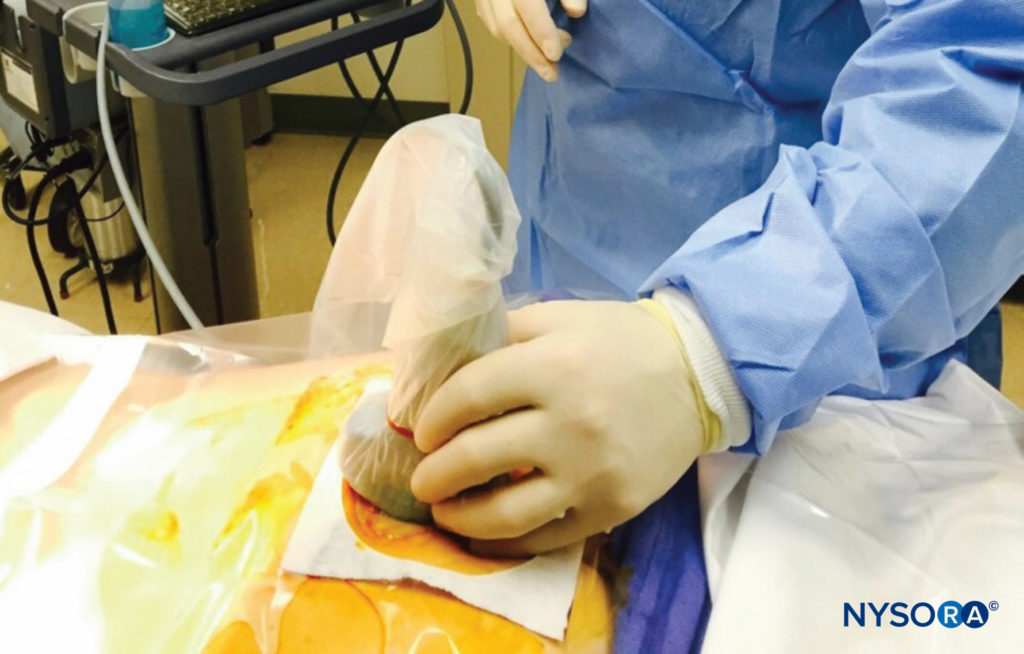
FIGURA 12. La sonda curvilinea a bassa frequenza posta sul piano sagittale lungo l'asse lungo del canale caudale.
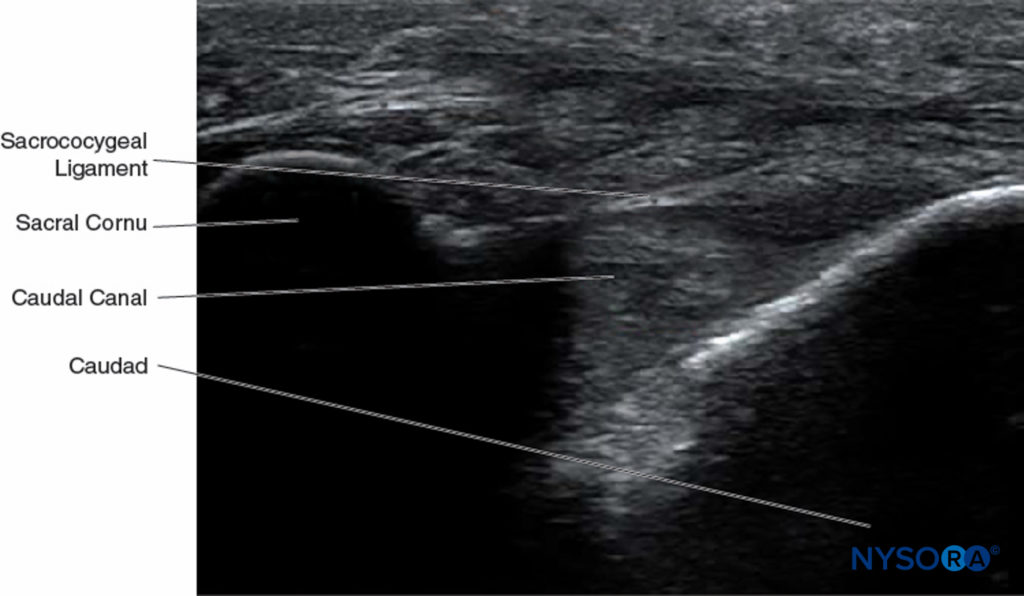
FIGURA 13. Immagine ecografica lungo l'asse lungo del canale caudale raffigurante la vista dell'asse lungo del canale caudale.
Consigli NYSORA
- Nei pazienti pediatrici, la stimolazione elettrica è stata utilizzata per accertare il corretto posizionamento dell'ago nel canale caudale. La contrazione dello sfintere anale (corrispondente alla stimolazione di S2–S4) viene ricercata con correnti da 1 a 10 mA.
- Se l'ago è stato inserito correttamente, spostando il mozzo da un lato all'altro, mentre l'asta è tenuta in corrispondenza della membrana sacro-coccigea, si consentirà alla punta di oscillare liberamente nel canale sacrale come un fulcro.
- Se si ottiene liquido cerebrospinale (CSF) dopo l'aspirazione, l'ago deve essere ritirato e l'iniezione non deve essere eseguita.
- Se il sangue viene aspirato, l'ago deve essere ritirato e reinserito fino a quando non è visibile sangue al mozzo.
- Quando l'iniezione di aria (o soluzione salina) per la tecnica della perdita di resistenza provoca un rigonfiamento sull'osso sacro, molto probabilmente la punta dell'ago si trova dorsalmente all'osso sacro nei tessuti sottocutanei.
- Se la punta dell'ago è sottoperiostale, l'iniezione incontrerà una resistenza significativa, causando un notevole disagio per il paziente. Lo strato corticale dell'osso sacrale è spesso sottile, in particolare nei neonati e nei soggetti più anziani, e la sua penetrazione può avvenire facilmente soprattutto se si esercita forza mentre si fa avanzare l'ago. La sensazione di entrare nell'osso spugnoso non è dissimile dalla penetrazione della membrana sacrococcigea; c'è una sensazione di resistenza che viene improvvisamente superata e l'ago avanza più liberamente e la successiva iniezione non è ostacolata.
Sono state descritte diverse complicazioni legate alla procedura tecnica. Le soluzioni iniettate possono essere assorbite rapidamente dal midollo osseo, provocando reazioni tossiche ai farmaci. In questa situazione, durante l'iniezione si nota tipicamente dolore sulla parte caudale dell'osso sacro. In questo caso, l'ago deve essere leggermente ritirato e ruotato sul proprio asse fino a quando non può essere reinserito in una direzione leggermente diversa.
Se l'iniezione viene effettuata anteriormente all'osso sacro, è possibile perforare il retto o, nelle partorienti, la testa del bambino può essere lesa. Ciò limita l'uso del blocco del nervo caudale nelle donne in travaglio una volta che la parte presentante è discesa nel perineo. Può anche verificarsi una puntura venosa involontaria e l'incidenza di questa è stata segnalata intorno allo 0.6%.
Il blocco del nervo caudale può essere utilizzato con una tecnica di catetere a colpo singolo o continuo. Per il blocco nervoso continuo, il catetere può essere anterogrado avanzato (convenzionalmente) o retrogrado. Il blocco del nervo caudale continuo può essere eseguito in modo retrogrado utilizzando l'inserimento dell'ago nello spazio epidurale lombare, ma diretto inferiormente anziché superiormente. In uno studio su 10 pazienti, i cateteri epidurali sono stati fatti avanzare attraverso aghi epidurali di tipo Tuohy calibro 18 in modo retrogrado dall'interspazio L4-L5. Questa tecnica era associata a un tasso di fallimento del 20%, con il catetere che entrava negli spazi paravertebrali o retrorettali, nonostante il facile ingresso nello spazio epidurale. Utilizzando l'approccio convenzionale, un ago Tuohy con punta Huber viene utilizzato come condotto per far passare il catetere epidurale nel canale. Questo ago ha una punta smussata curva che limita l'impigliamento o l'impigliamento sul periostio sacrale. L'ago viene inserito con la spalla rivolta anteriormente e l'orifizio dorsalmente. In alternativa, un catetere standard da 16 o 17 gauge (angiocatetere) può fungere da ago di introduzione per il successivo posizionamento del catetere. Il catetere viene avanzato sotto guida fluoroscopica, specialmente quando viene eseguito per la gestione del dolore cronico nella sindrome da chirurgia alla schiena fallita.
I cateteri devono essere fatti avanzare delicatamente perché sono stati segnalati casi di puntura durale con avanzamento rapido o aggressivo. È necessario ottenere una vista fluoroscopica laterale e antero-posteriore per dimostrare il posizionamento del catetere nello spazio epidurale (Figure 14 ed 9) e di seguirne il percorso in direzione cefalica o cefalolaterale. Quando viene raggiunto il livello desiderato, possono essere iniettati mezzi di contrasto non ionici iodati, seguiti dall'iniezione di anestetici locali, corticosteroidi o coadiuvanti (Figure 15 ). Di solito, il catetere non è avanzato al di sopra del livello del corpo vertebrale L4, anche se potrebbe essere avanzato ai livelli L1 o L2 per indicazioni specifiche. Alcuni autori raccomandano di non far avanzare il catetere di oltre 8-12 cm cefalea.
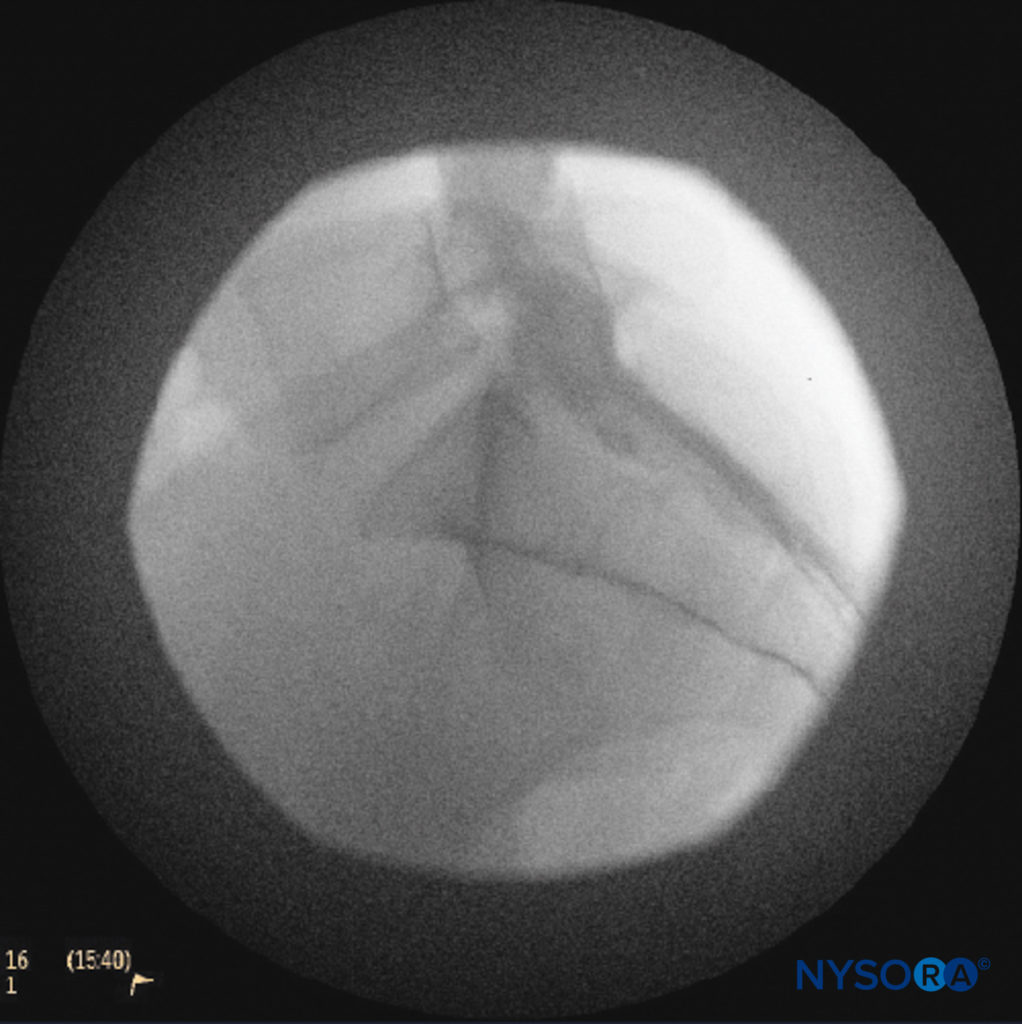
FIGURA 14. Immagine fluoroscopica laterale raffigurante mezzo di contrasto radiopaco negli spazi epidurali caudale e lombare inferiore. L'immagine mostra una notevole diffusione, sia anteriormente che posteriormente, dopo l'iniezione di 2 ml di colorante.
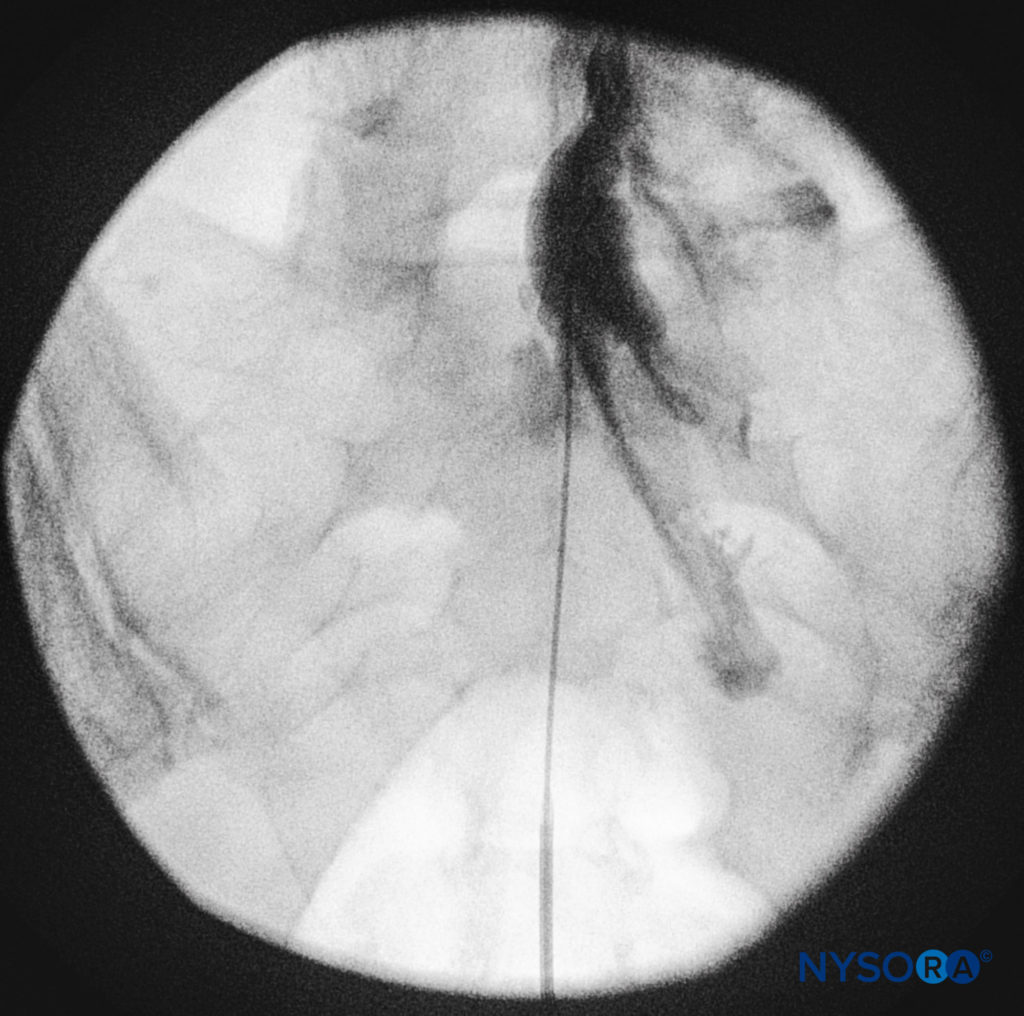
FIGURA 15. Immagine fluoroscopica anteroposteriore raffigurante un mezzo di contrasto radiopaco nello spazio epidurale
Consigli NYSORA
- La diffusione delle soluzioni di anestetico locale iniettate nello spazio epidurale caudale negli adulti è influenzata dal volume iniettato, dalla velocità di iniezione e dal posizionamento del paziente.
- Non vi è alcuna correlazione tra la velocità di iniezione e la diffusione dell'anestetico locale nei bambini sottoposti ad anestesia caudale.
CARATTERISTICHE DEL BLOCCO DEL NERVO EPIDURALE CAUDALE NEGLI ADULTI
Il blocco del nervo epidurale caudale provoca un blocco del nervo sensitivo e motorio delle radici sacrali e un blocco del nervo autonomo limitato. Il contributo sacrale del sistema nervoso parasimpatico viene bloccato causando la perdita della funzione visceromotoria della vescica e dell'intestino distalmente alla flessura splenica del colon. Si verifica un blocco del nervo simpatico, sebbene limitato rispetto al blocco del nervo epidurale lombare o toracico. Tuttavia, il deflusso simpatico dalle fibre simpatiche pregangliari del midollo spinale termina a livello L2; pertanto, il blocco del nervo caudale non dovrebbe comportare di routine una vasodilatazione periferica degli arti inferiori al livello osservato con il blocco epidurale lombare. Il blocco nervoso anestetico locale epidurale caudale negli adulti può essere scelto per interventi chirurgici dell'addome inferiore, del perineo o degli arti inferiori. Le miscele e le dosi di anestetico locale sono simili a quelle per il blocco del nervo epidurale lombare (Tabella 2). Uno studio recente che ha esaminato l'effetto del sesso sulle concentrazioni minime di anestetico locale (MLAC) di ropivacaina per l'anestesia caudale nei pazienti sottoposti a chirurgia anorettale ha rilevato che il MLAC per l'anestesia caudale nelle pazienti di sesso femminile è del 31% superiore rispetto ai pazienti di sesso maschile.
TABELLA 2. Anestetici locali comunemente usati per l'anestesia caudale negli adulti
| Agente | Concentrazione | Dose (mg) | Esordio sensoriale (Diffuso a 4 segmenti) | Durata (Regressione a 2 segmenti) |
|---|---|---|---|---|
| Lidocaina | 1.5% -2% | 300-600 | 10 – 20 min | 90 – 150 min |
| Cloroprocaina | 2% -3% | 400-900 | 8 – 15 min | 45 – 80 min |
| mepivacaina | 2% | 400-600 | 10 – 20 min | 90 – 240 min |
| Ropivacaine | 0.75% -1% | 150-300 | 15 – 25 min | 120 – 210 min |
| Bupivacaina/levobupivacaina | 0.5% -0.75% | 100-225 | 10 – 25 min | 180 – 270 min |
Diffusione di soluzioni di anestetico locale
La grande capacità del canale sacrale ospita volumi di soluzione corrispondentemente grandi; volumi significativi possono essere persi attraverso l'ampio forame sacrale anteriore. Pertanto, i requisiti di dose caudale degli anestetici locali per ottenere la stessa diffusione segmentale sono significativamente maggiori rispetto alle corrispondenti dosi lombari. È necessaria circa il doppio della dose di anestetico locale epidurale lombare affinché il blocco caudale raggiunga livelli simili di analgesia e anestesia e le soluzioni iniettate nello spazio caudale impiegano più tempo per diffondersi (Tabella 2). Bromage ha osservato che l'età non è correlata alla diffusione segmentale caudale negli adulti e il livello superiore di analgesia risultante da dosi di 20 ml di soluzione di anestetico locale varia ampiamente tra S2 e T8. Questa imprevedibilità limita l'utilità dell'applicazione dell'anestesia caudale per procedure chirurgiche che richiedono livelli di analgesia cefalica al di sopra del livello pelvico o dell'ombelico. Uno studio più recente ha confermato le scoperte di Bromage. In 172 donne sottoposte a chirurgia ginecologica minore in anestesia caudale con 20 ml di lidocaina all'1.5%, il livello di dermatomo sensoriale più alto raggiunto era inferiore a T10.
Consigli NYSORA
- Il canale sacrale contiene la cauda equina (compreso il filum terminale), le meningi spinali, il tessuto adiposo e il plesso venoso sacrale.
- Il volume del canale sacrale è in media di 14.4 ml.
- Le indicazioni per il blocco del nervo epidurale caudale sono le stesse di un blocco del nervo epidurale lombare.
- La neuroplastica epidurale percutanea è una tecnica di somministrazione di anestetici locali, corticosteroidi, ialuronidasi e soluzione salina ipertonica attraverso un catetere caudale allo scopo di lisare le aderenze epidurali.
- I pazienti adulti sono tipicamente posti proni al blocco nervoso, mentre la posizione di decubito laterale è preferita per la pediatria.
- Il blocco caudale in pediatria viene utilizzato principalmente per il controllo del dolore perioperatorio, mentre negli adulti è principalmente per la gestione del dolore cronico.
- Negli adulti, è necessaria circa il doppio della dose di anestetico locale per ottenere la stessa diffusione segmentale con il blocco del nervo caudale rispetto alla dose utilizzata per il blocco del nervo epidurale lombare.
Indicazioni per l'analgesia epidurale caudale negli adulti
Un blocco del nervo epidurale caudale è indicato ogni volta che l'area dell'intervento interessa le radici del nervo sacrale e lombare inferiore. La tecnica è adatta per chirurgia anale (emorroidectomia e dilatazione anale), procedure ginecologiche, chirurgia del pene o dello scroto e chirurgia degli arti inferiori. Utilizzando una tecnica di catetere, è possibile utilizzare il blocco del nervo epidurale caudale per il taglio cesareo, l'isterectomia vaginale e l'erniorrafia inguinale.
Un blocco del nervo epidurale caudale viene utilizzato meno frequentemente del blocco del nervo epidurale lombare o toracico per l'analgesia perioperatoria negli adulti. Il bacino si allarga notevolmente durante la pubertà, mentre il grasso epidurale nella regione lombosacrale subisce una compattazione e un aumento del contenuto fibroso. Ciò ostacola la diffusione cefalica delle soluzioni, in particolare se confrontata con la diffusione nei bambini.
In alternativa al blocco del nervo epidurale caudale negli adulti, si potrebbe considerare un approccio mediano al blocco del nervo epidurale transsacrale. Nella descrizione originale di quella tecnica, l'87% dei blocchi nervosi ha avuto successo per la resezione transuretrale dei tumori della vescica rispetto al 100% per le procedure sacrali. Il livello di anestesia, gli effetti collaterali e l'emodinamica erano simili tra i due gruppi studiati nel rapporto iniziale.
BLOCCO DEL NERVO CAUDALE PER ANALGESIA DEL LAVORO
Il canale sacrale partecipa all'ingorgo generale delle vene extradurali che si verifica nella tarda gravidanza o in qualsiasi condizione clinica in cui la vena cava inferiore (IVC) sia parzialmente ostruita. Poiché il volume effettivo del canale caudale è notevolmente diminuito durante l'ultima parte della gravidanza, il dosaggio caudale deve essere ridotto proporzionalmente nelle donne a termine. La diffusione segmentale degli anestetici locali può aumentare sostanzialmente nelle donne in gravidanza a termine, rendendo necessaria una riduzione dal 28% al 33% della dose richiesta in questa popolazione di pazienti. La scelta di un catetere continuo o di una tecnica a iniezione singola durante il travaglio attivo è limitata dalla relativa mancanza di sterilità allo iato sacrale, che può essere contaminato da feci e meconio.
Sono stati segnalati rari casi di sindrome di Horner quando grandi dosi di anestetici locali vengono iniettate caudalmente durante la somministrazione di analgesia del travaglio. È più probabile che ciò si verifichi se l'iniezione viene effettuata con il paziente sulla schiena (l'ingorgo del plesso venoso epidurale e la compressione dell'IVC sono massimi).
La cosiddetta tecnica duale (lombare e caudale) del blocco del nervo epidurale per il travaglio non è più ampiamente utilizzata. Poiché il dolore delle contrazioni uterine è mediato dalle fibre del sistema nervoso simpatico che originano dai segmenti spinali da T10 a L2, un catetere epidurale lombare è sufficiente sia per lo stadio I che per lo stadio II del parto, con aggiustamenti del dosaggio effettuati in base alle circostanze e ai requisiti esatti (vedi Anestesia regionale ostetrica).
INDICAZIONI PER L'ANALGESIA EPIDURALE CAUDALE NEI BAMBINI
Caratteristiche del blocco
Lo iato sacrale è solitamente facile da palpare nei neonati e nei bambini, il che rende questa tecnica molto più semplice e prevedibile. Di conseguenza, in molte istituzioni con un gran numero di pazienti pediatrici, il blocco del nervo epidurale caudale è parte integrante del trattamento intra e postoperatorio. gestione del dolore per i bambini sottoposti a un'ampia gamma di procedure chirurgiche sia sotto che sopra il diaframma. La tecnica si impara facilmente; uno studio ha dimostrato una percentuale di successo dell'80% nei tirocinanti residenti dopo aver completato 32 procedure eseguite senza guida fluoroscopica. Nei neonati e nei bambini piccoli, per le tecniche di iniezione singola può essere utilizzato un ago da 21 gauge, a smusso corto, da 1 pollice. Per i blocchi nervosi continui, un catetere epidurale standard può essere fatto avanzare attraverso un angiocatetere calibro 18 o attraverso un ago epidurale calibro 18 a parete sottile. È stato notato che a 4 o 5 anni di età il canale sacrale è generalmente abbastanza grande da accettare un tale ago per il passaggio di un catetere. L'elettrocardiogramma è stato utilizzato per verificare il posizionamento appropriato della punta del catetere toracico (elettrocardiografia epidurale).
Diffusione di soluzioni di anestetico locale
La diffusione segmentale dell'analgesia dopo somministrazione caudale è più prevedibile nei bambini fino a circa 12 anni di età. Alcuni studi hanno suggerito che la diffusione cefalica delle soluzioni caudali nei bambini non è ostacolata dagli stessi vincoli anatomici che si sviluppano dalla pubertà in poi. Prima della pubertà, le barriere anatomiche alla giunzione lombosacrale non si sono ancora sviluppate in misura marcata e le soluzioni caudali possono fluire liberamente verso l'alto nei recessi più alti del canale spinale. Di conseguenza, la diffusione rostrale dell'anestesia caudale è più estesa e più prevedibile nei bambini rispetto agli adulti.
Indicazioni nei bambini
Nei bambini, il blocco del nervo caudale è solitamente combinato con una leggera anestesia generale con ventilazione spontanea. Durante la chirurgia addominale inferiore e genitourinaria nei bambini, è stato dimostrato che il blocco del nervo caudale con bupivacaina allo 0.25% (2 mg/kg) riduce le risposte metaboliche ed endocrine allo stress, misurate dalle concentrazioni di glucosio; livelli medi di prolattina; insulina; e le concentrazioni di cortisolo, rispetto alla sola anestesia generale. Il posizionamento toracico dei cateteri è possibile nei neonati e nei bambini piccoli. Tuttavia, uno studio radiografico su 115 bambini ha rilevato che 10 cateteri posizionati caudalmente si trovavano nella regione toracica alta o cervicale bassa, quando il sito previsto era nei segmenti toracici inferiori.
I tre gruppi di indicazioni per il blocco del nervo epidurale caudale nei bambini sono i seguenti:
- Pazienti che necessitano di blocco del nervo sacrale (circoncisione, chirurgia anale)
- Pazienti che necessitano di blocco del nervo toracico inferiore (erniorrafia inguinale)
- Pazienti che richiedono analgesia dei dermatomi toracici superiori (chirurgia toracica)
Considerazioni farmacologiche per l'anestesia epidurale caudale nei bambini
È stato riscontrato che il blocco del nervo caudale con bupivacaina (4 mg/kg) e morfina (150 μg/kg) riduce il fabbisogno di fentanil durante la chirurgia cardiaca e riduce i tempi di estubazione in un gruppo di 30 pazienti pediatrici randomizzati a ricevere l'anestesia generale da sola o una combinazione di o blocco del nervo caudale.
La dose richiesta di anestetico è di circa 0.1 ml/segmento all'anno per l'1% di lidocaina o lo 0.25% di bupivacaina.1 La dose può anche essere calcolata in base al peso corporeo. La relazione tra età e dose richiesta è strettamente lineare, con un alto grado di correlazione fino a 12 anni. Uno studio recente che utilizzava la fluoroscopia con ropivacaina allo 0.2% contenente colorante radiopaco in un rapporto di 1:4 ha mostrato che le dosi basate sul peso per la bupivacaina allo 0.2% somministrata caudalmente erano applicabili anche alla ropivacaina allo 0.2%. Le concentrazioni plasmatiche di bupivacaina nei bambini che ricevevano il blocco del nervo caudale con lo 0.2% dell'anestetico locale (2 mg/kg) erano inferiori alle dosi equivalenti somministrate tramite il blocco del nervo ileoinguinale-ileoipogastrico per il controllo del dolore dopo erniotomia o orchidopessi. Inoltre, i tempi per raggiungere il picco delle concentrazioni plasmatiche sono stati più rapidi nel gruppo del blocco del nervo periferico, indicando che il blocco del nervo caudale è un'alternativa sicura alle tecniche di infiltrazione locale nella chirurgia inguinale.
In uno studio su bambini di età compresa tra 1 e 6 anni sottoposti a orchidopessi, un blocco del nervo caudale che utilizza volumi maggiori di bupivacaina diluita (0.2%) ha dimostrato di essere più efficace di un volume più piccolo della concentrazione standard (0.25%) per bloccare la risposta peritoneale alla trazione del cordone spermatico, senza alcun cambiamento nella qualità dell'analgesia postoperatoria. In quello studio, la dose totale di bupivacaina era identica in entrambi i gruppi (20 mg). La ropivacaina allo 0.5% ha dimostrato di fornire una durata significativamente più lunga dell'analgesia dopo l'erniorrafia inguinale nei bambini di età compresa tra 1.5 e 7 anni rispetto allo 0.25% di ropivacaina o allo 0.25% di bupivacaina. Tutti i bambini hanno ricevuto 0.75 ml/kg di anestetico locale. Tuttavia, i tempi della prima minzione e dello stare in piedi sono stati significativamente ritardati nel gruppo che ha ricevuto lo 0.5% di ropivacaina e si è verificato un caso di blocco del nervo motorio degli arti inferiori.
Un altro studio ha confrontato la ropivacaina ad alto volume/bassa concentrazione (1.5 ml/kg di soluzione allo 0.15%) e la ropivacaina a basso volume/alta concentrazione (1.0 ml/kg di soluzione allo 0.225%) per l'analgesia caudale nei bambini di età compresa tra 1 e 5 anni di età in fase di orchiopessia. Questo studio ha mostrato che un volume maggiore di ropivacaina diluita forniva una migliore qualità e una maggiore durata dell'analgesia dopo la dimissione rispetto a un volume minore di ropivacaina più concentrata.
La ropivacaina è stata utilizzata anche per il blocco del nervo caudale per la riparazione dell'ipospadia in uno studio randomizzato in doppio cieco su 26 bambini. La concentrazione minima efficace di anestetico locale di ropivacaina è risultata pari allo 0.11%, per fornire un'analgesia caudale efficace nei bambini in anestesia generale con una concentrazione alveolare minima di enflurano di 0.5.
Le concentrazioni plasmatiche di ropivacaina dopo il blocco del nervo caudale in 20 bambini di età compresa tra 1 e 8 anni, utilizzando 2 mg/mL, 1 mL/kg, hanno dimostrato frazioni libere del 5%, clearance di 7.4 mL/kg/min ed emivita terminale di 3.2 ore, ben al di sotto di quelli associati a sintomi tossici negli adulti. Un altro studio che ha esaminato la concentrazione analgesica locale minima di ropivacaina per l'analgesia caudale intraoperatoria nei bambini in età prescolare e in età scolare sottoposti a riparazione dell'ipospadia ha rilevato che era necessaria una concentrazione più elevata di ropivacaina per i bambini in età scolare rispetto ai bambini in età prescolare per fornire analgesia caudale intraoperatoria quando combinata con anestesia generale. Dei tre anestetici locali comunemente usati per l'anestesia caudale a iniezione singola (bupivacaina, ropivacaina e levobupivacaina), nessuna superiorità in termini di efficacia clinica è stata trovata per nessuno di questi farmaci in una meta-analisi di 17 studi randomizzati controllati che riguardavano sparato in anestesia caudale pediatrica con almeno due dei tre farmaci in questione. La bupivacaina e la ropivacaina hanno mostrato rispettivamente la più alta e la più bassa incidenza di blocco del nervo motorio.
Una revisione sistematica quantitativa di studi randomizzati controllati che esaminano la sicurezza e l'efficacia della clonidina come additivo per l'anestesia regionale caudale ha suggerito che la clonidina può fornire una durata estesa dell'analgesia con una ridotta incidenza per i requisiti di salvataggio analgesico e pochi effetti avversi rispetto agli anestetici locali caudali solo. I dati di 20 studi randomizzati controllati sono stati utilizzati in questa meta-analisi per valutare la sicurezza e l'efficacia della clonidina caudale aggiunta agli anestetici locali rispetto ai soli anestetici locali nei bambini sottoposti a chirurgia urologica, addominale inferiore o degli arti inferiori. È stato dimostrato che la dexmedetomidina (1 μg/kg) fornisce una maggiore durata del sollievo dal dolore quando aggiunta a bupivacaina 2.5 mg/mL, 1 mL/kg, rispetto a una dose identica di bupivacaina da sola nei bambini di età compresa tra 1 e 6 anni sottoposti a inguinale unilaterale riparazione dell'ernia/orchidopessia. Un altro studio ha confrontato gli effetti analgesici e gli effetti collaterali della dexmedetomidina e della clonidina aggiunti alla bupivacaina in pazienti pediatrici sottoposti a chirurgia addominale inferiore. Sessanta pazienti di età compresa tra 6 mesi e 6 anni sono stati assegnati in modo uniforme e casuale in tre gruppi in doppio cieco. Ciascun paziente ha ricevuto una singola dose caudale di bupivacaina 0.25% (1 ml/kg) combinata con dexmedetomidina 2 μg/kg in soluzione fisiologica 1 ml, clonidina 2 μg/kg in soluzione fisiologica 1 ml o un volume corrispondente di soluzione fisiologica normale. I risultati hanno dimostrato che, sebbene entrambi gli additivi aumentassero il periodo di analgesia, non vi era alcun vantaggio significativo nel selezionare la dexmedetomidina rispetto alla clonidina.
Gli anestetici locali tipicamente somministrati per i blocchi nervosi caudali a iniezione singola nei pazienti pediatrici sono elencati in Tabella 3.
TABELLA 3. Tipici anestetici locali per il blocco del nervo caudale in pediatria (colpo singolo).
| Agente | Concentrazione (%) | Dose (mg) | Esordio (minuti) | Durata dell'azione (minuti) |
|---|---|---|---|---|
| Ropivacaine74 | 0.2 | 2 mg / kg | 9 | 520 |
| Bupivacaine74 | 0.25 | 2 mg / kg | 12 | 253 |
| Ropivacaine75 | 0.2 | 0.7 mg / kg | 11.7 | 491 |
| Bupivacaine75 | 0.25 | 0.7 mg / kg | 13.1 | 457 |
| Ropivacaine76 | 0.2 | 1 ml/kg | 8.4 | Non disponibile |
| Levobupivacaina76 | 0.25 | 1 ml/kg | 8.8 | Non disponibile |
| Bupivacaine76 | 0.25 | 1 ml/kg | 8.8 | Non disponibile |
Consigli NYSORA
- Il rilassamento dello sfintere anale dopo l'iniezione di anestetico locale può predire il successo di un blocco del nervo caudale.
- Ciò è particolarmente utile nei bambini perché la maggior parte dei blocchi nervosi caudali viene eseguita mentre il bambino è anestetizzato e non è possibile valutare l'efficacia del blocco nervoso testando i livelli di analgesia sensoriale.
- Uno studio ha dimostrato che la presenza di uno sfintere anale rilassato al termine dell'intervento chirurgico era correlata alla ridotta necessità di somministrare oppioidi nel periodo perioperatorio.
Altre considerazioni sull'uso dell'anestesia epidurale caudale nei bambini
Sebbene il blocco del nervo caudale sia un pilastro del perioperatorio gestione del dolore in chirurgia pediatrica e rappresenta probabilmente il 60% di tutte le tecniche di anestesia regionale eseguite in questa popolazione di pazienti, non tutti gli studi hanno dimostrato un marcato beneficio del blocco del nervo caudale per l'analgesia postoperatoria rispetto ad altre modalità. A seguito di un'erniorrafia inguinale unilaterale, il blocco del nervo caudale ha dimostrato di fornire una gestione del dolore efficace, ma non superiore, rispetto all'infiltrazione locale della ferita in 54 bambini. Gli effetti collaterali e i requisiti di analgesia di salvataggio non differivano tra i due gruppi. Il blocco del nervo epidurale caudale nei bambini può indurre cambiamenti significativi nel flusso sanguigno aortico discendente mantenendo la frequenza cardiaca e la pressione arteriosa media. In uno studio su 10 bambini di età compresa tra 2 mesi e 5 anni, è stata utilizzata una sonda Doppler transesofagea per calcolare le variabili emodinamiche dopo l'iniezione di 1 mL/kg di bupivacaina allo 0.25% con epinefrina 5 μg/mL. Il volume di eiezione aortica è aumentato e la resistenza vascolare aortica è diminuita di circa il 40%. Un altro studio che ha esaminato l'emodinamica periferica utilizzando l'ecografia Doppler in bambini anestetizzati con sevoflurano prima e dopo un blocco del nervo caudale ha mostrato schemi di flusso significativamente alterati dopo il blocco nervoso. La velocità di picco è aumentata del 24%; il flusso di volume è aumentato del 76% e il diametro dell'arteria dorsale del piede è aumentato del 20%. Tuttavia, la pressione sanguigna e la frequenza cardiaca non sono state influenzate in modo significativo dal blocco del nervo caudale. Questi dati suggeriscono che il blocco del nervo caudale provoca vasodilatazione secondaria al blocco del sistema nervoso simpatico.
APPLICAZIONI DEL BLOCCO DEL NERVO EPIDURALE CAUDALE NELLA GESTIONE DEL DOLORE ACUTO E CRONICO
Radicolopatia refrattaria alla terapia convenzionale
Nei casi di radicolopatia refrattaria alle terapie analgesiche convenzionali, le tecniche analgesiche epidurali caudali possono ridurre significativamente e in modo affidabile il dolore. Una di queste tecniche è la neuroplastica epidurale percutanea: un catetere caudale viene lasciato in posizione per un massimo di 3 giorni allo scopo di iniettare soluzioni ipertoniche nello spazio epidurale per trattare la radicolopatia con lombalgia e cicatrici epidurali associate, tipicamente dovute a precedenti interventi chirurgici alla colonna lombare. Oltre agli anestetici locali e ai corticosteroidi, all'iniettato vengono aggiunti soluzione salina ipertonica e ialuronidasi. La tecnica richiede l'uso della guida fluoroscopica e dell'epidurografia caudale a causa della sua efficacia nel correlare un difetto di riempimento del mezzo di contrasto non ionico iodato iniettato con il livello di dolore riportato dal paziente.
L'iniezione di soluzioni nello spazio epidurale di un paziente con aderenze meningee è solitamente dolorosa a causa dell'allungamento delle radici nervose colpite. Desametasone o betametasone sono stati raccomandati al posto del metilprednisolone o del triamcinolone perché gli steroidi particellari possono occludere un catetere epidurale o causare ischemia spinale a seguito di iniezione intravascolare involontaria.
La soluzione salina ipertonica viene utilizzata per prolungare il sollievo dal dolore grazie ai suoi effetti anestetici locali e alla sua capacità di ridurre l'edema nelle radici nervose precedentemente cicatrizzate o infiammate. Si raccomanda un approccio laterale dell'ago nel canale caudale, dirigendo l'ago e il catetere verso il lato colpito. Il posizionamento laterale tende a ridurre al minimo la probabilità di penetrazione nel sacco durale o di iniezione subdurale. Quando 5-10 ml di mezzo di contrasto vengono iniettati nel canale caudale attraverso un catetere epidurale, si sviluppa un aspetto "albero di Natale" quando il colorante si diffonde nelle strutture perineurali all'interno del canale osseo e lungo i nervi quando escono dalla colonna vertebrale. Le aderenze epidurali impediscono la diffusione del colorante, quindi i nervi coinvolti non sono delineati dal contrasto. Una volta assicurato il corretto posizionamento del catetere nello spazio epidurale, vengono iniettate rapidamente 1500 unità di ialuronidasi in 10 ml di soluzione fisiologica priva di conservanti. Segue un'iniezione di 10 ml di ropivacaina allo 0.2% e 40 mg di triamcinolone. Dopo queste due iniezioni, viene infuso un volume aggiuntivo di 9 ml di soluzione salina ipertonica al 10% in 20-30 minuti. Nel secondo e terzo giorno, l'iniezione di anestetico locale (ropivacaina) è seguita dalla soluzione salina ipertonica.
Uno studio ha confrontato l'efficacia dell'adesiolisi percutanea epidurale utilizzando un'iniezione di 5 ml di lidocaina al 2% senza conservanti, seguita da 6 ml di soluzione di cloruro di sodio al 10% e 6 mg di betametasone non particolato tramite un posizionamento mirato guidato fluoroscopicamente di un catetere caudale (gruppo 1) rispetto a un'iniezione della stessa soluzione con 6 ml di soluzione di cloruro di sodio allo 0.9% invece della soluzione salina ipertonica tramite un catetere posizionato nel canale caudale con la punta a livello S3 (gruppo 2). Lo studio ha riscontrato un significativo sollievo dal dolore (76%) nel gruppo con soluzione salina ipertonica al follow-up di 1 anno, rispetto al 4% dei pazienti nel gruppo con soluzione salina normale.
Uno studio prospettico, in doppio cieco, randomizzato, che ha esaminato il ruolo dell'aggiunta della ialuronidasi agli steroidi epidurali caudali guidati fluoroscopicamente e alle iniezioni di soluzione salina ipertonica in pazienti con sindrome da chirurgia dorsale fallita, ha mostrato un miglioramento significativo nel sollievo dal dolore a lungo termine nei pazienti che hanno ricevuto ialuronidasi. Un totale di 38 pazienti sono stati arruolati nello studio. Venti pazienti hanno ricevuto iniezioni caudali guidate fluoroscopicamente di 10 ml di soluzione di bupivacaina allo 0.25% contenente 80 mg di metilprednisolone e 30 ml di soluzione salina ipertonica al 3% (gruppo 1). Diciotto pazienti hanno ricevuto la stessa quantità di anestetico locale e steroidi, seguiti da 1500 UI di ialuronidasi (che è stata sostituita da un volume equivalente di soluzione salina normale nei pazienti del gruppo 1) e 30 ml di soluzione salina ipertonica al 3% (gruppo 2).
Un altro studio randomizzato, controllato, in doppio cieco di iniezioni epidurali caudali guidate fluoroscopicamente ha confrontato 10 ml di lidocaina 0.5% e 9 ml di lidocaina 0.5% miscelati con 6 mg di betametasone o 40 mg di metilprednisolone (volume totale 10 ml). Questo studio ha mostrato una potenziale superiorità degli steroidi rispetto al solo anestetico locale al follow-up di 1 anno.
Analgesia postoperatoria in pazienti sottoposti a chirurgia della colonna lombare
Un'altra applicazione unica del blocco del nervo caudale è la fornitura di analgesia postoperatoria nei pazienti sottoposti a interventi chirurgici alla colonna lombare. In una serie di casi, i pazienti hanno ricevuto 20 ml di bupivacaina allo 0.25% con 0.1 mg di buprenorfina tramite l'approccio epidurale caudale, eseguito prima dell'incisione chirurgica. I pazienti sono stati sottoposti a fusione intersomatica posteriore e laminotomia per stenosi spinale e il controllo del dolore postoperatorio è stato confrontato nel gruppo caudale con un gruppo trattato con oppioidi parenterali convenzionali. Il gruppo caudale ha richiesto un minor numero di dosi di farmaci analgesici di salvataggio per le prime 12 ore dopo l'intervento chirurgico. Una riduzione della pressione sanguigna nei pazienti del gruppo caudale sottoposti a laminotomia, ma non a fusione, è stata notata nei pazienti con durata prolungata (24 ore) dell'analgesia postoperatoria.
Altre applicazioni
Il blocco del nervo epidurale caudale è stato anche confrontato con gli oppioidi intramuscolari nel trattamento del dolore dopo chirurgia ortopedica di emergenza degli arti inferiori. Il gruppo caudale che ha ricevuto 20 ml di bupivacaina allo 0.5% ha avuto 8 ore di analgesia superiore e ha anche avuto una significativa riduzione della necessità di farmaci oppioidi di salvataggio.
L'iniezione caudale di clonidina (75 μg con 7 mL di bupivacaina 0.5% e 7 mL di lidocaina 2% con epinefrina 5 μg/mL) è stata utilizzata per l'analgesia postoperatoria dopo emorroidectomia elettiva. Trentadue adulti hanno ricevuto la combinazione clonidina-locale, mentre un gruppo di controllo ha ricevuto solo anestetico locale.
L'analgesia è stata in media di 12 ore nel gruppo clonidina, rispetto a meno di 5 ore nel gruppo che ha ricevuto solo anestetico locale. La bradicardia si è verificata in circa il 22% dei pazienti nel gruppo della clonidina. Ciò contrasta con i risultati di una valutazione della clonidina utilizzata come coadiuvante per l'anestesia caudale pediatrica come notato in precedenza.
Iniezioni caudali di alcol o fenolo sono state utilizzate per trattare il dolore intrattabile dovuto al cancro. In uno studio su 67 blocchi nervosi, è stato riscontrato che le radici sacrali inferiori erano facilmente raggiungibili con l'iniezione caudale e che le radici S1 e S2 (contributo del plesso lombosacrale) erano state risparmiate.
COMPLICANZE ASSOCIATE AL BLOCCO DEL NERVO EPIDURALE CAUDALE
Le complicanze del blocco del nervo caudale sono le stesse che si verificano in seguito a lombare blocco del nervo epidurale e possono comprendere quelli relativi alla tecnica stessa e quelli relativi all'iniettato (anestetico locale o altra sostanza iniettata). Fortunatamente, gravi complicazioni si verificano raramente. L'elenco delle potenziali complicanze comprende ascessi epidurali, meningite, ematoma epidurale, puntura durale e cefalea post-puntura durale, iniezione subdurale, pneumocefalo ed embolia gassosa, mal di schiena e cateteri epidurali rotti o annodati. Altre complicazioni rare che sono state riportate con l'anestesia caudale includono gonfiore della parotide unilaterale, singhiozzo persistente dopo infusione caudale continua di ropivacaina allo 0.1% e cefalea da ipotensione intracranica dopo iniezione epidurale caudale non complicata.

Dal Compendio dell'anestesia regionale: Complicazioni dell'infografica sull'anestesia caudale.
Tossicità sistemica degli anestetici locali
L'incidenza di convulsioni indotte da anestetico locale dopo il blocco del nervo caudale sembra essere maggiore rispetto agli approcci lombari o toracici. In uno studio retrospettivo su 25,697 pazienti che hanno ricevuto blocchi del nervo del plesso brachiale, blocchi del nervo epidurale caudale o blocchi del nervo epidurale lombare dal 1985 al 1992, Brown ha notato 26 episodi convulsivi. La frequenza delle crisi negli adulti in ordine decrescente era il blocco del nervo caudale, del plesso brachiale, il blocco del nervo epidurale lombare o toracico. Nove casi sono stati attribuiti a blocchi del nervo caudale, otto si sono verificati con cloroprocaina e uno con lidocaina. C'è stata un'incidenza aumentata di 70 volte di reazioni tossiche da anestetico locale con l'anestesia epidurale caudale (0.69%) rispetto all'anestesia epidurale lombare o toracica negli adulti.
Consigli NYSORA
- L'incidenza di convulsioni indotte da anestetico locale a seguito di blocco del nervo epidurale caudale è maggiore rispetto a seguito di approcci lombari o toracici.
- Il rischio relativo di tossicità da anestetico locale segue questo ordine: caudale > blocco del nervo del plesso brachiale > blocco del nervo epidurale lombare o toracico.
- Un aumento della frequenza cardiaca di oltre 10 battiti al minuto o un aumento della pressione arteriosa sistolica di oltre 15 mmHg dopo l'iniezione di anestetico locale contenente epinefrina è indicativo di un'iniezione intravascolare.
Nei bambini, tuttavia, una revisione retrospettiva ha identificato solo due reazioni tossiche (cioè, convulsioni indotte da anestetici locali) in 15,000 blocchi nervosi caudali. Il gruppo di Dalens ha scoperto che l'iniezione intravascolare involontaria si verifica fino allo 0.4% dei blocchi nervosi caudali pediatrici,70 dimostrando l'importanza di eseguire test di dosaggio contenenti adrenalina in questa fascia di età. È stato suggerito che un aumento della frequenza cardiaca di oltre 10 battiti al minuto o un aumento della pressione arteriosa sistolica di oltre 15 mm Hg debbano essere considerati indicativi dell'iniezione sistemica. I cambiamenti dell'onda T sull'ECG si verificano prima dopo l'iniezione intravascolare, seguiti da variazioni della frequenza cardiaca e infine da variazioni della pressione sanguigna. Questi cambiamenti possono essere ritardati fino a 90 secondi dopo l'iniezione. Per ulteriori informazioni, vedere Tossicità sistemica anestetica locale.
Evento di anestesia spinale totale
Totale anestesia spinale può verificarsi quando una dose iniettata di anestetico locale destinato allo spazio epidurale accede allo spazio subaracnoideo. Nel caso clinico di un bambino di 18 mesi del peso di 10 kg che ha ricevuto un blocco del nervo caudale dopo l'intervento chirurgico dopo aver subito la riparazione di emergenza di un'ernia diaframmatica ricorrente, sono stati iniettati 4 ml di bupivacaina allo 0.5% e 2.5 μg/kg di buprenorfina in totale volume di 10 ml. L'apertura degli occhi e il movimento della mano sono stati ritardati di 3 ore a seguito di questa complicanza. In un altro neonato sottoposto a revisione di una fundoplicatio Nissen, un catetere posizionato caudalmente è stato involontariamente fatto avanzare nella regione cervicale spinale. La stimolazione elettrica del catetere (test Tsui) ha provocato la stimolazione del nervo frenico. Il catetere è stato riposizionato con successo e ulteriori cure non sono state complicate. Questo case report illustra la relativa facilità di passaggio del catetere a livelli vertebrali elevati nei neonati rispetto agli adulti.
Infezione
Un caso clinico ha documentato la rara insorgenza di discite a distanza e osteomielite vertebrale che coinvolgono livelli di salto e senza lo sviluppo di formazione di ascessi epidurali in una donna anziana che ha ricevuto steroidi epidurali caudali e anestetico locale per spondilolistesi degenerativa. Un mese dopo, ha sviluppato una discite infettiva L2–L3 e L4–L5, insieme a un'osteomielite vertebrale adiacente. Le colture hanno dimostrato la crescita di Pseudomonas aeruginosa, che è stata trattata con antibiotici.
SOMMARIO
Il blocco del nervo epidurale caudale è una tecnica per fornire analgesia e anestesia delle radici del nervo lombosacrale che precede gli approcci lombari convenzionali. Il blocco nervoso ha subito diversi periodi di accettabilità e, sebbene sia applicato raramente a casi chirurgici di routine negli adulti, è la tecnica di anestesia regionale più comunemente eseguita nei neonati e nei bambini. Il blocco del nervo caudale nei pazienti adulti ha goduto di una recrudescenza ultimamente, principalmente perché fornisce un percorso alternativo allo spazio epidurale lombare quando l'accesso diretto è limitato da precedenti interventi chirurgici e per l'esecuzione dell'epiduroscopia. I medici che utilizzano abitualmente la fluoroscopia e l'ecografia scopriranno che ha molte applicazioni, sia per casi di routine che complicati.
BIBLIOGRAFIA
- Bromage PR: analgesia epidurale. Saunders, 1978, pp 258–282.
- Racz G: Comunicazione personale, 12 ottobre 2003, Riunione annuale dell'American Society of Anesthesiologists, San Francisco.
- Trottatore M: Variazioni del canale sacrale: il loro significato nella somministrazione dell'analgesia caudale. Anesth Analg 1947;26:192–202.
- MacDonald A, Chatrath P, Spector T, et al: livello di terminazione del midollo spinale e del sacco durale: uno studio di risonanza magnetica. Clin Anat; 1999;12:149–152.
- Joo J, Kim J, Lee J: La prevalenza di variazioni anatomiche che possono causare la puntura durale involontaria durante l'esecuzione del blocco del nervo caudale nei coreani: uno studio che utilizza la risonanza magnetica. Anestesia 2010;65 (1):23–26.
- Igarashi T, Hirabayashi Y, Shimizu R, et al: La struttura extradurale lombare cambia con l'aumentare dell'età. Fr. J Anaest 1997;78:149–152.
- Crighton I, Barry B, Hobbs G: uno studio dell'anatomia dello spazio caudale utilizzando la risonanza magnetica. Fr. J Anaesth 1997;78:391–395.
- Sekiguchi M, Yabuki S, Satoh K, et al: uno studio anatomico dello iato sacrale. Una base per il successo del blocco del nervo epidurale. Clin J Pain 2004;20:51–54.
- Bryce-Smith R: La diffusione delle soluzioni nello spazio extradurale. Anestesia 1954;9:201–205.
- Brennero E: Anestesia sacrale. Ann Surg 1924;79:118–123.
- Aggarwal A, Kaur H, Batra YK, et al: Considerazione anatomica dello spazio epidurale caudale: uno studio su cadavere. Clin Anat 2009;22(6):730–737.
- Waldman S: blocco del nervo epidurale caudale. In Waldman S (a cura di): Gestione del dolore interventistica, 2a ed. Saunders, 2001, p 520.
- Winnie A, Candido KD: Blocco neurale differenziale per la diagnosi del dolore. In Waldman S (a cura di): Gestione del dolore interventistica, 2a ed. Saunders, 2001, pp 162–173.
- Candido KD, Stevens RA: blocchi neurolitici intratecali per il sollievo del dolore da cancro. Best Pract Res Clin Anaesthesiol 2003; 17: 407–428.
- Lou L, Racz G, Heavner J: neuroplastica epidurale percutanea. In Waldman S (a cura di): Gestione del dolore interventistica, 2a ed. Saunders, 2001, pp 434–445.
- Cook RA, Driver RP Jr: cerotto epidurale. WV Med J 2009; 105(5): 28–29.
- Heavner J, Racz G, Raj P: neuroplastica epidurale percutanea: valutazione prospettica dello 0.9% di NaCl rispetto al 10% di NaCl con o senza ialuronidasi. Reg Anesth Antidolorifico 1999;24:202–207.
- Manchikanti L, Bakhit C, Pampati V: Ruolo dell'epidurografia nella neuroplastica caudale. Pain Digest 1998;8:277–281.
- Kakiuchi M, Abe K: blocco epidurale caudale pre-incisionale e sollievo dal dolore dopo operazioni della colonna lombare. Int Orthop 1997;21:62–66.
- McCrirrick A, Ramage D: Blocco caudale per l'analgesia postoperatoria: un'utile aggiunta agli oppiacei intramuscolari a seguito di chirurgia ortopedica di emergenza della parte inferiore della gamba. Terapia intensiva di Anaesth 1991; 19:551–554.
- Van Elstraete A, Pastureau F, Lebrun T, et al: Clonidina caudale per analgesia postoperatoria negli adulti. Fr. J Anaesth 2000;84:401–402.
- Porges P, Zdrahal F: [Neurolisi alcolica intratecale delle radici sacrali inferiori nel cancro del retto inoperabile]. Anestesista 1985;34:627–629.
- Ivani G, DeNegri P, Conio A, et al: Confronto di bupivacaina racemica, ropivacaina e levobupivacaina per l'anestesia caudale pediatrica. Effetti sull'analgesia postoperatoria e sul blocco motorio. Reg Anesth Antidolorifico 2002;27:157–161.
- Chan S, Tay H, Thomas E: test "Whoosh" come ausilio didattico nel blocco caudale. Terapia intensiva di Anaesth 1993;21:414–415.
- Orme R, Berg S: Il test "swoosh", una valutazione di un test "swoosh" modificato nei bambini. Br J Aneaesth 2003;90:62–65.
- Kim MS, Han KH, Kim EM, et al: Il mito del triangolo equilatero per l'identificazione dello iato sacrale nei bambini smentito dall'ecografia. Reg Anesth Pain Med 2013;38(3):243–247.
- Yoon JS, Sim KH, Kim SJ, Kim WS, Koh SB, Kim BJ: La fattibilità dell'ecografia color Doppler per l'iniezione di steroidi epidurali caudali. Dolore 2005;118:210–214.
- Tsui B, Tarkkila P, Gupta S, Kearney R: Conferma del posizionamento dell'ago caudale mediante stimolazione nervosa. Anestesiologia 1999;91:374–378.
- Digiovanni A: Iniezione interossea involontaria: rischio di anestesia caudale. Anestesiologia 1971;34:92–94.
- Lofstrom B: Anestesia caudale. In Ejnar Eriksson (a cura di): Manuale illustrato in anestesia locale. Astra, 1969, pp 129–134.
- Blocco caudale. In Covino BG, Scott DB (a cura di): Manuale di anestesia epidurale e analgesia. Grune & Stratton, 1985, pp 104–108.
- Dawkins C: Un'analisi delle complicanze del blocco extradurale e caudale. Anestesia 1969;24:554–563.
- Chung Y, Lin C, Pang W, et al: un blocco caudale continuo alternativo con cateterizzazione caudale tramite l'interspazio lombare inferiore nei pazienti adulti. Acta Anaesthesiol Scand 1998;36:221–227.
- Triffterer L, Machata AM, Latzke D, et al: Valutazione ecografica della diffusione cranica durante il blocco caudale nei bambini: effetto della velocità di iniezione di anestetici locali. Fr. J Anaesth 2012;108(4):670–674.
- Li Y, Zhou Y, Chen H, Feng Z: L'effetto del sesso sulla concentrazione analgesica locale minima di ropivacaina per l'anestesia caudale nella chirurgia anorettale. Anesth Analg 2010;110:1490–1493.
- Wong S, Li J, Chen C, et al: Blocco epidurale caudale per procedure ginecologiche minori in chirurgia ambulatoriale. Chang Gung Med J 2004;27:116–121.
- Nishiyama T, Hanaoka K, Ochiai Y: L'approccio mediano al blocco epidurale transsacrale. Anesth Analg 2002;95:1067–1070.
- Schuepfer G, Konrad C, Schmeck J, et al: Generazione di una curva di apprendimento per i blocchi epidurali caudali pediatrici: una valutazione empirica delle abilità tecniche negli anestesisti principianti ed esperti. Reg Anesth Antidolorifico 2000;25:385–388.
- Tsui B, Seal R, Koller J: Posizionamento del catetere epidurale toracico tramite l'approccio caudale nei neonati utilizzando la guida elettrocardiografica. Anesth Analg 2002;95:326–330.
- Lundblad M, Lonnqvist PA, Eksborg S, Marhofer P: distribuzione segmentale dell'anestesia caudale ad alto volume nei neonati, nei neonati e nei bambini piccoli come valutata dall'ecografia. Paediatr Anaesth 2011;21(2): 121–127.
- Tuncer S, Yosunkaya A, Reisli R, et al: Effetto del blocco caudale sulla risposta allo stress nei bambini. Pediatr Int 2004;46:53–57.
- Valairucha S, Seefelder C, Houck C: Cateteri epidurali toracici posizionati per via caudale nei neonati: l'importanza della conformazione radiografica. Paediatr Anaest 2002;12:424–428.
- Rojas-Perez E, Castillo-Zamora C, Nava-Ocampo A: uno studio randomizzato di blocco caudale con bupivacaina 4 mg x kg-l (1.8 ml x kg-l) vs anestesia generale con fentanil per la chirurgia cardiaca. Paediatr Anaesth 2003; 13:311–317.
- Koo BN, Hong JY, Kil HK: Diffusione di ropivacaina mediante una formula basata sul peso in un blocco caudale pediatrico: un esame fluoroscopico. Acta Anaesthesiol Scand 2010;54(5):562–565.
- Stow P, Scott A, Phillips A, et al: Concentrazioni plasmatiche di bupivacaina durante analgesia caudale e blocco del nervo ileo-inguinale-ileoipogastrico nei bambini. Anestesia 1998;43:650–653.
- Verghese S, Hannallah R, Rice LJ, et al: Anestesia caudale nei bambini: effetto del volume rispetto alla concentrazione di bupivacaina sul blocco della risposta di trazione del cordone spermatico durante l'orchipessi. Anesth Analg 2002;95: 1219–1223.
- Koinig H, Krenn C, Glaser C, et al: La dose-risposta della ropivacaina caudale nei bambini. Anestesiologia 1999;90:1339–1344.
- Jeong-Yeon Hong MD, Sang W, Han MD, et al: un confronto tra ropivacaina ad alto volume/bassa concentrazione e basso volume/alta concentrazione nell'analgesia caudale per l'orchiopessia pediatrica. Anesth Anal 2009;109; 1073–1078.
- Deng S, Xiao, W, Tang G, et al: La concentrazione minima di anestetico locale di ropivacaina per l'analgesia caudale nei bambini. Anesth Analg 2002;94:1465–1468.
- Lonnqvist P, Westrin P, Larsson B, et al: farmacocinetica della ropivacaina dopo blocco caudale in bambini di età compresa tra 1 e 8 anni. Fr. J Anaesth 2000;85: 506–511.
- Deng XM, Xiao WJ, Tang GZ, Luo MP, Xu KL: Concentrazione analgesica locale minima di ropivacaina per l'analgesia caudale intraoperatoria nei bambini in età prescolare e scolare. Anestesia 2010;65(10):991–995.
- Dobereiner EF, Cox RG, Ewen A, Lardner DR: Aggiornamento clinico basato sull'evidenza: quale farmaco anestetico locale per il blocco caudale pediatrico fornisce un'efficacia ottimale con il minor numero di effetti collaterali? Can J Anaesth 2010;57(12):1102–1110.
- Schnabel A, Poepping DM, Pogatzki-Zahn EM, Zahn PK: Efficacia e sicurezza della clonidina come additivo per l'anestesia regionale caudale: una revisione sistematica quantitativa di studi randomizzati e controllati. Pediatr Anesth 2011;21:1219–1230.
- Saadawy I, Bolker A, Elshahawy MA, et al: Effetto della dexmedetomidina sulle caratteristiche della bupivacaina in un blocco caudale in pediatria. Acta Anesthesiol Scand 2009;53:251–256.
- El-Hennawy M, Abd-Elwahab AM, Abd-Elmaksoud AM, et al: L'aggiunta di clonidina o dexmedetomidina alla bupivacaina prolunga l'analgesia caudale nei bambini. Fr. J Anaesth 2009;103(2):268–274.
- Verghese S, Mostello L, Patel R: il test del tono dello sfintere anale predice l'efficacia dell'analgesia caudale nei bambini. Anesth Analg 2002;94: 1161–1164.
- Schindler M, Swann M, Crawford M: un confronto tra l'analgesia postoperatoria fornita dall'infiltrazione della ferita o dall'analgesia caudale. Anesth Terapia intensiva 1991; 19:46–49.
- Larousse E, Asehnoune K, Dartayet B, et al: Gli effetti emodinamici dell'anestesia caudale pediatrica valutati mediante Doppler esofageo. Anesth Analg 2002;94:1165–1168.
- Hong JY, Ahn S, Kil HK: Cambiamenti del pattern di flusso dell'arteria dorsale del pedis dopo il blocco caudale nei bambini: studio osservazionale utilizzando un'ecografia duplex. Pediatr Anesth 2011;21:116–120.
- Manchikanti L, Cash KA, McManus CD, et al. I risultati preliminari di una valutazione comparativa dell'efficacia dell'adesiolisi e delle iniezioni epidurali caudali nella gestione della lombalgia cronica secondaria a stenosi spinale: uno studio randomizzato e controllato di equivalenza. medico del dolore 2009; 12:E341–E354.
- Yousef AA, El-Deen AS, Al-Deeb AE: Il ruolo dell'aggiunta della ialuronidasi agli steroidi caudali guidati fluoroscopicamente e all'iniezione di soluzione salina ipertonica in pazienti con sindrome da chirurgia dorsale fallita: uno studio prospettico, in doppio cieco, randomizzato. Pratica del dolore 2010;10(6):548–553.
- Manchikanti L, Singh V, Cash KA, Pampati V: uno studio randomizzato, controllato, in doppio cieco di iniezioni epidurali caudali fluoroscopiche nel trattamento dell'ernia del disco lombare e della radicolite. Colonna vertebrale 2011;36(23): 1897–1905.
- Joshi W, Connelly R, Freeman K, et al: Effetto analgesico della clonidina aggiunto alla bupivacaina 0.125% nel blocco caudale pediatrico. Paediatr Anaesth 2004;14:483–486.
- Valois T, Otis A, Ranger M, Muir JG: Incidenza del mal di schiena autolimitante nei bambini dopo il blocco caudale: uno studio esplorativo. Pediatr Anesth 2010;20:844–850.
- Lin J, Zuo YX: gonfiore unilaterale della parotide, a seguito di blocco caudale senza posizionamento del dispositivo per le vie aeree. Pediatr Anesth 2011;21:169–178.
- Bagdure DN, Reiter PD, Bhoite GR, et al: singhiozzo persistente associato a ropivacaina epidurale in un neonato. Ann Pharmacother 2011; 45(6):e35.
- Thomas R, Thanthulage S: Cefalea da ipotensione intracranica dopo iniezione epidurale caudale semplice. Anestesia 2012;67: 416–419.
- Brown D, Ransom D, Hall J, et al: Anestesia regionale e tossicità sistemica indotta dall'anestetico locale: frequenza delle convulsioni e alterazioni cardiovascolari associate. Anesth Analg 1995;81:321–328.
- Giaufre E, Dalens B, Gombert A: Epidemiologia e morbilità dell'anestesia regionale nei bambini: un'indagine prospettica di un anno della Società di anestesisti pediatrici in lingua francese. Anesth Analg 1996:83: 904–912.
- Dalens B, Hansanoui A: Anestesia caudale in chirurgia pediatrica: percentuale di successo ed effetti avversi in 750 pazienti consecutivi. Anesth Analg 1989;8:83–89.
- Afshan G, Khan F: Anestesia spinale totale dopo blocco caudale con bupivacaina e buprenorfina. Paediatr Anaesth 1996;6:239–242.
- Tsui B, Malherbe S: posizionamento involontario del catetere epidurale cervicale per via caudale mediante stimolazione elettrica. Anesth Analg 2004;99: 259–261.
- Yue W, Tan S: Discite a livello di salto a distanza e osteomielite vertebrale dopo iniezione epidurale caudale: un caso clinico di una rara complicanza delle iniezioni epidurali. Colonna vertebrale 2003;1:209–211.
- Ivani G, Mereto N, Lampugnani E, et al: Ropivacaina in chirurgia pediatrica: risultati preliminari [Abstract]. Paediatr Anaesth 1998;8: 127–129.
- Ivani G, Lampugnani E, De Negri P, et al: Ropivacaina vs bupivacaina nella chirurgia maggiore nei bambini [abstract]. Can J Anaesth 1999;46: 467–469.
- Ivani G, De Negri P, Conio A, et al: Confronto di bupivacaina racemica, ropivacaina e levobupivacaina per l'anestesia caudale pediatrica. Effetti sull'analgesia postoperatoria e sul blocco motorio. Reg Anesth Antidolorifico 2002;27:157–161.

